I закон термодинамики. Термохимия.ppt
- Количество слайдов: 60

Курский государственный медицинский университет Кафедра общей и биоорганической химии Лекция № 1 Основы общей термодинамики. Термохимия ©Доцент , к. х. н. Оксененко О. И.

План 1. Основные понятия термодинамики 2. Нулевой закон термодинамики 3. Первый закон термодинамики 4. Выражения первого закона термодинамики для различных процессов 5. Закон Гесса и его следствия. 6. Теплоты различных процессов. 7. Теплоемкость. 8. Закон Кирхгофа

Термодинамика – это наука, изучающая законы превращения различных видов энергии, связанные с переходом энергии в виде тепла или работы, а также вероятность, направление и пределы самопроизвольного течения процессов в данных условиях.

Ограничения термодинамики 1. Не рассматривает внутреннее строение тел и механизмы процессов, которые протекают в т/д системах. 2. Изучает макроскопические системы. 3. В т/д отсутствует понятие «времени» .
Термодинамика физическая техническая химическая Химическая термодинамика изучает химические и физико-химические превращения на основе законов общей термодинамики.

Объект термодинамики - система Система – тело или группа взаимодействующих тел, фактически или мысленно выделенных из окружающей среды. Типы систем
http: //www. varson. ru/images/Himia_jpeg_big/4 -01. jpg

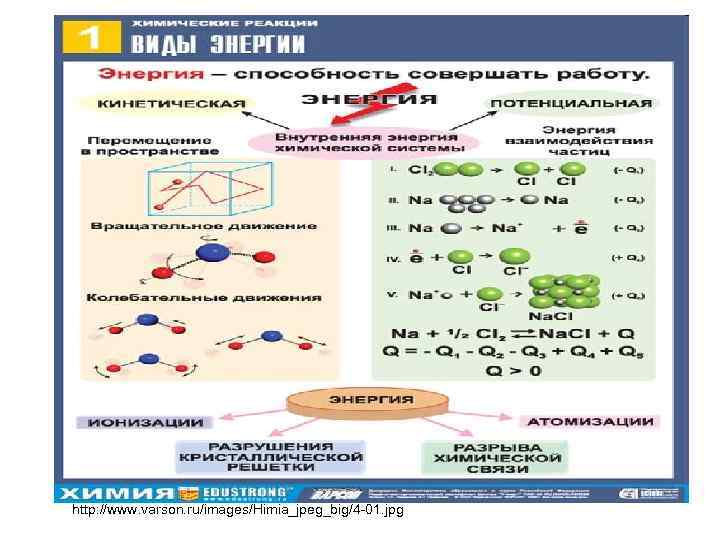
Энергия - мера способности системы совершать работу; общая качественная мера движения и взаимодействия материи. Полная энергия: E = Eкин + Eпот + Uвн Екин = 0 Епот = 0 • Е = Uвн • Uвн = Е/кин + E/пот Внутренняя энергия системы – полная энергия система; сумма кинетической и потенциальной энергии всех частиц, составляющих систему.

Молекулярная структура материи. Внутренняя энергия, ЗАО Новый диск, 2005
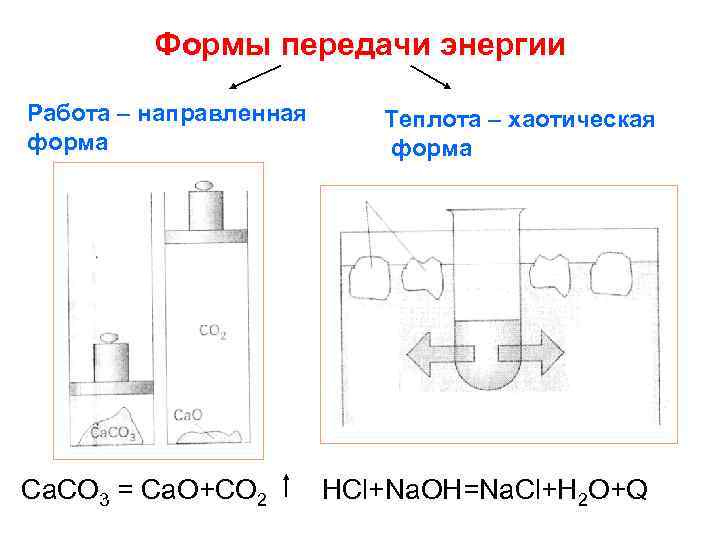
Формы передачи энергии Работа – направленная форма Са. СО 3 = Са. О+СО 2 Теплота – хаотическая форма HCl+Na. OH=Na. Cl+H 2 O+Q
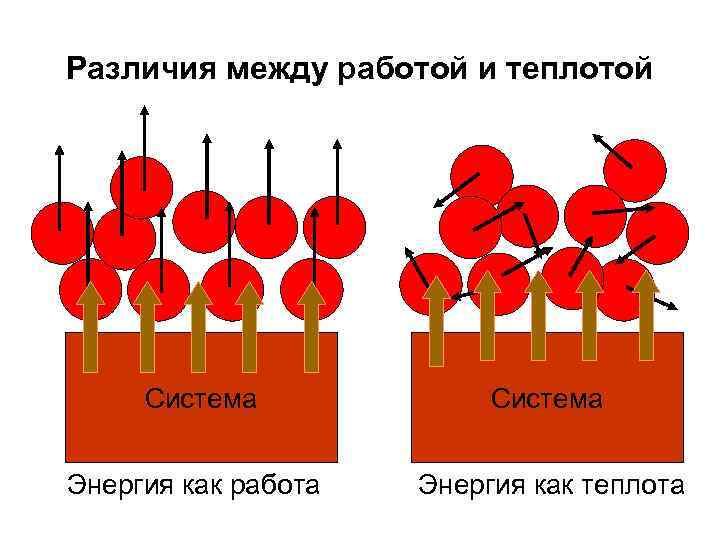
Различия между работой и теплотой Система Энергия как работа Энергия как теплота
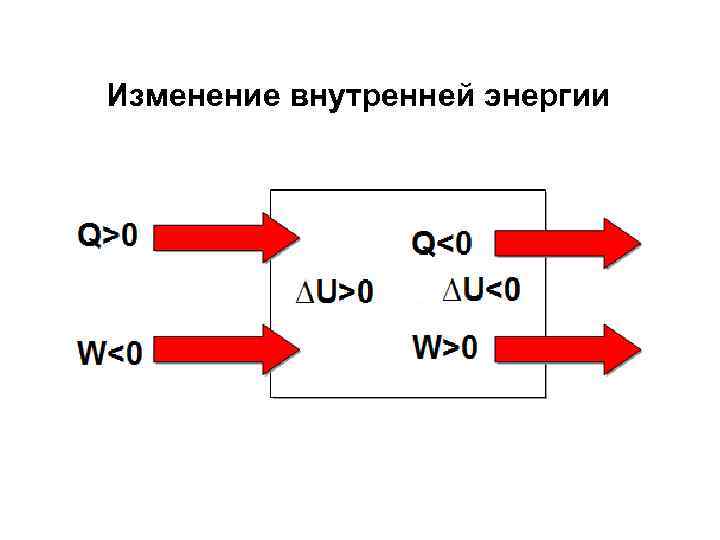
Изменение внутренней энергии

Нулевой закон термодинамики Если каждая из систем А и В находится в тепловом равновесии с системой С, то можно утверждать, что системы А и В находятся в тепловом равновесии друг с другом. ТА = Т С ТВ = Т С } => ТА = ТВ Условие термодинамического равновесия f. A (PA, VA) = f. B (PB, VB) = f. C (PC, VC) = T

Первый закон термодинамики 1. Энергия не исчезает и не возникает из ничего, а только превращается из одного вида в другой в строго эквивалентных количествах. 2. В изолированной системе внутренняя энергия постоянна, т. е. ∆U=0. 3. Вечный двигатель первого рода невозможен (т. е. устройство, которое производило бы работу без затраты энергии). 4. Если к закрытой системе подвести теплоту Q, то эта энергия расходуется на увеличение внутренней энергии системы U и на совершение системой работы против внешних сил окружающей среды.
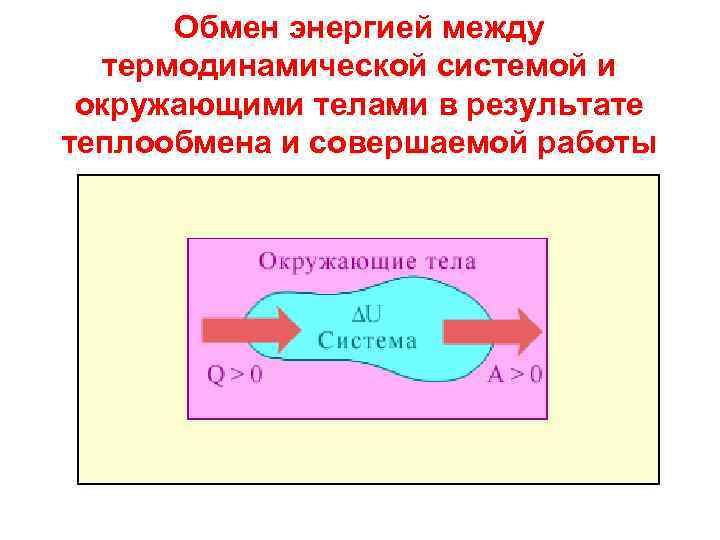
Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы

Математическое выражение I закона термодинамики • Дифференциальная форма Интегральная форма δQ = d. U +δW Q = ∆U + W δQ = d. U + pd. V Q = ∆U + p∆V

Первый закон термодинамики для различных процессов в системе идеального газа 1. T=const, U=const, ∆U=0 δ QT= δ W = pd. V QT = W = p ∆V Если n = 1 моль p. V = RT p=RT / V δ QT = RT d. V / V W =QT = RT ln(V 2 / V 1) = RT ln(P 1 / P 2)

Первый закон термодинамики различных процессов в системе идеального газа (продолжение). 2. p=const δ QP = d. U + pd. V QP = ∆H

Первый закон термодинамики различных процессов в системе идеального газа (продолжение). 3. V=const δQv = d. U Qv = 4. Q = 0, δQ = 0 δ W = - d. U W = - ∆U

Работа газа при расширении • P=const W= • V=const W=0 • T=const W = n. RT ln V 2 / V 1 = n. RT ln P 1/P 2 • Q=0 W = - n. Сv(T 2 – T 1) = p∆V
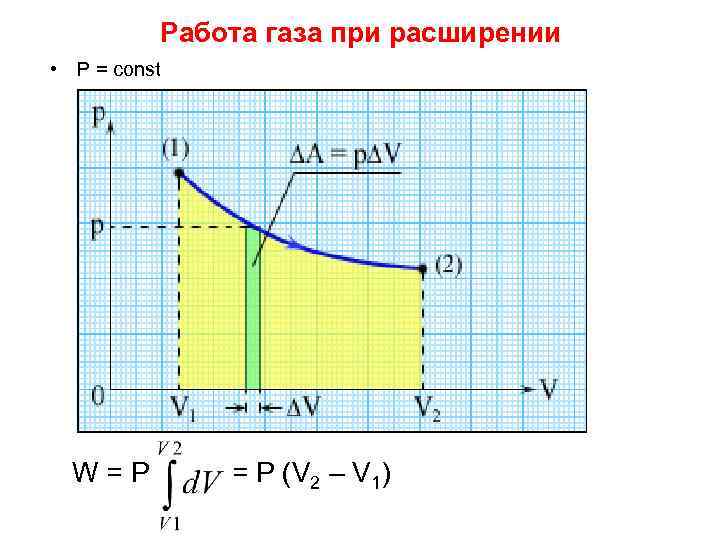
Работа газа при расширении • P = const W=P = P (V 2 – V 1)
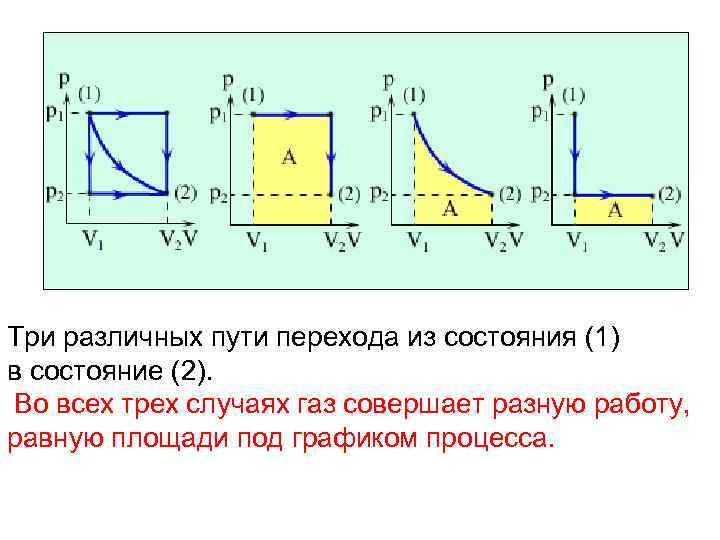
Три различных пути перехода из состояния (1) в состояние (2). Во всех трех случаях газ совершает разную работу, равную площади под графиком процесса.

• Тепловой эффект химической реакции – максимальное количество теплоты, которое выделяется или поглощается в ходе химической реакции. Условия 1. Tисх = Тпрод 2. Р = const, T = const 3. Не совершается других видов работы, кроме работы расширения.
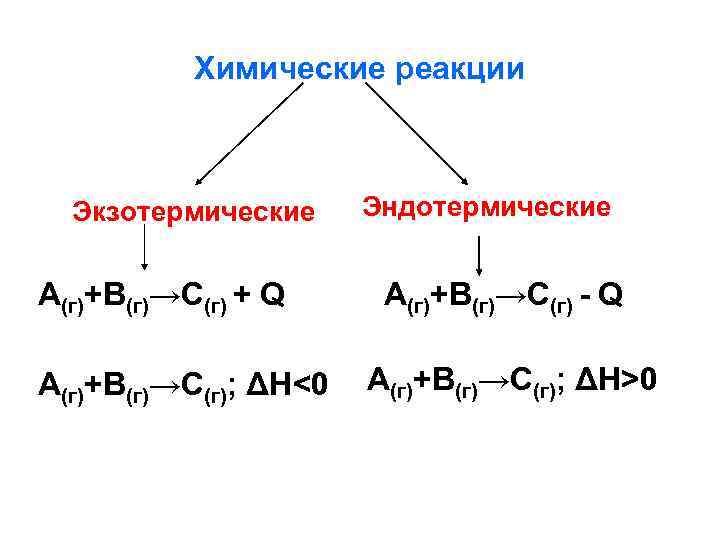
Химические реакции Экзотермические А(г)+В(г)→С(г) + Q А(г)+В(г)→С(г); ΔН<0 Эндотермические А(г)+В(г)→С(г) - Q А(г)+В(г)→С(г); ΔН>0
http: //900 igr. net/datas/fizika/Agregatnoe-sostojanie-veschestva/0005 -Plavlenie. Paroobrazovanie-Vozgonka. jpg
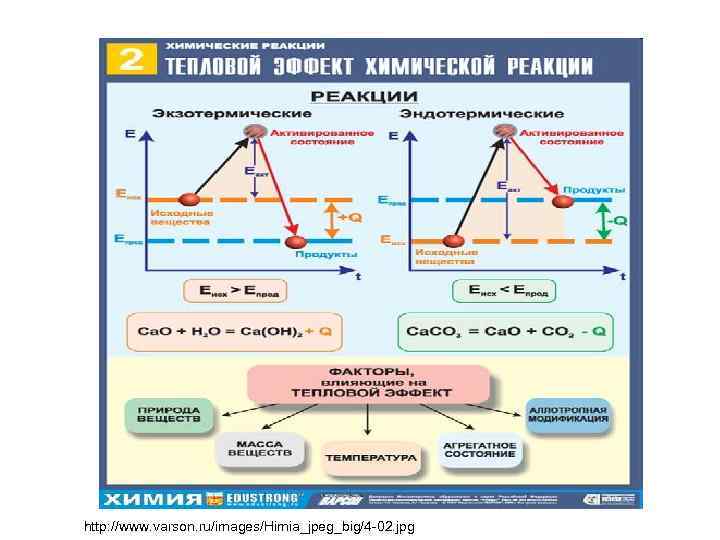
http: //www. varson. ru/images/Himia_jpeg_big/4 -02. jpg

Стандартное состояние Состояние чистого вещества при р = 1 атм = 101325 Па = 760 мм. рт. ст и заданной температуре (чаще 25°) 1) тв. в-ва - устойчивая модификация 2) р-ры – идеальные при единичной концентрации 3) газы - гипотетическое состояние идеального газа

Стандартная энтальпия (теплота) образования сложного вещества (Δf. Н°Т) равна ТЭ реакции образования 1 моль этого вещества из простых веществ при стандартных условиях. Пример Na +1/2 Cl 2 = Na. Cl ; Δr. HºT = Δf. HºT (Na. Cl)

Стандартная теплота образования простых веществ в их наиболее термодинамически устойчивом агрегатном и аллотропном состоянии при стандартных условиях принимается равной нулю. Пример

Стандартная энтальпия (теплота) сгорания (Δс. Н°Т) равна ТЭ реакции сгорания (окисления) 1 моль вещества в избытке кислорода до высших устойчивых оксидов при с. у. • Δс. Н 0 Т негорючих веществ = 0

Гесс Генрих Иванович (1802 -1850) Один из основоположников термохимии, докт. медицины, профессор Петербургского Горного института, академик Российской Академии наук http: //www. rustrana. ru/articles/25810/hess_1. jpg
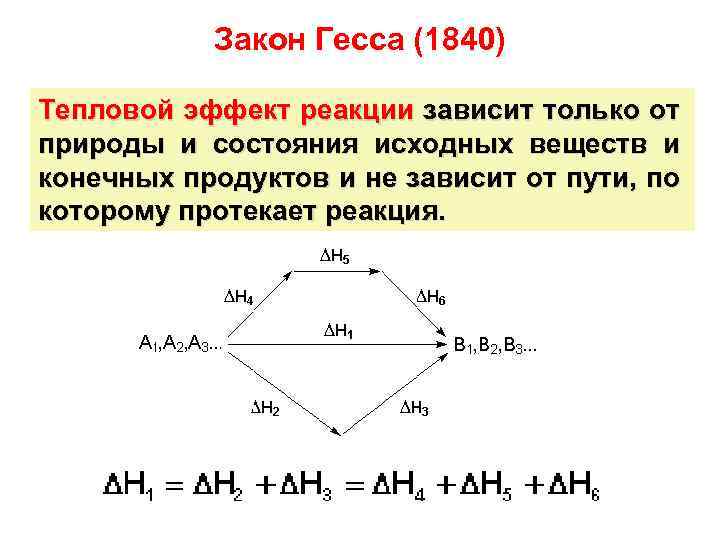
Закон Гесса (1840) Тепловой эффект реакции зависит только от природы и состояния исходных веществ и конечных продуктов и не зависит от пути, по которому протекает реакция.
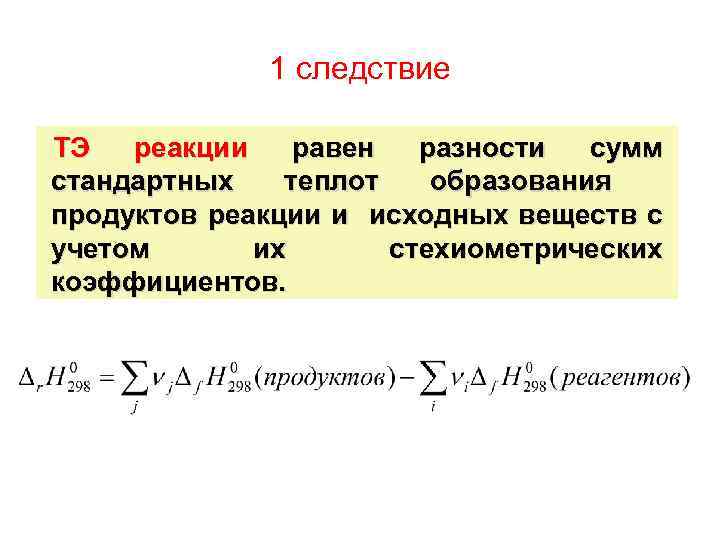
1 следствие ТЭ реакции равен разности сумм стандартных теплот образования продуктов реакции и исходных веществ с учетом их стехиометрических коэффициентов.

2 следствие ТЭ реакции равен разности сумм стандартных теплот сгорания исходных веществ и продуктов реакции с учетом их стехиометрических коэффициентов.

3 следствие ТЭ прямой реакции равен ТЭ обратной реакции с противоположным знаком.
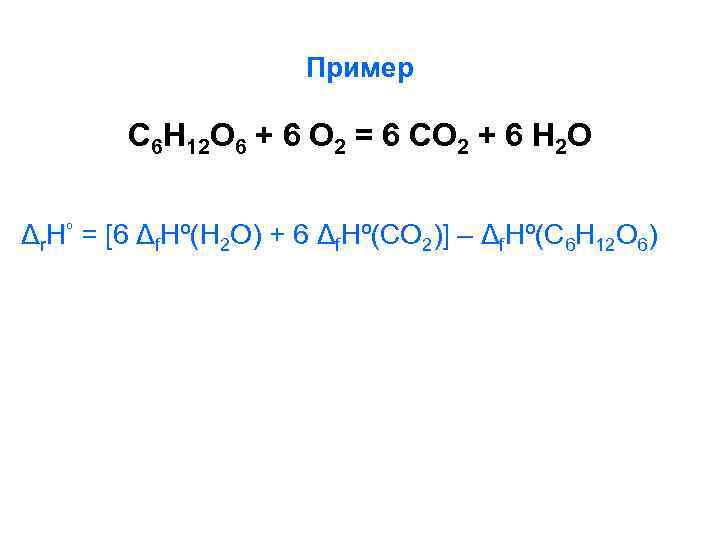
Пример С 6 Н 12 О 6 + 6 О 2 = 6 СО 2 + 6 Н 2 О Δr. Hº = [6 Δf. Hº(H 2 O) + 6 Δf. Hº(CO 2)] – Δf. Hº(C 6 H 12 O 6)
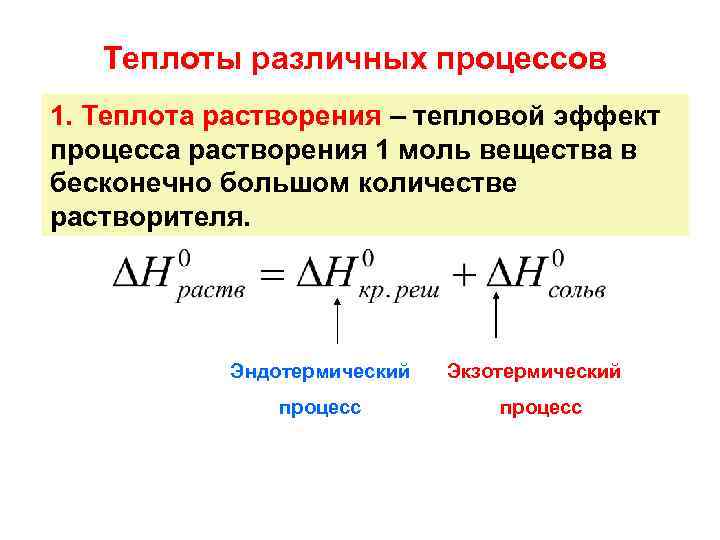
Теплоты различных процессов 1. Теплота растворения – тепловой эффект процесса растворения 1 моль вещества в бесконечно большом количестве растворителя. Эндотермический процесс Экзотермический процесс

2. Теплота реакции нейтрализации Теплота нейтрализации – теплота образования 1 моль жидкой Н 2 О из ионов Н+ и ОН-. 1. Реакция нейтрализации между сильной кислотой и сильным основанием Расчет ΔHºнейтр = - 286 + 230 = -56 к. Дж/моль

2. Реакция нейтрализации с участием слабого электролита OH‾ НА↔ H+ + A ‾ → A‾ + H 2 O ΔºH дис ΔHºнейтр эндоэкзо! Энергии выделяется меньше, чем в случае № 1
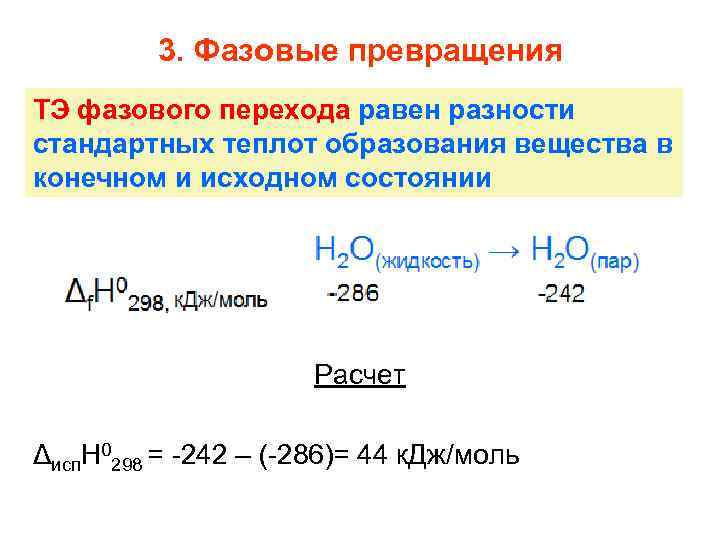
3. Фазовые превращения ТЭ фазового перехода равен разности стандартных теплот образования вещества в конечном и исходном состоянии Расчет Δисп. H 0298 = -242 – (-286)= 44 к. Дж/моль
![Теплоемкость [C] = Дж/К Истинная Средняя Связь между истинной и средней теплоемкостями: Теплоемкость [C] = Дж/К Истинная Средняя Связь между истинной и средней теплоемкостями:](https://present5.com/presentation/3/81651188_158778808.pdf-img/81651188_158778808.pdf-41.jpg)
Теплоемкость [C] = Дж/К Истинная Средняя Связь между истинной и средней теплоемкостями:
![Теплоемкость (продолжение) Удельная [Cуд]=Дж/г. К Молярная [Cм]=Дж/моль. К Связь между С и Суд где Теплоемкость (продолжение) Удельная [Cуд]=Дж/г. К Молярная [Cм]=Дж/моль. К Связь между С и Суд где](https://present5.com/presentation/3/81651188_158778808.pdf-img/81651188_158778808.pdf-42.jpg)
Теплоемкость (продолжение) Удельная [Cуд]=Дж/г. К Молярная [Cм]=Дж/моль. К Связь между С и Суд где С – истинная теплоемкость (Дж/К) m – масса вещества (г) С – удельная теплоемкость (Дж/г. К) Количество теплоты Q=m. CудΔt Q=CΔt
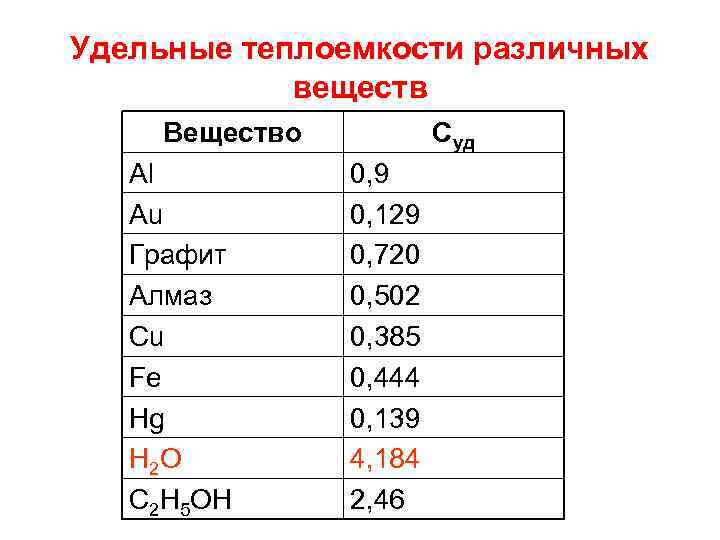
Удельные теплоемкости различных веществ Вещество Al Au Графит Алмаз Cu Fe Hg H 2 O C 2 H 5 OH Суд 0, 9 0, 129 0, 720 0, 502 0, 385 0, 444 0, 139 4, 184 2, 46

Теплоемкость (продолжение) Изохорная Изобарная Связь между Сv и Cp Идеальный газ ν=1 моль Cp = C v + R Формула Майера
![Физический смысл R [ R ] = Дж /моль К R = 8, 314 Физический смысл R [ R ] = Дж /моль К R = 8, 314](https://present5.com/presentation/3/81651188_158778808.pdf-img/81651188_158778808.pdf-45.jpg)
Физический смысл R [ R ] = Дж /моль К R = 8, 314 Дж/моль. К = 1, 987 кал/моль. К

Зависимость теплоемкости от температуры 1) Ср =a +b. T +c. T 2 + … 2) Ср =a +b. T +c/T 2 + … (более точное уравнение при высоких температурах)

Зависимость теплового эффекта химической реакции от температуры

Кирхгоф Густав Роберт (1824 -1887) — немецкий физик, иностранный членкорреспондент Петербургской АН (1862). Установил правила для электрической цепи, совместно с Р. В. Бунзеном заложил основы спектрального анализа (1859), открыл цезий (1860) и рубидий (1861). Ввел понятие абсолютно черного тела и открыл закон излучения. Труды по механике, математической физике. http: //astro. websib. ru/istor/9/Kirchhoff. jpg

Вывод уравнения Кирхгофа (1858) p = const
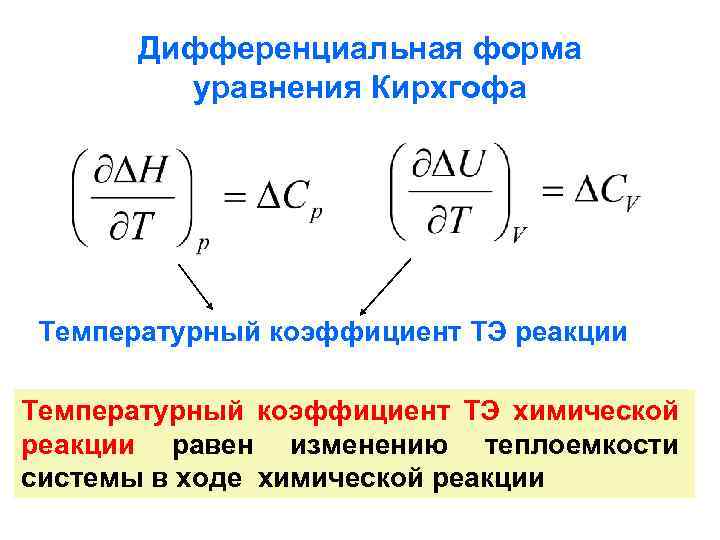
Дифференциальная форма уравнения Кирхгофа Температурный коэффициент ТЭ реакции Температурный коэффициент ТЭ химической реакции равен изменению теплоемкости системы в ходе химической реакции
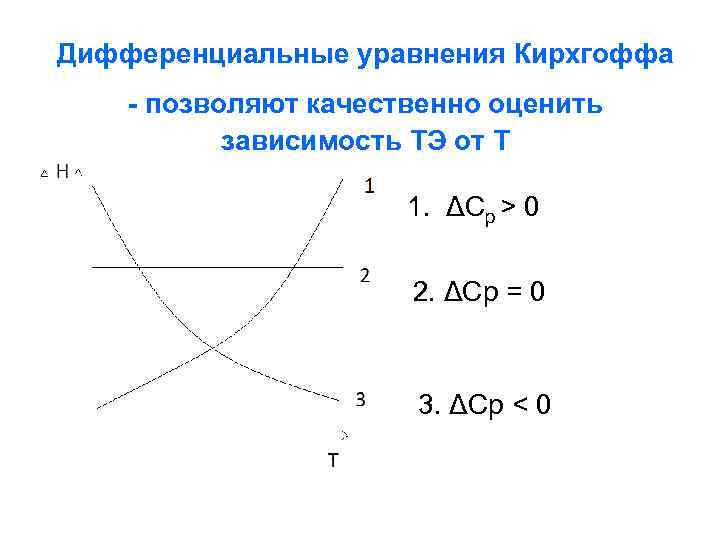
Дифференциальные уравнения Кирхгоффа - позволяют качественно оценить зависимость ТЭ от Т 1. ΔCp > 0 2. ΔCp = 0 3. ΔCp < 0

Интегральная форма уравнения Кирхгофа (применяется для вычислений тепловых эффектов при любых температурах) 298 - Т

(продолжение) 0 -Т

Соотношение между изобарным и изохорным ТЭ Qp =ΔH Qv=ΔU Qp –QV = ΔH – ΔU =pΔV Идеальный газ p. V = n. RT Qp –QV = Δn. RT pΔV = Δn. RT ΔH=ΔU + Δn. RT 1) Если Δn= 0, то ΔH=ΔU 2) если в реакции участвуют твердые и жидкие вещества, то при вычислении Δn они в расчет не принимаются.
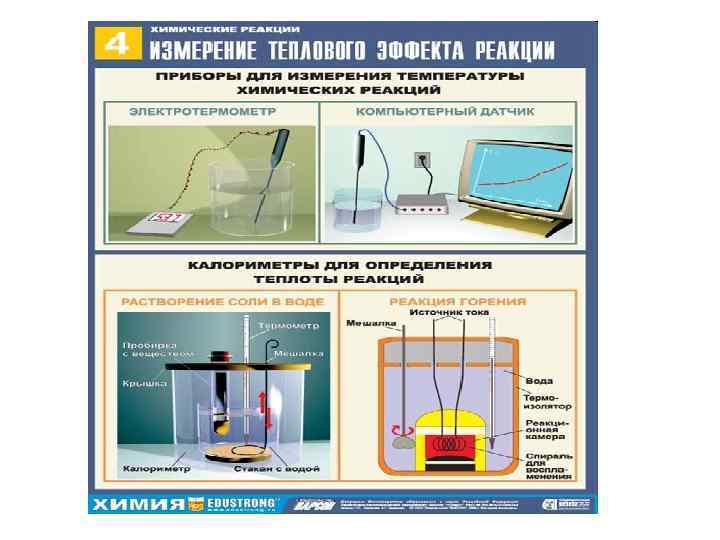
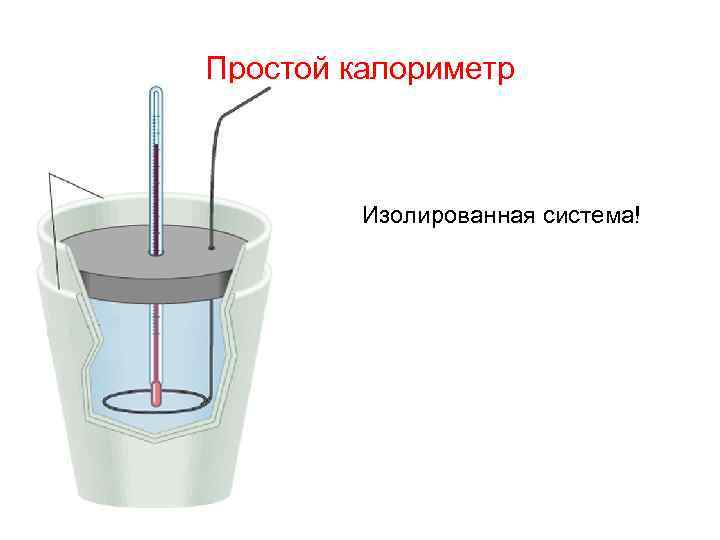
Простой калориметр Изолированная система!
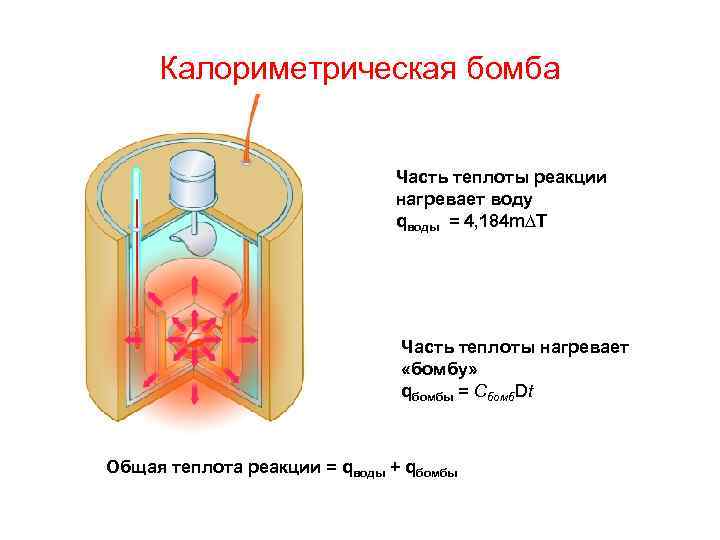
Калориметрическая бомба Часть теплоты реакции нагревает воду qводы = 4, 184 m∆T Часть теплоты нагревает «бомбу» qбомбы = Cбомб. Dt Общая теплота реакции = qводы + qбомбы

Эмпирические способы расчета ТЭ 1. Метод Караша 2. Метод введения поправки на заместитель 3. Формула Трутона

Список литературы • 1. Физическая и коллоидная химия: Учебник/Под ред. Проф. А. П. Беляева. М. : ГЭОТАР-Медиа, 2008. -704 с. • 2. Физическая химия. В 2 кн. Кн. 1/Под ред. К. С. Краснова - М: Высшая школа, 2001. -512 с. • 3. Стромберг А. Г. , Семченко Д. П. Физическая химия. М : Высшая школа, 1999.

Спасибо за внимание!
I закон термодинамики. Термохимия.ppt