3874202_Aminokislotuy.ppt
- Количество слайдов: 58

Курский государственный медицинский университет Кафедра биоорганической химии Аминокислоты. Пептиды и белки

Цель: Получить представление о взаимосвязи химического строения и биологической роли аминокислот, пептидов и белков

План лекции 1. Медико-биологическое значение аминокислот, пептидов и белков; 2. Строение, классификация аминокислот 3. Стереоизомерия α-аминокислот 4. Способы получения аминокислот 5. Общие и специфические химические свойства аминокислот 6. Химические свойства α-аминокислот in vitro; 7. Реакции α-аминокислот in vivo; 8. Первичная структура пептидов и белков; 9. Пространственное строение молекул белков.

Аминокислоты - это органические гетерофункциональные соединения, молекулы которых содержат одновременно карбоксильную группу-СООН и аминогруппу -NН 2 α R 1 СH O C OH NH 2 Например, глицин:
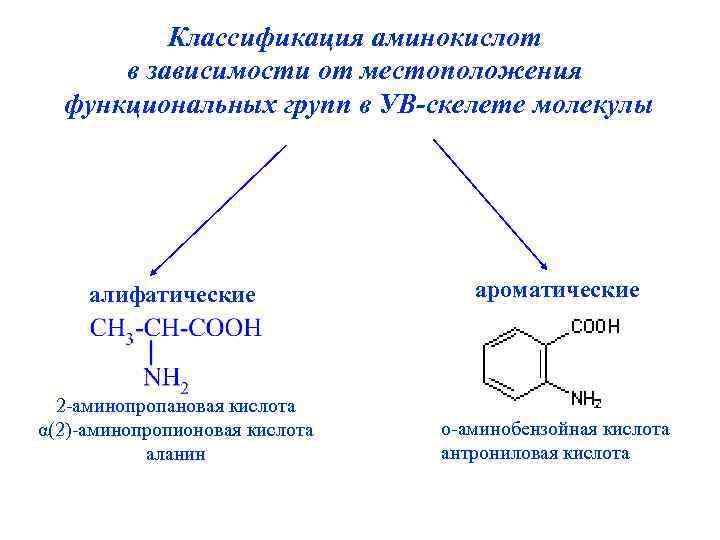
Классификация аминокислот в зависимости от местоположения функциональных групп в УВ-скелете молекулы алифатические ароматические 2 -аминопропановая кислота α(2)-аминопропионовая кислота аланин о-аминобензойная кислота антрониловая кислота
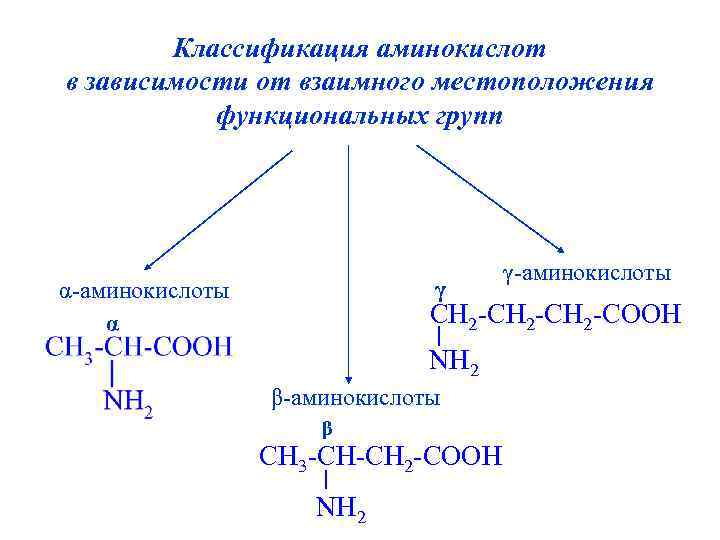
Классификация аминокислот в зависимости от взаимного местоположения функциональных групп γ α-аминокислоты α γ-аминокислоты CH 2 -CH 2 -COOH NH 2 β-аминокислоты β CH 3 -CH-CH 2 -COOH NH 2
Принципы классификации α-аминокислот Природа радикала По возможности синтеза Число функциональных групп (-СООН; -NH 2)
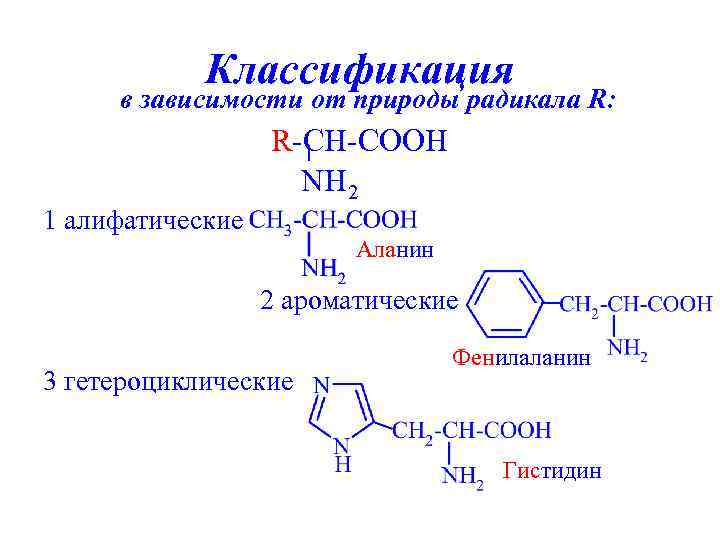
Классификация в зависимости от природы радикала R: R-CH-COOH NH 2 1 алифатические Аланин 2 ароматические 3 гетероциклические Фенилаланин Гистидин

Классификация алифатических α-аминокислот по содержанию «дополнительных» функциональных групп R-CH-COOH NH 2 Содержащие –ОН группу -серин (НО–СН 2–) Серосодержащие -цистеин (НS–СН 2–) -треонин (СН 3–СН–) -метионин (CH 3–S–CH 2–) ОН

Классификация в зависимости от числа карбоксильных и аминогрупп - Нейтральные – одна NH 2 и одна СООН группы Моноаминомонокарбоновые Аланин - Основные – две NH 2 и одна СООН группы Диаминомонокарбоновые Лизин - Кислые - одна NH 2 и две СООН группы Моноаминодикарбоновые Аспарагиновая кислота

Классификация α-аминокислот по возможности синтеза Заменимые синтезируются в организме Незаменимые не синтезируются в организме -валин -лейцин -изолейцин -лизин -треонин -метионин -фенилаланин -триптофан
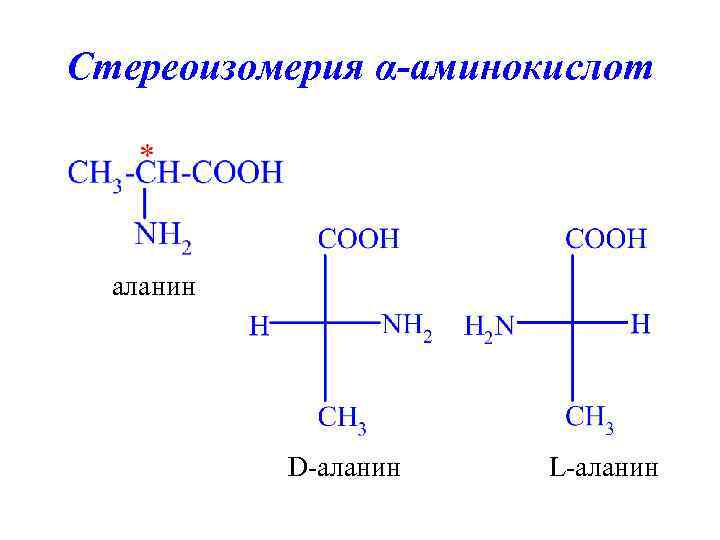
Стереоизомерия α-аминокислот аланин D-аланин L-аланин

Физические свойства Аминокислоты: R бесцветные кристаллические вещества R сладкие на вкус R хорошо растворяются в воде 0 R имеют температуру плавления 220 0 315 С.
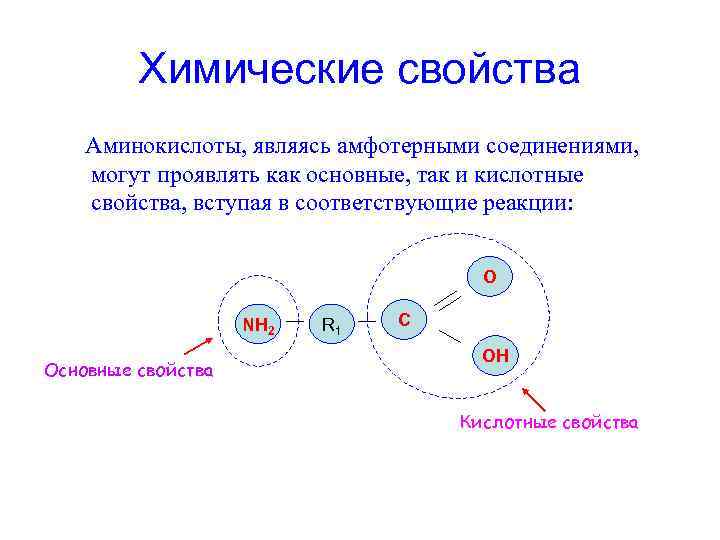
Химические свойства Аминокислоты, являясь амфотерными соединениями, могут проявлять как основные, так и кислотные свойства, вступая в соответствующие реакции: О NH 2 Основные свойства R 1 C OH Кислотные свойства
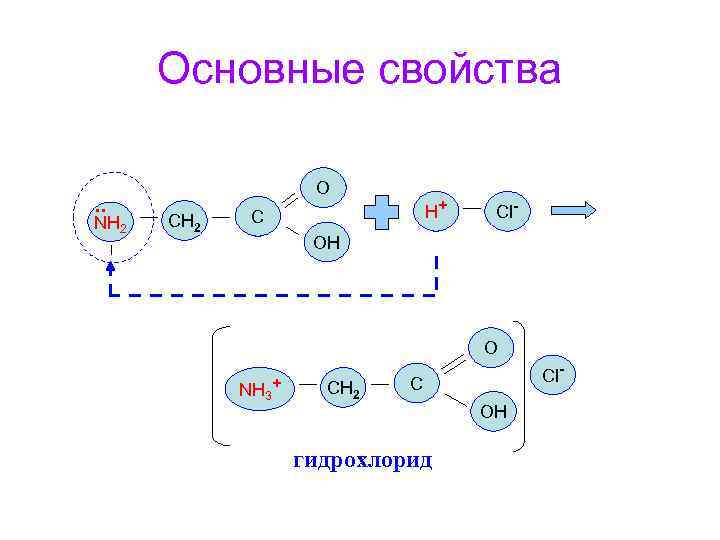
Основные свойства. . NH 2 О CH 2 H+ C Cl- OH О NH 3+ CH 2 Cl- C OH гидрохлорид
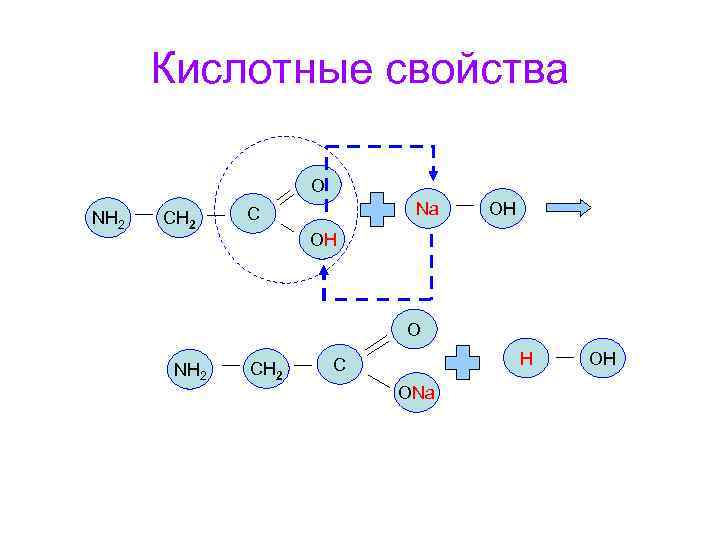
Кислотные свойства O NH 2 CH 2 Na C OH OH О NH 2 CH 2 H C ONa OH
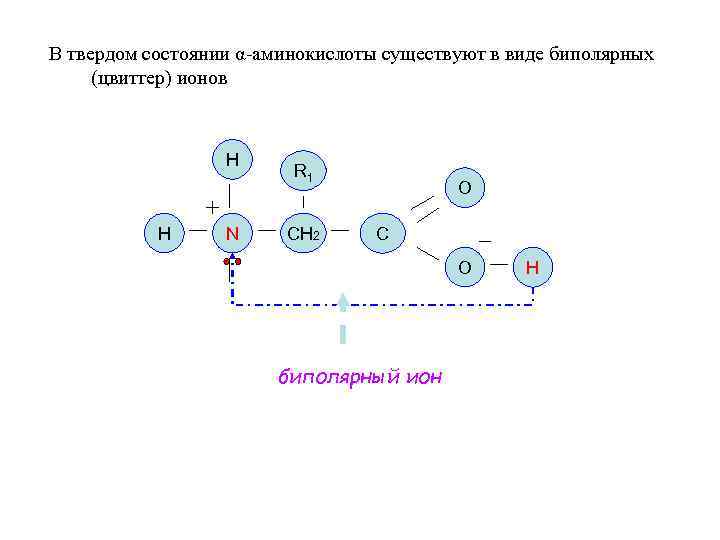
В твердом состоянии α-аминокислоты существуют в виде биполярных (цвиттер) ионов H H N R 1 СН 2 O C O биполярный ион H
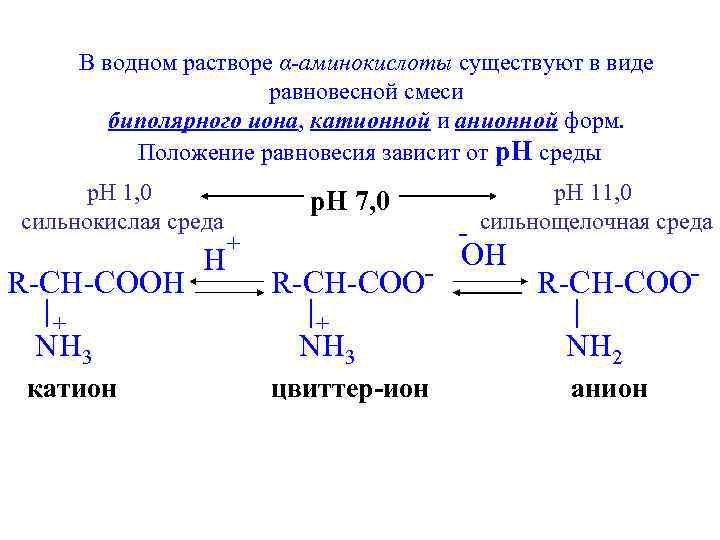
В водном растворе α-аминокислоты существуют в виде равновесной смеси биполярного иона, катионной и анионной форм. Положение равновесия зависит от p. H среды p. H 1, 0 сильнокислая среда R-CH-COOH + NH 3 катион H p. H 7, 0 + R-CH-COO+ NH 3 цвиттер-ион p. H 11, 0 сильнощелочная среда OH R-CH-COONH 2 анион

Изоэлектрическая точка α-аминокислоты – это то значение p. H раствора, при котором большинство молекул существуют в виде биполярных ионов, а концентрации катионной и анионной форм минимальны и равны.
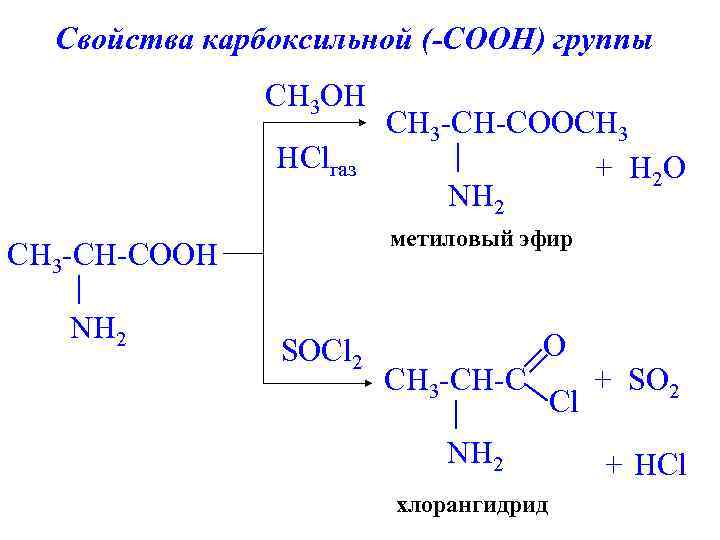
Свойства карбоксильной (-СООН) группы CH 3 OH HClгаз метиловый эфир CH 3 -CH-COOH NH 2 CH 3 -CH-COOCH 3 + H 2 O NH 2 SOCl 2 CH 3 -CH-C O NH 2 хлорангидрид Cl + SO 2 + HCl
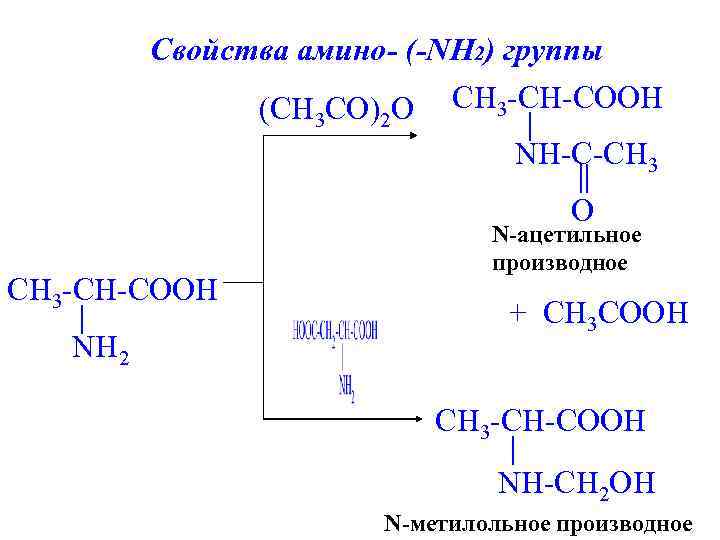
Свойства амино- (-NH 2) группы (CH СO) O CH 3 -CH-COOH 3 2 NH-C-CH 3 O CH 3 -CH-COOH NH 2 N-ацетильное производное + CH 3 COOH CH 3 -CH-COOH NH-CH 2 OH N-метилольное производное
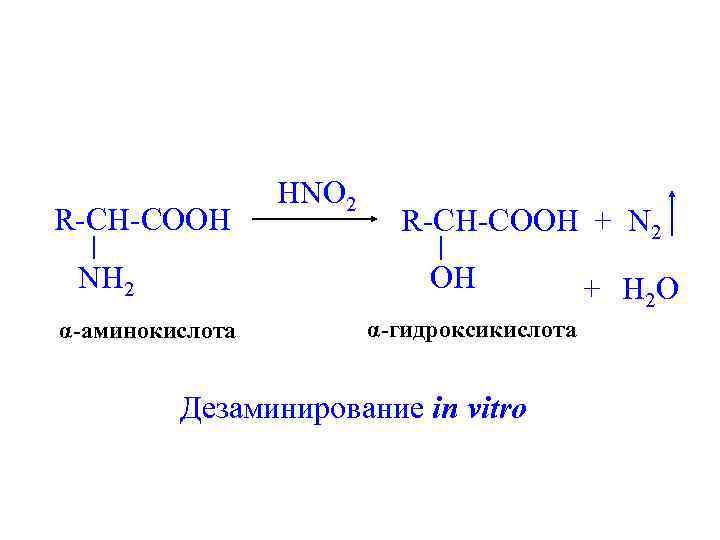
R-CH-COOH HNO 2 R-CH-COOH + N 2 OH NH 2 α-аминокислота α-гидроксикислота Дезаминирование in vitro + H 2 O
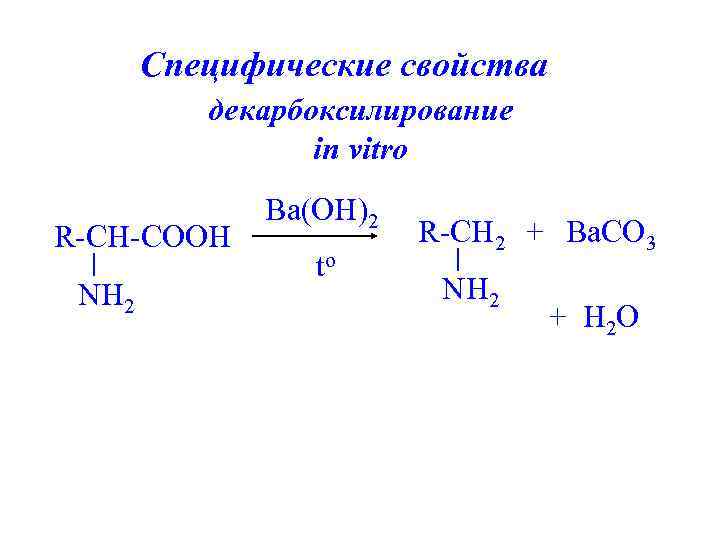
Специфические свойства декарбоксилирование in vitro R-CH-COOH NH 2 Ba(OH)2 to R-CH 2 + Ba. CO 3 NH 2 + H 2 O
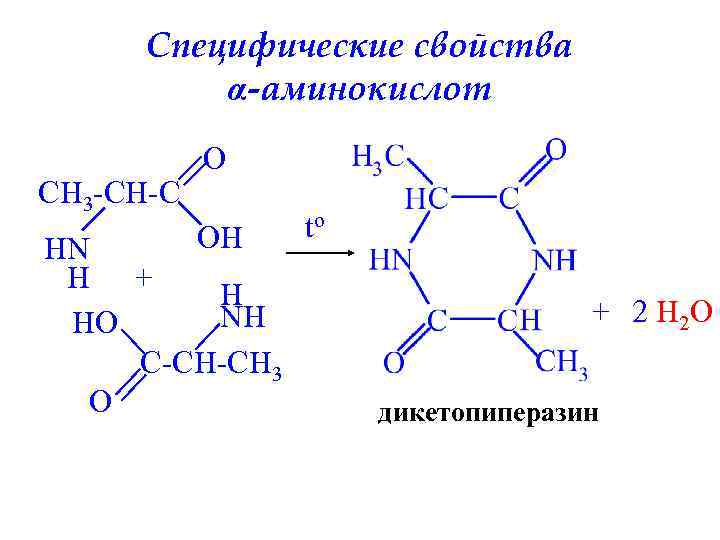
Специфические свойства α-аминокислот CH 3 -CH-C O OH HN H + H NH HO C-CH-CH 3 O to + 2 H 2 O дикетопиперазин
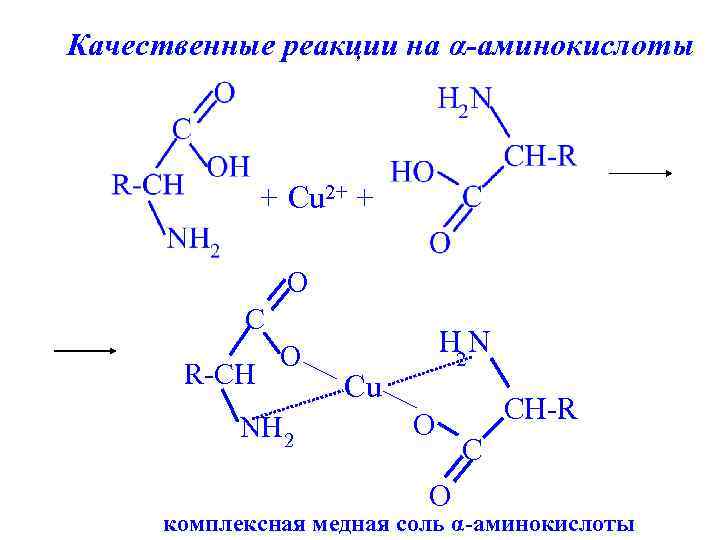
Качественные реакции на α-аминокислоты + Cu 2+ + O C R-CH O NH 2 H 2 N Cu O O CH-R C комплексная медная соль α-аминокислоты
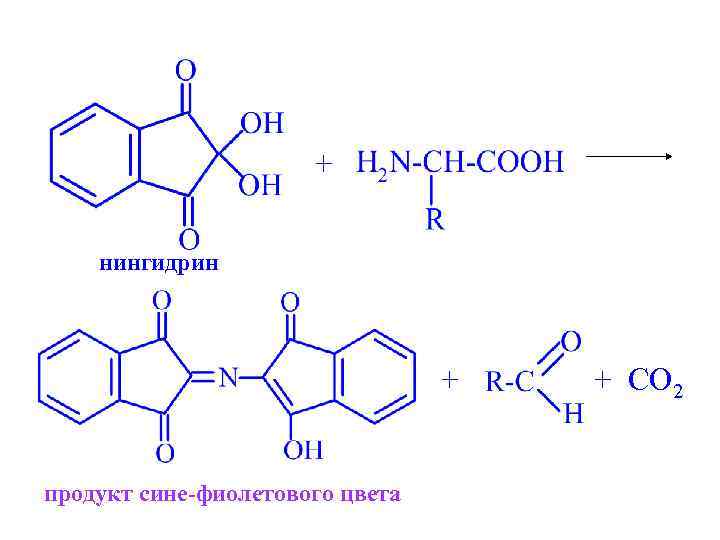
+ нингидрин + продукт сине-фиолетового цвета + CO 2
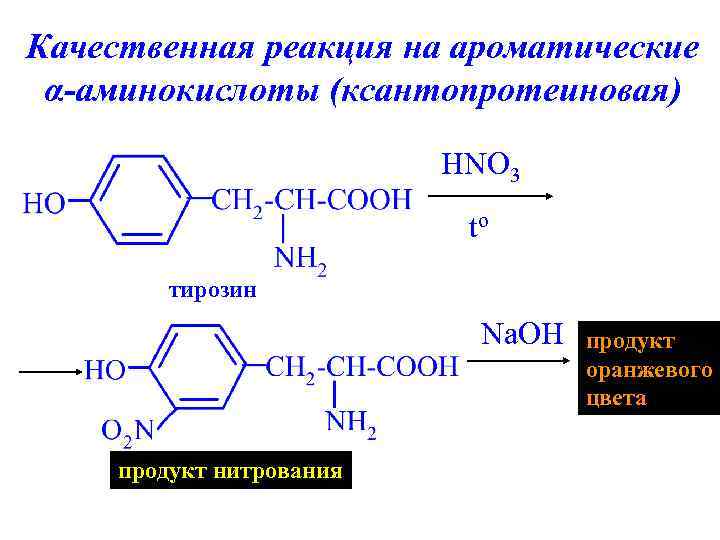
Качественная реакция на ароматические α-аминокислоты (ксантопротеиновая) HNO 3 to тирозин Na. OH продукт нитрования продукт оранжевого цвета
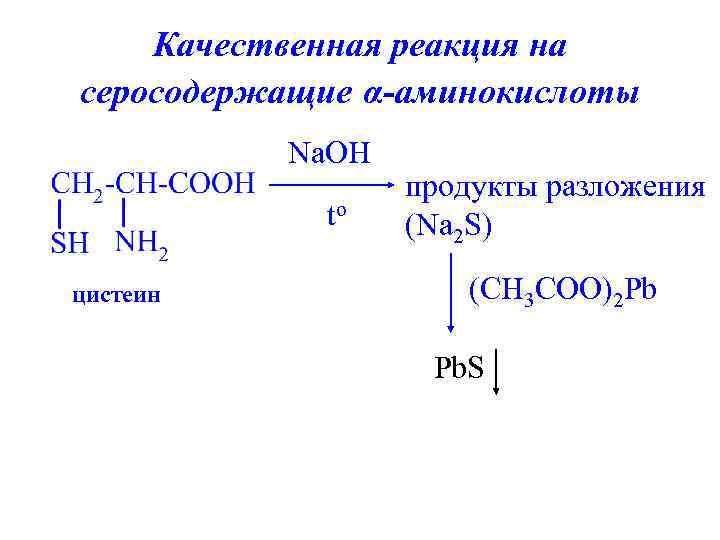
Качественная реакция на серосодержащие α-аминокислоты Na. OH to цистеин продукты разложения (Na 2 S) (CH 3 COO)2 Pb Pb. S
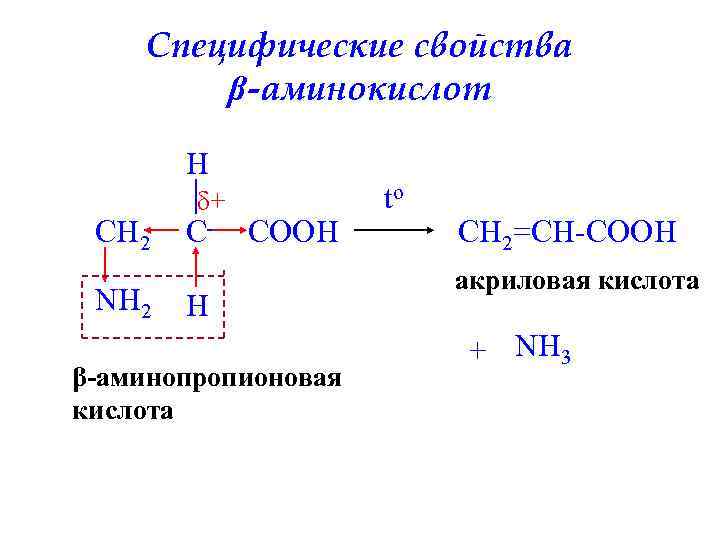
Специфические свойства β-аминокислот H CH 2 NH 2 δ+ C COOH H β-аминопропионовая кислота to CH 2=CH-COOH акриловая кислота + NH 3
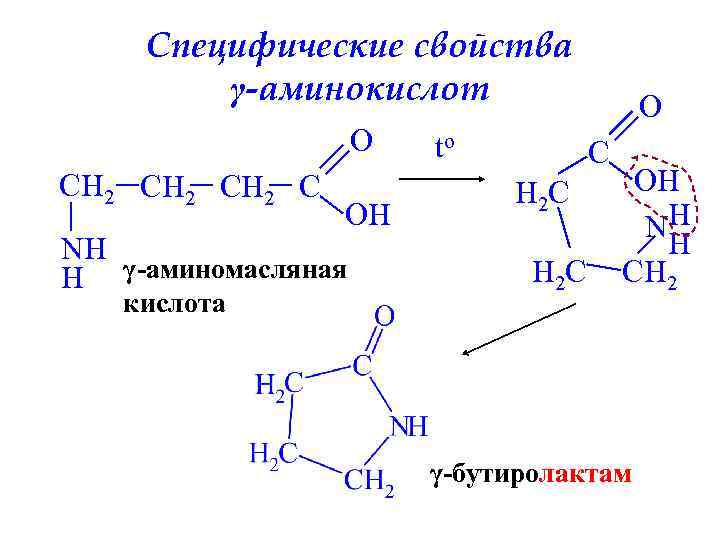
Специфические свойства γ-аминокислот O CH 2 C OH NH H γ-аминомасляная кислота to O C H 2 C OH NH H CH 2 γ-бутиролактам
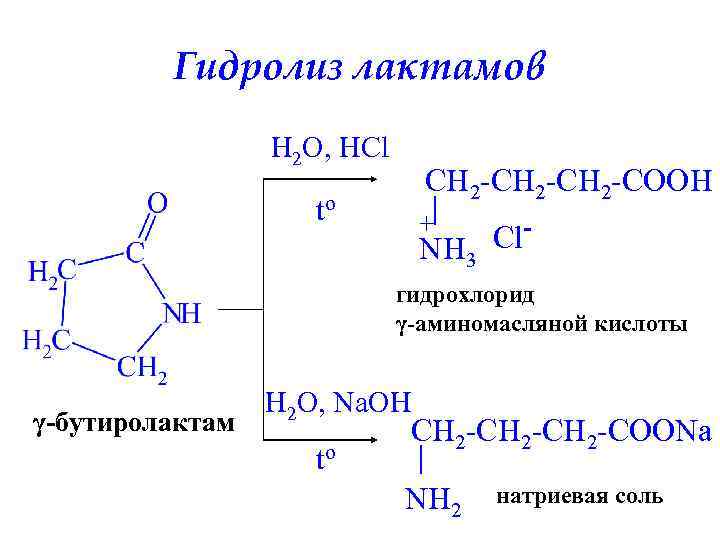
Гидролиз лактамов H 2 O, HCl CH 2 -CH 2 -COOH to + Cl. NH 3 гидрохлорид γ-аминомасляной кислоты γ-бутиролактам H 2 O, Na. OH to CH 2 -CH 2 -COONa NH 2 натриевая соль

Реакции α-аминокислот in vivo • декарбоксилирование • дезаминирование - окислительное; - неокислительное • переаминирование • образование пептидной связи
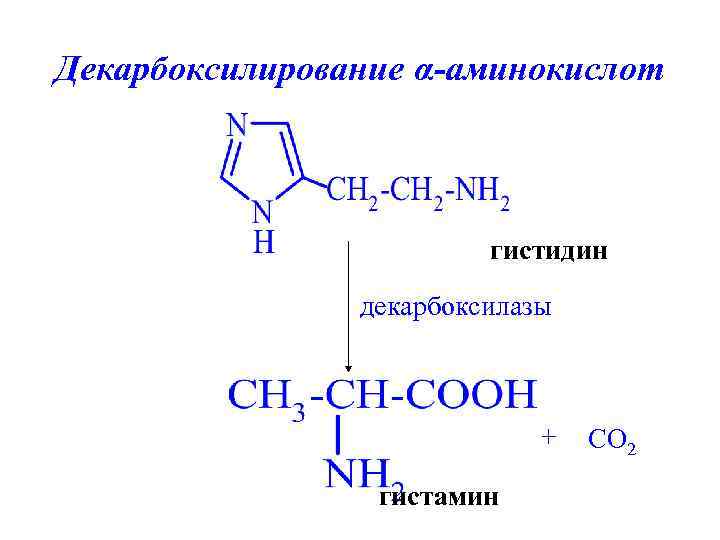
Декарбоксилирование α-аминокислот гистидин декарбоксилазы + гистамин CO 2

Неокислительное дезаминирование аспарагиновая кислота аспартаза + NH 3 фумаровая кислота
![Окислительное дезаминирование [O] фермент аланин H 2 O α-иминокислота + NH 3 фермент пировиноградная Окислительное дезаминирование [O] фермент аланин H 2 O α-иминокислота + NH 3 фермент пировиноградная](https://present5.com/presentation/11636707_437854751/image-35.jpg)
Окислительное дезаминирование [O] фермент аланин H 2 O α-иминокислота + NH 3 фермент пировиноградная кислота
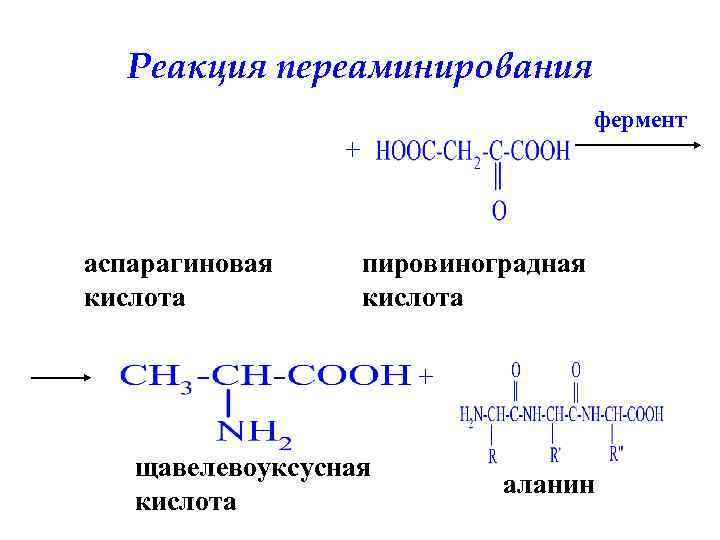
Реакция переаминирования фермент + аспарагиновая кислота пировиноградная кислота + щавелевоуксусная кислота аланин

Методы количественного определения α-аминокислот - метод формольного титрования; - метод Фишера; - метод Ван-Слайка; - электрофорез

Пептиды и белки
Медико-биологическое значение пептидов и белков Регуляторная функция (ферменты) Защитная функция (иммуноглобулины) Транспортная функция (гемоглобин) Структурная функция (коллаген)
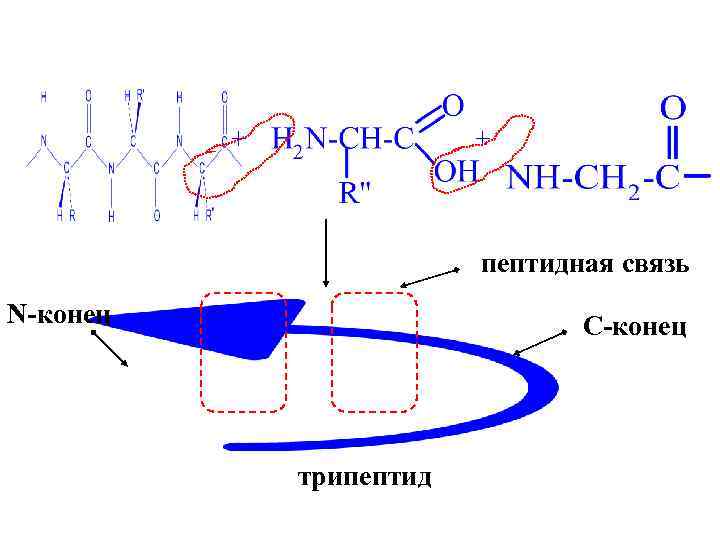
+ + пептидная связь N-конец C-конец трипептид
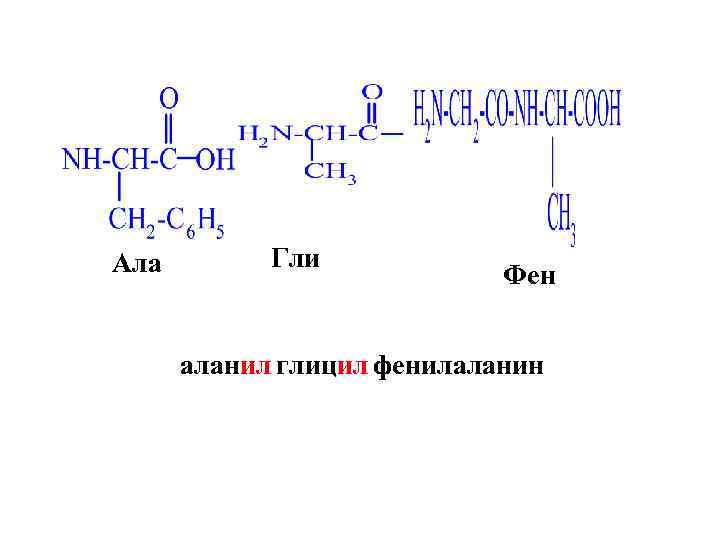
Ала Гли Фен аланил глицил фенилаланин
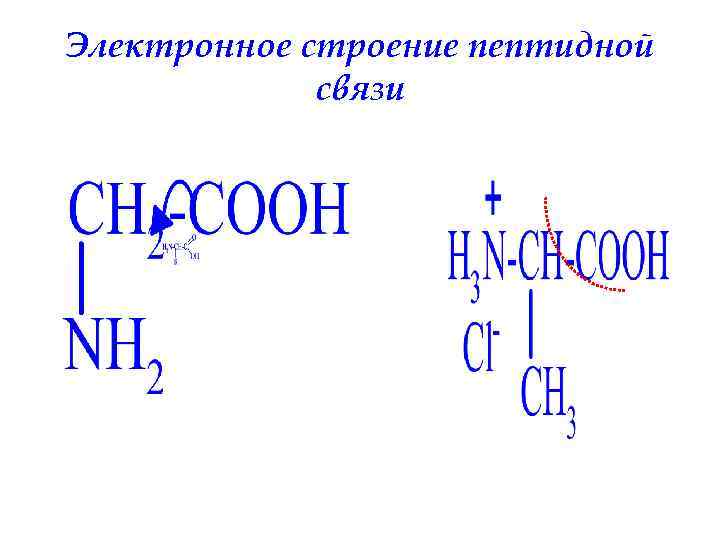
Электронное строение пептидной связи

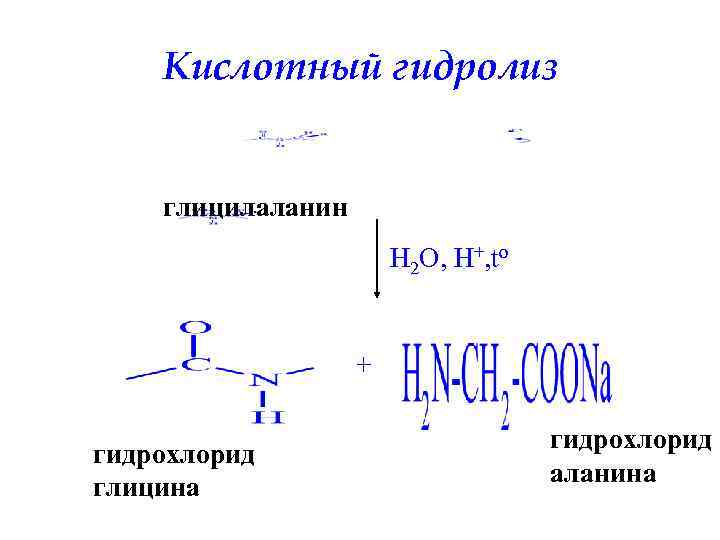
Кислотный гидролиз глицилаланин H 2 O, H+, to + гидрохлорид глицина гидрохлорид аланина

Щелочной гидролиз глицилаланин H 2 O, Na. OH, to + натриевая соль глицина натриевая соль аланина
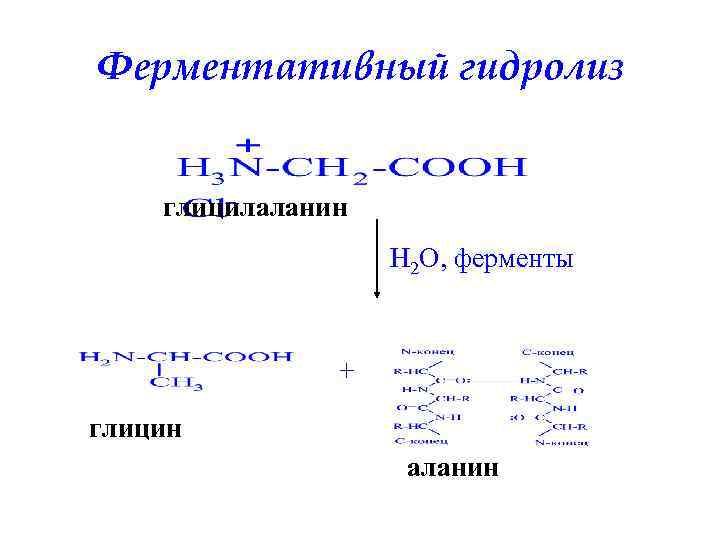
Ферментативный гидролиз глицилаланин H 2 O, ферменты + глицин аланин
Качественная реакция на пептидные связи Биуретовая реакция Белок + Cu(OH)2 красно-фиолетовое окрашивание
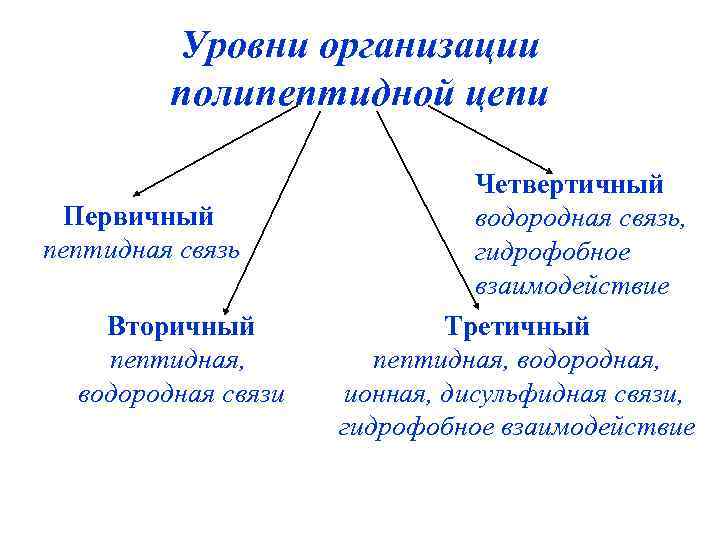
Уровни организации полипептидной цепи Первичный пептидная связь Вторичный пептидная, водородная связи Четвертичный водородная связь, гидрофобное взаимодействие Третичный пептидная, водородная, ионная, дисульфидная связи, гидрофобное взаимодействие
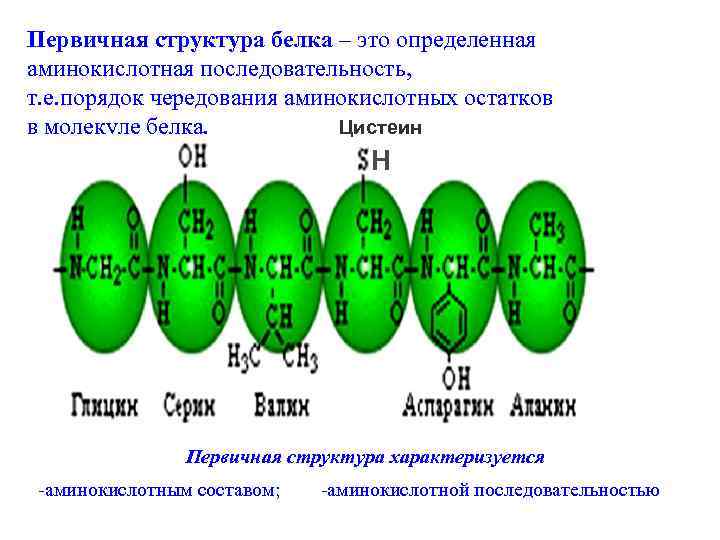
Первичная структура белка – это определенная аминокислотная последовательность, т. е. порядок чередования аминокислотных остатков в молекуле белка. Цистеин Н Первичная структура характеризуется -аминокислотным составом; -аминокислотной последовательностью

Вторичная структура белка – определенное пространственное расположение полипептидной цепи. • α-спираль • β-складчатая структура

α-спираль На один виток спирали – 3, 6 аминокислотных остатка.
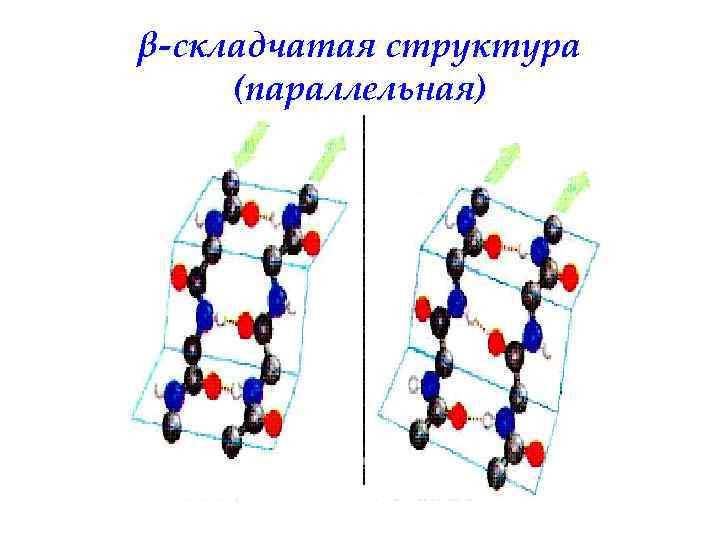
β-складчатая структура (параллельная)

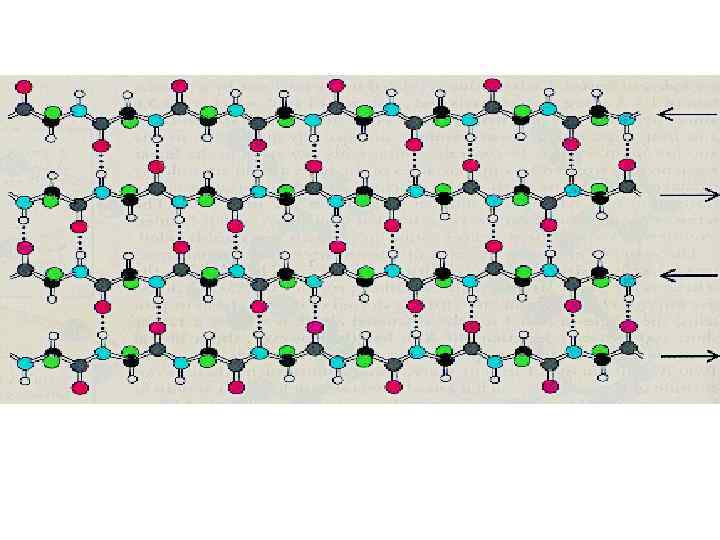
β-складчатая структура (антипараллельная)
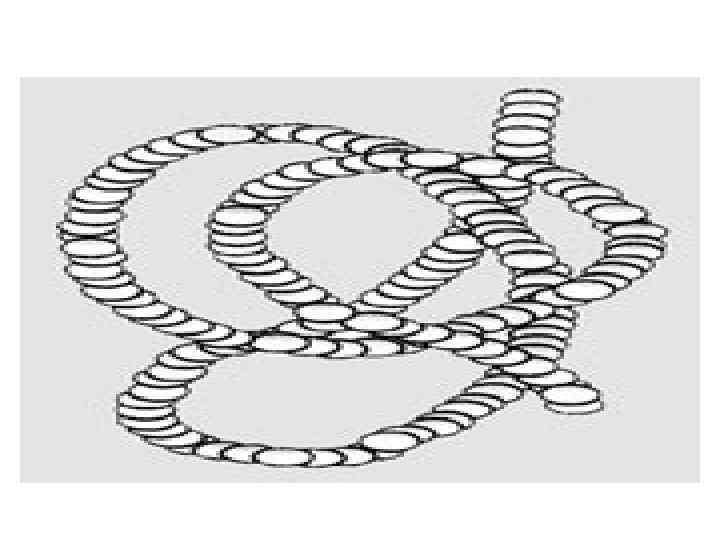

Третичная структура белка
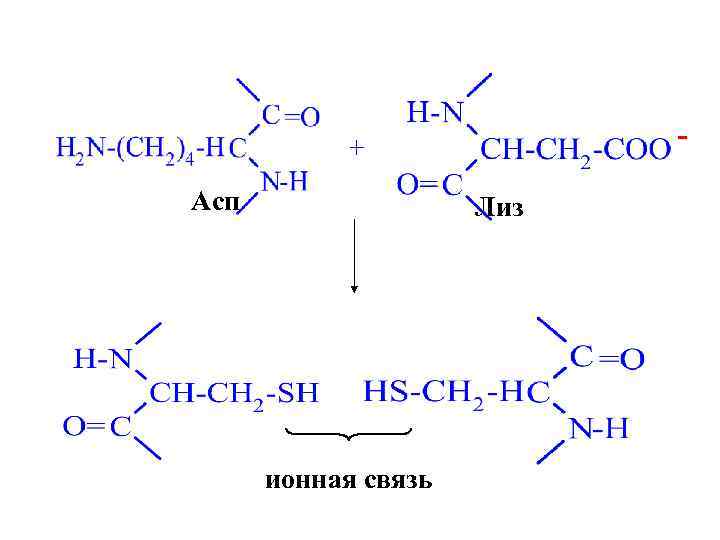
+ Асп Лиз ионная связь
![+ Цис [O] Цис + H 2 O дисульфидный мостик + Цис [O] Цис + H 2 O дисульфидный мостик](https://present5.com/presentation/11636707_437854751/image-58.jpg)
+ Цис [O] Цис + H 2 O дисульфидный мостик
3874202_Aminokislotuy.ppt