Лекция 11 - ФР-ГС.ppt
- Количество слайдов: 16

Курс «Общая химия» Лектор: проф. Майстренко Валерий Николаевич Башкирский государственный университет Кафедра неорганической химии Тел. : 229 -97 -08; E-mail: V_maystrenko@mail. ru 1

Лекция № 11 Фазовые равновесия (равновесие в гетерогенных системах) 2

3
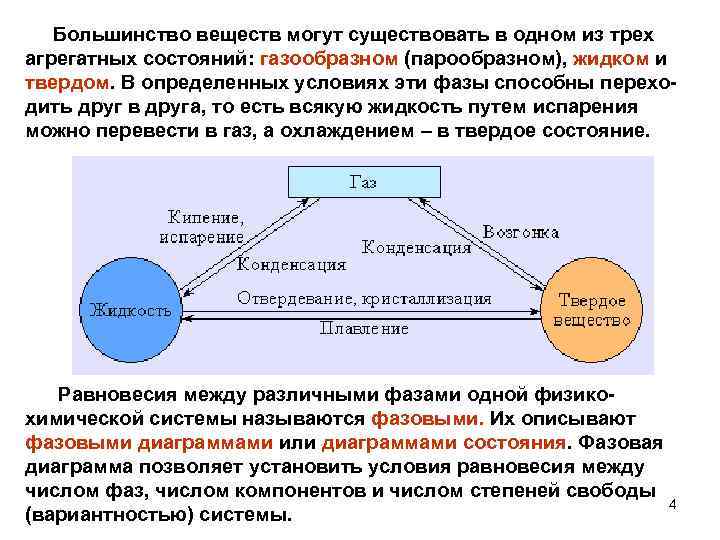
Большинство веществ могут существовать в одном из трех агрегатных состояний: газообразном (парообразном), жидком и твердом. В определенных условиях эти фазы способны переходить друг в друга, то есть всякую жидкость путем испарения можно перевести в газ, а охлаждением – в твердое состояние. Равновесия между различными фазами одной физикохимической системы называются фазовыми. Их описывают фазовыми диаграммами или диаграммами состояния. Фазовая диаграмма позволяет установить условия равновесия между числом фаз, числом компонентов и числом степеней свободы 4 (вариантностью) системы.

Фаза (Ф) – гомогенная (однородная по химическому составу и термодинамическим свойствам) часть системы, отделенная от других частей поверхностью раздела. Так, два нерастворимых друг в друге твердых вещества, как и две несмешивающиеся жидкости, образуют две фазы. Компоненты (К) – химически индивидуальные вещества, наименьшее число которых достаточно для образования фаз системы. Число компонентов определяется количеством индивидуальных веществ в системе за вычетом числа возможных между ними обратимых взаимодействий. Например, система из трех индивидуальных веществ H 2 O, H 2, O 2 будет двухкомпонентной, поскольку для образования всех фаз достаточно любых двух веществ: H 2 + ½O 2 ⇆ H 2 O По числу компонентов системы делятся на одно-, двух-, трех- и многокомпонентные. 5
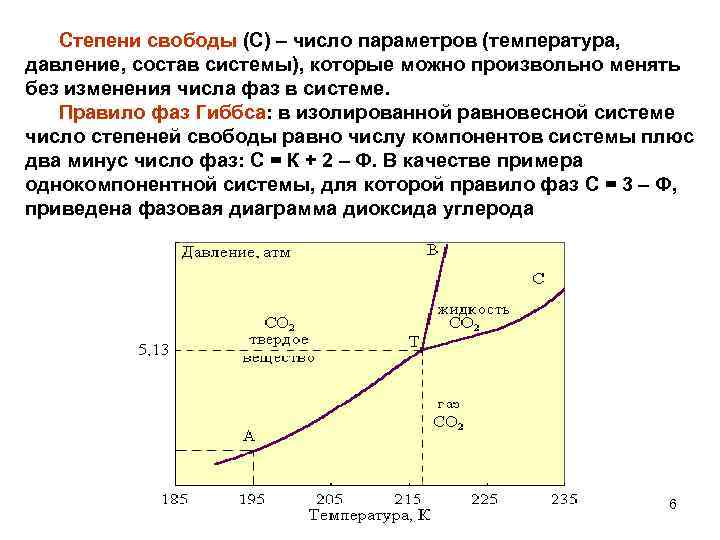
Степени свободы (С) – число параметров (температура, давление, состав системы), которые можно произвольно менять без изменения числа фаз в системе. Правило фаз Гиббса: в изолированной равновесной системе число степеней свободы равно числу компонентов системы плюс два минус число фаз: С = К + 2 – Ф. В качестве примера однокомпонентной системы, для которой правило фаз С = 3 – Ф, приведена фазовая диаграмма диоксида углерода 6

При P < 5, 13 атм. CO 2 в жидком состоянии не может находится. При атмосферном давлении твердый диоксид углерода сублимирует при 195 K. Если один из параметров системы (температура или давление) имеет постоянное значение, то правило фаз принимает вид: C = K + 1 – Ф. Это уравнение используется при изучении конденсированных систем, состоящих только из твердых и жидких фаз, поскольку состояния равновесия в таких системах малочувствительны к изменению давления. Наибольшее практическое значение имеют изобарные диаграммы двухкомпонентных систем, содержащие только конденсированные фазы. Кривые охлаждения и диаграммы плавкости веществ 7
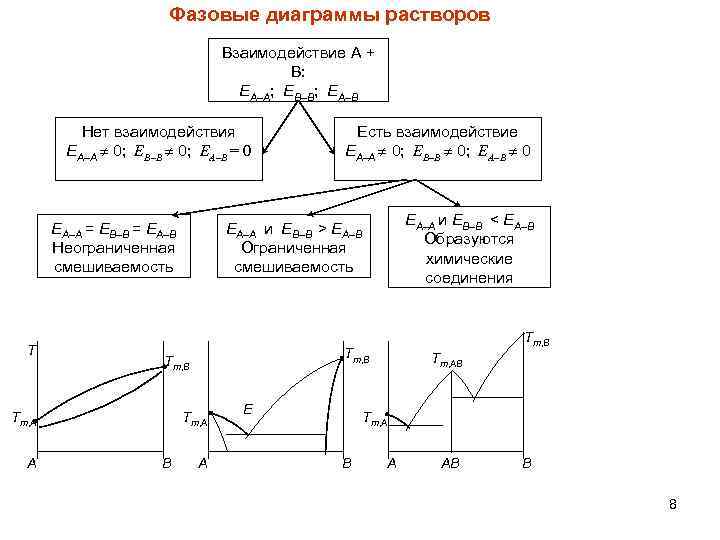
Фазовые диаграммы растворов Взаимодействие А + В: ЕА–А; ЕВ–В; ЕА–В Нет взаимодействия ЕА–А 0; ЕВ–В 0; ЕА–В = 0 ЕА–А = ЕВ–В = ЕА–В Неограниченная смешиваемость T А Тm, B Тm, A В ЕА–А и ЕВ–В < ЕА–В Образуются химические соединения ЕА–А и ЕВ–В > ЕА–В Ограниченная смешиваемость Тm, B Тm, A Есть взаимодействие ЕА–А 0; ЕВ–В 0; ЕА–В 0 А E Тm, AB Тm, A В А AВ В 8

Равновесия в растворах, содержащих осадки труднорастворимых электролитов 9

При образовании осадка сильного электролита между осадком и раствором устанавливается равновесие Ba. SO 4 ↓ ⇆ Ba+2 + SO 4 -2 Применив закон действующих масс, можно написать Для любого осадка трудно растворимого электролита Bx. Ay ⇆ x. B+y + y. A-x Для относительно хорошо растворимого электролита 10
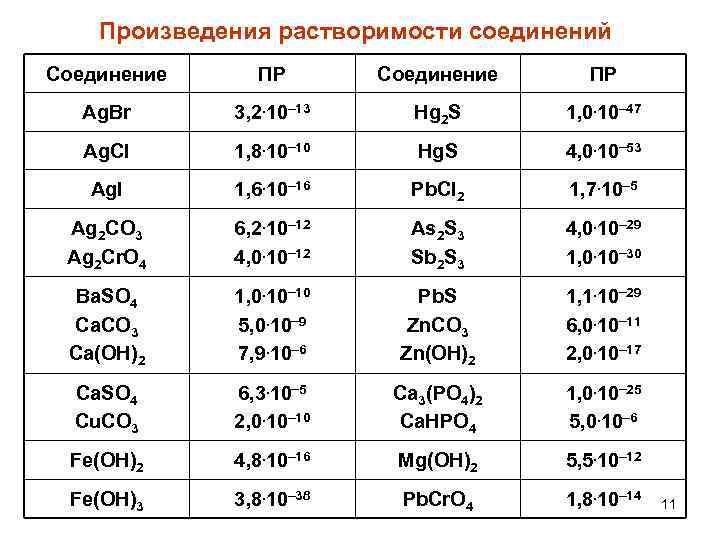
Произведения растворимости соединений Соединение ПР Ag. Br 3, 2. 10 13 Hg 2 S 1, 0. 10 47 Ag. Cl 1, 8. 10 10 Hg. S 4, 0. 10 53 Ag. I 1, 6. 10 16 Pb. Cl 2 1, 7. 10 5 Ag 2 CO 3 Ag 2 Cr. O 4 6, 2. 10 12 4, 0. 10 12 As 2 S 3 Sb 2 S 3 4, 0. 10 29 1, 0. 10 30 Ba. SO 4 Ca. CO 3 Ca(OH)2 1, 0. 10 10 5, 0. 10 9 7, 9. 10 6 Pb. S Zn. CO 3 Zn(OH)2 1, 1. 10 29 6, 0. 10 11 2, 0. 10 17 Ca. SO 4 Cu. CO 3 6, 3. 10 5 2, 0. 10 10 Ca 3(PO 4)2 Ca. HPO 4 1, 0. 10 25 5, 0. 10 6 Fe(OH)2 4, 8. 10 16 Mg(OH)2 5, 5. 10 12 Fe(OH)3 3, 8. 10 38 Pb. Cr. O 4 1, 8. 10 14 11

Растворимость труднорастворимых электролитов Bx. Ay ⇆ x. B+y + y. A-x S – растворимость электролита S – моль/л Поскольку а = С , то для любого электролита 12
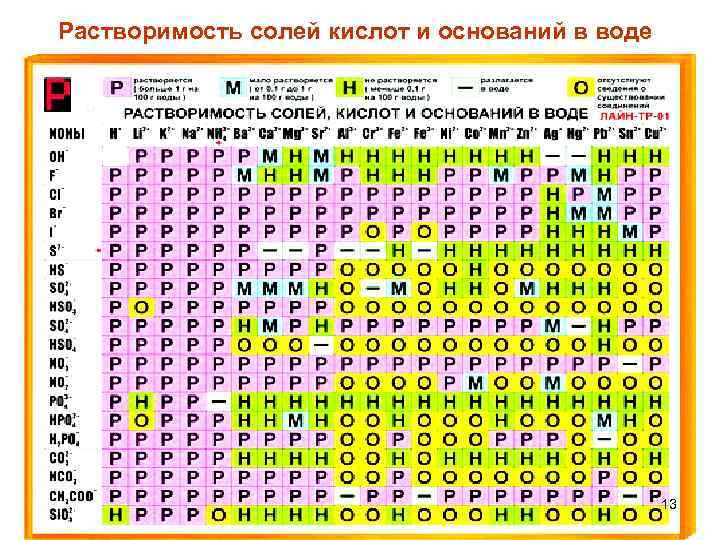
Растворимость солей кислот и оснований в воде 13

Солевой эффект - явление увеличения растворимости осадка при добавлении сильного электролита (не содержащего одноимённых ионов). В соответствии с уравнением Дебая. Хюккеля с увеличением ионной силы уменьшаются коэффициенты активности ионов и растворимость осадков возрастает. Введение в насыщенный раствор малорастворимого вещества раствора электролита, не содержащего одноименных ионов, вызывает увеличение растворимости осадка. Поскольку вводимые электролиты обычно представляют собой хорошо растворимые соли (КСl, Na. Cl, Na. N 03 и др. ), данное явление называют солевым эффектом. Растворимость осадка при этом возрастает с увеличением концентрации вводимого электролита; растворимость осадков, содержащих многозарядные ионы, изменяется более резко, чем в случае однозарядных. 14
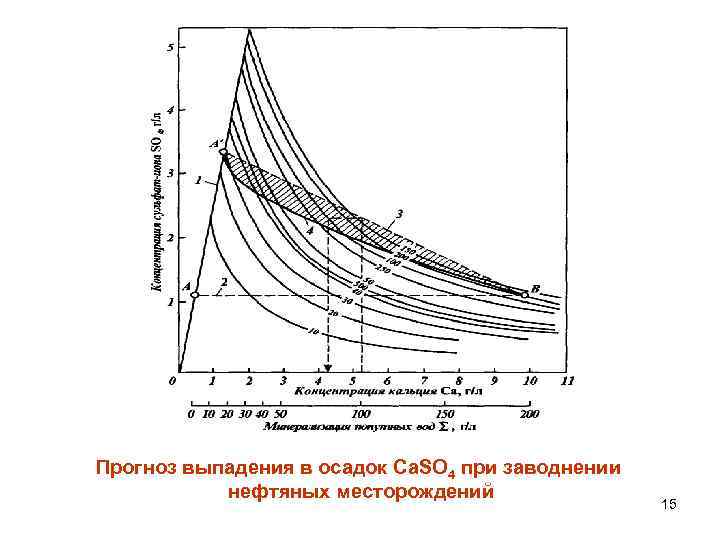
Прогноз выпадения в осадок Ca. SO 4 при заводнении нефтяных месторождений 15

Благодарю за внимание 16
Лекция 11 - ФР-ГС.ppt