Курс лекций по химии Тема: Металлы и


































































 Курс лекций по химии
Курс лекций по химии
 Тема: Металлы и их соединения • Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов)
Тема: Металлы и их соединения • Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов)
 Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • Если Ме активный восстановитель
Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • Если Ме активный восстановитель
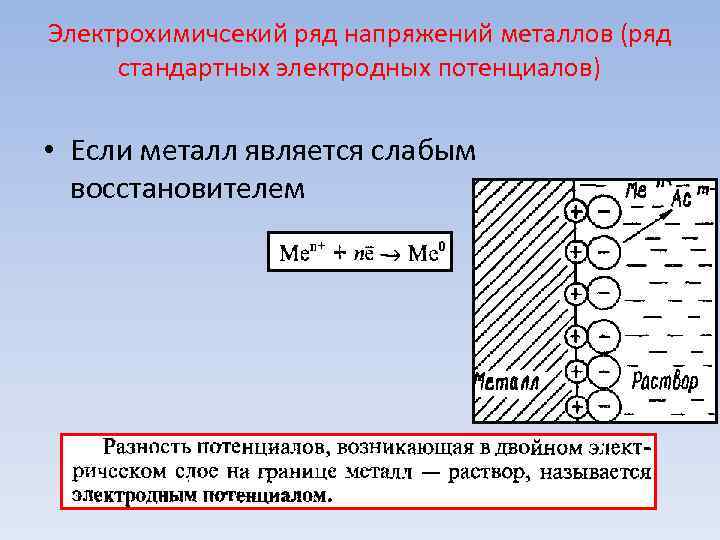
 Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • Если металл является слабым восстановителем
Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • Если металл является слабым восстановителем
 Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • Электродные потенциалы измеряют относительно стандартного водородного электрода, потенциал которого принимают за ноль.
Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • Электродные потенциалы измеряют относительно стандартного водородного электрода, потенциал которого принимают за ноль.
 Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) Восстановительная активность металлов уменьшается Окислительная активность увеличивается • Значение электродного потенциала количественно характеризует способность металла отдавать электроны, т. е. его восстановительные свойства
Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) Восстановительная активность металлов уменьшается Окислительная активность увеличивается • Значение электродного потенциала количественно характеризует способность металла отдавать электроны, т. е. его восстановительные свойства
 Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • На основании ряда напряжений можно сделать следующие заключения о химической активности металлов
Электрохимичсекий ряд напряжений металлов (ряд стандартных электродных потенциалов) • На основании ряда напряжений можно сделать следующие заключения о химической активности металлов
 Общая характеристика металлов
Общая характеристика металлов
 Общая характеристика металлов
Общая характеристика металлов
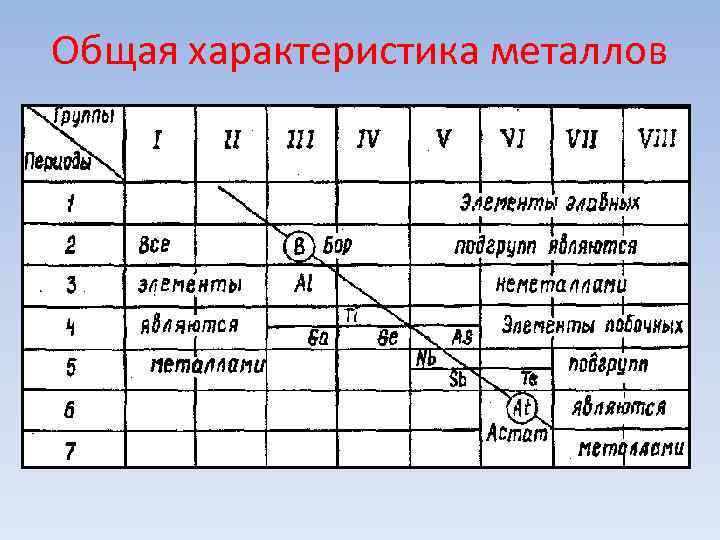
 Общая характеристика металлов • Деление элементов на металлы и неметаллы определяется различием в строении атомов
Общая характеристика металлов • Деление элементов на металлы и неметаллы определяется различием в строении атомов
 Общая характеристика металлов Физические свойства • При обычных условиях – твердые вещества (исключение ртуть) • Для всех металлов характерен металлический блеск и непрозрачность • Металлическая кристаллическая решетка • Между узлами решетки – свободные электроны • Высокая электро- и теплопроводность • Пластичны, упруги и прочны
Общая характеристика металлов Физические свойства • При обычных условиях – твердые вещества (исключение ртуть) • Для всех металлов характерен металлический блеск и непрозрачность • Металлическая кристаллическая решетка • Между узлами решетки – свободные электроны • Высокая электро- и теплопроводность • Пластичны, упруги и прочны
 Общая характеристика металлов Химические свойства металлов Атомы металлов более или менее легко отдают электроны, т. е. окисляются: Энергия ионизации!!! Атомы металлов не могут присоединять электроны являются только восстановителями
Общая характеристика металлов Химические свойства металлов Атомы металлов более или менее легко отдают электроны, т. е. окисляются: Энергия ионизации!!! Атомы металлов не могут присоединять электроны являются только восстановителями
 Общая характеристика металлов • Взаимодействие с простыми веществами
Общая характеристика металлов • Взаимодействие с простыми веществами
 Общая характеристика металлов • Взаимодействие со сложными веществами
Общая характеристика металлов • Взаимодействие со сложными веществами
 Общая характеристика металлов Оксиды и гидроксиды металлов Наиболее активные металлы – основные оксиды и сильные основания (щелочи) Некоторые металлы дают амфотерные оксиды и гидроксиды
Общая характеристика металлов Оксиды и гидроксиды металлов Наиболее активные металлы – основные оксиды и сильные основания (щелочи) Некоторые металлы дают амфотерные оксиды и гидроксиды
 Общая характеристика металлов • Общие способы получения металлов Металлургия! Любой металлургический процесс – процесс восстановления ионов металла с помощью различных восстановителей. Пирометаллургия – получение Ме из их соединений при высоких t с помощью различных восстановителей
Общая характеристика металлов • Общие способы получения металлов Металлургия! Любой металлургический процесс – процесс восстановления ионов металла с помощью различных восстановителей. Пирометаллургия – получение Ме из их соединений при высоких t с помощью различных восстановителей
 Общая характеристика металлов Металлургия! Гидрометаллургия Электрометаллургия – получение Ме электролизом растворов или расплавов их соединений
Общая характеристика металлов Металлургия! Гидрометаллургия Электрометаллургия – получение Ме электролизом растворов или расплавов их соединений
 Металлы главных подгрупп I и II групп. § Относятся к s-элементам § На внешнем электронном слое по 1 и по 2 электрона § В свободном состоянии в природе не встречаются § Все металлы серебристо-белого цвета § Имеют низкие температуры кипения и плавления
Металлы главных подгрупп I и II групп. § Относятся к s-элементам § На внешнем электронном слое по 1 и по 2 электрона § В свободном состоянии в природе не встречаются § Все металлы серебристо-белого цвета § Имеют низкие температуры кипения и плавления
 Металлы главных подгрупп I и II групп. • Получение
Металлы главных подгрупп I и II групп. • Получение
 Металлы главных подгрупп I и II групп.
Металлы главных подгрупп I и II групп.
 Металлы главных подгрупп I и II групп.
Металлы главных подгрупп I и II групп.
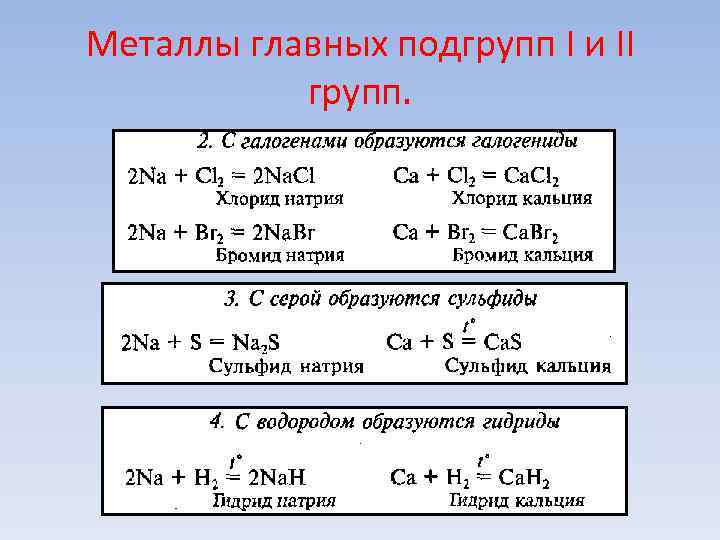
 Металлы главных подгрупп I и II групп. • Химические свойства • Самые активные и сильные восстановители I. Взаимодействие Na и Ca с неметаллами
Металлы главных подгрупп I и II групп. • Химические свойства • Самые активные и сильные восстановители I. Взаимодействие Na и Ca с неметаллами
 Металлы главных подгрупп I и II групп.
Металлы главных подгрупп I и II групп.
 Металлы главных подгрупп I и II групп. II. Взаимодействие Na и Ca со сложными веществами
Металлы главных подгрупп I и II групп. II. Взаимодействие Na и Ca со сложными веществами
 Металлы главных подгрупп I и II групп. • Оксиды и гидроксиды щелочных и щелочноземельных металлов
Металлы главных подгрупп I и II групп. • Оксиды и гидроксиды щелочных и щелочноземельных металлов
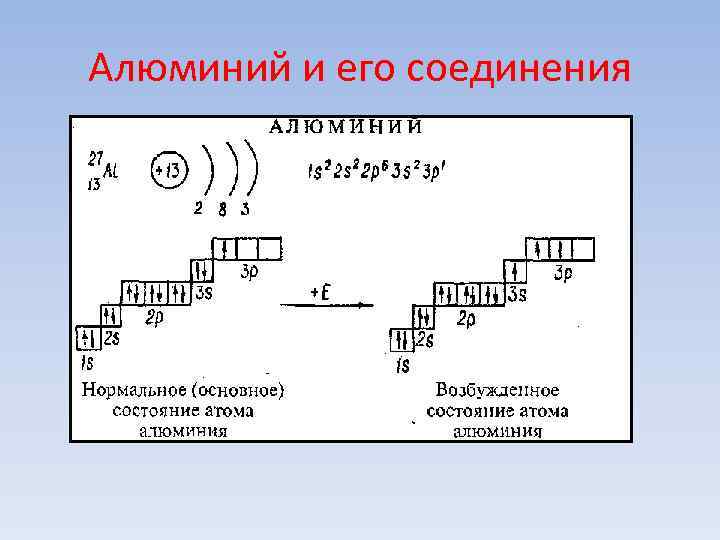
 Алюминий и его соединения • Общая характеристика главной подгруппы III группы • На внешнем электронном слое з электрона • р-элементы • Высшая степень окисления +3 • Образуют амфотерные оксиды и гидроксиды
Алюминий и его соединения • Общая характеристика главной подгруппы III группы • На внешнем электронном слое з электрона • р-элементы • Высшая степень окисления +3 • Образуют амфотерные оксиды и гидроксиды
 Алюминий и его соединения
Алюминий и его соединения
 Алюминий и его соединения • Получение
Алюминий и его соединения • Получение
 Алюминий и его соединения • Химические свойства Взаимодействие с простыми веществами
Алюминий и его соединения • Химические свойства Взаимодействие с простыми веществами
 Алюминий и его соединения
Алюминий и его соединения
 Алюминий и его соединения Взаимодействие алюминия со сложными веществами
Алюминий и его соединения Взаимодействие алюминия со сложными веществами
 Алюминий и его соединения
Алюминий и его соединения
 Алюминий и его соединения
Алюминий и его соединения
 Алюминий и его соединения • Оксид алюминия • Проявляет амфотерные свойства • Взаимодействует с кислотами и основаниями
Алюминий и его соединения • Оксид алюминия • Проявляет амфотерные свойства • Взаимодействует с кислотами и основаниями
 Алюминий и его соединения • Гидроксид алюминия • Проявляет амфотерные свойства • Взаимодействует с кислотами и основаниями
Алюминий и его соединения • Гидроксид алюминия • Проявляет амфотерные свойства • Взаимодействует с кислотами и основаниями
 Железо и его соединения • Общая характеристика § Железо, кобальт, никель – семейство железа § Остальные 6 Ме – платиновые Ме § d-элементы § Степени окисления +2, +3
Железо и его соединения • Общая характеристика § Железо, кобальт, никель – семейство железа § Остальные 6 Ме – платиновые Ме § d-элементы § Степени окисления +2, +3
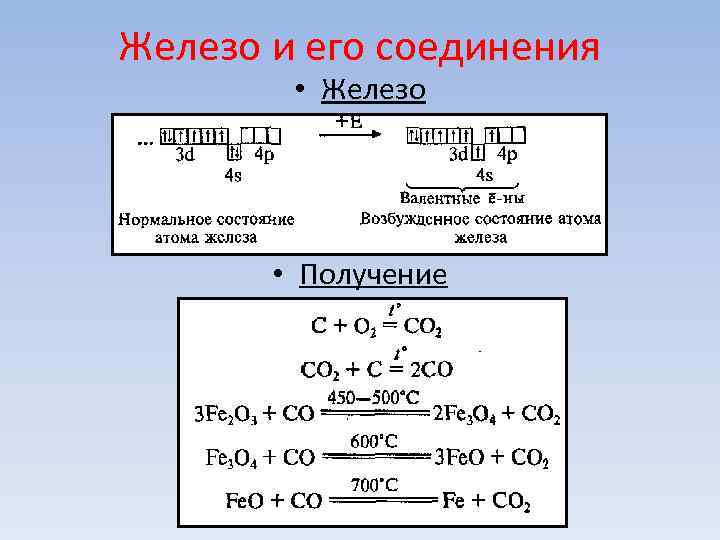
 Железо и его соединения • Железо • Получение
Железо и его соединения • Железо • Получение
 Железо и его соединения • Химические свойства • При обычной t железо не взаимодействует даже с самыми активными окислителями, но при нагревание становится активным Взаимодействие с простыми веществами:
Железо и его соединения • Химические свойства • При обычной t железо не взаимодействует даже с самыми активными окислителями, но при нагревание становится активным Взаимодействие с простыми веществами:
 Железо и его соединения Взаимодействие со сложными веществами
Железо и его соединения Взаимодействие со сложными веществами
 Железо и его соединения При очень высокой t раскалённое железо реагирует с водой
Железо и его соединения При очень высокой t раскалённое железо реагирует с водой
 Железо и его соединения
Железо и его соединения
 Железо и его соединения • Оксид железа (II) Получение: Химические свойства:
Железо и его соединения • Оксид железа (II) Получение: Химические свойства:
 Железо и его соединения • Гидроксид железа (II) Получение: Химические свойства:
Железо и его соединения • Гидроксид железа (II) Получение: Химические свойства:
 Железо и его соединения
Железо и его соединения
 Железо и его соединения
Железо и его соединения
 Железо и его соединения Качественная реакция на катион железа (II)
Железо и его соединения Качественная реакция на катион железа (II)
 Железо и его соединения • Оксид железа (III) Получение:
Железо и его соединения • Оксид железа (III) Получение:
 Железо и его соединения • Химические свойства:
Железо и его соединения • Химические свойства:
 Железо и его соединения • Гидроксид железа (III) Получение: Химические свойства:
Железо и его соединения • Гидроксид железа (III) Получение: Химические свойства:
 Железо и его соединения
Железо и его соединения
 Железо и его соединения
Железо и его соединения
 Железо и его соединения Качественные реакции на катион железа (II)
Железо и его соединения Качественные реакции на катион железа (II)
 Железо и его соединения
Железо и его соединения
 Хром и его соединения • Общая характеристика подгруппы хрома Атомы хрома и молибдена имеют по 1 электрону на внешнем электронном слое, атом вольфрама 2 d-элементы степени окисления от +2 до +6
Хром и его соединения • Общая характеристика подгруппы хрома Атомы хрома и молибдена имеют по 1 электрону на внешнем электронном слое, атом вольфрама 2 d-элементы степени окисления от +2 до +6
 Хром и его соединения • Хром Получение:
Хром и его соединения • Хром Получение:
 Хром и его соединения Химические свойства: В обычных условиях – хром Ме неактивный Взаимодействие с простыми веществами: Взаимодействие со сложными веществами:
Хром и его соединения Химические свойства: В обычных условиях – хром Ме неактивный Взаимодействие с простыми веществами: Взаимодействие со сложными веществами:
 Хром и его соединения
Хром и его соединения
 Хром и его соединения • Оксид хрома (II) Типичный основный оксид, ему соответствует гидроксид хрома (II) Химические свойства: Не растворяются в воде, но растворимы в кислотах
Хром и его соединения • Оксид хрома (II) Типичный основный оксид, ему соответствует гидроксид хрома (II) Химические свойства: Не растворяются в воде, но растворимы в кислотах
 Хром и его соединения • Оксид хрома (III) Получение:
Хром и его соединения • Оксид хрома (III) Получение:
 Хром и его соединения Химические свойства: Амфотерный оксид При обычных условиях плохо растворяется в щелочах и кислотах, но при сплавлении со щелочами или карбонатами щелочных металлов образует метахроматы
Хром и его соединения Химические свойства: Амфотерный оксид При обычных условиях плохо растворяется в щелочах и кислотах, но при сплавлении со щелочами или карбонатами щелочных металлов образует метахроматы
 Хром и его соединения • Гидроксид хрома (III) Получение: Действие щелочей на соли хрома Химические свойства: Растворим в кислотах И в избытке щелочей
Хром и его соединения • Гидроксид хрома (III) Получение: Действие щелочей на соли хрома Химические свойства: Растворим в кислотах И в избытке щелочей
 Хром и его соединения • Оксид хрома (VI) Свойства: Кислотный оксид
Хром и его соединения • Оксид хрома (VI) Свойства: Кислотный оксид
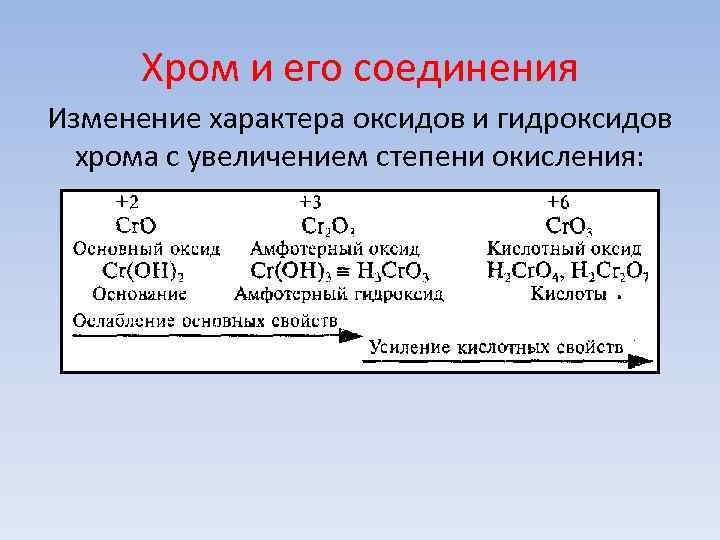
 Хром и его соединения Изменение характера оксидов и гидроксидов хрома с увеличением степени окисления:
Хром и его соединения Изменение характера оксидов и гидроксидов хрома с увеличением степени окисления:
 Хром и его соединения
Хром и его соединения
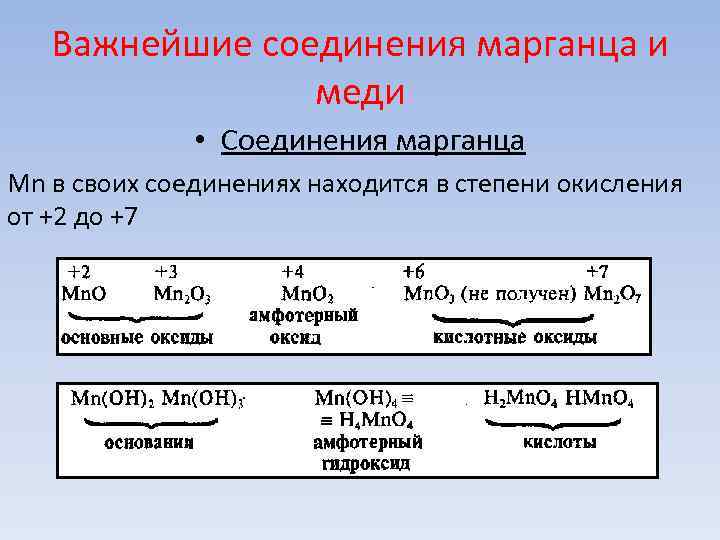
 Важнейшие соединения марганца и меди • Соединения марганца Мn в своих соединениях находится в степени окисления от +2 до +7
Важнейшие соединения марганца и меди • Соединения марганца Мn в своих соединениях находится в степени окисления от +2 до +7
 Важнейшие соединения марганца и меди • Соли Mn (II) Получение: Растворение Mn в разбавленных кислотах Свойства солей: При действии растворов щелочей на соли Mn выпадает белый осадок гидроксида Mn, который на воздухе быстро окисляется
Важнейшие соединения марганца и меди • Соли Mn (II) Получение: Растворение Mn в разбавленных кислотах Свойства солей: При действии растворов щелочей на соли Mn выпадает белый осадок гидроксида Mn, который на воздухе быстро окисляется
 Важнейшие соединения марганца и меди • Диоксид Mn Свойства: Достаточно сильный окислитель
Важнейшие соединения марганца и меди • Диоксид Mn Свойства: Достаточно сильный окислитель
 Важнейшие соединения марганца и меди • Марганцовая кислота Очень сильная кислота, существующая только в водных растворах Наиболее известная моль – перманганат калия
Важнейшие соединения марганца и меди • Марганцовая кислота Очень сильная кислота, существующая только в водных растворах Наиболее известная моль – перманганат калия
 Важнейшие соединения марганца и меди • Соединения меди (I): Основный оксид и соответствующий ему гидроксид – крайне нестойкое соединение
Важнейшие соединения марганца и меди • Соединения меди (I): Основный оксид и соответствующий ему гидроксид – крайне нестойкое соединение
 Важнейшие соединения марганца и меди • Соединения меди (II) Оксид меди (II) Получение: Свойства: Основный оксид
Важнейшие соединения марганца и меди • Соединения меди (II) Оксид меди (II) Получение: Свойства: Основный оксид
 Важнейшие соединения марганца и меди Гидроксид меди (II) Получение: Свойства: При слабом нагревании разлогается
Важнейшие соединения марганца и меди Гидроксид меди (II) Получение: Свойства: При слабом нагревании разлогается
 Важнейшие соединения марганца и меди Оксид и гидроксид меди (II) проявляют окислительные свойства Гидроксид меди (II) растворяется в концентрированных растворах щелочей
Важнейшие соединения марганца и меди Оксид и гидроксид меди (II) проявляют окислительные свойства Гидроксид меди (II) растворяется в концентрированных растворах щелочей

