Кислот-основ_МБФ.ppt
- Количество слайдов: 44

Курс лекций по органической химии МБФ, «БИОХИМИЯ» Кислотно-основные свойства органических соединений 4 -1
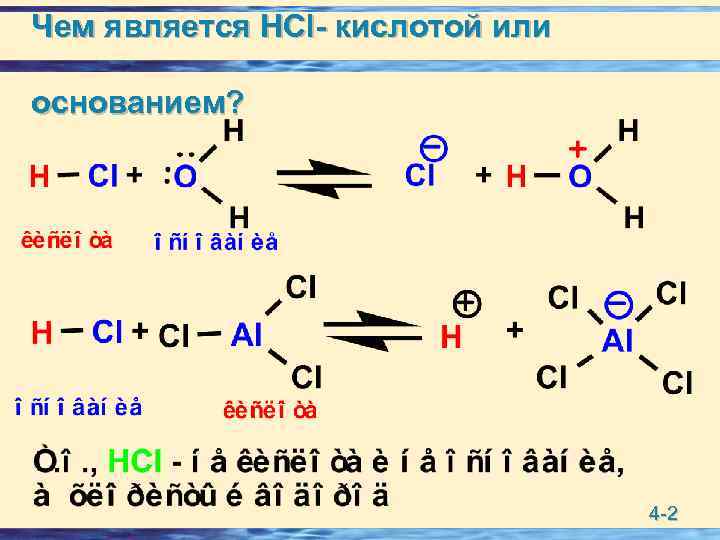
Чем является HCl- кислотой или основанием? 4 -2

Аррениусовские кислоты и основания u. В 1884 Сванте Аррениус предложил следующие определения • кислота: субстанция, которая продуцирует H 3 O+ ион (ион гидроксония) в водном растворе. • основание: субстанция, которая продуцирует OH- ион в водном растворе. • Это определения кислоты со времененем была модифицирована и кислота – это субстанция, которая продуцирует H+ в водном растворе. • Сегодня мы знаем, что H+ в воде существует в виде иона гидроксония (hydronium ion). 4 -3
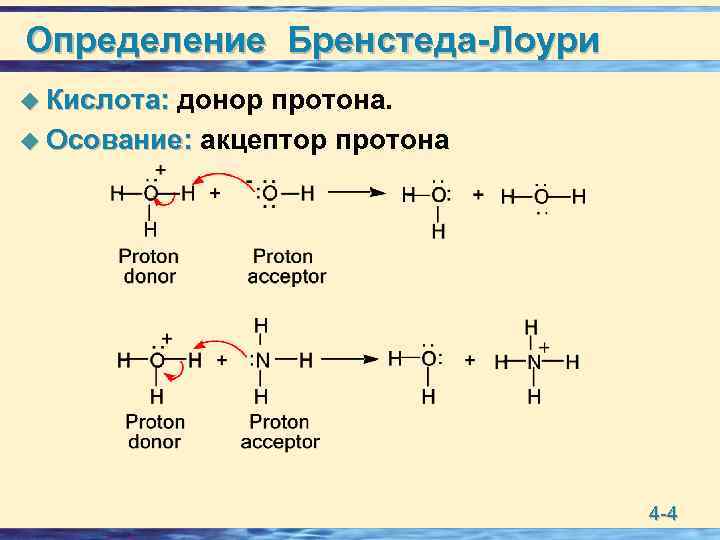
Определение Бренстеда-Лоури u Кислота: донор протона. u Осование: акцептор протона 4 -4

Сопряженные кислоты и основания • Сопряженное основание: частица, которая генерируется основание из кислоты в результате отдачи протона основанию. • Сопряженная кислота: частица, которая генерируется из основания в результате присоединения протона от кислоты. • Кислотно-основные реакции: это реакции передачи протона. 4 -5
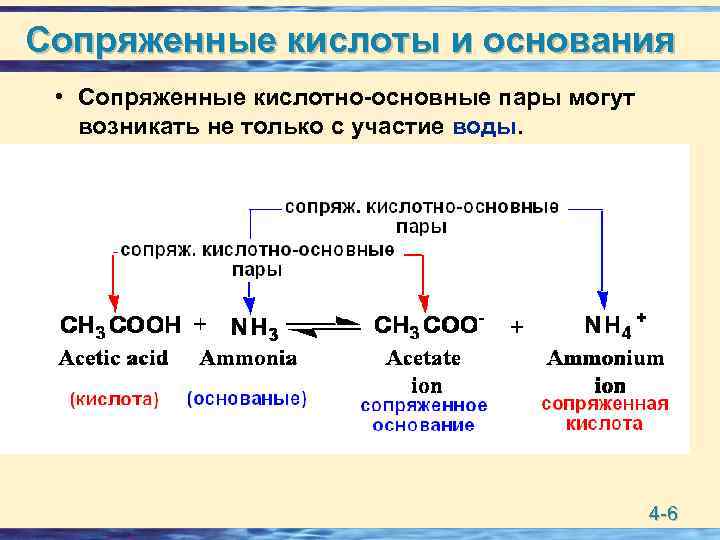
Сопряженные кислоты и основания • Сопряженные кислотно-основные пары могут возникать не только с участие воды. 4 -6
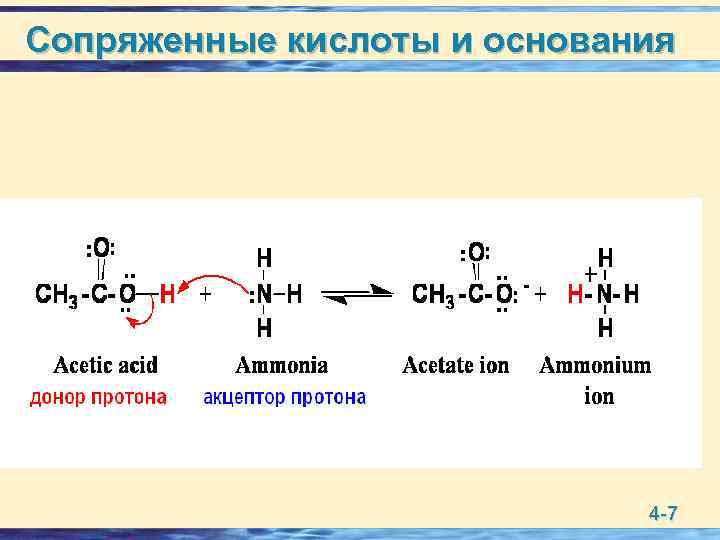
Сопряженные кислоты и основания 4 -7

Сила кислоты и основания u Ионизация кислоты (HA) в водном растворе, где вода играет роль основания: u. Концентрация воды постояннаяи равна приблизительно 55. 5 mol/л. u. Константа равновесия можно написать в новой форме, Ka, называется константой кислотности. 4 -8
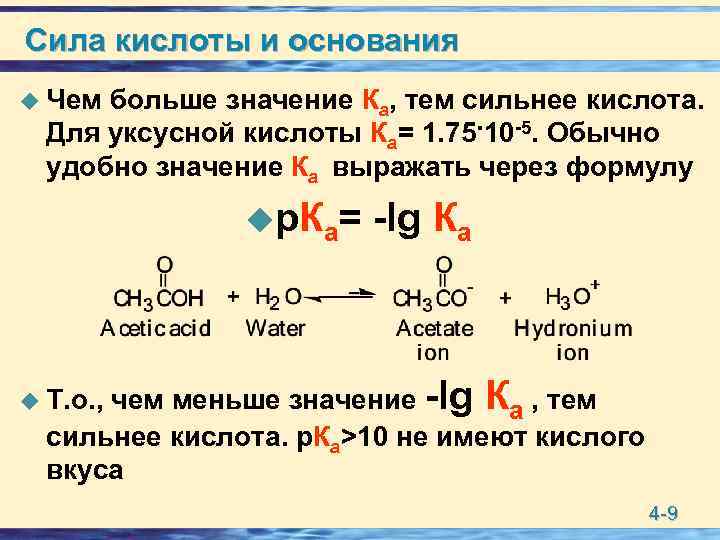
Сила кислоты и основания u Чем больше значение Ка, тем сильнее кислота. Для уксусной кислоты Ка= 1. 75. 10 -5. Обычно удобно значение Ка выражать через формулу uр. Ка= -lg Ка чем меньше значение -lg Ка , тем сильнее кислота. р. Ка>10 не имеют кислого вкуса u Т. о. , 4 -9
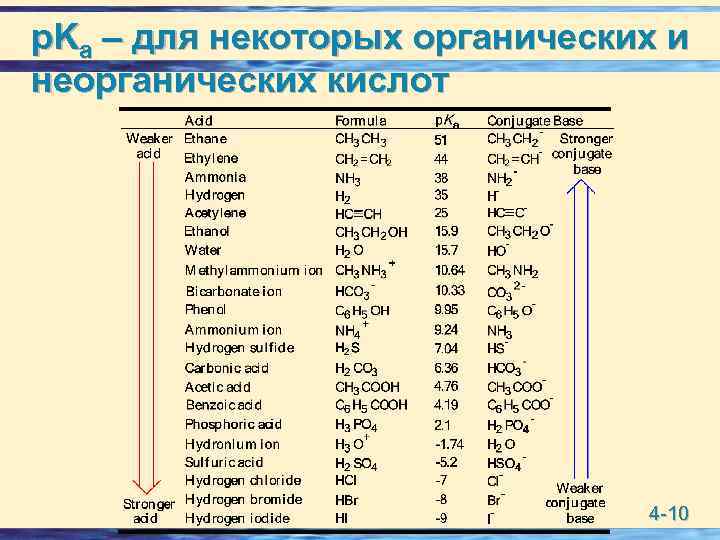
p. Ka – для некоторых органических и неорганических кислот 4 -10

Кислотно-основное равновесие u. В результате взаимодействия сильной кислоты и сильного основания образуются слабая кислота (ион аммония) и слабое основание (ацетат анион) 4 -11
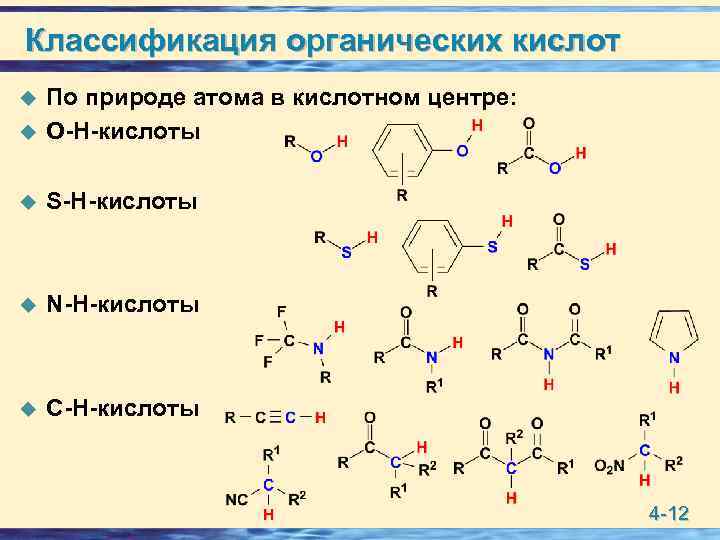
Классификация органических кислот u По природе атома в кислотном центре: О-Н-кислоты u S-H-кислоты u N-H-кислоты u С-Н-кислоты u 4 -12
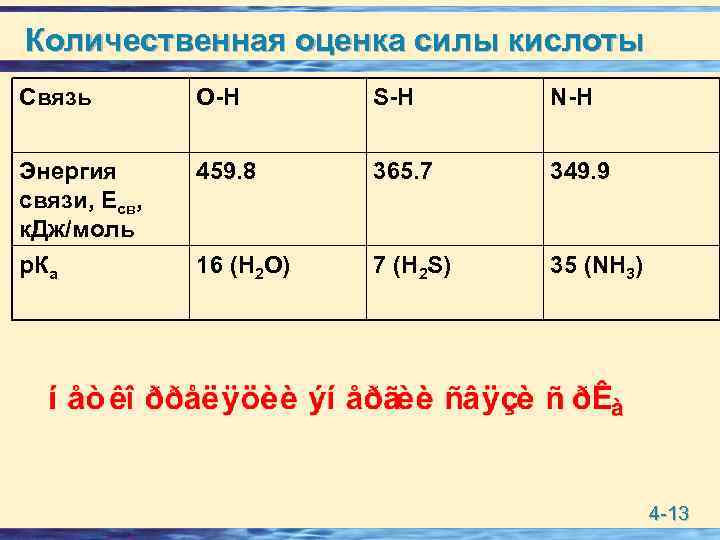
Количественная оценка силы кислоты Связь О-Н S-H N-H Энергия связи, Есв, к. Дж/моль р. Ка 459. 8 365. 7 349. 9 16 (H 2 O) 7 (H 2 S) 35 (NH 3) 4 -13
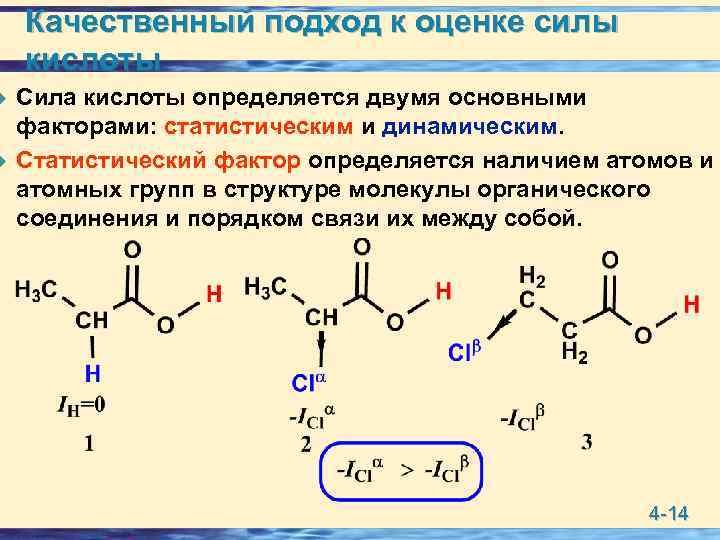
u u Качественный подход к оценке силы кислоты Сила кислоты определяется двумя основными факторами: статистическим и динамическим. Статистический фактор определяется наличием атомов и атомных групп в структуре молекулы органического соединения и порядком связи их между собой. 4 -14
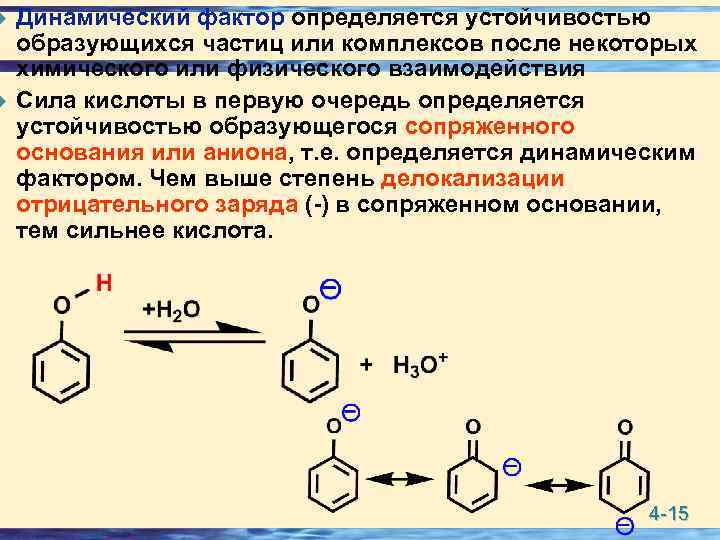
u u Динамический фактор определяется устойчивостью образующихся частиц или комплексов после некоторых химического или физического взаимодействия Сила кислоты в первую очередь определяется устойчивостью образующегося сопряженного основания или аниона, т. е. определяется динамическим фактором. Чем выше степень делокализации отрицательного заряда (-) в сопряженном основании, тем сильнее кислота. 4 -15
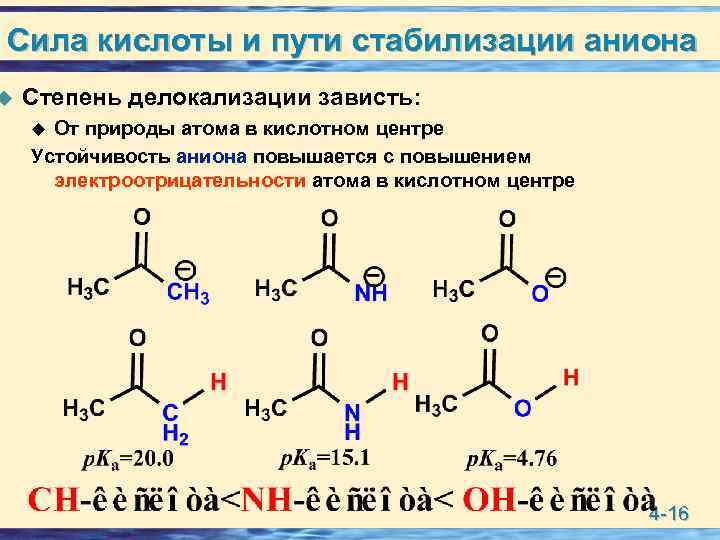
Сила кислоты и пути стабилизации аниона u Степень делокализации зависть: От природы атома в кислотном центре Устойчивость аниона повышается с повышением электроотрицательности атома в кислотном центре u 4 -16

Структура молекулы и кислотность A. В периуде с право на лево электротрицательность падает, значит и сила кислоты тоже падает. Электроотрицательность С (2, 5), N (3, 0), О (3, 5) 4 -17
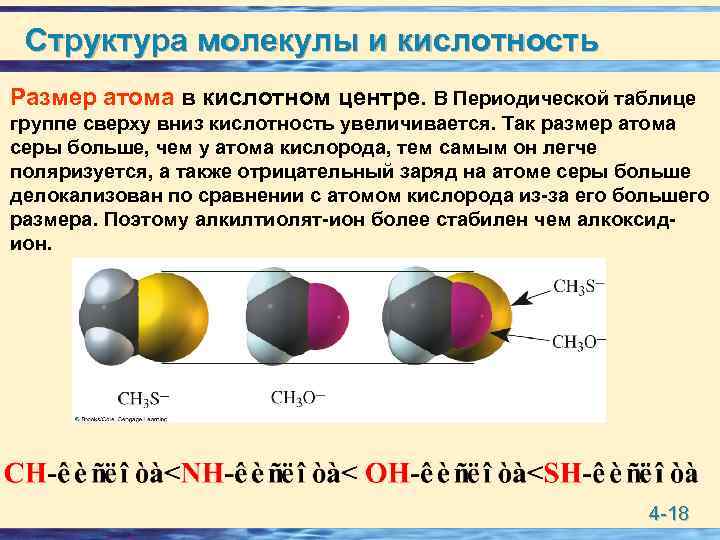
Структура молекулы и кислотность Размер атома в кислотном центре. В Периодической таблице группе сверху вниз кислотность увеличивается. Так размер атома серы больше, чем у атома кислорода, тем самым он легче поляризуется, а также отрицательный заряд на атоме серы больше делокализован по сравнении с атомом кислорода из-за его большего размера. Поэтому алкилтиолят-ион более стабилен чем алкоксидион. 4 -18
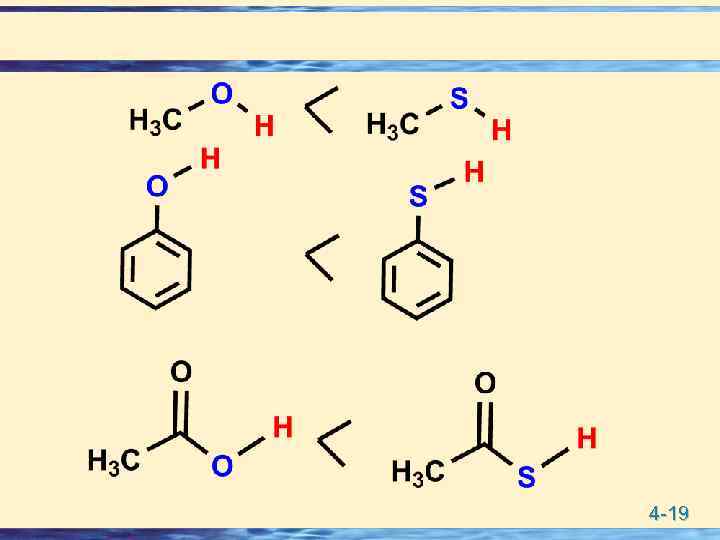
4 -19
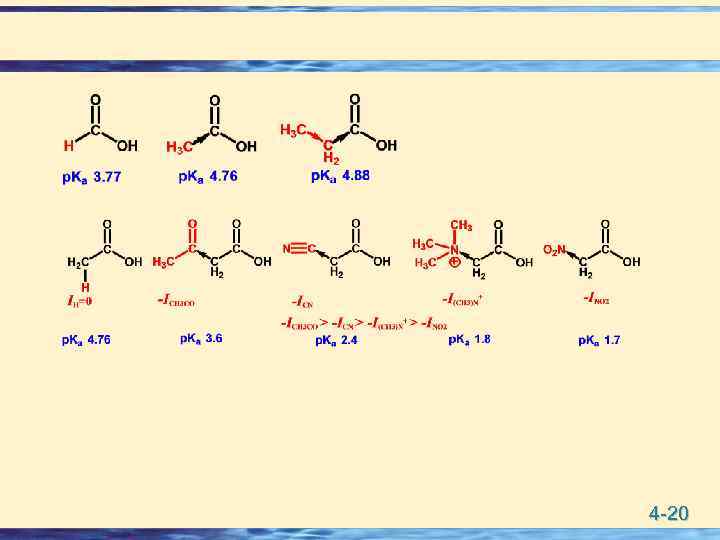
4 -20

Стабилизация аниона за счет элект. эффектов Заместители с –I и –M в структуре органической кислоты способствуют делокализации (-) заряда и стабилизируют анион, тем самым повышают кислотность. Электронодонорные заместители наоборот. Влияние индуктивного эффекта: 4 -21
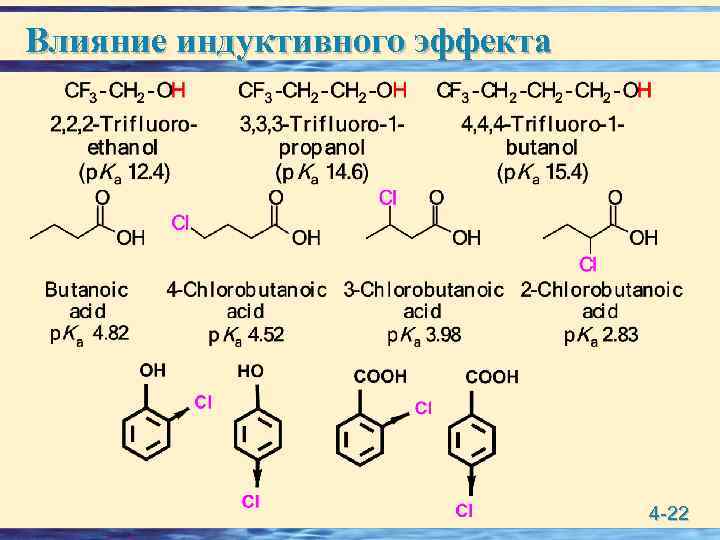
Влияние индуктивного эффекта 4 -22
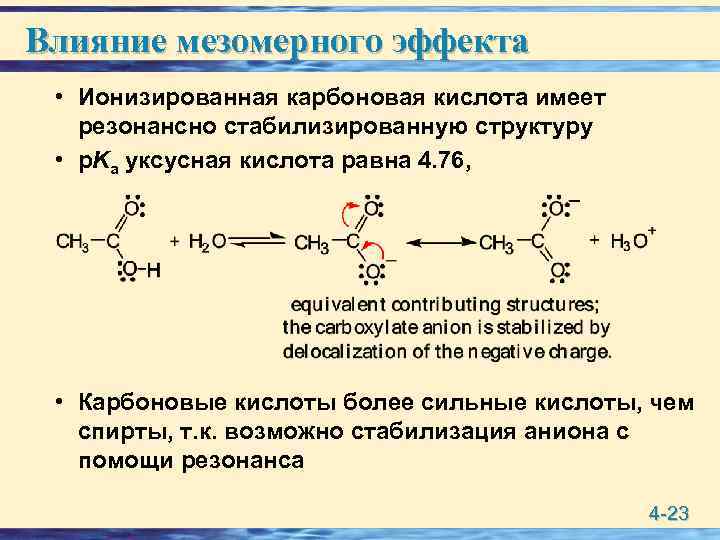
Влияние мезомерного эффекта • Ионизированная карбоновая кислота имеет резонансно стабилизированную структуру • p. Ka уксусная кислота равна 4. 76, • Карбоновые кислоты более сильные кислоты, чем спирты, т. к. возможно стабилизация аниона с помощи резонанса 4 -23
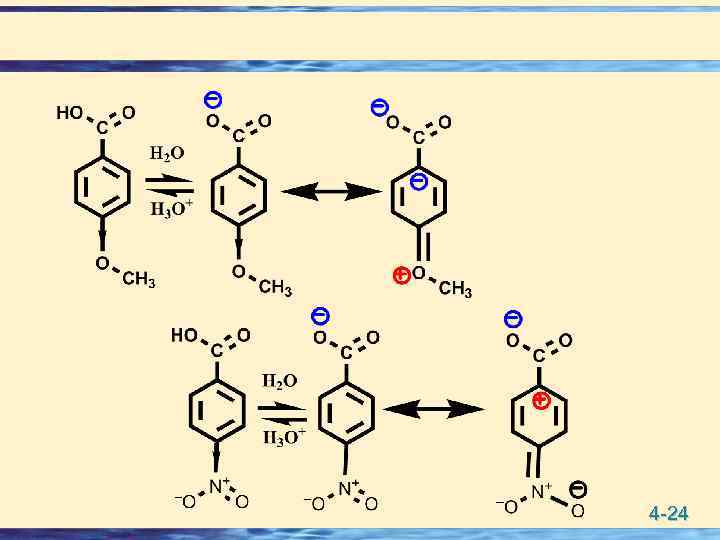
4 -24
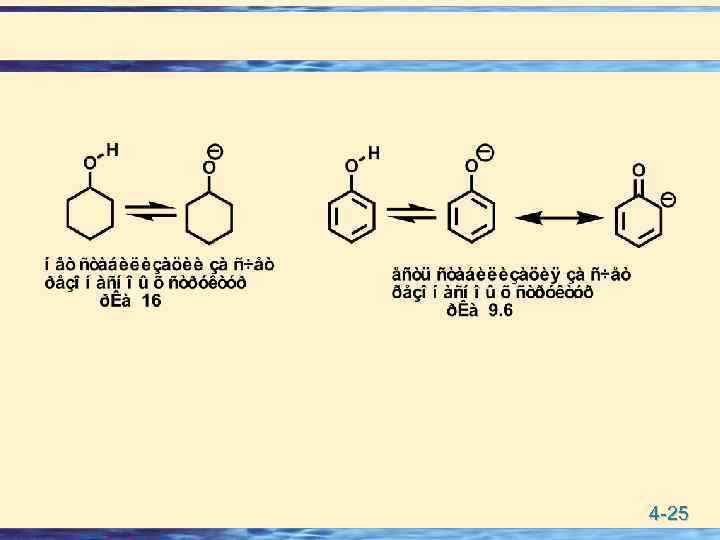
4 -25

Структура молекулы и кислотность E. Гибридизация. • Кислотность зависит от степени гибридизации атома углерода. 4 -26

Роль растворителя в стабилизации аниона u Чем выше диэлектрическая проницаемость растворителя и его способность сольватировать растворенные частицы, тем стабильнее анион. Лучшим растворителем является ВОДА, диэлектрическая проницаемость которого равна =80. В воде лучше происходить сольватирование ионов с меньшим размером и с большим локализованным в нем зарядом. u Важным следствием сольватации является: перераспределение заряда между анионом и молекулой растворителя. 4 -27
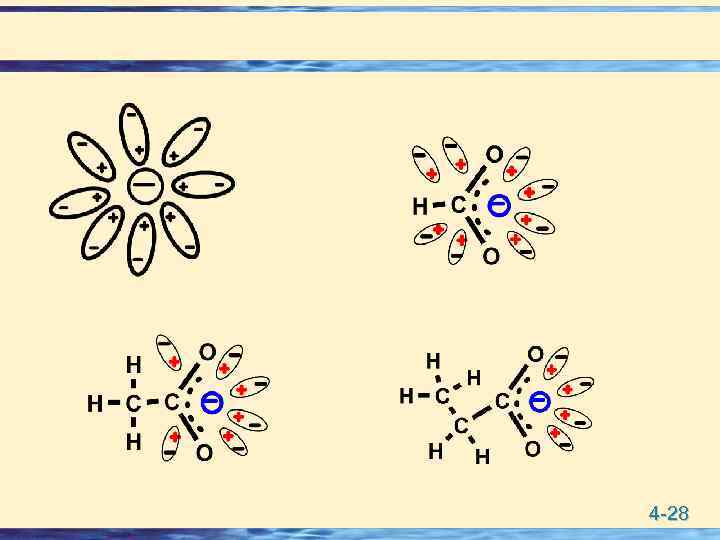
4 -28
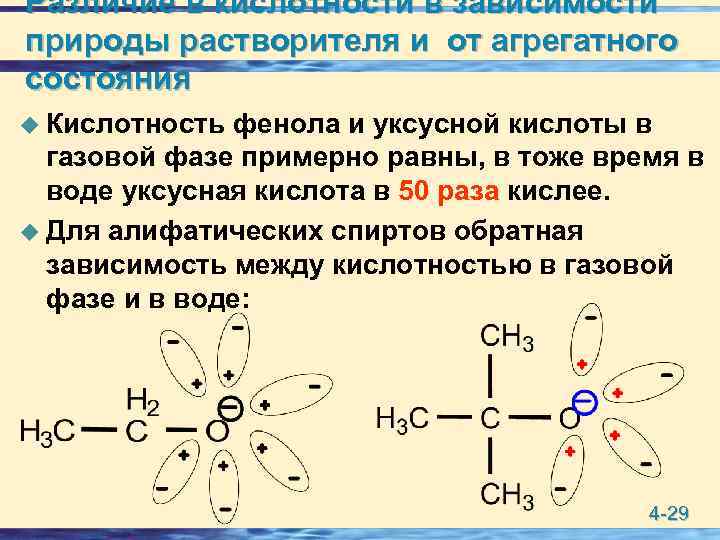
Различие в кислотности в зависимости природы растворителя и от агрегатного состояния u Кислотность фенола и уксусной кислоты в газовой фазе примерно равны, в тоже время в воде уксусная кислота в 50 раза кислее. u Для алифатических спиртов обратная зависимость между кислотностью в газовой фазе и в воде: 4 -29
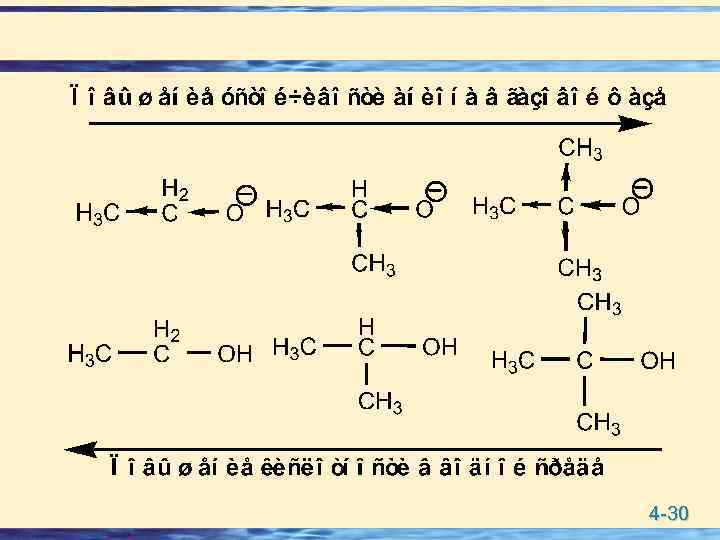
4 -30

Органические основания u Органические основания в зависимости от природы основного центра делятся на: u n-основания u n-основания по силе всегда более сильные основания, чем -основания u n-основания –это органические соединения имеющие в своей структуре атомы с неподеленной электронной парой u Классификация n-оснований: 4 -31
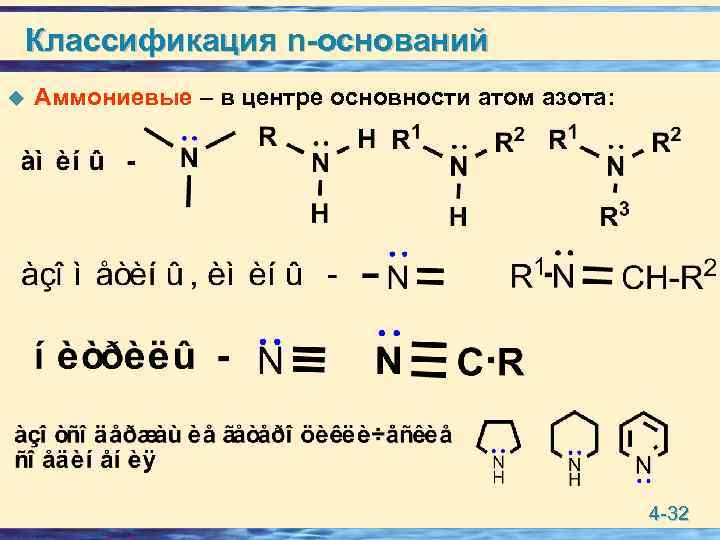
Классификация n-оснований u Аммониевые – в центре основности атом азота: 4 -32

u Оксониевые – в центре основности атом кислорода u Сульфониевые – в центре основности атом серы 4 -33
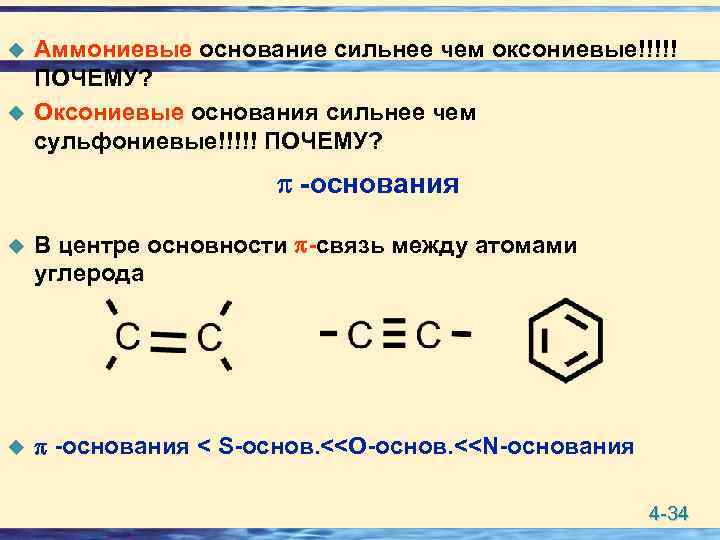
u u Аммониевые основание сильнее чем оксониевые!!!!! ПОЧЕМУ? Оксониевые основания сильнее чем сульфониевые!!!!! ПОЧЕМУ? -основания u В центре основности -связь между атомами углерода u -основания < S-основ. <<O-основ. <<N-основания 4 -34

Количественная оценка силы кислоты u Ионизация основания (В: ) в водном растворе, где вода играет роль кислоты: u 4 -35

Факторы влияющие на силы основания u u Как и в случае кислот, на силы основания влияют те же факторы (статистические и динамические). Вклад динамического фактора определяющее и сила основания зависит от стабильности катиона (сопряженной кислоты – аммоний катиона) Следует помнить, что Электронодонорные заместители увеличивают основность, а Электроноакцепторные снижают. (в случае кислот все наооборот). 4 -36
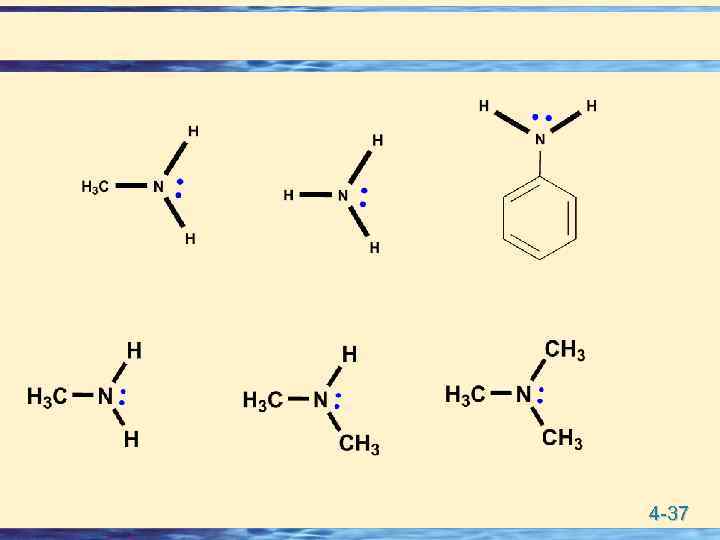
4 -37

Слабые кислоты и основания в биологических системах u Степень ионизации кислоты и основания в растворе зависит от р. Н растовра и р. Ка или р. КВН+ (табличные данные) 4 -38

Теория Льюиса кислот и оснований (Lewis Acids and Bases) u u По Льюису: кислота – это любая частица (атом, нейтральная молекула, катион (+)) имеющая вакантную орбиталь и способная принимать электрон. Кислоты Льюиса: Al. Cl 3, BF 3, Fe. Cl 3, Zn. Cl 2, Sb. Cl 3, Cl 2, Br 2 и т. д. , Основания Льюиса: любая частица (атом, нейтральная молекула, анион (-)) способная отдавать электроную пару для образования ковалентной связи. Основания Льюиса: все основания по Бренстеду. Лоури, а также 4 -39
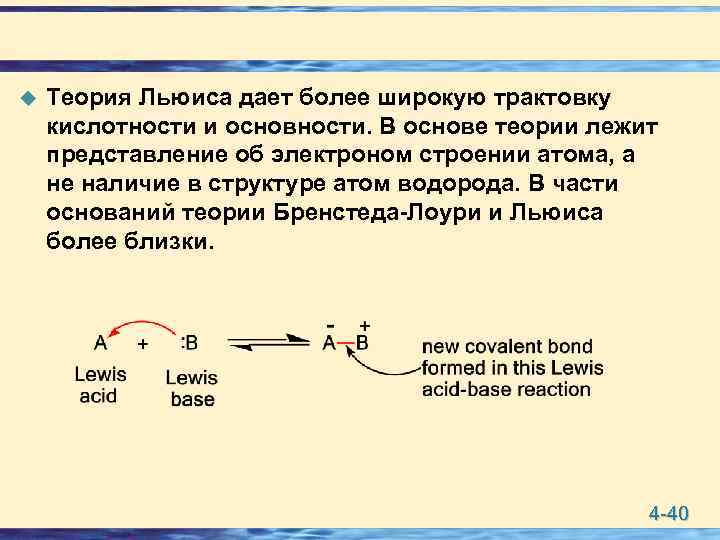
u Теория Льюиса дает более широкую трактовку кислотности и основности. В основе теории лежит представление об электроном строении атома, а не наличие в структуре атом водорода. В части оснований теории Бренстеда-Лоури и Льюиса более близки. 4 -40
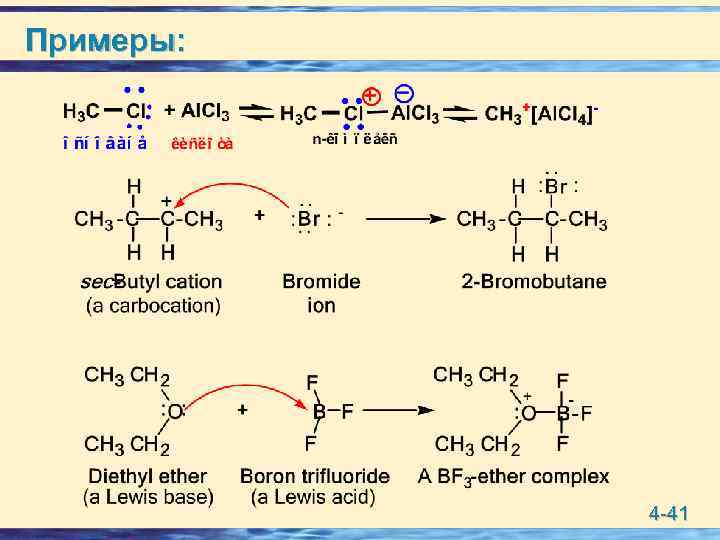
Примеры: 4 -41

Жесткие и мягкие кислоты и основания u. Теорию Льюиса развил Пирсон и вёл понятие жестких и мягких кислот и оснований. Он предположил, что кислотно-основное взаимодействие зависит не только от силы кислоты (или основания), но и от их жесткости и мягкости (ЖМКО). 4 -42

4 -43

Acids and Bases End Chapter 4 4 -44
Кислот-основ_МБФ.ppt