Лекция_5_биохим_организация_живой_системы2.ppt
- Количество слайдов: 46

Курс лекций по дисциплине «Биохимия» для специальности «Лечебное дело» БИОХИМИЧЕСКАЯ ОРГАНИЗАЦИЯ ЖИВОЙ КЛЕТКИ (ЛЕКЦИЯ № 5) Курс лекций читает д. б. н. , профессор Кершенгольц Борис Моисеевич

ВОПРОСЫ: 1. Общие принципы метаболизма. 1. 1. Метаболические пути как сложная сеть разветвленных и взаимозависимых последовательностей биохимических превращений. 1. 2. Основные принципы организации катаболических, анаболических и амфиболических путей, компартментализация этих процессов. 1. 3. Организация линейных и циклических путей. Организация разветвленных ферментативных цепей с обратной связью, обеспечивающих консервативность и мобильность метаболических систем как один из основных механизмов адаптации метаболизма к изменяющимся условиям внешней и внутренней среды. 1. 4. Энергетический цикл в клетках. Биологическое окисление как универсальный источник свободной химической энергии в живых клетках

2. Строение и функции клеточных мембран. 2. 1. Состав биомембран. Характеристика мембранных липидов. Функции мембранных липидов. 2. 2. Нелипидные компоненты мембран. Мембранные белки, их олигомерная организация и функции. Интегральные и периферические белки, их свойства. Функции мембранных белков: ферментативная, транспортная, регуляторная, рецепторная и структурная. 2. 3. Олигосахаридные компоненты мембран. Общие представления об их локализации и структуре. Механизм биосинтеза гликоконьюгатов- олигогликозилтрансферазы и олигогликозилгидролазы. Функции гликоконьюгатов: антигенные детерминанты групп крови, тканеспецифичные мембранные антигены, роль в процессинге, составная часть сигнального пептида, адгезивность и другие. 2. 4. Структура биологических мембран. Современная концепция структуры биологических мембран теория “Липидного моря”. Конформационные свойства мембран. Динамическое состояниие липидов в мембране. Фазовые переходы. Ассиметрия бислоя. Модификация бислоя белками. Влияние на липидный состав. Изменение гидратации бислоя.

2. 5. Перекисное окисление липидов как механизм поддержания нативного состава (соотношения предельных и непредельных жирных кислот), структуры, вязкости и функциональной лабильности мембран. 2. 6. Роль молекулярного кислорода, природного естественного радиационного фона Земли, супероксиддисмутаз и низкомолекулярных антиоксидантов в этом процессе. 2. 7. Функции биологических мембран. Мембранный транспорт и поддержание ионного гомеостаза. Характеристика различних транспортных процессов. Ионы металлов в биологических мембранных системах. Био логическая роль активного транспорта. Транспортные Na, K зависимые АТФ азы, протонная помпа. 2. 8. Общее представление о роли биологических мембран в механизмах биоэнергетических процессов в клетке. 2. 9. Рецепторные и иммуноантигенные функции мембран. Характеристика отдельных биологических мембранных систем. Роль повреждений биомембран в развитии неинфекционных заболеваний, онкопатологии, радиационных поражений, геронтологических и других из менениях. 2. 10. Функции лизосом. Лизосомные болезни

3. Общие принципы организации биоэнергетических систем. Энергетика живых систем. 3. 1. Энергетические ресурсы, виды источников энергии. Биологический принцип высвобождения энергии (теория Палладина о дегидрогенизации органического вещества при дыхании). 3. 2. Основные биологические окислительно восстановительные системы. Тер модинамика открытой системы и процессы жизнедеятельности. Понятие об знтропии и биологическая работа как векторный перенос энергии. Изменение свободной энергии при окислительно восстановительных реакциях, злектрохимический злемент как система для трансформации энер гии из химической формы в электрическую и обратно в химическую. Макроэрги. 3. 3. Биомембраны как материальные структуры, обеспечивающие трансформацию и аккумуляцию биологически полезной энергии (аналог электрохимического злемента). Молекулярные механизмы трансформации энергии: функциональные комплексы электрон транспортной цепи митохондрий. Понятие о трансмембранном потенциале (теория Митчела, эксперименты Скулачева).

3. 4. Процессы окислительного фосфорилирования, сопряженные с транспортом электронов: строение, свойства и механизм дей ствия АТФ синтетазы. Разобщение дыхания и окислительного фосфорилирования. Понятие о коэффициенте "Р/О". 3. 5. Терморегуляция и термоадаптация. Нарушение окисли тельного фосфорилирования. 3. 6. Электрохимический градиент ионов как универсальная биологическая форма запасания энергии. Формы и механизмы преобразования энергии электрохимического градиента ионов: реализация активного транспорта веществ в сократительных системах и синтез АТФ - основного "аккумулятора" биохимически полезной энергии в метаболических реакциях. 3. 7. Примеры субстратного фосфорелирования. 3. 8. Экологическая модификация режима работы биоэнергетического аппарата

1. Общие принципы метаболизма. 1. 1. Метаболические пути как сложная сеть разветвленных и взаимозависимых последовательностей биохимических превращений. В клетке постоянно происходит большое количество разнообразных химических реакций, которые формируют метаболические пути - последовательное превращение одних соединений в другие. Метаболизм - совокупность всех метаболических путей, протекающих в клетках организма. Среди всех метаболических путей, протекающих в организме, выделяют противоположно направленные процессы: катаболизм и анаболизм. Катаболизм - распад сложных веществ до простых с высвобождением энергии. Анаболизм - синтез из простых более сложных веществ. Метаболические пути согласованы между собой по месту, времени и интенсивности протекания. Эта согласованность протекания всех процессов обеспечивается сложными и многообразными механизмами регуляции. Основополагающим принципом организации метаболических сетей является то, что все биохимические реакции в клетке (организме) катализируются ФЕРМЕНТАМИ и именно через модулирование активности ферментов осуществляется формирование сетей и их регуляция !!
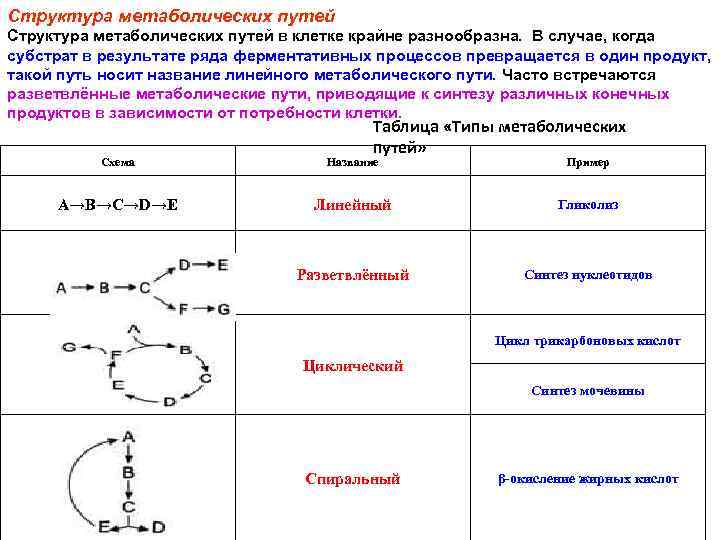
Структура метаболических путей в клетке крайне разнообразна. В случае, когда субстрат в результате ряда ферментативных процессов превращается в один продукт, такой путь носит название линейного метаболического пути. Часто встречаются разветвлённые метаболические пути, приводящие к синтезу различных конечных продуктов в зависимости от потребности клетки. Таблица «Типы метаболических путей» Схема Название Пример А→В→С→D→Е Линейный Гликолиз Разветвлённый Синтез нуклеотидов Цикл трикарбоновых кислот Циклический Синтез мочевины Спиральный β-окисление жирных кислот

В метаболических путях продукт первой ферментативной реакции служит субстратом второй и так далее до формирования конечного продукта. Промежуточные продукты метаболического пути могут высвобождаться из последовательности реакций и использоваться в других метаболических путях, т. е. метаболические пути связаны между собой промежуточными продуктами. А → В → С → Д и т. д. Y А’ → В’ → С’ → Д’ и т. д.



1. Общие принципы метаболизма. 1. 2. Основные принципы организации катаболических, анаболических и амфиболических путей, компартментализация этих процессов. 1. Пространственная локализация ферментов Большинство ферментов имеет внутриклеточную локализацию и распределены в организме неравномерно. Все ферменты одного метаболического пути, как правило, находятся в одном отделе клетки. Особенно разделение метаболических путей важно для противоположно направленных катаболических и анаболических процессов. Например, синтез жирных кислот происходит в цитоплазме, а их распад в митохондриях. Если бы такого разделения не существовало, образовывались бы бесполезные с функциональной и энергетической точки зрения пути. В ряде случаев пространственная организация ферментов настолько сильно выражена, что продукт реакции ни при каких условиях не может быть вычленен из метаболического пути и обязательно служит субстратом следующей реакции. Такая организация метаболического пути носит название мультиферментного комплекса и возникает в результате структурно-функциональной организации ферментов. Обычно такие комплексы связаны с мембранами. В качестве примеров мультиферментных комплексов можно привести пируватдегидрогеназный комплекс, под действием которого происходит окислительное декарбоксилирование пировиноградной кислоты (пирувата), синтазу жирных кислот, катализирующую синтез пальмитиновой кислоты

2. Органоспецифичность Ферментный состав различных клеток неодинаков. Ферменты, выполняющие функцию жизнеобеспечения клетки, находятся во всех клетках организма. В процессе дифференцировки клеток происходит изменение ферментного состава клеток. Так, фермент аргиназа, участвующий в синтезе мочевины, находится только в клетках печени, а кислая фосфатаза, участвующая в гидролизе моноэфиров ортофосфорной кислоты, в клетках простаты. Это так называемые органоспецифичные ферменты. Если говорить об узко специализированных клетках, то ферментов, выполняющих функции в этих клетках, находится больше, чем в других клетках. Например, в клетках сердечной мышцы имеется повышенное количество ферментов креатинкиназы и аспартатаминотрансферазы, в клетках печени аланинаминотрансферазы и аспартатаминотрансферазы, в остеобластах щелочной фосфатазы и т. д.
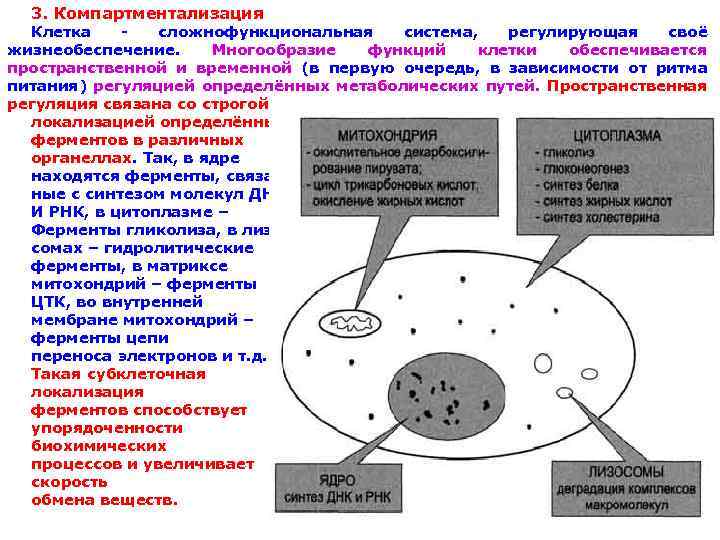
3. Компартментализация Клетка сложнофункциональная система, регулирующая своё жизнеобеспечение. Многообразие функций клетки обеспечивается пространственной и временной (в первую очередь, в зависимости от ритма питания) регуляцией определённых метаболических путей. Пространственная регуляция связана со строгой локализацией определённых ферментов в различных органеллах. Так, в ядре находятся ферменты, связан ные с синтезом молекул ДНК И РНК, в цитоплазме – Ферменты гликолиза, в лизо сомах – гидролитические ферменты, в матриксе митохондрий – ферменты ЦТК, во внутренней мембране митохондрий – ферменты цепи переноса электронов и т. д. Такая субклеточная локализация ферментов способствует упорядоченности биохимических процессов и увеличивает скорость обмена веществ.
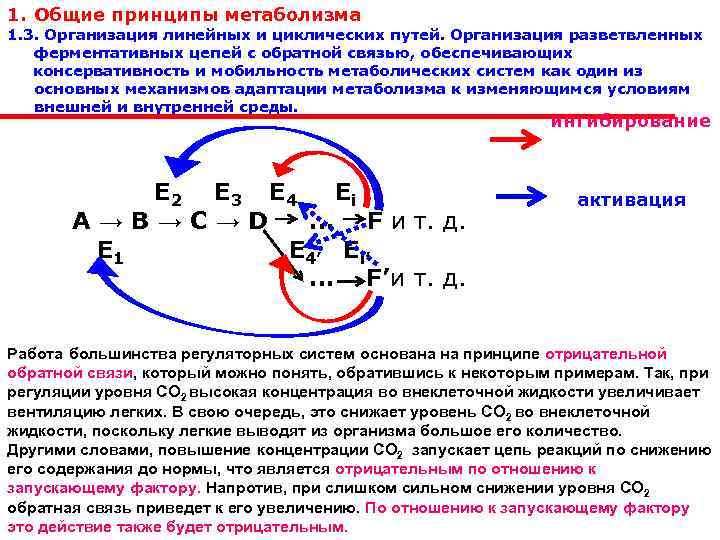
1. Общие принципы метаболизма 1. 3. Организация линейных и циклических путей. Организация разветвленных ферментативных цепей с обратной связью, обеспечивающих консервативность и мобильность метаболических систем как один из основных механизмов адаптации метаболизма к изменяющимся условиям внешней и внутренней среды. ингибирование E 2 E 3 E 4 Ei А → В → С → D … F и т. д. E 1 E 4’ Ei’ … F’и т. д. активация Работа большинства регуляторных систем основана на принципе отрицательной обратной связи, который можно понять, обратившись к некоторым примерам. Так, при регуляции уровня СО 2 высокая концентрация во внеклеточной жидкости увеличивает вентиляцию легких. В свою очередь, это снижает уровень СО 2 во внеклеточной жидкости, поскольку легкие выводят из организма большое его количество. Другими словами, повышение концентрации СО 2 запускает цепь реакций по снижению его содержания до нормы, что является отрицательным по отношению к запускающему фактору. Напротив, при слишком сильном снижении уровня СО 2 обратная связь приведет к его увеличению. По отношению к запускающему фактору это действие также будет отрицательным.

Примерно так же регулируется и артериальное давление: повышение показателя запускает серию биохимических реакций, способствующих его снижению, а снижение — реакций, обеспечивающих его повышение. В обоих случаях результат воздействия является отрицательным по отношению к запускающему сигналу. По таким же принципам регулируются биохимические реакции синтеза, например, пуриновых нуклеотидов (АТФ и ГТФ) и многие, многие другие метаболические цепи Положительная обратная связь. В некоторых случаях организм использует преимущества положительной обратной связи. В качестве примера можно привести свертывание крови. При нарушении целостности сосуда и начале формирования тромба происходит активация множества ферментов, называемых факторами свертывания. Некоторые из этих факторов влияют на другие неактивные ферменты в крови, окружающей тромб, таким образом продолжая его рост. Этот процесс идет до тех пор, пока дефект сосуда не закроется тромбом, и кровотечение не прекратится. Однако в некоторых случаях процесс может выходить из-под контроля, заканчиваясь нежелательным тромбообразованием. Так, основной причиной острого приступа стенокардии является формирование тромба на внутренней поверхности венечной артерии в области атеросклеротической бляшки. Рост тромба продолжается вплоть до полной закупорки просвета сосуда. Таким образом, когда некий параметр становится слишком высоким или низким, регуляторные системы включают отрицательные (либо положительные) обратные связи, которые путем некоторых изменений возвращают параметр к некий диапазон «НОРМЫ» и поддерживают гомеостаз.
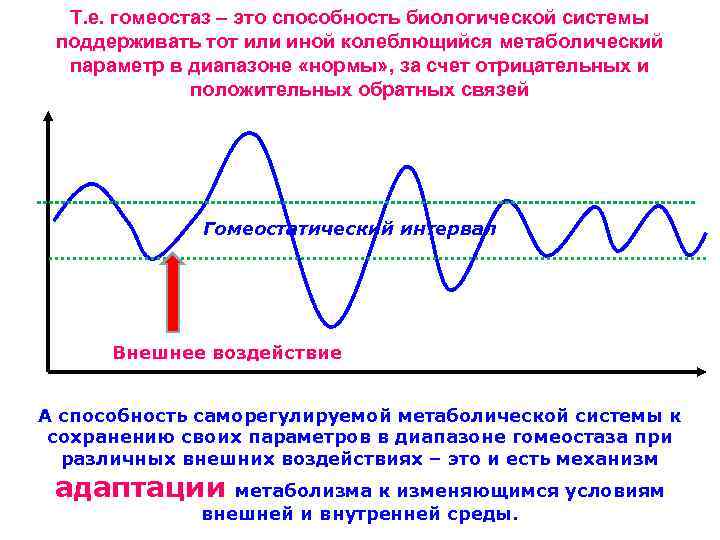
Т. е. гомеостаз – это способность биологической системы поддерживать тот или иной колеблющийся метаболический параметр в диапазоне «нормы» , за счет отрицательных и положительных обратных связей Гомеостатический интервал Внешнее воздействие А способность саморегулируемой метаболической системы к сохранению своих параметров в диапазоне гомеостаза при различных внешних воздействиях – это и есть механизм адаптации метаболизма к изменяющимся условиям внешней и внутренней среды.

1. Общие принципы метаболизма. 1. 4. Энергетический цикл в клетках. Биологическое окисление как уни версальный источник свободной химической энергии в живых клетках БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ совокупность ферментативных окислительно восстановительных реакций, протекающих в живых клетках. В процессе биологического окисления происходит расщепление питательных веществ, и освобождаемая при этом ЭНЕРГИЯ запасается в удобной для использования клетками форме т. н. богатых энергией (макроэргичес ких)соединений – пуриновых нуклеотидилтрифосфатов: АТФ, ГТФ и др. Эти соединения затем расходуются на обеспечение всех процессов жизнедеятельности; часть энергии рассеивается в виде тепла. Значительная часть реакций биологического окисления осуществляется в митохондриях.


Энергетический обмен (катаболизм, диссимиляция) — совокупность реакций расщепления органических веществ, сопровождающихся выделением энергии. Энергия, освобождающаяся при распаде органических веществ, не сразу используется клеткой, а запасается в форме АТФ и других макроэргических соединений. АТФ — универсальный аккумулятор биохимически полезной энергии, источник энергообеспечения клетки. Синтез АТФ происходит в клетках всех организмов в процессе фосфорилирования — присоединения неорганического фосфата к АДФ. У аэробных организмов (живущих в кислородной среде) выделяют три этапа энергетического обмена: подготовительный, бескислородное окисление и кислородное окисление; у анаэробных организмов (живущих в бескислородной среде) и аэробных при недостатке кислорода — два этапа: подготовительный, бескислородное окисление. Подготовительный этап Заключается в ферментативном расщеплении сложных органических веществ до простых: белковые молекулы — до аминокислот, жиры — до глицерина и карбоновых кислот, углеводы — до глюкозы, нуклеиновые кислоты — до нуклеотидов. Распад высокомолекулярных органических соединений осуществляется или ферментами желудочно кишечного тракта или ферментами лизосом. Вся высвобождающаяся при этом энергия рассеивается в виде тепла. Образовавшиеся небольшие органические молекулы могут быть использованы в качестве «строительного материала» или могут подвергаться дальнейшему расщеплению.

Бескислородное окисление, или гликолиз Этот этап заключается в дальнейшем расщеплении органических веществ, образовавшихся во время подготовительного этапа, происходит в цитоплазме клетки и в присутствии кислорода не нуждается. Главным источником энергии в клетке является глюкоза. Процесс бескислородного неполного расщепления глюкозы — гликолиз. Потеря электронов называется окислением, приобретение — восстановлением, при этом донор электронов окисляется, акцептор восстанавливается. Следует отметить, что биологическое окисление в клетках может происходить как с участием кислорода: А + О 2 → АО 2, так и без его участия, за счет переноса атомов водорода от одного вещества к другому. Например, вещество «А» окисляется за счет вещества «В» : АН 2 + В → А + ВН 2 или за счет переноса электронов, например, двухвалентное железо окисляется до трехвалентного: Fe 2+ → Fe 3+ + e—. Гликолиз — сложный многоступенчатый процесс, включающий в себя десять реакций. Во время этого процесса происходит дегидрирование глюкозы, акцептором водорода служит кофермент НАД+(никотинамидадениндинуклеотид). Глюкоза в результате цепочки ферментативных реакций превращается в две молекулы пировиноградной кислоты (ПВК), при этом суммарно образуются 2 молекулы АТФ и восстановленная форма переносчика водорода НАД·Н 2: С 6 Н 12 О 6 + 2 АДФ + 2 Н 3 РО 4 + 2 НАД+ → 2 С 3 Н 4 О 3 + 2 АТФ + 2 Н 2 О + 2 НАД·Н 2. Дальнейшая судьба ПВК зависит от присутствия кислорода в клетке. Если кислорода нет, у дрожжей и растений происходит спиртовое брожение, при котором сначала происходит образование уксусного альдегида, а затем этилового спирта: 1. С 3 Н 4 О 3 → СО 2 + СН 3 СОН, 2. СН 3 СОН + НАД·Н 2 → С 2 Н 5 ОН + НАД+.

У животных и некоторых бактерий при недостатке кислорода происходит молочнокислое брожение с образованием молочной кислоты: С 3 Н 4 О 3 + НАД·Н 2 → С 3 Н 6 О 3 + НАД+. В результате гликолиза одной молекулы глюкозы высвобождается 200 к. Дж, из которых 120 к. Дж рассеивается в виде тепла, а 80% запасается в связях АТФ. Кислородное окисление, или дыхание Заключается в полном расщеплении пировиноградной кислоты, происходит в митохондриях и при обязательном присутствии кислорода. Пировиноградная кислота транспортируется в митохондрии. Здесь происходит дегидрирование (отщепление водорода) и декарбоксилирование (отщепление углекислого газа) ПВК с образованием двухуглеродной ацетильной группы, которая вступает в цикл реакций, получивших название реакций цикла Кребса. Идет дальнейшее окисление, связанное с дегидрированием и декарбоксилированием. В результате на каждую Разрушенную молекулу ПВК из митохондрии удаляется три молекулы СО 2; образуется пять пар атомов водорода, связанных с переносчиками (4 НАД·Н 2, ФАД·Н 2), а также одна молекула ГТФ.

Суммарная реакция гликолиза и разрушения ПВК в митохондриях до водорода и углекислого газа выглядит следующим образом: С 6 Н 12 О 6 + 6 Н 2 О 6 СО 2 + 2 АТФ +2 ГТФ + 12 (2 Н) Две молекулы АТФ образуются в результате гликолиза, две ГТФ — в цикле Кребса; две молекулы НАДН (2 НАДН+Н+) восстанавливаются двумя парами атомов водорода в процессе гликолиза, восемь молекул НАДН пар — в цикле Кребса. В цикле Кребса же двумя парами атомов водорода восстанавливаются также две молекулы ФАД – до ФАДН +Н+ Последним этапом является окисление пар атомов водорода с участием кислорода до воды с одновременным фосфорилированием АДФ до АТФ. Водород передается трем большим ферментным комплексам (флавопротеины, коферменты Q, цитохромы) дыхательной цепи, расположенным во внутренней мембране митохондрий. У водорода отбираются электроны, которые в матриксе митохондрий в конечном итоге соединяются с кислородом: О 2 + e— О 2— Протоны закачиваются в межмембранное пространство митохондрий, в «протонный резервуар» . Внутренняя мембрана непроницаема для ионов водорода, с одной стороны она заряжается отрицательно (за счет О 2—), с другой — положительно (за счет Н+). Когда разность потенциалов на внутренней мембране достигает 200 м. В, протоны проходят через канал фермента АТФ синтетазы, образуется АТФ, а цитохромоксидаза катализирует восстановление кислорода до воды. Так в результате окисления 10 молекул НАДН и 2 молекул ФАДН образуется 34 молекулы АТФ: при окислении НАДН – 3 молекулы АТФ, ФАДН – 2 молекулы АТФ)

1 — наружная мембрана; 2 — межмембранное пространство, протонный резервуар; 3 — цитохромы; 4 — АТФ синтетаза. При перфорации внутренних митохондриальных мембран окисление НАД·Н 2 продолжается, но АТФ синтетаза не работает и образования АТФ в дыхательной цепи не происходит, энергия рассеивается в форме тепла (клетки «бурого жира» млекопитающих).
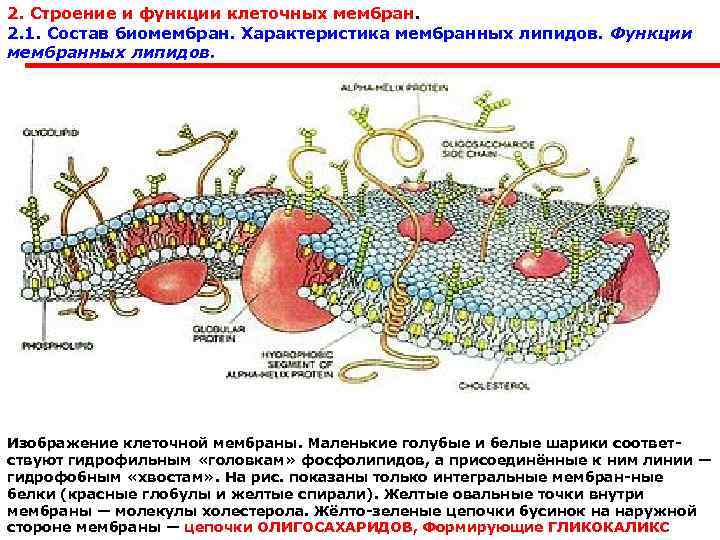
2. Строение и функции клеточных мембран. 2. 1. Состав биомембран. Характеристика мембранных липидов. Функции мембранных липидов. Изображение клеточной мембраны. Маленькие голубые и белые шарики соответ ствуют гидрофильным «головкам» фосфолипидов, а присоединённые к ним линии — гидрофобным «хвостам» . На рис. показаны только интегральные мембран ные белки (красные глобулы и желтые спирали). Желтые овальные точки внутри мембраны — молекулы холестерола. Жёлто зеленые цепочки бусинок на наружной стороне мембраны — цепочки ОЛИГОСАХАРИДОВ, Формирующие ГЛИКОКАЛИКС

Клеточная мембрана представляет собой двойной слой (БИСЛОЙ) молекул класса ЛИПИДОВ, большинство из которых представляет собой так называемые сложные липиды — ФОСФОЛИПИДОВ. Молекулы липидов имеют ГИДРОФИЛЬНУЮ ( «головка» ) и ГИДРОФОБНУЮ ( «хвост» ) часть. При образовании мембран гидрофобные участки молекул оказываются обращены внутрь, а ГИДРОФИЛЬНЫЕ — наружу. Мембраны — структуры ИНВАРИАБЕЛЬНЫ, весьма сходные у разных организмов. Толщина мембраны составляет 7— 8 нм. Биологическая мембрана включает и различные белки: интегральные (пронизывающие мембрану насквозь), полуинтегральные (погруженные одним концом во внешний или внутренний липидный слой), поверхностные (рас положенные на внешней или прилегающие к внутренней сторонам мембраны). Некоторые белки являются точками контакта клеточной мембраны с цитоскелетом Внутри клетки, и клеточной стенкой (если она есть) снаружи. Некоторые из интегральных белков выпол Няют функцию ионных каналов, различных транспортеров и рецепторов.

Мембраны состоят из липидов трёх классов: фосфолипиды, гликолипиды и холестерол. Фосфолипиды и гликолипиды (липиды с присоединёнными к ним углеводами) состоят из двух длинных гидрофобных углеводородных «хвостов» , которые связаны с заряженной гидрофильной «головой» . Холестерол придаёт мембране жёсткость, занимая свободное пространство между гидрофобными хвостами липидов и не позволяя им изгибаться. Поэтому мембраны с малым содержанием холестерола более гибкие, а с большим — более жёсткие и хрупкие. Также холестерол служит «стопором» , препятствующим перемещению полярных молекул из клетки и в клетку. Важную часть мембраны составляют белки, пронизывающие её и отвечающие за разнообразные свойства мембран. Их состав и ориентация в разных мембранах различаются. Клеточные мембраны часто асимметричны, то есть слои отличаются по составу липидов, переход отдельной молекулы из одного слоя в другой (так называемый флип флоп) затруднён.

Вторая часть

2. Строение и функции клеточных мембран. 2. 2. Функции биологических мембран ФУНКЦИИ: 1) Барьерная — обеспечивает регулируемый, избирательный, пассивный и активный обмен веществ с окружающей средой. Например, мембрана пероксисом защищает цитоплазму от опасных для клетки пероксидов. 2)Избирательная проницаемость означает, что проницаемость мембраны для различных атомов или молекул зависит не только от их размеров и электнрического заряда, но и от химических свойств. Избирательная проницаемость обеспечивает отделение клетки и клеточных компартментов от окружающей среды и снабжение их необходимыми веществами. 3) Транспортная — через мембрану происходит транспорт веществ в клетку и из клетки. Транспорт через мембраны обеспечивает: доставку питательных веществ, удаление конечных продуктов обмена, секрецию различных веществ, создание ионных градиентов, поддержание в клетке оптимального р. Н и концентрации ионов, которые нужны для работы клеточных ферментов. Частицы, по какой либо причине неспособные пересечь фосфолипидный бислой (например, из за гидрофильных свойств, так как мембрана внутри гидрофобна и не пропускает гидрофильные вещества, или из за крупных размеров), но необходимые для клетки, могут проникнуть сквозь мембрану через специальные белки переносчики (транспортеры) и белки каналы или путем эндоцитоза. При пассивном транспорте вещества пересекают липидный бислой без затрат энергии по градиенту концентрации путем диффузии. Вариантом этого механизма является облегчённая диффузий, при которой веществу помогает пройти через мембрану какая либо специфическая молекула. У этой молекулы может быть канал, пропускающий вещества только одного типа.

Активный транспорт требует затрат энергии, так как происходит против градиента концентрации. На мембране существуют специальные белки насосы, в том числе АТФаза, которая активно вкачивает в клетку ионы K+ и выкачивают из неё ионы Na+. 4) Матричная — обеспечивает определенное взаиморасположение и ориентацию мембранных белков, их оптимальное взаимодействие. 5) Механическая — обеспечивает автономность клетки, ее внутриклеточных структур, также соединение с другими клетками (в тканях). Большую роль в обеспечение механической функции имеют клеточные стенки, а у животных — межклеточное вещество. 6) Энергетическая — при фотосинтезе в хлоропластах и клеточном дыхании в митохондриях в их мембранах действуют системы переноса энергии, в которых также участвуют белки; 7) Рецепторная — некоторые белки, находящиеся в мембране, являются рецепторами (молекулами, при помощи которых клетка воспринимает те или иные сигналы). Например, гормоны, циркулирующие в крови, действуют только на такие клетки мишени, у которых есть соответствующие этим гормонам рецепторы. Нейромедиаторы(химические вещества, обеспечивающие проведение нервных импульсов) тоже связываются с особыми рецепторными белками клеток мишеней. ферментативная — мембранные белки нередко являются ферментами. Например, плазматические мембраны эпителиальных клеток кишечника содержат пищеварительные ферменты.

8) Осуществление генерации и проведения биопотенциалов. С помощью мембраны в клетке поддерживается постоянная концентрация ионов: концентрация иона К+ внутри клетки значительно выше, чем снаружи, а концентрация Na+ значительно ниже, что очень важно, так как это обеспечивает поддержание разности потенциалов на мембране и генерацию нервного импульса. 9) Маркировка клетки (ТКАНЕСПЕЦИФИЧНО АНТИГЕННАЯ ФУНКЦИЯ) — на мембране есть АНТИГЕНЫ, действующие как маркеры — «ярлыки» , позволяющие опознать клетку. Это ГЛИКОПРОТЕИНЫ (то есть белки с присоединенными к ним разветвленными олигосахаридными боковыми цепями), играющие роль «антенн» . Из за бесчисленного множества конфигурации боковых цепей возможно сделать для каждого типа клеток свой особый маркер. С помощью маркеров клетки могут распознавать другие клетки и действовать согласованно с ними, например, при формировании органов и тканей. Это же позволяет ИММУННОЙ СИСТЕМЕ распознавать чужеродные антигены.

2. 3. Олигосахаридные компоненты мембран. Общие представления об их локализации и структуре. Механизм биосинтеза гликоконьюгатов олиго гликозилтрансферазы и олигогликозилгидролазы. Функции гликоконью гатов: антигенные детерминанты групп крови, тканеспецифичные мембранные антигены, составная часть сигнального пептида, адгезивность и другие. Мембранные гликоконьюгаты синтезируются по блочному принципу на внутренней строне мембраны и с участием ферментов олигогликозилтрансфераз транспортируются на внешнюю сторону мембраны (гидролизуются с участием ферментов олигогликозилгидролаз). Функции гликоконьюгатов: антигенные детерминанты групп крови, тканеспецифичные мембранные антигены, составная часть сигнального пептида, адгезивность и другие. При их гидролизе клетка теряет специфичность (она становится невидимой для иммунокомпететных систем, не включается апоптоз, клетка становится «бессмертной» ), уменьшаются её адгезивность с соседними клетками (метастазирование), т. е. это один из основнх механизмов ЗЛОКАЧЕСТВЕННОГО ПЕРЕРОЖДЕНИЯ КЛЕТОК !!!

2. Строение и функции клеточных мембран. 2. 4. Структура биологических мембран. Современная концепция структуры биологических мембран теория “Липидного моря”. Конформационные свойства мембран. Динамическое состояние липидов в мембране. Фазовые переходы. Ассиметрия бислоя. Модификация бислоя белками. Влияние на липидный состав. Изменение гидратации бислоя.
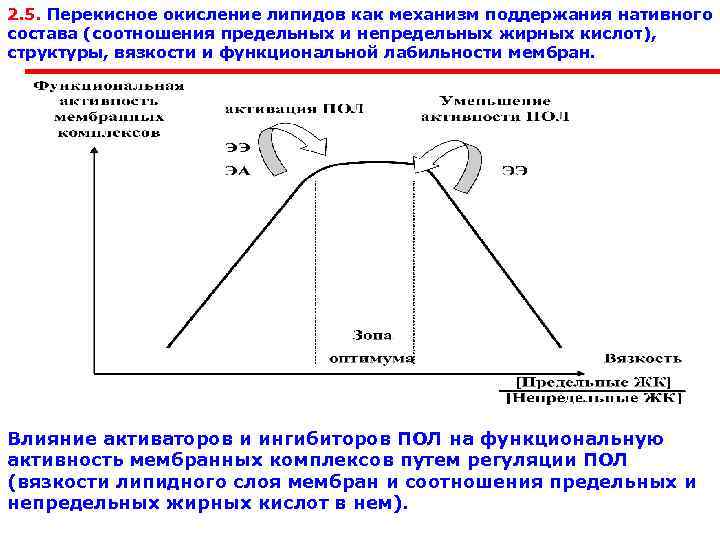
2. 5. Перекисное окисление липидов как механизм поддержания нативного состава (соотношения предельных и непредельных жирных кислот), структуры, вязкости и функциональной лабильности мембран. Влияние активаторов и ингибиторов ПОЛ на функциональную активность мембранных комплексов путем регуляции ПОЛ (вязкости липидного слоя мембран и соотношения предельных и непредельных жирных кислот в нем).

2. 6. Роль молекулярного кислорода, природного естественного радиаци онного фона Земли, супероксиддисмутаз и низкомолекулярных антиокси дантов в этом процессе. Молекулярный кислород, природный естественный радиационный фон Земли ПРООКСИДАНТЫ Супероксиддисмутазы, низкомолекулярные антиоксиданты – АНТИОКСИДАНТЫ ЭТО РЕГУЛЯТОРЫ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ МЕМБРАННЫХ КОМПЛЕКСОВ
![Оптимизация функциональной активности Хим. Активаторы ПОЛ всех мембранных комплексов [холестерин] [*O 2 -] Ионизирующее Оптимизация функциональной активности Хим. Активаторы ПОЛ всех мембранных комплексов [холестерин] [*O 2 -] Ионизирующее](https://present5.com/presentation/3/-42638375_166294737.pdf-img/-42638375_166294737.pdf-36.jpg)
Оптимизация функциональной активности Хим. Активаторы ПОЛ всех мембранных комплексов [холестерин] [*O 2 -] Ионизирующее и ЭМ излучение, холодовой фактор и т. д. Солюбилизаторы мембраны Увеличение степени погруженности белковых компонентов мембраны в липидный слой VПОЛ Доля ненасыщенных ЖК Снижение степени погруженности белковых компонентов мембраны в липидный слой Уплотнение мембран, Разжижение мембран, уменьшение увеличение вязкости Доля ненасыщенных ЖК Оптимизация функциональной активности всех мембранных комплексов V выхода липидов из мембран VПОЛ [*O 2 -] антиоксиданты V обновления липидов и белков мембран

2. 10. Функции лизосом. Лизосомные болезни

3. Общие принципы организации биоэнергетических систем. Энергетика живых систем. 3. 1. Энергетические ресурсы, виды источников энергии. Биологический принцип высвобождения энергии (теория Палладина о дегидрогенизации органического вещества при дыхании).

3. Общие принципы организации биоэнергетических систем. Энергетика живых систем. 3. 2. Основные биологические окислительно восстановительные системы. Термодинамика открытой системы и процессы жизнедеятельности. Понятие об знтропии и биологическая работа как векторный перенос энергии. Изменение свободной энергии при окислительно восстанови тельных реакциях, злектрохимический злемент как система для транс формации энергии из химической формы в электрическую и обратно в химическую. Макроэрги.

3. Общие принципы организации биоэнергетических систем. Энергетика живых систем. 3. 3. Биомембраны как материальные структуры, обеспечивающие транс формацию и аккумуляцию биологически полезной энергии (аналог элек трохимического злемента). Молекулярные механизмы трансформации энергии: функциональные комплексы электрон транспортной цепи митохондрий. Понятие о трансмембранном потенциале (теория Митчела, эксперименты Скулачева).
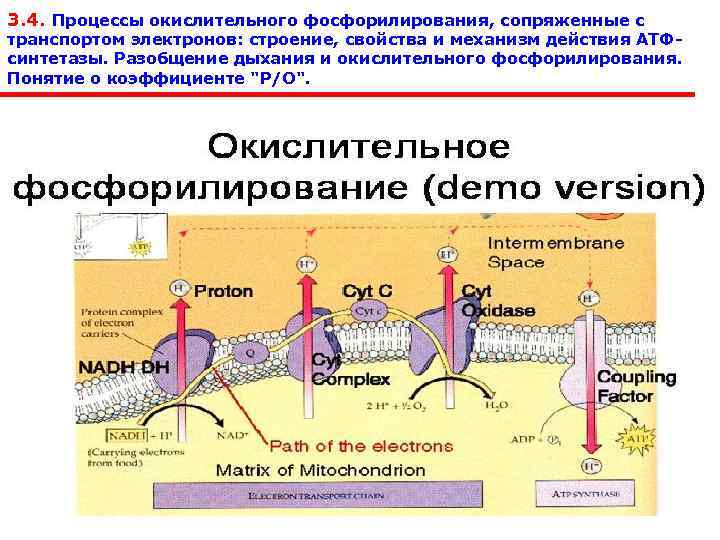
3. 4. Процессы окислительного фосфорилирования, сопряженные с транспортом электронов: строение, свойства и механизм действия АТФ синтетазы. Разобщение дыхания и окислительного фосфорилирования. Понятие о коэффициенте "Р/О".

3. 5. Терморегуляция и термоадаптация. Нарушение окисли тельного фосфорилирования.

3. 6. Электрохимический градиент ионов как универсальная биологичес- кая форма запасания энергии. Формы и механизмы преобразования энергии электрохимического градиента ионов: реализация активного транспорта веществ в сократительных системах и синтез АТФ - основного "аккумулятора" биохимически полезной энергии в метаболических реакциях.

3. 7. Примеры субстратного фосфорелирования.

3. 8. Экологическая модификация режима работы биоэнергетического аппарата

Благодарю за внимание ! Лекция окончена
Лекция_5_биохим_организация_живой_системы2.ppt