Курс лекций












































 Курс лекций «Физико-химические и физические методы аналитической химии» . Разделение и концентрирование. Гибридные методы анализа. Д. т. н. Алексей Леонидович Москвин
Курс лекций «Физико-химические и физические методы аналитической химии» . Разделение и концентрирование. Гибридные методы анализа. Д. т. н. Алексей Леонидович Москвин
 Предпосылки развития Почему существует необходимость в параллельном развитии методов определения и разделения? Как известно, есть изотопный, элементный, молекулярный и вещественный анализ. Возможности простых общедоступных (с экономической точки зрения) методов определения аналитов в любом виде анализа практически исчерпаны. Каждый новый шаг дается с большим трудом за счет усложнения и удорожания методов. Возможности известных методов определения ограничены и по селективности, и по пределам обнаружения. Причем для молекулярного анализа пока в принципе не существует прямых методов определения, обладающих необходимой чувствительностью и селективностью.
Предпосылки развития Почему существует необходимость в параллельном развитии методов определения и разделения? Как известно, есть изотопный, элементный, молекулярный и вещественный анализ. Возможности простых общедоступных (с экономической точки зрения) методов определения аналитов в любом виде анализа практически исчерпаны. Каждый новый шаг дается с большим трудом за счет усложнения и удорожания методов. Возможности известных методов определения ограничены и по селективности, и по пределам обнаружения. Причем для молекулярного анализа пока в принципе не существует прямых методов определения, обладающих необходимой чувствительностью и селективностью.
 Предпосылки развития Подавляющее большинство методов молекулярного анализа сегодня - гибридные, т. е. основанные на органичном сочетании методов разделения и определения (Hy-phenated methods). Наиболее распространенные среди них - хроматографические (более 50% анализов в мире выполняется хроматографи- ческими методами).
Предпосылки развития Подавляющее большинство методов молекулярного анализа сегодня - гибридные, т. е. основанные на органичном сочетании методов разделения и определения (Hy-phenated methods). Наиболее распространенные среди них - хроматографические (более 50% анализов в мире выполняется хроматографи- ческими методами).
 Предпосылки развития СТАДИИ ХИМИЧЕСКОГО АНАЛИЗА: -ПРОБООТБОР -ПРОБОПОДГОТОВКА; - ГРАДУИРОВКА СРЕДСТВ ИЗМЕРЕНИЯ; - СОБСТВЕННО ИЗМЕРЕНИЕ АНАЛИТИЧЕСКОГО СИГНАЛА; - ОБРАБОТКА И ПРЕДСТАВЛЕНИЕ ИНФОРМАЦИИ. ТОЧНОСТЬ РЕЗУЛЬТАТОВ АНАЛИЗА ВО МНОГОМ ОПРЕДЕЛЯЕТСЯ ПЕРВОЙ и ВТОРОЙ СТАДИЕЙ.
Предпосылки развития СТАДИИ ХИМИЧЕСКОГО АНАЛИЗА: -ПРОБООТБОР -ПРОБОПОДГОТОВКА; - ГРАДУИРОВКА СРЕДСТВ ИЗМЕРЕНИЯ; - СОБСТВЕННО ИЗМЕРЕНИЕ АНАЛИТИЧЕСКОГО СИГНАЛА; - ОБРАБОТКА И ПРЕДСТАВЛЕНИЕ ИНФОРМАЦИИ. ТОЧНОСТЬ РЕЗУЛЬТАТОВ АНАЛИЗА ВО МНОГОМ ОПРЕДЕЛЯЕТСЯ ПЕРВОЙ и ВТОРОЙ СТАДИЕЙ.
 Предпосылки развития Методы разделения применяются на ВТОРОЙ И ТРЕТЬЕЙ СТАДИЯХ. На ВТОРОЙ СТАДИИ, в связи с тем, что какими бы низкими не были пределы обнаружения аналитических методов, всегда возникают задачи, где нужны еще более низкие пределы обнаружения. Кроме того, «целевые» компоненты - аналиты всегда сопровождаются примесными и самой средой, которые оказывают мешающее действие на определение аналитов. Необходимость снижения пределов обнаружения аналитических методов легко проследить на примере уровней ПДК загрязнителй в объектах окружающей среды в различные периоды времени: 60 -70 г. г. - p. p. m. 80 -90 г. г. - p. p. b. 2000 -2010 г. г. - p. p. t.
Предпосылки развития Методы разделения применяются на ВТОРОЙ И ТРЕТЬЕЙ СТАДИЯХ. На ВТОРОЙ СТАДИИ, в связи с тем, что какими бы низкими не были пределы обнаружения аналитических методов, всегда возникают задачи, где нужны еще более низкие пределы обнаружения. Кроме того, «целевые» компоненты - аналиты всегда сопровождаются примесными и самой средой, которые оказывают мешающее действие на определение аналитов. Необходимость снижения пределов обнаружения аналитических методов легко проследить на примере уровней ПДК загрязнителй в объектах окружающей среды в различные периоды времени: 60 -70 г. г. - p. p. m. 80 -90 г. г. - p. p. b. 2000 -2010 г. г. - p. p. t.
 Предпосылки развития Чтобы оценивать влияние антропогенного вклада в содержание загрязнителей в объектах окружающей среды, необходимо определять фоновые концентрации, которые, как правило, ниже самых “жестких” норм. Потребность в методах разделения на ТРЕТЬЕЙ СТАДИИ - решение препаративных задач для градуировки, начиная с получения растворителей и кончая выделением определяемых веществ.
Предпосылки развития Чтобы оценивать влияние антропогенного вклада в содержание загрязнителей в объектах окружающей среды, необходимо определять фоновые концентрации, которые, как правило, ниже самых “жестких” норм. Потребность в методах разделения на ТРЕТЬЕЙ СТАДИИ - решение препаративных задач для градуировки, начиная с получения растворителей и кончая выделением определяемых веществ.
 Определения Разделение – процесс или операция, в результате которых из исходной смеси веществ получается несколько фракций ее компонентов с новым качественным и количественным составом; Концентрирование – процесс или операция увеличения содержания целевых компонентов по отношению к матрице. Разделение и концентрирование основано на общих физико- химических законах. Различия в целях: Разделение ставит своей целью компенсировать недостаточную селективность методов определения и обеспечить упрощение методов определения, а также решение препаративных задач. Концентрирование - снижение пределов обнаружения и тем самым расширение диапазонов определяемых концентраций.
Определения Разделение – процесс или операция, в результате которых из исходной смеси веществ получается несколько фракций ее компонентов с новым качественным и количественным составом; Концентрирование – процесс или операция увеличения содержания целевых компонентов по отношению к матрице. Разделение и концентрирование основано на общих физико- химических законах. Различия в целях: Разделение ставит своей целью компенсировать недостаточную селективность методов определения и обеспечить упрощение методов определения, а также решение препаративных задач. Концентрирование - снижение пределов обнаружения и тем самым расширение диапазонов определяемых концентраций.
 Определения Общие характеристики: (qi)кон/(qj)кон (qi)кон(qj)нач Кр=Кконц= ------------ = -----------, (qi)нач/(qj)нач (qj)кон (qi)нач где i - целевой компонент, j - мешающий Степень выделения: Ri = (qi)кон/(qi)нач Kp = Ri/Rj Ri и Rj не поддаются формализации, всегда взаимосвязаны. Повышение Ri редко приводит к повышению Кр.
Определения Общие характеристики: (qi)кон/(qj)кон (qi)кон(qj)нач Кр=Кконц= ------------ = -----------, (qi)нач/(qj)нач (qj)кон (qi)нач где i - целевой компонент, j - мешающий Степень выделения: Ri = (qi)кон/(qi)нач Kp = Ri/Rj Ri и Rj не поддаются формализации, всегда взаимосвязаны. Повышение Ri редко приводит к повышению Кр.
 Классификация методов разделения Первая классификация – по границе раздела: МЕТОДЫ РАЗДЕЛЕНИЯ ГЕТЕРОГЕННЫХ СМЕСЕЙ - макроскопически неоднородных систем, состоящих из частей, имеющих границы раздела. МЕТОДЫ РАЗДЕЛЕНИЯ ГОМОГЕННЫХ СМЕСЕЙ - макроскопически однородных; неоднородность на атомно- молекулярном или изотопном уровне.
Классификация методов разделения Первая классификация – по границе раздела: МЕТОДЫ РАЗДЕЛЕНИЯ ГЕТЕРОГЕННЫХ СМЕСЕЙ - макроскопически неоднородных систем, состоящих из частей, имеющих границы раздела. МЕТОДЫ РАЗДЕЛЕНИЯ ГОМОГЕННЫХ СМЕСЕЙ - макроскопически однородных; неоднородность на атомно- молекулярном или изотопном уровне.
 Классификация методов разделения МЕТОДЫ РАЗДЕЛЕНИЯ ГЕТЕРОГЕННЫХ СМЕСЕЙ: фильтрация, седиментация, центрифугирование, центробежная сепарация, флотация. Большинство методов хорошо известно. Граница между методами разделения гетерогенных и гомогенных смесей весьма условна, часто используются общие принципы. В аналитической химии часто СОЧЕТАЮТСЯ МЕТОДЫ РАЗДЕЛЕНИЯ ГОМОГЕННЫХ И ГЕТЕРОГЕННЫХ СМЕСЕЙ. Например, осаждение с фильтрацией или центрифугированием.
Классификация методов разделения МЕТОДЫ РАЗДЕЛЕНИЯ ГЕТЕРОГЕННЫХ СМЕСЕЙ: фильтрация, седиментация, центрифугирование, центробежная сепарация, флотация. Большинство методов хорошо известно. Граница между методами разделения гетерогенных и гомогенных смесей весьма условна, часто используются общие принципы. В аналитической химии часто СОЧЕТАЮТСЯ МЕТОДЫ РАЗДЕЛЕНИЯ ГОМОГЕННЫХ И ГЕТЕРОГЕННЫХ СМЕСЕЙ. Например, осаждение с фильтрацией или центрифугированием.
 Флотация - разделение порошкообразных материалов за счет различной смачиваемости водой их поверхности. При разделении этим методом водную суспензию измельченных компонентов смеси обрабатывают специальными реагентами (анионными и катионными или неионогенными поверхностно- активными веществами), которые избирательно адсорбируются на поверхности частиц извлекаемого компонента и понижают их смачиваемость водой. Затем через суспензию пропускают воздух в виде мелких пузырьков, прилипающих к гидрофобизи- рованной поверхности частиц твердой фазы. Частицы выделяемых компонентов с прилипшими пузырьками воздуха всплывают, в результате чего над поверхностью суспензии образуется довольно устойчивый слой пены, обогащенной извлекаемыми компонентами
Флотация - разделение порошкообразных материалов за счет различной смачиваемости водой их поверхности. При разделении этим методом водную суспензию измельченных компонентов смеси обрабатывают специальными реагентами (анионными и катионными или неионогенными поверхностно- активными веществами), которые избирательно адсорбируются на поверхности частиц извлекаемого компонента и понижают их смачиваемость водой. Затем через суспензию пропускают воздух в виде мелких пузырьков, прилипающих к гидрофобизи- рованной поверхности частиц твердой фазы. Частицы выделяемых компонентов с прилипшими пузырьками воздуха всплывают, в результате чего над поверхностью суспензии образуется довольно устойчивый слой пены, обогащенной извлекаемыми компонентами
 Седиментация Термин седиментация буквально обозначает оседание, т. е. процесс выделения взвешенных частиц из жидкости или газа под действием гравитационного поля. Этот термин одновременно является названием метода разделения частиц различной дисперсности, использующего в качестве их характеристического свойства скорость осаждения, которая помимо плотности вещества, из которого образованы частицы, и их собственных размеров зависит от плотности и вязкости среды, в которой они осаждаются. Эти параметры среды могут специально регулироваться в зависимости от природы разделяемых частиц. Основная область применения седиментации в анализе - препаративные задачи фракционирования сорбентов.
Седиментация Термин седиментация буквально обозначает оседание, т. е. процесс выделения взвешенных частиц из жидкости или газа под действием гравитационного поля. Этот термин одновременно является названием метода разделения частиц различной дисперсности, использующего в качестве их характеристического свойства скорость осаждения, которая помимо плотности вещества, из которого образованы частицы, и их собственных размеров зависит от плотности и вязкости среды, в которой они осаждаются. Эти параметры среды могут специально регулироваться в зависимости от природы разделяемых частиц. Основная область применения седиментации в анализе - препаративные задачи фракционирования сорбентов.
 Сепарационные методы Методы этой группы и технические средства сепарационного разделения различаются в зависимости от природы сил, вызывающих эффект разделения. Наиболее общий случай – центробежная сепарация, реже – магнитная. В границах первой выделяют воздушную сепарацию и сепарацию эмульсий. Оба варианта метода находят промышленное применение и имеют множество конструкций сепарационных устройств, различающихся по эффективности. Воздушная сепарация является одним из основных промышленных способов пылеулавливания. Основным типом эмульсий, разделяемых сепарационным методом, является молоко. Наконец, магнитная сепарация находит применение для обогащения магнитных фракций железосодержащих руд.
Сепарационные методы Методы этой группы и технические средства сепарационного разделения различаются в зависимости от природы сил, вызывающих эффект разделения. Наиболее общий случай – центробежная сепарация, реже – магнитная. В границах первой выделяют воздушную сепарацию и сепарацию эмульсий. Оба варианта метода находят промышленное применение и имеют множество конструкций сепарационных устройств, различающихся по эффективности. Воздушная сепарация является одним из основных промышленных способов пылеулавливания. Основным типом эмульсий, разделяемых сепарационным методом, является молоко. Наконец, магнитная сепарация находит применение для обогащения магнитных фракций железосодержащих руд.
 Сепарационные методы Среди методов сепарации сегодня развиваются методы рентгенолюминесцентной, рентгенофлюоресцентной и оптической сепарации. К числу сепарационных методов относится центрифугирование, являющееся одной из основных аналитических процедур при разделении веществ методом осаждения. Основываясь на принципах центробежной сепарации, аналитические центрифуги отличаются от промышленных сепараторов особенностями конструкций, позволяющих проводить последовательное разделение небольших порций гетерогенных смесей.
Сепарационные методы Среди методов сепарации сегодня развиваются методы рентгенолюминесцентной, рентгенофлюоресцентной и оптической сепарации. К числу сепарационных методов относится центрифугирование, являющееся одной из основных аналитических процедур при разделении веществ методом осаждения. Основываясь на принципах центробежной сепарации, аналитические центрифуги отличаются от промышленных сепараторов особенностями конструкций, позволяющих проводить последовательное разделение небольших порций гетерогенных смесей.
 Фильтрация только в грубом приближении может рассматриваться как метод, основанный на ситовом эффекте, т. е. удерживании частиц на фильтре, поры которого имеют более мелкие размеры, чем размеры удерживаемых частиц. Реально на ситовый эффект накладываются процессы ассоциации частиц с образованием более крупных конгломератов, электростатические взаимодействия фильтруемых частиц с матрицей фильтра и т. п. Поэтому фильтрация строго не может рассматриваться как метод разделения частиц различной дисперсности даже при наличии мембранных фильтров со строго регламентированными размерами пор. Фильтрация чаще является методом суммарного выделения взвешенных частиц осадка из жидкостей или аэрозолей из газовой фазы.
Фильтрация только в грубом приближении может рассматриваться как метод, основанный на ситовом эффекте, т. е. удерживании частиц на фильтре, поры которого имеют более мелкие размеры, чем размеры удерживаемых частиц. Реально на ситовый эффект накладываются процессы ассоциации частиц с образованием более крупных конгломератов, электростатические взаимодействия фильтруемых частиц с матрицей фильтра и т. п. Поэтому фильтрация строго не может рассматриваться как метод разделения частиц различной дисперсности даже при наличии мембранных фильтров со строго регламентированными размерами пор. Фильтрация чаще является методом суммарного выделения взвешенных частиц осадка из жидкостей или аэрозолей из газовой фазы.
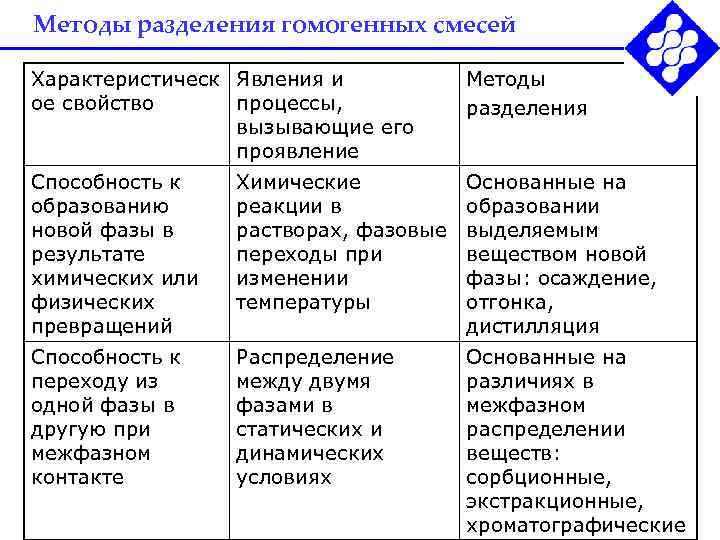
 Методы разделения гомогенных смесей Характеристическ Явления и Методы ое свойство процессы, разделения вызывающие его проявление Способность к Химические Основанные на образованию реакции в образовании новой фазы в растворах, фазовые выделяемым результате переходы при веществом новой химических или изменении фазы: осаждение, физических температуры отгонка, превращений дистилляция Способность к Распределение Основанные на переходу из между двумя различиях в одной фазы в фазами в межфазном другую при статических и распределении межфазном динамических веществ: контакте условиях сорбционные, экстракционные, хроматографические
Методы разделения гомогенных смесей Характеристическ Явления и Методы ое свойство процессы, разделения вызывающие его проявление Способность к Химические Основанные на образованию реакции в образовании новой фазы в растворах, фазовые выделяемым результате переходы при веществом новой химических или изменении фазы: осаждение, физических температуры отгонка, превращений дистилляция Способность к Распределение Основанные на переходу из между двумя различиях в одной фазы в фазами в межфазном другую при статических и распределении межфазном динамических веществ: контакте условиях сорбционные, экстракционные, хроматографические
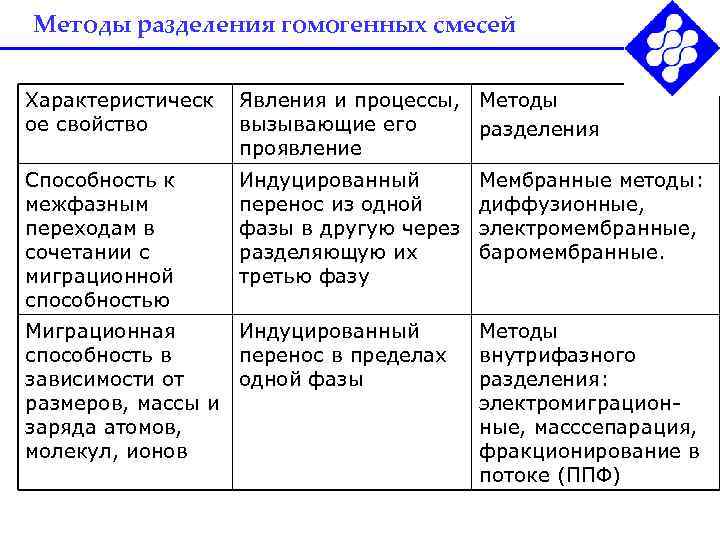
 Методы разделения гомогенных смесей Характеристическ Явления и процессы, Методы ое свойство вызывающие его разделения проявление Способность к Индуцированный Мембранные методы: межфазным перенос из одной диффузионные, переходам в фазы в другую через электромембранные, сочетании с разделяющую их баромембранные. миграционной третью фазу способностью Миграционная Индуцированный Методы способность в перенос в пределах внутрифазного зависимости от одной фазы разделения: размеров, массы и электромиграцион- заряда атомов, ные, масссепарация, молекул, ионов фракционирование в потоке (ППФ)
Методы разделения гомогенных смесей Характеристическ Явления и процессы, Методы ое свойство вызывающие его разделения проявление Способность к Индуцированный Мембранные методы: межфазным перенос из одной диффузионные, переходам в фазы в другую через электромембранные, сочетании с разделяющую их баромембранные. миграционной третью фазу способностью Миграционная Индуцированный Методы способность в перенос в пределах внутрифазного зависимости от одной фазы разделения: размеров, массы и электромиграцион- заряда атомов, ные, масссепарация, молекул, ионов фракционирование в потоке (ППФ)
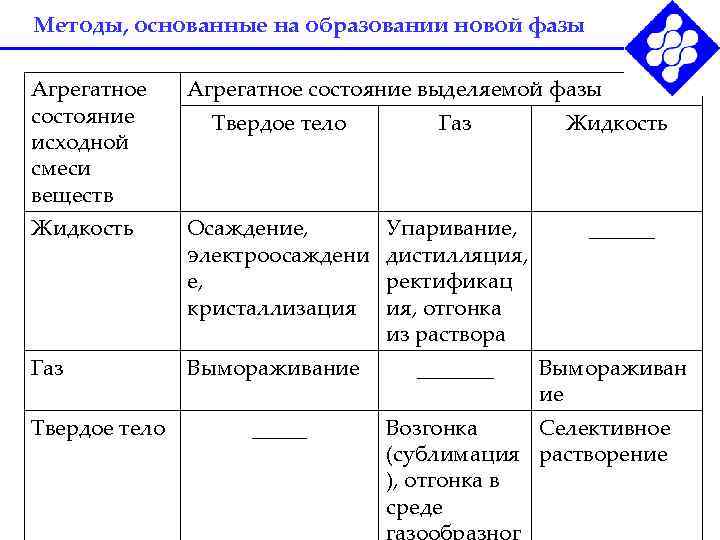
 Методы, основанные на образовании новой фазы Агрегатное состояние выделяемой фазы состояние Твердое тело Газ Жидкость исходной смеси веществ Жидкость Осаждение, Упаривание, ______ электроосаждени дистилляция, е, ректификац кристаллизация ия, отгонка из раствора Газ Вымораживание _______ Вымораживан ие Твердое тело _____ Возгонка Селективное (сублимация растворение ), отгонка в среде
Методы, основанные на образовании новой фазы Агрегатное состояние выделяемой фазы состояние Твердое тело Газ Жидкость исходной смеси веществ Жидкость Осаждение, Упаривание, ______ электроосаждени дистилляция, е, ректификац кристаллизация ия, отгонка из раствора Газ Вымораживание _______ Вымораживан ие Твердое тело _____ Возгонка Селективное (сублимация растворение ), отгонка в среде
 Осаждение – метод разделения веществ, находящихся в растворе или специально переведенных в растворенное состояние, основанный на образовании выделяемыми или отделяемыми компонентами раствора малорастворимых соединений за счет взаимодействия с реагентом – осадителем. Этот древнейший метод разделения не потерял своей актуальности как первая ступень метода гравиметрии. Кроме того, осаждение находит применение для препаративного выделения веществ из растворов и реже для отделения сопутствующих аналитам примесей на стадии пробоподготовки. С основными закономерностями реакций образования малорастворимых соединений вы знакомы из курса «Химические методы анализа» .
Осаждение – метод разделения веществ, находящихся в растворе или специально переведенных в растворенное состояние, основанный на образовании выделяемыми или отделяемыми компонентами раствора малорастворимых соединений за счет взаимодействия с реагентом – осадителем. Этот древнейший метод разделения не потерял своей актуальности как первая ступень метода гравиметрии. Кроме того, осаждение находит применение для препаративного выделения веществ из растворов и реже для отделения сопутствующих аналитам примесей на стадии пробоподготовки. С основными закономерностями реакций образования малорастворимых соединений вы знакомы из курса «Химические методы анализа» .
 Осаждение Эффект разделения проявляется за счет образования выделяемым веществом малорастворимых соединений: - соли минеральных кислот (Ba. SO 4, Ag. Cl) - гидроксиды и слабые минеральные кислоты (Fe(OH)3, H 2 WO 4) - вещества в элементарном состоянии ( Se, Te, Au и т. д. ) - соединения ионов металлов с органическими реагентами (диметилглиоксимат Ni). Влияние избытка реагента неоднозначно: Ba 2+ + SO 42 - = Ba. SO 4, чем больше концентрация сульфат-ионов, тем полнее осаждение сульфата бария; но Ag+ + Cl- = Ag. Cl + Cl- = [Ag. Cl 2]- где избыток хлорид-ионов приводит к растворению осадка.
Осаждение Эффект разделения проявляется за счет образования выделяемым веществом малорастворимых соединений: - соли минеральных кислот (Ba. SO 4, Ag. Cl) - гидроксиды и слабые минеральные кислоты (Fe(OH)3, H 2 WO 4) - вещества в элементарном состоянии ( Se, Te, Au и т. д. ) - соединения ионов металлов с органическими реагентами (диметилглиоксимат Ni). Влияние избытка реагента неоднозначно: Ba 2+ + SO 42 - = Ba. SO 4, чем больше концентрация сульфат-ионов, тем полнее осаждение сульфата бария; но Ag+ + Cl- = Ag. Cl + Cl- = [Ag. Cl 2]- где избыток хлорид-ионов приводит к растворению осадка.
 Осаждение Если при добавлении реагента-осадителя одно из двух разделяемых веществ А образует малорастворимое соединение, а другое вещество В его не образует, то коэффициент разделения этих веществ KA/B, согласно определению, теоретически будет стремиться к бесконечности. Если оба разделяемых вещества образуют малорастворимые соединения, то такой вариант осаждения называется совместным осаждением. При осаждении коэффициент разделения двух компонентов, одновременно образующих малорастворимое соединение, зависит от отношения исходных концентраций разделяемых веществ и тем больше, чем больше концентрация компонента, образующего менее растворимое соединение, и чем меньше концентрация компонента, образующего более растворимое соединение.
Осаждение Если при добавлении реагента-осадителя одно из двух разделяемых веществ А образует малорастворимое соединение, а другое вещество В его не образует, то коэффициент разделения этих веществ KA/B, согласно определению, теоретически будет стремиться к бесконечности. Если оба разделяемых вещества образуют малорастворимые соединения, то такой вариант осаждения называется совместным осаждением. При осаждении коэффициент разделения двух компонентов, одновременно образующих малорастворимое соединение, зависит от отношения исходных концентраций разделяемых веществ и тем больше, чем больше концентрация компонента, образующего менее растворимое соединение, и чем меньше концентрация компонента, образующего более растворимое соединение.
 Осаждение На практике, даже в том случае, когда одно из разделяемых веществ не образует осадка, коэффициент разделения, как правило, не превышает 103. В первую очередь это обусловлено соосаждением, то есть распределением компонента, не образующего малорастворимого соединения, между исходной жидкой и образующейся твердой фазой. Из основных областей применения осаждения как метода разделения в аналитической химии наряду с гравиметрией уже отмечалось препаративное выделение из раствора целевых компонентов в форме соединений определенного состава после их разделения другими методами. Реже осаждение применяется для концентрирования целевых компонентов по отношению к матрице и матричным компонентам. В первом случае с целью более высокой степени очистки выделяемых соединений от примесей нередко прибегают к переосаждению – повторению операций осаждения и растворения данного соединения.
Осаждение На практике, даже в том случае, когда одно из разделяемых веществ не образует осадка, коэффициент разделения, как правило, не превышает 103. В первую очередь это обусловлено соосаждением, то есть распределением компонента, не образующего малорастворимого соединения, между исходной жидкой и образующейся твердой фазой. Из основных областей применения осаждения как метода разделения в аналитической химии наряду с гравиметрией уже отмечалось препаративное выделение из раствора целевых компонентов в форме соединений определенного состава после их разделения другими методами. Реже осаждение применяется для концентрирования целевых компонентов по отношению к матрице и матричным компонентам. В первом случае с целью более высокой степени очистки выделяемых соединений от примесей нередко прибегают к переосаждению – повторению операций осаждения и растворения данного соединения.
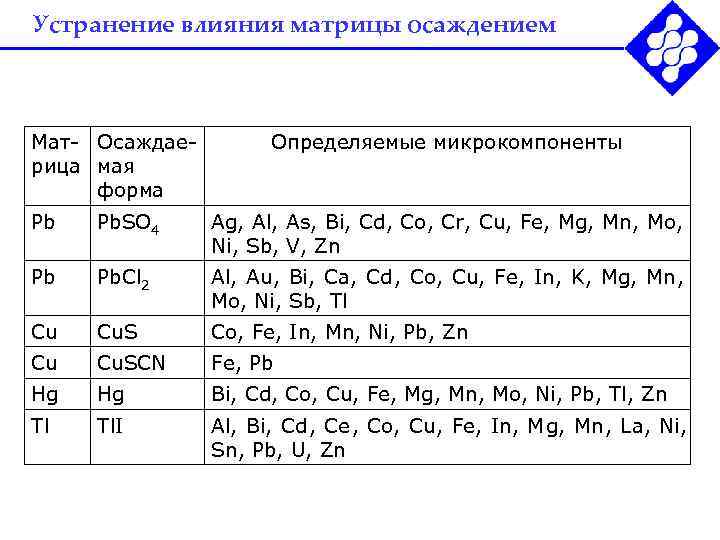
 Устранение влияния матрицы осаждением Мат- Осаждае- Определяемые микрокомпоненты рица мая форма Pb Pb. SO 4 Ag, Al, As, Bi, Cd, Co, Cr, Cu, Fe, Mg, Mn, Mo, Ni, Sb, V, Zn Pb Pb. Cl 2 Al, Au, Bi, Ca, Cd, Co, Cu, Fe, In, K, Mg, Mn, Mo, Ni, Sb, Tl Cu Cu. S Co, Fe, In, Mn, Ni, Pb, Zn Cu Cu. SCN Fe, Pb Hg Bi, Cd, Co, Cu, Fe, Mg, Mn, Mo, Ni, Pb, Tl, Zn Tl Tl. I Al, Bi, Cd, Ce, Co, Cu, Fe, In, Мg, Mn, La, Ni, Sn, Pb, U, Zn
Устранение влияния матрицы осаждением Мат- Осаждае- Определяемые микрокомпоненты рица мая форма Pb Pb. SO 4 Ag, Al, As, Bi, Cd, Co, Cr, Cu, Fe, Mg, Mn, Mo, Ni, Sb, V, Zn Pb Pb. Cl 2 Al, Au, Bi, Ca, Cd, Co, Cu, Fe, In, K, Mg, Mn, Mo, Ni, Sb, Tl Cu Cu. S Co, Fe, In, Mn, Ni, Pb, Zn Cu Cu. SCN Fe, Pb Hg Bi, Cd, Co, Cu, Fe, Mg, Mn, Mo, Ni, Pb, Tl, Zn Tl Tl. I Al, Bi, Cd, Ce, Co, Cu, Fe, In, Мg, Mn, La, Ni, Sn, Pb, U, Zn
 Электроосаждение В целом, осаждение – универсальный, широко доступный метод разделения преимущественно неорганических веществ. Основными недостатками этого метода являются большая трудоемкость и длительность экспериментальных процедур, а также ограниченность диапазона концентраций разделяемых веществ областью относительно высоких значений, которые должны обеспечивать достижение произведения растворимости. Электроосаждение – это процесс образования твердой фазы в результате электрохимических процессов на электродах. При этом электроосаждение возможно по двум различным схемам: в результате восстановления ионов металлов на катоде до элементарного состояния и в результате химических реакций в растворе с участием в качестве реагента - осадителя ионов, образовавшихся в результате электрохимических превращений в приэлектродном пространстве.
Электроосаждение В целом, осаждение – универсальный, широко доступный метод разделения преимущественно неорганических веществ. Основными недостатками этого метода являются большая трудоемкость и длительность экспериментальных процедур, а также ограниченность диапазона концентраций разделяемых веществ областью относительно высоких значений, которые должны обеспечивать достижение произведения растворимости. Электроосаждение – это процесс образования твердой фазы в результате электрохимических процессов на электродах. При этом электроосаждение возможно по двум различным схемам: в результате восстановления ионов металлов на катоде до элементарного состояния и в результате химических реакций в растворе с участием в качестве реагента - осадителя ионов, образовавшихся в результате электрохимических превращений в приэлектродном пространстве.
 Отгонка из раствора. Классическая схема отгонки основана на образовании летучих соединений в результате химических реакций в растворах. Наиболее частый случай аналитического применения: Ge. Cl 4, Si. F 4, BF 3 - вскрытие проб с одновременным отделением матрицы при анализе полупроводниковых материалов. Отгонка из твердой фазы в парах реагента. Определение C и S в сталях после прокаливания порошка или стружки в токе О 2 по содержанию в газовой фазе СО 2 и SO 2. Специфика этого метода - гетерогенные реакции, скорость которых зависит от поверхности межфазного контакта. Поэтому анализируемые образцы готовят в форме порошков, стружки или тонких пленок.
Отгонка из раствора. Классическая схема отгонки основана на образовании летучих соединений в результате химических реакций в растворах. Наиболее частый случай аналитического применения: Ge. Cl 4, Si. F 4, BF 3 - вскрытие проб с одновременным отделением матрицы при анализе полупроводниковых материалов. Отгонка из твердой фазы в парах реагента. Определение C и S в сталях после прокаливания порошка или стружки в токе О 2 по содержанию в газовой фазе СО 2 и SO 2. Специфика этого метода - гетерогенные реакции, скорость которых зависит от поверхности межфазного контакта. Поэтому анализируемые образцы готовят в форме порошков, стружки или тонких пленок.
 Упаривание Под упариванием понимается процесс частичного или полного удаления летучей матрицы из раствора за счет парообразования, которое может быть инициировано нагреванием (не обязательно до точки кипения) или понижением давления. Обычно такой матрицей является вода, а упаривание приводит к концентрированию нелетучих веществ, присутствующих в водных растворах. Если пренебречь потерей нелетучих веществ, которые практически незначимы при соблюдении специальных правил, достигаемый при выпаривании коэффициент концентрирования Кконц равен: Кконц = V 0/Vконц где V 0 и Vконц – объем раствора до и после упаривания, соответственно. При упаривании досуха величина Кконц стремится к бесконечности.
Упаривание Под упариванием понимается процесс частичного или полного удаления летучей матрицы из раствора за счет парообразования, которое может быть инициировано нагреванием (не обязательно до точки кипения) или понижением давления. Обычно такой матрицей является вода, а упаривание приводит к концентрированию нелетучих веществ, присутствующих в водных растворах. Если пренебречь потерей нелетучих веществ, которые практически незначимы при соблюдении специальных правил, достигаемый при выпаривании коэффициент концентрирования Кконц равен: Кконц = V 0/Vконц где V 0 и Vконц – объем раствора до и после упаривания, соответственно. При упаривании досуха величина Кконц стремится к бесконечности.
 Упаривание Наряду с концентрированием к упариванию нередко прибегают для того, чтобы перевести определяемые вещества из одной матрицы в другую, более удобную для анализа. Например, при определении металлов после их экстракционного выделения из водной в органическую фазу экстракт упаривают досуха, а сухой остаток снова переводят в водный раствор необходимого состава. При кажущейся простоте упаривание имеет свои методические проблемы. Для того, чтобы избежать потерь даже практически нелетучих веществ, необходимо считаться с возможностью их капельного уноса, особенно при кипячении. Поэтому упаривание, как правило, проводят при температурах ниже точки кипения раствора и добиваются его равномерного нагрева, используя, например, песчаную баню, или проводят поверхностный нагрев с помощью инфракрасной лампы.
Упаривание Наряду с концентрированием к упариванию нередко прибегают для того, чтобы перевести определяемые вещества из одной матрицы в другую, более удобную для анализа. Например, при определении металлов после их экстракционного выделения из водной в органическую фазу экстракт упаривают досуха, а сухой остаток снова переводят в водный раствор необходимого состава. При кажущейся простоте упаривание имеет свои методические проблемы. Для того, чтобы избежать потерь даже практически нелетучих веществ, необходимо считаться с возможностью их капельного уноса, особенно при кипячении. Поэтому упаривание, как правило, проводят при температурах ниже точки кипения раствора и добиваются его равномерного нагрева, используя, например, песчаную баню, или проводят поверхностный нагрев с помощью инфракрасной лампы.
 Дистилляция и ректификация Дистилляция – двухстадийный процесс, включающий фазовые переходы из жидкого состояния в газообразное и наоборот. . Ректификация - многократное повторение элементарных актов испарения-конденсации в специальных ректификационных колонках. Возможность разделения дистилляционными методами следует из закона Рауля: РА= РАо. ХА, соответственно где РА и РВ - парциальные давления А и В над раствором, ХА и ХВ - мольные доли А и В в р-ре, РАо. РВо - давления насыщенного пара при данной температуре. =Раo/Рвo, где - коэффициент относительной летучести жидкостей. Отличия относительно невелики. Поэтому дистилляция не обеспечивают высокие Kp.
Дистилляция и ректификация Дистилляция – двухстадийный процесс, включающий фазовые переходы из жидкого состояния в газообразное и наоборот. . Ректификация - многократное повторение элементарных актов испарения-конденсации в специальных ректификационных колонках. Возможность разделения дистилляционными методами следует из закона Рауля: РА= РАо. ХА, соответственно где РА и РВ - парциальные давления А и В над раствором, ХА и ХВ - мольные доли А и В в р-ре, РАо. РВо - давления насыщенного пара при данной температуре. =Раo/Рвo, где - коэффициент относительной летучести жидкостей. Отличия относительно невелики. Поэтому дистилляция не обеспечивают высокие Kp.
 Дистилляция и ректификация Под термином ректификация подразумевается метод и процесс дистилляции с многократным повторением фазовых переходов испарение – конденсация. При нагревании жидкости в перегонной колбе образующийся пар проходит через ректификационную колонку и конденсируется в конденсаторах-холодильниках. В отличие от одноступенчатой дистилляции часть сконденсированного пара возвращается в ректификационную колонку и стекает сверху вниз в перегонную колбу навстречу потоку восходящего пара. Конденсат пара, который возвращается в колонку, называется флегмой. Отношение количества флегмы к количеству дистиллята, отбираемого в приемник , называется флегмовым числом Ф. Применение - препаративное получение органических растворителей.
Дистилляция и ректификация Под термином ректификация подразумевается метод и процесс дистилляции с многократным повторением фазовых переходов испарение – конденсация. При нагревании жидкости в перегонной колбе образующийся пар проходит через ректификационную колонку и конденсируется в конденсаторах-холодильниках. В отличие от одноступенчатой дистилляции часть сконденсированного пара возвращается в ректификационную колонку и стекает сверху вниз в перегонную колбу навстречу потоку восходящего пара. Конденсат пара, который возвращается в колонку, называется флегмой. Отношение количества флегмы к количеству дистиллята, отбираемого в приемник , называется флегмовым числом Ф. Применение - препаративное получение органических растворителей.
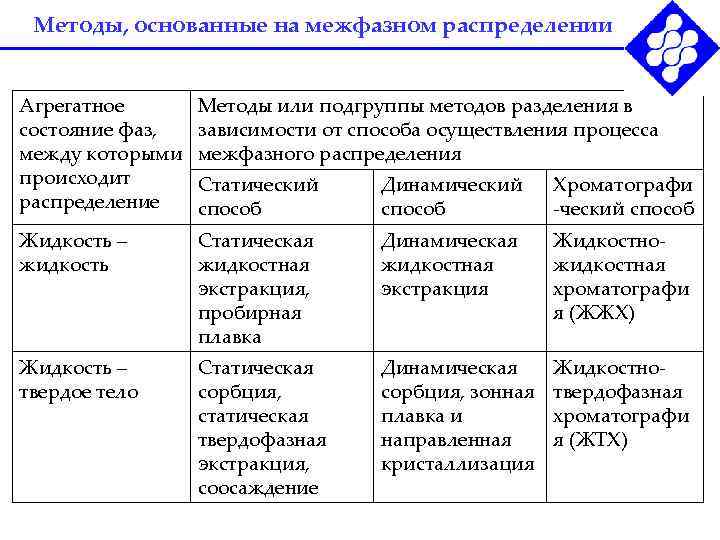
 Методы, основанные на межфазном распределении Агрегатное Методы или подгруппы методов разделения в состояние фаз, зависимости от способа осуществления процесса между которыми межфазного распределения происходит Статический Динамический Хроматографи распределение способ -ческий способ Жидкость – Статическая Динамическая Жидкостно- жидкость жидкостная экстракция, экстракция хроматографи пробирная я (ЖЖХ) плавка Жидкость – Статическая Динамическая Жидкостно- твердое тело сорбция, зонная твердофазная статическая плавка и хроматографи твердофазная направленная я (ЖТХ) экстракция, кристаллизация соосаждение
Методы, основанные на межфазном распределении Агрегатное Методы или подгруппы методов разделения в состояние фаз, зависимости от способа осуществления процесса между которыми межфазного распределения происходит Статический Динамический Хроматографи распределение способ -ческий способ Жидкость – Статическая Динамическая Жидкостно- жидкость жидкостная экстракция, экстракция хроматографи пробирная я (ЖЖХ) плавка Жидкость – Статическая Динамическая Жидкостно- твердое тело сорбция, зонная твердофазная статическая плавка и хроматографи твердофазная направленная я (ЖТХ) экстракция, кристаллизация соосаждение
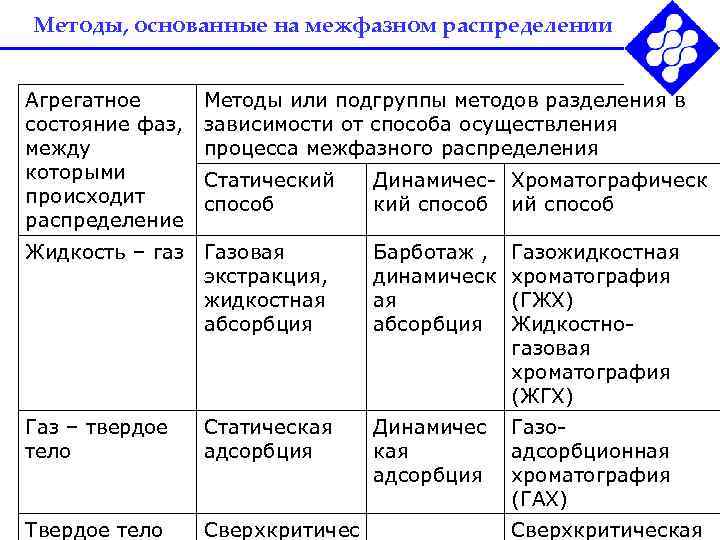
 Методы, основанные на межфазном распределении Агрегатное Методы или подгруппы методов разделения в состояние фаз, зависимости от способа осуществления между процесса межфазного распределения которыми Статический Динамичес- Хроматографическ происходит способ кий способ распределение Жидкость – газ Газовая Барботаж , Газожидкостная экстракция, динамическ хроматография жидкостная (ГЖХ) абсорбция Жидкостно- газовая хроматография (ЖГХ) Газ – твердое Статическая Динамичес Газо- тело адсорбция кая адсорбционная адсорбция хроматография (ГАХ) Твердое тело Сверхкритичес Сверхкритическая
Методы, основанные на межфазном распределении Агрегатное Методы или подгруппы методов разделения в состояние фаз, зависимости от способа осуществления между процесса межфазного распределения которыми Статический Динамичес- Хроматографическ происходит способ кий способ распределение Жидкость – газ Газовая Барботаж , Газожидкостная экстракция, динамическ хроматография жидкостная (ГЖХ) абсорбция Жидкостно- газовая хроматография (ЖГХ) Газ – твердое Статическая Динамичес Газо- тело адсорбция кая адсорбционная адсорбция хроматография (ГАХ) Твердое тело Сверхкритичес Сверхкритическая
 Характеристики методов Основной характеристикой группы методов является коэффициент межфазного распределения KD = (Ci)”/(Ci)’, где Ci - равновесные концентрации i-го вещества в ‘- отдающей и ”- извлекающей фазах. Понятие селективности относительное: Кс = KDi/KDj, т. е. утверждение: селективный сорбент - не строгое, всегда сорбент селективен к i-компоненту по отношению к j-компоненту и т. п. Связь Кр и Кс, Kр-коэффициент разделения веществ. Для методов, основанных на однократном межфазном распределении Кр Кс, для многоступенчатых процессов Кр (Кс)n, где n - число последовательных циклов межфазного распределения.
Характеристики методов Основной характеристикой группы методов является коэффициент межфазного распределения KD = (Ci)”/(Ci)’, где Ci - равновесные концентрации i-го вещества в ‘- отдающей и ”- извлекающей фазах. Понятие селективности относительное: Кс = KDi/KDj, т. е. утверждение: селективный сорбент - не строгое, всегда сорбент селективен к i-компоненту по отношению к j-компоненту и т. п. Связь Кр и Кс, Kр-коэффициент разделения веществ. Для методов, основанных на однократном межфазном распределении Кр Кс, для многоступенчатых процессов Кр (Кс)n, где n - число последовательных циклов межфазного распределения.
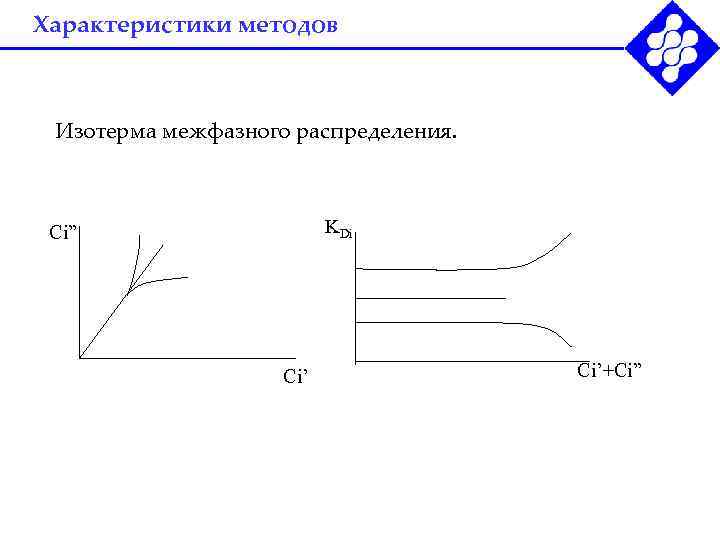
 Характеристики методов Изотерма межфазного распределения. Сi” KDi Ci’+Ci”
Характеристики методов Изотерма межфазного распределения. Сi” KDi Ci’+Ci”
 Сорбционные методы Извлечение из жидкой фазы в твердую - сорбция. Понятие сорбция - собирательное, употребляется, когда механизм извлечения из жидкой или газовой фазы в твердую или неизвестен или несущественен. СОРБЕНТ - извлекающая фаза, СОРБАТ - извлекаемое вещество. Если извлечение происходит за счет связывания сорбата поверхностью - адсорбция, если объемное - абсорбция.
Сорбционные методы Извлечение из жидкой фазы в твердую - сорбция. Понятие сорбция - собирательное, употребляется, когда механизм извлечения из жидкой или газовой фазы в твердую или неизвестен или несущественен. СОРБЕНТ - извлекающая фаза, СОРБАТ - извлекаемое вещество. Если извлечение происходит за счет связывания сорбата поверхностью - адсорбция, если объемное - абсорбция.
 Сорбционные методы. Механизмы. 1. Слабые межмолекулярные взаимодействия, определяемые силами Ван-дер-Ваальса. Обычно проявляются при адсорбции молекул из газовой или неполярных жидких фаз. Прочность удерживания определяется площадью поверхности сорбента. Адсорбенты характеризуются удельной поверхностью м 2/г и природой (полярностью) функциональных групп на поверхности. Примеры: угли; силикагели; цеолиты, органические полимеры. 2. Ионный обмен: (гетерогенная обменная реакция). 2(M-SO 3 Na)тв. ф. +(Са 2+)р-р = (M(SO 3)2 Ca)тв. ф. + 2(Na+)р-р, где М – полимерная матрица (М NOH)тв. ф. +(Cl-)р-р = (N NCl)тв. ф. + (ОН-)р-р 3. Донорно-акцепторное взаимодействие сорбата с функциональными группами сорбента: M-NH 2 + Pt[Cl 4]2 - = Pt[(M- NH 2)2 Cl 2] + 2 Cl- Случаи 2 и 3 относятся к сорбции из полярных жидких фаз.
Сорбционные методы. Механизмы. 1. Слабые межмолекулярные взаимодействия, определяемые силами Ван-дер-Ваальса. Обычно проявляются при адсорбции молекул из газовой или неполярных жидких фаз. Прочность удерживания определяется площадью поверхности сорбента. Адсорбенты характеризуются удельной поверхностью м 2/г и природой (полярностью) функциональных групп на поверхности. Примеры: угли; силикагели; цеолиты, органические полимеры. 2. Ионный обмен: (гетерогенная обменная реакция). 2(M-SO 3 Na)тв. ф. +(Са 2+)р-р = (M(SO 3)2 Ca)тв. ф. + 2(Na+)р-р, где М – полимерная матрица (М NOH)тв. ф. +(Cl-)р-р = (N NCl)тв. ф. + (ОН-)р-р 3. Донорно-акцепторное взаимодействие сорбата с функциональными группами сорбента: M-NH 2 + Pt[Cl 4]2 - = Pt[(M- NH 2)2 Cl 2] + 2 Cl- Случаи 2 и 3 относятся к сорбции из полярных жидких фаз.
 Сорбционные методы. Применения. Области аналитического применения: 1. Адсорбция применяется в ГАХ и ЖАХ и в технологических целях. 2. Ионный обмен - все начиналось с открытия механизма засоления почв за счет природных неорганических ионитов. Органические иониты - ионообменные смолы. Матрица - сополимер стирол + дивинилбензол. Функциональные группы определяют свойства, а форма ионита определяется ионами, компенсирующими заряд функциональной группы: сильнокислотные катиониты - SO 3 H слабокислотные «-» - СООН Н+-формы средней силы «-» - Р(О)(ОН)2 сильноосновные аниониты - N+ OH- или Cl-, OH- или Cl-- формы слабоосновные аниониты - -NH 2 =NH средней силы - N
Сорбционные методы. Применения. Области аналитического применения: 1. Адсорбция применяется в ГАХ и ЖАХ и в технологических целях. 2. Ионный обмен - все начиналось с открытия механизма засоления почв за счет природных неорганических ионитов. Органические иониты - ионообменные смолы. Матрица - сополимер стирол + дивинилбензол. Функциональные группы определяют свойства, а форма ионита определяется ионами, компенсирующими заряд функциональной группы: сильнокислотные катиониты - SO 3 H слабокислотные «-» - СООН Н+-формы средней силы «-» - Р(О)(ОН)2 сильноосновные аниониты - N+ OH- или Cl-, OH- или Cl-- формы слабоосновные аниониты - -NH 2 =NH средней силы - N
 Характеристики сорбентов Основные характеристики: Степень сшивки: % дивинилбензола - х. N (от 2 до 24)(КУ-2 х6, Dowex-50 x 8) Обменная емкость: полная (ПОЕ) и динамическая (ДОЕ) - количество вещества в молях, поглощаемое 1 кг сорбента. ПОЕ - строго соответствует концентрации функциональных групп на единицу массы ионообменной смолы. Сложнее ДОЕ – это условная характеристика. ДОЕ = Ciнач. Vпр/mi, определяется при фиксированных диаметре - d и высоте - l слоя сорбента, скорости фильтрации раствора и (Ciпр/Ciнач). 100%, где Ciпр - концентрация i-ионов в растворе на выходе из колонки, Ciнач - начальная концентрация, Vпр - объем до проскока, соответствующий заданному соотношению Ciпр/Ciнач
Характеристики сорбентов Основные характеристики: Степень сшивки: % дивинилбензола - х. N (от 2 до 24)(КУ-2 х6, Dowex-50 x 8) Обменная емкость: полная (ПОЕ) и динамическая (ДОЕ) - количество вещества в молях, поглощаемое 1 кг сорбента. ПОЕ - строго соответствует концентрации функциональных групп на единицу массы ионообменной смолы. Сложнее ДОЕ – это условная характеристика. ДОЕ = Ciнач. Vпр/mi, определяется при фиксированных диаметре - d и высоте - l слоя сорбента, скорости фильтрации раствора и (Ciпр/Ciнач). 100%, где Ciпр - концентрация i-ионов в растворе на выходе из колонки, Ciнач - начальная концентрация, Vпр - объем до проскока, соответствующий заданному соотношению Ciпр/Ciнач
 Характеристики сорбентов ДОЕ характеризует не только емкость, но и кинетику межфазного обмена, последняя зависит от размера частиц и жесткости сшивки полимера - х. Прочность сорбции определяется размерами ионов. Для сильнокислотных катионитов выполняется зависимость Cs+>Rb+>K+>Na+>Li+ Кс=KDCs/KDNa =1, 7 Для сильноосновных анионитов выполняется зависимость Cl. O 4 - >NO 3 ->Br->Cl->F- В зависимости от х порядок может нарушаться.
Характеристики сорбентов ДОЕ характеризует не только емкость, но и кинетику межфазного обмена, последняя зависит от размера частиц и жесткости сшивки полимера - х. Прочность сорбции определяется размерами ионов. Для сильнокислотных катионитов выполняется зависимость Cs+>Rb+>K+>Na+>Li+ Кс=KDCs/KDNa =1, 7 Для сильноосновных анионитов выполняется зависимость Cl. O 4 - >NO 3 ->Br->Cl->F- В зависимости от х порядок может нарушаться.
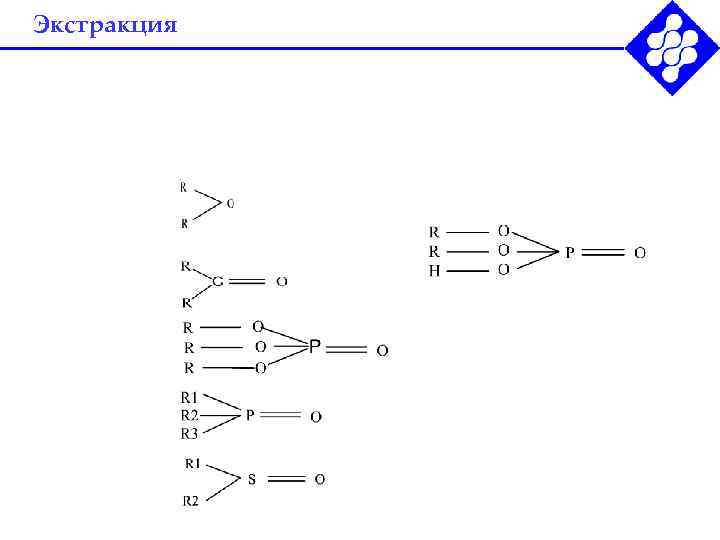
 Экстракция 1. Физическое распределение - переход из отдающей водной фазы в органический экстрагент без изменения химической формы за счет Есольв > Егидр Характерен для больших неполярных молекул Ge. Cl 4, Os. O 4, I 2, органические соединения. 2. Реакционная экстракция. х. Аводн + у. Ворг = [Ах. Ву]орг Гетерогенная реакция, характеризуемая константой Кэкс [Ах. Ву]орг Кэкс= ---------- [A]x водн[B]уорг Поскольку при экстракции редко образуются соединения определенного состава, универсальной характеристикой процесса экстракции остается КD.
Экстракция 1. Физическое распределение - переход из отдающей водной фазы в органический экстрагент без изменения химической формы за счет Есольв > Егидр Характерен для больших неполярных молекул Ge. Cl 4, Os. O 4, I 2, органические соединения. 2. Реакционная экстракция. х. Аводн + у. Ворг = [Ах. Ву]орг Гетерогенная реакция, характеризуемая константой Кэкс [Ах. Ву]орг Кэкс= ---------- [A]x водн[B]уорг Поскольку при экстракции редко образуются соединения определенного состава, универсальной характеристикой процесса экстракции остается КD.
 Экстракция
Экстракция
 Экстракция Для кислотных экстрагентов основной механизм экстракции - ионный обмен - замещение протона на ионы металлов. Для основных механизм экстракции – гидратосольватный - образование гидратосольватов протонов и ассоциатов последних с ацидокомплексами металлов: (H+ + m. H 2 O + X-)водн + n(R=O)орг {[H(H 2 O)m(R=O)n]+X-}орг Переход экстрагируемого соединения [MXq]-(q-z) в органическую фазу можно рассматривать как реакцию ионного обмена: (q-z){[H(H 2 O)m(R=O)n]+X-}орг + {[MXq]-(q-z)}водн {[H(H 2 O)m(R=O)n]+(q-z)[MXq]-(q-z)}орг + (q-z)(X-)водн
Экстракция Для кислотных экстрагентов основной механизм экстракции - ионный обмен - замещение протона на ионы металлов. Для основных механизм экстракции – гидратосольватный - образование гидратосольватов протонов и ассоциатов последних с ацидокомплексами металлов: (H+ + m. H 2 O + X-)водн + n(R=O)орг {[H(H 2 O)m(R=O)n]+X-}орг Переход экстрагируемого соединения [MXq]-(q-z) в органическую фазу можно рассматривать как реакцию ионного обмена: (q-z){[H(H 2 O)m(R=O)n]+X-}орг + {[MXq]-(q-z)}водн {[H(H 2 O)m(R=O)n]+(q-z)[MXq]-(q-z)}орг + (q-z)(X-)водн
 Экстракция При экстракции по гидратно-сольватному механизму существенную роль играет форма существования экстрагируемого вещества в водном растворе. Экстрагируемость ацидокомплексов определяется их прочностью и различиями энергий их гидратации и гидратации ацидолиганда или других анионов, присутствующих в водном растворе. Экстрагируемость будет тем выше, чем меньше заряд и чем больше размеры ацидокомплекса, т. е. чем меньше он гидратирован. Характерные формы соединений, хорошо экстрагируемых кислородсодержащими экстрагентами: [MX 4]- и [MX 6]- , где Х – галогенид-ион. Среди наиболее широко известных соединений – это [Fe. Cl 4]-, [Au. Cl 4]-, [Sb. Cl 6]-. Главные достоинства кислородсожержащих экстрагентов - обратимость экстракции и высокая селективность экстракции ацидокомплексов по отношению к металлам, не образующим подобных соединений
Экстракция При экстракции по гидратно-сольватному механизму существенную роль играет форма существования экстрагируемого вещества в водном растворе. Экстрагируемость ацидокомплексов определяется их прочностью и различиями энергий их гидратации и гидратации ацидолиганда или других анионов, присутствующих в водном растворе. Экстрагируемость будет тем выше, чем меньше заряд и чем больше размеры ацидокомплекса, т. е. чем меньше он гидратирован. Характерные формы соединений, хорошо экстрагируемых кислородсодержащими экстрагентами: [MX 4]- и [MX 6]- , где Х – галогенид-ион. Среди наиболее широко известных соединений – это [Fe. Cl 4]-, [Au. Cl 4]-, [Sb. Cl 6]-. Главные достоинства кислородсожержащих экстрагентов - обратимость экстракции и высокая селективность экстракции ацидокомплексов по отношению к металлам, не образующим подобных соединений
 Экстракция АЗОТСОДЕРЖАЩИЕ экстрагенты: амины и четвертичные аммониевые основания R-NH 2, R 2 NH, R 3 N, R 4 N+X-. В самом общем случае реализуется координационный механизм экстракции: [Me. Xn]-(n-Z) +m. RNH 2 = [Me(RNH 2)m. Xn-m]-(n-m-Z) + m. X- В случае R 4 N+X механизм экстракции - ионный обмен X- на Y- или на [Me. Xn]-(n-Z) В случае третичных аминов в сильнокислых растворах проходит реакция присоединения H+ + X- +(R 3 N)орг = [R 3 NH+X-]орг, а далее ионный обмен X- на Y- или ацидокомплекс. Достоинство - высокие KD по отношению к ацидокомплексам и во всех случаях при экстракции по механизму образования координационных соединений. СЕРОСОДЕРЖАЩИЕ экстрагенты: аналоги кислородсодержащих. Различия в механизме – возможно только образование координационных соединений: m. R 2 S + [Me. Xn]-(n-Z)вод = [Me(R 2 S)m. Xn-m]-(n-m-Z) + m. X- Применение - только концентрирование.
Экстракция АЗОТСОДЕРЖАЩИЕ экстрагенты: амины и четвертичные аммониевые основания R-NH 2, R 2 NH, R 3 N, R 4 N+X-. В самом общем случае реализуется координационный механизм экстракции: [Me. Xn]-(n-Z) +m. RNH 2 = [Me(RNH 2)m. Xn-m]-(n-m-Z) + m. X- В случае R 4 N+X механизм экстракции - ионный обмен X- на Y- или на [Me. Xn]-(n-Z) В случае третичных аминов в сильнокислых растворах проходит реакция присоединения H+ + X- +(R 3 N)орг = [R 3 NH+X-]орг, а далее ионный обмен X- на Y- или ацидокомплекс. Достоинство - высокие KD по отношению к ацидокомплексам и во всех случаях при экстракции по механизму образования координационных соединений. СЕРОСОДЕРЖАЩИЕ экстрагенты: аналоги кислородсодержащих. Различия в механизме – возможно только образование координационных соединений: m. R 2 S + [Me. Xn]-(n-Z)вод = [Me(R 2 S)m. Xn-m]-(n-m-Z) + m. X- Применение - только концентрирование.
 Экстракция ХЕЛАТООБРАЗУЮЩИЕ экстрагенты: имеют одновременно два донорных атома, участвующих в образовании химической связи с экстрагируемым ионом. Классический пример: диметилглиоксим СН 3 -С--С-СН 3 || || N N | | HO OH Достоинства - высокая селективность экстракции ионов, способных образовывать хелаты. Недостаток - необратимость экстракции исключает применение в препаративных целях. Область применения – образование окрашенных соединений в органической фазе: экстракционные фотометрия, спектрофотометрия и флюориметрия, где необратимость процесса становится достоинством, так как определение производится непосредственно в органической фазе.
Экстракция ХЕЛАТООБРАЗУЮЩИЕ экстрагенты: имеют одновременно два донорных атома, участвующих в образовании химической связи с экстрагируемым ионом. Классический пример: диметилглиоксим СН 3 -С--С-СН 3 || || N N | | HO OH Достоинства - высокая селективность экстракции ионов, способных образовывать хелаты. Недостаток - необратимость экстракции исключает применение в препаративных целях. Область применения – образование окрашенных соединений в органической фазе: экстракционные фотометрия, спектрофотометрия и флюориметрия, где необратимость процесса становится достоинством, так как определение производится непосредственно в органической фазе.
 Экстракция Макроциклические экстрагенты: как и хелато- образующие, объединяются в единую группу по принципу структурного подобия их молекул. Отправной точкой появления макроциклических экстрагентов явилось открытие в 60 -х годах 20 -го века гетероцепных соединений, представляющих собой макроциклы из нескольких чередующихся эфирных фрагментов, пространственное строение которых напоминало корону. Откуда и появилось общее название этого класса соединений – краун-эфиры. Если в молекуле макроцикла один или несколько атомов кислорода замещены на атомы азота, соответствующие соединения называют азо-краун-эфирами. Трехмерные аминоэфиры получили название криптандов.
Экстракция Макроциклические экстрагенты: как и хелато- образующие, объединяются в единую группу по принципу структурного подобия их молекул. Отправной точкой появления макроциклических экстрагентов явилось открытие в 60 -х годах 20 -го века гетероцепных соединений, представляющих собой макроциклы из нескольких чередующихся эфирных фрагментов, пространственное строение которых напоминало корону. Откуда и появилось общее название этого класса соединений – краун-эфиры. Если в молекуле макроцикла один или несколько атомов кислорода замещены на атомы азота, соответствующие соединения называют азо-краун-эфирами. Трехмерные аминоэфиры получили название криптандов.
 Экстракция Первоначальный интерес к экстракции неорганических веществ не дал существенных результатов. В настоящее время найдены условия селективной экстракции органических веществ. При экстракции краун-эфирами существенен стерический фактор - соответствие размеров ионов или молекул выделяемых веществ размерам полости в макроциклических молекулах.
Экстракция Первоначальный интерес к экстракции неорганических веществ не дал существенных результатов. В настоящее время найдены условия селективной экстракции органических веществ. При экстракции краун-эфирами существенен стерический фактор - соответствие размеров ионов или молекул выделяемых веществ размерам полости в макроциклических молекулах.
 Экстракция в расплавы металлов Реакционная экстракция в расплавы металлов – пробирная плавка. Метод пробирной плавки является специфическим методом концентрирования благородных металлов, основанный на их выделении в расплавы металлов, чаще всего в свинец, медь или серебро. Пробирная плавка является комплексным методом пробоподготовки, объединяющим стадии разложения пробы и концентрирования микроэлементов. Общая схема пробирной плавки: навеска пробы + шихта (коллектор + флюсы+ восстановители или окислители). Коллектор - обычно глет (Pb. O). Флюсы - бура, сода, поташ. Восстановители - уголь, мука, крахмал, сера и т. п. Окислители - Pb 3 O 4, KNO 3 и. т. п.
Экстракция в расплавы металлов Реакционная экстракция в расплавы металлов – пробирная плавка. Метод пробирной плавки является специфическим методом концентрирования благородных металлов, основанный на их выделении в расплавы металлов, чаще всего в свинец, медь или серебро. Пробирная плавка является комплексным методом пробоподготовки, объединяющим стадии разложения пробы и концентрирования микроэлементов. Общая схема пробирной плавки: навеска пробы + шихта (коллектор + флюсы+ восстановители или окислители). Коллектор - обычно глет (Pb. O). Флюсы - бура, сода, поташ. Восстановители - уголь, мука, крахмал, сера и т. п. Окислители - Pb 3 O 4, KNO 3 и. т. п.
 Разновидности экстракции Твердофазная экстракция – синоним сорбции по механизму слабых межмолекулярных взаимодействий. Газовая экстракция - В наиболее общем случае в основе лежат законы физического распределения. Частный случай - реакционная газовая экстракция - метод выделения веществ, способных образовывать летучие соединения в результате химических превращений. Применение - парофазный анализ - основной метод определения летучих соединений, растворенных в воде.
Разновидности экстракции Твердофазная экстракция – синоним сорбции по механизму слабых межмолекулярных взаимодействий. Газовая экстракция - В наиболее общем случае в основе лежат законы физического распределения. Частный случай - реакционная газовая экстракция - метод выделения веществ, способных образовывать летучие соединения в результате химических превращений. Применение - парофазный анализ - основной метод определения летучих соединений, растворенных в воде.
 Разновидности экстракции Сверхкритическая флюидная экстракция (СКФЭ) - метод, в котором в качестве экстрагента, т. е. извлекающей фазы, используются вещества в состоянии сверхкритического флюида (СФ), т. е. в агрегатном состоянии, соответствующем условиям, когда температура и давление превышают критические значения для данного вещества. Из применяемых в СКФЭ экстрагентов наиболее предпочтительным по своим свойства и доступности является СФ СО 2. Привлекательность СФ в качестве экстрагентов вызвана тем, что вещества в сверхкритическом состоянии по плотности и растворяющей способности приближаются к жидкостям и в то же время выделенные в СФ вещества легко освобождаются от экстрагента при изменении температуры и давления, что делает их привлекательными для решения препаративных задач. Извлекаемыми веществами чаще всего являются высокомолекулярные органические соединения.
Разновидности экстракции Сверхкритическая флюидная экстракция (СКФЭ) - метод, в котором в качестве экстрагента, т. е. извлекающей фазы, используются вещества в состоянии сверхкритического флюида (СФ), т. е. в агрегатном состоянии, соответствующем условиям, когда температура и давление превышают критические значения для данного вещества. Из применяемых в СКФЭ экстрагентов наиболее предпочтительным по своим свойства и доступности является СФ СО 2. Привлекательность СФ в качестве экстрагентов вызвана тем, что вещества в сверхкритическом состоянии по плотности и растворяющей способности приближаются к жидкостям и в то же время выделенные в СФ вещества легко освобождаются от экстрагента при изменении температуры и давления, что делает их привлекательными для решения препаративных задач. Извлекаемыми веществами чаще всего являются высокомолекулярные органические соединения.
 Пути развития Методы, основанные на однократном равновесном распределении, всегда ограничены по Кр. Разделение достигается только для заметно отличающихся по свойствам веществ. Прогресс в области этих методов - поиск «селективных» к выделяемым веществам по отношению к сопутствующим примесям извлекающих фаз - сорбентов и экстрагентов. Возможности во многом исчерпаны и интерес смещается в сторону процессов, обеспечивающих многократное последовательное перераспределение, где Кр ---> Ксn: Многоступенчатая экстракция, динамическая сорбция, барботаж. Важнейшими среди методов, основанных на многократном повторении актов межфазного распределения являются хроматографические методы.
Пути развития Методы, основанные на однократном равновесном распределении, всегда ограничены по Кр. Разделение достигается только для заметно отличающихся по свойствам веществ. Прогресс в области этих методов - поиск «селективных» к выделяемым веществам по отношению к сопутствующим примесям извлекающих фаз - сорбентов и экстрагентов. Возможности во многом исчерпаны и интерес смещается в сторону процессов, обеспечивающих многократное последовательное перераспределение, где Кр ---> Ксn: Многоступенчатая экстракция, динамическая сорбция, барботаж. Важнейшими среди методов, основанных на многократном повторении актов межфазного распределения являются хроматографические методы.
 Спасибо за внимание! Алексей Леонидович Москвин moskvin-al@rosanalyt. ru
Спасибо за внимание! Алексей Леонидович Москвин moskvin-al@rosanalyt. ru

