обзор анальгетиков.ppt
- Количество слайдов: 70

Критический обзор современных препаратов для послеоперационного обезболивания
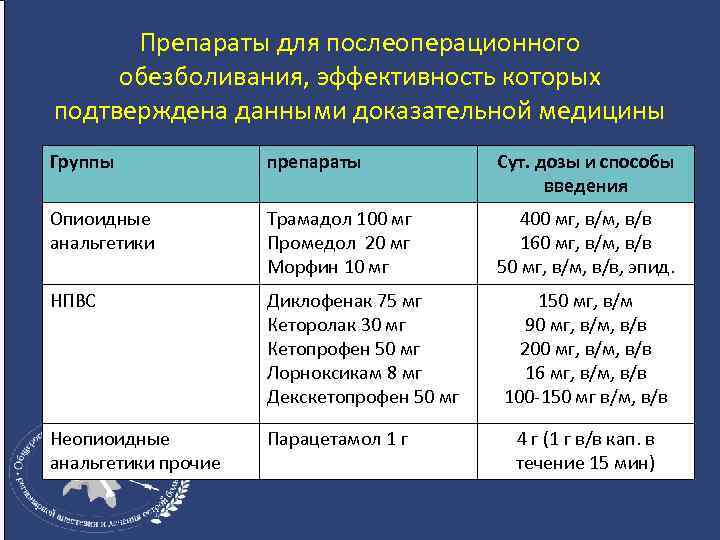
Препараты для послеоперационного обезболивания, эффективность которых подтверждена данными доказательной медицины Группы препараты Сут. дозы и способы введения Опиоидные анальгетики Трамадол 100 мг Промедол 20 мг Морфин 10 мг 400 мг, в/м, в/в 160 мг, в/м, в/в 50 мг, в/м, в/в, эпид. НПВС Диклофенак 75 мг Кеторолак 30 мг Кетопрофен 50 мг Лорноксикам 8 мг Декскетопрофен 50 мг Неопиоидные анальгетики прочие Парацетамол 1 г 150 мг, в/м 90 мг, в/м, в/в 200 мг, в/м, в/в 16 мг, в/м, в/в 100 -150 мг в/м, в/в 4 г (1 г в/в кап. в течение 15 мин)
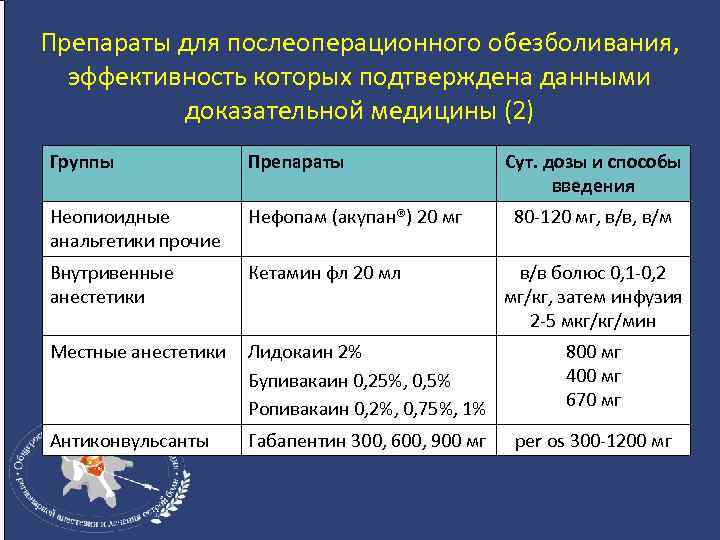
Препараты для послеоперационного обезболивания, эффективность которых подтверждена данными доказательной медицины (2) Группы Препараты Сут. дозы и способы введения Неопиоидные анальгетики прочие Нефопам (акупан®) 20 мг Внутривенные анестетики Кетамин фл 20 мл Местные анестетики Лидокаин 2% Бупивакаин 0, 25%, 0, 5% Ропивакаин 0, 2%, 0, 75%, 1% 800 мг 400 мг 670 мг Антиконвульсанты Габапентин 300, 600, 900 мг per os 300 -1200 мг 80 -120 мг, в/в, в/м в/в болюс 0, 1 -0, 2 мг/кг, затем инфузия 2 -5 мкг/кг/мин

Неопиоидные анальгетики и адьюванты: что у нас в арсенале? • • • НПВС Парацетамол Кетамин Нефопам Габапентин

НПВС

• 30 наиболее значимых инноваций в медицине за последние 30 лет по мнению 225 американских врачейэкспертов

30 наиболее значимых медицинских инноваций за последние 30 лет № событие рейтинг 1 Магнитно-резонансная и компьютерная томография 0, 878 3 Баллонная ангиопластика 0, 758 6 Операции аорто-коронарного шунтирования 0, 693 7 Ингибиторы протонной помпы 0, 687 10 Эндопротезирование крупных суставов 0, 649 14 Лапароскопическая хирургия 0, 558 15 НПВС и селективные ингибиторы ЦОГ-2 для послеоперационного обезболивания 0, 531 17 Фторхинолоны 0, 487 23 H. Pylori выявление и лечение 0, 351 26 Блокаторы кальциевых каналов 0, 291 30 Трансплантация костного мозга 0, 182

Нестероидные Противовоспалительные Препараты • «НПВС являются эффективными анальгетиками для лечения острой боли» (доказательства I-го уровня, Кокрановская база данных) • «Парацетамол, НПВС и ингибиторы ЦОГ-2 являются важнейшими компонентами мультимодальной анальгезии» (доказательства II-го уровня»

НПВС – препараты патогенетической терапии послеоперационной боли • ПГЕ 2 стимулируют синтез медиаторов боли (брадикинин, гистамин и др. ) и сенситизируют периферические ноцицепторы к их действию • • Концентрация ПГЕ 2 в тканях существенно возрастает по мере повышения интенсивности послеоперационного болевого синдрома (Gordon S et al. , 2002)

Механизмы действия НПВС Противовоспалительное действие: • Угнетение синтеза простагландинов: – ↓ вазодилятации Антипиретическое действие – опосредованный эффект • ↓ Снижение высвобождения эндогенных пирогенов из лейкоцитов - пирогены воздействуют на центр терморегуляции

Механизмы действия НПВС • За счет подавления воспалительного ответа на хирургическую травму НПВС препятствуют сенситизации (снижению порогов активации) периферических ноцицепторов • Таким образом, НПВС являются средствами патогенетической терапии острой боли

НПВС и гиперальгезия • Через 15 минут после в/в введения 30 мг кеторолака существенно снижается плазменная концентрация ПГЕ 2 • Через 30 минут достоверно повышаются сниженные пороги боли • Через 60 и 120 минут уменьшается площадь зоны вторичной гиперальгезии (Gordon S et al. // Clin. Pharmacol. Ther. ; 2002; V. 72; 175 -183, Stubhaug A et al. // Acta Anaesth. Scand. ; 2007; V. 51; 1138 -1146)

НПВС + парацетамол = эффективная комбинация • Сочетание НПВС с парацетамолом повышает эффективность обезболивания (доказательства I-го уровня, Кокрановская база данных)

Сфера применения НПВС – что нового Позитивное влияние на течение послеоперационного периода

· 22 контролируемых рандомизированных исследования, n = 2307 · Назначение НПВС снижает : ПОТР на 30% Глубину седации на 29% Не оказывает влияния на частоту кожного зуда, затруднения мочеиспускания, степень угнетения дыхания

• НПВС снижают проницаемость брюшины (особенно при возникновении хирургической инфекции) • НПВС оказывают положительное влияние на разрешение пареза кишечника, уменьшая отек и воспаление кишечной стенки, обусловленные системной воспалительной реакцией (выброс медиаторов воспаления – гистамин, простагландины и др. ) (Hollman M, Durieux M. // Anesthesiology. -2000. -V. 93)

Влияние НПВС на белковый метаболизм в раннем послеоперационном периоде l Простагландин Е 2 способствует белковому катаболизму, особенно на фоне лихорадки и сепсиса l НПВС снижают белковый катаболизм за счет подавления синтеза PGE 2 (Asoh T et al. // Ann. Surg. -1987. -V. 206. -P. 770 -7761, Barratt S, Smith R. // Reg Anesth Pain Med 2002; 27: 15 -22, Peng H. // Kidney Int. 2001; 59: 44 -51)

Влияние НПВС на белковый метаболизм в раннем послеоперационном периоде l Сочетание продленной ЭА и назначения НПВС позволяет снизить потери азота в первые 3 -е суток после операции на 80 -85% по сравнению с контрольной группой l Этот эффект более выражен, если НПВС введены до операции (Asoh T et al. // Ann. Surg. -1987. -V. 206. -P. 770 -7761, Barratt S, Smith R. // Reg Anesth Pain Med 2002; 27: 15 -22, Peng H. // Kidney Int. 2001; 59: 44 -51)

Периоперационное назначение НПВС достоверно снижает частоту фибрилляции предсердия после кардиоторакальных операций • Данные исследования AFIST (555 пациентов, возраст 67, 8± 8, 6) • Полученные результаты свидетельствуют о том, что воспаление является триггером послеоперационной фибрилляции предсердий (Ruffin R. , Kluger J. , Baker W. , Wills S. , . // Curr Med Res Opin. 2008 Apr; 24(4): 1131 -6)
Влияние кеторолака на частоту острой ишемии миокарда у больных некардиологического профиля • Рестроспективное когортное исследование у госпитализированных больных (35 клиник) • 10. 219 получали кеторолак – частота ОИМ – 0, 2%, 10. 145 получали опиоиды – частота ОИМ – 0, 4% • На основании мультивариантного анализа сделано заключение о кардиопротективных свойствах кеторолака (Kimmel S. , Berlin J. , Kinman J. // Pharmacoepidemiol. Drug. Saf. – 2002. – V. 11. – P. 113 -119)

• Болюс кеторолака 30 мг + в/в инфузия 5 мг/час в течение 24 часов • Длительность эпизодов ишемии миокарда была достоверно ниже на фоне инфузии кеторолака • На фоне инфузии кеторолака наблюдали снижение потребления морфина на 40%, снижение АД и ЧСС в сравнении с контрольной группой

• Кеторолак снижает частоту тромбозов микрососудов за счет подавления адреналин-индуцированной и аденозинфосфат-идуцированной агрегации тромбоцитов • Кеторолак характеризуется значительной селективностью в отношении ЦОГ-1 (тромбоциты продуцируют только ЦОГ-1) • Кеторолак способствует активации NO-синтазы

НПВС позитивно влияют на периоперационный иммунный статус препарат Потенциальное влияние на противораковый иммунитет НПВС и селективные ингибиторы ЦОГ-2 В эксперименте показано негативное влияние на ангиогенез и опухолевый рост, индуцируют апоптоз, нивелируют негативное влияние морфина на иммунный статус (Gottschalk A. , Sharma S. , Ford J. The role of the perioperative period in recurrence after cancer surgery. // Anesth. Analg. 2010; 110: 1636 -1643)

• Предоперационное в/в введение 8 -16 мг лорноксикама (ксефокама) снижало уровень послеоперационной иммуносупрессии после абдоминальной гистерэктомии за счет повышения плазменного уровня хемоаттрактантов (протеин 1), способствующих миграции в зону повреждения моноцитов и Т-лимфоцитов

• У пациентов, оперированных по поводу рака желудка, послеоперационная КПА ксефокамом и трамадолом сопровождалась минимальным угнетением функции Тлимфоцитов и натуральных клетоккиллеров, в сравнении с КПА морфином

Безопасно ли назначение НПВС? БЕЗОПАСНОСТЬ ПРЕЖДЕ ВСЕГО Safety first

Безопасность применения НПВС при обширных хирургических вмешательствах • Исследование POINT, 49 госпиталей, 8 стран Европы • 11. 245 пациентов (3. 208 старше 60 лет, 766 – ASA III-IV), • Максимальные суточные дозы: кетопрофен 200 мг, кеторолак 90 мг, диклофенак 150 мг (Forrest J. , Camu F. , Kehlet H. , Greer A. , Abdalla M. , Bonnet F. , Escolar G. , Jage J. , Velo G. , Langman M et al. // Brit. J. Anaesth. , 2002, 88, 227 -233)
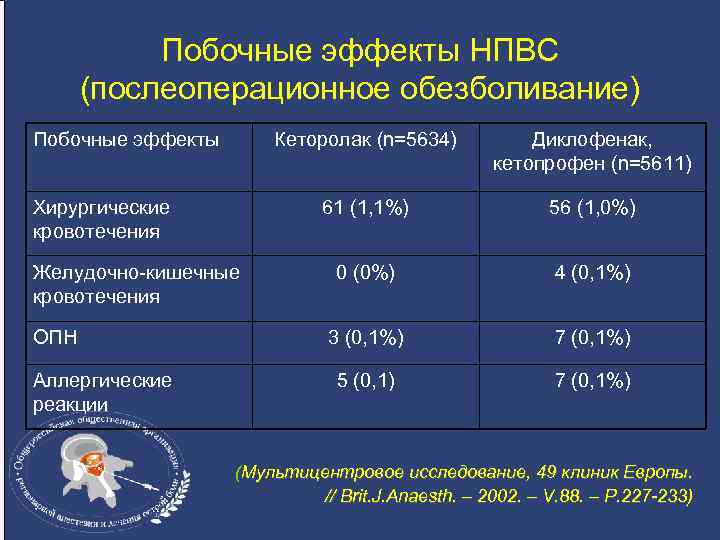
Побочные эффекты НПВС (послеоперационное обезболивание) Побочные эффекты Кеторолак (n=5634) 61 (1, 1%) ОПН Аллергические реакции 0 (0%) 4 (0, 1%) 7 (0, 1%) 5 (0, 1) Желудочно-кишечные кровотечения 56 (1, 0%) 3 (0, 1%) Хирургические кровотечения Диклофенак, кетопрофен (n=5611) 7 (0, 1%) (Мультицентровое исследование, 49 клиник Европы. // Brit. J. Anaesth. – 2002. – V. 88. – P. 227 -233)

Безопасность применения НПВС при обширных хирургических вмешательствах эффекты • Клинически значимые побочные были отмечены у 155 пациентов (1, 4%) • Наиболее часто – повышенная кровоточивость послеоперационной раны (1, 04%) • Риск повышенной кровоточивости повышался в 3, 05 раз на фоне параллельного назначения антикоагулянтов (чаще на фоне гепарина, чем НМГ)

Противопоказания к назначению НПВС Неселективные НПВС Селективные ингибиторы ЦОГ-2 Язвенная б-нь желудка и ДПК, ИБС, выраженный эрозивный гастрит атеросклероз коронарных и церебральных артерий, ОИМ Исходная гипокоагуляциия или ОНМК в анамнезе Почечная недостаточность (клиренс креатинина <50 мл/мин) мл/мин Гиповолемия, гипотензия Старческий возраст (? )

• Из соображений безопасности пациентов, не рекомендуется назначение НПВС > 3 -х суток послеоперационног о периода

Перфалган – парацетамол внутривенного введения Показания: • Кратковременное лечение болевого синдрома средней интенсивности • Кратковременное купирование гипертермии

Парацетамол является препаратом центрального действия 1, 2 n n Быстро проникает через гемато-энцефалический барьер Селективно подавляет синтез простагландинов в ЦНС 2, 3 Другие центральные механизмы действия связаны с бульбоспинальными нисходящими серотонинергическими тормозными путями 4, 5 n n Не имеет «потолочного» эффекта 1. Piguet V et al. Eur J Clin Pharmacol 1998; 53: 321 -4. 2. Carlsson KH et al. Pain 1988; 32: 313 -26. 3. Flower RJ et al. Nature 1972; 240: 410 -1. 4. Tjølsen A et al. Eur J Pharmacol 1991; 193: 193 -201. 5. Pélissier T et al. JPET 1996; 278: 8 -14.

Как назначать Перфалган Первое введение препарата – 1 г в/в за 30 минут до окончания операции (инфузия в течение 15 минут) n Повторное введение 1 г в/в через 4 часа после окончания операции n Последующие введения (инфузия в течение 15 минут) каждые 6 часов (не более 4 г в сутки), у подростков и пациентов весом < 50 кг – 15 мг/кг 4 раза в сутки n

Кетамин • Синтезирован в 1962 году • Свойства неконкурентного антагониста NMDAрецепторов, способного препятствовать развитию гипералгезии, открыты в 1990 году
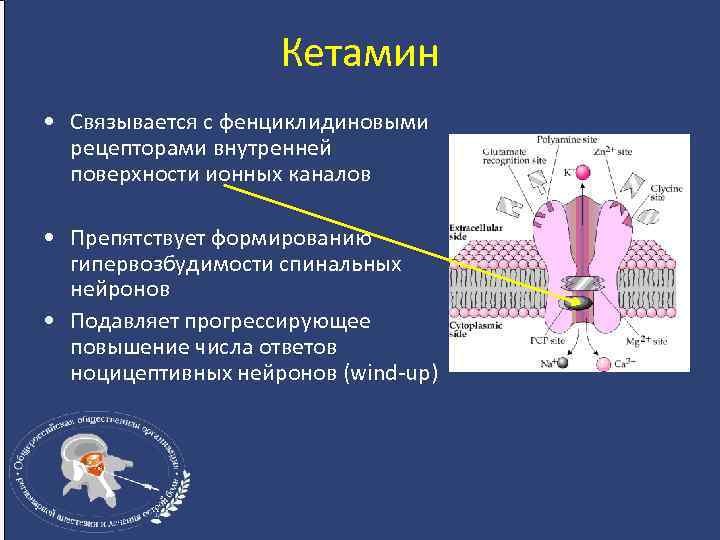
Кетамин • Связывается с фенциклидиновыми рецепторами внутренней поверхности ионных каналов • Препятствует формированию гипервозбудимости спинальных нейронов • Подавляет прогрессирующее повышение числа ответов ноцицептивных нейронов (wind-up)

Кетамин • Не только предупреждает развитие гипералгезии, но и усиливает анальгетический эффект опиоидов • Способен снизить выраженность гипералгезии, обусловленной введением налоксона
Кетамин • Болюсное введение кетамина 0, 20, 3 мг/кг во время индукции с последующей инфузией со скоростью 2 -5 мкг/кг/мин в течение 24 -48 часов достоверно уменьшает площадь зоны механической гипералгезии (Stubhaug A et al. // Acta Anaesth. Scand; 1997, Joly V et al. //Anesthesiology; 2005)

Кетамин • Чем больше площадь зоны механической гипералгезии и интенсивность боли в раннем послеоперационном периоде, тем выше риск формирования хронического болевого синдрома • Использование больших доз опиоидов короткого действия во время операции без кетамина опасно развитием хронического послеоперационного болевого синдрома (De Cock. // Anesthesiology; 2009; 111; 461)

Кетамин • На фоне превентивного введения кетамина время 1 -го требования анальгетика удлиняется ≈ на 35% • Послеоперационная потребность в анальгетиках (морфин) снижается в 1, 5 -2 раза • В большей степени снижается интенсивность динамической боли, чем C (Kwok R et al. //Anesth. Analg; 2004, Launo et al. // Minerva Anesthesiol; 2004) боли в покое

• Анализ 37 исследований (n=2385), преимущественно абдоминальная хирургия • Добавление кетамина к опиоидной анальгезии признано целесообразным в 54% случаев • Считают, что назначение кетамина более показано при операциях высокой травматичности

• ЭА+ кетамин – площадь зоны гиперальгезии через 24, 48 и 72 часа – 5, 10 и 10 см 2 • Кетамин без ЭА – площадь зоны гиперальгезии – 10, 75 и 155 см 2 • Без кетамина, но с ЭА – через 6 месяцев не имели боли 66%, кетамин + ЭА – без боли 100%


Габапентин • Внедрен в клиническую практику в 1993 г. в качестве противосудорожного ср-ва 2 -го поколения • В 2002 г. опубликованы данные исследования J. Dirks, позволившие рассматривать его как анальгетик широкого спектра действия


Каким образом антиконвульсант стал препаратом для лечения острой боли? • Послеоперационная боль имеет ноцицептивный и нейропатический компоненты • Ноцицептивный обусловлен активацией периферических ноцицепторов • Нейропатический связан с повреждением нервных волокон, характеризуется изменениями модуляции боли и центральной сенситизацией

Габапентин: механизм действия • Связывается с α 2 -дельта субъединицами пресинаптических Са 2+ каналов задних рогов спинного мозга • Активация α 2 -дельта субъединиц при повреждении периферических тканей усиливает вход Са 2+ в клетку • При этом усиливается выход глутамата из нервных окончаний • Глутамат активирует NMDA-рецепторы

Габапентин: эффекты • Прямое анальгетическое действие • Предотвращение развития острой толерантности к опиоидам • Снижение выраженности уже развившейся толерантности к опиоидам

Габапентин: схемы назначения • От 600 до 1200 мг per os за 1, 5 -2 часа до операции • Длительность назначения – от 1 -х до 30 суток (чаще 8 -10) • Суточная доза от 300 мг до 2400 мг (чаще 900 -1200 мг) в 3 -4 приема

• 18 исследований • В большинстве подтвержден опиоидсберегающий эффект ≈ 35% в первые 24 часа • Снижение интенсивности боли на 7 -14 мм по 100 мм ВАШ

Нефопам (Акупан®, Биокодекс, Франция) • Разработан в начале 1970 -х • Анальгетик центрального действия • Разовая доза 20 мг, максимальная суточная – 120 мг, чаще всего назначают 80 мг/сут
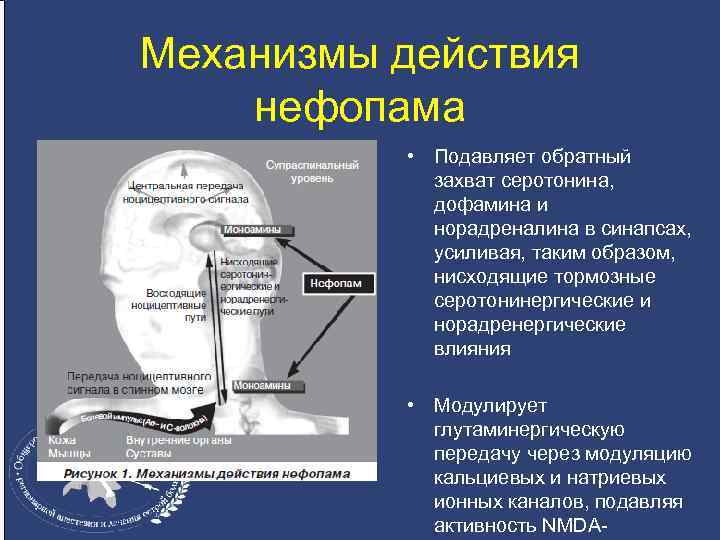
Механизмы действия нефопама • Подавляет обратный захват серотонина, дофамина и норадреналина в синапсах, усиливая, таким образом, нисходящие тормозные серотонинергические и норадренергические влияния • Модулирует глутаминергическую передачу через модуляцию кальциевых и натриевых ионных каналов, подавляя активность NMDA-

Влияние нефопама на ноцицептивный флексорный рефлекс RIII • Нефопам 20 мг в/в значительно подавляет выраженность рефлекса RIII, повышая его порог с 8, 5 до 11, 5 м. А • Максимальный эффект – через 30 мин, сохраняется на протяжении 90 мин

Влияние нефопама на ноцицептивный флексорный рефлекс RIII • Нефопам ограничивает передачу ноцицептивных стимулов на спинальном уровне • Ранее аналогичную депрессию RIII-рефлекса (≈ на 40%) наблюдали только после назначения опиоидных анальгетиков (морфин в/в 0, 2 мг/кг) • НПВС, парацетамол, трамадол оказывают минимальное влияние на амплитуду RIIIрефлекса (Guirimand F et al. // Pain. - 1999. - V. 80. - P. 399 -404, Willer J. // Brain Res. – 1985. – V. 331. - P. 105 -114, Willer J et al. // Pain. - 1989. – V. 38. – P. 1 -7)

• С 1. 01. 1995 по 31. 12. 2004 зафиксировано 114 случаев побочных эффектов, так или иначе связанных с назначением нефопама • Из них 26 клинически значимых

Побочные эффекты Количество Избыточная потливость 15 Тошнота 10 Тахикардия 8 Кожная эритема 7 Беспокойство 6 Рвота 5 Кожный зуд 4

Сочетанное применение нефопама и прочих анальгетиков • Идеальная комбинация: нефопам + НПВС (большинство исследований с кетопрофеном) – синергистический эффект, снижение доз каждого препарата ≈ в 2, 5 раза • Нефопам + парацетамол – отчасти синергистический, в большей степени аддитивный эффект • Нефопам + опиоидный анальгетик – аддитивный эффект (Girard P et al // Eur. J. Pharm. – 2008. – V. 584. – P. 263 -271, Delage N et al. // Anesthesiology. - 2005. – V. 102. - P. 1211 -1216, Beloeil H et al. // Anesth. Analg – 2004 - V. 98 - P. 395– 400)

Антигиперальгезивный эффект нефопама

• Кетамин – основной антагонист NMDA- рецепторов, препятствующий формированию острой толерантности к опиоидным анальгетикам • Добавление к анальгезии морфином 10 мг кетамина или 20 мг нефопама в равной степени потенцирует анальгетический эффект

• АКУПАН® - является препаратом выбора послеоперационной неопиоидной анальгезии для всех пациентов, имеющих противопоказания к назначению НПВС

Сочетанное применение нефопама и прочих анальгетиков • Идеальная комбинация: нефопам + НПВС (большинство исследований с кетопрофеном) – синергистический эффект, снижение доз каждого препарата ≈ в 2, 5 раза • Нефопам + парацетамол – отчасти синергистический, в большей степени аддитивный эффект • Нефопам + опиоидный анальгетик – аддитивный эффект (Girard P et al // Eur. J. Pharm. – 2008. – V. 584. – P. 263 -271, Delage N et al. // Anesthesiology. - 2005. – V. 102. - P. 1211 -1216, Beloeil H et al. // Anesth. Analg – 2004 - V. 98 - P. 395– 400)

Нефопам предотвращает послеоперационный озноб • Перед выполнением СА или ЭА пациенты получали нефопам 0, 15 мг/кг или трамадол 0, 5 мг/кг в/в • У пациентов, получавших нефопам, частота и выраженность послеоперационного озноба была достоверно ниже

Нефопам предотвращает послеоперационный озноб • Введение в конце операции нефопама 0, 2 мг/кг превосходило эффект клонидина 1, 5 мкг/кг • Введение клонидина сопровождалось снижением АД и седацией

Мета-анализ Park S et al. (2012) Профилактика озноба Акупаном® наиболее эффективна Park SM, Crit Care Med. 2012 Nov; 40(11): 3070 -82

• С 1. 01. 1995 по 31. 12. 2004 зафиксировано 114 случаев побочных эффектов, так или иначе связанных с назначением нефопама • Из них 26 клинически значимых

Побочные эффекты Количество Избыточная потливость 15 Тошнота 10 Тахикардия 8 Кожная эритема 7 Беспокойство 6 Рвота 5 Кожный зуд 4

• Аудит состояния послеоперационного обезболивания в 76 хирургических центрах Франции (06. 2004 – 0. 7. 2006) • Вывод 1: качество послеоперационного обезболивания постепенно повышается • Вывод 2: частота использования неопиоидных анальгетиков во Франции выше (95, 5%), чем в других странах Европы (64 -72%)
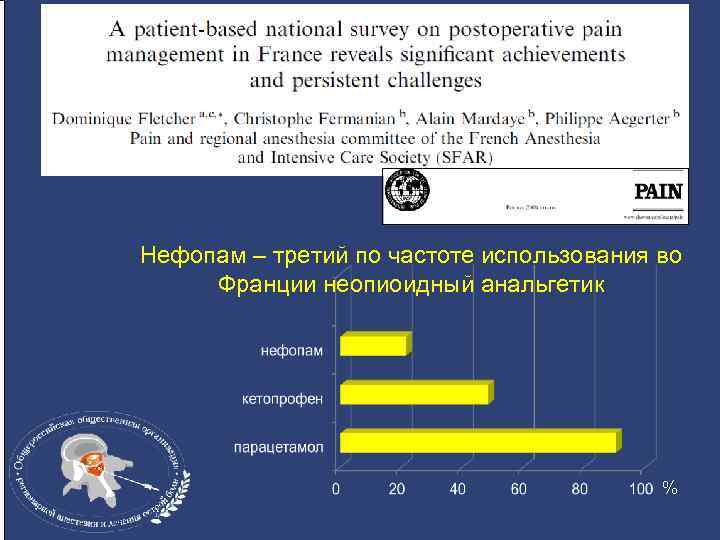
Нефопам – третий по частоте использования во Франции неопиоидный анальгетик %

ЗАКЛЮЧЕНИЕ • Все рассмотренные препараты оказывают влияние на патогенетические механизмы острого болевого синдрома • Ни один из этих препаратов при использовании в моно-виде не решает проблему адекватности послеоперационного обезболивания • Наиболее перспективным представляется сочетанное использование данных препаратов

Благодарю за внимание! © М. А. Дзядзько Роанн, 27 октября 2006 года
обзор анальгетиков.ppt