Яф-41 Елтаев Д.Т..pptx
- Количество слайдов: 50

Кристалдардың классификациясы даған: Елтаев Дінмұхамбет Астана қаласы

Кристалл торларының типтері.

Сабақтың мақсаты білімділік: кристалл торлары және оның түрлері жайлы ұғымды жүйелеу, кристалл тор типтерінің заттың физикалық қасиеттеріне тигізер әсерін түсіндіру; тәрбиелілік: студеттердің пәнге деген ынтасын арттыру;

Жер атмосферасы (ауа) негізінен екі газ – азот N 2 және оттегі О 2 молекулаларынан тұрады. Екі газ да түссіз, сондықтан ауаны көрмейміз. Өте кішкене болғандықтан жеке молекулаларды да көре алмаймыз. Газ, мысалы азот N 2 көзге көріну үшін не істеуіміз керек? Сірә молекулаларды бір- біріне жақындату керек шығар.

Мұны температураны төмендету арқылы жүзеге асырады. Газ молекулаларының ретсіз қозғаласы баяулап, молекула арасындағы қашықтық кемиді. Бір кезде молекулалардың жылдамдығы азайып, молекула арасындағы қашықтық кемігенде газ конденсациялана бастайды (тығыздалады, қоюланады), сөйтіп сұйық азот алынады. Біз оны көреміз.

Сұйық азот – түссіз, мөлдір сұйықтық. Сұйық азотты әрі қарай салқындатқанда азот молекулалары бір –біріне қарай еркін қозғала алмайтын, тек бір орында тербеліп қозғалатын күйге келеді. Қар тәрізді ақ зат - қатты азот түзіледі. Сұйықтық қатаяды. Химиялық біртекті (химиялық құрамы бірдей) газ, сұйықтық және қатты дене бір заттың үш агрегаттық күйі деп аталады.

Осы зат қандай күйде болса да, оның химиялық қасиеттері бірдей болады. Сондықтан газтәрізді, сұйық және қатты молекулалық азот – бір зат (үш түрлі зат емес). Ал, газ сұйық және қатты денедегі молекулалық күйінде N 2 –тың айырмашылығы бар екеніне әлгінде ғана көз жеткіздіңдер. Қатты денедегі молекулалар кеңістікте ретсіз емес, әр зат үшін белгілі бір заңдылықпен орналасады.

Бұл заңдылықты түсіну үшін, үш жақты кеңістікте ойша молекулалардың орталықтарын қосып қиылысатын түзу сызықтар жүргізейік. Бұл кезде кристалдық тор деп аталатын кеңістіктегі дұрыс пішін пайда болады. Сызықтар қиылысатын жердегі нүктелер кристалдық тордың түйіндері деп аталады. Қатты дененің өзі де кристалл түрінде болады. Кез келген қатты дененің белгілі бір кристалдық құрылымы бар.
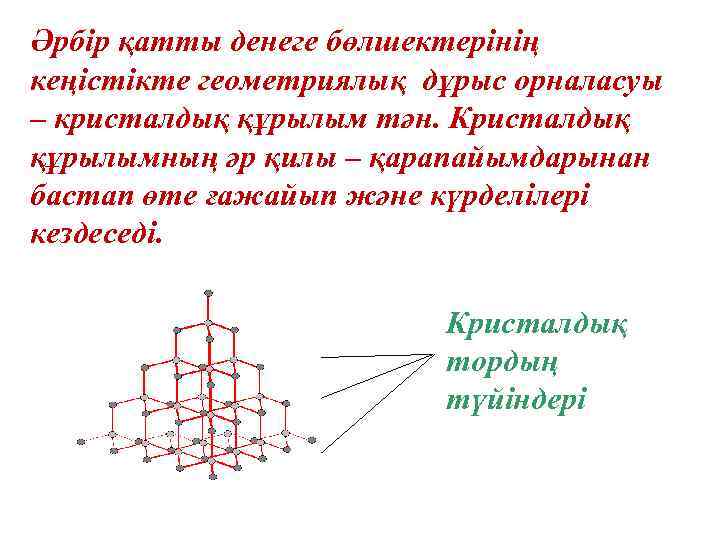
Әрбір қатты денеге бөлшектерінің кеңістікте геометриялық дұрыс орналасуы – кристалдық құрылым тән. Кристалдық құрылымның әр қилы – қарапайымдарынан бастап өте ғажайып және күрделілері кездеседі. Кристалдық тордың түйіндері

Кристалды заттар Белгілі балқу температурасы болады. Затты құрап тұрған бөлшектердің (атом, ион, молекула) белгілі бір ретпен орналасуымен сипатталады.

Кристалдар • Белгілі балқу температурасы бар, кристалдық құрылымы бар, физикалық денелер. • Кристалдар – анизотропты, яғни физикалық қасиеттері бағытқа тәуелді; • Кристалда жарықтың таралуы жылдамдығы, жылу өткізгіштігі, серпімділігі бағытқа тәуелді болады; • Кристалл атомдары кеңістікте қатаң тәртіппен орналасып кристалл торын құрайды. • Кристалдар белгілі бір бұрыштармен орналасқан жазық бұрыштардан тұратын болса, монокристалл деп аталады; • Егер кристалл өте ұсақ кристалл жиынтығынан тұратын болса, поликристалл деп аталады.
Кристалл торларының типтері • Молекулалық • Иондық • Атомдық ковалентті • Атомдық металды
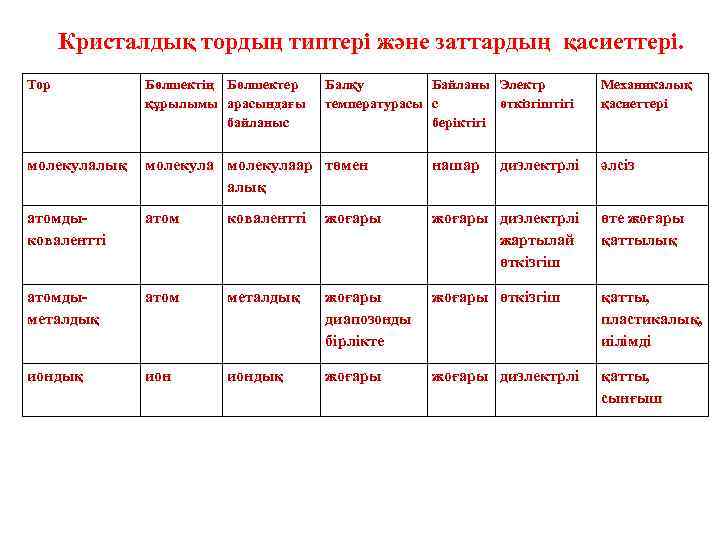
Кристалдық тордың типтері және заттардың қасиеттері. Тор Бөлшектің Бөлшектер құрылымы арасындағы байланыс Балқу Байланы Электр температурасы с өткізгіштігі беріктігі молекулалық молекулаар төмен алық нашар атомдыковалентті атом ковалентті жоғары диэлектрлі жартылай өткізгіш өте жоғары қаттылық атомдыметалдық атом металдық жоғары диапозонды бірлікте жоғары өткізгіш қатты, пластикалық, иілімді иондық жоғары диэлектрлі қатты, сынғыш диэлектрлі Механикалық қасиеттері әлсіз

Молекулалық кристалл тор Йодтың кристалл торы

Мына суретте иодтың кристалдық құрылымы бейнеленген. Тор түйіндерінде иод I 2 молекулалары орналасқан. Сондықтан тор молекулалық, ал күйі – қатты заттың өзі молекулалық кристалл деп аталады. Молекулалық кристалдың түйіндерінде полюссіз молекулалар (N 2 , I 2 т. б. ) орналасады. Олар бір – бірін қалай ұстап тұрады? Йодтың кристалл торы

Жай заттардың молекулалары полюссіз және бірбіріне әсерін тигізбейді. Заттың сұйық, әсіресе қатты күйінде молекулалар өте жақындасып, өзара әрекеттесе бастайды. Жай зат молекулаларында электрон тығыздығының ішкі және өте әлсіз ығысуы, яғни электр диполі пайда болады. Осының өзі әлсіз полюстенген молекулалардың диполдарының аттас емес жақындасуына жеткілікті. Осыдан әлсіз химиялық байланысу, яғни молекулааралық өзара әрекеттесудің бір түрі пайда болады.

Молекулалық кристалл торы бар заттарды мына сызбанұсқамен: «ҚҰРАМЫ → ҚҰРЫЛЫСЫ → ҚАСИЕТТЕРІ» бойынша сипаттайық. ҚҰРАМЫ: тордың түйіндерінде бейметалл pэлементтер атомдарынан түзілген молекулалар орналасады. ҚҰРЫЛЫСЫ → ҚАСИЕТТЕРІ: молекулалары әлсіз молекула аралық күшпен байланасады. Мұндай заттардың балқу және қайнау температуралары төмен, ұшқыш, қаттылығы және механикалық беріктігі аз болады.

Бөлме температурасында бұлар не газ (О 2, N 2) не қатты, бірақ ұшқыш (І2) заттар, бір ғана сұйықтық Br 2 белгілі. Кристалдарда валенттік электрондар араласпайды. Олардың электр тогын өткізбейтіндігі сонымен түсіндіріледі, бұлар диэлектриктер (немесе оқшаулағыштар (изоляторлар). Молекулалық кристалдарға қарай жүрген жолымызды былай бейнелеп көрсете аламыз:

Атом → Молекула → Кристалдық макродене асыл газдар да (VIII A топ элементтері) молекулалық кристалл торын түзеді. Қарастырылған жай заттардың О 2, N 2, І2 айырмашылығы асыл газдардың молекулалары бір атомды, яғни бұлар жай атомдар He, Ne, Ar және т. б. Сыртқы s – және p – деңгейшелері (ns 2 np 6) аяқталғандықтан бұл элементтердің атомдары өзара ковалентті байланыстар түзе алмайды және молекулаларға бірікпейді. Қатты асыл газдардың молекулалық кристалл торларының түйіндерінде атомдар орналасады.

Тор онша берік емес, ол қатты О 2, N 2, І2 тәрізді молекулааралық әрекеттесудің күштерімен ұсталып тұрады. Айырмашылығы, асыл газдардың атомдарында дипольдер қас қағым уақытта түзіледі. Асыл газдар өте төменгі температурада сұйылады және қатаяды. Молекулалық кристалл тор түзетін элементтер типтік бейметалдар фтор, хлор, бром, йод, күкірт, азот, фосфор (фосфор мен күкірт молекулалары бөлме температурасында күрделірек - (S 8 және P 4 ) молекулаларын түзеді.

Молекулалық кристалл торы бар күрделі заттар. Мұндай құрылысы бар күрделі заттарды білесіңдер. Мысалы, мұз – кристалдық су, құрғақ мұз – кристалдық көмір қышқыл газы, сахароза. Мұндай заттардың кристалл тор түйіндерінде молекулалар орналасады.

Бұл кристалдардың кристалл түйіндерінде молекулааралық тартылу күші әлсіз. Ол физикалық қасиеттерінен байқалады.

Иондық кристалдар аттас зарядталған иондардың электростатикалық әсерінің нәтижесінде түзіледі. Кристалдың иондық моделі әрбір ионның максималды жағдайда аттас зарядталған иондармен қоршалуы нәтижесінде түзіледі. АВ құрамды кристалдар үшін иондық радиустың қатынасы иондардың координациялық санын құрайды. Иондық кристалдық торды тұздар және сілтілер түзеді. Иондық байланыстың беріктігіне байланысты иондық кристалл торлы заттардың балқу температурасы жоғары және қатты болады.

Кристалдық тордағы катион мен анионды қоршайтын аттас емес иондар саны координация саны (КС) деп аталады. Ең жиі кезедесетін КС саны 4 және 6, 8 және 12 сирек кездеседі. Олар нақты кристалды құрылыммен, яғни иондардың мөлшеріне байланысты иондардың торда түйінделу түріне қарай және басқа факторлармен анықталады. Ас тұзы кристалдарында Na+ үшін де және Cl- үшін де КС – 6.
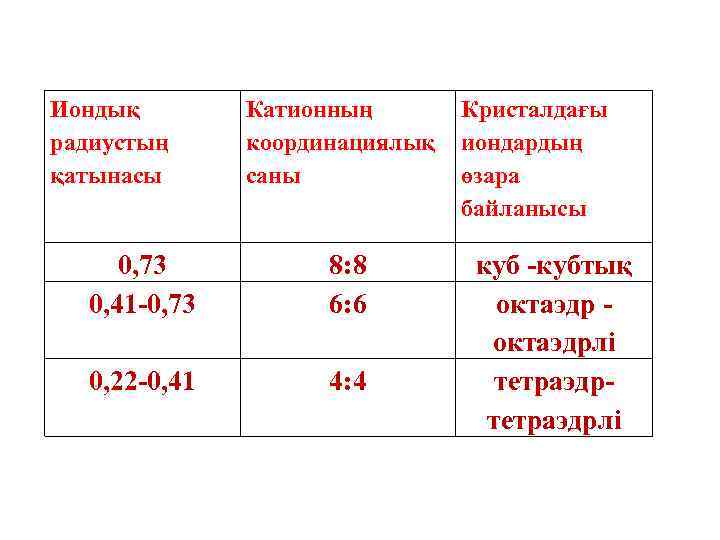
Иондық радиустың қатынасы Катионның координациялық саны 0, 73 0, 41 -0, 73 8: 8 6: 6 0, 22 -0, 41 4: 4 Кристалдағы иондардың өзара байланысы куб -кубтық октаэдрлі тетраэдрлі
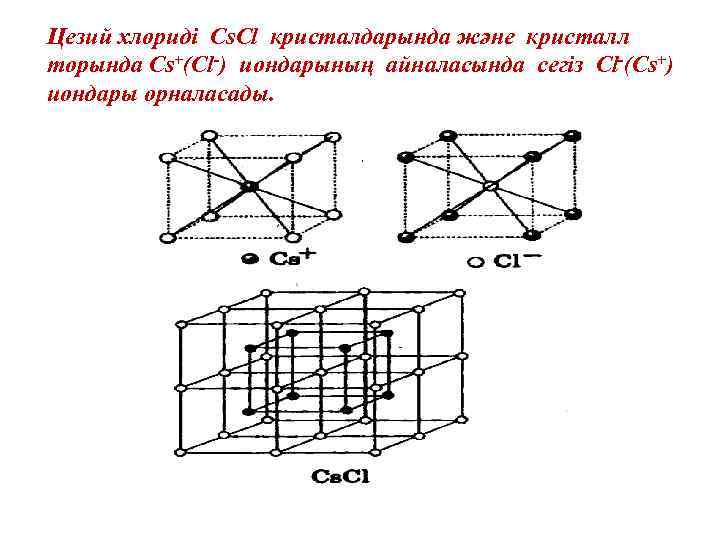
Цезий хлориді Cs. Cl кристалдарында және кристалл торында Cs+(Cl-) иондарының айналасында сегіз Cl-(Cs+) иондары орналасады.
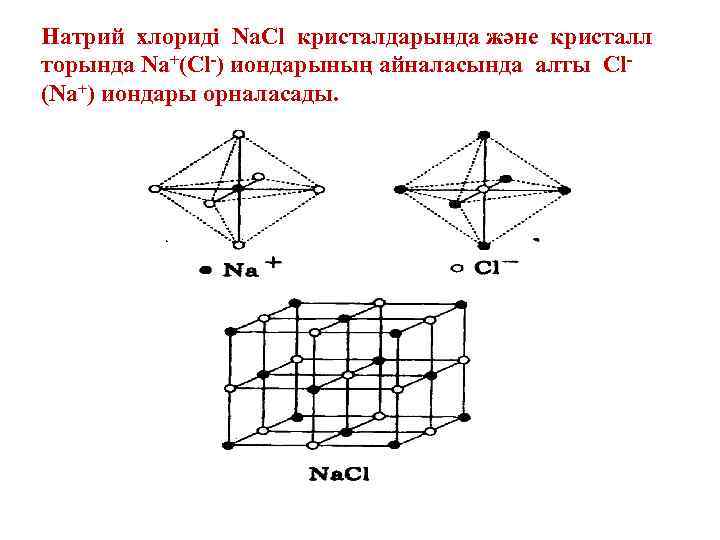
Натрий хлориді Na. Cl кристалдарында және кристалл торында Na+(Cl-) иондарының айналасында алты Cl(Na+) иондары орналасады.
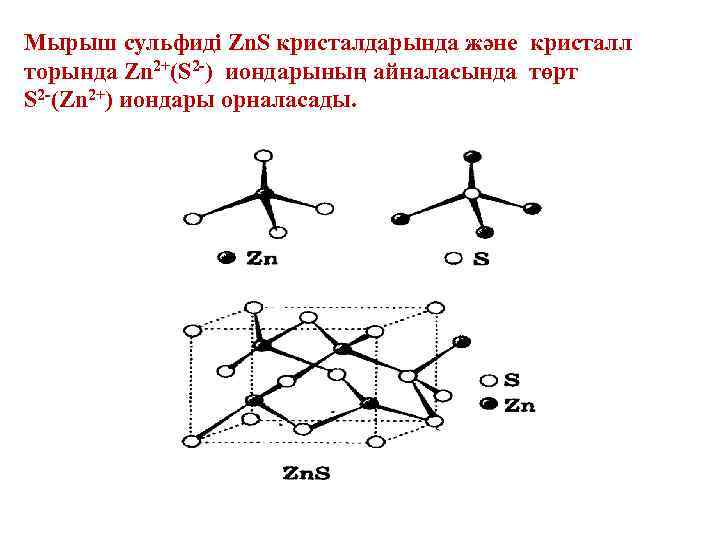
Мырыш сульфиді Zn. S кристалдарында және кристалл торында Zn 2+(S 2 -) иондарының айналасында төрт S 2 -(Zn 2+) иондары орналасады.
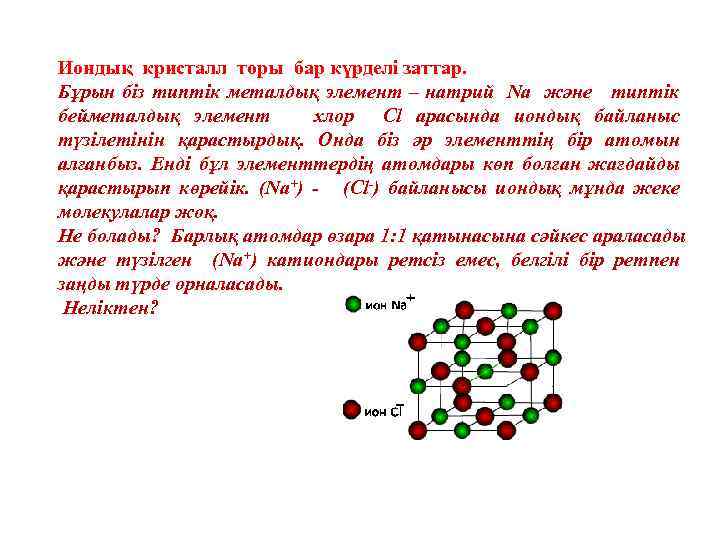
Иондық кристалл торы бар күрделі заттар. Бұрын біз типтік металдық элемент – натрий Na және типтік бейметалдық элемент хлор Cl арасында иондық байланыс түзілетінін қарастырдық. Онда біз әр элементтің бір атомын алғанбыз. Енді бұл элементтердің атомдары көп болған жағдайды қарастырып көрейік. (Na+) - (Cl-) байланысы иондық мұнда жеке молекулалар жоқ. Не болады? Барлық атомдар өзара 1: 1 қатынасына сәйкес араласады және түзілген (Na+) катиондары ретсіз емес, белгілі бір ретпен заңды түрде орналасады. Неліктен?

Аттас емес иондар (Na+) және (Cl-) тартылып бір -біріне жақындауға ұмтылады. Аттас иондар (Cl) және (Cl-), (Na+) және (Na+) бір-бірінен тебіледі және барынша алыстауға ұмтылады. Тартылу күші мен тебілу күші теңескенде, катиондар мен аниондар белгілі бір ретпен орналасады. Түйіндерінде иондар орналасқан иондық кристалдық торын құрайды. Ас тұзының кристалының моделі келтірілген. Модельден кристалда иондардың орналасуы жақсы көрінеді.

Иондық кристалдардың екі ерекшелігіне назар аударыңдар. Біріншіден, кристалда бір ионның екінші ионмен байланысының саны осы элемент атомдарындағы жұптаспаған электрон санына сәйкес келе бермейді. Салыстырыңдар: натрий және хлор атомында бір-бірден ғана жұптаспаған электрон болады.

Бұдан иондық байланыстардың бағытталмағандығы байқалады. Екіншіден, ковалентті байланыссыз екі атомды молекула Na. Cl түзілмейді, оның орнына көпатомды иондық кристалл қалыптасады. + + - - + + - +

Атомды – ковалентті кристалдар Атомды-кристалды заттарға мысал ретінде алмаз және кварц кристалдарын жатқызуға болады. Алмаз кристалдарында әрбір көміртегі атомдары С басқаларымен төрт байланыс түзеді. Ал кварц кристалдарында (Si. O 2) әрбір кремний атомдары Si төрт байланыс түзеді, ал әрбір оттек атомдары екі байланыс түзеді.
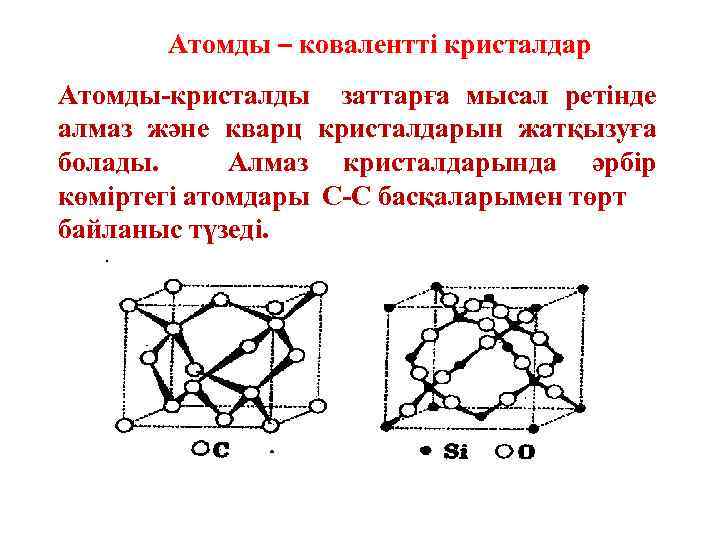
Атомды – ковалентті кристалдар Атомды-кристалды заттарға мысал ретінде алмаз және кварц кристалдарын жатқызуға болады. Алмаз кристалдарында әрбір көміртегі атомдары С-C басқаларымен төрт байланыс түзеді.

Атомды – металдық кристалдар Металдық байланыс деп металдық торда металдардың оң зарядталған иондары мен валенттік электрондардан тұратын электрон газының арасында пайда болатын химиялық байланыс. 0 0 + + - -+ 0 0 0

Атомды – металдық кристалдар Металдарды мына сызбанұсқамен : «құрамы қасиеттері” бойынша сипаттайық. құрылысы Құрамы: жай заттар – металдар бір металдық элемент атомдарынан тұрады. Құрылысы: металдардың кристалл торының түйіндерінде еркін қозғалатын ортақтасқан электрондармен (электрон газымен) байланысқан катиондар бар. Қасиеттері: валенттік электрондары қозғалғыш болғандықтан металдар иілгіш, электр және жылу өткізгіштігі жоғары, жылтыр болады және мөлдір емес.

Атомды – металдық кристалдар Атомды –металды кристалды заттарға: мыс, алюминий, қорғасын, темір жатады. Олардың пішіні төмендегідей кубты қырлы –центрлі кристалдық тор түзеді.
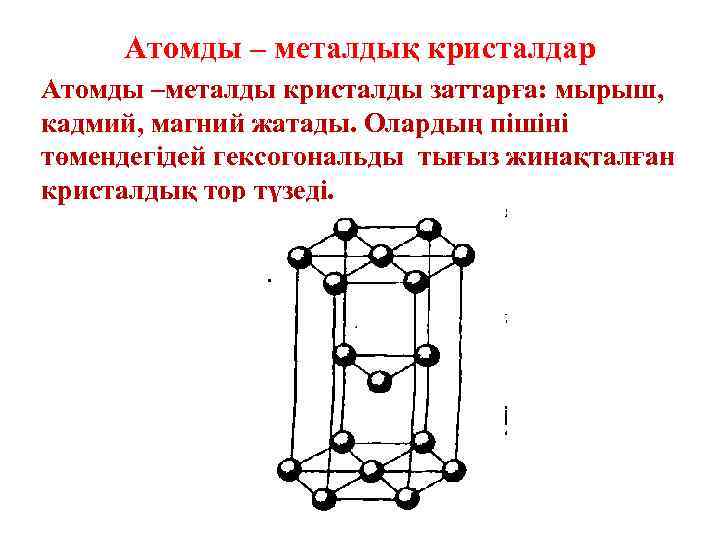
Атомды – металдық кристалдар Атомды –металды кристалды заттарға: мырыш, кадмий, магний жатады. Олардың пішіні төмендегідей гексогональды тығыз жинақталған кристалдық тор түзеді.

Атомды – металдық кристалдар Атомды –металды кристалды заттарға: натрий, калий, темір, хром, барий кристалдары жатады. Олардың пішіні төмендегідей кубты көлемді – центрлі кристалдық тор түзеді.

Кристалдағы ақаулар (дефектілер) Құрамы тұрақты заттар - дальтонидтер деп, ал құрамы ауыспалы заттарды – бертоллидтер деп атайды. Құрамы тұрақты заттарға молекулалық құрылысты заттарды жатқызамыз, себебі молекуланың құрамына қарай ондағы атомдардың құрылысын анықтауға болады. Атомды және ионды құрылысты заттарды анағұрлым тұрақты немесе ауыспалы құрамды заттарға жатқызуға болады. Мұның басты себебі кристалдағы нүктелік ақаулар. Ол энтропиялық фактор T ∆ S > 0 қосылыстың құрамының ауыспалы болуының әсерінен жүзеге асады.
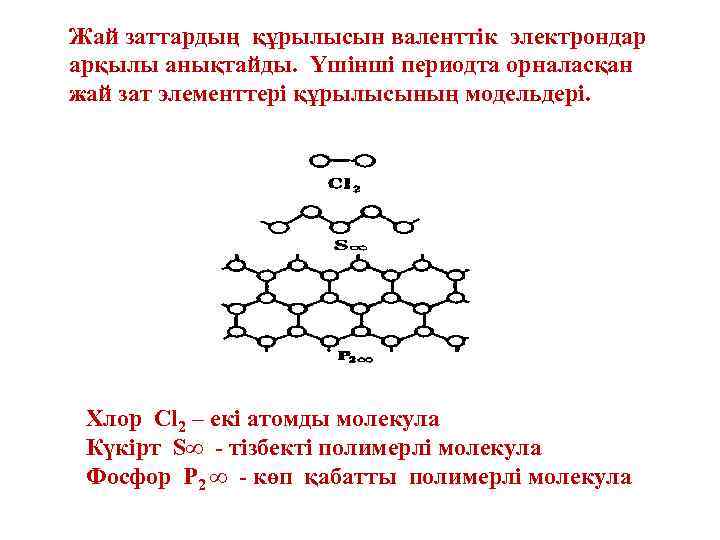
Жай заттардың құрылысын валенттік электрондар арқылы анықтайды. Үшінші периодта орналасқан жай зат элементтері құрылысының модельдері. Хлор Cl 2 – екі атомды молекула Күкірт S∞ - тізбекті полимерлі молекула Фосфор Р 2 ∞ - көп қабатты полимерлі молекула
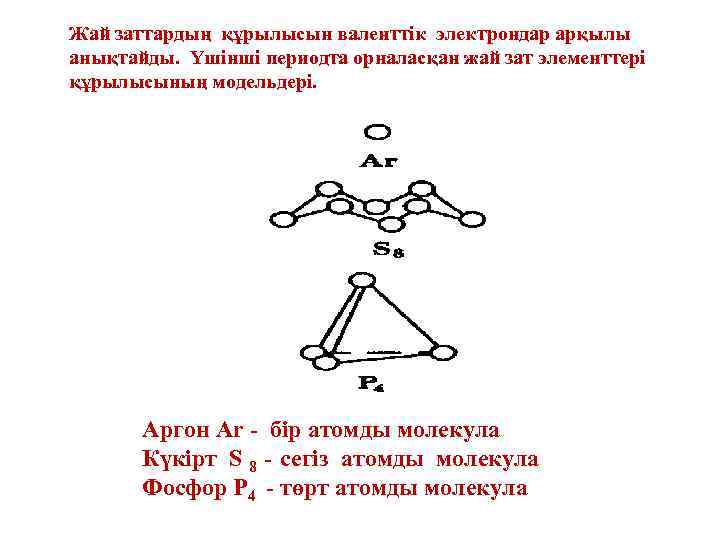
Жай заттардың құрылысын валенттік электрондар арқылы анықтайды. Үшінші периодта орналасқан жай зат элементтері құрылысының модельдері. Аргон Ar - бір атомды молекула Күкірт S 8 - сегіз атомды молекула Фосфор Р 4 - төрт атомды молекула
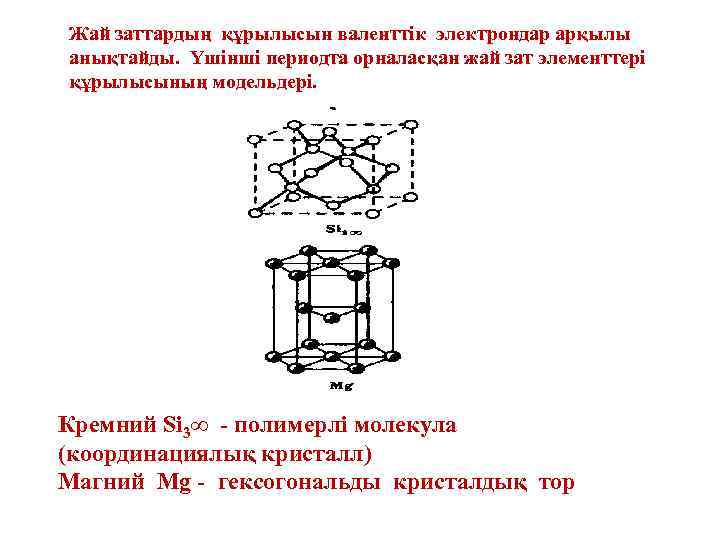
Жай заттардың құрылысын валенттік электрондар арқылы анықтайды. Үшінші периодта орналасқан жай зат элементтері құрылысының модельдері. Кремний Si 3∞ - полимерлі молекула (координациялық кристалл) Магний Mg - гексогональды кристалдық тор
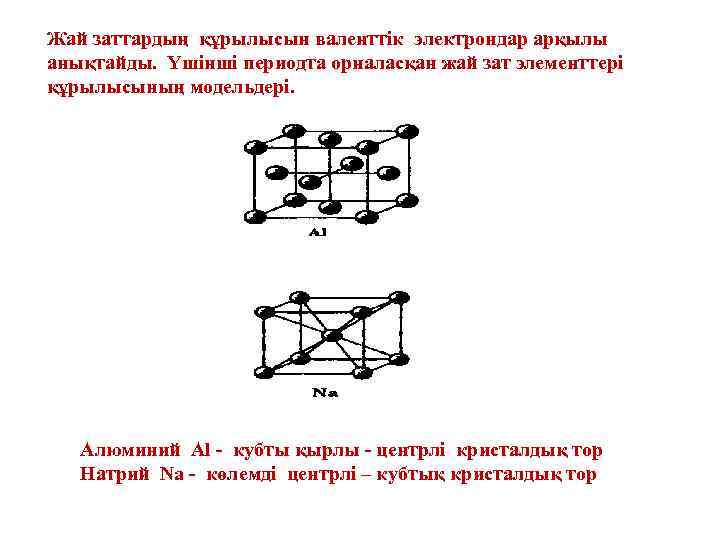
Жай заттардың құрылысын валенттік электрондар арқылы анықтайды. Үшінші периодта орналасқан жай зат элементтері құрылысының модельдері. Алюминий Al - кубты қырлы - центрлі кристалдық тор Натрий Na - көлемді центрлі – кубтық кристалдық тор

Кристалдардың дислокациялануы дегеніміз жазықты, бойлай, жақын маңда орналасқан атомдардың сипатының бұзылуы. Кристалл торларында ақаулардың (дефектілер) пайда болуы. Барлық атомдары минималды энергиялық жағдайда болатын идеалды кристалдар ешуақытта кездеспейді. Кристалдардың идеал торларында ауытқулардың екі түрі бар: тұрақты және уақытша түрі болады. Уақытша ауытқулар кристалдарға механикалық, жылулық және электромагниттік ауытқулардың әсерінен кристалдар арқылы тез бөлшектердің ағыны арқылы жүзеге асады.
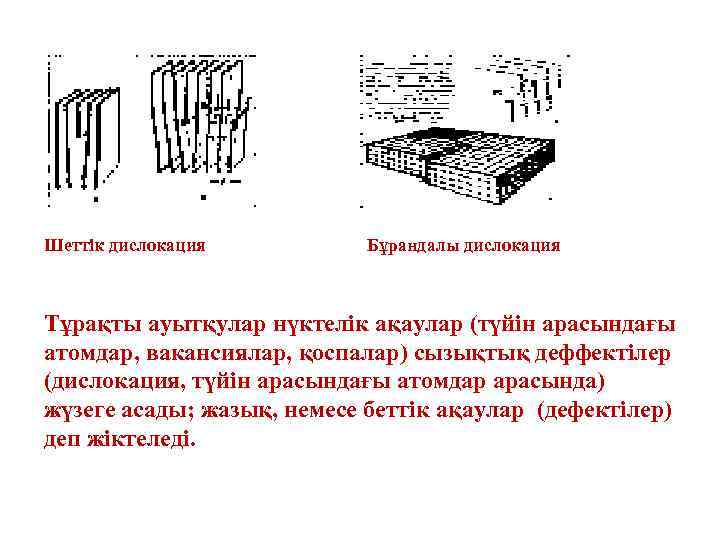
Шеттік дислокация Бұрандалы дислокация Тұрақты ауытқулар нүктелік ақаулар (түйін арасындағы атомдар, вакансиялар, қоспалар) сызықтық деффектілер (дислокация, түйін арасындағы атомдар арасында) жүзеге асады; жазық, немесе беттік ақаулар (дефектілер) деп жіктеледі.

Қазіргі уақытта дислокациялану теориясы қарқынды түрде дамып, құрылыс материалдарындағы әртүрлі процестерді түсіндіріп, құрылыс материалдарының сапасын арттыру мақсаты үшін қолданылады. Бейметалды құрылыс материалдары ретінде қолданылатын кальцит, гипстің қасиеттері мен жасанды құрылыс материалдары конгломераттардың қасиеттерімен танысуда қолданылады.

Қолданылған әдебиеттер 1. Интернет желісі. 2. http: //www. Открытый урок. рф/articles/subjects/4/

Назарларыңызға рахмет!
Яф-41 Елтаев Д.Т..pptx