eb05c43be11778647c43f402759eaf09.ppt
- Количество слайдов: 60
 Крестор – сравнительная эффективность 24. 11. 2014 CRE – 52 903 011 – 08/08/2013
Крестор – сравнительная эффективность 24. 11. 2014 CRE – 52 903 011 – 08/08/2013
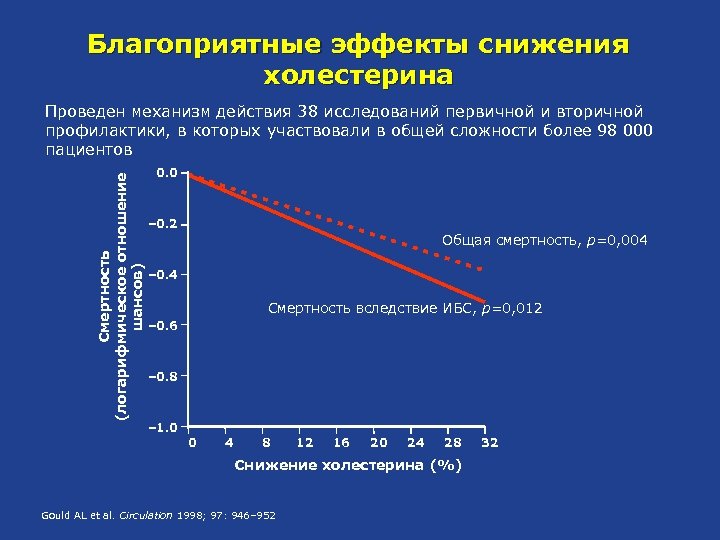 Благоприятные эффекты снижения холестерина Смертность (логарифмическое отношение шансов) Проведен механизм действия 38 исследований первичной и вторичной профилактики, в которых участвовали в общей сложности более 98 000 пациентов 0. 0 – 0. 2 Общая смертность, p=0, 004 – 0. 4 Смертность вследствие ИБС, p=0, 012 – 0. 6 – 0. 8 – 1. 0 0 4 8 12 16 20 24 28 Снижение холестерина (%) Gould AL et al. Circulation 1998; 97: 946– 952 32
Благоприятные эффекты снижения холестерина Смертность (логарифмическое отношение шансов) Проведен механизм действия 38 исследований первичной и вторичной профилактики, в которых участвовали в общей сложности более 98 000 пациентов 0. 0 – 0. 2 Общая смертность, p=0, 004 – 0. 4 Смертность вследствие ИБС, p=0, 012 – 0. 6 – 0. 8 – 1. 0 0 4 8 12 16 20 24 28 Снижение холестерина (%) Gould AL et al. Circulation 1998; 97: 946– 952 32
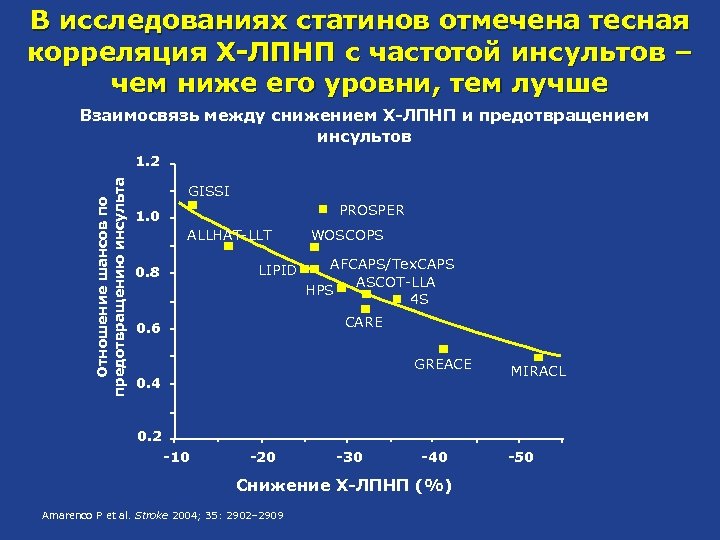 В исследованиях статинов отмечена тесная корреляция Х-ЛПНП с частотой инсультов – чем ниже его уровни, тем лучше Взаимосвязь между снижением Х-ЛПНП и предотвращением инсультов Отношение шансов по предотвращению инсульта 1. 2 GISSI PROSPER 1. 0 ALLHAT-LLT LIPID 0. 8 WOSCOPS AFCAPS/Tex. CAPS ASCOT-LLA HPS 4 S CARE 0. 6 GREACE 0. 4 MIRACL 0. 2 -10 -20 -30 -40 Снижение Х-ЛПНП (%) Amarenco P et al. Stroke 2004; 35: 2902– 2909 -50
В исследованиях статинов отмечена тесная корреляция Х-ЛПНП с частотой инсультов – чем ниже его уровни, тем лучше Взаимосвязь между снижением Х-ЛПНП и предотвращением инсультов Отношение шансов по предотвращению инсульта 1. 2 GISSI PROSPER 1. 0 ALLHAT-LLT LIPID 0. 8 WOSCOPS AFCAPS/Tex. CAPS ASCOT-LLA HPS 4 S CARE 0. 6 GREACE 0. 4 MIRACL 0. 2 -10 -20 -30 -40 Снижение Х-ЛПНП (%) Amarenco P et al. Stroke 2004; 35: 2902– 2909 -50
 Взаимосвязь между изменениями Х-ЛПНП и Х-ЛПВП, с одной стороны, и риском развития ИБС, с другой стороны Снижение ХЛПНП на 1 ммоль/л снижает риск развития ИБС на 22% 1 1. CTT Collaborators et al. Lancet. 2010; 376: 1670– 1676 2. Barter P et al. NEJM 2007; 357: 1301‒ 1310 Повышения уровней Х-ЛПВП на 0, 03 ммоль/л соответствует снижению риска развития ИБС на 1, 1% 2
Взаимосвязь между изменениями Х-ЛПНП и Х-ЛПВП, с одной стороны, и риском развития ИБС, с другой стороны Снижение ХЛПНП на 1 ммоль/л снижает риск развития ИБС на 22% 1 1. CTT Collaborators et al. Lancet. 2010; 376: 1670– 1676 2. Barter P et al. NEJM 2007; 357: 1301‒ 1310 Повышения уровней Х-ЛПВП на 0, 03 ммоль/л соответствует снижению риска развития ИБС на 1, 1% 2
 Европейские рекомендации, 2011 год Умеренный риск • Семейный анамнез ИБС, абдоминальное ожирение и др. 1 -2 ФР • SCORE >1% • 3, 0 ммоль/л 115 мг/дл Высокий риск • Ярко выраженный ФР, такой как семейная ГХС и тяжелая АГ • SCORE >5% 2, 5 ммоль/л 100 мг/дл Очень высокий риск ИБС, СД 2 типа, СД 1 типа с ПОМ, ОКС, коронарные вмешательства • SCORE >10% 1, 8 ммоль/л 70 мг/дл ESC/EAS Guidelines for the management of dyslipidaemias. European Heart J 2011; 32, 1769 -1818
Европейские рекомендации, 2011 год Умеренный риск • Семейный анамнез ИБС, абдоминальное ожирение и др. 1 -2 ФР • SCORE >1% • 3, 0 ммоль/л 115 мг/дл Высокий риск • Ярко выраженный ФР, такой как семейная ГХС и тяжелая АГ • SCORE >5% 2, 5 ммоль/л 100 мг/дл Очень высокий риск ИБС, СД 2 типа, СД 1 типа с ПОМ, ОКС, коронарные вмешательства • SCORE >10% 1, 8 ммоль/л 70 мг/дл ESC/EAS Guidelines for the management of dyslipidaemias. European Heart J 2011; 32, 1769 -1818
 Пересмотр европейских руководств: Рабочая группа по контролю дислипидемии при Европейском Кардиологическом Обществе (ESC) и Европейском Обществе по изучению атеросклероза (EAS) Популяция пациентов Уровни Х-ЛПНП, являющиеся терапевтическими целями Очень высокий сердечно-сосудистый риск - Поставлен диагноз сердечно-сосудистых заболеваний, наличие сахарного диабета типа 2, а также сахарного диабета типа 1 при поражении органов-мишеней, умеренная или тяжелая хроническая почечная недостаточность или уровень SCORE ≥ 10% <1, 8 ммоль/л (~<70 мг/дл) и/или снижение на ≥ 50% при невозможности достижения целевых уровней Высокий сердечно-сосудистый риск - выраженное повышение отдельных факторов риска, значение SCORE от ≥ 5 до <10% <2, 5 ммоль/л (~<100 мг/дл) Умеренный сердечно-сосудистый риск - значение SCORE от >1 до ≤ 5% <3, 0 ммоль/л (~<115 мг/дл) SCORE = Systematic Coronary Risk Estimation (Шкала систематической оценки коронарного риска) Reiner Z et al. Eur Heart J 2011; 32: 1769– 818
Пересмотр европейских руководств: Рабочая группа по контролю дислипидемии при Европейском Кардиологическом Обществе (ESC) и Европейском Обществе по изучению атеросклероза (EAS) Популяция пациентов Уровни Х-ЛПНП, являющиеся терапевтическими целями Очень высокий сердечно-сосудистый риск - Поставлен диагноз сердечно-сосудистых заболеваний, наличие сахарного диабета типа 2, а также сахарного диабета типа 1 при поражении органов-мишеней, умеренная или тяжелая хроническая почечная недостаточность или уровень SCORE ≥ 10% <1, 8 ммоль/л (~<70 мг/дл) и/или снижение на ≥ 50% при невозможности достижения целевых уровней Высокий сердечно-сосудистый риск - выраженное повышение отдельных факторов риска, значение SCORE от ≥ 5 до <10% <2, 5 ммоль/л (~<100 мг/дл) Умеренный сердечно-сосудистый риск - значение SCORE от >1 до ≤ 5% <3, 0 ммоль/л (~<115 мг/дл) SCORE = Systematic Coronary Risk Estimation (Шкала систематической оценки коронарного риска) Reiner Z et al. Eur Heart J 2011; 32: 1769– 818
 РОССИЙКИЕ РЕКОМЕНДАЦИИ ПО ДИСЛИПИДЕМИЯМ, 2012 год Умеренный риск • Семейный анамнез ИБС, абдоминальное ожирение и др. 1 -2 ФР • SCORE >1% • 3, 0 ммоль/л 115 мг/дл Высокий риск • Ярко выраженный ФР, такой как семейная ГХС и тяжелая АГ • SCORE >5% 2, 5 ммоль/л 100 мг/дл Очень высокий риск ИБС, СД 2 типа, СД 1 типа с ПОМ, ОКС, коронарные вмешательства • SCORE >10% 1, 8 ммоль/л 70 мг/дл Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации, V пересмотр, "Атеросклероз и дислипидемии" 2012; 9: 5 -51
РОССИЙКИЕ РЕКОМЕНДАЦИИ ПО ДИСЛИПИДЕМИЯМ, 2012 год Умеренный риск • Семейный анамнез ИБС, абдоминальное ожирение и др. 1 -2 ФР • SCORE >1% • 3, 0 ммоль/л 115 мг/дл Высокий риск • Ярко выраженный ФР, такой как семейная ГХС и тяжелая АГ • SCORE >5% 2, 5 ммоль/л 100 мг/дл Очень высокий риск ИБС, СД 2 типа, СД 1 типа с ПОМ, ОКС, коронарные вмешательства • SCORE >10% 1, 8 ммоль/л 70 мг/дл Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации, V пересмотр, "Атеросклероз и дислипидемии" 2012; 9: 5 -51
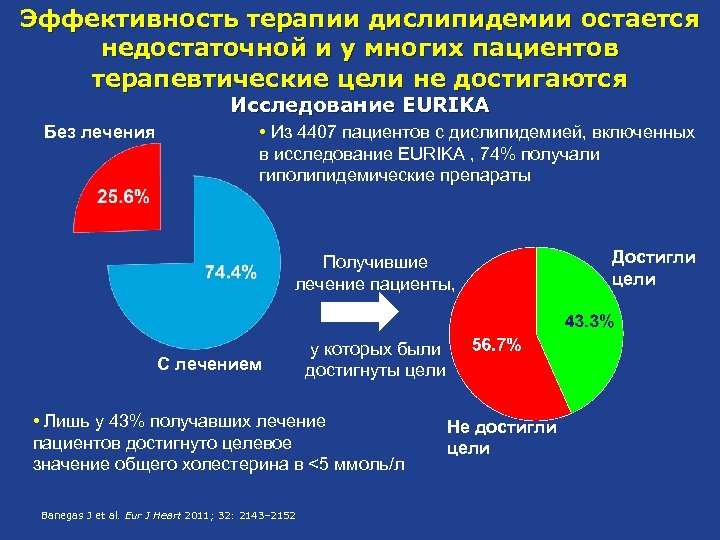 Эффективность терапии дислипидемии остается недостаточной и у многих пациентов терапевтические цели не достигаются Исследование EURIKA Без лечения • Из 4407 пациентов с дислипидемией, включенных в исследование EURIKA , 74% получали гиполипидемические препараты Получившие лечение пациенты, С лечением у которых были достигнуты цели • Лишь у 43% получавших лечение пациентов достигнуто целевое значение общего холестерина в <5 ммоль/л Banegas J et al. Eur J Heart 2011; 32: 2143– 2152 Не достигли цели Достигли цели
Эффективность терапии дислипидемии остается недостаточной и у многих пациентов терапевтические цели не достигаются Исследование EURIKA Без лечения • Из 4407 пациентов с дислипидемией, включенных в исследование EURIKA , 74% получали гиполипидемические препараты Получившие лечение пациенты, С лечением у которых были достигнуты цели • Лишь у 43% получавших лечение пациентов достигнуто целевое значение общего холестерина в <5 ммоль/л Banegas J et al. Eur J Heart 2011; 32: 2143– 2152 Не достигли цели Достигли цели
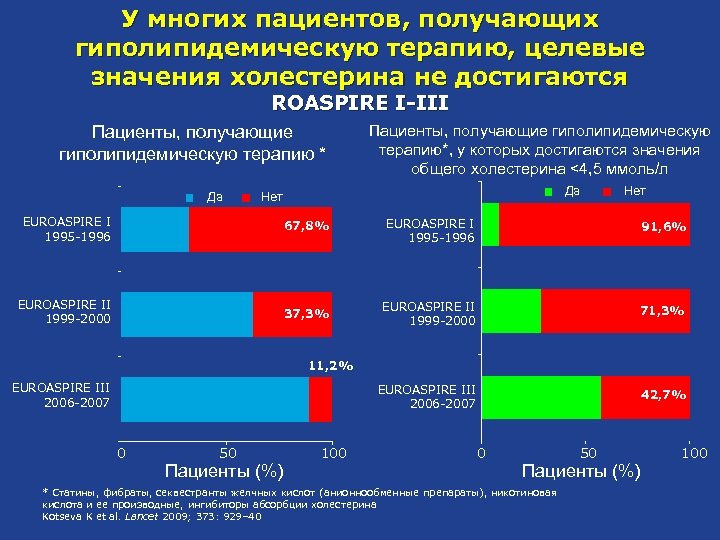 У многих пациентов, получающих гиполипидемическую терапию, целевые значения холестерина не достигаются ROASPIRE I-III Пациенты, получающие гиполипидемическую терапию * Да Пациенты, получающие гиполипидемическую терапию*, у которых достигаются значения общего холестерина <4, 5 ммоль/л Да Нет EUROASPIRE I 1995 -1996 67, 8% EUROASPIRE I 1995 -1996 91, 6% EUROASPIRE II 1999 -2000 37, 3% EUROASPIRE II 1999 -2000 71, 3% EUROASPIRE III 2006 -2007 42, 7% 11, 2% EUROASPIRE III 2006 -2007 0 50 Пациенты (%) 100 0 50 Пациенты (%) * Статины, фибраты, секвестранты желчных кислот (анионнообменные препараты), никотиновая кислота и ее производные, ингибиторы абсорбции холестерина Kotseva K et al. Lancet 2009; 373: 929– 40 100
У многих пациентов, получающих гиполипидемическую терапию, целевые значения холестерина не достигаются ROASPIRE I-III Пациенты, получающие гиполипидемическую терапию * Да Пациенты, получающие гиполипидемическую терапию*, у которых достигаются значения общего холестерина <4, 5 ммоль/л Да Нет EUROASPIRE I 1995 -1996 67, 8% EUROASPIRE I 1995 -1996 91, 6% EUROASPIRE II 1999 -2000 37, 3% EUROASPIRE II 1999 -2000 71, 3% EUROASPIRE III 2006 -2007 42, 7% 11, 2% EUROASPIRE III 2006 -2007 0 50 Пациенты (%) 100 0 50 Пациенты (%) * Статины, фибраты, секвестранты желчных кислот (анионнообменные препараты), никотиновая кислота и ее производные, ингибиторы абсорбции холестерина Kotseva K et al. Lancet 2009; 373: 929– 40 100
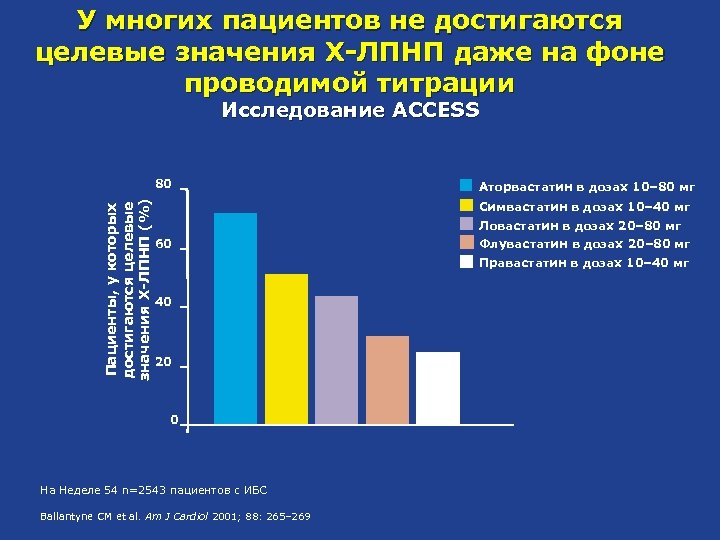 У многих пациентов не достигаются целевые значения Х-ЛПНП даже на фоне проводимой титрации Исследование ACCESS Пациенты, у которых достигаются целевые значения Х-ЛПНП (%) 80 Аторвастатин в дозах 10– 80 мг Симвастатин в дозах 10– 40 мг Ловастатин в дозах 20– 80 мг 60 Флувастатин в дозах 20– 80 мг Правастатин в дозах 10– 40 мг 40 20 0 На Неделе 54 n=2543 пациентов с ИБС Ballantyne CM et al. Am J Cardiol 2001; 88: 265– 269
У многих пациентов не достигаются целевые значения Х-ЛПНП даже на фоне проводимой титрации Исследование ACCESS Пациенты, у которых достигаются целевые значения Х-ЛПНП (%) 80 Аторвастатин в дозах 10– 80 мг Симвастатин в дозах 10– 40 мг Ловастатин в дозах 20– 80 мг 60 Флувастатин в дозах 20– 80 мг Правастатин в дозах 10– 40 мг 40 20 0 На Неделе 54 n=2543 пациентов с ИБС Ballantyne CM et al. Am J Cardiol 2001; 88: 265– 269
 Розувастатин: подход к решению проблемы недостаточной эффективности лечения дислипидемии l Требуется более эффективная терапия, которая позволила бы добиться: – Более выраженных снижений Х-ЛПНП на более низких дозах – Более выраженных снижений Х-ЛПНП во всем диапазоне доз – Достижения целевых значений Х-ЛПНП согласно руководствам, при очередных пересмотрах которых эти показатели становятся все более низкими
Розувастатин: подход к решению проблемы недостаточной эффективности лечения дислипидемии l Требуется более эффективная терапия, которая позволила бы добиться: – Более выраженных снижений Х-ЛПНП на более низких дозах – Более выраженных снижений Х-ЛПНП во всем диапазоне доз – Достижения целевых значений Х-ЛПНП согласно руководствам, при очередных пересмотрах которых эти показатели становятся все более низкими
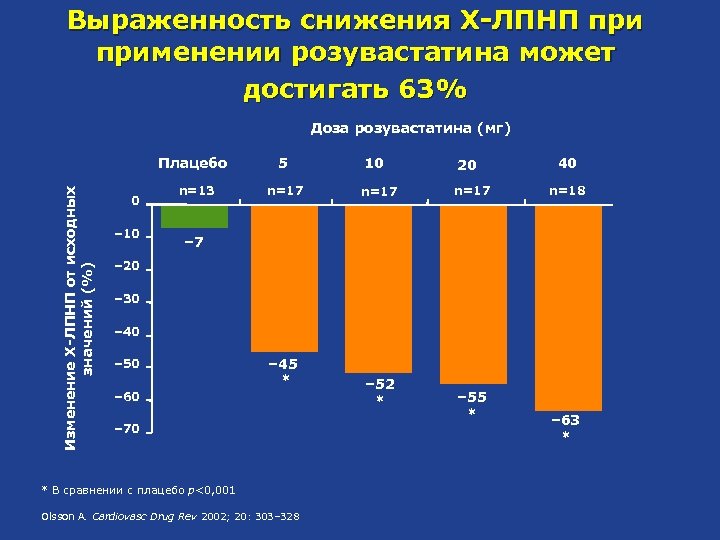 Выраженность снижения Х-ЛПНП применении розувастатина может достигать 63% Доза розувастатина (мг) Изменение Х-ЛПНП от исходных значений (%) Плацебо 0 – 10 n=13 5 n=17 10 20 n=17 40 n=18 – 7 – 20 – 30 – 40 – 50 – 45 * – 60 – 70 * В сравнении с плацебо p<0, 001 Olsson A. Cardiovasc Drug Rev 2002; 20: 303– 328 – 52 * – 55 * – 63 *
Выраженность снижения Х-ЛПНП применении розувастатина может достигать 63% Доза розувастатина (мг) Изменение Х-ЛПНП от исходных значений (%) Плацебо 0 – 10 n=13 5 n=17 10 20 n=17 40 n=18 – 7 – 20 – 30 – 40 – 50 – 45 * – 60 – 70 * В сравнении с плацебо p<0, 001 Olsson A. Cardiovasc Drug Rev 2002; 20: 303– 328 – 52 * – 55 * – 63 *
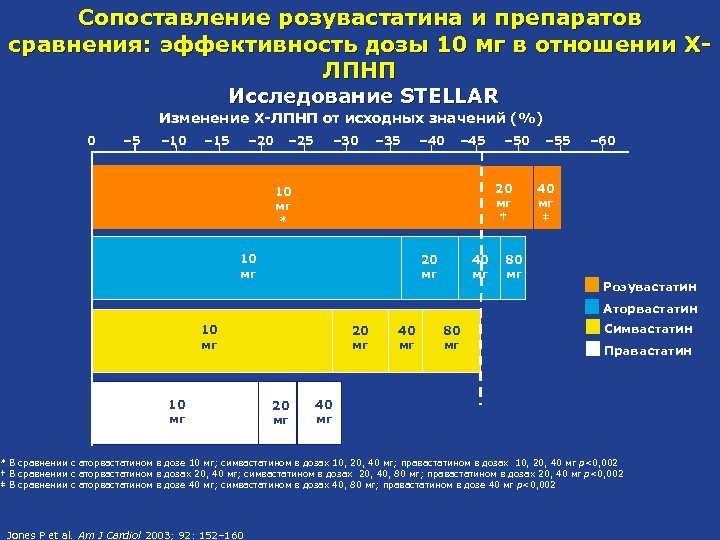 Сопоставление розувастатина и препаратов сравнения: эффективность дозы 10 мг в отношении ХЛПНП Исследование STELLAR Изменение Х-ЛПНП от исходных значений (%) 0 – 5 – 10 – 15 – 20 – 25 – 30 – 35 – 40 – 45 – 50 20 мг † 10 мг * 10 мг 20 мг 40 мг 80 мг – 55 – 60 40 мг ‡ Розувастатин Аторвастатин 10 мг 20 мг 40 мг 80 мг Симвастатин Правастатин 40 мг * В сравнении с аторвастатином в дозе 10 мг; симвастатином в дозах 10, 20, 40 мг; правастатином в дозах 10, 20, 40 мг p<0, 002 † В сравнении с аторвастатином в дозах 20, 40 мг; симвастатином в дозах 20, 40, 80 мг; правастатином в дозах 20, 40 мг p<0, 002 ‡ В сравнении с аторвастатином в дозе 40 мг; симвастатином в дозах 40, 80 мг; правастатином в дозе 40 мг p<0, 002 Jones P et al. Am J Cardiol 2003; 92: 152– 160
Сопоставление розувастатина и препаратов сравнения: эффективность дозы 10 мг в отношении ХЛПНП Исследование STELLAR Изменение Х-ЛПНП от исходных значений (%) 0 – 5 – 10 – 15 – 20 – 25 – 30 – 35 – 40 – 45 – 50 20 мг † 10 мг * 10 мг 20 мг 40 мг 80 мг – 55 – 60 40 мг ‡ Розувастатин Аторвастатин 10 мг 20 мг 40 мг 80 мг Симвастатин Правастатин 40 мг * В сравнении с аторвастатином в дозе 10 мг; симвастатином в дозах 10, 20, 40 мг; правастатином в дозах 10, 20, 40 мг p<0, 002 † В сравнении с аторвастатином в дозах 20, 40 мг; симвастатином в дозах 20, 40, 80 мг; правастатином в дозах 20, 40 мг p<0, 002 ‡ В сравнении с аторвастатином в дозе 40 мг; симвастатином в дозах 40, 80 мг; правастатином в дозе 40 мг p<0, 002 Jones P et al. Am J Cardiol 2003; 92: 152– 160
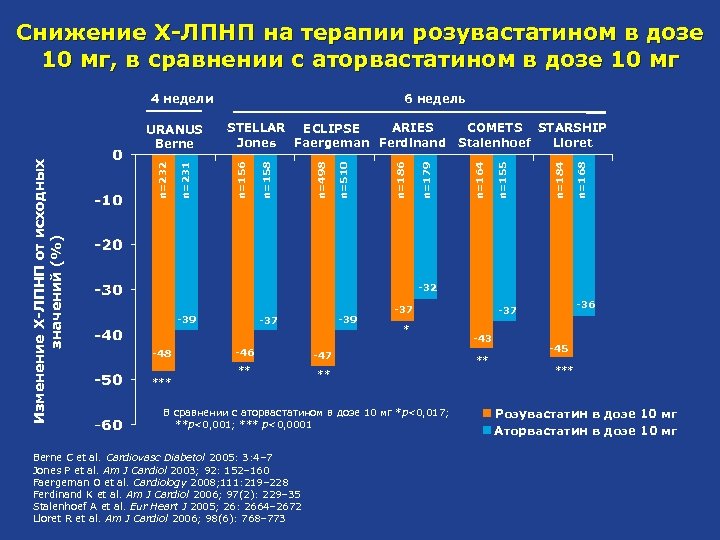 Снижение Х-ЛПНП на терапии розувастатином в дозе 10 мг, в сравнении с аторвастатином в дозе 10 мг 6 недель 4 недели n=168 n=184 n=155 n=164 n=179 n=186 n=510 n=498 n=158 STELLAR ECLIPSE ARIES COMETS STARSHIP Jones Lloret Faergeman Ferdinand Stalenhoef n=156 n=231 n=232 Изменение Х-ЛПНП от исходных значений (%) URANUS Berne -32 -39 -48 *** -39 -37 -46 * -47 ** -37 ** В сравнении с аторвастатином в дозе 10 мг *p<0, 017; **p<0, 001; *** p<0, 0001 Berne C et al. Cardiovasc Diabetol 2005: 3: 4– 7 Jones P et al. Am J Cardiol 2003; 92: 152– 160 Faergeman O et al. Cardiology 2008; 111: 219– 228 Ferdinand K et al. Am J Cardiol 2006; 97(2): 229– 35 Stalenhoef A et al. Eur Heart J 2005; 26: 2664– 2672 Lloret R et al. Am J Cardiol 2006; 98(6): 768– 773 -36 -37 -43 ** -45 *** Розувастатин в дозе 10 мг Аторвастатин в дозе 10 мг
Снижение Х-ЛПНП на терапии розувастатином в дозе 10 мг, в сравнении с аторвастатином в дозе 10 мг 6 недель 4 недели n=168 n=184 n=155 n=164 n=179 n=186 n=510 n=498 n=158 STELLAR ECLIPSE ARIES COMETS STARSHIP Jones Lloret Faergeman Ferdinand Stalenhoef n=156 n=231 n=232 Изменение Х-ЛПНП от исходных значений (%) URANUS Berne -32 -39 -48 *** -39 -37 -46 * -47 ** -37 ** В сравнении с аторвастатином в дозе 10 мг *p<0, 017; **p<0, 001; *** p<0, 0001 Berne C et al. Cardiovasc Diabetol 2005: 3: 4– 7 Jones P et al. Am J Cardiol 2003; 92: 152– 160 Faergeman O et al. Cardiology 2008; 111: 219– 228 Ferdinand K et al. Am J Cardiol 2006; 97(2): 229– 35 Stalenhoef A et al. Eur Heart J 2005; 26: 2664– 2672 Lloret R et al. Am J Cardiol 2006; 98(6): 768– 773 -36 -37 -43 ** -45 *** Розувастатин в дозе 10 мг Аторвастатин в дозе 10 мг
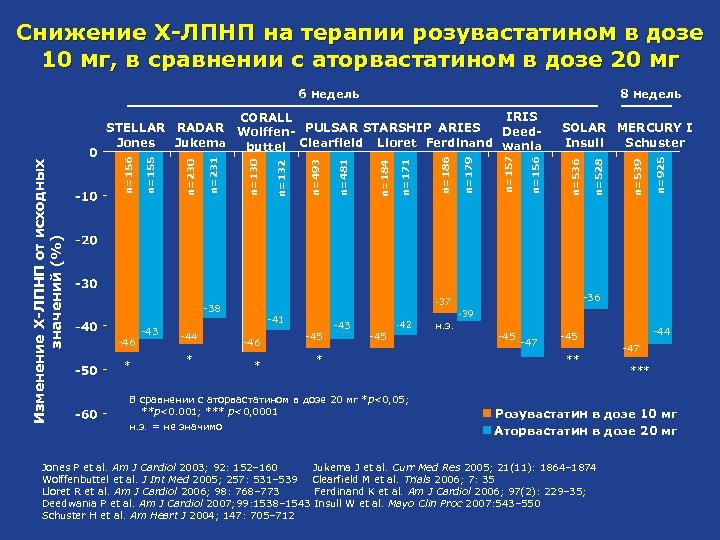 Снижение Х-ЛПНП на терапии розувастатином в дозе 10 мг, в сравнении с аторвастатином в дозе 20 мг 6 недель 8 недель * -43 -44 * -46 * n=925 n=539 n=528 n=536 n=157 n=186 n=171 n=184 n=481 n=493 n=179 -36 -39 -41 -45 -43 -42 -45 * В сравнении с аторвастатином в дозе 20 мг *p<0, 05; **p<0. 001; *** p<0, 0001 н. з. = не значимо SOLAR MERCURY I Insull Schuster -37 -38 -46 n=132 n=130 n=231 n=230 n=155 n=156 Изменение Х-ЛПНП от исходных значений (%) IRIS CORALL STELLAR RADAR Wolffen- PULSAR STARSHIP ARIES Deed. Jones Jukema buttel Clearfield Lloret Ferdinand wania н. з. -45 -47 -45 ** -44 -47 *** Розувастатин в дозе 10 мг Аторвастатин в дозе 20 мг Jones P et al. Am J Cardiol 2003; 92: 152– 160 Jukema J et al. Curr Med Res 2005; 21(11): 1864– 1874 Wolffenbuttel et al. J Int Med 2005; 257: 531– 539 Clearfield M et al. Trials 2006; 7: 35 Lloret R et al. Am J Cardiol 2006; 98: 768– 773 Ferdinand K et al. Am J Cardiol 2006; 97(2): 229– 35; Deedwania P et al. Am J Cardiol 2007; 99: 1538– 1543 Insull W et al. Mayo Clin Proc 2007: 543– 550 Schuster H et al. Am Heart J 2004; 147: 705– 712
Снижение Х-ЛПНП на терапии розувастатином в дозе 10 мг, в сравнении с аторвастатином в дозе 20 мг 6 недель 8 недель * -43 -44 * -46 * n=925 n=539 n=528 n=536 n=157 n=186 n=171 n=184 n=481 n=493 n=179 -36 -39 -41 -45 -43 -42 -45 * В сравнении с аторвастатином в дозе 20 мг *p<0, 05; **p<0. 001; *** p<0, 0001 н. з. = не значимо SOLAR MERCURY I Insull Schuster -37 -38 -46 n=132 n=130 n=231 n=230 n=155 n=156 Изменение Х-ЛПНП от исходных значений (%) IRIS CORALL STELLAR RADAR Wolffen- PULSAR STARSHIP ARIES Deed. Jones Jukema buttel Clearfield Lloret Ferdinand wania н. з. -45 -47 -45 ** -44 -47 *** Розувастатин в дозе 10 мг Аторвастатин в дозе 20 мг Jones P et al. Am J Cardiol 2003; 92: 152– 160 Jukema J et al. Curr Med Res 2005; 21(11): 1864– 1874 Wolffenbuttel et al. J Int Med 2005; 257: 531– 539 Clearfield M et al. Trials 2006; 7: 35 Lloret R et al. Am J Cardiol 2006; 98: 768– 773 Ferdinand K et al. Am J Cardiol 2006; 97(2): 229– 35; Deedwania P et al. Am J Cardiol 2007; 99: 1538– 1543 Insull W et al. Mayo Clin Proc 2007: 543– 550 Schuster H et al. Am Heart J 2004; 147: 705– 712
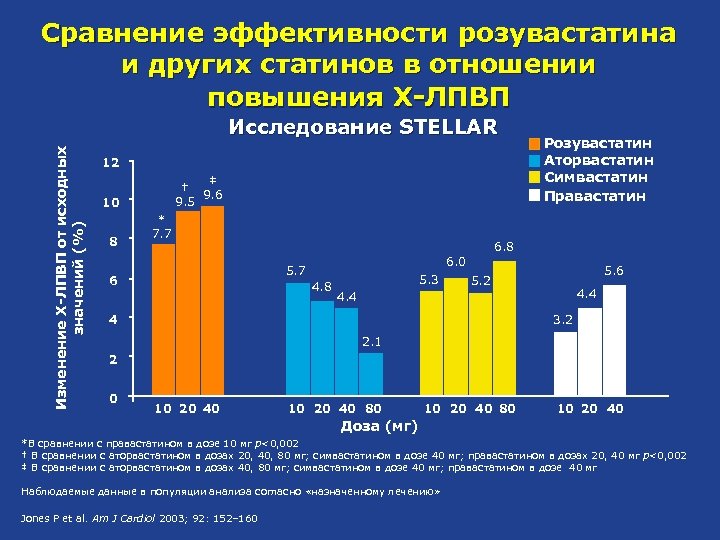 Сравнение эффективности розувастатина и других статинов в отношении повышения Х-ЛПВП Изменение Х-ЛПВП от исходных значений (%) Исследование STELLAR 12 ‡ † 9. 6 9. 5 10 8 * 7. 7 6. 8 6. 0 5. 7 6 Розувастатин Аторвастатин Симвастатин Правастатин 4. 8 5. 3 5. 6 5. 2 4. 4 4 3. 2 2. 1 2 0 10 20 40 80 10 20 40 Доза (мг) *В сравнении с правастатином в дозе 10 мг p<0, 002 † В сравнении с аторвастатином в дозах 20, 40, 80 мг; симвастатином в дозе 40 мг; правастатином в дозах 20, 40 мг p<0, 002 ‡ В сравнении с аторвастатином в дозах 40, 80 мг; симвастатином в дозе 40 мг; правастатином в дозе 40 мг Наблюдаемые данные в популяции анализа согласно «назначенному лечению» Jones P et al. Am J Cardiol 2003; 92: 152– 160
Сравнение эффективности розувастатина и других статинов в отношении повышения Х-ЛПВП Изменение Х-ЛПВП от исходных значений (%) Исследование STELLAR 12 ‡ † 9. 6 9. 5 10 8 * 7. 7 6. 8 6. 0 5. 7 6 Розувастатин Аторвастатин Симвастатин Правастатин 4. 8 5. 3 5. 6 5. 2 4. 4 4 3. 2 2. 1 2 0 10 20 40 80 10 20 40 Доза (мг) *В сравнении с правастатином в дозе 10 мг p<0, 002 † В сравнении с аторвастатином в дозах 20, 40, 80 мг; симвастатином в дозе 40 мг; правастатином в дозах 20, 40 мг p<0, 002 ‡ В сравнении с аторвастатином в дозах 40, 80 мг; симвастатином в дозе 40 мг; правастатином в дозе 40 мг Наблюдаемые данные в популяции анализа согласно «назначенному лечению» Jones P et al. Am J Cardiol 2003; 92: 152– 160
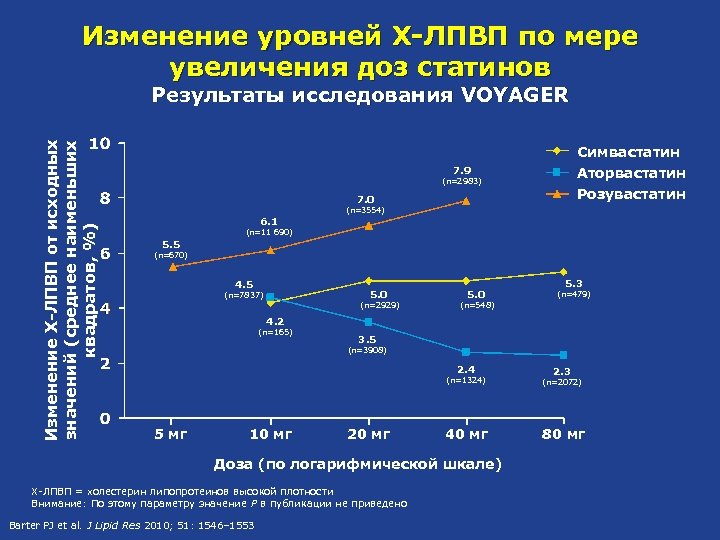 Изменение уровней Х-ЛПВП по мере увеличения доз статинов Изменение Х-ЛПВП от исходных значений (среднее наименьших квадратов, %) Результаты исследования VOYAGER Симвастатин Аторвастатин Розувастатин 7. 9 (n=2983) 7. 0 (n=3554) 6. 1 (n=11 690) 5. 5 (n=670) 4. 5 5. 0 (n=7837) (n=2929) 5. 0 5. 3 (n=479) (n=548) 4. 2 (n=165) 3. 5 (n=3908) 2. 4 2. 3 (n=1324) 5 мг 10 мг 20 мг (n=2072) 40 мг 80 мг Доза (по логарифмической шкале) Х-ЛПВП = холестерин липопротеинов высокой плотности Внимание: По этому параметру значение P в публикации не приведено Barter PJ et al. J Lipid Res 2010; 51: 1546– 1553
Изменение уровней Х-ЛПВП по мере увеличения доз статинов Изменение Х-ЛПВП от исходных значений (среднее наименьших квадратов, %) Результаты исследования VOYAGER Симвастатин Аторвастатин Розувастатин 7. 9 (n=2983) 7. 0 (n=3554) 6. 1 (n=11 690) 5. 5 (n=670) 4. 5 5. 0 (n=7837) (n=2929) 5. 0 5. 3 (n=479) (n=548) 4. 2 (n=165) 3. 5 (n=3908) 2. 4 2. 3 (n=1324) 5 мг 10 мг 20 мг (n=2072) 40 мг 80 мг Доза (по логарифмической шкале) Х-ЛПВП = холестерин липопротеинов высокой плотности Внимание: По этому параметру значение P в публикации не приведено Barter PJ et al. J Lipid Res 2010; 51: 1546– 1553
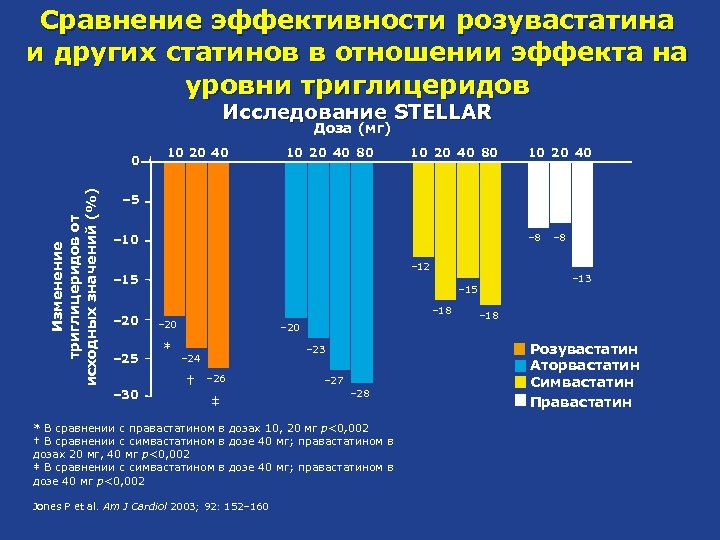 Сравнение эффективности розувастатина и других статинов в отношении эффекта на уровни триглицеридов Исследование STELLAR Доза (мг) Изменение триглицеридов от исходных значений (%) 0 10 20 40 80 10 20 40 – 5 – 8 – 10 – 12 – 15 – 20 – 25 – 30 – 13 – 15 – 18 – 20 * – 8 – 18 – 20 – 23 – 24 † – 26 ‡ – 27 – 28 * В сравнении с правастатином в дозах 10, 20 мг p<0, 002 † В сравнении с симвастатином в дозе 40 мг; правастатином в дозах 20 мг, 40 мг p<0, 002 ‡ В сравнении с симвастатином в дозе 40 мг; правастатином в дозе 40 мг p<0, 002 Jones P et al. Am J Cardiol 2003; 92: 152– 160 Розувастатин Аторвастатин Симвастатин Правастатин
Сравнение эффективности розувастатина и других статинов в отношении эффекта на уровни триглицеридов Исследование STELLAR Доза (мг) Изменение триглицеридов от исходных значений (%) 0 10 20 40 80 10 20 40 – 5 – 8 – 10 – 12 – 15 – 20 – 25 – 30 – 13 – 15 – 18 – 20 * – 8 – 18 – 20 – 23 – 24 † – 26 ‡ – 27 – 28 * В сравнении с правастатином в дозах 10, 20 мг p<0, 002 † В сравнении с симвастатином в дозе 40 мг; правастатином в дозах 20 мг, 40 мг p<0, 002 ‡ В сравнении с симвастатином в дозе 40 мг; правастатином в дозе 40 мг p<0, 002 Jones P et al. Am J Cardiol 2003; 92: 152– 160 Розувастатин Аторвастатин Симвастатин Правастатин
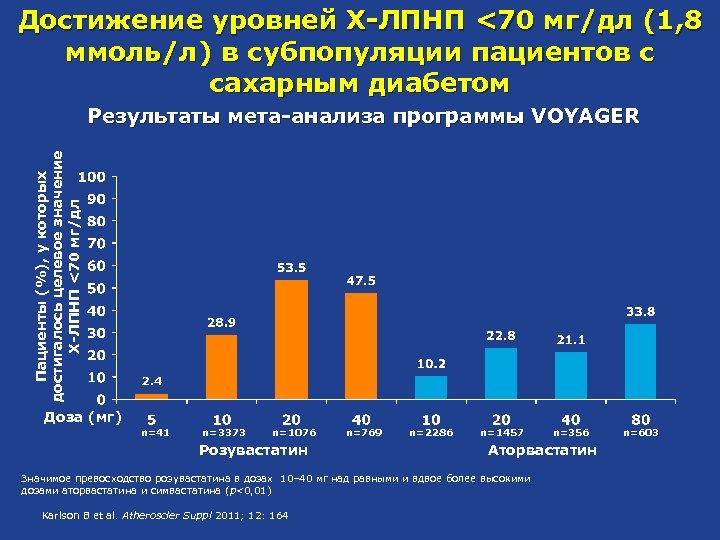 Достижение уровней Х-ЛПНП <70 мг/дл (1, 8 ммоль/л) в субпопуляции пациентов с сахарным диабетом Пациенты (%), у которых достигалось целевое значение Х-ЛПНП <70 мг/дл Результаты мета-анализа программы VOYAGER Доза (мг) n=41 n=3373 n=1076 Розувастатин n=769 n=2286 n=1457 Аторвастатин Значимое превосходство розувастатина в дозах 10‒ 40 мг над равными и вдвое более высокими дозами аторвастатина и симвастатина (p<0, 01) Karlson B et al. Atheroscler Suppl 2011; 12: 164 n=356 n=603
Достижение уровней Х-ЛПНП <70 мг/дл (1, 8 ммоль/л) в субпопуляции пациентов с сахарным диабетом Пациенты (%), у которых достигалось целевое значение Х-ЛПНП <70 мг/дл Результаты мета-анализа программы VOYAGER Доза (мг) n=41 n=3373 n=1076 Розувастатин n=769 n=2286 n=1457 Аторвастатин Значимое превосходство розувастатина в дозах 10‒ 40 мг над равными и вдвое более высокими дозами аторвастатина и симвастатина (p<0, 01) Karlson B et al. Atheroscler Suppl 2011; 12: 164 n=356 n=603
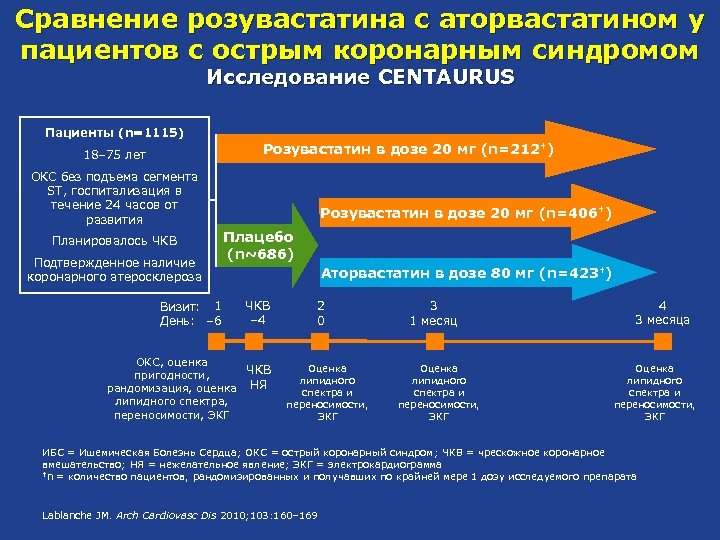 Сравнение розувастатина с аторвастатином у пациентов с острым коронарным синдромом Исследование CENTAURUS Пациенты (n=1115) Розувастатин в дозе 20 мг (n=212†) 18– 75 лет ОКС без подъема сегмента ST, госпитализация в течение 24 часов от развития Планировалось ЧКВ Подтвержденное наличие коронарного атеросклероза Визит: 1 День: – 6 Розувастатин в дозе 20 мг (n=406†) Плацебо (n~686) Аторвастатин в дозе 80 мг (n=423†) ЧКВ – 4 ОКС, оценка ЧКВ пригодности, рандомизация, оценка НЯ липидного спектра, переносимости, ЭКГ 2 0 Оценка липидного спектра и переносимости, ЭКГ 3 1 месяц Оценка липидного спектра и переносимости, ЭКГ 4 3 месяца Оценка липидного спектра и переносимости, ЭКГ ИБС = Ишемическая Болезнь Сердца; ОКС = острый коронарный синдром; ЧКВ = чрескожное коронарное вмешательство; НЯ = нежелательное явление; ЭКГ = электрокардиограмма †n = количество пациентов, рандомизированных и получавших по крайней мере 1 дозу исследуемого препарата Lablanche JM. Arch Cardiovasc Dis 2010; 103: 160‒ 169
Сравнение розувастатина с аторвастатином у пациентов с острым коронарным синдромом Исследование CENTAURUS Пациенты (n=1115) Розувастатин в дозе 20 мг (n=212†) 18– 75 лет ОКС без подъема сегмента ST, госпитализация в течение 24 часов от развития Планировалось ЧКВ Подтвержденное наличие коронарного атеросклероза Визит: 1 День: – 6 Розувастатин в дозе 20 мг (n=406†) Плацебо (n~686) Аторвастатин в дозе 80 мг (n=423†) ЧКВ – 4 ОКС, оценка ЧКВ пригодности, рандомизация, оценка НЯ липидного спектра, переносимости, ЭКГ 2 0 Оценка липидного спектра и переносимости, ЭКГ 3 1 месяц Оценка липидного спектра и переносимости, ЭКГ 4 3 месяца Оценка липидного спектра и переносимости, ЭКГ ИБС = Ишемическая Болезнь Сердца; ОКС = острый коронарный синдром; ЧКВ = чрескожное коронарное вмешательство; НЯ = нежелательное явление; ЭКГ = электрокардиограмма †n = количество пациентов, рандомизированных и получавших по крайней мере 1 дозу исследуемого препарата Lablanche JM. Arch Cardiovasc Dis 2010; 103: 160‒ 169
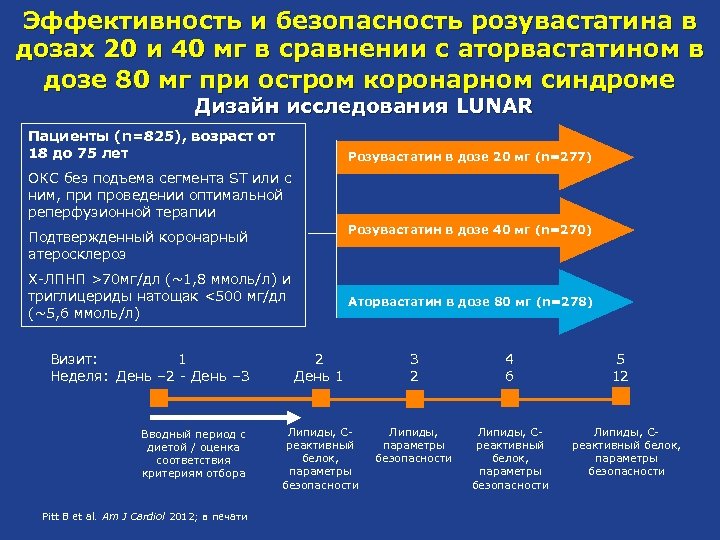 Эффективность и безопасность розувастатина в дозах 20 и 40 мг в сравнении с аторвастатином в дозе 80 мг при остром коронарном синдроме Дизайн исследования LUNAR Пациенты (n=825), возраст от 18 до 75 лет Розувастатин в дозе 20 мг (n=277) ОКС без подъема сегмента ST или с ним, при проведении оптимальной реперфузионной терапии Розувастатин в дозе 40 мг (n=270) Подтвержденный коронарный атеросклероз Х-ЛПНП >70 мг/дл (~1, 8 ммоль/л) и триглицериды натощак <500 мг/дл (~5, 6 ммоль/л) Визит: 1 Неделя: День – 2 - День – 3 Вводный период с диетой / оценка соответствия критериям отбора Pitt B et al. Am J Cardiol 2012; в печати Аторвастатин в дозе 80 мг (n=278) 2 День 1 3 2 4 6 Липиды, Cреактивный белок, параметры безопасности 5 12 Липиды, Cреактивный белок, параметры безопасности
Эффективность и безопасность розувастатина в дозах 20 и 40 мг в сравнении с аторвастатином в дозе 80 мг при остром коронарном синдроме Дизайн исследования LUNAR Пациенты (n=825), возраст от 18 до 75 лет Розувастатин в дозе 20 мг (n=277) ОКС без подъема сегмента ST или с ним, при проведении оптимальной реперфузионной терапии Розувастатин в дозе 40 мг (n=270) Подтвержденный коронарный атеросклероз Х-ЛПНП >70 мг/дл (~1, 8 ммоль/л) и триглицериды натощак <500 мг/дл (~5, 6 ммоль/л) Визит: 1 Неделя: День – 2 - День – 3 Вводный период с диетой / оценка соответствия критериям отбора Pitt B et al. Am J Cardiol 2012; в печати Аторвастатин в дозе 80 мг (n=278) 2 День 1 3 2 4 6 Липиды, Cреактивный белок, параметры безопасности 5 12 Липиды, Cреактивный белок, параметры безопасности
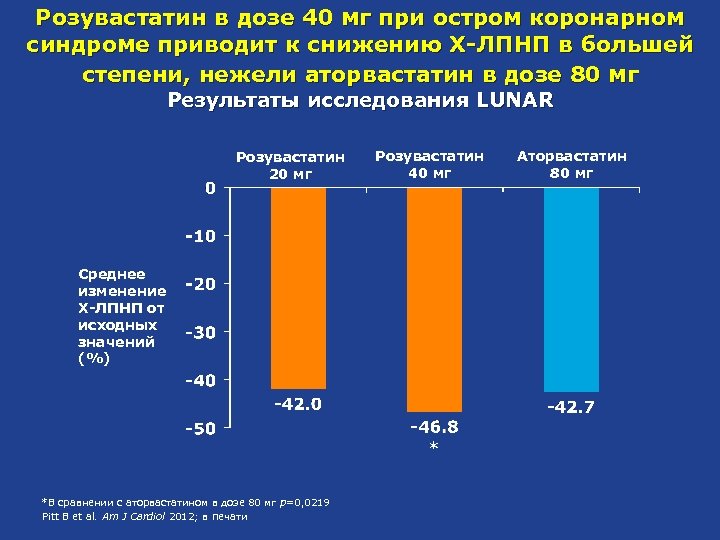 Розувастатин в дозе 40 мг при остром коронарном синдроме приводит к снижению Х-ЛПНП в большей степени, нежели аторвастатин в дозе 80 мг Результаты исследования LUNAR Розувастатин 20 мг Розувастатин 40 мг Среднее изменение Х-ЛПНП от исходных значений (%) * *В сравнении с аторвастатином в дозе 80 мг p=0, 0219 Pitt B et al. Am J Cardiol 2012; в печати Аторвастатин 80 мг
Розувастатин в дозе 40 мг при остром коронарном синдроме приводит к снижению Х-ЛПНП в большей степени, нежели аторвастатин в дозе 80 мг Результаты исследования LUNAR Розувастатин 20 мг Розувастатин 40 мг Среднее изменение Х-ЛПНП от исходных значений (%) * *В сравнении с аторвастатином в дозе 80 мг p=0, 0219 Pitt B et al. Am J Cardiol 2012; в печати Аторвастатин 80 мг
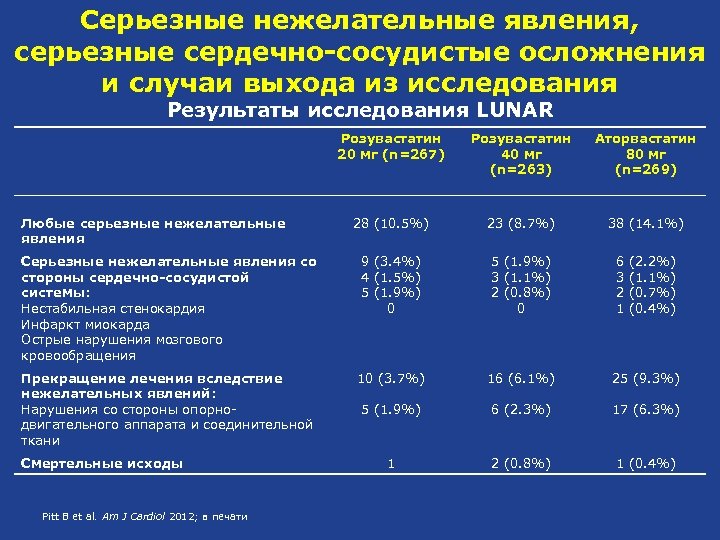 Серьезные нежелательные явления, серьезные сердечно-сосудистые осложнения и случаи выхода из исследования Результаты исследования LUNAR Розувастатин 20 мг (n=267) Розувастатин 40 мг (n=263) Аторвастатин 80 мг (n=269) 28 (10. 5%) 23 (8. 7%) 38 (14. 1%) Серьезные нежелательные явления со стороны сердечно-сосудистой системы: Нестабильная стенокардия Инфаркт миокарда Острые нарушения мозгового кровообращения 9 (3. 4%) 4 (1. 5%) 5 (1. 9%) 0 5 (1. 9%) 3 (1. 1%) 2 (0. 8%) 0 Прекращение лечения вследствие нежелательных явлений: Нарушения со стороны опорнодвигательного аппарата и соединительной ткани 10 (3. 7%) 16 (6. 1%) 25 (9. 3%) 5 (1. 9%) 6 (2. 3%) 17 (6. 3%) 1 2 (0. 8%) 1 (0. 4%) Любые серьезные нежелательные явления Смертельные исходы Pitt B et al. Am J Cardiol 2012; в печати 6 3 2 1 (2. 2%) (1. 1%) (0. 7%) (0. 4%)
Серьезные нежелательные явления, серьезные сердечно-сосудистые осложнения и случаи выхода из исследования Результаты исследования LUNAR Розувастатин 20 мг (n=267) Розувастатин 40 мг (n=263) Аторвастатин 80 мг (n=269) 28 (10. 5%) 23 (8. 7%) 38 (14. 1%) Серьезные нежелательные явления со стороны сердечно-сосудистой системы: Нестабильная стенокардия Инфаркт миокарда Острые нарушения мозгового кровообращения 9 (3. 4%) 4 (1. 5%) 5 (1. 9%) 0 5 (1. 9%) 3 (1. 1%) 2 (0. 8%) 0 Прекращение лечения вследствие нежелательных явлений: Нарушения со стороны опорнодвигательного аппарата и соединительной ткани 10 (3. 7%) 16 (6. 1%) 25 (9. 3%) 5 (1. 9%) 6 (2. 3%) 17 (6. 3%) 1 2 (0. 8%) 1 (0. 4%) Любые серьезные нежелательные явления Смертельные исходы Pitt B et al. Am J Cardiol 2012; в печати 6 3 2 1 (2. 2%) (1. 1%) (0. 7%) (0. 4%)
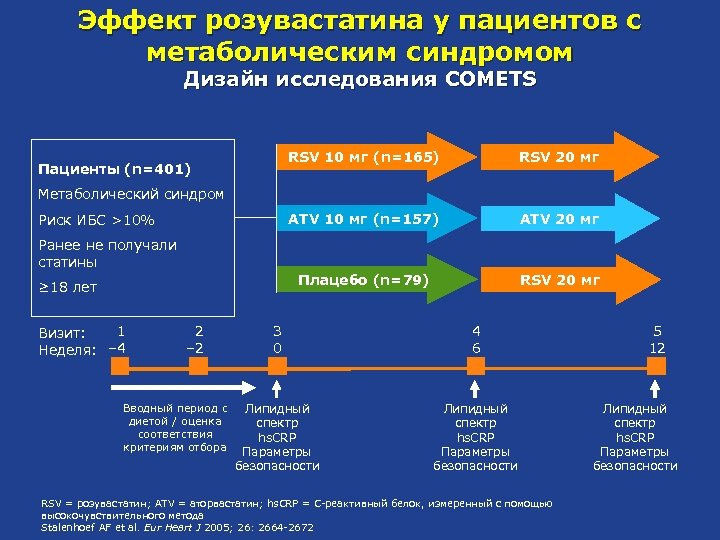 Эффект розувастатина у пациентов с метаболическим синдромом Дизайн исследования COMETS RSV 10 мг (n=165) RSV 20 мг ATV 10 мг (n=157) ATV 20 мг Плацебо (n=79) Пациенты (n=401) RSV 20 мг Метаболический синдром Риск ИБС >10% Ранее не получали статины ≥ 18 лет 1 Визит: Неделя: – 4 2 – 2 Вводный период с диетой / оценка соответствия критериям отбора 3 0 4 6 Липидный спектр hs. CRP Параметры безопасности RSV = розувастатин; ATV = аторвастатин; hs. CRP = C-реактивный белок, измеренный с помощью высокочувствительного метода Stalenhoef AF et al. Eur Heart J 2005; 26: 2664 -2672 5 12 Липидный спектр hs. CRP Параметры безопасности
Эффект розувастатина у пациентов с метаболическим синдромом Дизайн исследования COMETS RSV 10 мг (n=165) RSV 20 мг ATV 10 мг (n=157) ATV 20 мг Плацебо (n=79) Пациенты (n=401) RSV 20 мг Метаболический синдром Риск ИБС >10% Ранее не получали статины ≥ 18 лет 1 Визит: Неделя: – 4 2 – 2 Вводный период с диетой / оценка соответствия критериям отбора 3 0 4 6 Липидный спектр hs. CRP Параметры безопасности RSV = розувастатин; ATV = аторвастатин; hs. CRP = C-реактивный белок, измеренный с помощью высокочувствительного метода Stalenhoef AF et al. Eur Heart J 2005; 26: 2664 -2672 5 12 Липидный спектр hs. CRP Параметры безопасности
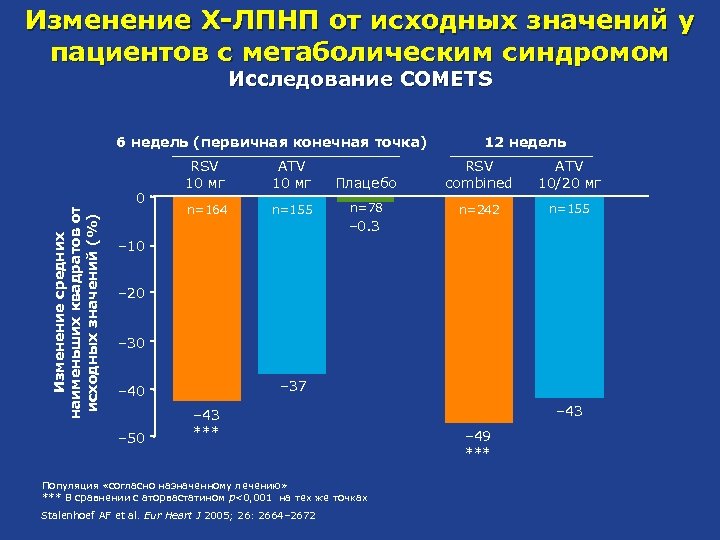 Изменение Х-ЛПНП от исходных значений у пациентов с метаболическим синдромом Исследование COMETS Изменение средних наименьших квадратов от исходных значений (%) 6 недель (первичная конечная точка) 0 RSV 10 мг ATV 10 мг n=164 n=155 12 недель Плацебо RSV combined ATV 10/20 мг n=78 n=242 n=155 – 0. 3 – 10 – 20 – 37 – 40 – 50 – 43 *** Популяция «согласно назначенному лечению» *** В сравнении с аторвастатином p<0, 001 на тех же точках Stalenhoef AF et al. Eur Heart J 2005; 26: 2664– 2672 – 43 – 49 ***
Изменение Х-ЛПНП от исходных значений у пациентов с метаболическим синдромом Исследование COMETS Изменение средних наименьших квадратов от исходных значений (%) 6 недель (первичная конечная точка) 0 RSV 10 мг ATV 10 мг n=164 n=155 12 недель Плацебо RSV combined ATV 10/20 мг n=78 n=242 n=155 – 0. 3 – 10 – 20 – 37 – 40 – 50 – 43 *** Популяция «согласно назначенному лечению» *** В сравнении с аторвастатином p<0, 001 на тех же точках Stalenhoef AF et al. Eur Heart J 2005; 26: 2664– 2672 – 43 – 49 ***
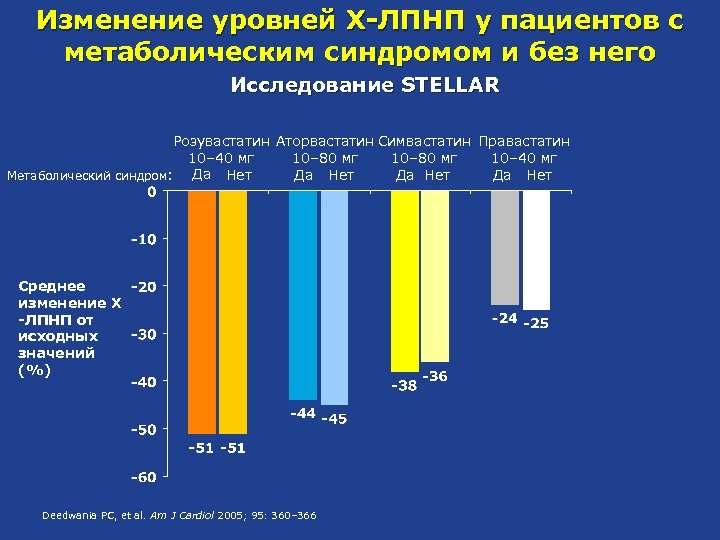 Изменение уровней Х-ЛПНП у пациентов с метаболическим синдромом и без него Исследование STELLAR Розувастатин Аторвастатин Симвастатин Правастатин 10– 40 мг 10– 80 мг 10– 40 мг Да Нет Метаболический синдром: Да Нет Среднее изменение Х -ЛПНП от исходных значений (%) Deedwania PC, et al. Am J Cardiol 2005; 95: 360– 366
Изменение уровней Х-ЛПНП у пациентов с метаболическим синдромом и без него Исследование STELLAR Розувастатин Аторвастатин Симвастатин Правастатин 10– 40 мг 10– 80 мг 10– 40 мг Да Нет Метаболический синдром: Да Нет Среднее изменение Х -ЛПНП от исходных значений (%) Deedwania PC, et al. Am J Cardiol 2005; 95: 360– 366
 Розувастатин Применение в составе комбинированной терапии с эзетимибом
Розувастатин Применение в составе комбинированной терапии с эзетимибом
 Комбинация розувастатина в дозе 40 мг и эзетимиба в дозе 10 мг – снижение Х-ЛПНП на 70% к 6 неделям Исследование EXPLORER Не значимо Среднее изменение от исходных значений (%) 20 10 0 Х-ЛПНП n=230 n=235 -10 8. 5% n=230 10. 8% n=235 Х-ЛПВП -20 -30 -40 -50 -60 -70 Розувастатин в дозе 40 мг -57. 1% -69. 8% * * В сравнении с розувастатином p<0, 05 Ballantyne C et al. Am J Cardiol 2007; 99: 673– 680 Розувастатин в дозе 40 мг / эзетимиб в дозе 10 мг
Комбинация розувастатина в дозе 40 мг и эзетимиба в дозе 10 мг – снижение Х-ЛПНП на 70% к 6 неделям Исследование EXPLORER Не значимо Среднее изменение от исходных значений (%) 20 10 0 Х-ЛПНП n=230 n=235 -10 8. 5% n=230 10. 8% n=235 Х-ЛПВП -20 -30 -40 -50 -60 -70 Розувастатин в дозе 40 мг -57. 1% -69. 8% * * В сравнении с розувастатином p<0, 05 Ballantyne C et al. Am J Cardiol 2007; 99: 673– 680 Розувастатин в дозе 40 мг / эзетимиб в дозе 10 мг
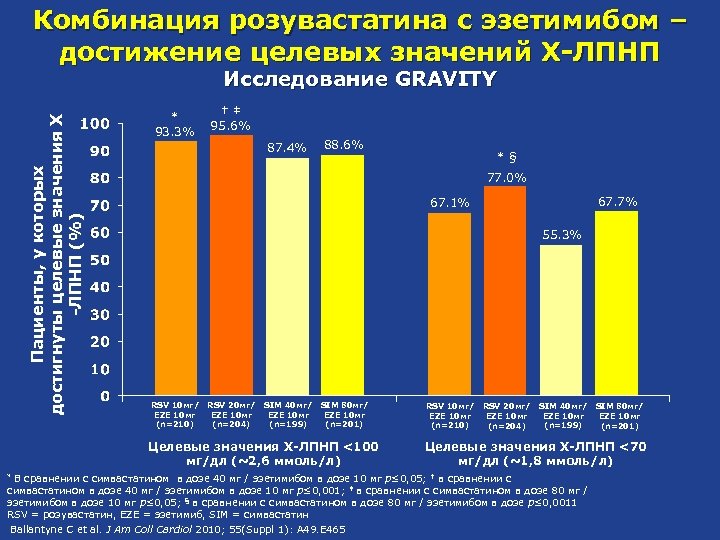 Комбинация розувастатина с эзетимибом – достижение целевых значений Х-ЛПНП Пациенты, у которых достигнуты целевые значения Х -ЛПНП (%) Исследование GRAVITY * 93. 3% †‡ 95. 6% 87. 4% 88. 6% *§ 77. 0% 67. 7% 67. 1% 55. 3% RSV 10 мг/ EZE 10 мг (n=210) RSV 20 мг/ EZE 10 мг (n=204) SIM 40 мг/ EZE 10 мг (n=199) SIM 80 мг/ EZE 10 мг (n=201) Целевые значения Х-ЛПНП <100 мг/дл (~2, 6 ммоль/л) RSV 10 мг/ EZE 10 мг (n=210) RSV 20 мг/ EZE 10 мг (n=204) SIM 40 мг/ EZE 10 мг (n=199) Целевые значения Х-ЛПНП <70 мг/дл (~1, 8 ммоль/л) В сравнении с симвастатином в дозе 40 мг / эзетимибом в дозе 10 мг p≤ 0, 05; † в сравнении с симвастатином в дозе 40 мг / эзетимибом в дозе 10 мг p≤ 0, 001; ‡ в сравнении с симвастатином в дозе 80 мг / эзетимибом в дозе 10 мг p≤ 0, 05; § в сравнении с симвастатином в дозе 80 мг / эзетимибом в дозе p≤ 0, 0011 RSV = розувастатин, EZE = эзетимиб, SIM = симвастатин Ballantyne C et al. J Am Coll Cardiol 2010; 55(Suppl 1): A 49. E 465 * SIM 80 мг/ EZE 10 мг (n=201)
Комбинация розувастатина с эзетимибом – достижение целевых значений Х-ЛПНП Пациенты, у которых достигнуты целевые значения Х -ЛПНП (%) Исследование GRAVITY * 93. 3% †‡ 95. 6% 87. 4% 88. 6% *§ 77. 0% 67. 7% 67. 1% 55. 3% RSV 10 мг/ EZE 10 мг (n=210) RSV 20 мг/ EZE 10 мг (n=204) SIM 40 мг/ EZE 10 мг (n=199) SIM 80 мг/ EZE 10 мг (n=201) Целевые значения Х-ЛПНП <100 мг/дл (~2, 6 ммоль/л) RSV 10 мг/ EZE 10 мг (n=210) RSV 20 мг/ EZE 10 мг (n=204) SIM 40 мг/ EZE 10 мг (n=199) Целевые значения Х-ЛПНП <70 мг/дл (~1, 8 ммоль/л) В сравнении с симвастатином в дозе 40 мг / эзетимибом в дозе 10 мг p≤ 0, 05; † в сравнении с симвастатином в дозе 40 мг / эзетимибом в дозе 10 мг p≤ 0, 001; ‡ в сравнении с симвастатином в дозе 80 мг / эзетимибом в дозе 10 мг p≤ 0, 05; § в сравнении с симвастатином в дозе 80 мг / эзетимибом в дозе p≤ 0, 0011 RSV = розувастатин, EZE = эзетимиб, SIM = симвастатин Ballantyne C et al. J Am Coll Cardiol 2010; 55(Suppl 1): A 49. E 465 * SIM 80 мг/ EZE 10 мг (n=201)
 Розувастатин Исследования, в которых изучалось влияние терапии на атеросклероз
Розувастатин Исследования, в которых изучалось влияние терапии на атеросклероз
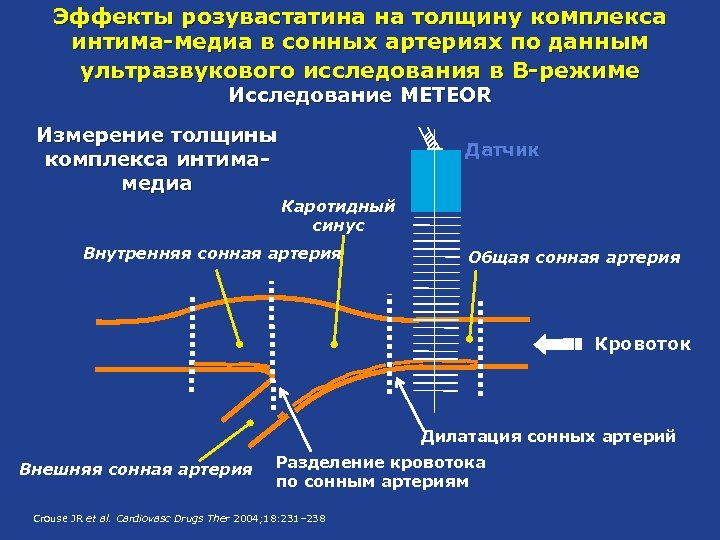 Эффекты розувастатина на толщину комплекса интима-медиа в сонных артериях по данным ультразвукового исследования в B-режиме Исследование METEOR Измерение толщины комплекса интимамедиа Датчик Каротидный синус Внутренняя сонная артерия Общая сонная артерия Кровоток Дилатация сонных артерий Внешняя сонная артерия Разделение кровотока по сонным артериям Crouse JR et al. Cardiovasc Drugs Ther 2004; 18: 231– 238
Эффекты розувастатина на толщину комплекса интима-медиа в сонных артериях по данным ультразвукового исследования в B-режиме Исследование METEOR Измерение толщины комплекса интимамедиа Датчик Каротидный синус Внутренняя сонная артерия Общая сонная артерия Кровоток Дилатация сонных артерий Внешняя сонная артерия Разделение кровотока по сонным артериям Crouse JR et al. Cardiovasc Drugs Ther 2004; 18: 231– 238
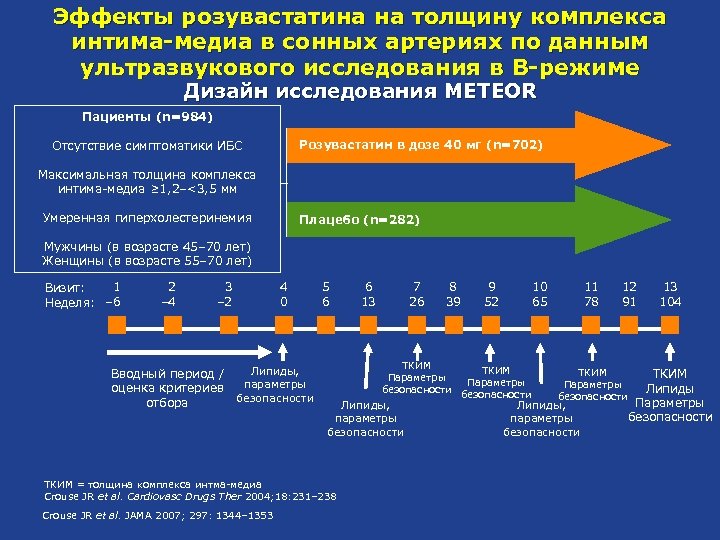 Эффекты розувастатина на толщину комплекса интима-медиа в сонных артериях по данным ультразвукового исследования в B-режиме Дизайн исследования METEOR Пациенты (n=984) Розувастатин в дозе 40 мг (n=702) Отсутствие симптоматики ИБС Максимальная толщина комплекса интима-медиа ≥ 1, 2–<3, 5 мм Умеренная гиперхолестеринемия Плацебо (n=282) Мужчины (в возрасте 45– 70 лет) Женщины (в возрасте 55– 70 лет) 1 Визит: Неделя: – 6 2 – 4 3 – 2 Вводный период / оценка критериев отбора 4 0 Липиды, параметры безопасности 5 6 7 26 8 39 ТКИМ Параметры безопасности Липиды, параметры безопасности ТКИМ = толщина комплекса интма-медиа Crouse JR et al. Cardiovasc Drugs Ther 2004; 18: 231– 238 Crouse JR et al. JAMA 2007; 297: 1344– 1353 6 13 9 52 10 65 ТКИМ Параметры безопасности 11 78 12 91 ТКИМ Параметры безопасности Липиды, параметры безопасности 13 104 ТКИМ Липиды Параметры безопасности
Эффекты розувастатина на толщину комплекса интима-медиа в сонных артериях по данным ультразвукового исследования в B-режиме Дизайн исследования METEOR Пациенты (n=984) Розувастатин в дозе 40 мг (n=702) Отсутствие симптоматики ИБС Максимальная толщина комплекса интима-медиа ≥ 1, 2–<3, 5 мм Умеренная гиперхолестеринемия Плацебо (n=282) Мужчины (в возрасте 45– 70 лет) Женщины (в возрасте 55– 70 лет) 1 Визит: Неделя: – 6 2 – 4 3 – 2 Вводный период / оценка критериев отбора 4 0 Липиды, параметры безопасности 5 6 7 26 8 39 ТКИМ Параметры безопасности Липиды, параметры безопасности ТКИМ = толщина комплекса интма-медиа Crouse JR et al. Cardiovasc Drugs Ther 2004; 18: 231– 238 Crouse JR et al. JAMA 2007; 297: 1344– 1353 6 13 9 52 10 65 ТКИМ Параметры безопасности 11 78 12 91 ТКИМ Параметры безопасности Липиды, параметры безопасности 13 104 ТКИМ Липиды Параметры безопасности
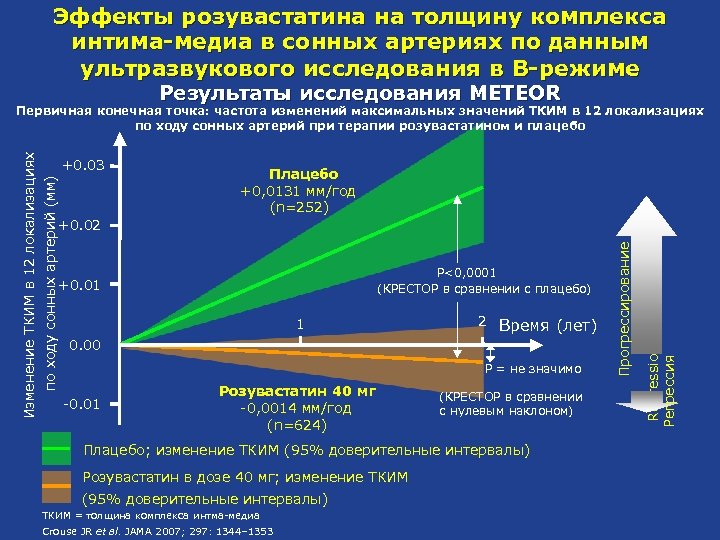 Эффекты розувастатина на толщину комплекса интима-медиа в сонных артериях по данным ультразвукового исследования в B-режиме Результаты исследования METEOR +0. 03 по ходу сонных артерий (мм) Плацебо +0, 0131 мм/год +0. 0131 mm/yr (n=252) P<0, 0001 P<0. 0001 (КРЕСТОР в сравнении с плацебо) +0. 01 1 2 Время (лет) 0. 00 P = не значимо -0. 01 Розувастатин 40 мг -0, 0014 мм/год -0. 0014 mm/yr (n=624) (КРЕСТОР в сравнении с нулевым наклоном) Плацебо; изменение ТКИМ (95% доверительные интервалы) Розувастатин в дозе 40 мг; изменение ТКИМ (95% доверительные интервалы) ТКИМ = толщина комплекса интма-медиа Crouse JR et al. JAMA 2007; 297: 1344– 1353 Regression Регрессия +0. 02 Прогрессирование Изменение ТКИМ в 12 локализациях Первичная конечная точка: частота изменений максимальных значений ТКИМ в 12 локализациях по ходу сонных артерий при терапии розувастатином и плацебо
Эффекты розувастатина на толщину комплекса интима-медиа в сонных артериях по данным ультразвукового исследования в B-режиме Результаты исследования METEOR +0. 03 по ходу сонных артерий (мм) Плацебо +0, 0131 мм/год +0. 0131 mm/yr (n=252) P<0, 0001 P<0. 0001 (КРЕСТОР в сравнении с плацебо) +0. 01 1 2 Время (лет) 0. 00 P = не значимо -0. 01 Розувастатин 40 мг -0, 0014 мм/год -0. 0014 mm/yr (n=624) (КРЕСТОР в сравнении с нулевым наклоном) Плацебо; изменение ТКИМ (95% доверительные интервалы) Розувастатин в дозе 40 мг; изменение ТКИМ (95% доверительные интервалы) ТКИМ = толщина комплекса интма-медиа Crouse JR et al. JAMA 2007; 297: 1344– 1353 Regression Регрессия +0. 02 Прогрессирование Изменение ТКИМ в 12 локализациях Первичная конечная точка: частота изменений максимальных значений ТКИМ в 12 локализациях по ходу сонных артерий при терапии розувастатином и плацебо
 Профиль безопасности розувастатина • Профиль нежелательных явлений ‒ Общие характеристики ‒ Распределение по полу ‒ У пожилых пациентов ‒ У пациентов высокого риска • Эффекты в отношении печени • Эффекты в отношении мышечной ткани • Эффекты в отношении почек
Профиль безопасности розувастатина • Профиль нежелательных явлений ‒ Общие характеристики ‒ Распределение по полу ‒ У пожилых пациентов ‒ У пациентов высокого риска • Эффекты в отношении печени • Эффекты в отношении мышечной ткани • Эффекты в отношении почек
 Профиль безопасности розувастатина Нежелательные явления в контролируемых клинических исследованиях
Профиль безопасности розувастатина Нежелательные явления в контролируемых клинических исследованиях
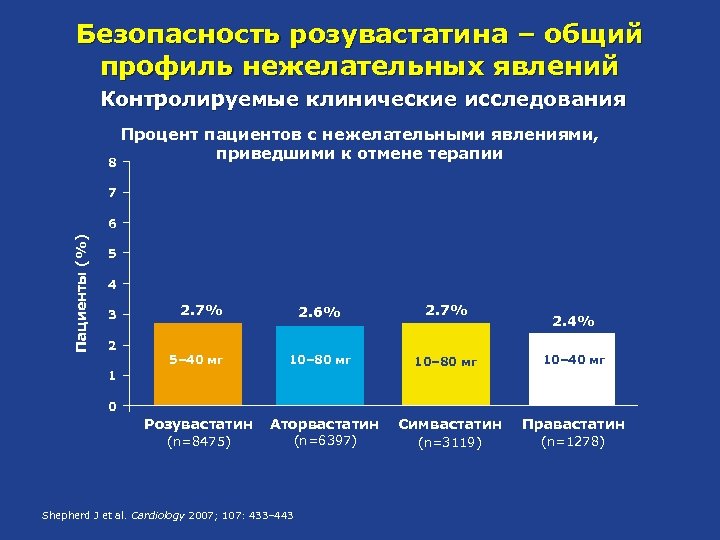 Безопасность розувастатина – общий профиль нежелательных явлений Контролируемые клинические исследования 8 Процент пациентов с нежелательными явлениями, приведшими к отмене терапии 7 Пациенты (%) 6 5 4 3 2 2. 6% 2. 7% 10– 80 мг 2. 7% 5– 40 мг 1 2. 4% 10– 40 мг 0 Розувастатин Аторвастатин Симвастатин Правастатин (n=8475) (n=6397) (n=3119) (n=1278) Shepherd J et al. Cardiology 2007; 107: 433– 443
Безопасность розувастатина – общий профиль нежелательных явлений Контролируемые клинические исследования 8 Процент пациентов с нежелательными явлениями, приведшими к отмене терапии 7 Пациенты (%) 6 5 4 3 2 2. 6% 2. 7% 10– 80 мг 2. 7% 5– 40 мг 1 2. 4% 10– 40 мг 0 Розувастатин Аторвастатин Симвастатин Правастатин (n=8475) (n=6397) (n=3119) (n=1278) Shepherd J et al. Cardiology 2007; 107: 433– 443
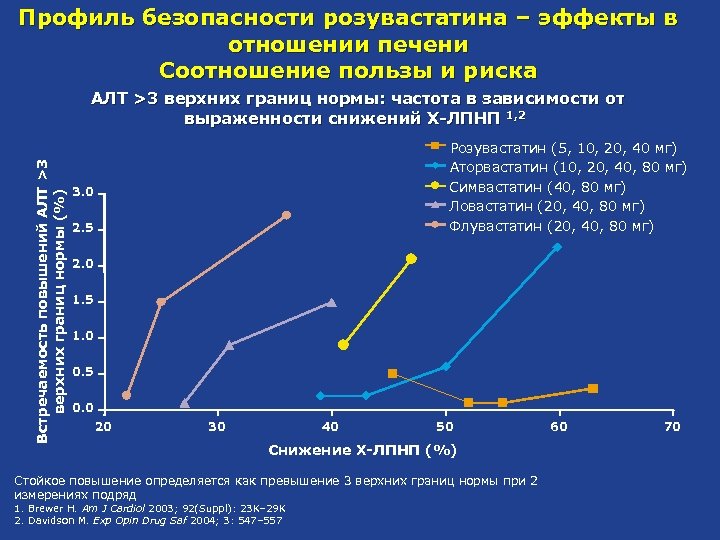 Профиль безопасности розувастатина – эффекты в отношении печени Соотношение пользы и риска Встречаемость повышений АЛТ >3 верхних границ нормы (%) АЛТ >3 верхних границ нормы: частота в зависимости от выраженности снижений Х-ЛПНП 1, 2 Розувастатин (5, 10, 20, 40 мг) Аторвастатин (10, 20, 40, 80 мг) Симвастатин (40, 80 мг) Ловастатин (20, 40, 80 мг) Флувастатин (20, 40, 80 мг) 3. 0 2. 5 2. 0 1. 5 1. 0 0. 5 0. 0 20 30 40 50 Снижение Х-ЛПНП (%) Стойкое повышение определяется как превышение 3 верхних границ нормы при 2 измерениях подряд 1. Brewer H. Am J Cardiol 2003; 92(Suppl): 23 K– 29 K 2. Davidson M. Exp Opin Drug Saf 2004; 3: 547– 557 60 70
Профиль безопасности розувастатина – эффекты в отношении печени Соотношение пользы и риска Встречаемость повышений АЛТ >3 верхних границ нормы (%) АЛТ >3 верхних границ нормы: частота в зависимости от выраженности снижений Х-ЛПНП 1, 2 Розувастатин (5, 10, 20, 40 мг) Аторвастатин (10, 20, 40, 80 мг) Симвастатин (40, 80 мг) Ловастатин (20, 40, 80 мг) Флувастатин (20, 40, 80 мг) 3. 0 2. 5 2. 0 1. 5 1. 0 0. 5 0. 0 20 30 40 50 Снижение Х-ЛПНП (%) Стойкое повышение определяется как превышение 3 верхних границ нормы при 2 измерениях подряд 1. Brewer H. Am J Cardiol 2003; 92(Suppl): 23 K– 29 K 2. Davidson M. Exp Opin Drug Saf 2004; 3: 547– 557 60 70
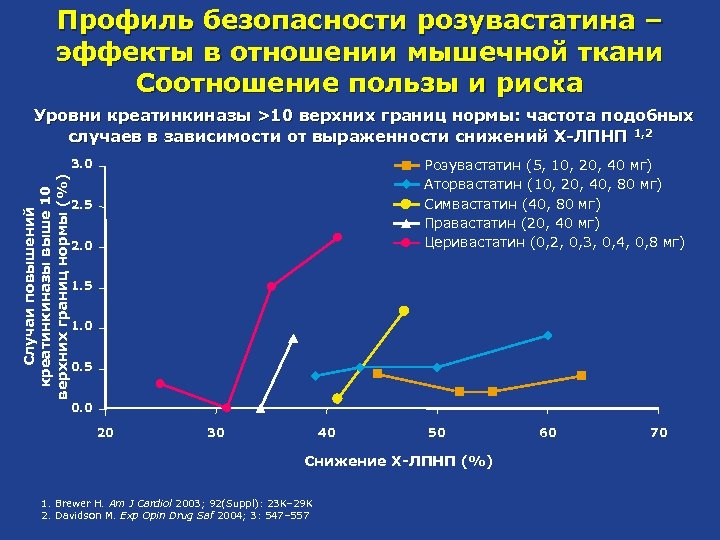 Профиль безопасности розувастатина – эффекты в отношении мышечной ткани Соотношение пользы и риска Уровни креатинкиназы >10 верхних границ нормы: частота подобных случаев в зависимости от выраженности снижений Х-ЛПНП 1, 2 Розувастатин (5, 10, 20, 40 мг) Аторвастатин (10, 20, 40, 80 мг) Симвастатин (40, 80 мг) Правастатин (20, 40 мг) Церивастатин (0, 2, 0, 3, 0, 4, 0, 8 мг) Случаи повышений креатинкиназы выше 10 верхних границ нормы (%) 3. 0 2. 5 2. 0 1. 5 1. 0 0. 5 0. 0 20 30 40 50 Снижение Х-ЛПНП (%) 1. Brewer H. Am J Cardiol 2003; 92(Suppl): 23 K– 29 K 2. Davidson M. Exp Opin Drug Saf 2004; 3: 547– 557 60 70
Профиль безопасности розувастатина – эффекты в отношении мышечной ткани Соотношение пользы и риска Уровни креатинкиназы >10 верхних границ нормы: частота подобных случаев в зависимости от выраженности снижений Х-ЛПНП 1, 2 Розувастатин (5, 10, 20, 40 мг) Аторвастатин (10, 20, 40, 80 мг) Симвастатин (40, 80 мг) Правастатин (20, 40 мг) Церивастатин (0, 2, 0, 3, 0, 4, 0, 8 мг) Случаи повышений креатинкиназы выше 10 верхних границ нормы (%) 3. 0 2. 5 2. 0 1. 5 1. 0 0. 5 0. 0 20 30 40 50 Снижение Х-ЛПНП (%) 1. Brewer H. Am J Cardiol 2003; 92(Suppl): 23 K– 29 K 2. Davidson M. Exp Opin Drug Saf 2004; 3: 547– 557 60 70
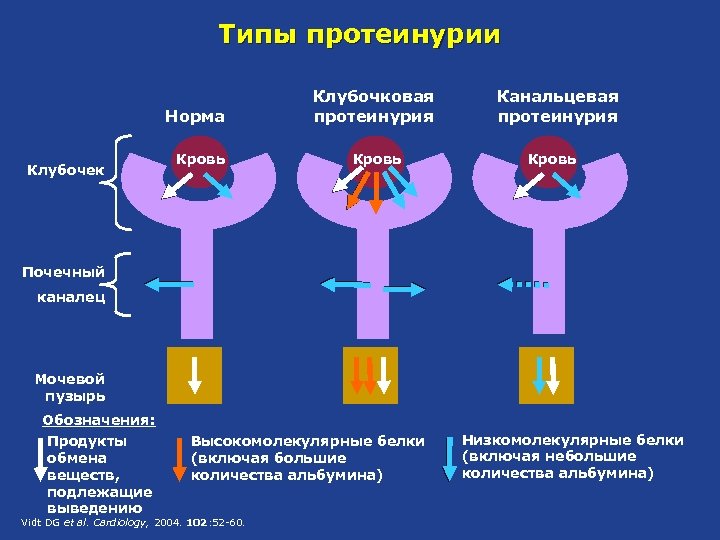 Типы протеинурии Норма Клубочек Кровь Клубочковая протеинурия Кровь Канальцевая протеинурия Кровь Почечный каналец Мочевой пузырь Обозначения: Продукты обмена веществ, подлежащие выведению Высокомолекулярные белки (включая большие количества альбумина) Vidt DG et al. Cardiology, 2004. 102: 52 -60. Низкомолекулярные белки (включая небольшие количества альбумина)
Типы протеинурии Норма Клубочек Кровь Клубочковая протеинурия Кровь Канальцевая протеинурия Кровь Почечный каналец Мочевой пузырь Обозначения: Продукты обмена веществ, подлежащие выведению Высокомолекулярные белки (включая большие количества альбумина) Vidt DG et al. Cardiology, 2004. 102: 52 -60. Низкомолекулярные белки (включая небольшие количества альбумина)
 Безопасность розувастатина – эффекты в отношении почек Контролируемые клинические исследования l Протеинурия* отмечалась у небольшого количества пациентов, получавших все виды изученных статинов, а также плацебо 1 l Данное наблюдение было тщательно изучено у получавших розувастатин пациентов; было отмечено, что явление носит, как правило, транзиторный характер, часто разрешается на фоне продолжения лечения и не является предвестником острой почечной недостаточности или нарастающего ухудшения функции почек 1 l Протеинурия, наблюдающаяся применении розувастатина, является по своему происхождению канальцевой (характеризующейся снижением реабсорбции белков, в норме фильтруемых) 1 – Развитие подобной канальцевой протеинурии является, скорее всего, последствием фармакологического эффекта розувастатина – т. е. ингибирования ГМГ-Ко. А-редуктазы в клетках почечных канальцев 2, 3 – Высокоэффективное ингибирование ГМГ-Ко. А-редуктазы, наряду с более высокими показателями выделительной функции почек, вносят свой вклад в подобное наблюдение на фоне терапии розувастатина * Положительные результаты полуколичественного анализа мочи на протеинурию, в виде сдвига от исходного отсутствия или исходных следов белка до ≥++ 1. Vidt DG et al. Cardiology 2004; 102: 52– 60 2. Sidaway J et al. J Am Soc Nephrol 2004; 15: 2258– 2265 3. Verhulst A et al. J Am Soc Nephrol 2004; 15: 2249– 2257
Безопасность розувастатина – эффекты в отношении почек Контролируемые клинические исследования l Протеинурия* отмечалась у небольшого количества пациентов, получавших все виды изученных статинов, а также плацебо 1 l Данное наблюдение было тщательно изучено у получавших розувастатин пациентов; было отмечено, что явление носит, как правило, транзиторный характер, часто разрешается на фоне продолжения лечения и не является предвестником острой почечной недостаточности или нарастающего ухудшения функции почек 1 l Протеинурия, наблюдающаяся применении розувастатина, является по своему происхождению канальцевой (характеризующейся снижением реабсорбции белков, в норме фильтруемых) 1 – Развитие подобной канальцевой протеинурии является, скорее всего, последствием фармакологического эффекта розувастатина – т. е. ингибирования ГМГ-Ко. А-редуктазы в клетках почечных канальцев 2, 3 – Высокоэффективное ингибирование ГМГ-Ко. А-редуктазы, наряду с более высокими показателями выделительной функции почек, вносят свой вклад в подобное наблюдение на фоне терапии розувастатина * Положительные результаты полуколичественного анализа мочи на протеинурию, в виде сдвига от исходного отсутствия или исходных следов белка до ≥++ 1. Vidt DG et al. Cardiology 2004; 102: 52– 60 2. Sidaway J et al. J Am Soc Nephrol 2004; 15: 2258– 2265 3. Verhulst A et al. J Am Soc Nephrol 2004; 15: 2249– 2257
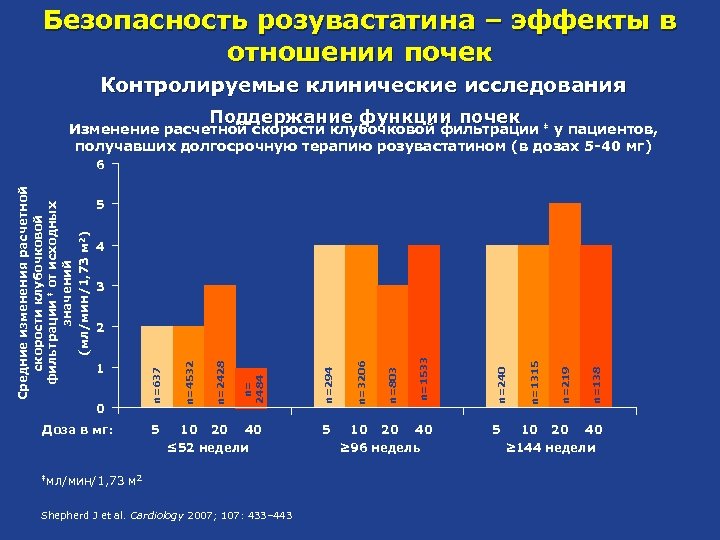 Безопасность розувастатина – эффекты в отношении почек Контролируемые клинические исследования Поддержание функции почек Изменение расчетной скорости клубочковой фильтрации ‡ у пациентов, получавших долгосрочную терапию розувастатином (в дозах 5 -40 мг) 5 4 3 5 10 20 40 ≤ 52 недели ‡мл/мин/1, 73 м 2 Shepherd J et al. Cardiology 2007; 107: 433– 443 ≥ 96 недель 5 n=138 n=1533 40 n=219 n=803 20 n=1315 n=3206 10 10 n=240 n=294 Доза в мг: n= 2484 0 n=2428 5 1 n=4532 2 n=637 Средние изменения расчетной скорости клубочковой фильтрации ‡ от исходных значений (мл/мин/1, 73 м 2) 6 20 40 ≥ 144 недели
Безопасность розувастатина – эффекты в отношении почек Контролируемые клинические исследования Поддержание функции почек Изменение расчетной скорости клубочковой фильтрации ‡ у пациентов, получавших долгосрочную терапию розувастатином (в дозах 5 -40 мг) 5 4 3 5 10 20 40 ≤ 52 недели ‡мл/мин/1, 73 м 2 Shepherd J et al. Cardiology 2007; 107: 433– 443 ≥ 96 недель 5 n=138 n=1533 40 n=219 n=803 20 n=1315 n=3206 10 10 n=240 n=294 Доза в мг: n= 2484 0 n=2428 5 1 n=4532 2 n=637 Средние изменения расчетной скорости клубочковой фильтрации ‡ от исходных значений (мл/мин/1, 73 м 2) 6 20 40 ≥ 144 недели
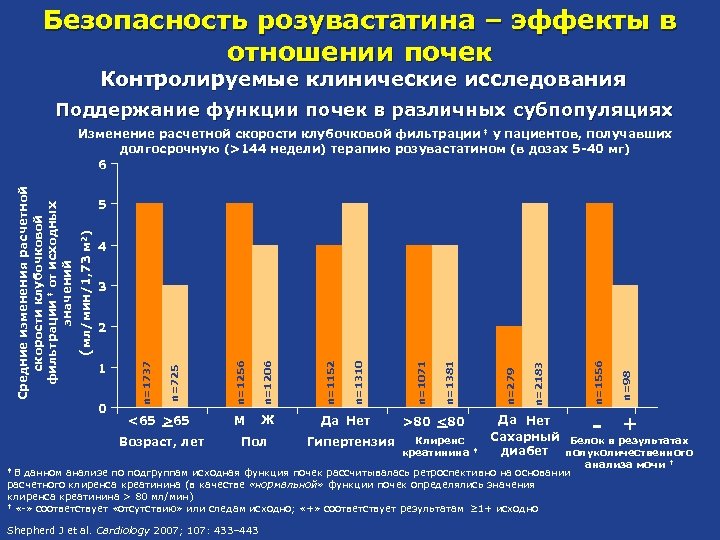 Безопасность розувастатина – эффекты в отношении почек Контролируемые клинические исследования Поддержание функции почек в различных субпопуляциях 5 4 3 Возраст, лет Гипертензия ‡ В данном анализе по подгруппам исходная функция почек рассчитывалась ретроспективно на основании расчетного клиренса креатинина (в качестве «нормальной» функции почек определялись значения клиренса креатинина > 80 мл/мин) † «-» соответствует «отсутствию» или следам исходно; «+» соответствует результатам ≥ 1+ исходно ‡ Shepherd J et al. Cardiology 2007; 107: 433– 443 n=98 n=1556 Да Нет + Сахарный Белок в результатах диабет полуколичественного - >80 <80 Клиренс креатинина n=2183 n=279 Да Нет n=1381 Ж n=1071 M Пол n=1310 n=1152 <65 >65 n=1206 0 n=1256 1 n=725 2 n=1737 (мл/мин/1, 73 м 2) Средние изменения расчетной скорости клубочковой фильтрации ‡ от исходных значений Изменение расчетной скорости клубочковой фильтрации ‡ у пациентов, получавших долгосрочную (>144 недели) терапию розувастатином (в дозах 5 -40 мг) 6 анализа мочи †
Безопасность розувастатина – эффекты в отношении почек Контролируемые клинические исследования Поддержание функции почек в различных субпопуляциях 5 4 3 Возраст, лет Гипертензия ‡ В данном анализе по подгруппам исходная функция почек рассчитывалась ретроспективно на основании расчетного клиренса креатинина (в качестве «нормальной» функции почек определялись значения клиренса креатинина > 80 мл/мин) † «-» соответствует «отсутствию» или следам исходно; «+» соответствует результатам ≥ 1+ исходно ‡ Shepherd J et al. Cardiology 2007; 107: 433– 443 n=98 n=1556 Да Нет + Сахарный Белок в результатах диабет полуколичественного - >80 <80 Клиренс креатинина n=2183 n=279 Да Нет n=1381 Ж n=1071 M Пол n=1310 n=1152 <65 >65 n=1206 0 n=1256 1 n=725 2 n=1737 (мл/мин/1, 73 м 2) Средние изменения расчетной скорости клубочковой фильтрации ‡ от исходных значений Изменение расчетной скорости клубочковой фильтрации ‡ у пациентов, получавших долгосрочную (>144 недели) терапию розувастатином (в дозах 5 -40 мг) 6 анализа мочи †
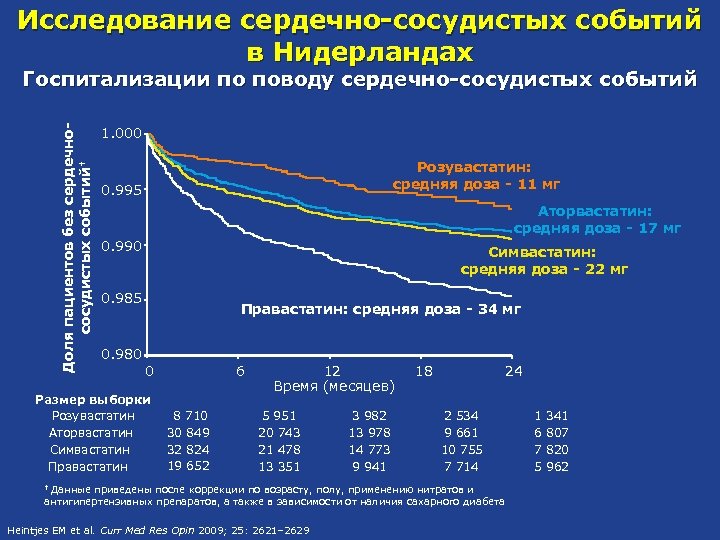 Исследование сердечно-сосудистых событий в Нидерландах Доля пациентов без сердечнососудистых событий† Госпитализации по поводу сердечно-сосудистых событий 1. 000 Розувастатин: средняя доза - 11 мг 0. 995 Аторвастатин: средняя доза - 17 мг 0. 990 Симвастатин: средняя доза - 22 мг 0. 985 Правастатин: средняя доза - 34 мг 0. 980 0 Размер выборки Розувастатин Аторвастатин Симвастатин Правастатин 6 8 710 30 849 32 824 19 652 12 Время (месяцев) 5 951 20 743 21 478 13 351 3 982 13 978 14 773 9 941 18 24 2 534 9 661 10 755 7 714 Данные приведены после коррекции по возрасту, полу, применению нитратов и антигипертензивных препаратов, а также в зависимости от наличия сахарного диабета † Heintjes EM et al. Curr Med Res Opin 2009; 25: 2621– 2629 1 6 7 5 341 807 820 962
Исследование сердечно-сосудистых событий в Нидерландах Доля пациентов без сердечнососудистых событий† Госпитализации по поводу сердечно-сосудистых событий 1. 000 Розувастатин: средняя доза - 11 мг 0. 995 Аторвастатин: средняя доза - 17 мг 0. 990 Симвастатин: средняя доза - 22 мг 0. 985 Правастатин: средняя доза - 34 мг 0. 980 0 Размер выборки Розувастатин Аторвастатин Симвастатин Правастатин 6 8 710 30 849 32 824 19 652 12 Время (месяцев) 5 951 20 743 21 478 13 351 3 982 13 978 14 773 9 941 18 24 2 534 9 661 10 755 7 714 Данные приведены после коррекции по возрасту, полу, применению нитратов и антигипертензивных препаратов, а также в зависимости от наличия сахарного диабета † Heintjes EM et al. Curr Med Res Opin 2009; 25: 2621– 2629 1 6 7 5 341 807 820 962
 Исследования сердечно-сосудистых событий Общий обзор l Согласно результатам проведенного в США исследования, частота сердечно-сосудистых событий была существенно ниже у пациентов, получавших розувастатин, по сравнению с пациентами, получавшими другие статины, при длительности подобной терапии ≥ 270 дней – Тем не менее, после длительности ≥ 360 дней различие не было статистически значимым 1 l Результаты проведенного в Нидерландах исследования, при средней длительности наблюдения в 382 дня, позволяют предполагать, что у пациентов, получавших розувастатин, частота сердечно-сосудистых событий была существенно ниже, по сравнению с пациентами, получавшими симвастатин и правастатин – Статистически значимых различий по сравнению с аторвастатином не наблюдалось 2 1. Motsko SP et al. Pharmacoepidemiol Drug Saf 2009; 18: 1214– 1222 2. Heintjes EM et al. Curr Med Res Opin 2009; 25: 2621– 2692
Исследования сердечно-сосудистых событий Общий обзор l Согласно результатам проведенного в США исследования, частота сердечно-сосудистых событий была существенно ниже у пациентов, получавших розувастатин, по сравнению с пациентами, получавшими другие статины, при длительности подобной терапии ≥ 270 дней – Тем не менее, после длительности ≥ 360 дней различие не было статистически значимым 1 l Результаты проведенного в Нидерландах исследования, при средней длительности наблюдения в 382 дня, позволяют предполагать, что у пациентов, получавших розувастатин, частота сердечно-сосудистых событий была существенно ниже, по сравнению с пациентами, получавшими симвастатин и правастатин – Статистически значимых различий по сравнению с аторвастатином не наблюдалось 2 1. Motsko SP et al. Pharmacoepidemiol Drug Saf 2009; 18: 1214– 1222 2. Heintjes EM et al. Curr Med Res Opin 2009; 25: 2621– 2692
 Розувастатин Клиническая фармакология
Розувастатин Клиническая фармакология
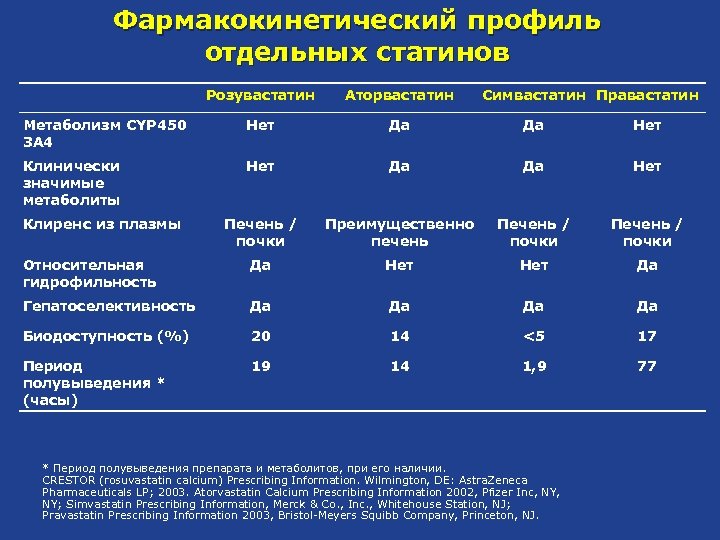 Фармакокинетический профиль отдельных статинов Розувастатин Аторвастатин Метаболизм CYP 450 3 A 4 Нет Да Да Нет Клинически значимые метаболиты Нет Да Да Нет Печень / почки Преимущественно печень Печень / почки Относительная гидрофильность Да Нет Да Гепатоселективность Да Да Биодоступность (%) 20 14 <5 17 Период полувыведения * (часы) 19 14 1, 9 77 Клиренс из плазмы Симвастатин Правастатин * Период полувыведения препарата и метаболитов, при его наличии. CRESTOR (rosuvastatin calcium) Prescribing Information. Wilmington, DE: Astra. Zeneca Pharmaceuticals LP; 2003. Atorvastatin Calcium Prescribing Information 2002, Pfizer Inc, NY; Simvastatin Prescribing Information, Merck & Co. , Inc. , Whitehouse Station, NJ; Pravastatin Prescribing Information 2003, Bristol-Meyers Squibb Company, Princeton, NJ.
Фармакокинетический профиль отдельных статинов Розувастатин Аторвастатин Метаболизм CYP 450 3 A 4 Нет Да Да Нет Клинически значимые метаболиты Нет Да Да Нет Печень / почки Преимущественно печень Печень / почки Относительная гидрофильность Да Нет Да Гепатоселективность Да Да Биодоступность (%) 20 14 <5 17 Период полувыведения * (часы) 19 14 1, 9 77 Клиренс из плазмы Симвастатин Правастатин * Период полувыведения препарата и метаболитов, при его наличии. CRESTOR (rosuvastatin calcium) Prescribing Information. Wilmington, DE: Astra. Zeneca Pharmaceuticals LP; 2003. Atorvastatin Calcium Prescribing Information 2002, Pfizer Inc, NY; Simvastatin Prescribing Information, Merck & Co. , Inc. , Whitehouse Station, NJ; Pravastatin Prescribing Information 2003, Bristol-Meyers Squibb Company, Princeton, NJ.
 Взаимодействия розувастатина с другими препаратами l Взаимодействия, не считаемые клинически значимыми: – флуконазол, кетоконазол и итраконазол – фенофибрат – дигоксин l Взаимодействия с ограниченной клинической значимостью: – Антациды – снижение уровней розувастатина на 50% – Эритромицин – незначительное снижение уровней розувастатина в плазме l Клинически значимые взаимодействия: – Пероральные контрацептивы - уровней этинилэстрадиола и норгестрела, что может повлиять на выбор перорального контрацептива – Гемфиброзил – 2 x уровней розувастатина в плазме. Комбинированная терапия не рекомендована – Циклоспорин – 7 x уровней розувастатина в плазме. Вне США подобная комбинированная терапия противопоказана – Варфарин – МНО – требуется контроль МНО – Липонавир / ритонавир – 2 x уровней розувастатина в плазме. Комбинированная терапия не рекомендована Инструкция по медицинскому применению препарата Крестор, Рег. удос. № 015644/01 от 19. 02. 2010
Взаимодействия розувастатина с другими препаратами l Взаимодействия, не считаемые клинически значимыми: – флуконазол, кетоконазол и итраконазол – фенофибрат – дигоксин l Взаимодействия с ограниченной клинической значимостью: – Антациды – снижение уровней розувастатина на 50% – Эритромицин – незначительное снижение уровней розувастатина в плазме l Клинически значимые взаимодействия: – Пероральные контрацептивы - уровней этинилэстрадиола и норгестрела, что может повлиять на выбор перорального контрацептива – Гемфиброзил – 2 x уровней розувастатина в плазме. Комбинированная терапия не рекомендована – Циклоспорин – 7 x уровней розувастатина в плазме. Вне США подобная комбинированная терапия противопоказана – Варфарин – МНО – требуется контроль МНО – Липонавир / ритонавир – 2 x уровней розувастатина в плазме. Комбинированная терапия не рекомендована Инструкция по медицинскому применению препарата Крестор, Рег. удос. № 015644/01 от 19. 02. 2010
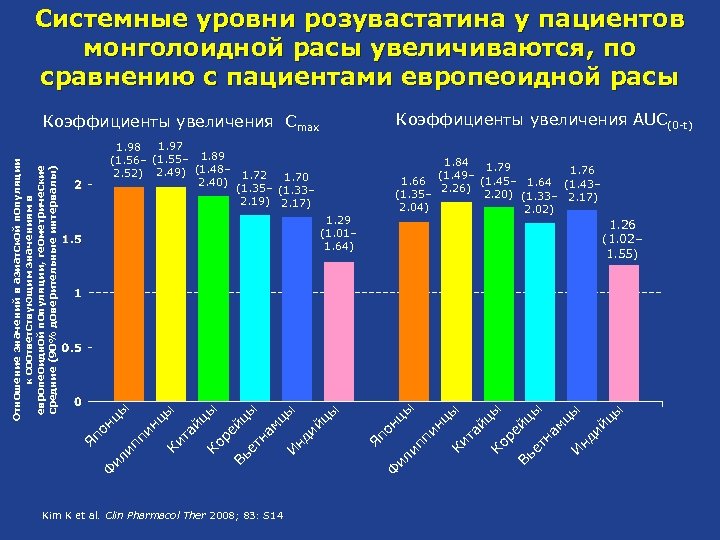 Системные уровни розувастатина у пациентов монголоидной расы увеличиваются, по сравнению с пациентами европеоидной расы Коэффициенты увеличения AUC(0 -t) Коэффициенты увеличения Cmax 1. 84 1. 79 1. 76 (1. 49‒ (1. 45‒ 1. 64 (1. 43‒ 1. 66 2. 26) 2. 20) (1. 33‒ 2. 17) (1. 35‒ 2. 04) 2. 02) Kim K et al. Clin Pharmacol Ther 2008; 83: S 14 цы ий ы нд И на мц ет ей цы ы йц ы та Ко р Вь Ф ил Ки нц пи он цы 1. 26 (1. 02‒ 1. 55) Яп цы ий ы нд И на мц Вь ет ей цы ы Ко р та йц ы Ки нц пи ил ип Ф Яп он цы 1. 29 (1. 01‒ 1. 64) ип Отношение значений в азиатской популяции к соответствующим значениям в европеоидной популяции, геометрические средние (90% доверительные интервалы) 1. 97 1. 98 (1. 56‒ (1. 55‒ 1. 89 2. 52) 2. 49) (1. 48‒ 1. 72 1. 70 2. 40) (1. 35‒ (1. 33‒ 2. 19) 2. 17)
Системные уровни розувастатина у пациентов монголоидной расы увеличиваются, по сравнению с пациентами европеоидной расы Коэффициенты увеличения AUC(0 -t) Коэффициенты увеличения Cmax 1. 84 1. 79 1. 76 (1. 49‒ (1. 45‒ 1. 64 (1. 43‒ 1. 66 2. 26) 2. 20) (1. 33‒ 2. 17) (1. 35‒ 2. 04) 2. 02) Kim K et al. Clin Pharmacol Ther 2008; 83: S 14 цы ий ы нд И на мц ет ей цы ы йц ы та Ко р Вь Ф ил Ки нц пи он цы 1. 26 (1. 02‒ 1. 55) Яп цы ий ы нд И на мц Вь ет ей цы ы Ко р та йц ы Ки нц пи ил ип Ф Яп он цы 1. 29 (1. 01‒ 1. 64) ип Отношение значений в азиатской популяции к соответствующим значениям в европеоидной популяции, геометрические средние (90% доверительные интервалы) 1. 97 1. 98 (1. 56‒ (1. 55‒ 1. 89 2. 52) 2. 49) (1. 48‒ 1. 72 1. 70 2. 40) (1. 35‒ (1. 33‒ 2. 19) 2. 17)
 Розувастатин – общий обзор l Розувастатин обладает благоприятными эффектами на ключевые параметры липидного спектра во всем диапазоне используемых доз l В различных исследованиях неизменно отмечается, что розувастатин эффективнее всех статинов снижает Х-ЛПНП 1– 29 – Превосходство над аторвастатином в плане снижения Х-ЛПНП продемонстрировано в 25 сравнительных исследованиях с участием >20 000 пациентов 1 -15, 18 -28 l Розувастатин в дозе 10 мг снижает Х-ЛПНП в большей степени, нежели аторвастатин в дозах 10 мг и 20 мг 2, 13– 15 l Розувастатин позволяет добиться целевых значений Х-ЛПНП у большего количества пациентов, нежели другие статины, присутствующие на рынке в настоящее время, в чаще всего используемых дозировках 1 -5, 14, 21, 22, 30– 32, что позволяет избежать необходимости титрации до более высоких доз l Розувастатин приводит к существенному увеличению уровней ХЛПВП, сохраняющемуся, в отличие от аторвастатина, во всем диапазоне используемых доз 1 Полный список источников литературы приведен на последнем слайде
Розувастатин – общий обзор l Розувастатин обладает благоприятными эффектами на ключевые параметры липидного спектра во всем диапазоне используемых доз l В различных исследованиях неизменно отмечается, что розувастатин эффективнее всех статинов снижает Х-ЛПНП 1– 29 – Превосходство над аторвастатином в плане снижения Х-ЛПНП продемонстрировано в 25 сравнительных исследованиях с участием >20 000 пациентов 1 -15, 18 -28 l Розувастатин в дозе 10 мг снижает Х-ЛПНП в большей степени, нежели аторвастатин в дозах 10 мг и 20 мг 2, 13– 15 l Розувастатин позволяет добиться целевых значений Х-ЛПНП у большего количества пациентов, нежели другие статины, присутствующие на рынке в настоящее время, в чаще всего используемых дозировках 1 -5, 14, 21, 22, 30– 32, что позволяет избежать необходимости титрации до более высоких доз l Розувастатин приводит к существенному увеличению уровней ХЛПВП, сохраняющемуся, в отличие от аторвастатина, во всем диапазоне используемых доз 1 Полный список источников литературы приведен на последнем слайде
 Розувастатин – общий обзор l Было показано, что эффективное снижение Х-ЛПНП и увеличение Х-ЛПВП при терапии розувастатином – Замедляет увеличение толщины комплекса интима-медиа у пациентов на ранних стадиях заболевания и с низким риском ИБС 33, а также l В исследовании JUPITER продемонстрировано выраженное снижение серьезных сердечно-сосудистых событий (совокупной конечной точки, включавшей в себя сердечно-сосудистую смертность, ИМ, инсульт, нестабильную стенокардию, реваскуляризацию артерий) применении розувастатина в дозе 20 мг по сравнению с плацебо (p<0, 00001) 34 l Профиль безопасности розувастатина схож с аналогичным профилем других статинов, в настоящее время присутствующих на рынке; отношение пользы и риска является благоприятным 35– 37 Полный список источников литературы приведен на последнем слайде
Розувастатин – общий обзор l Было показано, что эффективное снижение Х-ЛПНП и увеличение Х-ЛПВП при терапии розувастатином – Замедляет увеличение толщины комплекса интима-медиа у пациентов на ранних стадиях заболевания и с низким риском ИБС 33, а также l В исследовании JUPITER продемонстрировано выраженное снижение серьезных сердечно-сосудистых событий (совокупной конечной точки, включавшей в себя сердечно-сосудистую смертность, ИМ, инсульт, нестабильную стенокардию, реваскуляризацию артерий) применении розувастатина в дозе 20 мг по сравнению с плацебо (p<0, 00001) 34 l Профиль безопасности розувастатина схож с аналогичным профилем других статинов, в настоящее время присутствующих на рынке; отношение пользы и риска является благоприятным 35– 37 Полный список источников литературы приведен на последнем слайде
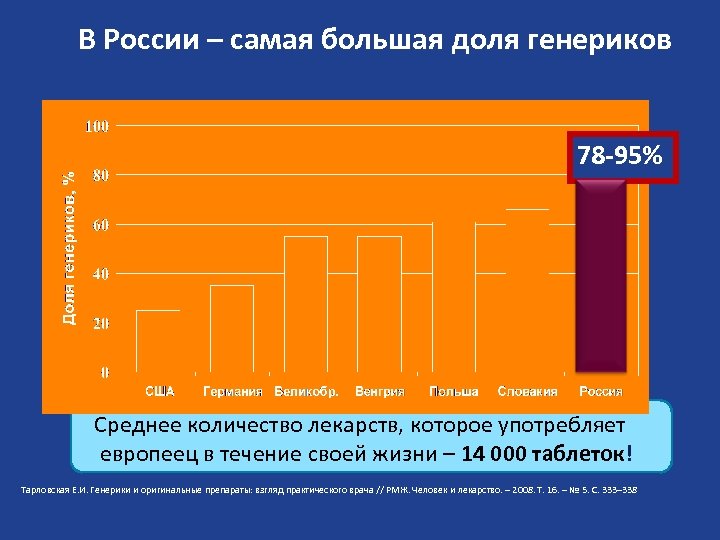 В России – самая большая доля генериков 78 -95% Среднее количество лекарств, которое употребляет европеец в течение своей жизни – 14 000 таблеток! Тарловская Е. И. Генерики и оригинальные препараты: взгляд практического врача // РМЖ. Человек и лекарство. – 2008. Т. 16. – № 5. С. 333– 338
В России – самая большая доля генериков 78 -95% Среднее количество лекарств, которое употребляет европеец в течение своей жизни – 14 000 таблеток! Тарловская Е. И. Генерики и оригинальные препараты: взгляд практического врача // РМЖ. Человек и лекарство. – 2008. Т. 16. – № 5. С. 333– 338
 Оригинальный препарат Оригинальное лекарственное средство, содержащее впервые полученную фармацевтическую субстанцию или новую комбинацию фармацевтических субстанций, эффективность и безопасность которых подтверждены результатами доклинических исследований лекарственных средств и клинических исследований лекарственных препаратов Федеральный закон от 12 апреля 2010 г. N 61 -ФЗ "Об обращении лекарственных средств"
Оригинальный препарат Оригинальное лекарственное средство, содержащее впервые полученную фармацевтическую субстанцию или новую комбинацию фармацевтических субстанций, эффективность и безопасность которых подтверждены результатами доклинических исследований лекарственных средств и клинических исследований лекарственных препаратов Федеральный закон от 12 апреля 2010 г. N 61 -ФЗ "Об обращении лекарственных средств"
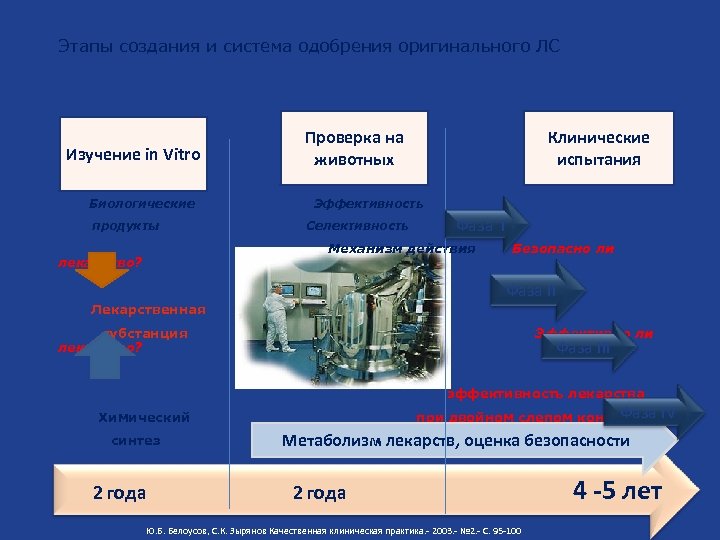 Этапы создания и система одобрения оригинального ЛС Изучение in Vitro Биологические продукты Проверка на животных Клинические испытания Эффективность Селективность Фаза I Механизм действия лекарство? Безопасно ли Фаза II Лекарственная субстанция лекарство? Эффективно ли Фаза III эффективность лекарства Фаза IV при двойном слепом контроле Химический синтез 2 года Метаболизм лекарств, оценка безопасности 2 года Ю. Б. Белоусов, С. К. Зырянов Качественная клиническая практика. - 2003. - № 2. - С. 95 -100 4 -5 лет
Этапы создания и система одобрения оригинального ЛС Изучение in Vitro Биологические продукты Проверка на животных Клинические испытания Эффективность Селективность Фаза I Механизм действия лекарство? Безопасно ли Фаза II Лекарственная субстанция лекарство? Эффективно ли Фаза III эффективность лекарства Фаза IV при двойном слепом контроле Химический синтез 2 года Метаболизм лекарств, оценка безопасности 2 года Ю. Б. Белоусов, С. К. Зырянов Качественная клиническая практика. - 2003. - № 2. - С. 95 -100 4 -5 лет
 Биоэквивалентность Эквивалентность скорости и степени всасывания оригинала и генерика в одинаковых дозах по концентрации в жидкостях и тканях организма Проводится на небольших (18 -24 человека) гомогенных группах здоровых некурящих испытуемых, мужского пола в возрасте 18 - 55 лет, не получающих каких-либо медикаментозных средств, обладающих нормальным ростом и весом, придерживающихся стабильной диеты Генерик и оригинальный препарат назначается в течение одного дня в одной и той же суточной дозе Если концентрация генерика укладывается в пределы от +25% оригинального препарата, то считается, что биоэквивалентность подтверждена -20%, до Meyer MC. Generic drug product equivalence: Current status. Am J Manag Care. 1998; 4: 1183 -1189.
Биоэквивалентность Эквивалентность скорости и степени всасывания оригинала и генерика в одинаковых дозах по концентрации в жидкостях и тканях организма Проводится на небольших (18 -24 человека) гомогенных группах здоровых некурящих испытуемых, мужского пола в возрасте 18 - 55 лет, не получающих каких-либо медикаментозных средств, обладающих нормальным ростом и весом, придерживающихся стабильной диеты Генерик и оригинальный препарат назначается в течение одного дня в одной и той же суточной дозе Если концентрация генерика укладывается в пределы от +25% оригинального препарата, то считается, что биоэквивалентность подтверждена -20%, до Meyer MC. Generic drug product equivalence: Current status. Am J Manag Care. 1998; 4: 1183 -1189.
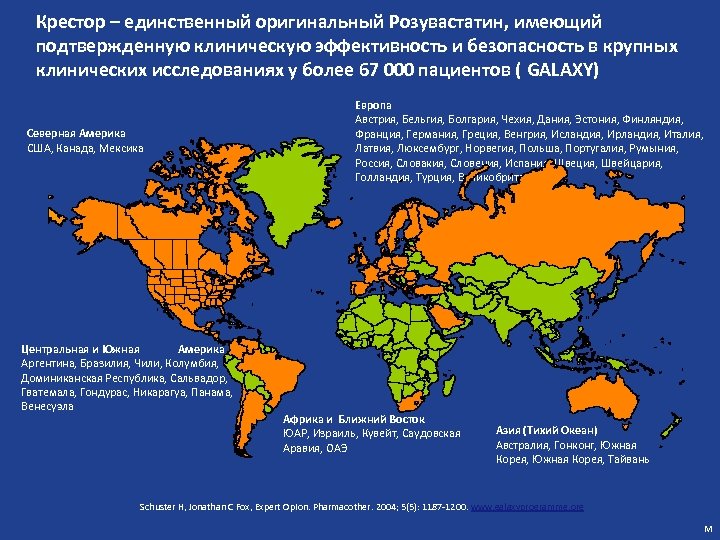 Крестор – единственный оригинальный Розувастатин, имеющий подтвержденную клиническую эффективность и безопасность в крупных клинических исследованиях у более 67 000 пациентов ( GALAXY) Северная Америка США, Канада, Мексика Центральная и Южная Америка Аргентина, Бразилия, Чили, Колумбия, Доминиканская Республика, Сальвадор, Гватемала, Гондурас, Никарагуа, Панама, Венесуэла Европа Австрия, Бельгия, Болгария, Чехия, Дания, Эстония, Финляндия, Франция, Германия, Греция, Венгрия, Исландия, Ирландия, Италия, Латвия, Люксембург, Норвегия, Польша, Португалия, Румыния, Россия, Словакия, Словения, Испания, Швеция, Швейцария, Голландия, Турция, Великобритания Африка и Ближний Восток ЮАР, Израиль, Кувейт, Саудовская Аравия, ОАЭ Азия (Тихий Океан) Австралия, Гонконг, Южная Корея, Тайвань Schuster H, Jonathan C Fox, Expert Opion. Pharmacother. 2004; 5(5): 1187 -1200. www. galaxyprogramme. org М
Крестор – единственный оригинальный Розувастатин, имеющий подтвержденную клиническую эффективность и безопасность в крупных клинических исследованиях у более 67 000 пациентов ( GALAXY) Северная Америка США, Канада, Мексика Центральная и Южная Америка Аргентина, Бразилия, Чили, Колумбия, Доминиканская Республика, Сальвадор, Гватемала, Гондурас, Никарагуа, Панама, Венесуэла Европа Австрия, Бельгия, Болгария, Чехия, Дания, Эстония, Финляндия, Франция, Германия, Греция, Венгрия, Исландия, Ирландия, Италия, Латвия, Люксембург, Норвегия, Польша, Португалия, Румыния, Россия, Словакия, Словения, Испания, Швеция, Швейцария, Голландия, Турция, Великобритания Африка и Ближний Восток ЮАР, Израиль, Кувейт, Саудовская Аравия, ОАЭ Азия (Тихий Океан) Австралия, Гонконг, Южная Корея, Тайвань Schuster H, Jonathan C Fox, Expert Opion. Pharmacother. 2004; 5(5): 1187 -1200. www. galaxyprogramme. org М

 ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ КРЕСТОРА ПОДТВЕРЖДЕНА В КЛИНИЧЕСКИХ ИССЛЕДОВАНИЯХ У БОЛЕЕ 67 000 ПАЦИЕНТОВ Только исследование на биоэквивалентность на 18 -24 здоровых добровольцах3 Ген ери к к и енер Г ОБЪЯСНИТЕ ВАШИМ ПАЦИЕНТАМ РАЗНИЦУ МЕЖДУ ОРИГИНАЛЬНЫМ ПРЕПАРАТОМ И ГЕНЕРИКОМ! 1 - Инструкция по медицинскому применению лекарственного препарата Крестор (таблетки, покрытые оболочкой, 10, 20, 40 мг), РУ П N 015644/01 (Изменение № 5) 2 - Press releases Tuesday, 15 November 2011/Media//Официальный сайт компании astrazeneca. com. [Электронный ресурс], август 2012. URL: http: //www. astrazeneca. com/Media/Press-releases/Article/20111115 --saturn-results-aha US FDA Approves New Indication for Crestor (Rosuvastatin Calcium)// Медицинский портал invasivecardiology. com [электронный ресурс], 26 июля 2011 г URL: http: //www. invasivecardiology. com/US-FDA-Approves-new-Indication-Crestor. Rosuvastatin-Calcium 3. Ю. Б. Белоусов, С. К. Зырянов Качественная клиническая практика. - 2003. - № 2. - С. 95 -100
ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ КРЕСТОРА ПОДТВЕРЖДЕНА В КЛИНИЧЕСКИХ ИССЛЕДОВАНИЯХ У БОЛЕЕ 67 000 ПАЦИЕНТОВ Только исследование на биоэквивалентность на 18 -24 здоровых добровольцах3 Ген ери к к и енер Г ОБЪЯСНИТЕ ВАШИМ ПАЦИЕНТАМ РАЗНИЦУ МЕЖДУ ОРИГИНАЛЬНЫМ ПРЕПАРАТОМ И ГЕНЕРИКОМ! 1 - Инструкция по медицинскому применению лекарственного препарата Крестор (таблетки, покрытые оболочкой, 10, 20, 40 мг), РУ П N 015644/01 (Изменение № 5) 2 - Press releases Tuesday, 15 November 2011/Media//Официальный сайт компании astrazeneca. com. [Электронный ресурс], август 2012. URL: http: //www. astrazeneca. com/Media/Press-releases/Article/20111115 --saturn-results-aha US FDA Approves New Indication for Crestor (Rosuvastatin Calcium)// Медицинский портал invasivecardiology. com [электронный ресурс], 26 июля 2011 г URL: http: //www. invasivecardiology. com/US-FDA-Approves-new-Indication-Crestor. Rosuvastatin-Calcium 3. Ю. Б. Белоусов, С. К. Зырянов Качественная клиническая практика. - 2003. - № 2. - С. 95 -100
 …ЧТО ПОЛУЧАЕТ ВРАЧ ВЫБИРАЯ КРЕСТОР…? УВЕРЕННОСТЬ В ЭФФЕКТИВНОСТИ 1 УВЕРЕННОСТЬ В ХОРОШЕЙ ПЕРЕНОСИМОСТИ 2 УВЕРЕННОСТЬ В УЛУЧШЕНИИ ПРОГНОЗА УВЕРЕННОСТЬ В ИЗУЧЕННОСТИ У 4 ПАЦИЕНТОВ С ДИСЛИПИДЕМИЕЙ 1. Jones PH, Davidson MH, Stein EA, et al. Am. J. Cardiology 2003; 93: 152 -160. 2. Brewer H Am J Cardiol 2003; 92(Suppl): 23 K– 29 K 3. Ridker P et al. N Eng J Med 2008; 359: 2195 -2207 4. Schuster H, Fox J. Exp Opin Pharmacother 2004; 5: 1187 -1200 3
…ЧТО ПОЛУЧАЕТ ВРАЧ ВЫБИРАЯ КРЕСТОР…? УВЕРЕННОСТЬ В ЭФФЕКТИВНОСТИ 1 УВЕРЕННОСТЬ В ХОРОШЕЙ ПЕРЕНОСИМОСТИ 2 УВЕРЕННОСТЬ В УЛУЧШЕНИИ ПРОГНОЗА УВЕРЕННОСТЬ В ИЗУЧЕННОСТИ У 4 ПАЦИЕНТОВ С ДИСЛИПИДЕМИЕЙ 1. Jones PH, Davidson MH, Stein EA, et al. Am. J. Cardiology 2003; 93: 152 -160. 2. Brewer H Am J Cardiol 2003; 92(Suppl): 23 K– 29 K 3. Ridker P et al. N Eng J Med 2008; 359: 2195 -2207 4. Schuster H, Fox J. Exp Opin Pharmacother 2004; 5: 1187 -1200 3
 Крестор – единственный оригинальный Розувастатин, имеющий подтвержденную клиническую эффективность и безопасность в крупных клинических исследованиях у более 67 000 пациентов Ridker P et al. N Eng J Med 2008; 359: 2195 -2207
Крестор – единственный оригинальный Розувастатин, имеющий подтвержденную клиническую эффективность и безопасность в крупных клинических исследованиях у более 67 000 пациентов Ridker P et al. N Eng J Med 2008; 359: 2195 -2207
 l СПАСИБО! l ЗДОРОВЬЯ ВАМ И ВАШИМ БЛИЗКИМ!
l СПАСИБО! l ЗДОРОВЬЯ ВАМ И ВАШИМ БЛИЗКИМ!


