Кремний.ppt
- Количество слайдов: 24
 КРЕМНИЙ Получен в 1811 г, природные соединения известны давно. Электронный аналог углерода. У кремния больше размер атома, меньшая энергия ионизации, большее сродство к электрону и большая поляризуемость атома, чем у углерода. рπ рπ связывание для кремния не характерно, т. е. sр и sр2 гибридные состояния для него не устойчивы. В соединениях имеет степени окисления +4, -4. Для кремния характерны связи Si-F и Si-О.
КРЕМНИЙ Получен в 1811 г, природные соединения известны давно. Электронный аналог углерода. У кремния больше размер атома, меньшая энергия ионизации, большее сродство к электрону и большая поляризуемость атома, чем у углерода. рπ рπ связывание для кремния не характерно, т. е. sр и sр2 гибридные состояния для него не устойчивы. В соединениях имеет степени окисления +4, -4. Для кремния характерны связи Si-F и Si-О.
 Сравнение углерода и кремния
Сравнение углерода и кремния
 Нахождение в природе: По распространению кремния занимает второе место после кислорода. Природные минералы 2 Si. О 2 2 Н 2 О гранит, слюда, силикатные и алюмосиликатные минералы: ортоклаз К 2 О А 12 О 3 6 Si. О 2 и др. Земная кора более, чем на половину состоит из кремнезема. Si. О 2 встречается обычно в виде песка.
Нахождение в природе: По распространению кремния занимает второе место после кислорода. Природные минералы 2 Si. О 2 2 Н 2 О гранит, слюда, силикатные и алюмосиликатные минералы: ортоклаз К 2 О А 12 О 3 6 Si. О 2 и др. Земная кора более, чем на половину состоит из кремнезема. Si. О 2 встречается обычно в виде песка.
 Простое вещество: Твердое вещество с блеском. Характерный тип гибридизации валентных орбиталей (sр3). Устойчива алмазоподобная (кубическая) модификация: тугоплавкая (tпл = 14150 С), с высокой твердостью, темно-серого цвета. При комнатной температуре полупроводник. При нагревании элетропроводность увеличивается. Гексагональная (графитоподобная) модификация кремния неустойчивая. Применение: 1) полупроводник в электронике; 2) изготовление солнечных батарей; 3) получение кислотоупорных сталей. Получение: 1) Кремний технически чистый (95 -98%): Si. О 2 +С=Si+CO 2 2) Кремний высокочистый полупроводниковый (содержание примесей менее 10 -5%): 9500 С Si. C 14(пар) + Zn(пар) = Si. Н 4 = Si + 2 Н 2 Si + 2 Zn. C 12
Простое вещество: Твердое вещество с блеском. Характерный тип гибридизации валентных орбиталей (sр3). Устойчива алмазоподобная (кубическая) модификация: тугоплавкая (tпл = 14150 С), с высокой твердостью, темно-серого цвета. При комнатной температуре полупроводник. При нагревании элетропроводность увеличивается. Гексагональная (графитоподобная) модификация кремния неустойчивая. Применение: 1) полупроводник в электронике; 2) изготовление солнечных батарей; 3) получение кислотоупорных сталей. Получение: 1) Кремний технически чистый (95 -98%): Si. О 2 +С=Si+CO 2 2) Кремний высокочистый полупроводниковый (содержание примесей менее 10 -5%): 9500 С Si. C 14(пар) + Zn(пар) = Si. Н 4 = Si + 2 Н 2 Si + 2 Zn. C 12
 3) В лаборатории в качестве восстановителя используют магний. При этом образуется сильно загрязненный примесями коричневый порошок кремния.
3) В лаборатории в качестве восстановителя используют магний. При этом образуется сильно загрязненный примесями коричневый порошок кремния.
 Химические свойства: 1)В обычных условиях инертен. 2) При нагревании реагирует с: при 4000 С: Si + С 12 = Si. С 12 ; при 6000 С: Si + О 2 = Si. О 2 ; при 10000 С: 3 Si +2 N 2 = Si 3 N 4; при 20000 С: Si + С = Si. C. 3) Пассивируется в кислородсодержащих кислотах – окислителях. 4) Растворяется в смеси кислот: плавиковой и азотной: 3 Si+4 НNО 3+18 НF=3 Н 2 Si. F 6+ 4 NО +8 Н 2 О В этой реакции НNО 3 – окислитель, НF – комплексообразующая среда. Кремний переходит в устойчивую степень окисления +4. 5) С водой в обычных условиях не реагирует, но при высокой температуре протекает процесс: Si + 3 Н 2 О(г) = Н 2 Si. О 3 + 2 Н 2(г)
Химические свойства: 1)В обычных условиях инертен. 2) При нагревании реагирует с: при 4000 С: Si + С 12 = Si. С 12 ; при 6000 С: Si + О 2 = Si. О 2 ; при 10000 С: 3 Si +2 N 2 = Si 3 N 4; при 20000 С: Si + С = Si. C. 3) Пассивируется в кислородсодержащих кислотах – окислителях. 4) Растворяется в смеси кислот: плавиковой и азотной: 3 Si+4 НNО 3+18 НF=3 Н 2 Si. F 6+ 4 NО +8 Н 2 О В этой реакции НNО 3 – окислитель, НF – комплексообразующая среда. Кремний переходит в устойчивую степень окисления +4. 5) С водой в обычных условиях не реагирует, но при высокой температуре протекает процесс: Si + 3 Н 2 О(г) = Н 2 Si. О 3 + 2 Н 2(г)
 6) Растворяется в щелочах с выделением водорода: Si +Н 2 О + 2 Na. ОН = Na 2 Si. О 3 + 2 Н 2 При этом Н 2 О – окислитель, КОН – комплексообразующая среда.
6) Растворяется в щелочах с выделением водорода: Si +Н 2 О + 2 Na. ОН = Na 2 Si. О 3 + 2 Н 2 При этом Н 2 О – окислитель, КОН – комплексообразующая среда.
 СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ -4 Окислительная активность кремния проявляется по отношению к металлам: 2 Мg + Si = Мg 2 Si. Образуются силициды. Силициды под действием кислот легко разлагаются: Са 2 Si + 4 НС 1 = 2 Са. С 12 + 2 Si. Н 4 – силан
СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ -4 Окислительная активность кремния проявляется по отношению к металлам: 2 Мg + Si = Мg 2 Si. Образуются силициды. Силициды под действием кислот легко разлагаются: Са 2 Si + 4 НС 1 = 2 Са. С 12 + 2 Si. Н 4 – силан
 Силан – газообразное вещество, на воздухе самовоспламеняется: Si. H 4 + 2 О 2 = Si. О 2 + 2 Н 2 О Гомоцепи Si-Si- образуются в гидридах (силанах). Силаны по свойствам сходны с соответствующими углеводородами. В обычных условиях моносилан Si. Н 4 и дисилан Si 2 Н 6 газообразны, трисилан Si 3 Н 8 - жидкость , высшие представители гомологического ряда – полимеры. Химические свойства: Связи Si-Н и Si-Si слабее связей С-Н и С-С, и кремневодороды менее устойчивы и более реакционноспособны, чем углеводороды. 1)С галогенами взаимодействуют со взрывом. 2)Кислотные гидриды, реагируют даже со следами щелочей. 3)В нейтральной и кислой средах устойчивы.
Силан – газообразное вещество, на воздухе самовоспламеняется: Si. H 4 + 2 О 2 = Si. О 2 + 2 Н 2 О Гомоцепи Si-Si- образуются в гидридах (силанах). Силаны по свойствам сходны с соответствующими углеводородами. В обычных условиях моносилан Si. Н 4 и дисилан Si 2 Н 6 газообразны, трисилан Si 3 Н 8 - жидкость , высшие представители гомологического ряда – полимеры. Химические свойства: Связи Si-Н и Si-Si слабее связей С-Н и С-С, и кремневодороды менее устойчивы и более реакционноспособны, чем углеводороды. 1)С галогенами взаимодействуют со взрывом. 2)Кислотные гидриды, реагируют даже со следами щелочей. 3)В нейтральной и кислой средах устойчивы.
 Получение силанов: Мg 2 Si + 2 Н 2 SО 4===== Si. Н 4 + 2 Мg. SО 4 в жид. аммиаке Мg 2 Si + 4 NН 4 Вr==== Si. Н 4 + 2 Мg. Вr 2 + 4 NН 3 Гидриды с двойными и тройными связями, аналоги этилена, ацетилена, бензола – неизвестны, т. к. связи типа рπ-рπ для кремния не характерны. Силициды металлов имеют полупроводниковый или металлический характер и переменный состав. Многие кислотоупорны и тугоплавки. Из Мо. Si 2 делают электронагреватели печей, работающие в агрессивных средах.
Получение силанов: Мg 2 Si + 2 Н 2 SО 4===== Si. Н 4 + 2 Мg. SО 4 в жид. аммиаке Мg 2 Si + 4 NН 4 Вr==== Si. Н 4 + 2 Мg. Вr 2 + 4 NН 3 Гидриды с двойными и тройными связями, аналоги этилена, ацетилена, бензола – неизвестны, т. к. связи типа рπ-рπ для кремния не характерны. Силициды металлов имеют полупроводниковый или металлический характер и переменный состав. Многие кислотоупорны и тугоплавки. Из Мо. Si 2 делают электронагреватели печей, работающие в агрессивных средах.
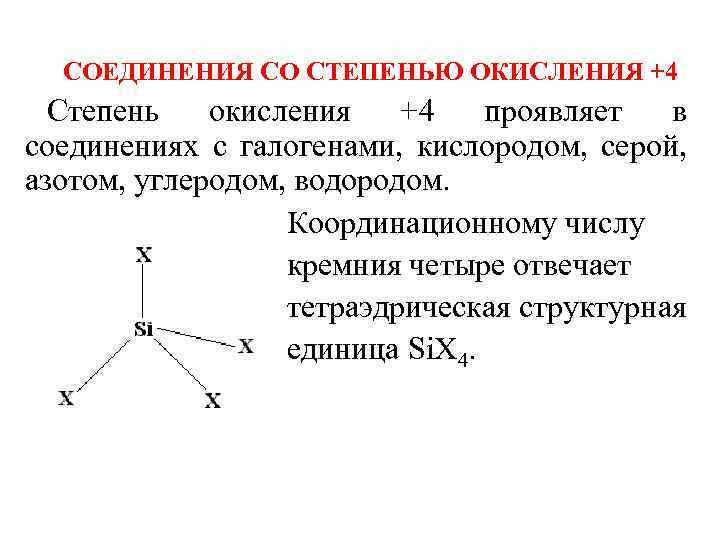 СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +4 Степень окисления +4 проявляет в соединениях с галогенами, кислородом, серой, азотом, углеродом, водородом. Координационному числу кремния четыре отвечает тетраэдрическая структурная единица Si. Х 4.
СОЕДИНЕНИЯ СО СТЕПЕНЬЮ ОКИСЛЕНИЯ +4 Степень окисления +4 проявляет в соединениях с галогенами, кислородом, серой, азотом, углеродом, водородом. Координационному числу кремния четыре отвечает тетраэдрическая структурная единица Si. Х 4.
 Химические свойства: Кислотные соединения. 1) Взаимодействуют с щелочами (в растворах и при сплавлении): сплавление Si. О 2 + Са(ОН)2=======Са. Si. О 3 + Н 2 О Si. Н 4 + 2 КОН + Н 2 О = Н 2 Si. О 3 + Н 2 2)Взаимодействуют с другими основными соединениями: Ca. S + Si. S 2=Са. Si. S 3 3) При гидролизе образуют кислоты: Si. C 14+3 Н 2 О = Н 2 Si. О 3 + 4 НС 1 Si. S 2 + 3 Н 2 О = Н 2 Si. О 3 + 2 Н 2 S
Химические свойства: Кислотные соединения. 1) Взаимодействуют с щелочами (в растворах и при сплавлении): сплавление Si. О 2 + Са(ОН)2=======Са. Si. О 3 + Н 2 О Si. Н 4 + 2 КОН + Н 2 О = Н 2 Si. О 3 + Н 2 2)Взаимодействуют с другими основными соединениями: Ca. S + Si. S 2=Са. Si. S 3 3) При гидролизе образуют кислоты: Si. C 14+3 Н 2 О = Н 2 Si. О 3 + 4 НС 1 Si. S 2 + 3 Н 2 О = Н 2 Si. О 3 + 2 Н 2 S
 ДИОКСИД КРЕМНИЯ Физические свойства: Твердое кристаллическое вещество, Тпл= 17130 С, Ткип=25900 С. Нахождение в природе: Обычный и кварцевый песок, крупные кристаллы горного хрусталя, аметиста, агата, яшмы. Кварцевый песок используется в производстве стекла, цемента, фарфора и др. Si. О 2 – кремнезем, кристаллическая модификация диоксида кремния – легко переходит в стеклообразное состояние. Аморфный кремнезем является также основой ряда минералов: халцедона, опала, агата и др. В аморфной модификации Si. О 2 - в кварцевом стекле тетраэдрические единицы Si. О 4 расположены неупорядочено. Кварцевое стекло химически и термически устойчиво. Его применяют для изготовления химической аппаратуры и в оптических приборах. При сверхвысоком давлении и нагревании получена особая модификация Si. О 2, названная стишовитом. Стишовит имеет плотность на 60% выше плотности кварца, т. к. к него более плотная структура. Стишовит менее активен, чем кварц, устойчив даже к действию концентрированной плавиковой кислоты.
ДИОКСИД КРЕМНИЯ Физические свойства: Твердое кристаллическое вещество, Тпл= 17130 С, Ткип=25900 С. Нахождение в природе: Обычный и кварцевый песок, крупные кристаллы горного хрусталя, аметиста, агата, яшмы. Кварцевый песок используется в производстве стекла, цемента, фарфора и др. Si. О 2 – кремнезем, кристаллическая модификация диоксида кремния – легко переходит в стеклообразное состояние. Аморфный кремнезем является также основой ряда минералов: халцедона, опала, агата и др. В аморфной модификации Si. О 2 - в кварцевом стекле тетраэдрические единицы Si. О 4 расположены неупорядочено. Кварцевое стекло химически и термически устойчиво. Его применяют для изготовления химической аппаратуры и в оптических приборах. При сверхвысоком давлении и нагревании получена особая модификация Si. О 2, названная стишовитом. Стишовит имеет плотность на 60% выше плотности кварца, т. к. к него более плотная структура. Стишовит менее активен, чем кварц, устойчив даже к действию концентрированной плавиковой кислоты.
 Химические свойства: 1)В воде Si. О 2 нерастворим. 2)Кислоты на него не действуют, кроме НF: Si. О 2+4 НF=Si. F 4+2 Н 2 О 3) Сплавляется со щелочами или карбонатами щелочных металлов: Si. О 2 +2 КОН = К 2 Si. О 3 + Н 2 О Si. О 2 + К 2 СО 3 = К 2 Si. О 3 + СО 2 Реакция сводится к выделению Н 2 СО 3 кремневой кислотой. 4) Реагирует со щелочами: Si. О 2 + 2 Nа. ОН = Nа 2 Si. О 3 + Н 2 О
Химические свойства: 1)В воде Si. О 2 нерастворим. 2)Кислоты на него не действуют, кроме НF: Si. О 2+4 НF=Si. F 4+2 Н 2 О 3) Сплавляется со щелочами или карбонатами щелочных металлов: Si. О 2 +2 КОН = К 2 Si. О 3 + Н 2 О Si. О 2 + К 2 СО 3 = К 2 Si. О 3 + СО 2 Реакция сводится к выделению Н 2 СО 3 кремневой кислотой. 4) Реагирует со щелочами: Si. О 2 + 2 Nа. ОН = Nа 2 Si. О 3 + Н 2 О
 Сравнение соединений кремния и углерода
Сравнение соединений кремния и углерода
 Кремневая кислота Н 2 Si. О 3 Физические свойства: студенистое, нерастворимое в воде вещество, хорошо растворимая в щелочах. Химические свойства: 1) Н 2 Si. О 3 слабая , малоустойчивая кислота. В растворе угольная кислота выделяет кремниевую из её солей, а при прокаливании происходит обратное выделение. К 2 Si. О 3+СО 2+Н 2 О=К 2 СО 3+Н 2 Si. О 3 К 2 Si. О 3+2 СО 2+2 Н 2 О=2 КНСО 3+Н 2 Si. О 3 выделение в растворе ―――――――――→ НС 1 Н 2 SО 4 Н 3 РО 4 Н 2 Si. О 3 ←————————— выделение при прокаливании Перовое направление обусловлено меньшей силой кремниевой кислоты, второе – её меньшей летучестью при нагревании. 2) Образует коллоидные растворы, осаждается частично. Осадок бесцветный студень, состава n. НSi. О 2 m. Н 2 О, где n и m изменяются от условий осаждения. 3) Образует соли метакремниевой Н 2 Si. О 3 или ортакремниевой кислоты Н 4 Si. О 4. 4) При нагревании теряет воду, превращаясь в Si. О 2. Частично обезвоженная Н 2 Si. О 3 (силикагель) используется для адсорбции влаги и других веществ.
Кремневая кислота Н 2 Si. О 3 Физические свойства: студенистое, нерастворимое в воде вещество, хорошо растворимая в щелочах. Химические свойства: 1) Н 2 Si. О 3 слабая , малоустойчивая кислота. В растворе угольная кислота выделяет кремниевую из её солей, а при прокаливании происходит обратное выделение. К 2 Si. О 3+СО 2+Н 2 О=К 2 СО 3+Н 2 Si. О 3 К 2 Si. О 3+2 СО 2+2 Н 2 О=2 КНСО 3+Н 2 Si. О 3 выделение в растворе ―――――――――→ НС 1 Н 2 SО 4 Н 3 РО 4 Н 2 Si. О 3 ←————————— выделение при прокаливании Перовое направление обусловлено меньшей силой кремниевой кислоты, второе – её меньшей летучестью при нагревании. 2) Образует коллоидные растворы, осаждается частично. Осадок бесцветный студень, состава n. НSi. О 2 m. Н 2 О, где n и m изменяются от условий осаждения. 3) Образует соли метакремниевой Н 2 Si. О 3 или ортакремниевой кислоты Н 4 Si. О 4. 4) При нагревании теряет воду, превращаясь в Si. О 2. Частично обезвоженная Н 2 Si. О 3 (силикагель) используется для адсорбции влаги и других веществ.
 Соли кремневой кислоты - силикаты Растворимы соли щелочных металлов. Силикаты – соли метакремниевой кислоты. Продукты полного или частичного замещения водорода в кислоте на металлы называются простыми силикатами, например асбест (Мg 3 НSi 2 О 9 или 3 Мg. О· 2 Н 2 О· 2 Si. О 2).
Соли кремневой кислоты - силикаты Растворимы соли щелочных металлов. Силикаты – соли метакремниевой кислоты. Продукты полного или частичного замещения водорода в кислоте на металлы называются простыми силикатами, например асбест (Мg 3 НSi 2 О 9 или 3 Мg. О· 2 Н 2 О· 2 Si. О 2).
 Более распространены в природе сложные силикаты, например, алюмосиликаты, относящиеся к группе полевых шпатов: х. А 12 О 3·у. Si. О 2·z. Н 2 О Основные нерастворимые продукты распада алюмосиликатов - кварц (Si. О 2) и каолин (Н 4 А 12 Si 2 О 9 или А 12 О 3· 2 Si. О 2· 2 Н 2 О). Процесс выветривания алюмосиликатов: К 2 А 12 Si 6 О 16(ортоклаз)+2 Н 2 О+СО 2=К 2 СО 3+Н 4 А 12 Si 2 О 9(каолин)+4 Si. О 2(кварц) Песок и глина создают минеральную основу всех видов почв.
Более распространены в природе сложные силикаты, например, алюмосиликаты, относящиеся к группе полевых шпатов: х. А 12 О 3·у. Si. О 2·z. Н 2 О Основные нерастворимые продукты распада алюмосиликатов - кварц (Si. О 2) и каолин (Н 4 А 12 Si 2 О 9 или А 12 О 3· 2 Si. О 2· 2 Н 2 О). Процесс выветривания алюмосиликатов: К 2 А 12 Si 6 О 16(ортоклаз)+2 Н 2 О+СО 2=К 2 СО 3+Н 4 А 12 Si 2 О 9(каолин)+4 Si. О 2(кварц) Песок и глина создают минеральную основу всех видов почв.
 Применение соединений кремния: 1)Жидкое (растворимое) стекло (соли К, Nа) и твердое стекло (соли Са). 2)Получение стекла: 6 Si. О 2+Са. СО 3+Nа 2 СО 3=Nа 2 О·Са. О· 6 Si. О 2 + 2 СО 2 Стекло - трехмерный аморфный полимер, свойства можно изменять, вводя добавки в процессе его приготовления: Fe 3+ придает стеклу зеленый цвет, Со 2+ - синий, Сr 3+-изумрудный, Мn 2+ - фиолетовый. Для получения хрусталя в смесь вводят Рb. О, добавки В 2 О 3 - термостойкое стекло, Ва. О –йенское стекло. Вода частично разлагает стекло, вымывая с поверхности натрий. Подобно воде действуют и кислоты (кроме НF) – стекло, находившееся в контакте с водой и кислотами дальше практически не разрушается. Действие на стекло щелочей имеет длительный характер. Поэтому хранящиеся в стеклянной посуде щелочные жидкости обычно содержат примеси растворимых силикатов.
Применение соединений кремния: 1)Жидкое (растворимое) стекло (соли К, Nа) и твердое стекло (соли Са). 2)Получение стекла: 6 Si. О 2+Са. СО 3+Nа 2 СО 3=Nа 2 О·Са. О· 6 Si. О 2 + 2 СО 2 Стекло - трехмерный аморфный полимер, свойства можно изменять, вводя добавки в процессе его приготовления: Fe 3+ придает стеклу зеленый цвет, Со 2+ - синий, Сr 3+-изумрудный, Мn 2+ - фиолетовый. Для получения хрусталя в смесь вводят Рb. О, добавки В 2 О 3 - термостойкое стекло, Ва. О –йенское стекло. Вода частично разлагает стекло, вымывая с поверхности натрий. Подобно воде действуют и кислоты (кроме НF) – стекло, находившееся в контакте с водой и кислотами дальше практически не разрушается. Действие на стекло щелочей имеет длительный характер. Поэтому хранящиеся в стеклянной посуде щелочные жидкости обычно содержат примеси растворимых силикатов.
 3) Изготовление кварцевого стекла Ампулы источников УФ изготовляют из кварцевого стекла, которое из -за тугоплавкости чистого Si. О 2 с трудом поддается обработке и отличается хрупкостью.
3) Изготовление кварцевого стекла Ампулы источников УФ изготовляют из кварцевого стекла, которое из -за тугоплавкости чистого Si. О 2 с трудом поддается обработке и отличается хрупкостью.
 Кварцевое стекло не боится резких перепадов температур.
Кварцевое стекло не боится резких перепадов температур.
 4) Изготовление ситалл: Ситаллы (закристаллизованные стекла) – обладают повышенной прочностью, твердостью, химической устойчивостью, высокой температурой размягчения (15000 С), не боятся резких перепадов температур. Получают при введении в расплавленное стекло специальных добавок (тонкоизмельченные порошки благородных металлов, Сu, Тi. О 2). Вокруг зерен добавки, которые становятся центрами кристаллизации стекла, происходит рост кристаллов стекла при охлаждении его расплава.
4) Изготовление ситалл: Ситаллы (закристаллизованные стекла) – обладают повышенной прочностью, твердостью, химической устойчивостью, высокой температурой размягчения (15000 С), не боятся резких перепадов температур. Получают при введении в расплавленное стекло специальных добавок (тонкоизмельченные порошки благородных металлов, Сu, Тi. О 2). Вокруг зерен добавки, которые становятся центрами кристаллизации стекла, происходит рост кристаллов стекла при охлаждении его расплава.
 5) Концентрированный раствор Nа 2 Si. О 3 – жидкое стекло, применяют как клей, для пропитки тканей и дерева для придания им не горючести, для укрепления грунта при строительстве. 6) Производство керамики: основано на превращении пластического сырья в твердые прочные термостойкие изделия нужной формы. Реакция фарфорово-фаянсовой промышленности: обжиг каолина: 3(А 12 О 3· 2 Si. О 2· 2 Н 2 О) = 3 А 12 О 3(муллит) + 6 Si. О 2 + 6 Н 2 О. 6) Вяжущие вещества: Цементы – смесь силикатов и алюминатов кальция. Различают силикатный (портландцемент) и алюминатный (глиноземистый) цемент. Силикатный получают обжигом (до спекания) смеси глины (богатой Si. О 2) с известняком.
5) Концентрированный раствор Nа 2 Si. О 3 – жидкое стекло, применяют как клей, для пропитки тканей и дерева для придания им не горючести, для укрепления грунта при строительстве. 6) Производство керамики: основано на превращении пластического сырья в твердые прочные термостойкие изделия нужной формы. Реакция фарфорово-фаянсовой промышленности: обжиг каолина: 3(А 12 О 3· 2 Si. О 2· 2 Н 2 О) = 3 А 12 О 3(муллит) + 6 Si. О 2 + 6 Н 2 О. 6) Вяжущие вещества: Цементы – смесь силикатов и алюминатов кальция. Различают силикатный (портландцемент) и алюминатный (глиноземистый) цемент. Силикатный получают обжигом (до спекания) смеси глины (богатой Si. О 2) с известняком.
 Другие соединеия кремния Карбид кремния Si. С (карборунд) – существует в виде кубической (алмазоподобной) и гексагональной модификации. В чистом виде диэлектрик, но с примесями становится полупроводником и n – или р-проводимостью. Тугоплавок (tпл=28300 С), по твердости близок к алмазу, химически стоек. Разрушается лишь при нагревании с НF+НNО 3 и при сплавлении со щелочами в присутствии окислителя: Si. С + 2 КОН + 2 О 2 = К 2 Si. О 3 + СО 2 +Н 2 О Получают в дуговых электропечах ( при 2000 -22000 С) из смеси кварцевого песка и кокса, применяется как абразивный материал, в радиотехнике. Нитрид кремния Si 3 N 4 – кристаллическое вещество, бесцветно, проявляет полупроводниковые свойства, жаропрочен, химически стоек, твердый тугоплавкий порошок (tвозг=19000 С). Устойчив к воздействиям НF, растворов щелочей. Используют в качестве химически стойкого огнеупорного материала, в создании коррозионностойких и тугоплавких сплавов, в качестве высокотемпературного полупроводника. Соединения кремния, в которых его атомы связаны с атомами углерода, входящими в состав органических радикалов называют кремнийорганическими соединениями. В зависимости от характера цепи и природы обрамляющих радикалов среди кремнийорганических соединений встречаются смолы, каучуки, масла и др. Общее свойство полимерных кремнийорганических соединений – относительно высокая теплостойкость.
Другие соединеия кремния Карбид кремния Si. С (карборунд) – существует в виде кубической (алмазоподобной) и гексагональной модификации. В чистом виде диэлектрик, но с примесями становится полупроводником и n – или р-проводимостью. Тугоплавок (tпл=28300 С), по твердости близок к алмазу, химически стоек. Разрушается лишь при нагревании с НF+НNО 3 и при сплавлении со щелочами в присутствии окислителя: Si. С + 2 КОН + 2 О 2 = К 2 Si. О 3 + СО 2 +Н 2 О Получают в дуговых электропечах ( при 2000 -22000 С) из смеси кварцевого песка и кокса, применяется как абразивный материал, в радиотехнике. Нитрид кремния Si 3 N 4 – кристаллическое вещество, бесцветно, проявляет полупроводниковые свойства, жаропрочен, химически стоек, твердый тугоплавкий порошок (tвозг=19000 С). Устойчив к воздействиям НF, растворов щелочей. Используют в качестве химически стойкого огнеупорного материала, в создании коррозионностойких и тугоплавких сплавов, в качестве высокотемпературного полупроводника. Соединения кремния, в которых его атомы связаны с атомами углерода, входящими в состав органических радикалов называют кремнийорганическими соединениями. В зависимости от характера цепи и природы обрамляющих радикалов среди кремнийорганических соединений встречаются смолы, каучуки, масла и др. Общее свойство полимерных кремнийорганических соединений – относительно высокая теплостойкость.


