 Красноярский край. г. Минусинск. МОУ «СОШ № 16» Проектная работа: Периодическая система химических элементов в POWER POINT Выполнила: Учитель химии высшей квалификационной категории Генералова Тамара Яковлевна 11. 03. 2009 Генералова Т. Я.
Красноярский край. г. Минусинск. МОУ «СОШ № 16» Проектная работа: Периодическая система химических элементов в POWER POINT Выполнила: Учитель химии высшей квалификационной категории Генералова Тамара Яковлевна 11. 03. 2009 Генералова Т. Я.
 Пери оды Ряды Периодическая система химических элементов Д. И. Менделеева 1 2 3 4 5 6 Группы элементов I 1 1 H 1, 00797 II III Si IV V 14 VI VIII 2 He 4, 0026 4 Гелий 3 4 5 6 7 8 9 10 2 Li 6, 939 Be 9, 0122 В 10, 811 С 812, 0112 N 14, 0067 O 15, 9994 F 18, 9984 Ne 20, 163 Литий Вериллий Бор Углерод 28, 086 Кислород Фтор Азот Неон 2 11 12 13 16 18 14 15 17 3 Na 22, 989 Mg 24, 312 Al 26, 982 Si 28, 086 Р 30, 9738 S 32, 064 Cl 35, 453 Ar 39, 948 Кремний Натрий Магний Алюминий Кремний 1824 г. Сера Фосфор Хлор Аргон Silicium Й. Берцелиус 4 Водород 5 6 7 8 9 7 10 Найди горячую зону
Пери оды Ряды Периодическая система химических элементов Д. И. Менделеева 1 2 3 4 5 6 Группы элементов I 1 1 H 1, 00797 II III Si IV V 14 VI VIII 2 He 4, 0026 4 Гелий 3 4 5 6 7 8 9 10 2 Li 6, 939 Be 9, 0122 В 10, 811 С 812, 0112 N 14, 0067 O 15, 9994 F 18, 9984 Ne 20, 163 Литий Вериллий Бор Углерод 28, 086 Кислород Фтор Азот Неон 2 11 12 13 16 18 14 15 17 3 Na 22, 989 Mg 24, 312 Al 26, 982 Si 28, 086 Р 30, 9738 S 32, 064 Cl 35, 453 Ar 39, 948 Кремний Натрий Магний Алюминий Кремний 1824 г. Сера Фосфор Хлор Аргон Silicium Й. Берцелиус 4 Водород 5 6 7 8 9 7 10 Найди горячую зону
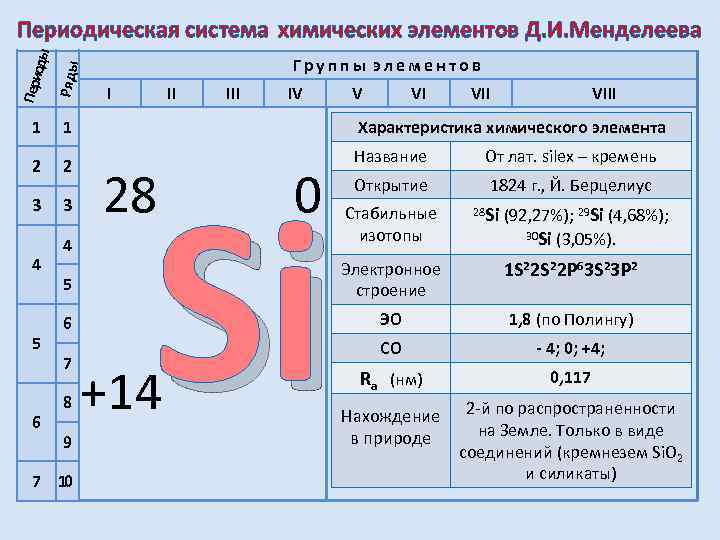 Пери оды Ряды Периодическая система химических элементов Д. И. Менделеева 1 2 3 3 II I III IV 1 2 Группы элементов 4 5 6 7 8 9 7 10 V VI VIII Характеристика химического элемента Si 28 +14 0 Название От лат. silex – кремень Открытие 1824 г. , Й. Берцелиус Стабильные изотопы Si (92, 27%); 29 Si (4, 68%); 30 Si (3, 05%). 28 Электронное строение 1 S 22 P 63 S 23 P 2 ЭО 1, 8 (по Полингу) СО - 4; 0; +4; Ra (нм) 0, 117 Нахождение в природе 2 -й по распространенности на Земле. Только в виде соединений (кремнезем Si. O 2 и силикаты)
Пери оды Ряды Периодическая система химических элементов Д. И. Менделеева 1 2 3 3 II I III IV 1 2 Группы элементов 4 5 6 7 8 9 7 10 V VI VIII Характеристика химического элемента Si 28 +14 0 Название От лат. silex – кремень Открытие 1824 г. , Й. Берцелиус Стабильные изотопы Si (92, 27%); 29 Si (4, 68%); 30 Si (3, 05%). 28 Электронное строение 1 S 22 P 63 S 23 P 2 ЭО 1, 8 (по Полингу) СО - 4; 0; +4; Ra (нм) 0, 117 Нахождение в природе 2 -й по распространенности на Земле. Только в виде соединений (кремнезем Si. O 2 и силикаты)
 Кремний 1. Электронное строение 2. Нахождение в природе; строение кремния 3. Аллотропия кремния 4. Физические свойства 5. Химические свойства 6. Получение и применение 7. Проверка знаний
Кремний 1. Электронное строение 2. Нахождение в природе; строение кремния 3. Аллотропия кремния 4. Физические свойства 5. Химические свойства 6. Получение и применение 7. Проверка знаний
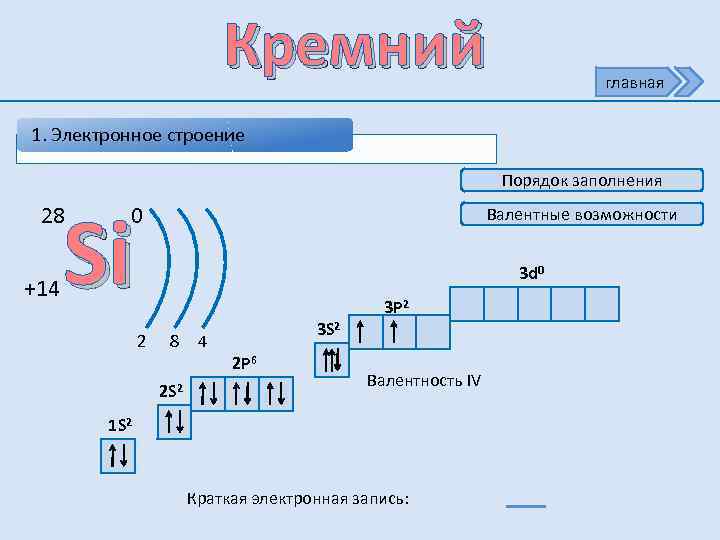 Кремний главная 1. Электронное строение Порядок заполнения Si 28 +14 0 Валентные возможности 3 d 0 3 P 2 2 8 3 S 2 4 2 P 6 2 S 2 Валентность IV 1 S 2 Краткая электронная запись:
Кремний главная 1. Электронное строение Порядок заполнения Si 28 +14 0 Валентные возможности 3 d 0 3 P 2 2 8 3 S 2 4 2 P 6 2 S 2 Валентность IV 1 S 2 Краткая электронная запись:
 Кремний главная 6. Нахождение в природе; строение кремния Кремнийсодержащие минералы Кремнезем Si. O 2 Ортоклаз K 2 O∙Al 2 O 3∙ 6 Si. O 2 Альбит Na 2 O∙Al 2 O 3∙ 6 Si. O 2 Анортит Ca. O∙Al 2 O 3 вывод 2 о Сделайте ∙ 2 Si. O Каолин Кварц Нефелин распространении Si Al O ∙ 2 Si. O Тальк Mg. O∙ 4 Si. O 2∙H 2]O в природе. ∙ 2 H O Si. O 2 Na[Al. Si. O 4 2 3 2 2 Лунный грунт – до 40% Si. O 2 Каменные метеориты – до 20% Si. O 2 Строение кремния 3 S 1 Si 3 Р 3 Какой вид химической связи и тип • • • кристаллической решетки у кремния? Si Si Si* Si
Кремний главная 6. Нахождение в природе; строение кремния Кремнийсодержащие минералы Кремнезем Si. O 2 Ортоклаз K 2 O∙Al 2 O 3∙ 6 Si. O 2 Альбит Na 2 O∙Al 2 O 3∙ 6 Si. O 2 Анортит Ca. O∙Al 2 O 3 вывод 2 о Сделайте ∙ 2 Si. O Каолин Кварц Нефелин распространении Si Al O ∙ 2 Si. O Тальк Mg. O∙ 4 Si. O 2∙H 2]O в природе. ∙ 2 H O Si. O 2 Na[Al. Si. O 4 2 3 2 2 Лунный грунт – до 40% Si. O 2 Каменные метеориты – до 20% Si. O 2 Строение кремния 3 S 1 Si 3 Р 3 Какой вид химической связи и тип • • • кристаллической решетки у кремния? Si Si Si* Si
 Кремний 2. Аллотропия кремния 3. Физические свойства Кристаллический кремний • Тугоплавкое вещество (tпл. =1400°С) темносерого цвета с металлическим блеском, хрупкое, плохо проводит электрический ток. • Неметалл Аморфный кремний • Бурый порошок, не имеющий постоянной температуры плавления. главная
Кремний 2. Аллотропия кремния 3. Физические свойства Кристаллический кремний • Тугоплавкое вещество (tпл. =1400°С) темносерого цвета с металлическим блеском, хрупкое, плохо проводит электрический ток. • Неметалл Аморфный кремний • Бурый порошок, не имеющий постоянной температуры плавления. главная
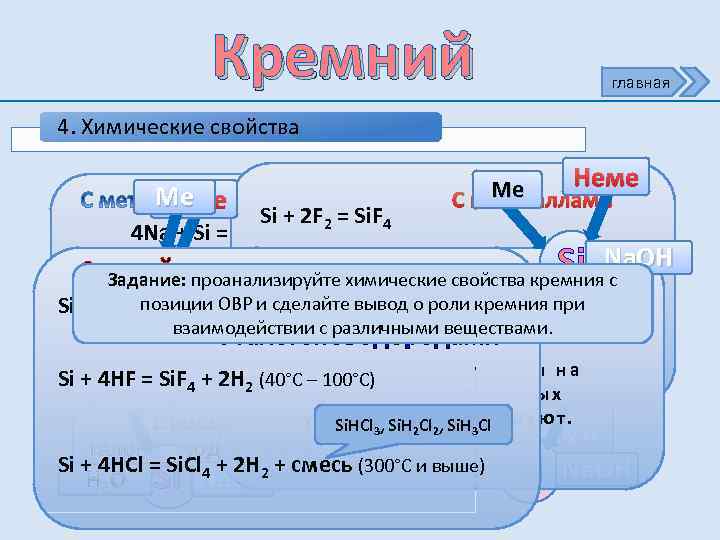 Кремний главная 4. Химические свойства Неме Ме С неметаллами Ме Неме Si + 2 F 2 = Si. F 4 4 Na + Si = Na 4 Si C металлами (сплавление) С неметаллами Si + 2 Cl 2 химические свойства кремния с С водой проанализируйте = Si. Cl 4 (340°C – 420°C) Si Na. OH Задание: Si Н 20 2 Mg + Si = Mg 2 Si (сплавление) позиции + 2 H (400°C вывод о Si + 2 H 2 O = Si. O 2 ОВР и 2 сделайте– 500°C)роли кремния при Si + O с различными Na 2 Si. O 3 + Si + 2 Na. OH + (1200°C – 1300°C) взаимодействии 2 = Si. O 2 H 2 O =веществами. 2 H 2 2 Ca + Si C Ca 2 Si (сплавление) = галогеноводородами М нер Si + – 100°C) л ь н ы к и с л о Si + 4 HF = Si. F 4 + 2 H 2 (40°CCи= Si. Cа(1200°Cе– 1300°C) т ы н а Неме Ме Si кремний при обычных у с л. Si. HCl , я. Si. H н е, Si. H й с т в у ю т. о в и х Cl д е Cl С водой и 3 2 2 3 Со щелочами галогеноводородами Si + 4 HCl = Si. Cl 4 + 2 H 2 + cмесь (300°С и выше) Н 20 Na. OH H 2 O Si Si
Кремний главная 4. Химические свойства Неме Ме С неметаллами Ме Неме Si + 2 F 2 = Si. F 4 4 Na + Si = Na 4 Si C металлами (сплавление) С неметаллами Si + 2 Cl 2 химические свойства кремния с С водой проанализируйте = Si. Cl 4 (340°C – 420°C) Si Na. OH Задание: Si Н 20 2 Mg + Si = Mg 2 Si (сплавление) позиции + 2 H (400°C вывод о Si + 2 H 2 O = Si. O 2 ОВР и 2 сделайте– 500°C)роли кремния при Si + O с различными Na 2 Si. O 3 + Si + 2 Na. OH + (1200°C – 1300°C) взаимодействии 2 = Si. O 2 H 2 O =веществами. 2 H 2 2 Ca + Si C Ca 2 Si (сплавление) = галогеноводородами М нер Si + – 100°C) л ь н ы к и с л о Si + 4 HF = Si. F 4 + 2 H 2 (40°CCи= Si. Cа(1200°Cе– 1300°C) т ы н а Неме Ме Si кремний при обычных у с л. Si. HCl , я. Si. H н е, Si. H й с т в у ю т. о в и х Cl д е Cl С водой и 3 2 2 3 Со щелочами галогеноводородами Si + 4 HCl = Si. Cl 4 + 2 H 2 + cмесь (300°С и выше) Н 20 Na. OH H 2 O Si Si
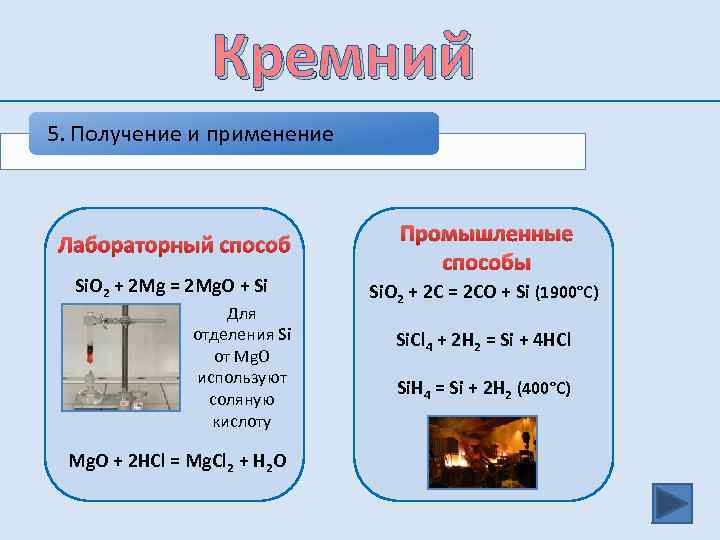 Кремний 5. Получение и применение Лабораторный способ Si. O 2 + 2 Mg = 2 Mg. O + Si Для отделения Si от Мg. O используют соляную кислоту Mg. O + 2 HCl = Mg. Cl 2 + H 2 O Промышленные способы Si. O 2 + 2 C = 2 CO + Si (1900°C) Si. Cl 4 + 2 H 2 = Si + 4 HCl Si. H 4 = Si + 2 H 2 (400°C)
Кремний 5. Получение и применение Лабораторный способ Si. O 2 + 2 Mg = 2 Mg. O + Si Для отделения Si от Мg. O используют соляную кислоту Mg. O + 2 HCl = Mg. Cl 2 + H 2 O Промышленные способы Si. O 2 + 2 C = 2 CO + Si (1900°C) Si. Cl 4 + 2 H 2 = Si + 4 HCl Si. H 4 = Si + 2 H 2 (400°C)
 Кремний 5. Применение и получение Керамика: Строительная; для быта; промышленная. Стекло цемент, бетон, железобетон Si Восстановитель в металлургии, добавка в чугуны и стали, выпрямители переменного тока, солнечные батареи.
Кремний 5. Применение и получение Керамика: Строительная; для быта; промышленная. Стекло цемент, бетон, железобетон Si Восстановитель в металлургии, добавка в чугуны и стали, выпрямители переменного тока, солнечные батареи.
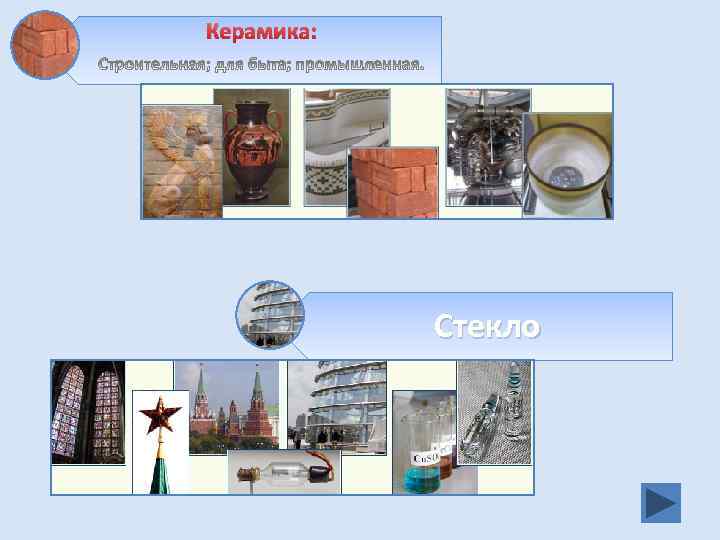 Керамика: Стекло
Керамика: Стекло
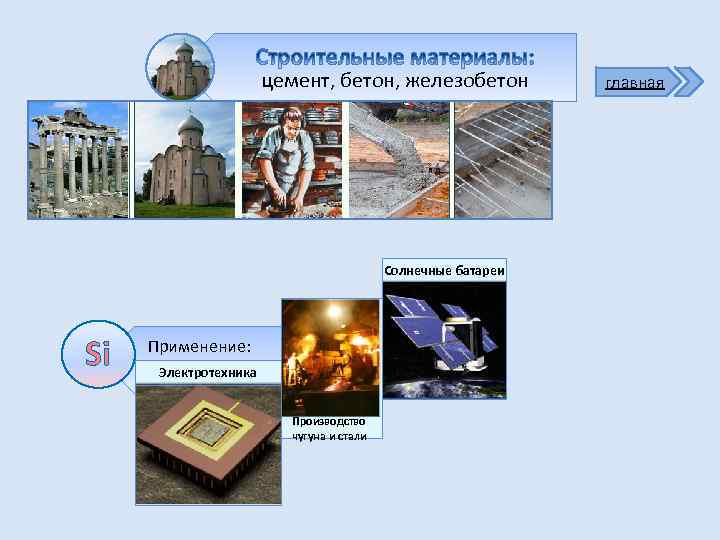 цемент, бетон, железобетон Солнечные батареи Si Применение: Электротехника Производство чугуна и стали главная
цемент, бетон, железобетон Солнечные батареи Si Применение: Электротехника Производство чугуна и стали главная
 Кремний 7. Проверка знаний В атомах каких химических элементов К какой группе оксидов относится оксид С какими электронную кремния Укажите веществами формулу Кристаллическая решеткареагирует содержится одинаковое число кремния в возбужденном состоянии. кристаллический кремний? кремния? электронов, протонов и нейтронов? Вопрос 1 Вопрос 2 А KOH 2 несолеобразующий 2 Молекулярная В С D [Ne]3 S 3 P P HFSO 4 основный 2 Атомная [Ne]3 S 23 P 3 Вопрос 4 Вопрос 5 HCl 1 3 амфотерный C Ионная [Ne]3 S 3 P Cl кислотный Si 2 Металлическая [Ne]3 S 23 P 4
Кремний 7. Проверка знаний В атомах каких химических элементов К какой группе оксидов относится оксид С какими электронную кремния Укажите веществами формулу Кристаллическая решеткареагирует содержится одинаковое число кремния в возбужденном состоянии. кристаллический кремний? кремния? электронов, протонов и нейтронов? Вопрос 1 Вопрос 2 А KOH 2 несолеобразующий 2 Молекулярная В С D [Ne]3 S 3 P P HFSO 4 основный 2 Атомная [Ne]3 S 23 P 3 Вопрос 4 Вопрос 5 HCl 1 3 амфотерный C Ионная [Ne]3 S 3 P Cl кислотный Si 2 Металлическая [Ne]3 S 23 P 4
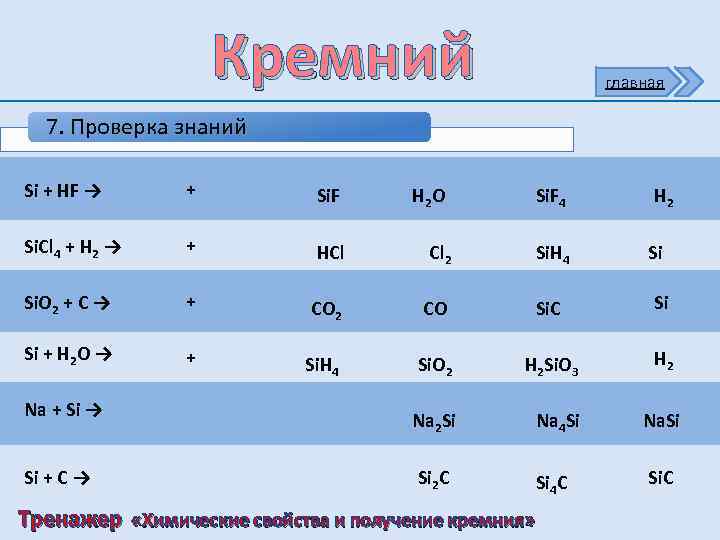 Кремний главная 7. Проверка знаний Si + HF → + Si. F Si. Cl 4 + H 2 → + HCl Si. O 2 + C → + Si + H 2 O → + Na + Si → Si + C → H 2 O Si. F 4 H 2 Cl 2 Si. H 4 Si CO 2 CO Si. C Si Si. H 4 Si. O 2 H 2 Si. O 3 H 2 Na 2 Si Na 4 Si Na. Si Si 2 C Si 4 C Si. C Тренажер «Химические свойства и получение кремния»
Кремний главная 7. Проверка знаний Si + HF → + Si. F Si. Cl 4 + H 2 → + HCl Si. O 2 + C → + Si + H 2 O → + Na + Si → Si + C → H 2 O Si. F 4 H 2 Cl 2 Si. H 4 Si CO 2 CO Si. C Si Si. H 4 Si. O 2 H 2 Si. O 3 H 2 Na 2 Si Na 4 Si Na. Si Si 2 C Si 4 C Si. C Тренажер «Химические свойства и получение кремния»


