 Ковалентные молекулы В зависимости от вида ковалентных связей в молекуле, она может быть полярной и неполярной
Ковалентные молекулы В зависимости от вида ковалентных связей в молекуле, она может быть полярной и неполярной
 Дипольные молекулы n n Если центры тяжести зарядов (+) и (-) совпадают, то молекула не полярная. Полярные молекулы являются диполями, то есть системами, состоящими из двух зарядов, равных по величине, но противоположных по знаку, находящихся на некотором расстоянии L друг от друга. Расстояние между центрами тяжести положительного и отрицательного зарядов называется длиной диполя. Полярность молекулы (связи) оценивается её электрическим моментом диполя μ: μ = L q ; где q – величина электрического заряда.
Дипольные молекулы n n Если центры тяжести зарядов (+) и (-) совпадают, то молекула не полярная. Полярные молекулы являются диполями, то есть системами, состоящими из двух зарядов, равных по величине, но противоположных по знаку, находящихся на некотором расстоянии L друг от друга. Расстояние между центрами тяжести положительного и отрицательного зарядов называется длиной диполя. Полярность молекулы (связи) оценивается её электрическим моментом диполя μ: μ = L q ; где q – величина электрического заряда.
 Дипольные молекулы (2) n n n Длина диполя имеет значение порядка размера атома (10 -10 м), а заряд электрона 1, 6 10 -19 кулона, поэтому дипольный момент выражается величиной порядка 10 -29 Кл м. Величина 3, 33 10 -29 Кл м = 1 D (дебай). Изменение электронной плотности на атомах приводит к появлению на них эффективного заряда δ. Электрический момент диполя молекулы является векторной суммой моментов всех связей и неподелённых электронных пар.
Дипольные молекулы (2) n n n Длина диполя имеет значение порядка размера атома (10 -10 м), а заряд электрона 1, 6 10 -19 кулона, поэтому дипольный момент выражается величиной порядка 10 -29 Кл м. Величина 3, 33 10 -29 Кл м = 1 D (дебай). Изменение электронной плотности на атомах приводит к появлению на них эффективного заряда δ. Электрический момент диполя молекулы является векторной суммой моментов всех связей и неподелённых электронных пар.
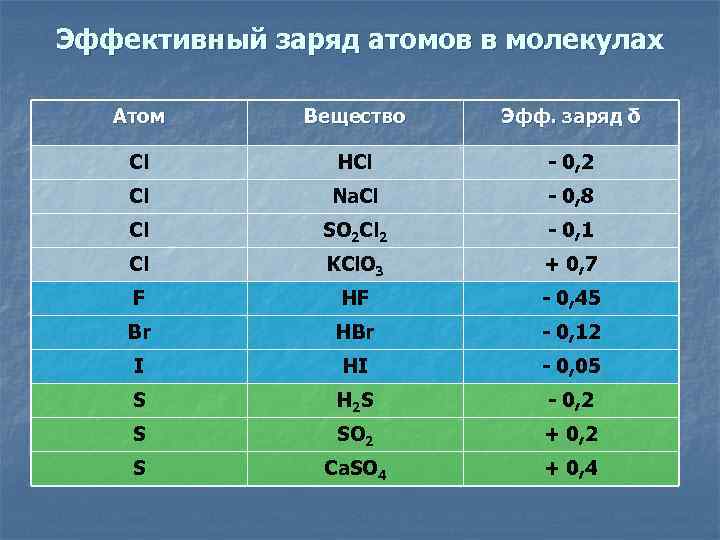 Эффективный заряд атомов в молекулах Атом Вещество Эфф. заряд δ Cl HCl - 0, 2 Cl Na. Cl - 0, 8 Cl SO 2 Cl 2 - 0, 1 Cl KCl. O 3 + 0, 7 F HF - 0, 45 Br HBr - 0, 12 I HI - 0, 05 S H 2 S - 0, 2 S SO 2 + 0, 2 S Ca. SO 4 + 0, 4
Эффективный заряд атомов в молекулах Атом Вещество Эфф. заряд δ Cl HCl - 0, 2 Cl Na. Cl - 0, 8 Cl SO 2 Cl 2 - 0, 1 Cl KCl. O 3 + 0, 7 F HF - 0, 45 Br HBr - 0, 12 I HI - 0, 05 S H 2 S - 0, 2 S SO 2 + 0, 2 S Ca. SO 4 + 0, 4
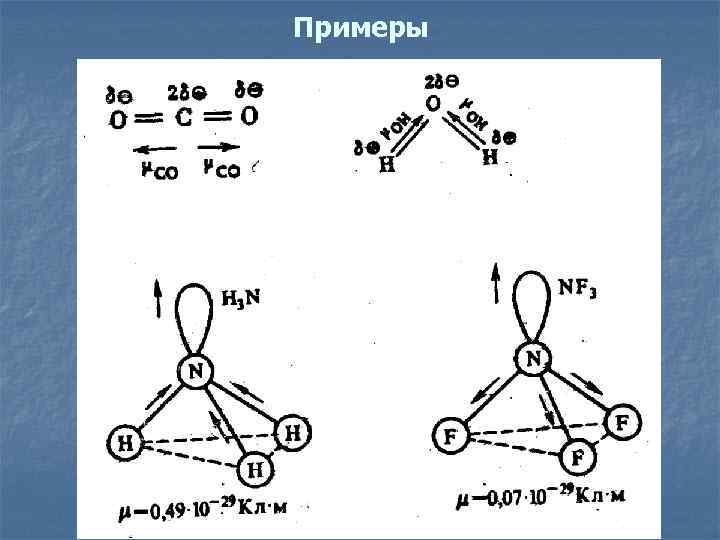 Примеры
Примеры