Lektsia_15_Zaschita_metallov_ot_korrozii.ppt
- Количество слайдов: 35
 Коррозия металлов Защита металлов от коррозии
Коррозия металлов Защита металлов от коррозии
 Основные антикоррозионные мероприятия 1. 2. 3. 4. 5. Рациональное конструирование Выбор устойчивых к коррозии конструкционных материалов Химическая обработка среды Применение защитных покрытий Электрохимическая защита
Основные антикоррозионные мероприятия 1. 2. 3. 4. 5. Рациональное конструирование Выбор устойчивых к коррозии конструкционных материалов Химическая обработка среды Применение защитных покрытий Электрохимическая защита

 3. Химическая обработка среды 3. 1. Удаление деполяризаторов (кислород, ионы водорода) 3. 2. Удаление солей 3. 3. Удаление кислых газов 3. 4. Применение ингибиторов коррозии
3. Химическая обработка среды 3. 1. Удаление деполяризаторов (кислород, ионы водорода) 3. 2. Удаление солей 3. 3. Удаление кислых газов 3. 4. Применение ингибиторов коррозии
 3. 1. Удаление деполяризатора а) кислород (нейтральная или щелочная среда) l l Кипячение Пропускание через поглощающие кислород фильтры Содержащая кислород жидкая среда → Фильтр с железной стружкой l Обработка сульфитами l Обработка гидразином → Среда с меньшим содержанием
3. 1. Удаление деполяризатора а) кислород (нейтральная или щелочная среда) l l Кипячение Пропускание через поглощающие кислород фильтры Содержащая кислород жидкая среда → Фильтр с железной стружкой l Обработка сульфитами l Обработка гидразином → Среда с меньшим содержанием
 3. 1. Удаление деполяризатора б) ионы водорода (кислая среда) Нейтрализация растворами щелочей ( гидроксид натрия, гидроксид кальция) l Обработка растворами гидролизующихся по аниону солей ( карбонат натрия, фосфат натрия) l
3. 1. Удаление деполяризатора б) ионы водорода (кислая среда) Нейтрализация растворами щелочей ( гидроксид натрия, гидроксид кальция) l Обработка растворами гидролизующихся по аниону солей ( карбонат натрия, фосфат натрия) l
 3. 2. Удаление солей Используемые методы: l дистилляция l ионный обмен l обратный осмос
3. 2. Удаление солей Используемые методы: l дистилляция l ионный обмен l обратный осмос
 3. 3. Удаление кислых газов l l l Нейтрализация щелочными реагентами: H 2 S + 2 Na. OH → Na 2 S + 2 H 2 O CO 2 + Ca(OH)2 → Ca. CO 3↓ + H 2 O Осаждение в виде малорастворимых соединений (сульфидов, карбонатов) H 2 S + Cu. SO 4 → Cu. S↓ + 2 H 2 SO 4 Окисление сероводорода сильными окислителями (KMn. O 4, K 2 Cr 2 O 7) S-2 -2 e → So
3. 3. Удаление кислых газов l l l Нейтрализация щелочными реагентами: H 2 S + 2 Na. OH → Na 2 S + 2 H 2 O CO 2 + Ca(OH)2 → Ca. CO 3↓ + H 2 O Осаждение в виде малорастворимых соединений (сульфидов, карбонатов) H 2 S + Cu. SO 4 → Cu. S↓ + 2 H 2 SO 4 Окисление сероводорода сильными окислителями (KMn. O 4, K 2 Cr 2 O 7) S-2 -2 e → So
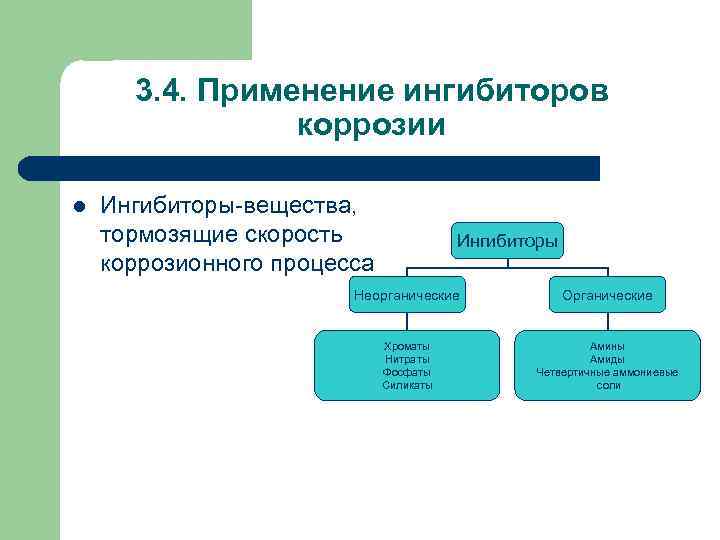 3. 4. Применение ингибиторов коррозии l Ингибиторы-вещества, тормозящие скорость коррозионного процесса Ингибиторы Неорганические Органические Хроматы Нитраты Фосфаты Силикаты Амины Амиды Четвертичные аммониевые соли
3. 4. Применение ингибиторов коррозии l Ингибиторы-вещества, тормозящие скорость коррозионного процесса Ингибиторы Неорганические Органические Хроматы Нитраты Фосфаты Силикаты Амины Амиды Четвертичные аммониевые соли
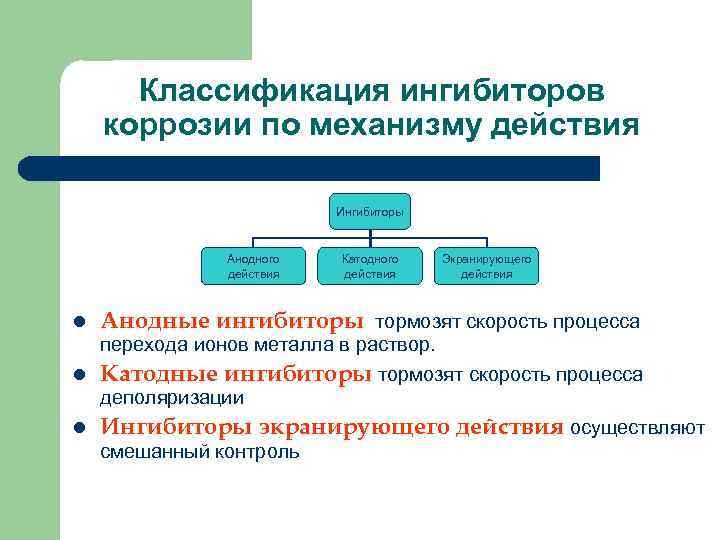 Классификация ингибиторов коррозии по механизму действия Ингибиторы Анодного действия l Катодного действия Экранирующего действия Анодные ингибиторы тормозят скорость процесса перехода ионов металла в раствор. l Катодные ингибиторы тормозят скорость процесса деполяризации l Ингибиторы экранирующего действия осуществляют смешанный контроль
Классификация ингибиторов коррозии по механизму действия Ингибиторы Анодного действия l Катодного действия Экранирующего действия Анодные ингибиторы тормозят скорость процесса перехода ионов металла в раствор. l Катодные ингибиторы тормозят скорость процесса деполяризации l Ингибиторы экранирующего действия осуществляют смешанный контроль
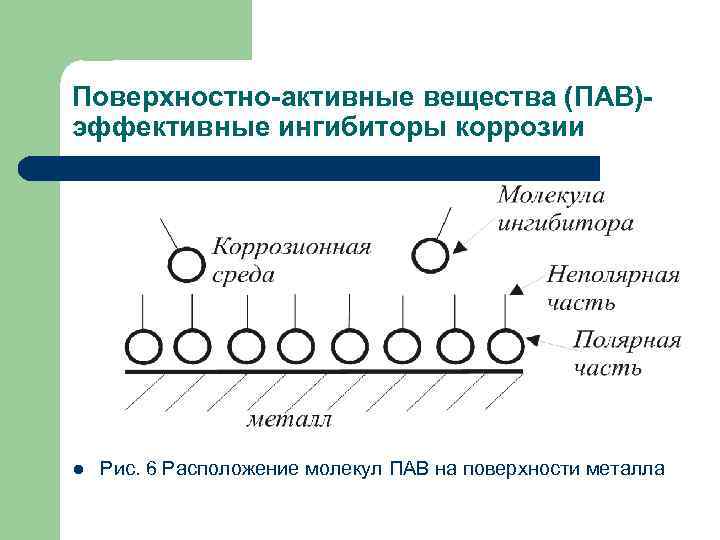 Поверхностно-активные вещества (ПАВ)эффективные ингибиторы коррозии l Рис. 6 Расположение молекул ПАВ на поверхности металла
Поверхностно-активные вещества (ПАВ)эффективные ингибиторы коррозии l Рис. 6 Расположение молекул ПАВ на поверхности металла

 4. Применение защитных покрытий Классификация защитных покрытий. Все защитные покрытия подразделяются на: l l l неметаллические химические
4. Применение защитных покрытий Классификация защитных покрытий. Все защитные покрытия подразделяются на: l l l неметаллические химические
 4. 1. Неметаллические защитные покрытия l l l Краски Лаки Эмали Полимерные материалы (каучуки, резина, эпоксидные смолы) Битумы Цементы
4. 1. Неметаллические защитные покрытия l l l Краски Лаки Эмали Полимерные материалы (каучуки, резина, эпоксидные смолы) Битумы Цементы





 4. 2. Металлические защитные покрытия l l l l l Хромирование Никелирование Алитирование Меднение Серебрение Золочение Кадмирование Цинкование Лужение Cr Ni Al Cu Ag Au Cd Zn Sn На защиту металлов от коррозии расходуется от мирового производства: Ni - 15%, Sn - 25%, Cd - 50%
4. 2. Металлические защитные покрытия l l l l l Хромирование Никелирование Алитирование Меднение Серебрение Золочение Кадмирование Цинкование Лужение Cr Ni Al Cu Ag Au Cd Zn Sn На защиту металлов от коррозии расходуется от мирового производства: Ni - 15%, Sn - 25%, Cd - 50%
 4. 3. Металлические защитные покрытия l l l Способы нанесения металлических защитных и декоративных покрытий: металлизация плакирование электролиз
4. 3. Металлические защитные покрытия l l l Способы нанесения металлических защитных и декоративных покрытий: металлизация плакирование электролиз
 Классификация металлических покрытий по механизму защитного действия l l Катодные покрытияпокрытие менее активным металлами Анодные покрытия более активными металлами Металлические покрытия Катодные Анодные
Классификация металлических покрытий по механизму защитного действия l l Катодные покрытияпокрытие менее активным металлами Анодные покрытия более активными металлами Металлические покрытия Катодные Анодные
 Механизм действия катодного металлического покрытия рис. 5 Коррозия луженого железа в кислой среде: φ0(Fe)= - 0, 44 B, φ0(Sn)= -0, 136 B Железо-анод Олово- катод l
Механизм действия катодного металлического покрытия рис. 5 Коррозия луженого железа в кислой среде: φ0(Fe)= - 0, 44 B, φ0(Sn)= -0, 136 B Железо-анод Олово- катод l
 Механизм действия анодного металлического покрытия Коррозия оцинкованного железа φ(Fe)= - 0, 44 B, φ(zn)= -0, 76 B Fe-катод, Zn- анод l
Механизм действия анодного металлического покрытия Коррозия оцинкованного железа φ(Fe)= - 0, 44 B, φ(zn)= -0, 76 B Fe-катод, Zn- анод l
 4. 3. Химические защитные покрытия l Оксидирование Рецептура состава для «воронения» стали: l Фосфатирование
4. 3. Химические защитные покрытия l Оксидирование Рецептура состава для «воронения» стали: l Фосфатирование

 Электрохимическая защита металлов от коррозии Электрохимическая защита Протекторная Катодная
Электрохимическая защита металлов от коррозии Электрохимическая защита Протекторная Катодная
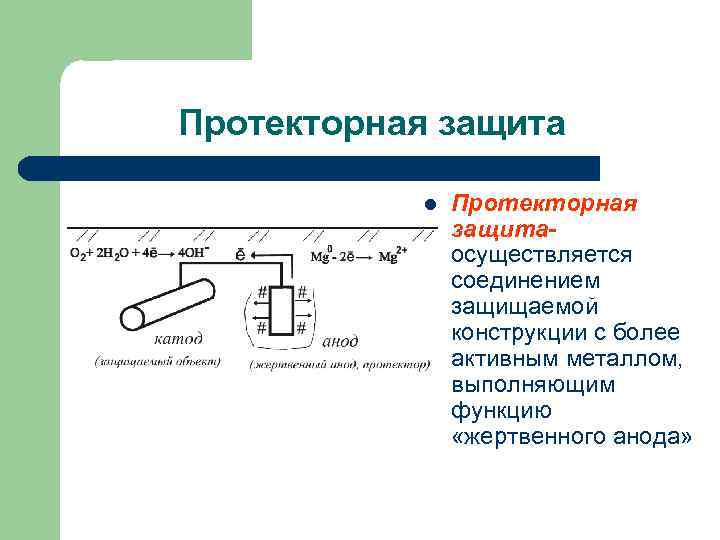 Протекторная защита l Протекторная защитаосуществляется соединением защищаемой конструкции с более активным металлом, выполняющим функцию «жертвенного анода»
Протекторная защита l Протекторная защитаосуществляется соединением защищаемой конструкции с более активным металлом, выполняющим функцию «жертвенного анода»




 Катодная защита - l Катодная защита обеспечивается поляризацией защищаемого объекта от внешнего источника тока (станции катодной защиты) +
Катодная защита - l Катодная защита обеспечивается поляризацией защищаемого объекта от внешнего источника тока (станции катодной защиты) +




