 КОРРОЗИЯ МЕТАЛЛОВ Выполнил: Сосков. C. C
КОРРОЗИЯ МЕТАЛЛОВ Выполнил: Сосков. C. C
 САМОПРОИЗВОЛЬНОГО РАЗРУШЕНИЯ МЕТАЛЛА ПОД ДЕЙСТВИЕМ ОКРУЖАЮЩЕЙ СРЕДЫ. 2. Коррозия– это процесс перехода металла в то природное, естественное состояние, в котором мы встречаем его в земной коре.
САМОПРОИЗВОЛЬНОГО РАЗРУШЕНИЯ МЕТАЛЛА ПОД ДЕЙСТВИЕМ ОКРУЖАЮЩЕЙ СРЕДЫ. 2. Коррозия– это процесс перехода металла в то природное, естественное состояние, в котором мы встречаем его в земной коре.
 Ущерб, наносимый коррозией Мировая потеря 20 млн. тонн металла в год Еще более значимы косвенные потери
Ущерб, наносимый коррозией Мировая потеря 20 млн. тонн металла в год Еще более значимы косвенные потери
 Делийская железная колонна Возраст 1600 лет Высота 7, 2 м, вес около 6 тонн Эйфелева башня Красили 18 раз, отчего ее масса 9000 т каждый раз увеличивалась на 70 т (в сумме - 1260 т)
Делийская железная колонна Возраст 1600 лет Высота 7, 2 м, вес около 6 тонн Эйфелева башня Красили 18 раз, отчего ее масса 9000 т каждый раз увеличивалась на 70 т (в сумме - 1260 т)
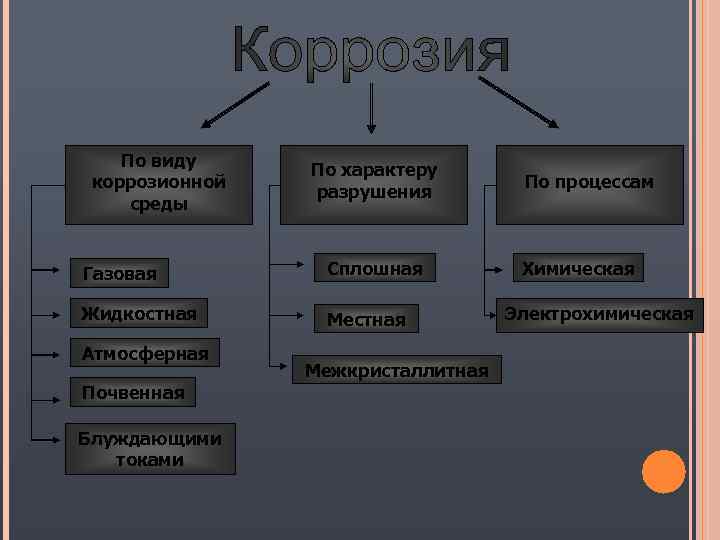 По виду коррозионной среды По характеру разрушения Газовая Сплошная Жидкостная Местная Атмосферная Почвенная Блуждающими токами Межкристаллитная По процессам Химическая Электрохимическая
По виду коррозионной среды По характеру разрушения Газовая Сплошная Жидкостная Местная Атмосферная Почвенная Блуждающими токами Межкристаллитная По процессам Химическая Электрохимическая
 По виду коррозионной среды
По виду коррозионной среды
 Газовая Жидкостная Атмосферная Почвенная Блуждающими токами
Газовая Жидкостная Атмосферная Почвенная Блуждающими токами
 ПО ХАРАКТЕРУ РАЗРУШЕНИЙ
ПО ХАРАКТЕРУ РАЗРУШЕНИЙ
 СПЛОШНАЯ КОРРОЗИЯ Равномерная Неравномерная
СПЛОШНАЯ КОРРОЗИЯ Равномерная Неравномерная
 МЕСТНАЯ КОРРОЗИЯ Язвенная Точечная Пятнами
МЕСТНАЯ КОРРОЗИЯ Язвенная Точечная Пятнами
 ПРИЧИНЫ ВОЗНИКНОВЕНИЯ МЕСТНОЙ КОРРОЗИИ Соль на дорогах Морская вода Межкристаллитная коррозия
ПРИЧИНЫ ВОЗНИКНОВЕНИЯ МЕСТНОЙ КОРРОЗИИ Соль на дорогах Морская вода Межкристаллитная коррозия
 По процессам
По процессам
 ХИМИЧЕСКАЯ КОРРОЗИЯ Химическая коррозия – самопроизвольное разрушение металлов в среде окислительного газа (кислорода, галогенов и т. д. ) при повышенных температурах или в жидких не электролитах. Газовая 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 4 Fe + 3 О 2 = 2 Fe 2 О 3 В жидких не электролитах • В нефти • В сере • В органических веществах Cu + S = Cu. S 2 Ag + S = Ag 2 S 2 Al + 6 ССl 4 = 3 C 2 Cl 6 + 3 Al. Cl 3
ХИМИЧЕСКАЯ КОРРОЗИЯ Химическая коррозия – самопроизвольное разрушение металлов в среде окислительного газа (кислорода, галогенов и т. д. ) при повышенных температурах или в жидких не электролитах. Газовая 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 4 Fe + 3 О 2 = 2 Fe 2 О 3 В жидких не электролитах • В нефти • В сере • В органических веществах Cu + S = Cu. S 2 Ag + S = Ag 2 S 2 Al + 6 ССl 4 = 3 C 2 Cl 6 + 3 Al. Cl 3
 ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Электрохимическая коррозия металлов – самопроизвольный процесс разрушения металлов в среде электролитов. Me – ne = Me +n 2 Сu + O 2+ 2 H 2 O + CO 2= Cu. CO 3∙Cu(OH)2 2 Fe + O 2 + 2 H 2 O = 2 Fe(OH)2
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Электрохимическая коррозия металлов – самопроизвольный процесс разрушения металлов в среде электролитов. Me – ne = Me +n 2 Сu + O 2+ 2 H 2 O + CO 2= Cu. CO 3∙Cu(OH)2 2 Fe + O 2 + 2 H 2 O = 2 Fe(OH)2
 ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
 ПРИМЕНЕНИЕ ИНГИБИТОРОВ Ингибиторы - это вещества, способные замедлять протекание химических процессов или останавливать их. Известно более 5 тысяч
ПРИМЕНЕНИЕ ИНГИБИТОРОВ Ингибиторы - это вещества, способные замедлять протекание химических процессов или останавливать их. Известно более 5 тысяч
 НАНЕСЕНИЕ ЗАЩИТНЫХ ПОКРЫТИЙ • Краска • Лак • Грунтовка • Смола • Эмаль Пластмасса Масло
НАНЕСЕНИЕ ЗАЩИТНЫХ ПОКРЫТИЙ • Краска • Лак • Грунтовка • Смола • Эмаль Пластмасса Масло
 АНТИКОРРОЗИОННЫМ МЕТАЛЛОМ Никелирование Хромирование Оцинковка
АНТИКОРРОЗИОННЫМ МЕТАЛЛОМ Никелирование Хромирование Оцинковка
 АНТИКОРРОЗИОННЫМ МЕТАЛЛОМ Покрытие алюминием Лужение Позолота
АНТИКОРРОЗИОННЫМ МЕТАЛЛОМ Покрытие алюминием Лужение Позолота