Коррозия.ppt
- Количество слайдов: 26
 Коррозия металлов
Коррозия металлов
 УМК «ХИМИЯ» Коррозия металлов Тема лекции: Лектор – Иванов М. Г.
УМК «ХИМИЯ» Коррозия металлов Тема лекции: Лектор – Иванов М. Г.
 Цель лекции: изложение основных понятий химической и электрохимической коррозии Компетенции, формируемые у студента: Умения: q прогнозировать на основе современных представлений о строении атомов и химической связи, возможность протекания ОВР реакций, протекающих при химической и электрохимической коррозии металлов.
Цель лекции: изложение основных понятий химической и электрохимической коррозии Компетенции, формируемые у студента: Умения: q прогнозировать на основе современных представлений о строении атомов и химической связи, возможность протекания ОВР реакций, протекающих при химической и электрохимической коррозии металлов.
 СОДЕРЖАНИЕ Основные понятия Виды коррозии Скорость коррозии Химическая коррозия Электрохимическая коррозия Анодный процесс Катодный процесс Деполяризаторы Коррозия с водородной деполяризацией Коррозия с кислородной деполяризацией Поляризация электродных процессов Пассивация Литература
СОДЕРЖАНИЕ Основные понятия Виды коррозии Скорость коррозии Химическая коррозия Электрохимическая коррозия Анодный процесс Катодный процесс Деполяризаторы Коррозия с водородной деполяризацией Коррозия с кислородной деполяризацией Поляризация электродных процессов Пассивация Литература
 Основные понятия содержание Коррозия металлов - самопроизвольное разрушение металлов и сплавов в результате химического и электрохимического взаимодействия с агрессивной средой.
Основные понятия содержание Коррозия металлов - самопроизвольное разрушение металлов и сплавов в результате химического и электрохимического взаимодействия с агрессивной средой.
 Виды коррозии содержание Коррозия металлов Химическая коррозия Электрохимическая коррозия
Виды коррозии содержание Коррозия металлов Химическая коррозия Электрохимическая коррозия
 Виды коррозии Сплошная (общая) q Равномерная коррозия q Неравномерная коррозия q Избирательная коррозия Местная (локальная коррозия) q Коррозия пятнами q Коррозия язвами q Точечная коррозия (питтинг) q Межкристаллитная коррозия q Коррозионное растрескивание содержание
Виды коррозии Сплошная (общая) q Равномерная коррозия q Неравномерная коррозия q Избирательная коррозия Местная (локальная коррозия) q Коррозия пятнами q Коррозия язвами q Точечная коррозия (питтинг) q Межкристаллитная коррозия q Коррозионное растрескивание содержание
 Виды коррозии содержание q Атмосферная коррозия – коррозия металлов в естественных атмосферных условиях (около 80% металлических конструкций эксплуатируются в атмосфере воздуха). q Коррозия в электролитах (солевая, кислотная, щелочная) – коррозия металлов в проводящих электрический ток средах. q Грунтовая (почвенная) коррозия –коррозия металлов в почвах и грунтах. q Контактная коррозия – электрохимическая коррозия, вызванная контактом металлов, имеющих разные электродные потенциалы в данной коррозионной среде. q Коррозия под напряжением – коррозия металла при одновременном воздействии коррозионной среды и постоянных или переменных механических напряжений (статических или меняющихся по величине и знаку). q Коррозия при трении (фретинг-коррозия) – при одновременном воздействии коррозионной среды и сил трения. q Коррозия при кавитации – коррозия при ударном воздействии коррозионной среды. q Электрокоррозия – коррозия под действием токов рассеивания (блуждающих токов) и тока от внешних источников. q Щелевая коррозия – коррозия, протекающая в узких щелях и зазорах между двумя металлами или в местах неплотного контакта металла с неметаллическим коррозионно- инертным материалом.
Виды коррозии содержание q Атмосферная коррозия – коррозия металлов в естественных атмосферных условиях (около 80% металлических конструкций эксплуатируются в атмосфере воздуха). q Коррозия в электролитах (солевая, кислотная, щелочная) – коррозия металлов в проводящих электрический ток средах. q Грунтовая (почвенная) коррозия –коррозия металлов в почвах и грунтах. q Контактная коррозия – электрохимическая коррозия, вызванная контактом металлов, имеющих разные электродные потенциалы в данной коррозионной среде. q Коррозия под напряжением – коррозия металла при одновременном воздействии коррозионной среды и постоянных или переменных механических напряжений (статических или меняющихся по величине и знаку). q Коррозия при трении (фретинг-коррозия) – при одновременном воздействии коррозионной среды и сил трения. q Коррозия при кавитации – коррозия при ударном воздействии коррозионной среды. q Электрокоррозия – коррозия под действием токов рассеивания (блуждающих токов) и тока от внешних источников. q Щелевая коррозия – коррозия, протекающая в узких щелях и зазорах между двумя металлами или в местах неплотного контакта металла с неметаллическим коррозионно- инертным материалом.
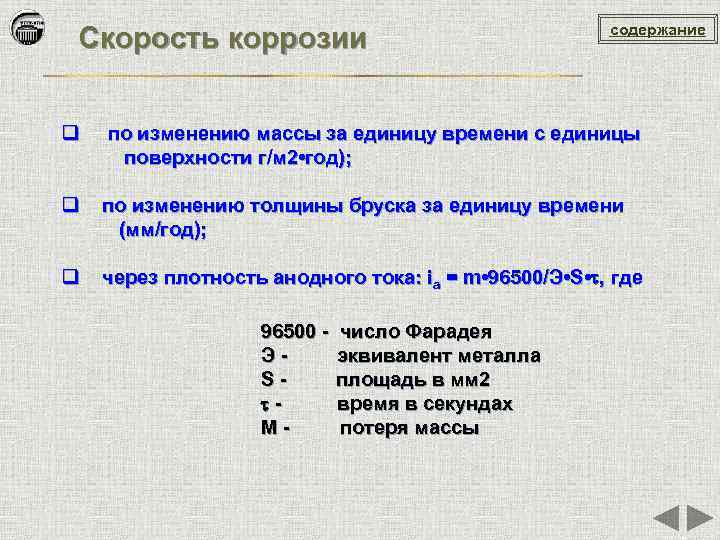 Скорость коррозии содержание q по изменению массы за единицу времени с единицы поверхности г/м 2 • год); q по изменению толщины бруска за единицу времени (мм/год); q через плотность анодного тока: ia = m • 96500/Э • S • , где 96500 - число Фарадея Э - эквивалент металла S - площадь в мм 2 - время в секундах M - потеря массы
Скорость коррозии содержание q по изменению массы за единицу времени с единицы поверхности г/м 2 • год); q по изменению толщины бруска за единицу времени (мм/год); q через плотность анодного тока: ia = m • 96500/Э • S • , где 96500 - число Фарадея Э - эквивалент металла S - площадь в мм 2 - время в секундах M - потеря массы
 Химическая коррозия содержание Это взаимодействие металлов с коррозионной средой, при котором окисление металла и восстановление окислительного компонента коррозионной среды протекает без пространственного разделения процессов окисления и восстановления: восстановления n. Me + m/2 O 2 = Men. Om
Химическая коррозия содержание Это взаимодействие металлов с коррозионной средой, при котором окисление металла и восстановление окислительного компонента коррозионной среды протекает без пространственного разделения процессов окисления и восстановления: восстановления n. Me + m/2 O 2 = Men. Om
 Электрохимическая коррозия содержание Это самопроизвольное разрушение металлов в присутствии электролитически проводящих сред (раствор или расплав электролита), при котором окисление (ионизация) металла и восстановление окислительного компонента коррозионной среды пространственно разделены и представляют собой различные стадии сопряженного процесса окисления-восстановления Me - ne = Men+ Анодный процесс Ox + ne = Red Катодный процесс
Электрохимическая коррозия содержание Это самопроизвольное разрушение металлов в присутствии электролитически проводящих сред (раствор или расплав электролита), при котором окисление (ионизация) металла и восстановление окислительного компонента коррозионной среды пространственно разделены и представляют собой различные стадии сопряженного процесса окисления-восстановления Me - ne = Men+ Анодный процесс Ox + ne = Red Катодный процесс
 Электрохимическая коррозия содержание
Электрохимическая коррозия содержание
 Электрохимическая коррозия содержание Причины электрохимической гетерогенности q Контакт двух и более металлов с различными потенциалами q Контакт металла с различными средами q Наличие на поверхности металла оксидных пленок q Структурная неоднородность металла q Неоднородность внутренних напряжений в металле q Разность температур на различных участках металла
Электрохимическая коррозия содержание Причины электрохимической гетерогенности q Контакт двух и более металлов с различными потенциалами q Контакт металла с различными средами q Наличие на поверхности металла оксидных пленок q Структурная неоднородность металла q Неоднородность внутренних напряжений в металле q Разность температур на различных участках металла
 Анодный процесс содержание Me - ne = Men+ Gо = – Еоn. F G <0, когда E > 0 Самопроизвольный процесс
Анодный процесс содержание Me - ne = Men+ Gо = – Еоn. F G <0, когда E > 0 Самопроизвольный процесс
 Катодный процесс содержание Уравнения катодного процесса в отсутствие растворенного кислорода (с водородной деполяризацией) в присутствии растворенного кислорода (с кислородной деполяризацией) кислая среда (1) нейтральная и щелочная среда (2) (3) (4)
Катодный процесс содержание Уравнения катодного процесса в отсутствие растворенного кислорода (с водородной деполяризацией) в присутствии растворенного кислорода (с кислородной деполяризацией) кислая среда (1) нейтральная и щелочная среда (2) (3) (4)
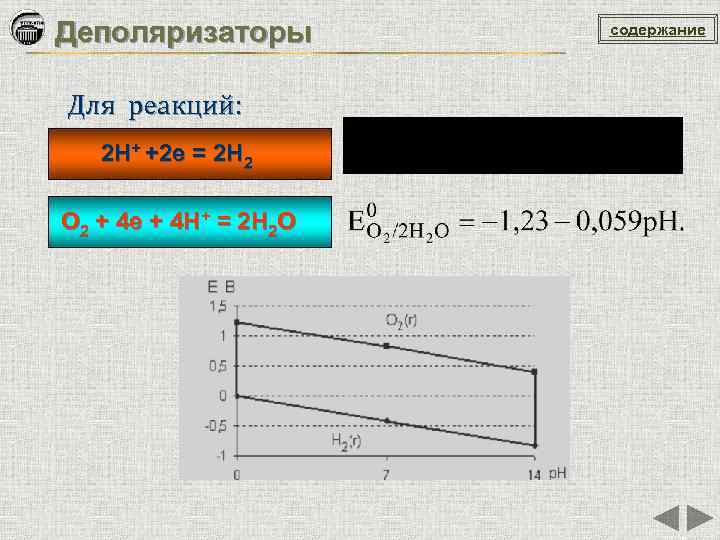 Деполяризаторы Для реакций: 2 H+ +2 e = 2 H 2 O 2 + 4 e + 4 H+ = 2 H 2 O содержание
Деполяризаторы Для реакций: 2 H+ +2 e = 2 H 2 O 2 + 4 e + 4 H+ = 2 H 2 O содержание
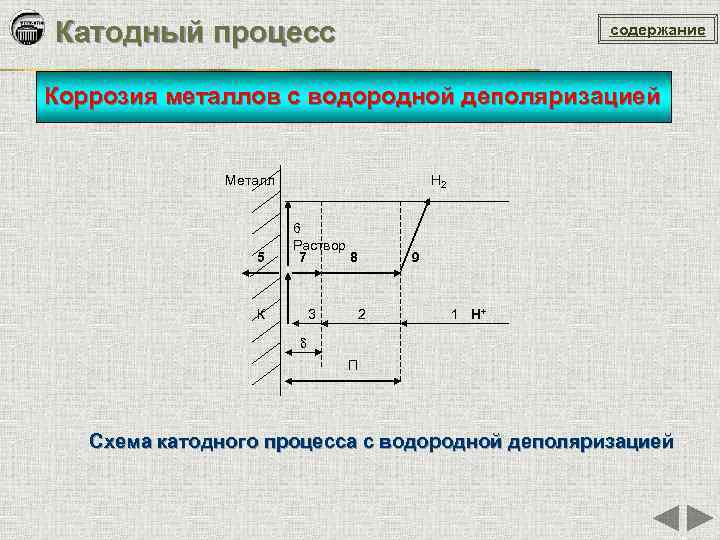 Катодный процесс содержание Коррозия металлов с водородной деполяризацией Металл Н 2 6 Раствор 5 7 8 9 К 3 2 1 H+ δ П Схема катодного процесса с водородной деполяризацией
Катодный процесс содержание Коррозия металлов с водородной деполяризацией Металл Н 2 6 Раствор 5 7 8 9 К 3 2 1 H+ δ П Схема катодного процесса с водородной деполяризацией
 Катодный процесс содержание Коррозия металлов с водородной деполяризацией = - 0, 059 р. Н Для кислой среды Для нейтральной среды Для щелочной среды Коррозия с водородной деполяризацией возможна, если:
Катодный процесс содержание Коррозия металлов с водородной деполяризацией = - 0, 059 р. Н Для кислой среды Для нейтральной среды Для щелочной среды Коррозия с водородной деполяризацией возможна, если:
 Катодный процесс содержание Коррозия металлов с водородной деполяризацией протекает в следующих условиях: q для большинства металлов в растворах кислот q для активных металлов в нейтральных растворах q для амфотерных металлов в растворах щелочей
Катодный процесс содержание Коррозия металлов с водородной деполяризацией протекает в следующих условиях: q для большинства металлов в растворах кислот q для активных металлов в нейтральных растворах q для амфотерных металлов в растворах щелочей
 Катодный процесс содержание Коррозия металлов с кислородной деполяризацией Металл O 2 6 2 5 К 4 δ 3 П Схема катодного процесса с кислородной деполяризацией
Катодный процесс содержание Коррозия металлов с кислородной деполяризацией Металл O 2 6 2 5 К 4 δ 3 П Схема катодного процесса с кислородной деполяризацией
 Катодный процесс содержание Коррозия металлов с кислородной деполяризацией Для кислой среды Для нейтральной среды Для щелочной среды Коррозия с водородной деполяризацией возможна, если:
Катодный процесс содержание Коррозия металлов с кислородной деполяризацией Для кислой среды Для нейтральной среды Для щелочной среды Коррозия с водородной деполяризацией возможна, если:
 Поляризация электродных процессов Изменение потенциала электрода при прохождении тока называется поляризацией: ΔЕ = Еi – EР где ΔЕ – поляризация; Еi - потенциал электрода под током; ЕР – равновесный потенциал содержание
Поляризация электродных процессов Изменение потенциала электрода при прохождении тока называется поляризацией: ΔЕ = Еi – EР где ΔЕ – поляризация; Еi - потенциал электрода под током; ЕР – равновесный потенциал содержание
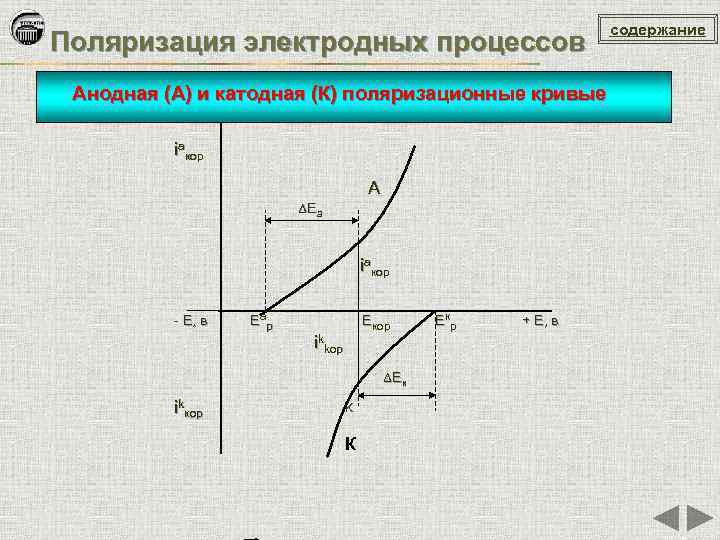 Поляризация электродных процессов Анодная (А) и катодная (К) поляризационные кривые iaкор A ΔЕ а iaкор - Е, в Еа р Екор ikkop ΔЕ к ikкор K К Ек р + Е, в содержание
Поляризация электродных процессов Анодная (А) и катодная (К) поляризационные кривые iaкор A ΔЕ а iaкор - Е, в Еа р Екор ikkop ΔЕ к ikкор K К Ек р + Е, в содержание
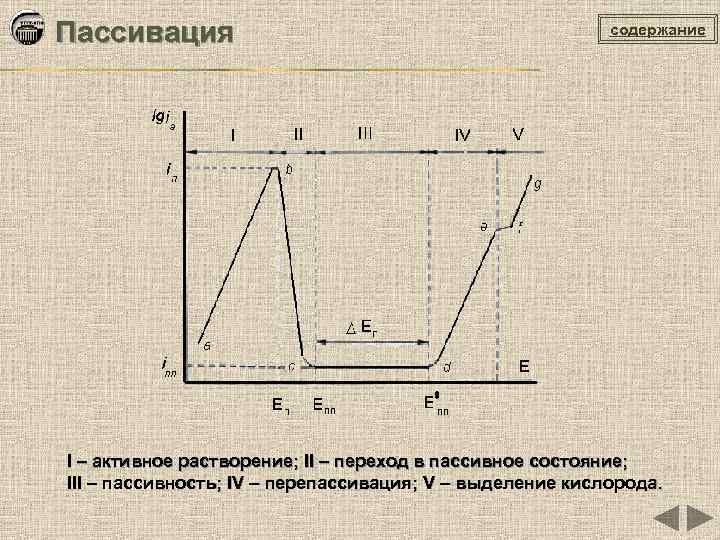 Пассивация содержание I – активное растворение; II – переход в пассивное состояние; III – пассивность; IV – перепассивация; V – выделение кислорода.
Пассивация содержание I – активное растворение; II – переход в пассивное состояние; III – пассивность; IV – перепассивация; V – выделение кислорода.
 Выводы и заключения n содержание Электрохимическая коррозия протекает через сопряженные процессы анодного растворения металла и катодного восстановления окислителя.
Выводы и заключения n содержание Электрохимическая коррозия протекает через сопряженные процессы анодного растворения металла и катодного восстановления окислителя.
 Список литературы n n n содержание 1. Ахметов Н. С. Общая и неорганическая химия. М. : Высшая школа. 2002. 2. О. М. Полторак, Л. М. Ковба. «Физико-химические основы неорганической химии» . М. : МГУ, 1994. 3. В. И. Горшков, И. А. Кузнецов. «Физическая химия» . М. : МГУ, 1993. 4. А. Джонсон. Термодинамические аспекты в курсе неорганической химии. М. : Мир. 1985. 5. Анорганикум. Под ред. Л. Кольдица. М. Мир. 1984. Т. 1. 6. Хьюи Дж. Неорганическая химия. Строение вещества и реакционная способность. М. , Химия, 1987. 7. Фичини Ж. , Ламброзо-Бадер Н. , Депезе Ж. -К. Основы физической химии. М. Мир. 1972. стр. 276 -283. 8. Дж. Кемпбел. Современная общая химия. М. : Мир. 1975 г. Т. 2. стр. 90. гл. 20. , Т 3. 9. Дикерсон Р. , Грей Г. , Хейт Дж. Основные законы химии. М. : Мир, 1982. Т. 2. 10. Б. Б. Дамаскин, О. А. Петрий. Электрохимия. М: Высшая школа, 1987. 11. CRC Hand book of Chemistry and Physics. 82 издание. 2001 -2002
Список литературы n n n содержание 1. Ахметов Н. С. Общая и неорганическая химия. М. : Высшая школа. 2002. 2. О. М. Полторак, Л. М. Ковба. «Физико-химические основы неорганической химии» . М. : МГУ, 1994. 3. В. И. Горшков, И. А. Кузнецов. «Физическая химия» . М. : МГУ, 1993. 4. А. Джонсон. Термодинамические аспекты в курсе неорганической химии. М. : Мир. 1985. 5. Анорганикум. Под ред. Л. Кольдица. М. Мир. 1984. Т. 1. 6. Хьюи Дж. Неорганическая химия. Строение вещества и реакционная способность. М. , Химия, 1987. 7. Фичини Ж. , Ламброзо-Бадер Н. , Депезе Ж. -К. Основы физической химии. М. Мир. 1972. стр. 276 -283. 8. Дж. Кемпбел. Современная общая химия. М. : Мир. 1975 г. Т. 2. стр. 90. гл. 20. , Т 3. 9. Дикерсон Р. , Грей Г. , Хейт Дж. Основные законы химии. М. : Мир, 1982. Т. 2. 10. Б. Б. Дамаскин, О. А. Петрий. Электрохимия. М: Высшая школа, 1987. 11. CRC Hand book of Chemistry and Physics. 82 издание. 2001 -2002


