Коррозия[1].ppt
- Количество слайдов: 67

КОРРОЗИЯ МЕТАЛЛОВ Общие понятия о коррозии 1/31/2018 1 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Коррозия металлов Коррозией называют самопроизвольное разрушение материалов вследствие химического или электрохи-мического взаимодействия их с окружающей средой. При коррозии металлов происходит гетерогенное окисление металла или какого-либо другого компонента материала, сопровождаемое восстановлением одного или нескольких компонентов среды. Если среда электропроводна, эти реакции электрохимические (окисление – анодный процесс, восстановление – катодный ). 1/31/2018 2 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

КОРРОЗИЯ МЕТАЛЛОВ Первопричиной коррозии металлов является термодинамическая неустойчивость металлов в различных средах при данных внешних условиях. Термодинамика даёт исчерпывающие сведения о возможности или невозможности самопроизвольного протекания коррозионного процесса при определённых условиях. Коррозионный процесс протекает на границе двух фаз: металлокружающая среда, т. е. является гетерогенным процессом взаимодействия жидкой или газообразной среды (или их окислительных компонентов) с металлом. 1/31/2018 3 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Стадии коррозионного процесса Отличительной особенностью коррозионных процессов является их сложность и многостадийность. Обычно кор-розионный процесс состоит по меньшей мере из трёх ста-дий: Перенос реагирующих веществ к поверхности раздела фаз – к реакционной зоне; Собственно гетерогенной реакции; Отвода продуктов реакции из реакционной зоны. Движущая сила процесса Скорость коррозии= ----------------------Торможение процесса 1/31/2018 4 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Классификация коррозионных процессов (по механизму процесса) Химическая коррозия – взаимодействие металлической поверхности с окружающей средой, не сопровождающееся возникновением электрохимических (электродных) процессов на границе фаз. Взаимодействие металла при высоких температурах с газообразными активными средами (сероводород, углекислый газ, сернистый или серный ангидрид, галогены, водяные пары и др. ) носит так же название газовой коррозии. 1/31/2018 5 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Классификация коррозионных процессов (по механизму процесса) Электрохимическая коррозия – процесс взаимодействия металлов с электролитами (в виде водных растворов, реже с неводными электролитами, например с некоторыми органическими электропроводными соединениями или безводными расплавами солей при повышенных температурах). Процессы электрохимической коррозии протекают по законам электрохимической кинетики, когда общая реакция взаимодействия может разделена на два самостоятельных электродных процесса: 1/31/2018 6 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Коррозионные процессы (по условиям протекания коррозии) Газовая Коррозия внешним током Атмосферная Коррозия блуждающим током Жидкостная Щелевая Подземная Коррозия под напряжением Биокоррозия Коррозионная кавитация Структурная Коррозия при трении 1/31/2018 7 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ТИПЫ КОРРОЗИОННЫХ РАЗРУШЕНИЙ (по характеру разрушений) Общая коррозия (по поверхности металла)– равномерная, неравномерная, избирательная Местная (локальная) коррозия: 1. Пятнами (коррозия латуни в морской воде) 2. Язвенная (коррозия углеродистой стали в грунте) 3. Точечная или питтинг (характерно для аустенитных хромоникелевых сталей в водных соленых средах) 4. Сквозная (питтинг листового металла) 1/31/2018 8 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ТИПЫ КОРРОЗИОННЫХ РАЗРУШЕНИЙ (по характеру разрушений) 5. Нитевидная(в виде нитей под плёнкой лака на угл. стали) 6. Подповерхностная 7. Межкристаллитная –распространяется по границам кристаллитов (зёрен) 8. Ножевая – в зоне сплавления сварных соединений 9. Коррозионное растрескивание 10. Коррозионная хрупкость 1/31/2018 9 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Анодный процесс-переход металла в раствор в виде ионов (в водных растворах, обычно гидратированных) с оставлением эквивалентного количества электронов в ме-талле. Катодный процесс-ассимиляция появившихся в металле избыточных электронов какими либо деполяризаторами. Различают электрохимическую коррозию с водородной, кислородной или окислительной деполяризацией. Наиболее часто встречаемые источники, усиливающие коррозию металла на буровой: 1. кислород 2. Углекислый газ 3. Сероводород 1/31/2018 10 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.
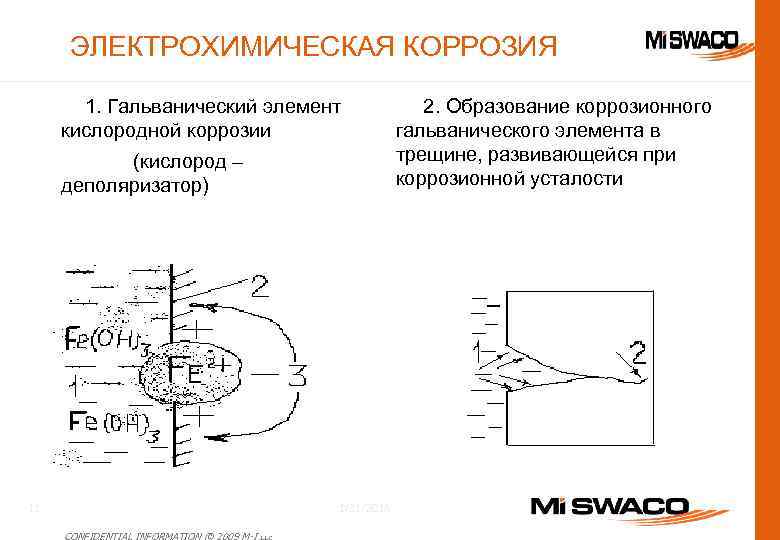
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ 1. Гальванический элемент кислородной коррозии (кислород – деполяризатор) 1/31/2018 11 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C. 2. Образование коррозионного гальванического элемента в трещине, развивающейся при коррозионной усталости

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Пояснения к рис. 1 Пояснения к рис. 2 1 - буровой раствор 1 - КАТОД 2 - бурильная труба 2 - АНОД 3 - электрический ток Если на катоде накапливаются продукты коррозии, появляется препятствие для потока электро-нов, Это значит, что катод поля-ризован. Растворенный О 2, реагируя с Н (в результате образу-ется Н 2 О), может действовать как деполяризатор, то есть ускорять процесс коррозии. Под ржавчиной - АНОД: Fe 0 - 2 e → Fe 2+ На поверхности трубы – КАТОД: О 2 + 2 Н 2 О +4 е → 4 ОН - и в сумме: 4 Fe 2+ + 6 H 2 O + 4 e → 4 Fe(OH)3 1/31/2018 12 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Факторы влияющие на коррозию р. Н Минерализация Давление Температура Бактерии Растворенные в растворе газы О 2, СО 2, Н 2 S являются основной причиной коррозии 1/31/2018 13 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.
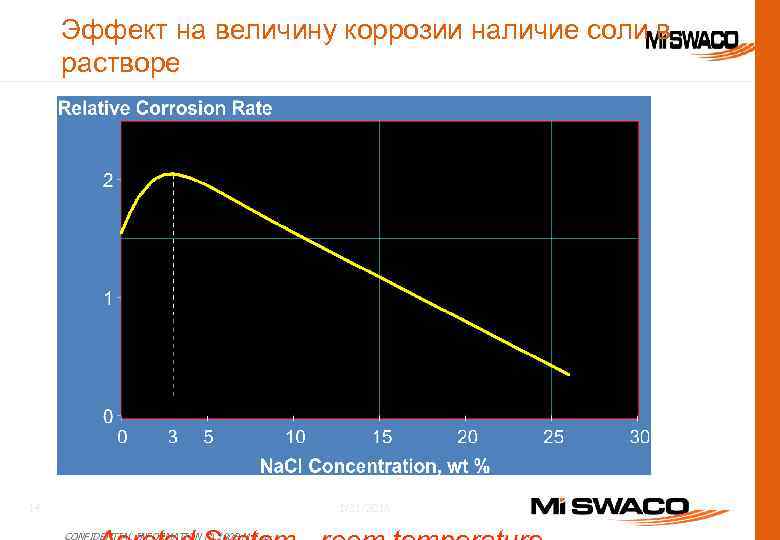
Эффект на величину коррозии наличие соли в растворе 1/31/2018 14 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Эффект на величину коррозии наличие соли в растворе Коррозия металла максимальна при концентрации соли Na. Cl = 30000 ppm Все РВО коррозионны, но величина коррозии зависит от множества факторов. 1/31/2018 15 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.
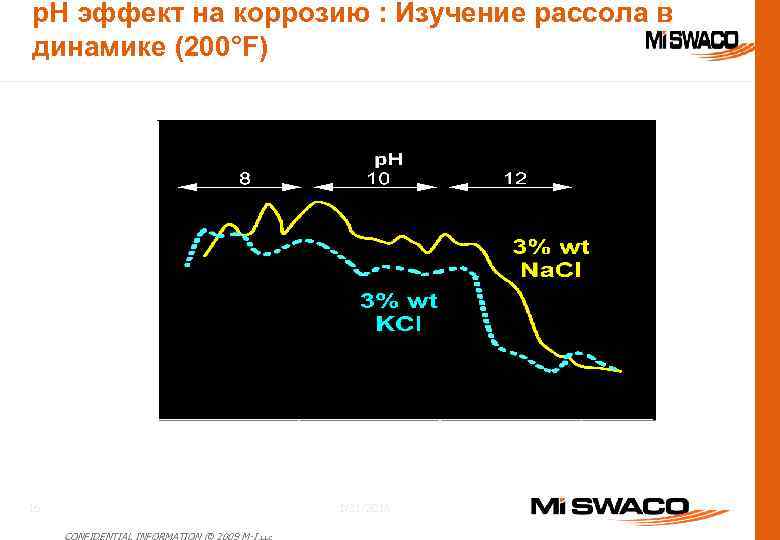
p. H эффект на коррозию : Изучение рассола в динамике (200°F) 1/31/2018 16 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.
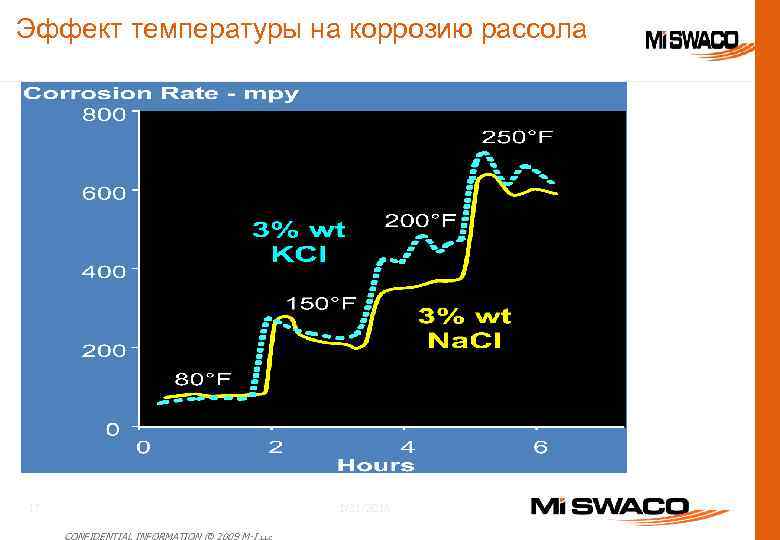
Эффект температуры на коррозию рассола 1/31/2018 17 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.
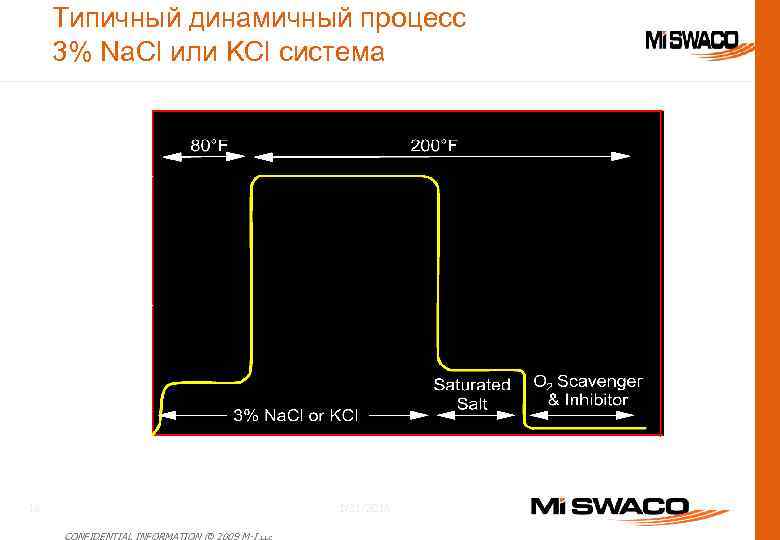
Типичный динамичный процесс 3% Na. Cl или KCl система 1/31/2018 18 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.
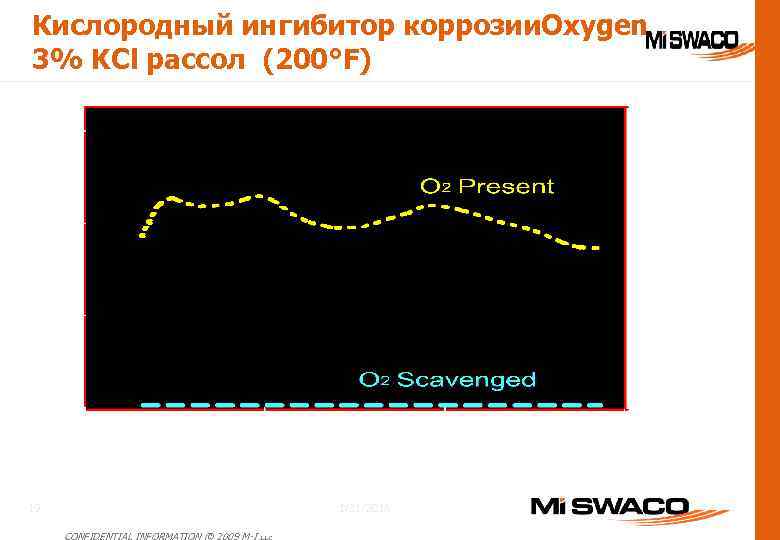
Кислородный ингибитор коррозии. Oxygen 3% KCl рассол (200°F) 1/31/2018 19 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ СЕРОВОДОРОДА Этот вид коррозии известен в практике под названием сульфидное растрескивание под напряжением. Для высокопрочных сталей (буровой инструмент) этот вид разрушения металла может наступить при его прочности при растяжении более 620 МПа и твердостью по Роквеллу более 22 по шкале С. При этом необходимы следующие сопутствующие условия: металл контактирует с электро-проводной жидкой средой, в которой растворен Н 2 S (при-чем достаточно пленочной влаги) и наличие в металле внутренних напряжений (остаточных или развивающихся под действием внешнего источника). Источники загрязнения растворов серводородом можно отметить: 1. Газ пласта при бурении 2. Температурная деградация химреагентов в растворе 1/31/2018 20 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ СЕРОВОДОРОДА Для сталей с прочностными характеристиками ниже указанных (пластичные стали), разрушения имеют вид расслоений, вздутий в полостях которых скапливается молекулярный водород. В обоих случаях коррозионный процесс с точки зрения механизма относится к низкотемпературной сероводо-родной коррозии, протекающей по электрохимическому механизму. В отличие от высокотемпературной сероводо-родной коррозии, протекающей по химическому механиз-му при температурах выше 250 -2600 С, с характером разрушений в виде общего неравномерного износа, поз-воляющем прогнозировать срок службы оборудования. 1/31/2018 21 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ СЕРОВОДОРОДА Сероводород в водной среде при растворении диссоциирует на ионы в две стадии: 1. H 2 S H+ + HS- 2. HS- + OH- S 2 - + H 2 O На эти обратимые реакции влияет р. Н среды. Сульфид имеет при р. Н≤ 6 формулу Н 2 S, при р. Н = 8 -11 находится в виде гидросульфид-иона HS- и при р. Н>12 в виде сульфид-иона S--. 2. Поскольку сульфидное растрескивание под напря-жением вызывается атомарным водородом (ион водорода это протон), который образуется на первой стадии диссоиации в диапазоне р. Н=8 -11, для подавления коррозионного процесса бесполезно применять метод регулирования р. Н. 22 1/31/2018

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ СЕРОВОДОРОДА Поэтому основным методом является использование реагентовнейтрализаторов сероводорода. Наиболее применяемые это - окись цинка (SULF-X), оксиды железа высокой степени дисперсности и пористости, которые влияют на поглотительную способность реагентов. Продукты реакции - сульфиды цинка и железа являются нерастворимыми соединениями в водной среде. Из оксидов железа наиболее известна торговая марка ЭКОСПОНЖ 23 (смесь оксидов железа в виде синтетичес-кого магнезита Fe 3 O 4) , скорость реакции самая высокая при низких значениях р. Н, благодаря чему этот материал оказывается наиболее эффективным для нейтрализации неожиданно резких притоков H 2 S. 1/31/2018 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ коррозия в присутствиии сероводорода Перечень основных ингибиторов сероводородной коррозии металла на буровой: 1. Известь 2. Zn. Ox - оксид цинка 3. Каустик 1/31/2018 24 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ УГЛЕКИСЛОГО ГАЗА Углекислый газ, как и сероводород, при бурении скважин может поступать в буровой раствор вместе с пластовыми флюидами. Он при растворении в водной фазе снижает р. Н, образуя углекислоту Н 2 СО 3, которая диссоциирует так же, как и Н 2 S в две стадии: 1. Н 2 СО 3 = Н+ + НСО 3 - 2. НСО 3 - = Н+ + СО 3 - Образующиеся карбонаты кальция Са. СО 3 осаждаются на поверхности металла с образованием нерастворимых слоев, которые способствуют появлению коррозионных гальванических элементов. 1/31/2018 25 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ УГЛЕКИСЛОГО ГАЗА Для предотвращения этого применяют ингибиторы осадкообразования (фосфорорганические комплексоны) и производят очистку труб во время спуско -подъемных операций. Особенно следует отметить на синергетический эффект совместного присутствия СО 2 и Н 2 S. Коррозионная агрессивность среды возрастает на порядки. Инкубационный (скрытый) период сульфидного растрескивания уменьшается до часов, что затем приводит к катастрофическим последствиям. Источники загрязнения раствора углекислым газом при бурении: 1. Попадание в виде газа пласта 2. Попадание с пластовой водой 3. Температурная деградация химреагентов в растворе 1/31/2018 26 4. Барит не высокого качества с выделением газа при его добавке к раствору CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ КИСЛОРОДА В буровых растворах почти всегда присутствует кислород, растворившийся в буровом растворе во время его приготовления и обработки, причем несколько его миллиграммов на 1 л достаточно для того, чтобы вызвать сильную коррозию. Для кислородной коррозии характерна питтинговая форма в связи с образованием кислородных элементов на участках, покрытых ржавчиной или другими осадками. Кислородная коррозия резко усиливается с повышением температуры, на неё влияет также соленость раствора. Рассолы и буровые растворы на минерализованной воде более агрессивны, растворы на пресной воде, из-за более высокой электропроводности. Однако при очень высокой солености скорость коррозии снижается благодаря меньшей растворимости кислорода. 1/31/2018 27 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ КИСЛОРОДА При р. Н <4 и р. Н>12 скорость кислородной коррозии максимальна. Необходимые мероприятия для подавления коррозии: Снижение до минимума поступления воздуха в буровой раствор на всех этапах промывки; Осуществлять контроль полевым тестированием или при-борными методами (измерители поляризационного сопротивления или резистометрические); Применение поглотителей О 2 (реагент OS-1 L); Применение ингибиторов кислородной коррозии аминного типа с целью гидрофобизации поверхности труб 1/31/2018 28 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ В ПРИСУТСТВИИ КИСЛОРОДА Основные источники кислорода при циркуляции раствора на буровой: 1. Гидропистолеты 2. Вибросита 3. Поверхностное оборудование 4. Сама атмосфера 1/31/2018 29 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

МИКРОБИОЛОГИЧЕСКАЯ КОРРОЗИЯ В буровых растворах на водной основе присутствуют разнообразные микроорганизмы, которые способствуют коррозии по различным механизмам воздействия. Их разделяют на 2 большие группы: аэробные (жизнедеятельность в присутствии О 2) и анаэробные (жизнедеятельность в отсутствие О 2). Более значительный ущерб наносят анаэробные бактерии Desulfovibrio. Они восстанавливают сульфаты, присутствующие в буровом растворе, с образованием Н 2 S при реакции с водородом на катоде: SO 42 - + 10 H+ 1/31/2018 30 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C. H 2 S + 4 H 2 O

МИКРОБИОЛОГИЧЕСКАЯ КОРРОЗИЯ Коррозии в этом случае способствует не только образующейся Н 2 S , но и деполяризация катода. Эти же бактерии способны разлагать реагенты на основе лигносульфонатов, отрицательно влияя на реологические и фильтрационные свойства системы. Ферментативному разложению микроорганизмами (дрожжевыми грибками, плесенью, бактериями) подвергается крахмал и др. полимеры. Борьба с микроорганизмами осуществляется добавлением в буровой раствор бактерицидов (X-CIDE 102, X-CIDE 207). Требования к ним: не влиять отрицательно на свойства буровых растворов, не быть коррозионно агрессивными и удовлетворять экологическому мониторингу. 1/31/2018 31 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Количественная характеристика коррозионных процессов При относительно равномерном типе коррозионного разрушения скорость коррозии может быть выражена массовым показателем коррозии (К), равным массе металла (в граммах), превращенного в продукты коррозии за единицу времени (час или сутки) с единицы его поверхности. Скорость коррозии выражают так же глубинным пока-зателем коррозии (П) – усреднённое проникновение коррозионного разрушения в металл в мм/год. 8, 7 П(мм/год) = -----К (г/м 2 1/31/2018 32 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C. * час) плотность металла (г/см 3)

Количественная характеристика коррозионных процессов Какова приемлимая величина коррозии в РВО для предотвращения питинговой коррозии металла? Величина менее 2 фунтов на квадратный фут в течении года 1/31/2018 33 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Количественная характеристика коррозионных процессов Какое оборудование может быть использовано для замера коррозии металла на буровой? 1. Купоны коррозии 2. Кольца коррозии 1/31/2018 34 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Количественная характеристика коррозионных процессов Испытание бурового раствора на коррозионную активность можно осуществлять в лаборатории. Для этого применяются специальнные стальные камеры (модернизированные «камеры старения» ), в которых под давлением и требуемой температурой находятся испытуемые образцы в среде бурового раствора. Для оценки коррозии в процессе бурения скважины, используют специально изготовленные образцы - стальные кольца, размещаемые в канавке муфты замкового соединения бурильных труб. Рекомендуемое время экc-позиции в скважине колеблется от 40 часов до 7 суток. Затем кольца извлекают, очищают от продуктов коррозии и определяют потерю их массы. Точность взвешивания до и после испытаний необходима до 0, 0001 г. Этим обеспечивается короткий срок испытаний. 1/31/2018 35 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Количественная характеристика коррозионных процессов Схематическое изображение модифицированной камеры старения для проведения коррозионных испытаний в условиях высоких температуры и давления. На след. Слайде показаны компоненты камеры для коррозионных испытаний. 1/31/2018 36 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Количественная характеристика коррозионных процессов 1/31/2018 37 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

CONQOR 404 -SSW раствор 38 1/31/2018

Блокнот коррозии 39 1/31/2018

Замеры коррозии на буровой Обязательно контролировать величину коррозии металла на буровой Купон коррозии или кольцо помещабт внутри резьбового переводника один над УБТ или как можно бдиже к забою, другой под квадрат или верхний привод Купоны необходимо извлечь в первый подъем инструмента или через 100 часов работы Купон отправляют в Хьюстон для визуального осмотра, замера потери веса и определения типа коррозии 40 1/31/2018

Анализ купона коррозии Извлеченный купон должен быть аккуратно вытерт сухой мягкой ткани насухо и завернут в бумагу, в которой он был прислан из лаборатории в Хьюстоне. В лаборатории образец должен быть: обследован на предмет поверхностных следов коррозии (не грамма замасленности образца) и замерен на предмет потери веса или формы. 41 1/31/2018

МЕТОДЫ ЗАЩИТЫ Широко применяются следующие методы защиты металлических конструкций от коррозии: 1. Защитные покрытия 2. Обработка коррозионной среды с целью снижения коррозионной активности. 3. Защита металлов электрохимическая. 4. Разработка и производство новых металлических конструкционных материалов. 1/31/2018 42 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

МЕТОДЫ ЗАЩИТЫ 5. Переход в ряде конструкций от металлических к химически стойким неметаллическим материалам (пластмасса, стекло, керамика и др. ). 6. Рациональное конструирование и эксплуатация металлических конструкций и деталей. 7. Профессиональный подбор материального оформления оборудования или его частей. 1/31/2018 43 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Контроль Коррозии в бурении р. Н 8. 3 – 9. 0 Предотвращение аэрации раствора Использование ингибиторов коррозии Использование бактерицидов Проведение тестовых испытаний по контролю коррозионной агрессивности рабочих сред 1/31/2018 44 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ИНГИБИТОРЫ КОРОЗИИ Ингибиторы коррозии, вещества, введение которых в относительно небольших количествах в агрессивную среду, смазку, полимерное покрытие или упаковочный материал вызывает заметное замедление коррозии. Условно подразделяются на адсорбционные и пассиви-рующие. Первые защищают металл благодаря воздействию на кинетику электродных процессов, проис-ходящих при коррозии. Пассивирующие способствуют образованию на металле оксидных, гидроксидных и др. пленок и переводят металл в пассивное состояние. 1/31/2018 45 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ИНГИБИТОРЫ КОРОЗИИ Торможение коррозионного процесса м. б. обусловлено: непосредственным исключением поверхности, покрытой ингибитором коррозии, из коррозионного процесса; изменением структуры двойного электрического слоя; блокировкой активных центров; изменением условий адсорбции участников корро-зионного процесса. Для каждого применяемого ингибитора коррозии имеется технический бюллетень, где оговариваются его назначе-ние, свойства и условия применения. 1/31/2018 46 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ИНГИБИТОРЫ КОРОЗИИ Различают ингибиторы кислотной коррозии и ингибиторы атмосферной коррозии (т. н. летучие ингибиторы). Последние обладают повышенной упругостью пара, что позволяет им насыщать окружающую металл атмосферу или пространство между металлом и упаковочным материалом. Применение ингибиторов коррозии – эффективный метод борьбы с коррозией, особенно в нефте- и газодобывающей промышленности. 1/31/2018 47 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ИНГИБИТОРЫ КОРОЗИИ • CONQOR 101 Вододиспергируемый пленкообразующй амин (для пресных надпакерных растворов) • CONQOR 202 B Пленкообразующий амин (для пресных и минерализованных растворов) • CONQOR 303 A Растворимый в воде/рассолах электролитов амин (для Na. Cl, KCL, Ca. Cl 2, Ca. Br 2 рассолов) • CONQOR 404 Органофосфорный состав для замедления коррозии в пресных и минерализованных растворах 1/31/2018 48 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

ИНГИБИТОРЫ КОРРОЗИИ • SI-1000 органический фосфат ингибитор адсорбции минералов результатов коррозии(для пресных растворов и растворов электролитов) • SULF-X Оксид цинка. Нейтрализатор сероводорода для растворов на водной и нефтяной основе • X-CIDE 102 Глютералдексайд, бактерицид для растворов на водной основе и рассолов электролитов • X-CIDE 207 Триазин, бактерицид для растворов на водной основе и рассолов электролитов • OS-1 L Нейтрализатор (окислитель) кислорода для пресных и минерализованных растворов 1/31/2018 49 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

Ингибиторы коррозии • CONQOR 303 A • Амины растворимые в рассолах • SI-1000 • Ингибитор органического фосфата для предотвращения ржавчины 50 1/31/2018

CONQOR 404 Пассивирующий ингибитор на все случаи при концентрации обработки: 2 -5 gal/100 bbl Для аэрированного раствора применяют: 10 -12 gal/100 bbl для начала Не для пакерных жидкостей: раствор должен циркулировать для работы ингибитора CONQOR 404 Применять в заданных конценрациях 51 1/31/2018

Пленочные амины Предохраняют сталь путем замещения воды и формирования защитной пленки масляной основы CONQOR 101 CONQOR 202 B CONQOR 303 A 52 1/31/2018

CONQOR 101 Растворим в РУО, деспергируем в РВО с образованием аминной пленки для дисперсных пакерных систем Может флокулировать при большом содержании твердой фазы или легко обработанный раствор Обработка: 0. 5 gal/bbl Форма защиты это образование маслозащитной пленки на поверхности стали 53 1/31/2018

CONQOR 202 B Формируется пленочно пенное аминное покрытие непосредственно наносимое на трубы ли путем закачки тяжелой пачки с ингибитором (slug) Применять когда CONQOR 404 не возможно применять Защитное / покрывающее будет уменьшаться со временем циркуляции и времени Может начаться пенообразование 54 1/31/2018

CONQOR 303 A Амины растворимы в рассолах и воде применяют при капитальных работах по скважине или пакерные жидкости Обработка: 55 gal/100 bbl (0. 5 gal/bbl) Пленкообразовательный ингибитор на стальной защищаемой поверхности Не эффективен в рассолах цинка (смотри справочник CBF (рассолы для заканчивания скважин) 55 1/31/2018

Ингибитор ржавчины-SI-1000 пределы ржавчино образования по нормообразованию ржавчины на буровом инструменте и на НКТ Предохраняет перемещение ржавчины на металл Базирование на химии органических фосфатах. Обработка: 1 gal/200 bbl начальное, с добавочной обработкой 5 gal/цикл для поддержания эффективности 56 1/31/2018

Химические ингибиторы OS-1 L (кислородный ингибитор) кислород Уменьшает растворенный SULF-XВысаживает сульфиды из H 2 S * Обработка: 1 lb/bbl может быть увеличена до удаления 1, 100 mg/l определяемых сульфидов 57 1/31/2018

Кислородный ингибитор Бисульфат Амония (SO 3)2 - + ½ O 2 (SO 4)2 Врезка во всасывающую линию с помощью нагнетатального насоса (эта врезка должна иметь отсекающую задвижку Поддерживать 300 -500 ppm сульфатов в желобной линии 0. 5 - 2. 0 gal/час типичная обработка 58 1/31/2018

H 2 S, O 2 , CO 2 разрушение со временем 1/31/2018 59 CONFIDENTIAL INFORMATION © 2009 M-I L. L. C.

SULF-X Ингибитор сероводорода на Цынке Zn 2+ + S 2 Zn. SСпециальный высокоэффективный ингибитор zinc oxide - 80. 3% по весу *Обработка: 1 lb/bbl может быть увеличена до 1, 100 mg/l по замеряемым сульфатам Предварительная обработка до 1 lb/bbl Может вызывать флокуляцию и увеличение вязкости раствора 60 1/31/2018

Бактерициды Глютералдегид Glutaraldehyde (25% активности) жидкий биосайд для решения проблем с бактериальной деградацией - другое наименование этого продукта (Myacide 25 GA) (X-CIDE 102) Обработка: 8 gal 25% glutaraldehyde/100 bbl (максимум 2, 000 mg/l) 4 gal допустимо Oсовместим с другими биосайдами Использовать специальную тару для контроля эфективнгости обработки“Bug Bottles” 61 1/31/2018

Пакерная жидкость на водной основе Высококачественный раствор отличной формы с высоким p. H Использовать биосайд Triazine ? Для снижения бакариальной активности Используй ингибиторы для снижения коррозии в виде покрытия труб Знай M-I SWACO продуктов для ингибирования коррозии и контроля ржавчены 62 1/31/2018

Ингибиторы для пакерных жидкостей на УО Подготовить пакерную жидкость для длительного хранения путем увеличения ее стабильности Увеличить ES Увеличить до максимально возможного Pom (Vsa) добавкой Извести для увеличения щелочности Cтщательно проциркулировать пакерную жидкость и добавить химреагенты Iингибиторы не использовать в РУО 63 1/31/2018

Главна линии обработки раствора При обнаружении впервые проблемы коррозии, необходимо: провести обработку необходимыми ингибиторами коррозии компании M-I для снижения скорости коррозии Контролировать и обрабатывать металл для снижения скорости коррозии с помощью купонов коррозии 64 1/31/2018

Заключение Определяй величину коррозии методом купонов Все РВО коррозионно опасные, разница в величине этих коррозий ! Многие растворы высоко коррозионно опасные из-за соленности, растворенных газов и требований защиты окружающей среды Всегда контролирую коррозию по снижению ее величины. Используй технологию компании M-ISWACO для контроля коррозии металла труб и оборудования. 65 1/31/2018

Удачи Помеите, что коррозия будет протекать в любом растворе и рассоле, но с разной скоростью. Имейте специальный справочник по коррозии и используй химреагенты компании M-I. 66 1/31/2018

Удачи Описывай технологию коррозии, ее историю и методы борьбы с ней. Всегда предполагай наличие коррозии металла в среде растворов. Будь всегда готов к обработке и борьбе с коррозией! 67 1/31/2018
Коррозия[1].ppt