10. КОРРОЗИЯ МЕТАЛЛОВ.pptx
- Количество слайдов: 28
 КОРРОЗИЯ МЕТАЛЛОВ
КОРРОЗИЯ МЕТАЛЛОВ
 Коррозия – это самопроизвольный процесс разрушения металлов и сплавов в рез-те окислительно-восстановительного ( ) взаимодействия их с окружающей средой.
Коррозия – это самопроизвольный процесс разрушения металлов и сплавов в рез-те окислительно-восстановительного ( ) взаимодействия их с окружающей средой.
 Меn+ + nе- Мео ( ) металлургия Коррозия протекает с ум-нием эн. Гиббса: Мео - ne- Меn+ ( ) коррозия Основной причиной корроз. разрушения металлов и сплавов является их термодинамическая неустойчивость.
Меn+ + nе- Мео ( ) металлургия Коррозия протекает с ум-нием эн. Гиббса: Мео - ne- Меn+ ( ) коррозия Основной причиной корроз. разрушения металлов и сплавов является их термодинамическая неустойчивость.
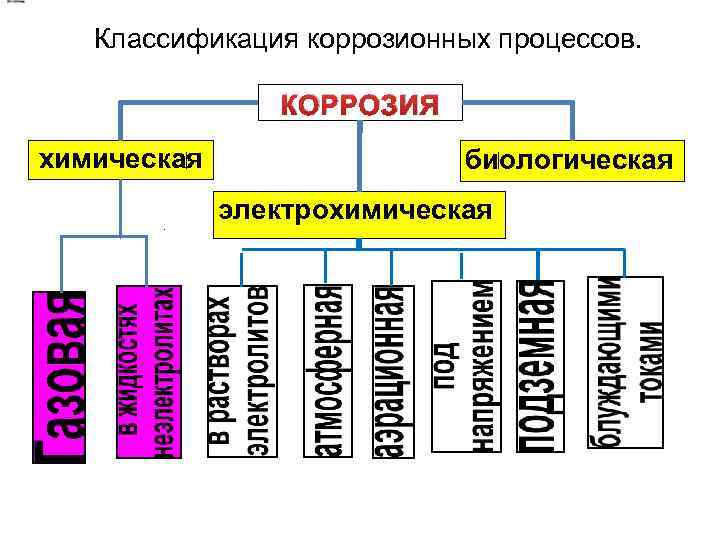 Классификация коррозионных процессов. КОРРОЗИЯ химическая биологическая электрохимическая
Классификация коррозионных процессов. КОРРОЗИЯ химическая биологическая электрохимическая
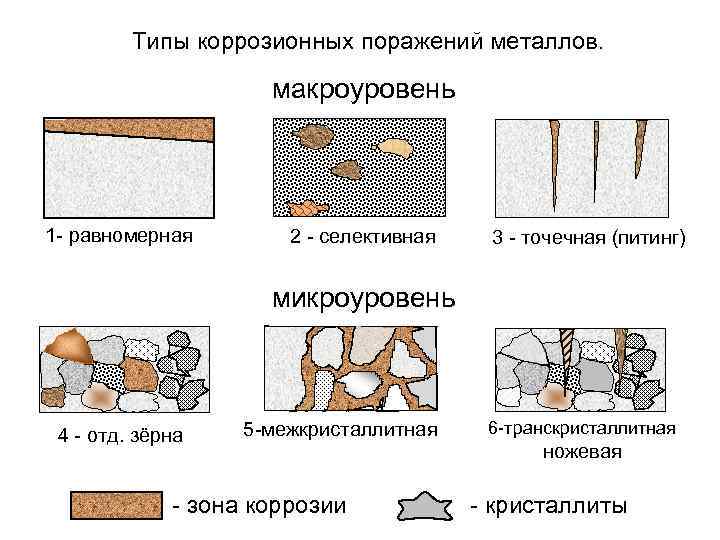 Типы коррозионных поражений металлов. макроуровень 1 - равномерная 2 - селективная 3 - точечная (питинг) микроуровень 4 - отд. зёрна 5 -межкристаллитная - зона коррозии 6 -транскристаллитная ножевая - кристаллиты
Типы коррозионных поражений металлов. макроуровень 1 - равномерная 2 - селективная 3 - точечная (питинг) микроуровень 4 - отд. зёрна 5 -межкристаллитная - зона коррозии 6 -транскристаллитная ножевая - кристаллиты
 Химическая коррозия – это самопроизвольное разрушение металлов под действием окислителей-неэлтов, обычно газов и орг. жидкостей, не проводящих эл. ток. Различают газовую коррозию и коррозию в жидких неэлектролитах. – это разрушение металла при контакте с сухими газами при высоких т-рах. Она имеет место при работе двигателей внутреннего сгорания, при хим. обработке металлов, горячей прокатке, ковке, в энергетических установках и др. При газовой коррозии происходит химическое взаимодействие металла с активными средами (CO 2; H 2 S; O 2; SO 2; галогенами).
Химическая коррозия – это самопроизвольное разрушение металлов под действием окислителей-неэлтов, обычно газов и орг. жидкостей, не проводящих эл. ток. Различают газовую коррозию и коррозию в жидких неэлектролитах. – это разрушение металла при контакте с сухими газами при высоких т-рах. Она имеет место при работе двигателей внутреннего сгорания, при хим. обработке металлов, горячей прокатке, ковке, в энергетических установках и др. При газовой коррозии происходит химическое взаимодействие металла с активными средами (CO 2; H 2 S; O 2; SO 2; галогенами).
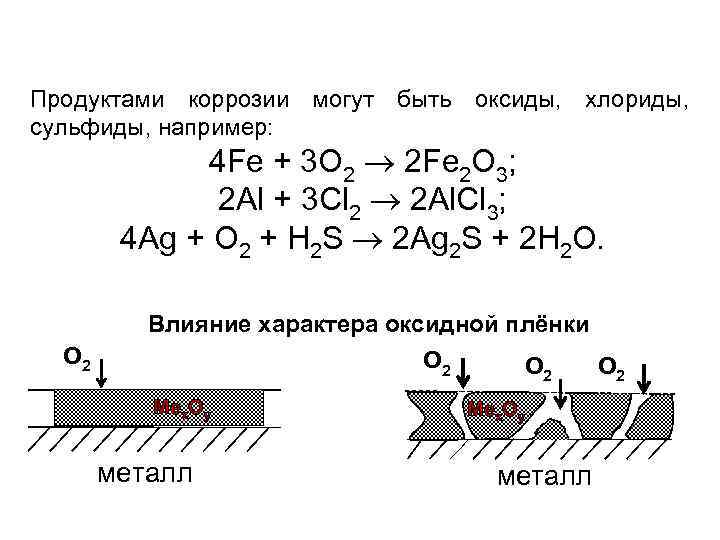 Продуктами коррозии могут быть оксиды, хлориды, сульфиды, например: 4 Fe + 3 O 2 2 Fe 2 O 3; 2 Al + 3 Cl 2 2 Al. Cl 3; 4 Ag + O 2 + H 2 S 2 Ag 2 S + 2 H 2 O. Влияние характера оксидной плёнки O 2 Меx. Oy металл O 2
Продуктами коррозии могут быть оксиды, хлориды, сульфиды, например: 4 Fe + 3 O 2 2 Fe 2 O 3; 2 Al + 3 Cl 2 2 Al. Cl 3; 4 Ag + O 2 + H 2 S 2 Ag 2 S + 2 H 2 O. Влияние характера оксидной плёнки O 2 Меx. Oy металл O 2
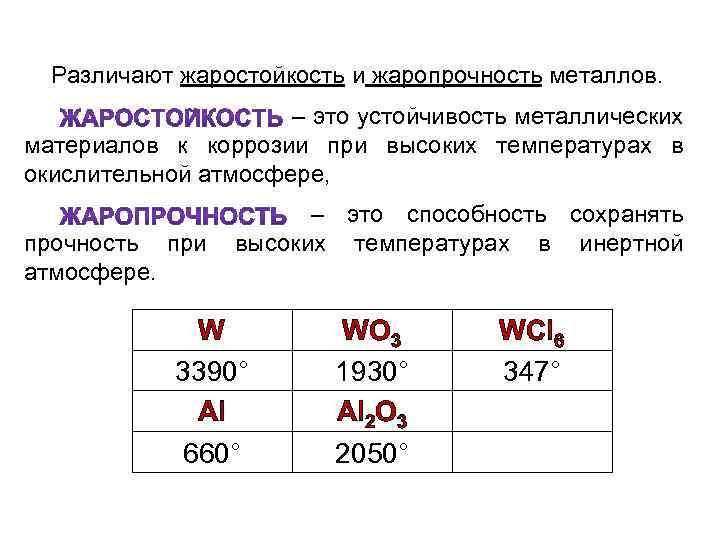 Различают жаростойкость и жаропрочность металлов. – это устойчивость металлических материалов к коррозии при высоких температурах в окислительной атмосфере, прочность при атмосфере. – это способность сохранять высоких температурах в инертной W 3390° Al 660° WО 3 1930° Al 2 О 3 2050° WCl 6 347°
Различают жаростойкость и жаропрочность металлов. – это устойчивость металлических материалов к коррозии при высоких температурах в окислительной атмосфере, прочность при атмосфере. – это способность сохранять высоких температурах в инертной W 3390° Al 660° WО 3 1930° Al 2 О 3 2050° WCl 6 347°
 . К неэлектролитам (непроводящим эл. ток) относятся жидкости орг. происхождения – спирты, бензол, хлороформ, керосин, нефть, бензин и др. , а также ряд жидкостей неорг. происхождения – расплавленная сера, жидкий бром и др. В чистом виде орг. жидкости практически не реагируют с металлами, но в присутствии даже незначительного колва примесей процессы взаимодействия резко усиливаются. Ускоряет коррозионные процессы наличие серосодержащих в-в, растворённого кислорода, повышение т-ры. Несмотря на сложность коррозионных процессов, в принципе они представляют собой обычные гетерогенные химические реакции: а) 2 R - Cl + Me Me. Cl 2 + R - R б) R 1 S + Me Me. S + R 1 – R 2 где R - органический радикал.
. К неэлектролитам (непроводящим эл. ток) относятся жидкости орг. происхождения – спирты, бензол, хлороформ, керосин, нефть, бензин и др. , а также ряд жидкостей неорг. происхождения – расплавленная сера, жидкий бром и др. В чистом виде орг. жидкости практически не реагируют с металлами, но в присутствии даже незначительного колва примесей процессы взаимодействия резко усиливаются. Ускоряет коррозионные процессы наличие серосодержащих в-в, растворённого кислорода, повышение т-ры. Несмотря на сложность коррозионных процессов, в принципе они представляют собой обычные гетерогенные химические реакции: а) 2 R - Cl + Me Me. Cl 2 + R - R б) R 1 S + Me Me. S + R 1 – R 2 где R - органический радикал.
 возникает при соприкосновении металла с электропроводящей средой (водой, водн. р-рами солей, кислот, щелочей; расплавленными солями и щелочами). Разрушение металла происходит за счет образования на поверхности металла микрогальванических элементов. Причины: наличие в основном металле примесей др. металлов или неметаллов, что приводит к появлению в местах их контакта и возникновению микротока. Участки относительно чистого металла поляризуются анодно, а примеси – катодно.
возникает при соприкосновении металла с электропроводящей средой (водой, водн. р-рами солей, кислот, щелочей; расплавленными солями и щелочами). Разрушение металла происходит за счет образования на поверхности металла микрогальванических элементов. Причины: наличие в основном металле примесей др. металлов или неметаллов, что приводит к появлению в местах их контакта и возникновению микротока. Участки относительно чистого металла поляризуются анодно, а примеси – катодно.
 Причиной образования короткозамкнутых микро-ГЭ в металле, кроме примесей, может быть любая энергетическая неоднородность его пов -сти, вызванная неоднородностью хим. или фаз. состава как самого металла, так и окружающей его коррозионной среды, а также мех. состояния металла. Наличие энергетической неоднородности на соседних участках металл. пов-сти приводит к тому, что участок с электродным потенциалом становится анодом, а с – катодом.
Причиной образования короткозамкнутых микро-ГЭ в металле, кроме примесей, может быть любая энергетическая неоднородность его пов -сти, вызванная неоднородностью хим. или фаз. состава как самого металла, так и окружающей его коррозионной среды, а также мех. состояния металла. Наличие энергетической неоднородности на соседних участках металл. пов-сти приводит к тому, что участок с электродным потенциалом становится анодом, а с – катодом.
 На аноде происходит окисление растворение металла по схеме: (−)А: Me 0 – nе- Men+ На катоде протекает восстановление в виде одного из двух процессов : и
На аноде происходит окисление растворение металла по схеме: (−)А: Me 0 – nе- Men+ На катоде протекает восстановление в виде одного из двух процессов : и
 – с восстановлением водорода. : (+)К: 2 Н+ + 2 е- = Н 20; (Н+/Н 20)=− 0, 059 р. Н ; : (+)К: Н 2 О + 2 е- = Н 20 + 2 ОН−; (Н 2 О/Н 20)=− 0, 059 р. Н. протекает при ограниченном доступе кислорода. Ех. , под толстым слоём воды или в кислых р-рах, в к-рых растворимость кислорода очень низка.
– с восстановлением водорода. : (+)К: 2 Н+ + 2 е- = Н 20; (Н+/Н 20)=− 0, 059 р. Н ; : (+)К: Н 2 О + 2 е- = Н 20 + 2 ОН−; (Н 2 О/Н 20)=− 0, 059 р. Н. протекает при ограниченном доступе кислорода. Ех. , под толстым слоём воды или в кислых р-рах, в к-рых растворимость кислорода очень низка.
 с восстановлением атмосферного кислорода, растворённого в коррозионной среде протекает по схеме: (+)К: О 2 + 2 Н 2 О + 4 e- = 4 OH−; (О 2/Н 2 О) = +1, 23 − 0, 059 р. Н При водородной деполяризации эл. хим. коррозии могут подвергаться металлы с электродным потенциалом более отрицательным, чем у водородного электрода в соответствующей среде (или активные металлы, расположенные в ряду напряжений слева от водорода). При кислородной деполяризации коррозии могут подвергаться и неактивные металлы вплоть до серебра ( 0 Ag+/Ag = 0, 8 B).
с восстановлением атмосферного кислорода, растворённого в коррозионной среде протекает по схеме: (+)К: О 2 + 2 Н 2 О + 4 e- = 4 OH−; (О 2/Н 2 О) = +1, 23 − 0, 059 р. Н При водородной деполяризации эл. хим. коррозии могут подвергаться металлы с электродным потенциалом более отрицательным, чем у водородного электрода в соответствующей среде (или активные металлы, расположенные в ряду напряжений слева от водорода). При кислородной деполяризации коррозии могут подвергаться и неактивные металлы вплоть до серебра ( 0 Ag+/Ag = 0, 8 B).
 При эл. хим. коррозии металлов выделяют четыре механизма, вызывающих образование и работу короткозамкнутых микро-ГЭ в результате: 1) контакта двух разных металлов; 2) контакта металла с продуктом коррозии; 3) разной конц-ции ок-ля на пов-сти металла; 4) изменения электродного потенциала металла под действием механических напряжений. Как особый случай рассматривается коррозия под действием блуждающих токов.
При эл. хим. коррозии металлов выделяют четыре механизма, вызывающих образование и работу короткозамкнутых микро-ГЭ в результате: 1) контакта двух разных металлов; 2) контакта металла с продуктом коррозии; 3) разной конц-ции ок-ля на пов-сти металла; 4) изменения электродного потенциала металла под действием механических напряжений. Как особый случай рассматривается коррозия под действием блуждающих токов.
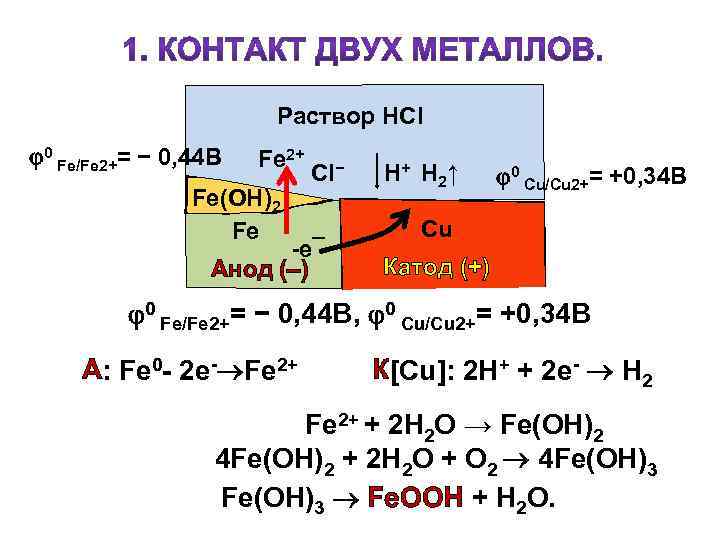 Раствор HCl 0 Fe/Fe 2+= − 0, 44 B Fe 2+ Fe(OH)2 Fe Cl− -e¯ Анод (–) Н + H 2↑ 0 Сu/Cu 2+= +0, 34 B Cu Катод (+) 0 Fe/Fe 2+= − 0, 44 B, 0 Сu/Cu 2+= +0, 34 B А: Fe 0 - 2 e- Fe 2+ К[Cu]: 2 Н+ + 2 e- Н 2 Fe 2+ + 2 H 2 O → Fe(OH)2 4 Fe(OH)2 + 2 H 2 O + O 2 4 Fe(OH)3 Fe(ОН)3 Fe. OOH + Н 2 О.
Раствор HCl 0 Fe/Fe 2+= − 0, 44 B Fe 2+ Fe(OH)2 Fe Cl− -e¯ Анод (–) Н + H 2↑ 0 Сu/Cu 2+= +0, 34 B Cu Катод (+) 0 Fe/Fe 2+= − 0, 44 B, 0 Сu/Cu 2+= +0, 34 B А: Fe 0 - 2 e- Fe 2+ К[Cu]: 2 Н+ + 2 e- Н 2 Fe 2+ + 2 H 2 O → Fe(OH)2 4 Fe(OH)2 + 2 H 2 O + O 2 4 Fe(OH)3 Fe(ОН)3 Fe. OOH + Н 2 О.
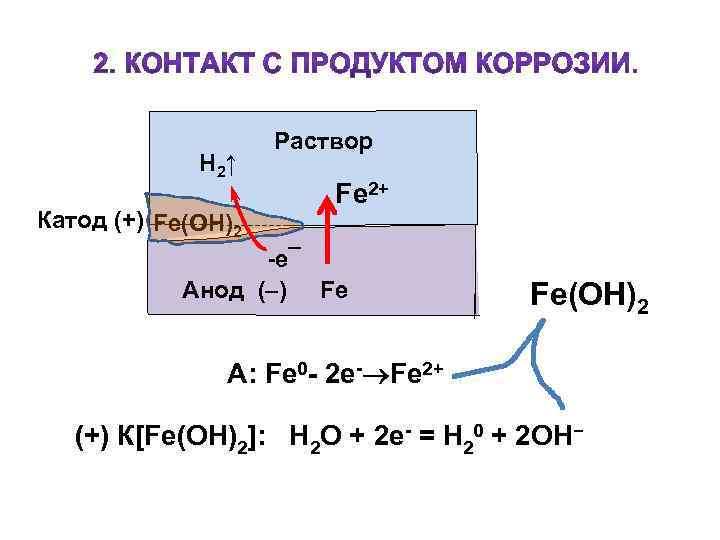 H 2↑ Катод (+) Fe(OH)2 Раствор Fe 2+ -e¯ Анод (–) Fe Fe(OH)2 А: Fe 0 - 2 e- Fe 2+ (+) К[Fe(OH)2]: Н 2 О + 2 е- = Н 20 + 2 ОН−
H 2↑ Катод (+) Fe(OH)2 Раствор Fe 2+ -e¯ Анод (–) Fe Fe(OH)2 А: Fe 0 - 2 e- Fe 2+ (+) К[Fe(OH)2]: Н 2 О + 2 е- = Н 20 + 2 ОН−
![(О 2/Н 2 О) = +1, 23 + 0, 03 lg[O 2] − (О 2/Н 2 О) = +1, 23 + 0, 03 lg[O 2] −](https://present5.com/presentation/1/65540125_41106744.pdf-img/65540125_41106744.pdf-18.jpg) (О 2/Н 2 О) = +1, 23 + 0, 03 lg[O 2] − 0, 059 р. Н [O 2 ]I > [O 2 ]II О 2 Fe 0 I О 2 Fe 3+ II е- О 2 + 2 Н 2 О + 4 е- 4 ОН- е- Fe 0 - 3 e- Fe 3+, Схема аэрационной коррозии. Fe 3+ +3 OH- Fe(OH) , 3 или Fe 0 - 2 e- Fe 2+, Fe 2+ +2 OH- Fe(OH)2, 4 Fe(OH)2 + O 2 +2 H 2 O 4 Fe(OH)3.
(О 2/Н 2 О) = +1, 23 + 0, 03 lg[O 2] − 0, 059 р. Н [O 2 ]I > [O 2 ]II О 2 Fe 0 I О 2 Fe 3+ II е- О 2 + 2 Н 2 О + 4 е- 4 ОН- е- Fe 0 - 3 e- Fe 3+, Схема аэрационной коррозии. Fe 3+ +3 OH- Fe(OH) , 3 или Fe 0 - 2 e- Fe 2+, Fe 2+ +2 OH- Fe(OH)2, 4 Fe(OH)2 + O 2 +2 H 2 O 4 Fe(OH)3.
 . Статические механ. напряжения могут понижать термодинамическую устойчивость металла, разрушать защитные пленки. При их неравномерном распределении сжатые области крист. решетки металлов вследствие перераспределения электронов, заряжаются положительно, а растянутые – отрицательно. При одноврем. воздействии коррозионной среды и механических напряжений происходит растрескивание металла (или ножевая коррозия) – один из наиболее опасных видов коррозионного разрушения.
. Статические механ. напряжения могут понижать термодинамическую устойчивость металла, разрушать защитные пленки. При их неравномерном распределении сжатые области крист. решетки металлов вследствие перераспределения электронов, заряжаются положительно, а растянутые – отрицательно. При одноврем. воздействии коррозионной среды и механических напряжений происходит растрескивание металла (или ножевая коррозия) – один из наиболее опасных видов коррозионного разрушения.
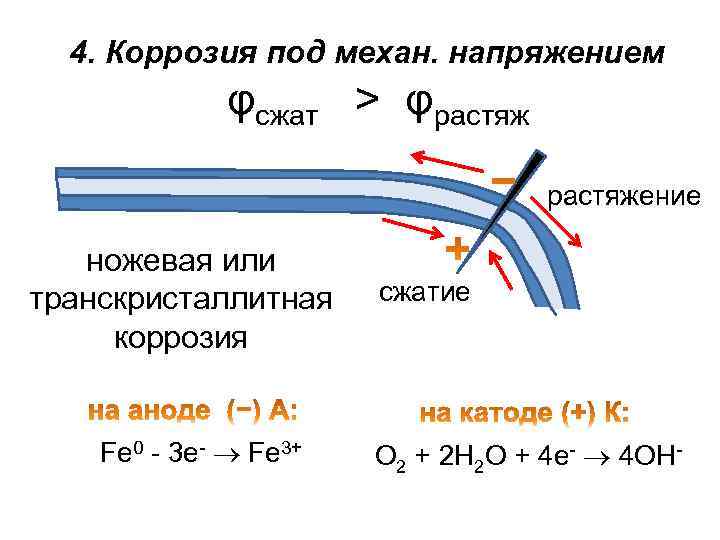 4. Коррозия под механ. напряжением φсжат > φрастяжение ножевая или транскристаллитная коррозия Fe 0 - 3 e- Fe 3+ сжатие О 2 + 2 Н 2 О + 4 е- 4 ОН-
4. Коррозия под механ. напряжением φсжат > φрастяжение ножевая или транскристаллитная коррозия Fe 0 - 3 e- Fe 3+ сжатие О 2 + 2 Н 2 О + 4 е- 4 ОН-
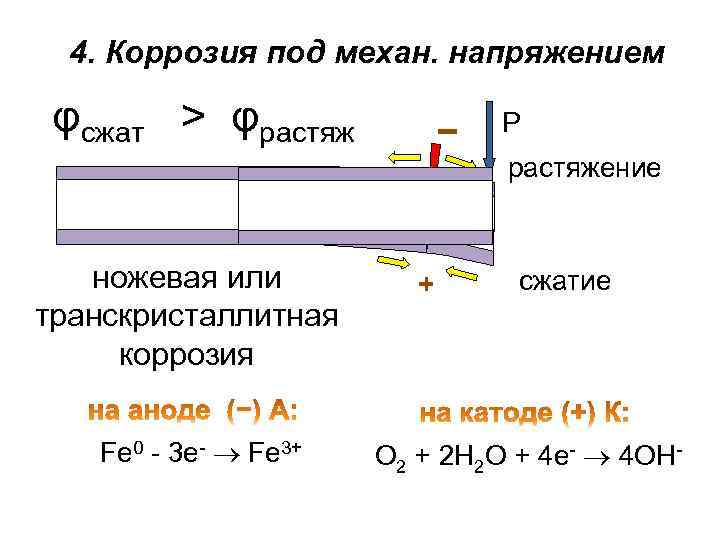 4. Коррозия под механ. напряжением φсжат > φрастяж P растяжение ножевая или транскристаллитная коррозия Fe 0 - 3 e- Fe 3+ + сжатие О 2 + 2 Н 2 О + 4 е- 4 ОН-
4. Коррозия под механ. напряжением φсжат > φрастяж P растяжение ножевая или транскристаллитная коррозия Fe 0 - 3 e- Fe 3+ + сжатие О 2 + 2 Н 2 О + 4 е- 4 ОН-
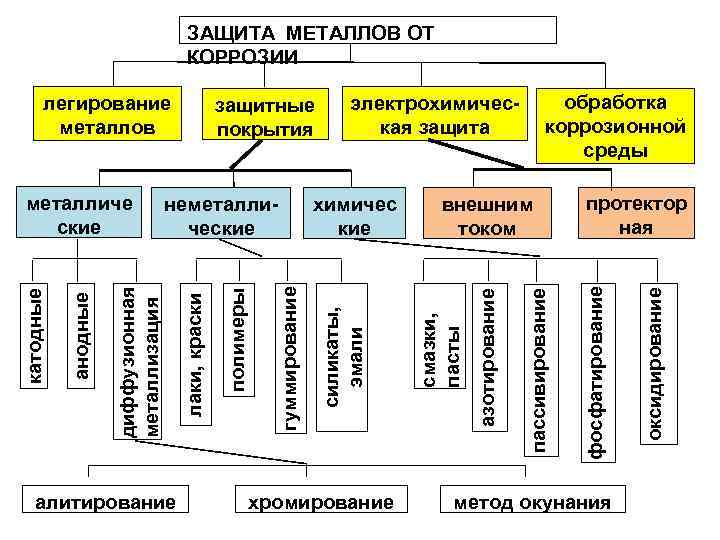 ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ алитирование обработка коррозионной среды хромирование протектор ная метод окунания оксидирование пассивирование внешним током азотирование химичес кие фосфатирование электрохимическая защита смазки, пасты гуммирование полимеры лаки, краски неметаллические диффузионная металлизация анодные катодные металличе ские защитные покрытия силикаты, эмали легирование металлов
ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ алитирование обработка коррозионной среды хромирование протектор ная метод окунания оксидирование пассивирование внешним током азотирование химичес кие фосфатирование электрохимическая защита смазки, пасты гуммирование полимеры лаки, краски неметаллические диффузионная металлизация анодные катодные металличе ские защитные покрытия силикаты, эмали легирование металлов
 Катодное покрытие – это покрытие менее активным металлом. ехр: Sn на Fe (луженое железо). Тип покрытия легко определяется при нарушении его целостности. При наличии плёнки влаги образуется гальваническая пара, в к-рой анодом явл-ся более акт. металл – железо, а катодом – менее акт. металл (олово – покрытие). Более акт. металл – железо - будет окисляться, корродировать, а на менее акт. металле – олове - будут идти процессы восстановления. Н 2 H 2 O ]: 2 H+ + 2 e- H 20 (p. H 7); Fe 2+ Sn Fe е- Схема коррозии. K H 2 O + O 2 + 4 e- 4 OH- (p. H = 7) : Fe 0 - 2 e- Fe 2+ A Fe 2+ + 2 OH- Fe(OH)2 4 Fe(OH)2 + O 2 + 2 H 2 O 4 Fe(OH)3 Принцип защиты основан на том, что менее активный металл более стоек к коррозии, и пока он сохраняет целостность, основной металл защищён от коррозионно-активной среды. В местах нарушения покрытия защищаемый металл будет подвергаться коррозии.
Катодное покрытие – это покрытие менее активным металлом. ехр: Sn на Fe (луженое железо). Тип покрытия легко определяется при нарушении его целостности. При наличии плёнки влаги образуется гальваническая пара, в к-рой анодом явл-ся более акт. металл – железо, а катодом – менее акт. металл (олово – покрытие). Более акт. металл – железо - будет окисляться, корродировать, а на менее акт. металле – олове - будут идти процессы восстановления. Н 2 H 2 O ]: 2 H+ + 2 e- H 20 (p. H 7); Fe 2+ Sn Fe е- Схема коррозии. K H 2 O + O 2 + 4 e- 4 OH- (p. H = 7) : Fe 0 - 2 e- Fe 2+ A Fe 2+ + 2 OH- Fe(OH)2 4 Fe(OH)2 + O 2 + 2 H 2 O 4 Fe(OH)3 Принцип защиты основан на том, что менее активный металл более стоек к коррозии, и пока он сохраняет целостность, основной металл защищён от коррозионно-активной среды. В местах нарушения покрытия защищаемый металл будет подвергаться коррозии.
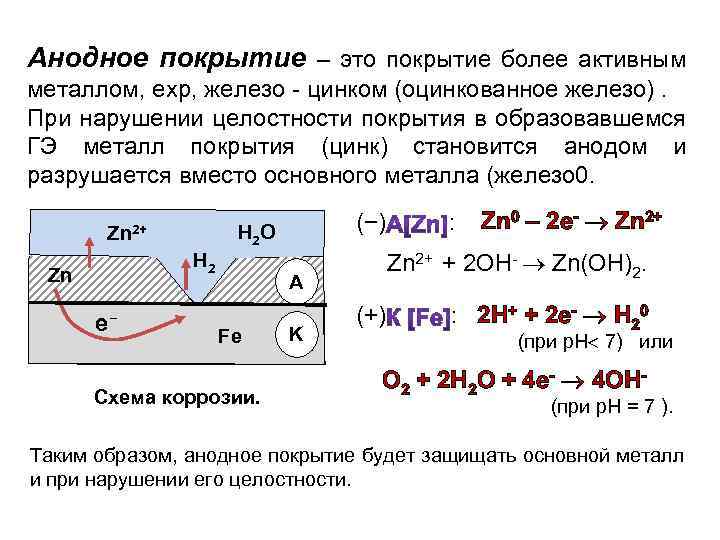 Анодное покрытие – это покрытие более активным металлом, ехр, железо - цинком (оцинкованное железо). При нарушении целостности покрытия в образовавшемся ГЭ металл покрытия (цинк) становится анодом и разрушается вместо основного металла (железо 0. Н 2 Zn е− (−) H 2 O Zn 2+ Схема коррозии. K Zn 0 – 2 e- Zn 2+ + 2 OH- Zn(OH)2. A Fe : (+) : 2 H+ + 2 e- H 20 (при р. Н 7) или О 2 + 2 Н 2 О + 4 е- 4 ОН- (при р. Н = 7 ). Таким образом, анодное покрытие будет защищать основной металл и при нарушении его целостности.
Анодное покрытие – это покрытие более активным металлом, ехр, железо - цинком (оцинкованное железо). При нарушении целостности покрытия в образовавшемся ГЭ металл покрытия (цинк) становится анодом и разрушается вместо основного металла (железо 0. Н 2 Zn е− (−) H 2 O Zn 2+ Схема коррозии. K Zn 0 – 2 e- Zn 2+ + 2 OH- Zn(OH)2. A Fe : (+) : 2 H+ + 2 e- H 20 (при р. Н 7) или О 2 + 2 Н 2 О + 4 е- 4 ОН- (при р. Н = 7 ). Таким образом, анодное покрытие будет защищать основной металл и при нарушении его целостности.
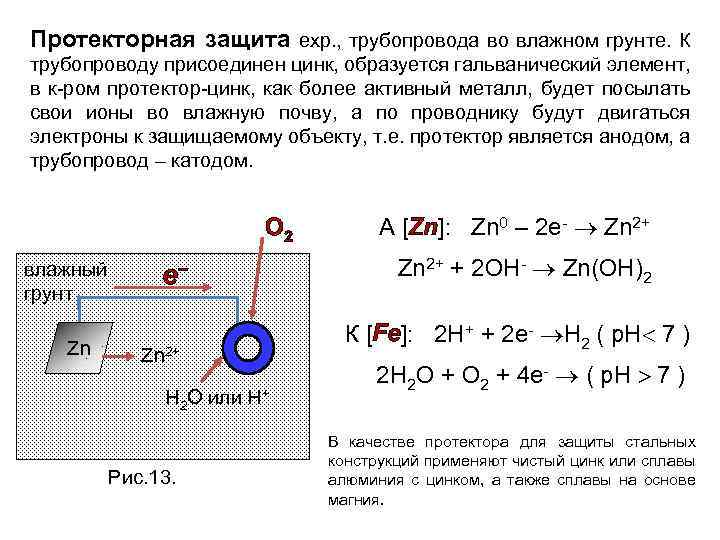 Протекторная защита ехр. , трубопровода во влажном грунте. К трубопроводу присоединен цинк, образуется гальванический элемент, в к-ром протектор-цинк, как более активный металл, будет посылать свои ионы во влажную почву, а по проводнику будут двигаться электроны к защищаемому объекту, т. е. протектор является анодом, а трубопровод – катодом. О 2 влажный грунт Zn e− Zn 2+ Н 2 О или Н+ Рис. 13. А [Zn]: Zn 0 – 2 e- Zn 2+ + 2 OH- Zn(OH)2 К [Fe]: 2 Н+ + 2 е- Н 2 ( р. Н 7 ) 2 H 2 O + O 2 + 4 e- ( p. H 7 ) В качестве протектора для защиты стальных конструкций применяют чистый цинк или сплавы алюминия с цинком, а также сплавы на основе магния.
Протекторная защита ехр. , трубопровода во влажном грунте. К трубопроводу присоединен цинк, образуется гальванический элемент, в к-ром протектор-цинк, как более активный металл, будет посылать свои ионы во влажную почву, а по проводнику будут двигаться электроны к защищаемому объекту, т. е. протектор является анодом, а трубопровод – катодом. О 2 влажный грунт Zn e− Zn 2+ Н 2 О или Н+ Рис. 13. А [Zn]: Zn 0 – 2 e- Zn 2+ + 2 OH- Zn(OH)2 К [Fe]: 2 Н+ + 2 е- Н 2 ( р. Н 7 ) 2 H 2 O + O 2 + 4 e- ( p. H 7 ) В качестве протектора для защиты стальных конструкций применяют чистый цинк или сплавы алюминия с цинком, а также сплавы на основе магния.
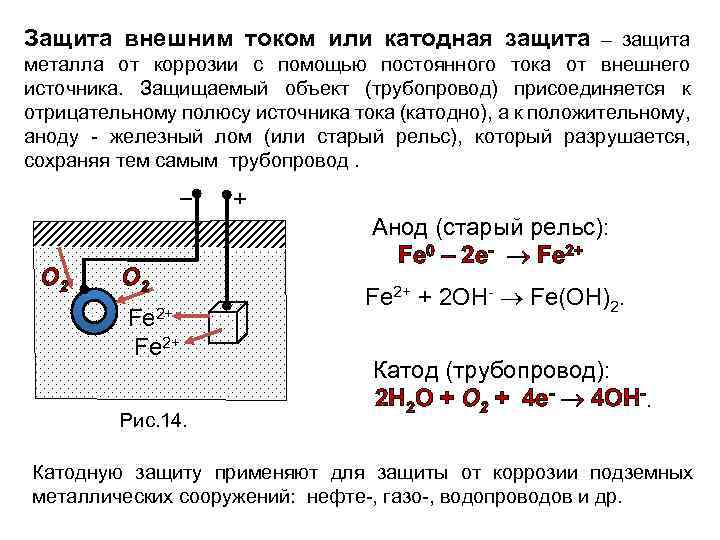 Защита внешним током или катодная защита – защита металла от коррозии с помощью постоянного тока от внешнего источника. Защищаемый объект (трубопровод) присоединяется к отрицательному полюсу источника тока (катодно), а к положительному, аноду - железный лом (или старый рельс), который разрушается, сохраняя тем самым трубопровод. − О 2 Fe 2+ Рис. 14. + Анод (старый рельс): Fe 0 – 2 e- Fe 2+ + 2 OH- Fe(OH)2. Катод (трубопровод): 2 H 2 O + O 2 + 4 e- 4 OH-. Катодную защиту применяют для защиты от коррозии подземных металлических сооружений: нефте-, газо-, водопроводов и др.
Защита внешним током или катодная защита – защита металла от коррозии с помощью постоянного тока от внешнего источника. Защищаемый объект (трубопровод) присоединяется к отрицательному полюсу источника тока (катодно), а к положительному, аноду - железный лом (или старый рельс), который разрушается, сохраняя тем самым трубопровод. − О 2 Fe 2+ Рис. 14. + Анод (старый рельс): Fe 0 – 2 e- Fe 2+ + 2 OH- Fe(OH)2. Катод (трубопровод): 2 H 2 O + O 2 + 4 e- 4 OH-. Катодную защиту применяют для защиты от коррозии подземных металлических сооружений: нефте-, газо-, водопроводов и др.