 Коррозия металлов и методы защиты от нее
Коррозия металлов и методы защиты от нее
 План лекции n Классификации коррозионных процессов n Химическая коррозия n Электрохимическая n Защита коррозия металлов от коррозии
План лекции n Классификации коррозионных процессов n Химическая коррозия n Электрохимическая n Защита коррозия металлов от коррозии
 Классификации коррозии І. Классификация металлов по их коррозионной стойкости: а) по положению в периодической системе элементов Д. И. Менделеева б) по значению стандартного электродного потенциала ІІ. Классификация коррозионных процессов: а) по виду поражений б) по механизму протекания
Классификации коррозии І. Классификация металлов по их коррозионной стойкости: а) по положению в периодической системе элементов Д. И. Менделеева б) по значению стандартного электродного потенциала ІІ. Классификация коррозионных процессов: а) по виду поражений б) по механизму протекания
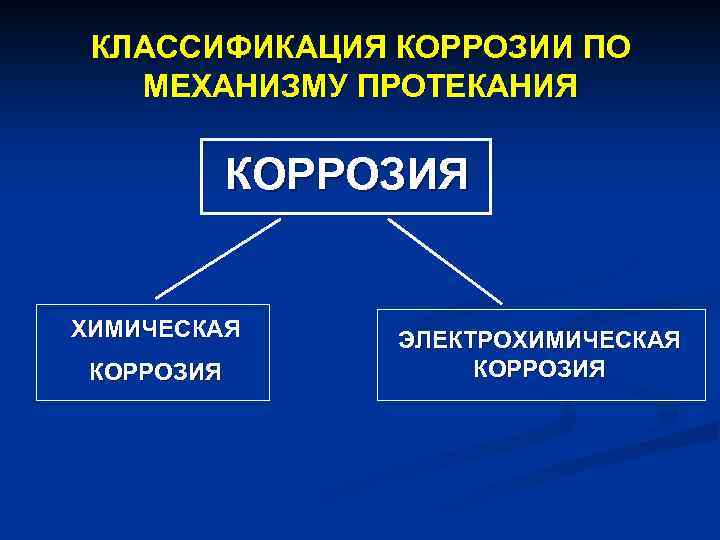 КЛАССИФИКАЦИЯ КОРРОЗИИ ПО МЕХАНИЗМУ ПРОТЕКАНИЯ КОРРОЗИЯ ХИМИЧЕСКАЯ КОРРОЗИЯ ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
КЛАССИФИКАЦИЯ КОРРОЗИИ ПО МЕХАНИЗМУ ПРОТЕКАНИЯ КОРРОЗИЯ ХИМИЧЕСКАЯ КОРРОЗИЯ ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
 Классификация химической коррозии по условиям протекания Газовая В среде неэлектролита Органических маслах Нефтяных маслах Расплавах металлов Наводораживание Жидкой сере Декарбонизация Бромной воде Ванадиевая Водородная Графитизация
Классификация химической коррозии по условиям протекания Газовая В среде неэлектролита Органических маслах Нефтяных маслах Расплавах металлов Наводораживание Жидкой сере Декарбонизация Бромной воде Ванадиевая Водородная Графитизация
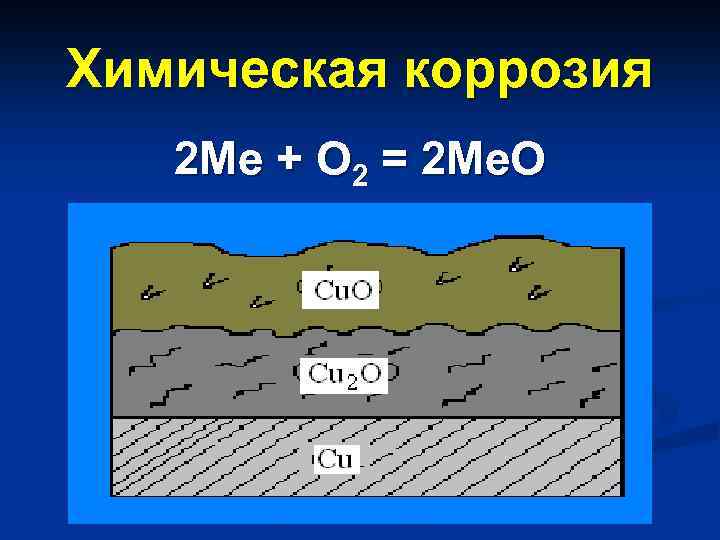 Химическая коррозия 2 Ме + О 2 = 2 Ме. О
Химическая коррозия 2 Ме + О 2 = 2 Ме. О
 Классификация электрохимической коррозии по условиям протекания n n n n атмосферная контактная при различном доступе О 2 почвенная морская фреттинг (агрессивная среда + силы трения) кавитация (ударное действие агрессивной среды) электрокоррозия под действием блуждающих токов
Классификация электрохимической коррозии по условиям протекания n n n n атмосферная контактная при различном доступе О 2 почвенная морская фреттинг (агрессивная среда + силы трения) кавитация (ударное действие агрессивной среды) электрокоррозия под действием блуждающих токов
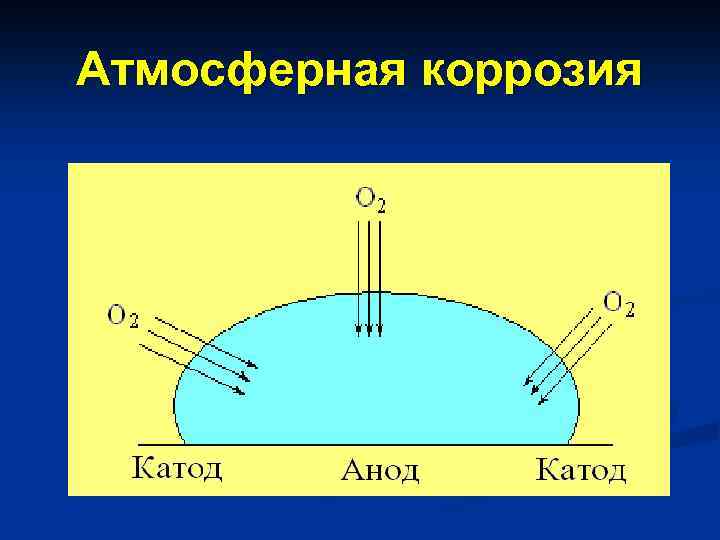 Атмосферная коррозия
Атмосферная коррозия
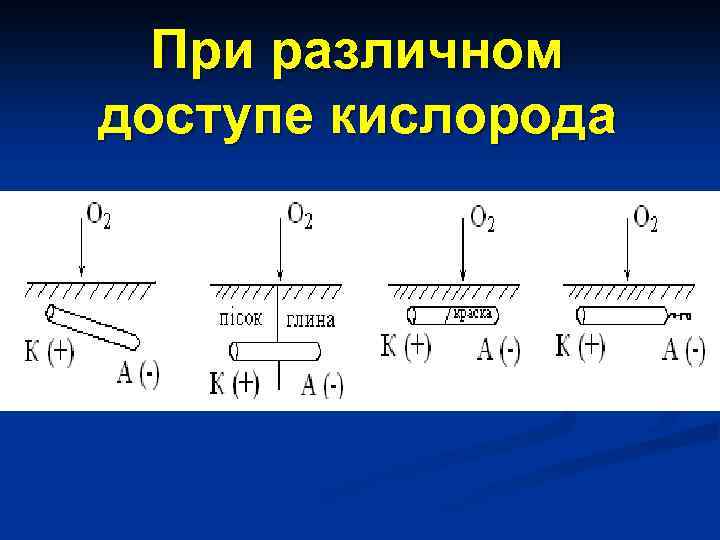 При различном доступе кислорода
При различном доступе кислорода
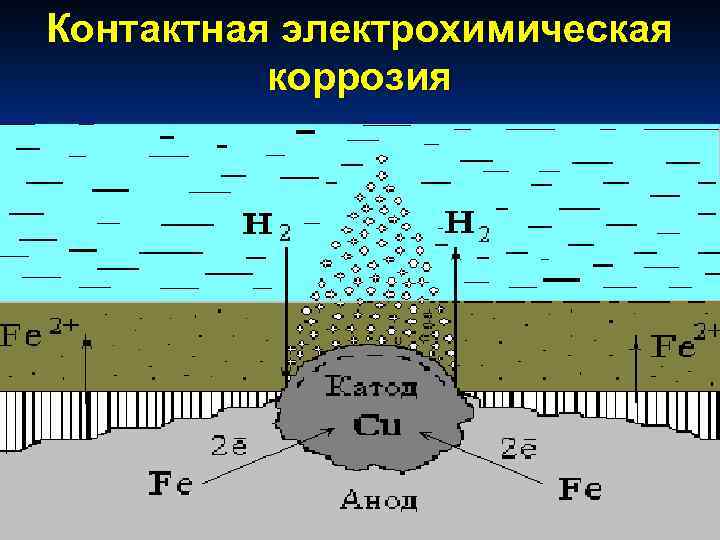 Контактная электрохимическая коррозия
Контактная электрохимическая коррозия
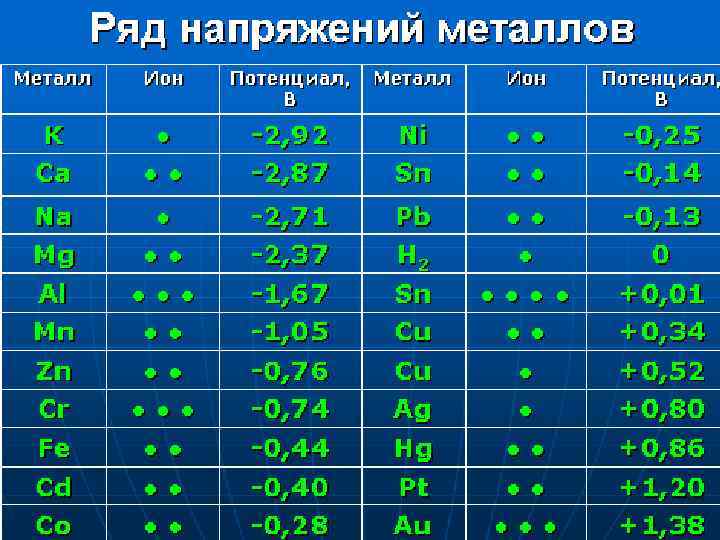
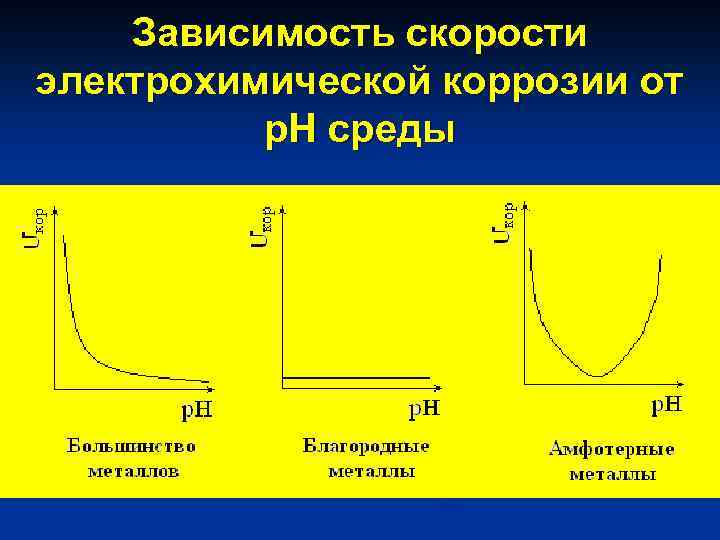 Зависимость скорости электрохимической коррозии от р. Н среды
Зависимость скорости электрохимической коррозии от р. Н среды
 Основные методы защиты металлов от коррозии n Действие на металл n Действие на агрессивную среду n Рациональное изделий конструирование
Основные методы защиты металлов от коррозии n Действие на металл n Действие на агрессивную среду n Рациональное изделий конструирование
 Действие на металл а)обработка поверхности б)легирование в) нанесение металлических и неметаллических покрытий г) электрохимическая защита
Действие на металл а)обработка поверхности б)легирование в) нанесение металлических и неметаллических покрытий г) электрохимическая защита
 Обработка поверхности металлов - Механическая зачистка для снятия окалины - Обезжиривание органическими растворителями, щелочами, мылами - Травление - Фосфатирование
Обработка поверхности металлов - Механическая зачистка для снятия окалины - Обезжиривание органическими растворителями, щелочами, мылами - Травление - Фосфатирование
 ТРАВЛЕНИЕ РЯД НАПРЯЖЕНИЙ АНИОНОВ I- > Cl- > SO 42 - > NO 3 - > CO 32 - > PO 43 ИНГИБИТОРЫ КОРРОЗИИ
ТРАВЛЕНИЕ РЯД НАПРЯЖЕНИЙ АНИОНОВ I- > Cl- > SO 42 - > NO 3 - > CO 32 - > PO 43 ИНГИБИТОРЫ КОРРОЗИИ
 ФОСФАТИРОВАНИЕ 3 Fe + 2 H 3 PO 4 → Fe 3(PO 4)2 + 3 H 2 Fe + H 3 PO 4 → Fe. HPO 4 + H 2 Fe + 2 H 3 PO 4 → Fe(H 2 PO 4)2 + H 2
ФОСФАТИРОВАНИЕ 3 Fe + 2 H 3 PO 4 → Fe 3(PO 4)2 + 3 H 2 Fe + H 3 PO 4 → Fe. HPO 4 + H 2 Fe + 2 H 3 PO 4 → Fe(H 2 PO 4)2 + H 2
 Легирование n Rлег. ион < Rосн. ион n Образование на поверхности сплава слоя оксида легирующего металла n Образование двойных оксидов основного и легирующего металла: Ме. О · Ме 2*О 3 Ме. О · Ме 2*О 4
Легирование n Rлег. ион < Rосн. ион n Образование на поверхности сплава слоя оксида легирующего металла n Образование двойных оксидов основного и легирующего металла: Ме. О · Ме 2*О 3 Ме. О · Ме 2*О 4
 Неметаллические покрытия n Лакокрасочные n Полимерные n Эмали n Смазки n Оксидирование (анодирование) n Фосфатирование
Неметаллические покрытия n Лакокрасочные n Полимерные n Эмали n Смазки n Оксидирование (анодирование) n Фосфатирование
 Металлические покрытия анодные катодные Покрытия для железа Al…Zn…Cr…Fe…Ni…Pb…Cu анодные покрытия катодные покрытия
Металлические покрытия анодные катодные Покрытия для железа Al…Zn…Cr…Fe…Ni…Pb…Cu анодные покрытия катодные покрытия
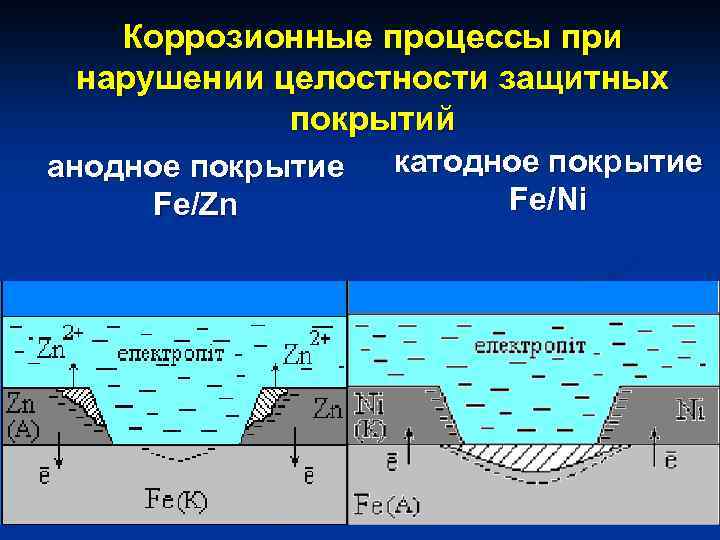 Коррозионные процессы при нарушении целостности защитных покрытий анодное покрытие Fe/Zn катодное покрытие Fe/Ni
Коррозионные процессы при нарушении целостности защитных покрытий анодное покрытие Fe/Zn катодное покрытие Fe/Ni
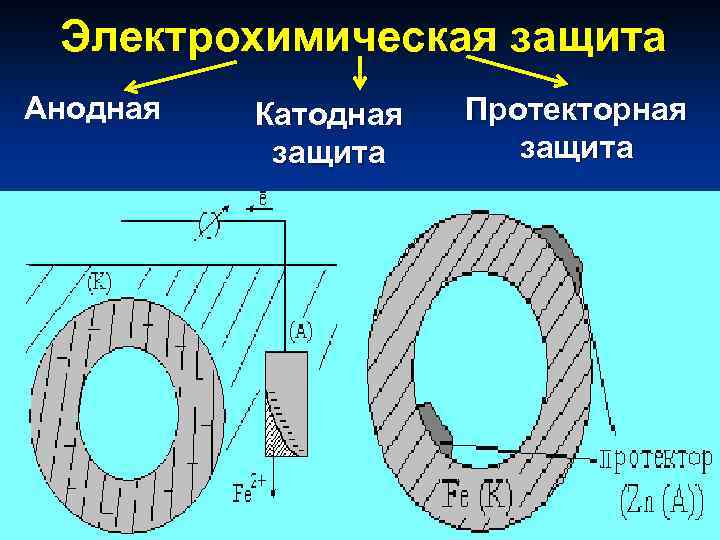 Электрохимическая защита Анодная Катодная защита Протекторная защита
Электрохимическая защита Анодная Катодная защита Протекторная защита
 Методы воздействия на агрессивную среду n Создание инертной атмосферы n Обескислороживание агрессивной среды n Введение ингибиторов в агрессивную среду
Методы воздействия на агрессивную среду n Создание инертной атмосферы n Обескислороживание агрессивной среды n Введение ингибиторов в агрессивную среду
 Классификация ингибиторов По химической природе По механизму действия n Органические ингибиторы n Анодные пиридин, амины R-NH 2 тиоспирты R-SH тиоэфиры R 1 -S-R 2 ацетилены Cn. Hn n Катодные n Неорганические ингибиторы Na 2 Cr. O 4, K 2 Cr 2 O 7 Na. NO 2, KNO 2 Na 3 BO 3, Na 2 B 4 O 7 Na 3 PO 4, Na 2 HPO 4
Классификация ингибиторов По химической природе По механизму действия n Органические ингибиторы n Анодные пиридин, амины R-NH 2 тиоспирты R-SH тиоэфиры R 1 -S-R 2 ацетилены Cn. Hn n Катодные n Неорганические ингибиторы Na 2 Cr. O 4, K 2 Cr 2 O 7 Na. NO 2, KNO 2 Na 3 BO 3, Na 2 B 4 O 7 Na 3 PO 4, Na 2 HPO 4
 Методы рационального конструирования изделий Сведение к минимуму контактов разных металлов n Изоляционные прокладки n Замена металлических деталей на детали из других материалов n Уменьшение количества щелей и зазоров n Учет возможности повторного нанесения защитных покрытий n
Методы рационального конструирования изделий Сведение к минимуму контактов разных металлов n Изоляционные прокладки n Замена металлических деталей на детали из других материалов n Уменьшение количества щелей и зазоров n Учет возможности повторного нанесения защитных покрытий n
 Примеры тестовых заданий КОБАЛЬТ НАХОДИТСЯ В КОНТАКТЕ С МЕДЬЮ В НЕЙТРАЛЬНОЙ СРЕДЕ. ПРИ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ НА КАТОДЕ БУДЕТ ПРОТЕКАТЬ РЕАКЦИЯ а) Co 2+ + 2 e = Co 0 б) Cu 2+ + 2 e = Cu 0 в) 2 H 2 O + O 2 + 4 e = 4 OHг) H+ + OH- = H 2 O д) 2 H+ + 2 e = H 2
Примеры тестовых заданий КОБАЛЬТ НАХОДИТСЯ В КОНТАКТЕ С МЕДЬЮ В НЕЙТРАЛЬНОЙ СРЕДЕ. ПРИ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ НА КАТОДЕ БУДЕТ ПРОТЕКАТЬ РЕАКЦИЯ а) Co 2+ + 2 e = Co 0 б) Cu 2+ + 2 e = Cu 0 в) 2 H 2 O + O 2 + 4 e = 4 OHг) H+ + OH- = H 2 O д) 2 H+ + 2 e = H 2
 Примеры тестовых заданий В ЩЕЛОЧНОЙ СРЕДЕ МОЖЕТ ПРОТЕКАТЬ КОРРОЗИЯ КОНТАКТНОЙ ПАРЫ МЕТАЛЛОВ А. Fe / Mn Б. Fe / Zn В. Fe / Ni
Примеры тестовых заданий В ЩЕЛОЧНОЙ СРЕДЕ МОЖЕТ ПРОТЕКАТЬ КОРРОЗИЯ КОНТАКТНОЙ ПАРЫ МЕТАЛЛОВ А. Fe / Mn Б. Fe / Zn В. Fe / Ni
 Примеры тестовых заданий В КЛАССИФИКАЦИЮ КОРРОЗИОННЫХ ПРОЦЕССОВ ПО ВИДУ ПОРАЖЕНИЙ НЕ ВКЛЮЧЕНЫ А. равномерная общая коррозия Б. коррозия пятнами В. межкристаллитная коррозия Г. коррозия под действием блуждающих токов
Примеры тестовых заданий В КЛАССИФИКАЦИЮ КОРРОЗИОННЫХ ПРОЦЕССОВ ПО ВИДУ ПОРАЖЕНИЙ НЕ ВКЛЮЧЕНЫ А. равномерная общая коррозия Б. коррозия пятнами В. межкристаллитная коррозия Г. коррозия под действием блуждающих токов
 ЗАЩИТУ СТАЛЬНОЙ КОНСТРУКЦИИ ОТ КОРРОЗИИ ПРОТЕКТОРОМ ИЗ МАГНИЯ В КИСЛОЙ СРЕДЕ ОТОБРАЖАЮТ УРАВНЕНИЯ 1. 2. 3. 4. А (-) Fe – 2 e- = Fe 2+ А (-) Mg – 2 e- = Mg 2+ А (-) Mg 0 – 2 e- = Mg 2+ А (-) Mg – 2 e- = Mg 2+ К (+) 2 H+ + 2 e- = H 2 К (+) Fe 2+ + 2 e- = Fe К(+)O 2+2 H 2 O+4 e- = 4 OH К (+) 2 H+ + 2 e- = H 2
ЗАЩИТУ СТАЛЬНОЙ КОНСТРУКЦИИ ОТ КОРРОЗИИ ПРОТЕКТОРОМ ИЗ МАГНИЯ В КИСЛОЙ СРЕДЕ ОТОБРАЖАЮТ УРАВНЕНИЯ 1. 2. 3. 4. А (-) Fe – 2 e- = Fe 2+ А (-) Mg – 2 e- = Mg 2+ А (-) Mg 0 – 2 e- = Mg 2+ А (-) Mg – 2 e- = Mg 2+ К (+) 2 H+ + 2 e- = H 2 К (+) Fe 2+ + 2 e- = Fe К(+)O 2+2 H 2 O+4 e- = 4 OH К (+) 2 H+ + 2 e- = H 2
 Методы защиты металлов от коррозии Сущность метода Классификация метода 1. Легирование А. Влияние на агрессивную среду 2. Введение ингибитора Б. Влияние на металл 3. Протекторная защита В. Учет особенностей металлоконструкций 4. Обескислороживание 5. Защитные покрытия
Методы защиты металлов от коррозии Сущность метода Классификация метода 1. Легирование А. Влияние на агрессивную среду 2. Введение ингибитора Б. Влияние на металл 3. Протекторная защита В. Учет особенностей металлоконструкций 4. Обескислороживание 5. Защитные покрытия


