20_Коррозия металлов и электролиз.ppt
- Количество слайдов: 18
 Коррозия металлов и электролиз Лекция 20 по курсу «Общая химия»
Коррозия металлов и электролиз Лекция 20 по курсу «Общая химия»
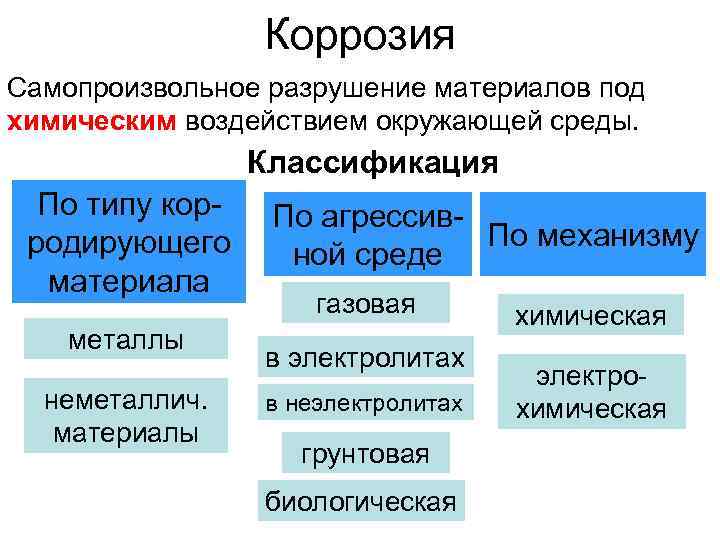 Коррозия Самопроизвольное разрушение материалов под химическим воздействием окружающей среды. Классификация По типу корродирующего материала металлы неметаллич. материалы По агрессив. По механизму ной среде газовая в электролитах в неэлектролитах грунтовая биологическая химическая электрохимическая
Коррозия Самопроизвольное разрушение материалов под химическим воздействием окружающей среды. Классификация По типу корродирующего материала металлы неметаллич. материалы По агрессив. По механизму ной среде газовая в электролитах в неэлектролитах грунтовая биологическая химическая электрохимическая
 Химическая коррозия Химическое взаимодействие металла с агрессивной средой Примеры 4 Fe + 3 O 2 = 2 Fe 2 O 3 в кислородсодержащей атмосфере при высокой 3 Fe + 2 O 2 = Fe 3 O 4 температуре При воздействии органи. Cu + RCl = ческих хлорпроизводных = Cu. Cl 2 + R–R (фреонов и т. п. ) Если подойник из Zn + 2 CH 3 CH(OH)COOH = = Zn(CH 3 CH(OH)COO)2 + H 2 оцинкованной стали
Химическая коррозия Химическое взаимодействие металла с агрессивной средой Примеры 4 Fe + 3 O 2 = 2 Fe 2 O 3 в кислородсодержащей атмосфере при высокой 3 Fe + 2 O 2 = Fe 3 O 4 температуре При воздействии органи. Cu + RCl = ческих хлорпроизводных = Cu. Cl 2 + R–R (фреонов и т. п. ) Если подойник из Zn + 2 CH 3 CH(OH)COOH = = Zn(CH 3 CH(OH)COO)2 + H 2 оцинкованной стали
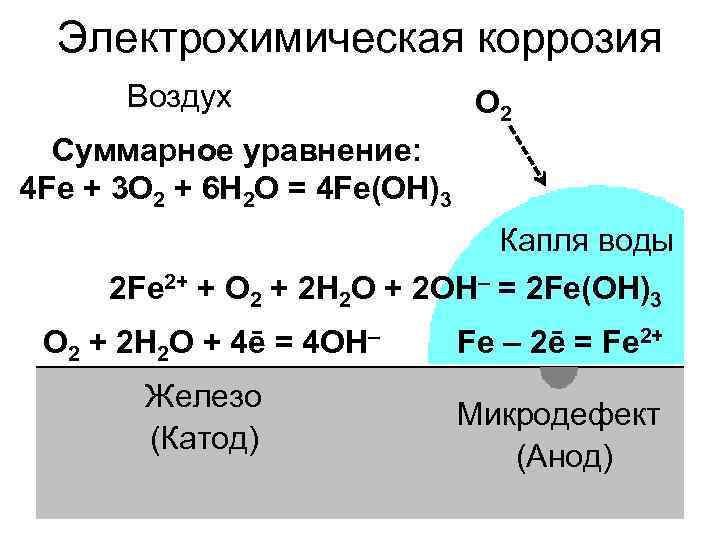 Электрохимическая коррозия Воздух O 2 Суммарное уравнение: 4 Fe + 3 O 2 + 6 H 2 O = 4 Fe(OH)3 Капля воды 2 Fe 2+ + O 2 + 2 H 2 O + 2 OH– = 2 Fe(OH)3 O 2 + 2 H 2 O + 4ē = 4 OH– Железо (Катод) Fe – 2ē = Fe 2+ Микродефект (Анод)
Электрохимическая коррозия Воздух O 2 Суммарное уравнение: 4 Fe + 3 O 2 + 6 H 2 O = 4 Fe(OH)3 Капля воды 2 Fe 2+ + O 2 + 2 H 2 O + 2 OH– = 2 Fe(OH)3 O 2 + 2 H 2 O + 4ē = 4 OH– Железо (Катод) Fe – 2ē = Fe 2+ Микродефект (Анод)
 Способы защиты от коррозии Конструкционный Кортеновская сталь Нержавеющая сталь Содержит ~ 2% Cu Плотная оксидная пленка Один из составов: 18% Cr, 10% Ni
Способы защиты от коррозии Конструкционный Кортеновская сталь Нержавеющая сталь Содержит ~ 2% Cu Плотная оксидная пленка Один из составов: 18% Cr, 10% Ni
 Способы защиты от коррозии Нанесение защитных покрытий Пассивный лакокрасочные полимерные Есть и другие… металлические Zn Анимация Sn
Способы защиты от коррозии Нанесение защитных покрытий Пассивный лакокрасочные полимерные Есть и другие… металлические Zn Анимация Sn
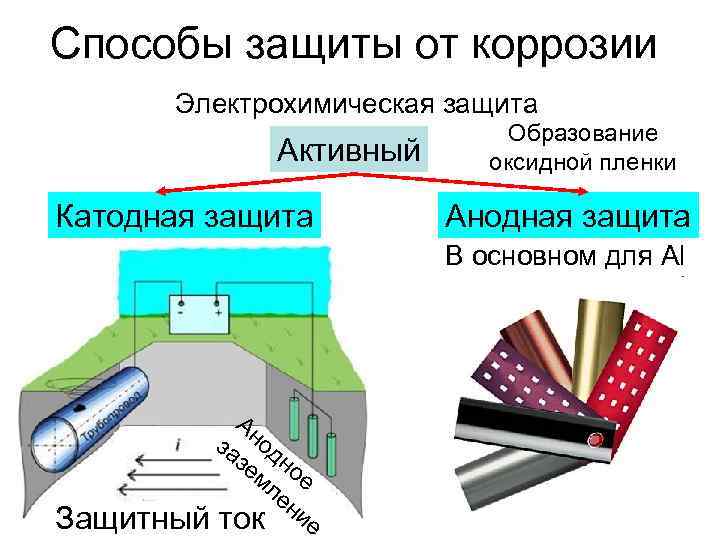 Способы защиты от коррозии Электрохимическая защита Активный Катодная защита Образование оксидной пленки Анодная защита В основном для Al Ан за од зе но мл е ен Защитный ток ие
Способы защиты от коррозии Электрохимическая защита Активный Катодная защита Образование оксидной пленки Анодная защита В основном для Al Ан за од зе но мл е ен Защитный ток ие
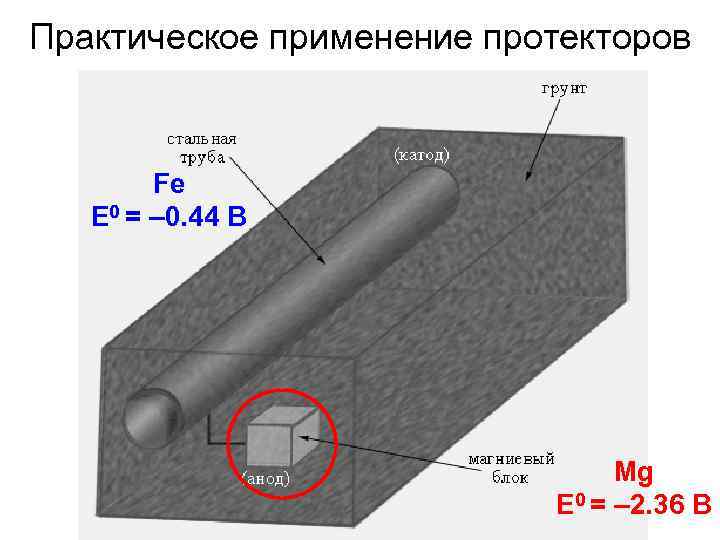 Практическое применение протекторов Fe E 0 = – 0. 44 В Mg E 0 = – 2. 36 В
Практическое применение протекторов Fe E 0 = – 0. 44 В Mg E 0 = – 2. 36 В
 Электролиз Окислительно-восстановительные реакции в растворе или расплаве электролитов под действием электрического тока. Окислитель: анод Не материал анода и катода, Восстановитель: катод а электрический ток! Водные растворы Неводные растворы Расплавы Восстанавливаются: Катионы металлов Катионы Н+ и вода Катионы металлов Окисляются: Анионы кислот и ОН– Материал анода Вода Анионы Материал анода
Электролиз Окислительно-восстановительные реакции в растворе или расплаве электролитов под действием электрического тока. Окислитель: анод Не материал анода и катода, Восстановитель: катод а электрический ток! Водные растворы Неводные растворы Расплавы Восстанавливаются: Катионы металлов Катионы Н+ и вода Катионы металлов Окисляются: Анионы кислот и ОН– Материал анода Вода Анионы Материал анода
 Электролиз расплавов: алгоритм 1. Написать уравнение диссоциации вещества в расплаве; 2. Написать полуреакцию восстановления катиона; 3. Написать полуреакции окисления для аниона и/или материала анода; 4. Сложить полученные полуреакции (если материал анода окисляется – может быть 2 параллельных процесса); 5. Превратить ионное уравнение в молекулярное, если нужно.
Электролиз расплавов: алгоритм 1. Написать уравнение диссоциации вещества в расплаве; 2. Написать полуреакцию восстановления катиона; 3. Написать полуреакции окисления для аниона и/или материала анода; 4. Сложить полученные полуреакции (если материал анода окисляется – может быть 2 параллельных процесса); 5. Превратить ионное уравнение в молекулярное, если нужно.
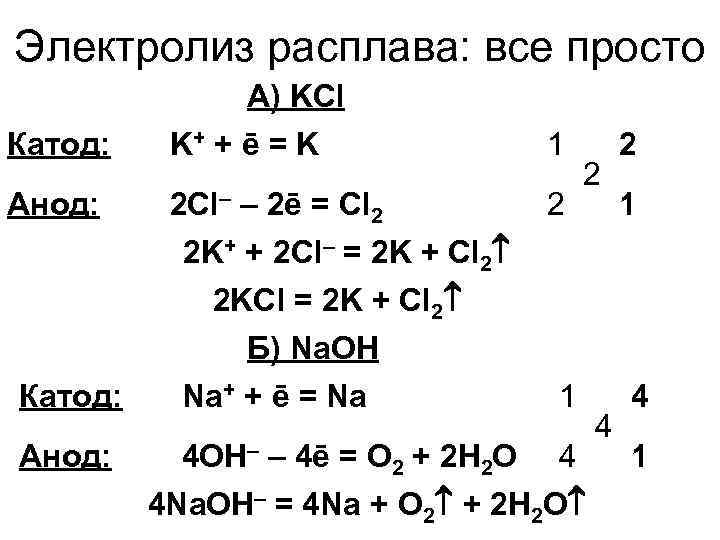 Электролиз расплава: все просто Катод: Анод: А) KCl K+ + ē = K 2 Cl– – 2ē = Cl 2 2 K+ + 2 Cl– = 2 K + Cl 2 2 KCl = 2 K + Cl 2 Б) Na. OH Na+ + ē = Na 1 2 2 1 4 OH– – 4ē = O 2 + 2 H 2 O 4 4 Na. OH– = 4 Na + O 2 + 2 H 2 O 4 2 1 4 1
Электролиз расплава: все просто Катод: Анод: А) KCl K+ + ē = K 2 Cl– – 2ē = Cl 2 2 K+ + 2 Cl– = 2 K + Cl 2 2 KCl = 2 K + Cl 2 Б) Na. OH Na+ + ē = Na 1 2 2 1 4 OH– – 4ē = O 2 + 2 H 2 O 4 4 Na. OH– = 4 Na + O 2 + 2 H 2 O 4 2 1 4 1
 Электролиз растворов: алгоритм 1. Написать уравнения диссоциации всех присутствующих сильных электролитов; 2. Что может реагировать на катоде? 3. Написать полуреакции восстановления для всего, найти по справочнику Е 0; 4. Стандартны ли условия (Е = Е 0)? 5. Выбрать преобладающую полуреакцию (с наибольшим значением Е) для катода; 6. Повторить шаги 2 -5 для анодных процессов (выбрать полуреакцию с наименьшим Е); 7. Сложить выбранные полуреакции.
Электролиз растворов: алгоритм 1. Написать уравнения диссоциации всех присутствующих сильных электролитов; 2. Что может реагировать на катоде? 3. Написать полуреакции восстановления для всего, найти по справочнику Е 0; 4. Стандартны ли условия (Е = Е 0)? 5. Выбрать преобладающую полуреакцию (с наибольшим значением Е) для катода; 6. Повторить шаги 2 -5 для анодных процессов (выбрать полуреакцию с наименьшим Е); 7. Сложить выбранные полуреакции.
 Электролиз растворов А) Раствор KCl Катод: K+ + ē = K 2 H 2 O + 2ē = 2 OH– + H 2 (E 0 = – 2. 924 В) (E = – 0. 414 В) H 2 O намного легче восстанавливается, чем K+ Анод: 2 Cl– – 2ē = Cl 2 2 H 2 O – 4ē = O 2 + 4 H+ (E 0 = 1. 359 В) (E 0 = 1. 228 В) Сравнимые стандартные потенциалы, НО! Условия не стандартные (p. H = 7), Е = 1. 642 В 2 Cl– + 2 H 2 O = Cl 2 + 2 OH– + H 2 2 KCl + 2 H 2 O = Cl 2 + 2 KOH + H 2
Электролиз растворов А) Раствор KCl Катод: K+ + ē = K 2 H 2 O + 2ē = 2 OH– + H 2 (E 0 = – 2. 924 В) (E = – 0. 414 В) H 2 O намного легче восстанавливается, чем K+ Анод: 2 Cl– – 2ē = Cl 2 2 H 2 O – 4ē = O 2 + 4 H+ (E 0 = 1. 359 В) (E 0 = 1. 228 В) Сравнимые стандартные потенциалы, НО! Условия не стандартные (p. H = 7), Е = 1. 642 В 2 Cl– + 2 H 2 O = Cl 2 + 2 OH– + H 2 2 KCl + 2 H 2 O = Cl 2 + 2 KOH + H 2
 Электролиз растворов Б) Раствор Cu. SO 4 Катод: 2 H 2 O + 2ē = 2 OH– + H 2 Cu 2+ + 2ē = Cu (E = – 0. 414 В) (E 0 = 0. 337 В) Cu 2+ легче восстанавливается, чем H 2 O Анод: 2 H 2 O – 4ē = O 2 + 4 H+ (E 0 = 1. 359 В, Е = 1. 642 В с учетом p. H) 2 SO 42– – 2ē = 2 S 2 O 82– (E 0 = 2. 010 В) 2 Cu 2+ + 2 H 2 O = 2 Cu + O 2 + 4 H+ 2 Cu. SO 4 + 2 H 2 O = 2 Cu + O 2 + 2 H 2 SO 4
Электролиз растворов Б) Раствор Cu. SO 4 Катод: 2 H 2 O + 2ē = 2 OH– + H 2 Cu 2+ + 2ē = Cu (E = – 0. 414 В) (E 0 = 0. 337 В) Cu 2+ легче восстанавливается, чем H 2 O Анод: 2 H 2 O – 4ē = O 2 + 4 H+ (E 0 = 1. 359 В, Е = 1. 642 В с учетом p. H) 2 SO 42– – 2ē = 2 S 2 O 82– (E 0 = 2. 010 В) 2 Cu 2+ + 2 H 2 O = 2 Cu + O 2 + 4 H+ 2 Cu. SO 4 + 2 H 2 O = 2 Cu + O 2 + 2 H 2 SO 4
 Правила электролиза растворов Катодные процессы E 0 Металлы <<– 0. 414 В До Ti – 0. 414 В От Ti до Sn >>– 0. 414 В После Sn Катодный процесс Выделение водорода Водород + металл Выделение металла Анодные процессы Анион Анодный процесс Бескислородный Окисление до (кроме F–) свободного неметалла Кислородсодержащий Выделение O 2
Правила электролиза растворов Катодные процессы E 0 Металлы <<– 0. 414 В До Ti – 0. 414 В От Ti до Sn >>– 0. 414 В После Sn Катодный процесс Выделение водорода Водород + металл Выделение металла Анодные процессы Анион Анодный процесс Бескислородный Окисление до (кроме F–) свободного неметалла Кислородсодержащий Выделение O 2
 Участие материала анода Только металлы до Cu включительно А) Окисление электрическим током Cu – 2ē = Cu 2+ А на катоде – обратный процесс! Б) Окисление продуктами электролиза Электролиз Al 2 O 3, графитовые аноды O 2– + 2 ē = O 2 O + C = CO 2
Участие материала анода Только металлы до Cu включительно А) Окисление электрическим током Cu – 2ē = Cu 2+ А на катоде – обратный процесс! Б) Окисление продуктами электролиза Электролиз Al 2 O 3, графитовые аноды O 2– + 2 ē = O 2 O + C = CO 2
 Количественные законы электролиза 1) При электролизе масса превращенного вещества прямо пропорциональна электрическому заряду, прошедшему через раствор. 2) При равном заряде масса превращенного вещества зависит от массы и заряда ионов вещества. М. Фарадей
Количественные законы электролиза 1) При электролизе масса превращенного вещества прямо пропорциональна электрическому заряду, прошедшему через раствор. 2) При равном заряде масса превращенного вещества зависит от массы и заряда ионов вещества. М. Фарадей
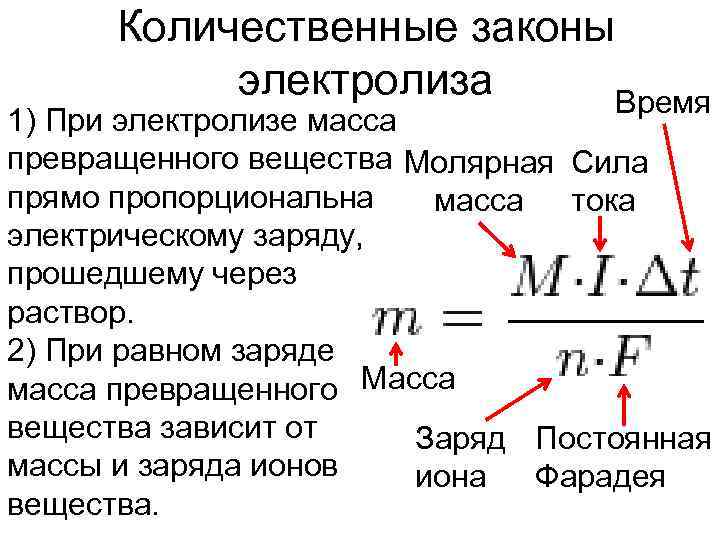 Количественные законы электролиза Время 1) При электролизе масса превращенного вещества Молярная Сила прямо пропорциональна масса тока электрическому заряду, прошедшему через раствор. 2) При равном заряде масса превращенного Масса вещества зависит от Заряд Постоянная массы и заряда ионов иона Фарадея вещества.
Количественные законы электролиза Время 1) При электролизе масса превращенного вещества Молярная Сила прямо пропорциональна масса тока электрическому заряду, прошедшему через раствор. 2) При равном заряде масса превращенного Масса вещества зависит от Заряд Постоянная массы и заряда ионов иона Фарадея вещества.


