c0ed20fe2c288275779bb244042d6bff.ppt
- Количество слайдов: 87

Коррекция нарушений при врожденных и приобретенных иммунодефицитных заболеваниях Проф. кафедры педиатрии ИПО Ширяева Г. П.

n Основные элементы иммунной системы полностью закладываются на 15 й неделе внутриутробного развития человека. Однако иммунная система является незрелой и в период младенчества нуждается в антигенной селекции и «обучении» для достижения полной зрелости.

Иммунная система Неспецифические факторы защиты: n Кожа и слизистые n Цитокины и комплемент Специфические иммунные механизмы: n Антитела n лимфоциты

Иммунитет Врожденный: Формируется в онтогенезе вне зависимости от «запроса» Эффекторы миелоидные клетки Распознаются группы чужеродных молекул, связанных с патогенностью Популяции клеток реагируют как целое Угроза аутоагрессии минимальна Память отсутствует Распознавание и удаление опасного Адаптивный: Формируется в ответ на «запрос» Эффекторы лимфоидные клетки Распознаютс индивидуальные молекулы (антигены) Реакция на антиген клональная Велика угроза аутоагрессии Существует иммунологическая память Распознавание и удаление чужого Память

Иммунологические механизмы: первая линия защиты от внутриклеточных паразитов Инфицированные клетки

Факторы врожденного иммунитета. Первая линия защиты Лимфоидные клетки: Миелоидные клетки: n n n Контактный киллинг (NK и NKT клетки) Активность Т клеток Продукты В 1 клеток (естест. антитела) Интерфероны 1 типа Фагоцитоз и внутриклеточный киллинг (нейтрофилы, моноциты, макрофаги) Внутриклеточный киллинг Гепатоциты и др. : (эозинофилы и нейтрофилы) Система комплемента (внутрикл. цитолиз) Противоспалительные цитокины Белки острой фазы (опсонизация и др. )

Гуморальные факторы врожденного иммунитета Факторы системы комплемента Способствует фагоцитозу (опсонизация) Вызывает лизис клеток – мишеней Служат источником провоспалительных факторов
Гуморальные факторы врожденного иммунитета Белки острой фазы Способствуют осуществлению фагоцитоза Активируют систему комплемента Усиливают Образование провоспалительных цитокинов
Гуморальные факторы врожденного иммунитета Цитокины Обуславливают местные и общие проявления воспалительной реакции Активируют фагоцитоз и другие проявления врожденного иммунитета

Адекватный тип иммунной защиты n n Гуморально/клеточная (Th 2, TH 17 клетки, нейтрофилы, В клетки, антитела) Клеточно/гуморальная внеклеточный цитолиз (Th 2 клетки, эозинофилы и их факторы) Клеточно воспалительная (Th 1 клетки, макрофаги, цитокины) Клеточная цитотоксическая контактный цитолиз (цитотоксические лимфоциты Т, NК)

Преимущества Т клеток памяти перед наивными клетками 1. 2. 3. 4. 5. Исходная численность клетокв клонах клеток памяти на 2 3 порядка выше, чем в клонах наивных клеток. Клетки памяти находятся в клеточном цикле, а наивные лимфоциты в фазе покоя, для выхода из которой требуется время и особые воздействия. При ответе на антиген клетки памяти не должны проходить некоторые стадии развития, обязательные при ответе наивных лимфоцитов. Клетки памяти быстрее и эффективнее реагитруют на антиген (активируются и дифференцируются в эффекторные клетки). В результате Т клетки памяти могут быть активированы любыми антигенпрезентирующими клетками (АПК), тогда как наивные Т клетки только дендритными клетками. Антиген может быть презентирован клетками памяти «на месте» , тогда как наивным лимфоцитам только в лимфатическом узле.

Цитокины представляют собой регуляторные пептиды, продуцируемые клетками организма. К системе цитокинов в настоящее время относят около 200 индивидуальных полипептидных веществ с молекулярной массой от 5 до 50 к. Да.

Классы цитокинов 1) Провоспалительные; 2) Противоспалительные; 3) Факторы, вызывающие рост и дифференцировку лимфоцитов; 4) Гемопоэтические колониестимулирующие факторы; 5) Факторы, вызывающие рост мезенхимальных клеток.

Функции цитокинов n n n Синтезируются в процессе реализации механизмов неспецифического или специфического иммунитета; Служат медиаторами иммунной и воспалительной реакций Действуют опосредованно, изменяя функциональное состояние клеток—мишеней с помощью вторичных мессенджеров Оказывают аутокринное (на клетку—продуцент), паракринное (на соседние с клеткой—продуцентом клетки) и дистантное (на клетки удаленных на значительное расстояние органов и тканей) действие; Образуют регуляторную сеть, в которой отдельные элементы обладают синергическим или антагонистическим действием; Обладают полифункциональной активностью и перекрывающимися функциями

Первичные иммунодефицитные состояния (ИДС) n n n Это генетически детерминированные заболевания, обусловленные нарушением сложного каскада реакций, необходимых для элиминации чужеродных агентов из организма и развития адекватных воспалительных реакций. Их типичными проявлениями являются тяжело протекающие бактериальные, вирусные и грибковые инфекции, аутоиммунные заболевания и повышенная склонность к развитию злокачественных новообразований. В настоящее время описано более 80 форм первичных ИДС. Частота встречаемости первичных иммунодефицитов составляет от 1: 1000 до 1: 5 ООО, в зависимости от формы.

Неинфекционные проявления первичных иммунодефицитов n Гипоплазия лимфоидной ткани n n n Гиперплазия лимфоидной ткани n n Лейкопения, лимфопения n n Нейтропения n гепатит, неспецифический язвенный колит, болезнь Крона и др. Агаммаглобулинемия, тяжелая комбинированная иммунная недостаточность (общий вариабельный иммунодефицит, синдром Ниймеген)* Аутоиммунный лимфопролиферативный синдром, гипер-1§М-синдром, общая вариабельная иммунная недостаточность (синдром Ниймеген)* Тяжелый комбинированный иммунодефицит Агаммаглобулинемия, общий вариабельный иммунодефицит, rnneplg. M-синдром, синдром Ниймеген, аутоиммунный лимфопролиферативный синдром (синдром Вискотта-Олдрича)*

Неинфекционные проявления первичных иммунодефицитов n Тромбоцитопения n Гемолитическая анемия n Артрит n Нефротический синдром, миозит, склередема, аутоиммунныйгепатит, НЯК, болезнь Крона n n Синдром Вискотта Олдрича, общий вариабельный иммунодефицит, гипер 1§М синдром, синдром Ниймеген, аутоиммунный лимфопролиферативный синдром Общий вариабельный иммунодефицит, гипер 1§М синдром, синдром Ниймеген, аутоиммунный лимфопролиферативный синдром Агаммаглобулинемия, общий вариабельный иммунодефицит, гипер 1§М синдром, синдром Ниймеген, аутоиммунный лимфопролиферативный синдром, синдром Вискотта Олдрича Агаммаглобулинемия, общий вариабельный иммунодефицит, гипер ^М синдром, синдром Ниймеген, аутоиммунный лимфопролиферативный синдром, синдром Вискотта Олдрича

Классификация ИДС n n преимущественно гуморальные или В клеточные (50%); комбинированные: при всех Т клеточных иммунодефицитах в результате нарушений регуляции страдает функция В клеток (30%); дефекты фагоцитоза (18%); дефекты комплемента (2%).

ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ ОСНОВНЫХ ФОРМ ПЕРВИЧНЫХ ИММУНОДЕФИЦИТОВ n n n Они разделены на 3 категории: достоверные, вероятные и предположительные. Различное сочетание диагностических признаков отражает степень точности диагноза. Для установления диагноза пациент должен иметь определенное сочетание признаков. Достоверным считается диагноз, основанный на клинических, иммунологических и молекулярно генетических данных. Точность диагностики составляет более 98%. Выявление мутаций причинного гена является наиболее точным методом. Заболевание вероятно, если имеются характерные клинические и иммунологические показатели. Пациентами с вероятным диагнозом являются те, у которых наличествуют характерные клинические и лабораторные признаки, однако диагноз не подтвержден выявлением мутации гена или экспрессии m. RNA или протеина, ответственных за развитие болезни. Точность диагностики у этих больных составляет 85%. Если больной имеет только часть клинических или иммунологических показателей, характерных для данной нозологии, диагноз считается предположительным.

ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ n n n Большое значение в диагностике иммунодефицитов имеет семейный анамнез. Приблизительно в 50% случаев пациенты с Х сцепленными заболеваниями, подтвержденными идентификацией характерных мутаций, не имеют семейного анамнеза, потому что эти пациенты могут быть первым ребенком в семье, имеющим болезнь, или иметь новую мутацию. Наличие родственных браков повышает риск появления аутосомно рецессивных болезней. Многие пациенты с редкими иммунодефицитами являются «компаунд гетерозиготами» , то есть имеют мутации в разных аллелях гена, переданных со стороны матери и отца. Для многих болезней необходимо проведение дифференциальной диагностики. Для некоторых состояний существуют критерии исключения.

Селективный дефицит Ig. A (SDIg. A) n Диагноз достоверен: пациент женского или мужского пола n Диагноз предположителен: пациент женского или муж ского старше 4 лет со снижением концентрации сывороточного Ig. A менее 7 мг/дл (0, 07 г/л), нормальным уровнем Ig. G, Ig. M, нормальным поствакцинальным синтезом Ig. G антител. При этом другие причины гипогаммаглобулинемии должны быть исключены. пола старше 4 лет, имеющий снижение концентрации сывороточного Ig. A на 2 стандартных отклонения (SD) ни же возрастной нормы при нормальных концентрациях Ig. G и Ig. M, у которого были исключены другие причины гипо гаммаглобулинемии. Поствакцинальный синтез Ig. G анти тел нормален.

Проявления болезни. n n n Большая часть субъектов, имеющих дефицит Ig. A, не имеют клинических проявлений заболевания. У части пациентов с дефицитом Ig. A повышена частота заболеваемости инфекциями верхних дыхательных путей, аллергическими и аутоиммунными болезнями. У некоторых развиваются повторные или персистирующие инфекционные процессы, возможна трансформация дефицита Ig. A в общую вариабельную иммунную недостаточность (CVID).

Лечение n Специфического метода лечения селективной недостаточности Ig. A не существует. Необходимо проводить лечение основных клинических проявлений и связанных с ними нарушений. Больным не показаны препараты иммуноглобулинов, содержащие даже незначительные количества Ig. A.

Дифференциальная диагностика гипогаммаглобулинемии Лекарственноиндуцированная: n n n n n противомалярийные препараты; каптоприл; карбамазепин; глюкокортикоиды; фенклофенак; соли золота; пеницилламин; фенитоин; сульфасалазин. Генетические синдромы: n n n n атаксия телеангиэктазия; аутосомные формы тяжелой комбинированной иммунной недостаточности (SCID); гипер ^М синдром; дефицит транскобаламина II с гипогаммаглобулинемией; Х сцепленная агаммаглобулинемия; Х сцепленные лимфопролиферативные болезни (EBV ассоциированные); Х сцепленная SCID; метаболические нарушения; хромосомные аномалии; синдром 18 q xpo. Moco. Mbi; моносомия 22; трисомия 8; трисомия 21.

Дифференциальная диагностика гипогаммаглобулинемии Системные болезни: n Инфекционные болезни: n n ВИЧ инфекция; врожденная краснуха; врожденная CMV инфекция; врожденная инфекция, вызванная Toxoplasma gondii; n инфекция EBV. Онкология: n n хронический лимфобластный лейкоз; иммунодефицит с тимомой; неходжкинская лимфома; В клеточная пролиферация. n иммунодефицит, связанный с гиперкатаболизмом иммуноглобулинов; иммунодефицит, связанный с выраженной потерей иммуноглобулинов (нефроз, тяжелые ожоги, лимфан гиэктазия, тяжелая диарея).

Х-сцепленная агаммаглобулинемия Диагноз достоверен: Диагноз вероятен: n n n пациент мужского пола со сниже нием количества CD 19+ В клеток менее 2%, имеющий хотя бы один из следующих признаков: мутация в Btk; отсутствие Btk m. RNA при анализе нейтрофилов или моноцитов методом northern blot; отсутствие Btk протеина в моноцитах или тромбоцитах; родственники мужского пола по материнской линии (дяди, двоюродные братья, племянники) с содержанием CD 19+ В клеток менее 2%. n n пациент мужского пола со снижением количества CD 19+ В клеток менее 2%, имеющий все нижеперечисленные признаки: начало рецидивирующих бактериальных инфекций в первые 5 лет жизни; снижение сывороточных уровней Ig. G, Ig. A, Ig. M более чем на 2 SD от возрастной нормы; отсутствие изогемагглютининов и/или сниженный ответ на введение вакцин. Другие причины гипогаммаглобулинемии должны быть исключены.

Клинические проявления n n n Длябольшинства пациентов с Х сцепленной агаммаглобулинемией характерны повторные бактериальные инфекции в течение первых двух лет жизни (чаще отиты, синуситы и пневмонии). Наиболее частой патогенной флорой является S. pneumoniae и Н. influenzae. Уровень сывороточного Ig. G обычно ниже 200 мг/дл (2 г/л), a Ig. M и Ig. A — ниже 20 мг/дл (0, 2 г/л). Приблизительно в 20% случаев развиваются очень тяжелые инфекции, часто с нейтропенией. У 10 15% пациентов концентрации сыворо точных иммуноглобулинов могут быть несколько выше, чем должны были бы быть при агаммаглобулинемии, и иммунодефицит диагностируется после 5 лет.

Х-сцепленный синдром гипериммуноглобулинемии М (HIGM 1) Диагноз достоверен: Диагноз вероятен: n n пациент мужского пола, имеющий снижение сывороточного Ig. G не более 2 SD от средне возрастной нормы, а также мутации в гене CD 40 L или родственников мужского пола по материнской линии (дяди, двоюродные братья, племянники) с документированным HIGM 1. n n n пациент мужского пола, имеющий кроме снижения Ig. G не более 2 SD от возрастной нормы все нижеперечисленные проявления: нормальное количество и митогениндуцированная пролиферация Т клеток; нормальное или повышенное количество В клеток при отсутствии антигенспецифичных Ig. G-антител; одно из следующих осложнений: персистирующие тяжелые бактериальные инфекции в первые 5 лет жизни; пневмоцистную инфекцию на первом голу жизни; нейтропению; диарею, вызванную Cryptosporidium, склерозирующий холангит; парвовирусиндуцированную апластическую анемию; отсутствие экспрессии CD 40 L на поверхности активированных CD 4+ Т клеток, иденифицированное с помощью растворимого CD 40 или моноклональных анти- CD 40 L антител.

Клинические проявления n n n У пациентов с HIGM 1 наблюдаются повторные бактериальные и оппортунистические инфекции, дебютирующие на первом году жизни. Часто развивается пневмония, вызванная Pneumocystis carinii. У части пациентов развивается хроническая профузная диарея, требующая назначения парентерального питания. Примерно у 50% больных присутсвует хроническая или интермиттирующая нейтропения, обычно ассоциированная с язвенным стоматитом. Криптоспоридиальная инфекция может привести к тяжелому поражению желчных протоков и раку печени. Концентрация сывороточного Ig. G обычно ниже 200 мг/дл; уровень Ig. M может быть сниженным, нормальным или повышенным. Атипичные случаи болезни могут быть представлены повторными инфекциями, анемией или гепатитом в течение второй или третьей декад жизни.

Х-сцепленный синдром гипериммуноглобулинемии М (HIGM 1) n Диагноз достоверен: пациент мужского пола, имеющий снижение сывороточного Ig. G не более 2 SD от средне возрастной нормы, а также мутации в гене CD 40 L или родственников мужского пола по материнской линии (дяди, двоюродные братья, племянники) с документированным HIGM 1. n n n Диагноз вероятен: пациент мужского пола, имеющий кроме снижения Ig. G не более 2 SD от возрастной нормы все нижеперечисленные проявления: нормальное количество и митогениндуцированная пролиферация Т клеток; нормальное или повышенное количество В клеток при отсутствии антигенспецифичных Ig. G антител; одно из следующих осложнений: персистирующие тя желые бактериальные инфекции в первые 5 лет жизни; пневмоцистную инфекцию на первом голу жизни; нейтропению; диарею, вызванную Cryptosporidium, склерозирующий холангит; парвовирусиндуцированную апластическую анемию; отсутствие экспрессии CD 40 L на поверхности активированных CD 4+ Т клеток, иденифицированное с помощью растворимого CD 40 или моноклональных анти CD 40 L антител.

Клинические проявления n n n У пациентов с HIGM 1 наблюдаются повторные бактериальные и оппортунистические инфекции, дебютирующие на первом году жизни. Часто развивается пневмония, вызванная Pneumocystis carinii. У части пациентов развивается хроническая профузная диарея, требующая назначения парентерального питания. Примерно у 50% больных присутсвует хроническая или интермиттирующая нейтропения, обычно ассоциированная с язвенным стоматитом. Криптоспоридиальная инфекция может привести к тяжелому поражению желчных протоков и раку печени. Концентрация сывороточного Ig. G обычно ниже 200 мг/дл; уровень Ig. M может быть сниженным, нормальным или повышенным. Атипичные случаи болезни могут быть представлены повторными инфекциями, анемией или гепатитом в течение второй или третьей декад жизни.

Критерии исключения HIGM 1: n n n Дефекты Т клеточной активации (в т. ч. дефекты экс прессии D 69 или CD 25 после C активации Т клеток in vitro). ВИЧ инфекция. Врожденная краснуха. Дефицит молекул HLA II. Дефицит CD 4+ Т клеток. Воздействие лекарственных веществ или инфекцион ных агентов, ведущее к поражению иммунной системы.

Лечение ИММУНОДЕФИЦИТов СО ЗНАЧИТЕЛЬНЫМ НАРУШЕНИЕМ ПРОДУКЦИИ АНТИТЕЛ (Агаммаглобулинемия с дефицитом В клеток и общая вариабельная иммунная недостаточность, sunep-Ig. Mсиндромы) n n n Заместительная терапия препаратами иммуноглобулинов для внутривенного введения в сочетании с аптибактериальной терапией. Заместительная терапия начинается с момента установления диагноза и проводится 1 раз в 34 недели пожизненно. В начале лечения или при обострении инфекций проводится терапия насыщения — 1 -1, 5 г/кг массы тела больного в месяц, поддерживающая доза составляет — 0, 3 -0, 5 г/кг 1 раз в 3 -4 нед. Доза иммуноглобулина 0, 3 -0, 5 г/кг вводится одномоментно со скоростью 20 капель в минуту. Цель заместительной терапии — достижение претрансфузионного уровня Ig. G в сыворотке крови больного более 500 мг/дл. Этот уровень в обычных условиях предохраняет пациента от тяжелых бактериальных инфекций. Использование криоконсервированной плазмы опасно из-за высокого риска инфицирования гепатитами и другими вирусными инфекциями! Для профилактики бактериальных инфекций назначается постоянная терапия триметопримом-сульфометоксазолом в возрастной дозе. При наличии хронических инфекций проводится длительная (в течение многих месяцев) терапия ципрофлоксацином или макролидами, что позволяет значительно уменьшить частоту и тяжесть рецидивов. При обострениях бактериальной инфекции проводится парентеральная антибактериальная терапия антибиотиками широкого спектра действия. Как правило, это 2 или 3 двухнедельных курса комбинированной терапии 2 антибактериальными препаратами в высоких дозах. Хороший эффект дает комбинация цефалоспоринов с аминогликози-дами, в случае тяжелых и/или госпитальных инфекций показано назначение ванкомицина, имипенемов, сульперазона; для лечения лямблиоза — метронидазола.

n n n Противовирусные и противогрибковые препараты применяют при общей вариабельной иммунной недостаточности и гипер-Ig. Мсиндромах, синдроме Ниймеген постоянно или интермиттирующими курсами, в зависимости от тяжести течения соответствующих инфекций. Для терапии гемоцитопений показано применение ростовых факторов (нейпоген, граноцит). При аутоиммунных цитопениях применяют глюкокортикоиды, иммунодепрессанты (азатиоприн, селлсепт, циклоспорин А), моноклональные антитела (ритуксимаб), при их неэффективности возможна спленэктомия. В случае развития энтеровирусного энцефалита показано проведение 3 -4 курсов высокодозовой терапии внутривенным иммуноглобулином: 2 г/кг массы тела больного в течение 2 -3 дней. Курсы высокодозовой терапии проводят 1 раз в 5 -7 дней в течение 1 -2 мес.

n n n Важным является вопрос о проведении специфической иммунопрофилактики у больных с тотальными дефектами продукции антител. Вакцинация недостаточно эффективна в связи с ограниченной способностью больных вырабатывать антитела, однако в основном безопасна. Противопоказана живая полиовакцина в связи с высокой чувствительностью больных к энтеровирусам. При контакте с больными острозаразными инфекционными болезнями показано дополнительное внеочередное введение препаратов иммуноглобулинов. В связи с неблагоприятным прогнозом болезни при Х сцепленом гипер Ig М синдроме показана трансплантация костного мозга (ТКМ) или гемопоэтических стволовых клеток (ТГСК) от HLA идентичного донора.

Атаксия-телеангиэктазия (синдром Луи. Барр) n n Диагноз достоверен у пациентов Диагноз вероятен у пациентов женского пли мужского пола с повышенным уровнем хромосомных аббераций и ломкости хромосом при n цитогенетическом исследовании, прогрессирующей мозжечковой n атаксией, имеющих серьезные мутации в обеих аллелях ATM, задержке роста, Отсутствии сывороточных Ig. A, n Ig. M, появлении в возрасте от 2 х до 6 ти лет телеангиэктазий на n конъюнктиве, открытых участках тела, слизистых оболочках. или мужского пола с прогрессирующей мозжечковой атаксией, имеющих 3 из 4 нижеперечисленных признаков: конъюнктивальные или лицевые телеангиэктазии; снижение уровня сывороточного Ig. A более чем на 2 SD от возрастной нормы; повышение альфа фетопротеина более чем на 2 SD от возрастной нормы; повышение уровня хромосомных аббераций и ломкости хромосом при цитогенетическом исследовании.

Клинические проявления Атаксия телеангиэктазия — n прогрессирующее неврологическое заболевание. У большинства пациентов изменения походки начинаются к концу первого года жизни и к подростковому возрасту вызывают стойкую инвалидизацию (невозможность самостоятельно ходить). Глазные или лицевые телеангиэктазии обычно формируются к 3 6 годам жизни. У многих больных развиваются повторные инфекции респираторного тракта. Лейкозы и лимфомы наблюдаются у 10 15% пациентов. n У части больных атаксия телеангиэктазия не диагностируется до второго десятилетия жизни.

n n n Методов излечения атаксии-телеангиэктазии до настоящего времени не разработано. Больные нуждаются в паллиативной терапии неврологических расстройств. В случае выявления серьезных иммунологических изменений и/или хронических или рецидивирующих бактериальных инфекций показана антибактериальная терапия (длительность определяется тяжестью иммунодефицита и инфекции), заместительная терапия внутривенным иммуноглобулином, по показаниям — противогрибковая и противовирусная терапия.

Х-сцепленный тяжелый комбинированный иммунодефицит (XSCID) Диагноз достоверен у пациентов мужского пола, имеющих: n а) приживление полученных трансплацентарно материнских Т клеток, б) содержание CD 3+ Т клеток менее 10%, CD 16/56+ NK клеток менее 2% и более 75% CD 19+ В клеток; n при наличии 1 из нижеперечисленных признаков: идентифицированные мутации общей ус цитокинов; отсутствие ус m. RNA при анализе лимфоцитов методом northern blot; отсутствие экспрессии с протеина на поверхности лимфоцитов; наличие родственников мужского пола по материнской линии (дяди, двоюродные братья, племянники), имеющих признаки SCID. n Диагноз вероятен у пациентов мужского пола, имеющих содержание CD 3+ Т клеток менее 10%, CD 16/56+ NK клеток менее 2% и более 75% CD 19+ В клеток, а также задержку физического развития на первом году жизни, снижение концентраций сывороточных иммуноглобулинов А и G (более 2 SD от возрастной нормы), персистирующую диарею, инфекции респираторного тракта, молочницу

Клинические проявления n n У мальчиков с X SCID к 4 мес обычно развиваются повторные инфекции респираторного тракта, диарея, задержка физического развития, кандидоз. Распознавание иммунодефицита у таких детей, как правило, происходит между 6 7 м месяцами жизни. Многие больные имеют нормальную концентрацию сывороточного Ig. M, а уровни Ig. G и Ig. A обычно очень низкие. Некоторые, но не все пациенты с приживлением трансплацентарных материнских Т лимфоцитов имеют признаки реакции «трансплантат против хозяина» , такие как сыпь и повышение печеночных ферментов. Крайне редко у больных могут выявляться некоторые количества собственных Т и/или NK клеток.

Тяжелый комбинированный иммунодефицит (SCID) n n n Диагноз достоверен у пациентов мужского или женского пола младше 2 лет, имеющих: а) приживление трансплацентарно приобретенных материнских Т лимфоцитов; б) менее 20% CD 3+ Т клеток и снижение абсолютного ко личества лимфоцитов ниже 3000/мм 3, а также при наличии хотя бы 1 из нижеперечисленных признаков: мутация в гене общей гамма цепи цитокинов (7 с); мутация JAK 3; мутация RAG 1 и RAG 2; мутация IL 7 Ra; активность ADA ниже 2% от контрольной или мутация в обеих аллелях ADA. n Диагноз вероятен у пациентов мужского или женского пола младше 2 лет, имеющих менее 20% CD 3+ Т клеток и снижение абсолютного количества лимфоцитов ниже 3000/мм 3, снижение пролиферативного ответа на митогены ниже 10% от контроля или с наличием в циркуляции материнских лимфоцитов.

Клинические проявления n n n У пациентов с SCID, как правило, развивается задержка физического развития, диарея, инфекции респираторного тракта, молочница на 2 7 м месяцах жизни. Наиболее частые заболевания при SCID: пневмоцистная пневмония, тяжелые бактериальные инфекции и диссеминированная БЦЖ инфекция. У малого числа пациентов, не имеющих грубого отставания в физическом развитии, первичный иммунодефицит не распознается в течение первого года жизни. Дети с SCID умирают в течение первых 2 лет, если не попадают в условия строгого стерильного режима, в котором проводится адекватная терапия, и не подвергаются трансплантации гемопоэтических стволовых клеток или терапии, замещающей дефектный ген или его продукт.

n n Единственным способом лечения SCID (включая дефицит МНС II) является трансплантация костного мозга. Заместительная терапия внутривенными иммуноглобулинами, интенсивная антибактериальная, противогрибковая и противовирусная терапия проводятся детям с SCID, страдающим инфекциями в период подготовки к пересадке костного мозга и поиска донора. При установлении диагноза SCID младенцев помещают в специализированные гнотобиологические боксы.

Синдром Di. George n n n Диагноз достоверен у пациентов женского или мужского пола (тип наследования — аутосомно доминантный) с редуцированным числом CD 3+ (менее 500 клеток в мм 3) и 2 из 3 нижеперечисленных признаков: дефекты артериального ствола (общий артериальный ствол, тетрада Фалло, стеноз дуги аорты (аплазия), аномальное отхождение подключичной артерии); гипокальциемия продолжительностью более 3 нед, требующая лечения (вследствие гипопаратиреоза); делеция 22 ql 1. 2 хромосомы. Кроме того, у этих пациентов имеет место гипо или аплазия тимуса. n n n Диагноз вероятен. Пациент женского или мужского по ла с редуцированным числом CD 3+ (менее 500 клеток в мм 3) и делецией 22 ql 1. 2 хромосомы. Диагноз предположителен у пациентов женского или мужского пола с редуцированным числом CD 3+ (менее 500 клеток в мм 3) и имеющих хотя бы 1 из нижеперечисленных признаков: порок сердца; гипокальциемия продолжительностью более 3 нед, требующая лечения; лицевой дизморфизм или дефекты твердого нёба.

Клинические проявления n n n У большинства пациентов иммунодефицит распознается в первые месяцы жизни, когда их начинают обследовать по поводу врожденных мальформаций сердца, которые очень часто ассоциированы с синдромом и/или делецией 22 ql 1. 2 хромосомы. У небольшого числа пациентов с синдромом Di. George болезнь дебютирует в виде персистирующих вирусных или грибковых инфекций или начинается с гипокальциемических судорог. Тяжесть Т клеточного дефекта варьирует в широких пределах. У многих больных иммунодефицит разрешается в течение первых лет жизни. Обычными проявлениями у детей с синдромом Di. George являются лицевой дизморфизм и отставание в интеллектуальном развитии. В старшем возрасте могут наблюдаться аутоиммунные болезни.

Лечение СИНДРОМа DIGEORGE n n Пациенты с DGS /VCFS нуждаются в назначении про тивомикробной и противовирусной терапии, особенно при повышенной склонности к инфекциям. Без терапии продолжительность жизни больных с полной формой DGS сравнима с продолжительностью жизни пациентов со SCID. В литературе есть единичные описания трансплантаций костного мозга, однако, учитывая механизм развития DGS, при котором созревание Т клеток нарушено из за отсутствия эпителия тимуса, проведение ТКМ для таких больных не рационально. Оправданным для пациентов с полной формой DGS является трансплантация эпителиальной ткани тимуса. После пересадки эпителиальной ткани тимуса отмечено восстановление количества и функциональной активности Т клеток.

Синдром Вискотта-Олдрича (WAS) n n n Диагноз достоверен у пациентов мужского пола с врож денной тромбоцитопенией (количество тромбоцитов мень ше 70 х109/л), уменьшенным диаметромбоцитов и имеющих хотя бы 1 из следующих признаков: мутации в WASP; отсутствие WASP m. RNA при анализе лимфоцитов мето дом orthern blot; n отсутствие Ш 45 Р протеина в лимфоцитах; наличие по материнской линии родственников мужско го пола (дяди, двоюродные братья, племянники), имею щих тромбоцитопению и малый диаметр тромбоцитов. Диагноз вероятен у пациентов мужского пола с врожденной тромбоцитопенией (количество тромбоцитов меньше 70 Х 109/Л)> уменьшенным диаметромбо цитов, имеющих хотя бы 1 из нижеперечисленных прояв лений: экзема; нарушенный антительный ответ на полисахаридные антигены; рецидивирующие бактериальные или вирусные ин фекции; аутоиммунные заболевания; лимфома, лейкоз или опухоль головного мозга.

Диагноз предположителен: пациент мужского пола с тромбоцитопенией (количество тромбоцитов меньше 70 тыс. в мм 3), с маленьким диаметромбоцитов; либо перенесший спленэктомию по поводу тромбоцитопении, имеющий также хотя бы 1 из нижеперечисленных клинических проявлений: n экзема; n нарушенный антительный ответ на полисахаридные антигены; n рецидивирующие бактериальные или вирусные инфекции; n аутоиммунные заболевания; n лимфома, лейкоз или опухоль головного мозга.

Клинические проявления n n n Врожденная тромбоцитопения с уменьшенным размером тромбоцитов является главным диагностическим признаком WAS. У многих пациентов болезнь дебютирует с диареи с кишечным кровотечением на первом месяце жизни. Экзема, развивающаяся у многих, но не у всех больных, может быть преобладающим клиническим проявлением. Характерны отиты, синуситы, тяжелые инфекции, вызванные Herpes simplex и EBV. У многих пациентов повышены концентрации сыворточных Ig. E и Ig. A и снижена концентрация Ig. M. Количество и функциональная активность Т лимфоцитов с возрастом снижаются. При WAS повышена частота развития аутоиммунных заболеваний (васкулит, гемолитическая анемия, нефротический синдром) и опухолей (лейкоз, лимфома, EBV ассоциированная опухоль головного мозга). Очень редко пациенты с WAS имеют умеренную тромбоцитопению (50, 000 100, 000 тромбоцитов в микролитре) без каких либо других проявлений.

Лечение n n n n n Единственным методом излечения больных с синдромом Вискотта-Олдрича (WAS) является ТКМ от HLA-идентичного донора. При отсутствии возможности ТКМ показано проведение спленэктомии, так как это приводит к значительному уменьшению геморрагического синдрома (очевидно, из-за исчезновения плацдарма, в котором происходит массовая гибель дефектных тромбоцитов). Перед спленэктомией необходима вакцинация пневмококковой вакциной. Необходима постоянная терапия противопневмококковыми антибиотиками (антибиотики пенициллинового ряда, например бициллин). Пациенты с WAS нуждаются в регулярной заместительной терапии внутривенным иммуноглобулином, постоянной профилактической антибактериальной (триметопримсульфаметоксазол), противовирусной (ацикловир в поддерживающей дозе) и противогрибковой (флуконазол или итраконазол) терапии. Для лечения острых инфекций проводится соответствующая интенсивная антимикробная терапия (комбинация 2 антибиотиков, 2 -3 двухнедельных курса, дополнительные введения иммуноглобулина). Для лечения аутоиммунных расстройств, в том числе доказанной иммунной тромбоцитопении (особенно возникшей после спленэктомии), используются глюкокортикоиды, азатиоприн, циклоспорин А. Необходима симптоматическая терапия экземы и других аллергических болезней. Больным противопоказаны внутримышечные инъекции из-за опасности развития гематом с последующим их инфицированием. Переливания тромбоцитов проводятся только для купирования тяжелых кровотечений при неэффективности других методов терапии. Вакцинация возможна только инактивированными вакцинами и анатоксинами.

Х-сцепленный лимфопролиферативный синдром (XLP) n Диагноз достоверен у пациентов мужского пола с лим фомой/болезнью Ходжкина, фатальной EBV инфекцией, иммунодефицитом, апластической анемией или лимфогистиоцитозом, имеющих мутацию в SH 2 D 1 A/SAP/DSHP. n Диагноз вероятен у пациентов мужского пола, умерших от лимфомы/болезни Ходжкина, иммунодефицита, апластической анемии или лимфогистиоцитоза в результате острой EBV инфекции, при наличии родственников мужского пола по материнской линии (дяди, двоюродные братья, племянники), имевших подобные болезни, развившиеся после острой EBV инфекции.

Клинические проявления n n n Мальчики с XLP обычно не имеют никаких клинических проявлений, пока не разовьется EBV инфекция, которая может привести к фульминантному гепатиту (60% всех больных), преимущественно в раннем детстве. В более старшем возрасте могут развиться болезнь Ходжкина или неходжкинская лимфома (30%) и/или иммунодефицит с низкой концентрацией сыворо точного g. G I и нарушениями функций NK клеток (30%). Менее часто встречаются EBV ассоциированный гемофа гоцитарный синдром и васкулит. Большинство пациентов умирает в детском возрасте; уровень выживаемости очень низкий у мальчиков с фульминантным гепатитом (< 5%), и более высокий — у мальчиков с изолированной дисгам маглобулинемией (50%).

Лечение Х-сцепленного лимфопролиферативного синдрома (XLP) n n Единых подходов к терапии больных с Х-сцепленным лимфопролиферативным синдромом не выработано. Различные профилактические режимы могут быть использованы в случае выявления дефекта на доклинических этапах течения XLP. Предположить болезнь можно у мальчиков с характерным семейным анамнезом и серо или PCR негативных в отношении EBV. В качестве профилактического средства рассматривается применение ацикловира. Было показано, что его раннее назначение ингибирует репликацию вируса в ротоглотке. Также с профилактической целью рекомендуется применять терапию высокодозного иммуноглобулина для внутривенного введения (ВВИГ). Однако, ни ацикловир, ни ВВИГ не предотвращают инфицирования EBV.

n n n При развившейся клинической картине одного из фенотипов XLP необходима специфическая терапия. При гипогаммаглобулинемиях рекомендуется применять ВВИГ ежемесячно в поддерживающей дозе, а также антибактериальную терапию. Для лечения фульминантного инфекционного мононуклеоза могут быть использованы сочетание высоких доз ацикловира (500 мг/м 2) и метилпреднизолона (до 5 6 мг/кг/сут), высокодозовый иммуноглобулин с высоким титром анти EBV антител или сочетание ВВИГ с интерфероном альфа. При развитии гемофагоцитарного лимфогистиоцитоза рекомендуется лечение по протоколу HLН 94: сочетание высоких доз дексаметазона с вепезидом в течение 15 мес с хорошим эффектом (контроль лихорадки, уменьшение лимфопролиферации и купирование явлений гемофагоцитоза). Для лечения злокачественных болезней применяются стандартные протоколы. Учитывая плохой прогноз течения болезни, радикальным методом лечения XLP является ТКМ от HLA совместимых доноров.

Хроническая гранулематозная болезнь (CGD) n n Диагноз достоверен у пациентов женского или мужско го пола, имеющих сниженную продукцию перекисных радикалов (менее 5% от контроля) при оценке с помощью НСТ теста и люминолзависимой хемилюминесценции и 1 из следующих признаков: мутации в gp 91, р22, р47 или р67 phox; отсутствие m. RNA одного из указанных генов при анализе методом northern blot; наличие родственников по материнской линии (дяди, двоюродные братья, племянники), имеющих сниженную продукцию перекисных радикалов. n n Диагноз вероятен у пациентов женского или мужского пола со сниженной продукцией перекисных радикалов (менее 5% от контроля) при оценке с помощью НСТ теста и люминолзависимой хемилюминесценции, имееющих 1 из следующих признаков: тяжелые абсцедирующие инфекции внутренних органов — печени, параректальной клетчатки и легких, лимфадениты, остеомиелиты, вызванные staphylococcus, serratia marcescens, Candida или aspergillus; формирование гранулем респираторного, желудочно кишечного или урогенитального трактов; задержка физического развития, гепатоспленомегалия или лимфаденопатия.

Клинические проявления n n n У пациентов с Х сцепленной формой CGD (60 70% пациентов) болезнь дебютирует раньше и имеет более тяжелые клинические проявления, чем при аутосомно рецессивных формах. Большинство больных с X CGD с первого года жизни имеют задержку физического развития, тяжелые бактериальные лимфадениты, абсцессы или остеомиелиты. Наиболее частыми инфекционными проявлениями при всех формах CGD являются пневмонии и лимфадениты, вызванные каталазопозитивными микроорганизмами (в основном стафилококками) или грибами. Формирование гранулем может вызвать симптомы обструкции желудочно кишечного тракта или мочевых путей. Крайне редко первые клинические проявления появляются в старшем возрасте.

Дефект адгезии лейкоцитов I типа (LAD I) n n n Диагноз достоверен у пациентов женского или мужско го пола со снижением экспрессии CD 18 в нейтрофилах (менее 5% от нормы) и имеющих хотя бы 1 из следующих признаков: мутация в гене Ь 2 интегрина; отсутствие m. RNA Ь 2 интегрина в лейкоцитах. n n Диагноз вероятен у пациентов женского или мужско го пола с дефектной экспрессией CD 18 на лейкоцитах (менее 5% от нормы) и имеющих все нижеперечисленные признаки: упорные, персистирующие бактериальные или грибковые инфекции; лейкоцитоз (более 25 х109/л); позднее отпадение пуповины и/или плохое заживле ние ран.

Клинические проявления n n n Выраженный лейкоцитоз и повторные бактериальные инфекции являются характерными для LAD. Особенно тяжело протекают инфекции, вызванные стафилококком, граммнегативными энтеробактериями и грибами. Частой находкой является персистирующий периодонтит. При тяжелых формах болезни отмечается полное отсутствие экспрессии CD 18 в нейтрофилах, такие больные не выживают без трансплантации костного мозга. При среднетяжелых формах экспрессируется небольшое количество CD 18, и пациенты могут до живать до взрослого возраста. Некоторые больные могут иметь нормальную экспрессию CD 18, но сниженную активность Ь 2 интегрина. Критерии исключения: n нормальная экспрессия CD 18 и CD 15 а на нейтро филах; n нормальное количество нейтрофилов; n нормальная адгезия нейтрофилов.

Аутоиммунный лимфопролиферативный синдром Обязательные критерии: n n n хроническая незлокачественная лимфопролиферация; дефекты апоптоза лимфоцитов in vitro; ss 1% TCR a/p+ CD 4 CD 8 T клеток (a/p+ двойные негативные клетки — double negative — DN) в периферической крови или в лимфоидной ткани. Сопроводительные критерии: n n аутоиммунные проявления /аутоантитела; мутации в генах TNFRSF 6 или каспазы 10.

Лечение n n Дети, находящиеся в благоприятном состоянии, то есть не имеющие гематологичесих изменений, не страдающие гиперспленизмом и нарушениями дыхания вследствие лимфопролиферации, не требуют лечения. При наличии аутоиммунных осложнений, в первую очередь — гемоцитопе пий, показано назначение преднизолона в дозе 2 мг/кг массы тела до получения гематологической ремиссии с последующим постепенным снижением дозы до минимальной поддерживающей. При недостаточном эффекте глюкокортикоидов назначаются иммунодепрессанты (азатиоприн, циклофосфан, хлорамбуцил), проводится спленэктомиия. Назначение глюкокортикоидов, а в ряде случаев спленэктомии, показано также и при выраженной лимфопролиферации, вызывающей дыхательные расстройства. Всем больным с аутоиммунным лимфоиролиферативным синдромом при наличии хронической нейтропении показана постоянная антибактериальная терапия, так как без этого развиваются тяжелые, угрожающие жизни инфекционные осложнения, эффективно применение ростовых факторов (нейпоген, граноцит).

Синдром гипериммуноглобулинемии Е n n Гипер Ig. E syndrome (HIES), называемый так же синдромом Иова ( «Job syndrome» ) впервые описан в 1966, 1972 гг. как иммунодефицит, характеризующийся повторными абсцессами кожи и подкожной клетчатки стафилококковой этиологии, пневмониями с формированием пневмоцеле, аномалиями строения лицевого скелета, атоническим дерматитом и существенным повышением уровня сывороточного Ig. E. Молекулярно генетическая природа HIES до сих пор не установлена.

Диагностика При HIES выявляются разнообразные иммунологические нарушения: n эозинофилия в периферичекой крови и содержимом абсцессов; n повышение концентрации сывороточного Ig. E. С возрастом концентрация сывороточного Ig. E и количество эозинофилов периферической крови могут уменьшиться до нормальных уровней; n нарушения хемотаксиса нейтрофилов; n нарушение продукции антител; n дисбаланс соотношения Thl/Th 2 иммунного ответа в сторону Th 2; n нормальное количество CD 3+, CD 4+, CD 8+ Т клеток и В клеток; n снижение реакции гиперчувствительности замедленного типа на кандидин, дифтерийный и столбнячный анатоксины; n снижение пролиферативной активности Т клеток на некоторые ангигены (кандида, столбнячный анатоксин), а на митогены — в норме; n повышение продукции гранулоцитарно колониестмулирующего фактора и продукция перекисных радикалов нейтрофилами, что способствует нарушению хемотаксиса и повреждению тканей;

Клинические проявления HIES n Неинфекционные проявления n n n n Экзема среднетяжелого/тяжелого течения присутствует, как правило, с раннего возраста. Затем сохраняется фолликулит, грубая кожа с расширенными порами (особенно на лице). Аномалии развития скелета. Подавляющее большинство пациентов с HIES имеют: характерные специфические черты лица (гипертелоризм, широкая переносица, широкий курносый нос, асимметрия лицевого скелета, выступающий лоб, глубоко посаженые глаза, прогнатия, высокое нёбо); сколиоз; гипермобильность суставов; склонность к переломам костей после незначительных травм (из за повышения активности остеокластов и макрофагов); нарушения смены зубов (позднее прорезывание молоч ных зубов и значительная задержка или отсутствие самостоятельной смены зубов).

Инфекционные проявления n n n Характерными инфекционными проявления HIES являются абсцессы кожи, подкожной клетчатки и лимфоузлов, кандидоз, пневмонии. После перенесенных пневмоний формируются пневмоцеле, которые могут ошибочно трактоваться как поликистоз легких. Наиболеее частым возбудителем пневмоний является Staphylococcus aureus или Haemophilus influenzae. Пневмоцеле могут инфицироваться. Pseudomonas aeruginosa и Aspergillus fumigatus. Более редкими инфекциями при HIES являются абсцессы печени и посттравматические стафилококковые остеомиелиты, не кротизирующий фасциит. Гнойные инфекции у пациентов HIES характеризуются «холодным» течением: отсутствуют местная гиперемия, гипертермия и болевой синдром. Пневмонии могут протекать без повышения температуры тела. Хронический кандидоз слизистых оболочек и ногтей развивается приблизительно в 83% случаев.

Задачи иммунокоррекции: 1. Обеспечить адекватный иммунный ответ на инфекцию. 2. Активировать системы мукоцилиарной защиты верхних дыхательных путей. 3. Уменьшить глубину повреждения пораженной ткани. 4. Уменьшить интоксикацию. 5. Сократить сроки заболевания. 6. Предотвратить формирование резистентности патогена. 7. Предупредить хронизацию процесса.

ЛЕЧЕНИЕ БОЛЬНЫХ С ДЕФЕКТАМИ ФАГОЦИТОЗА n n Тактика лечения больных CGD, LAD и гипер 1 й. Е синдромом однотипна и зависит от фазы болезни. В период клинически выраженных инфекционных осложнений основным средством терапии является агрессивная противомикробная терапия. Предпочтение отдается бактерицидным препаратам, проникающим внутриклеточно. Антибиотики применяются в высоких дозах, длительно, парентерально. Больные должны постоянно получать триметоприм сульфометосксазол, в более тяжелых случаях — сочетание триметоприма сульфометоксазола с фторхинолонами. Учитывая предрасположенность больных к грибковым инфекциям, одновременно с антибактериальными средствами профилактически назначается противогрибковая терапия. Больным с CGD обязательно назначается итраконазол, применение которого существенно снижает частоту развития аспергиллеза, больным с LAD и гипер Ig. E синдромом назначают преимущественно флуконазол.

НЕДОСТАТОЧНОСТЬ СИСТЕМЫ КОМПЛЕМЕНТА n n n Система комлемента состоит из 9 компонентов (Q Cg) и 5 регуляторных белков (Ct ингибитор, С 4 связывающий протеин, пропердин и факторы Н и I). Система комплемента играет существенную роль в развитии воспалительного ответа и защите организма от инфекционных агентов. К настоящему времени описаны врожденные дефекты практически всех компонентов комплемента. В зависимости от дефицита конкретных компонентов системы комплемента клинически дефекты биосинтеза компонентов комплемента проявляются в виде тяжелых инфекционных полезней, аутоиммунных синдромов, наследственного ангионевротического отека.

НАСЛЕДСТВЕННЫЙ АНГИОНЕВРОТИЧЕСКИЙ ОТЕК n n n Наследственный ангионевротический отек (НАО) — дефицит Сг эстеразы — характеризуется рецидивирующими отеками подкожно жировой клетчатки и подслизистого слоя любой локализации: кожи, лица, шеи, туловища, конечностей. Начало болезни в детском возрасте, обычно от 2 лет до 8 10 лет, реже первые симптомы возникают в среднем и даже пожилом возрасте. Приступы отека возникают с раз личной периодичностью и могут провоцироваться травмой, психическим напряжением, чрезмерным переутомлением, менструацией, но могут появляться и спонтанно. Отеки холодные, плотные. Лечение. Наиболее широко для базисной терапии применяются препараты даназола. В экстренных ситуациях (отек гортани, отек кишечника и т. н. ) показано введение свежезамороженной плазмы 250 300 мл. В последние годы создан эффективный препарат Сг ингибитора.

ХРОНИЧЕСКИЙ КОЖНО-СЛИЗИСТЫЙ КАНДИДОЗ n n n Хронический кожно слизитый кандидоз — заболевание неизвестной этиологии. Лабораторных иммунологических критериев, кроме снижения Т клеточного ответа на анти ген. Candida albicans, не выявлено. Характерными клиническими проявлениями являются упорный кандидоз слизистых полости рта; реже — кожи, онихомикоз. Кандидозные поражения никогда не бывают глубокими и не приводят в серьезным поражениям органов. Прогноз этих больных определяют тяжелые бактериальные инфекции и аутоиммун ные расстройства в виде тяжелых полиэндокринопатий, поражений печени, гемоцитопений. Лечение: антибиотикотерапия, длительная, а иногда — пожизненная; кандидоз хорошо контролируется приемом кетоконазола или флуконазола. По поводу эндокринопатий проводится соответствующая заместительная терапия, при развитии аутоиммунных гемоцитопений и поражений печени применяют иммунодепрессанты.

Вторичные ИДС n n Вторичные ИДС характеризуются нарушениями функционирования иммунной системы, не связанными с генетическими дефектами и развивающимися в постнатальном периоде или у взрослых. Снижение иммунного ответа вызывает нарушение важнейшей функции иммунной системы — защиты организма от внешней и внутренней агрессии (прежде всего от инфекционных агентов или измененных клеток организма, включая злокачественные клетки)

n n Более логично обозначать подобные изменения термином «вторичная иммунная недостаточность» , а не «иммунодефицит» , поскольку в этих случаях отмечается лишь несостоятельность иммунного ответа, а не дефицит в иммунной системе. В последние десятилетия наблюдается постоянный рост ВИН, способной осложнять течение любой патологии человека, ухудшать прогноз и резко снижать качество жизни.

Клинические критерии: Частые обострения вялотекущих хронических воспалительных заболеваний различной этиологии (бактерии, грибы, вирусы) и локализации (кожа, легкие, ЖКТ, мочеполовая система и др. ) n n Частые ОРВИ (более пяти раз в год) n Частые обострения герпетической инфекции n Длительный субфебрилитет n Лимфоаденопатия и др. n Отсутствие достаточного клинического эффекта после назначения стандартной терапии по поводу имеющегося у пациента заболевания

Лабораторные критерии: n n n n Гемограмма: снижение содержания форменных элементов периферической крови снижение содержания Ig. A, Ig. M, Ig. G в сыворотке крови снижение содержания общей и отдельных субпопуляций лимфоцитов снижение функциональной активности фагоцитов, комплемента нарушения продукции интерферонов дисбаланс синтеза цитокинов Th 1' и Th 2'клетками изменения состояния спонтанного и индуцированного апоптоза снижение аффинности АТ к ОАД бактерий и др. Транзиторные изменения параметров иммунной системы возможны у практически здоровых лиц, и их выявление не всегда свидетельствует о наличии ВИН

Прежде, чем выставить диагноз ВИН, необходимо: n n n Тщательно собрать анамнез жизни и болезни, Провести тщательный анализ предшествующей терапии, Провести объективную оценку клинико лабораторных показателей.
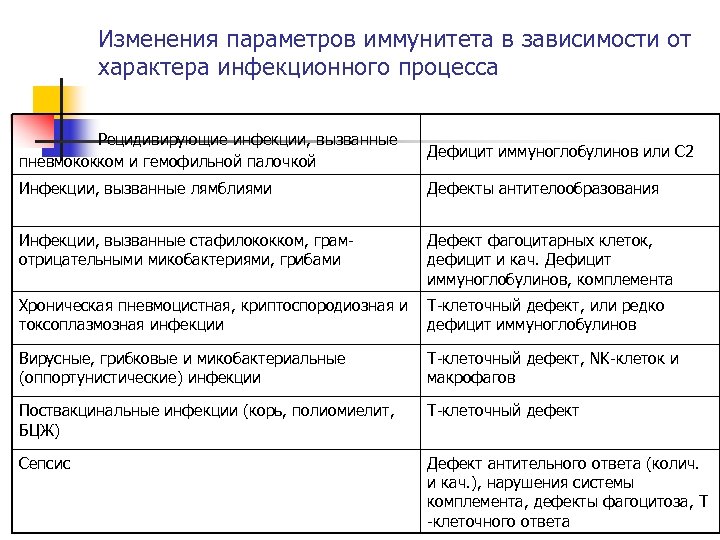
Изменения параметров иммунитета в зависимости от характера инфекционного процесса Рецидивирующие инфекции, вызванные пневмококком и гемофильной палочкой Дефицит иммуноглобулинов или С 2 Инфекции, вызванные лямблиями Дефекты антителообразования Инфекции, вызванные стафилококком, грам отрицательными микобактериями, грибами Дефект фагоцитарных клеток, дефицит и кач. Дефицит иммуноглобулинов, комплемента Хроническая пневмоцистная, криптоспородиозная и Т клеточный дефект, или редко токсоплазмозная инфекции дефицит иммуноглобулинов Вирусные, грибковые и микобактериальные (оппортунистические) инфекции Т клеточный дефект, NK клеток и макрофагов Поствакцинальные инфекции (корь, полиомиелит, БЦЖ) Т клеточный дефект Сепсис Дефект антительного ответа (колич. и кач. ), нарушения системы комплемента, дефекты фагоцитоза, Т клеточного ответа

Причины гипердиагностики ВИН: n n Наличие рецидивирующих инфекционно воспалительных заболеваний, обусловленных неадекватной терапией основного заболевания, что является причиной отсутствия эффекта от проводимого лечения, неадекватная терапия сопутствующей патологии, несбалансированное питание, нарушение санитарно гигиенических правил, воздействие хронического и острого стресса (конфликты в детском и учебном учреждениях, на работе и т. п. ) и другие.

Обратимые ВИН n К развитию могут приводить: несбалансированное питание (голодание, дефицит отдельных пищевых ингредиентов), n острый и хронический стресс, n эндокринная патология (сахарный диабет, заболевания щитовидной железы и др. ), n ятрогенные факторы (длительная терапия антибиотиками, цитостатиками, ГКС, иммунодепрессантами и т. п. ), n состояния после трансплантации органов и тканей, экологические факторы (воздействие неблагоприятных факторов внешней среды, в том числе антропогенного характера: радиационное воздействие, химические факторы, воздействие ксенобиотиков и др. ). n

n ВИН с необратимыми дисфункциями иммунной системы развивается при ВИЧ инфекции, n воздействии запредельных доз ионизирующей радиации, n n n токсическом воздействии на систему кроветворения (лекарственные агранулоцитозы, лимфотоксический эффект препаратов и т. п. ), при лимфопролиферативных и злокачественных заболеваниях, необратимых поражениях иммунной системы вследствие тяжелых бактериальных, вирусных, грибковых и других заболеваний (стафилококковые, туберкулез, системные микозы и т. п. )

Иммуномодуляторы n n Это— медикаменты с иммунотропым эффектом (способны взаимодействовать с клетками иммунной системы), которые в терапевтических дозах восстанавливают нарушенный иммунный ответ. Патогенетическим обоснованием для назначения этой группы препаратов является наличие иммунной недостаточности или иммунодефицита, развивающегося на фоне любой патологии, как у взрослых, так и у детей.

Иммуностимуляторы n Это — вещества различной природы (медикаменты, витамины, гормоны, БАДы и др. , физические воздействия и пр. ), способные стимулировать иммунную систему. Показанием для назначения этой группы препаратов является наличие соответствующих соматических заболеваний (заболевания ЖКТ, глистные и паразитарные заболевания, обменные нарушения и др. ). n n Эффективность иммуностимуляторов при ВИН либо отсутствует, либо сомнительна, поскольку они имеют иные механизмы действия.

n n Иммунокорректоры —медикаменты, которые должны обладать выраженным иммунотропным эффектом и в терапевтических дозах восстанавливать нарушения в конкретном звене иммунной системы (воздействуя, например, на дифференцировку В' или Т'лимфоцитов, систему комплемента и т. п. ). Таких медикаментов в практическом здравоохранении пока нет. Иммунодепрессанты— препараты, подавляющие иммунный ответ. Они используются в онкологии, при системных заболеваниях, некоторых болезнях крови и др.

Принципы клинического применения иммуномодуляторов: I. Иммуномодуляторы назначают в комплексной терапии одновременно с антибактериальными или противовирусными препаратами, при этом по возбудителю наносится «двойной удар» : антибактериальный препарат снижает функциональную активность микроба, а иммуномодулятор повышает функциональную активность клеток иммунной системы. II. Иммуномодуляторы целесообразно включать в комплексную терапию с первых дней заболевания (вместе с этиотропными противоинфекционными средствами). III. Иммуномодуляторы можно назначать в виде монотерапии проведении иммунореабилитационных мероприятий. IV. При наличии материально технической базы применять иммуномодулятор целесообразно на фоне иммунологического мониторинга.

Показания к включению иммуномодуляторов в ком, плексную терапию заболеваний, протекающих в сочетании с ВИН , у взрослых и детей: n n n n сепсис, гнойно септические хирургические инфекции, пиодермия и другие гнойно воспалительные процессы кожи и мягких тканей тяжелого течения, хронические, рецидивирующие урогенитальные инфекции, рецидивирующие герпетические инфекции, хронические неспецифические заболевания бронхолегочного аппарата, онкологические заболевания (на фоне химио или радиотерапии и др. ), АСИТ у больных с аллергическими заболеваниями, протекающими в сочетании с ВИН, и др.

Показания к применению иммуномодуляторов в виде монотерапии (иммунореабилитация) у взрослых и детей: n n n n восстановление иммунитета после перенесенных «истощающих» болезней (тяжелые инфекции, ожоговая болезнь и др. , у больных с неполным выздоровлением, профилактика респираторных инфекций в группе ЧБД (перед началом осенне зимнего сезона для профилактики обострений воспалительных заболеваний), профилактика инфекций и восстановление иммунитета после радио и химиотерапии у онкологических больных, восстановление иммунитета после перенесенного инфекционного заболевания у лиц с «физиологическим» ИДС (дети раннего возраста, лица пожилого и старческого возраста перед началом осенне зимнего сезона для профилактики обострений воспалительных заболеваний), профилактика инфекций и восстановление иммунитета у лиц, подвергающегося постоянному воздействию малых доз радиации или химических факторов (работники химических предприятий, АЭС и т. п. ) и входящих в группу риска по ИН, и др.

n При ВИН предпочтение отдается только тем иммуномодуляторам, которые относятся к лекарственным средствам с выраженным иммуномодулирующим эффектом, используемым именно с этой целью и отвечающим требованиям доказательной медицины.

Названия иммуномодуляторов n n n Рибомунил Бронхомунал, Имудон, ИРС 19 Ликопид Тактивин, Тималин Тимостимулин Тимоген Бестим Иммунофан Миелопид Серамил Лейкинферон, n n n n Суперлимф Ронколейкин Беталейкин Лейкомакс, Нейпоген Натрия нуклеинат Деринат Полудан Галавит Гепон Глутоксим Аллоферон Полиоксидоний

Интерфероны и индукторы интерфкронов n n n n n Интерферон Реальдирон Интрон'А Виферон, Реаферон, Генферон Роферон'А Бетаферон и др. Амиксин Циклоферон Неовир Полифенолы растительного происхождения и др.
c0ed20fe2c288275779bb244042d6bff.ppt