Neorg_chem_basic_4.ppt
- Количество слайдов: 81
 Координационные (комплексные) соединения (КС) до 1893 г. строение КС не было известно • название присваивались именами известных химиков: Pt 6 NH 3 4 Cl ( [Pt(NH 3)6]Cl 4 ) – соль Дрекселя; Pt 2 NH 3 2 Cl ( транс-[Pt(NH 3)2 Cl 2] ) – соль Пейроне; 2 Pd 4 NH 3 4 Cl ( [Pd(NH 3)4][Pd. Cl 4] – соль Вокелена; 2 Pt 4 NH 3 4 Cl ( [Pt(NH 3)4][Pt. Cl 4] – зеленая соль Магнуса; • или по окраске: Co 6 NH 3 3 Cl ( [Co(NH 3)6]Cl 3 ) – лутеосоль кобальта (от лат. luteus – желтый); Ir 6 NH 3 3 Cl ( [Co(NH 3)6]Cl 3 ) – лутеосоль иридия (хотя окраска белая. . . ? )
Координационные (комплексные) соединения (КС) до 1893 г. строение КС не было известно • название присваивались именами известных химиков: Pt 6 NH 3 4 Cl ( [Pt(NH 3)6]Cl 4 ) – соль Дрекселя; Pt 2 NH 3 2 Cl ( транс-[Pt(NH 3)2 Cl 2] ) – соль Пейроне; 2 Pd 4 NH 3 4 Cl ( [Pd(NH 3)4][Pd. Cl 4] – соль Вокелена; 2 Pt 4 NH 3 4 Cl ( [Pt(NH 3)4][Pt. Cl 4] – зеленая соль Магнуса; • или по окраске: Co 6 NH 3 3 Cl ( [Co(NH 3)6]Cl 3 ) – лутеосоль кобальта (от лат. luteus – желтый); Ir 6 NH 3 3 Cl ( [Co(NH 3)6]Cl 3 ) – лутеосоль иридия (хотя окраска белая. . . ? )
 Координационные (комплексные) соединения (КС) Нобелевская премия по химии Швейцарский химик Альфред Вернер (1866 -1919)
Координационные (комплексные) соединения (КС) Нобелевская премия по химии Швейцарский химик Альфред Вернер (1866 -1919)
 Координационные (комплексные) соединения координационная теория Вернера – основа для создания номенклатуры и прорыв в теории строения этого класса соединений «АНАТОМИЯ» КОМПЛЕКСНЫХ СОЕДИНЕНИЙ лиганды (от лат. ligare – связывать, соединять) [ Ru (NO)(NH 3)4 Cl] Cl 2 центральный атом (ЦА) внутренняя сфера внешняя сфера
Координационные (комплексные) соединения координационная теория Вернера – основа для создания номенклатуры и прорыв в теории строения этого класса соединений «АНАТОМИЯ» КОМПЛЕКСНЫХ СОЕДИНЕНИЙ лиганды (от лат. ligare – связывать, соединять) [ Ru (NO)(NH 3)4 Cl] Cl 2 центральный атом (ЦА) внутренняя сфера внешняя сфера
![Комплекс - центральный атом или ион (чаще всего металла), окруженный набором лигандов. [Co(NH 3)6]3+ Комплекс - центральный атом или ион (чаще всего металла), окруженный набором лигандов. [Co(NH 3)6]3+](https://present5.com/presentation/37029447_137937197/image-5.jpg) Комплекс - центральный атом или ион (чаще всего металла), окруженный набором лигандов. [Co(NH 3)6]3+ - комплекс [Co(NH 3)6]Cl 3 – комплексное соединение. [Fe(CO)5] – комплекс и комплексное соединение
Комплекс - центральный атом или ион (чаще всего металла), окруженный набором лигандов. [Co(NH 3)6]3+ - комплекс [Co(NH 3)6]Cl 3 – комплексное соединение. [Fe(CO)5] – комплекс и комплексное соединение
 Лиганд – ион или нейтральная молекула, которые связаны с центральным атомом. Донорный атом – атом в лиганде, который непосредственно связан с центральным атомом. Координационное число (КЧ) – число донорных атомов, которые связаны с центральным атомом. [Co(NH 3)6]3+ [Fe(CO)5]
Лиганд – ион или нейтральная молекула, которые связаны с центральным атомом. Донорный атом – атом в лиганде, который непосредственно связан с центральным атомом. Координационное число (КЧ) – число донорных атомов, которые связаны с центральным атомом. [Co(NH 3)6]3+ [Fe(CO)5]
 • Донорно-акцепторный механизм: лиганд предоставляет электронную пару (основание Льюиса), а центральный атом вакантную орбиталь (кислота Льюиса). • Координационные (комплексные) соединения характерны прежде всего для d - элементов (а также f – элементов) – есть вакантные орбитали металла и они способны принимать электронную пару от лиганда.
• Донорно-акцепторный механизм: лиганд предоставляет электронную пару (основание Льюиса), а центральный атом вакантную орбиталь (кислота Льюиса). • Координационные (комплексные) соединения характерны прежде всего для d - элементов (а также f – элементов) – есть вакантные орбитали металла и они способны принимать электронную пару от лиганда.
 ЛИГАНДЫ Амбидентатные лиганды – содержат несколько различных донорных атомов Роданид анион SCN-: если донорный атом S – тиоцианато-лиганд, если донорный атом N – изотиоцианато-лиганд Цианид ион CN-: если донорный атом C – циано-лиганд, если донорный атом N – изоциано-лиганд. нитро-лиганд нитрито-лиганд
ЛИГАНДЫ Амбидентатные лиганды – содержат несколько различных донорных атомов Роданид анион SCN-: если донорный атом S – тиоцианато-лиганд, если донорный атом N – изотиоцианато-лиганд Цианид ион CN-: если донорный атом C – циано-лиганд, если донорный атом N – изоциано-лиганд. нитро-лиганд нитрито-лиганд
 Полидентатные лиганды (dens, р. пад. dentis – лат. зуб)– содержат несколько донорных атомов и занимают несколько координационных мест в координационной сфере. Полидентатные лиганды часто образуют хелаты (от греч. «клешня» ) – комплексы, в которых лиганд и центральный атом образуют цикл. Этилендиамин (en) - лиганд Этилендиаминтераацетато (edta)-лиганд
Полидентатные лиганды (dens, р. пад. dentis – лат. зуб)– содержат несколько донорных атомов и занимают несколько координационных мест в координационной сфере. Полидентатные лиганды часто образуют хелаты (от греч. «клешня» ) – комплексы, в которых лиганд и центральный атом образуют цикл. Этилендиамин (en) - лиганд Этилендиаминтераацетато (edta)-лиганд
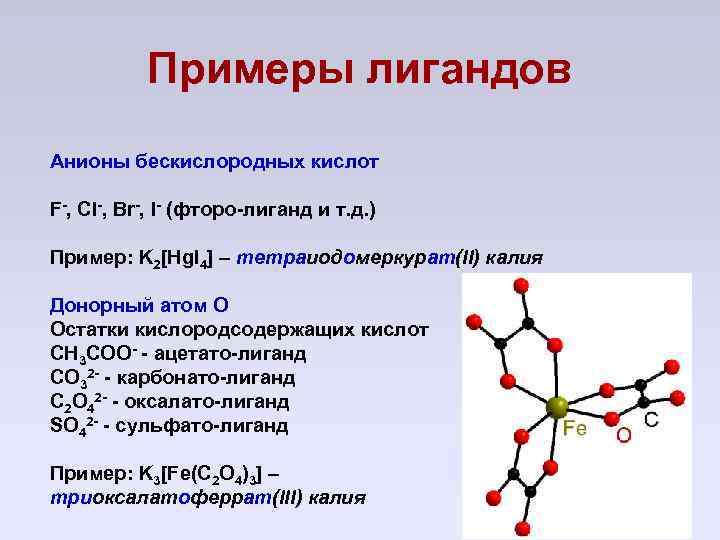 Примеры лигандов Анионы бескислородных кислот F-, Cl-, Br-, I- (фторо-лиганд и т. д. ) Пример: K 2[Hg. I 4] – тетраиодомеркурат(II) калия Донорный атом O Остатки кислородсодержащих кислот CH 3 COO- - ацетато-лиганд CO 32 - - карбонато-лиганд C 2 O 42 - - оксалато-лиганд SO 42 - - сульфато-лиганд Пример: K 3[Fe(C 2 O 4)3] – триоксалатоферрат(III) калия
Примеры лигандов Анионы бескислородных кислот F-, Cl-, Br-, I- (фторо-лиганд и т. д. ) Пример: K 2[Hg. I 4] – тетраиодомеркурат(II) калия Донорный атом O Остатки кислородсодержащих кислот CH 3 COO- - ацетато-лиганд CO 32 - - карбонато-лиганд C 2 O 42 - - оксалато-лиганд SO 42 - - сульфато-лиганд Пример: K 3[Fe(C 2 O 4)3] – триоксалатоферрат(III) калия
 Донорный атом O OH- - гидроксо-лиганд O 2 - - оксо-лиганд O 22 - - пероксо-лиганд K 2[Zn(OH)4] – тетрагидроксоцинкат(II) калия Электоронейтральные молекулы с донорными атомами O: H 2 O – аква-лиганд [Fe(H 2 O)6](Cl. O 4)3 – гексаакважелезо(III) перхлорат
Донорный атом O OH- - гидроксо-лиганд O 2 - - оксо-лиганд O 22 - - пероксо-лиганд K 2[Zn(OH)4] – тетрагидроксоцинкат(II) калия Электоронейтральные молекулы с донорными атомами O: H 2 O – аква-лиганд [Fe(H 2 O)6](Cl. O 4)3 – гексаакважелезо(III) перхлорат
 Электоронейтральные молекулы с донорными атомами N NH 3 – аммин (лиганд) Пиридин (Py) Этилендиамин (en) [Pt(en)2]Cl 2 – бис(этилендиамин)платина(II) хлорид Электоронейтральные молекулы с донорными атомами S H 2 S (“плохой” лиганд) Тиоэфиры, тиоспирты, тиомочевина (Thio) Электоронейтральные молекулы с донорными атомами P Ph 3 P – трифенилфосфин [Pt(PPh 3)4] – тетракис(трифенилфосфин)платина
Электоронейтральные молекулы с донорными атомами N NH 3 – аммин (лиганд) Пиридин (Py) Этилендиамин (en) [Pt(en)2]Cl 2 – бис(этилендиамин)платина(II) хлорид Электоронейтральные молекулы с донорными атомами S H 2 S (“плохой” лиганд) Тиоэфиры, тиоспирты, тиомочевина (Thio) Электоронейтральные молекулы с донорными атомами P Ph 3 P – трифенилфосфин [Pt(PPh 3)4] – тетракис(трифенилфосфин)платина
 КООРДИНАЦИОННЫЕ ЧИСЛА И КООРДИНАЦИОННЫЕ ПОЛИЭДРЫ Низкие КЧ = 2, 3 – встречаются редко КЧ = 2 характерно для Cu(I), Ag(I), Au(I) и Hg(II), линейные комплексы ( угол 180 о) КЧ = 3 встречается очень редко, K[Cu(CN)2]
КООРДИНАЦИОННЫЕ ЧИСЛА И КООРДИНАЦИОННЫЕ ПОЛИЭДРЫ Низкие КЧ = 2, 3 – встречаются редко КЧ = 2 характерно для Cu(I), Ag(I), Au(I) и Hg(II), линейные комплексы ( угол 180 о) КЧ = 3 встречается очень редко, K[Cu(CN)2]
 КЧ = 4 - огромное число соединений (тетраэдр или квадрат) Тетраэдрическое окружение характерно для оксоанионов металлов 5, 6 и 7 групп в высших степенях окисления и для галогенидных комплексов M(II) элементов 8 -12 групп.
КЧ = 4 - огромное число соединений (тетраэдр или квадрат) Тетраэдрическое окружение характерно для оксоанионов металлов 5, 6 и 7 групп в высших степенях окисления и для галогенидных комплексов M(II) элементов 8 -12 групп.
 Квадрат характерен для металлов с электронной конфигурацией d 8 Очень характерен для Pt(II) и Pd(II); часто образуют Ni(II), Rh(I), Ir(I), Au(III). [Pt(NH 3)2 Cl 2] - два геометрически изомера – цис и транс. Свойства отличаются очень сильно: цис-изомер является лучшим препаратом для хемиотерапии рака, транс-изомер – ядовит и не обладает противораковыми свойствами.
Квадрат характерен для металлов с электронной конфигурацией d 8 Очень характерен для Pt(II) и Pd(II); часто образуют Ni(II), Rh(I), Ir(I), Au(III). [Pt(NH 3)2 Cl 2] - два геометрически изомера – цис и транс. Свойства отличаются очень сильно: цис-изомер является лучшим препаратом для хемиотерапии рака, транс-изомер – ядовит и не обладает противораковыми свойствами.
![КЧ = 5 – менее распространен (квадратная пирамида и тригональная бипирамида) Пентацианоникелат (II), [Ni(CN)5]3 КЧ = 5 – менее распространен (квадратная пирамида и тригональная бипирамида) Пентацианоникелат (II), [Ni(CN)5]3](https://present5.com/presentation/37029447_137937197/image-16.jpg) КЧ = 5 – менее распространен (квадратная пирамида и тригональная бипирамида) Пентацианоникелат (II), [Ni(CN)5]3 -
КЧ = 5 – менее распространен (квадратная пирамида и тригональная бипирамида) Пентацианоникелат (II), [Ni(CN)5]3 -
 Гемоглобин Порфириновый цикл Гемовое железо
Гемоглобин Порфириновый цикл Гемовое железо
 КЧ = 6 – наиболее распространено Координационные полиэдры для почти всех комплексов с КЧ = 6 являются октаэдрами, редко - тригональная призма [Re(CH 3)6] Молибденит Mo. S 2
КЧ = 6 – наиболее распространено Координационные полиэдры для почти всех комплексов с КЧ = 6 являются октаэдрами, редко - тригональная призма [Re(CH 3)6] Молибденит Mo. S 2
 КЧ = 6 – наиболее характерно для металлов с электронной конфигурацией от d 0 до d 9 Примеры: d 0 – [Sc(H 2 O)6]3+; d 3 – [Cr(H 2 O)6]3+; d 5 – [Fe(CN)6]3 -; d 6 – [Rh. Cl 6]3 -
КЧ = 6 – наиболее характерно для металлов с электронной конфигурацией от d 0 до d 9 Примеры: d 0 – [Sc(H 2 O)6]3+; d 3 – [Cr(H 2 O)6]3+; d 5 – [Fe(CN)6]3 -; d 6 – [Rh. Cl 6]3 -
![КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+ Тригональная призма с одной шапкой КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+ Тригональная призма с одной шапкой](https://present5.com/presentation/37029447_137937197/image-20.jpg) КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+ Тригональная призма с одной шапкой [Nb. F 7]2 - Октаэдр с одной шапкой [Ta. Cl 4(PMe 3)3]
КЧ = 7 Пентагональная бипирамида [UO 2(H 2 O)5]2+ Тригональная призма с одной шапкой [Nb. F 7]2 - Октаэдр с одной шапкой [Ta. Cl 4(PMe 3)3]
![КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3 - КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3 -](https://present5.com/presentation/37029447_137937197/image-21.jpg) КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3 -
КЧ = 8 додекаэдр [Hf(ox)4]4 - квадратная антипризма [Mo(CN)8]3 -
 КЧ = 9 важно для лантаноидов, т. к. катионы Ln 3+ имеют достаточно большие размеры: (тригональная призма с тремя шапками) [Nd(H 2 O)9]3+ [Re. H 9]2 -
КЧ = 9 важно для лантаноидов, т. к. катионы Ln 3+ имеют достаточно большие размеры: (тригональная призма с тремя шапками) [Nd(H 2 O)9]3+ [Re. H 9]2 -
![КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ = 10, [Bi(NO 3)5]2 - КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ = 10, [Bi(NO 3)5]2 -](https://present5.com/presentation/37029447_137937197/image-23.jpg) КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ = 10, [Bi(NO 3)5]2 -
КЧ = 10, 12 КЧ=12, [Ce(NO 3)6]2 - КЧ = 10, [Bi(NO 3)5]2 -
![НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: 1. Сначала записывают катион, затем анион: X+ [MLn] или НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: 1. Сначала записывают катион, затем анион: X+ [MLn] или](https://present5.com/presentation/37029447_137937197/image-24.jpg) НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: 1. Сначала записывают катион, затем анион: X+ [MLn] или [MLn]+ X , например: K 2[Pt. Cl 4] или [Cu(NH 3)4]Cl 2 2. Если в состав внутренней сферы входят разные по заряду лиганды, их располагают: [M (L+) (L 0) (L )] например: [Ru (NO) (NH 3)2 Cl 3] (NH 4)[Ru (NO) (H 2 O) Cl 4] [Ru (NO) (NH 3)4 Cl] Cl 2
НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: 1. Сначала записывают катион, затем анион: X+ [MLn] или [MLn]+ X , например: K 2[Pt. Cl 4] или [Cu(NH 3)4]Cl 2 2. Если в состав внутренней сферы входят разные по заряду лиганды, их располагают: [M (L+) (L 0) (L )] например: [Ru (NO) (NH 3)2 Cl 3] (NH 4)[Ru (NO) (H 2 O) Cl 4] [Ru (NO) (NH 3)4 Cl] Cl 2
 НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: 3. Если в состав внутренней сферы входят несколько одинаковых по заряду лигандов: перечисление по алфавиту 4. При одинаковом химическом, но разном изотопном составе: лиганд с более тяжелом изотопом данного элемента располагают после лиганда с более легким изотопом: [Ru(NH 3)3(ND 3)3]Cl 2
НОМЕНКЛАТУРА (ИЮПАК) КС Построение формул: 3. Если в состав внутренней сферы входят несколько одинаковых по заряду лигандов: перечисление по алфавиту 4. При одинаковом химическом, но разном изотопном составе: лиганд с более тяжелом изотопом данного элемента располагают после лиганда с более легким изотопом: [Ru(NH 3)3(ND 3)3]Cl 2
 НОМЕНКЛАТУРА (ИЮПАК) КС Построение названий: 1. Названия "читаются" справа налево по правильно составленной формуле: сначала анион, затем катион
НОМЕНКЛАТУРА (ИЮПАК) КС Построение названий: 1. Названия "читаются" справа налево по правильно составленной формуле: сначала анион, затем катион
 НОМЕНКЛАТУРА (ИЮПАК) КС Названия лигандов: 2. Названия отрицательных лигандов: корень + -о. Br – бромо; O 2 – оксо; Cl – хлоро; O 22 – пероксо; F – фторо; O 3 – озоно; I – иодо; N 3 – нитридо; Н – гидридо; N 3 – азидо; S 2 – тио (традиционно); S 22 – дисульфидо(2 ); S 52 – пентасульфидо(2 );
НОМЕНКЛАТУРА (ИЮПАК) КС Названия лигандов: 2. Названия отрицательных лигандов: корень + -о. Br – бромо; O 2 – оксо; Cl – хлоро; O 22 – пероксо; F – фторо; O 3 – озоно; I – иодо; N 3 – нитридо; Н – гидридо; N 3 – азидо; S 2 – тио (традиционно); S 22 – дисульфидо(2 ); S 52 – пентасульфидо(2 );
 НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- OH – гидроксо; NO – нитрозо; CN – циано; NH 2 – амидо; NН 2 – имидо; NCS – тиоцианато-N (координация через атом N); SNC – тиоцианато-S (координация через атом S); (изотиоцианато)
НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- OH – гидроксо; NO – нитрозо; CN – циано; NH 2 – амидо; NН 2 – имидо; NCS – тиоцианато-N (координация через атом N); SNC – тиоцианато-S (координация через атом S); (изотиоцианато)
 НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- CO 32 – карбонато; NO 3 – нитрато; NO 2 – нитро (координация через атом N); ONO – нитрито (координация через атом О); SO 42 – сульфато; PO 43 – фосфато; SO 3(S)2 – тиосульфато;
НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- CO 32 – карбонато; NO 3 – нитрато; NO 2 – нитро (координация через атом N); ONO – нитрито (координация через атом О); SO 42 – сульфато; PO 43 – фосфато; SO 3(S)2 – тиосульфато;
 НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- HCOO – формиато; СН 3 СОО – ацетато; СН 3 СН 2 СОО – бутирато; – 2 -метилпропионат о; С 2 О 42 – оксалато; С 6 Н 5 СОО – бензоато;
НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных лигандов: корень + -о- HCOO – формиато; СН 3 СОО – ацетато; СН 3 СН 2 СОО – бутирато; – 2 -метилпропионат о; С 2 О 42 – оксалато; С 6 Н 5 СОО – бензоато;
 НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных органических углеводородов: без соединительной гласной C 6 Н 5 – фенил; C 5 Н 5 – циклопентадиенил;
НОМЕНКЛАТУРА (ИЮПАК) КС Названия отрицательных органических углеводородов: без соединительной гласной C 6 Н 5 – фенил; C 5 Н 5 – циклопентадиенил;
 НОМЕНКЛАТУРА (ИЮПАК) КС Названия положительных лигандов: корень + -ий. NO+ – нитрозилий; NO 2+ – нитроилий; N 2 Н 5+ – гидразиний
НОМЕНКЛАТУРА (ИЮПАК) КС Названия положительных лигандов: корень + -ий. NO+ – нитрозилий; NO 2+ – нитроилий; N 2 Н 5+ – гидразиний
 НОМЕНКЛАТУРА (ИЮПАК) КС Названия нейтральных лигандов: N 2 – диазот; SO 2 – диоксосера; СS 2 – сероуглерод; N 2 Н 4 – гидразин; NH 2 OH – гидроксиламин; C 2 H 4 – этилен; P(C 6 H 5)3 – трифенилфосфин; без изменений
НОМЕНКЛАТУРА (ИЮПАК) КС Названия нейтральных лигандов: N 2 – диазот; SO 2 – диоксосера; СS 2 – сероуглерод; N 2 Н 4 – гидразин; NH 2 OH – гидроксиламин; C 2 H 4 – этилен; P(C 6 H 5)3 – трифенилфосфин; без изменений
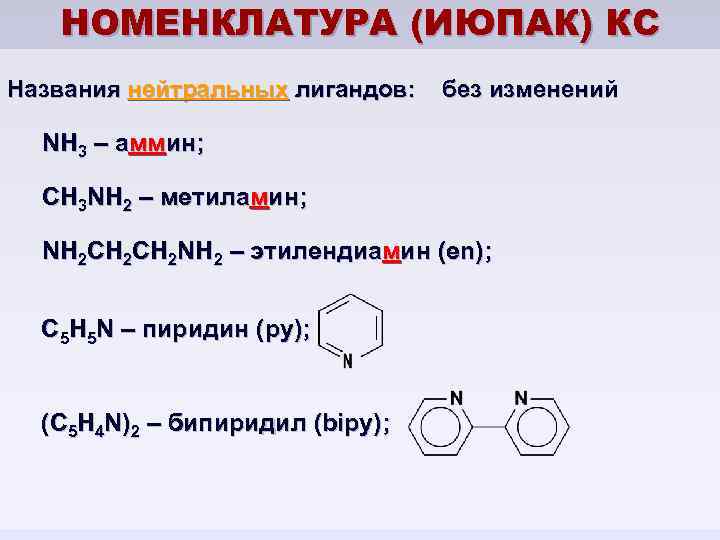 НОМЕНКЛАТУРА (ИЮПАК) КС Названия нейтральных лигандов: без изменений NН 3 – аммин; CH 3 NH 2 – метиламин; NH 2 CH 2 NH 2 – этилендиамин (en); С 5 Н 5 N – пиридин (py); (С 5 Н 4 N)2 – бипиридил (bipy);
НОМЕНКЛАТУРА (ИЮПАК) КС Названия нейтральных лигандов: без изменений NН 3 – аммин; CH 3 NH 2 – метиламин; NH 2 CH 2 NH 2 – этилендиамин (en); С 5 Н 5 N – пиридин (py); (С 5 Н 4 N)2 – бипиридил (bipy);
![НОМЕНКЛАТУРА (ИЮПАК) КС [Co(en)3]Cl 3 – хлорид трис(этилендиамин)кобальта(III) [(NH 3)5 Cr O Cr(NH 3)5]Cl НОМЕНКЛАТУРА (ИЮПАК) КС [Co(en)3]Cl 3 – хлорид трис(этилендиамин)кобальта(III) [(NH 3)5 Cr O Cr(NH 3)5]Cl](https://present5.com/presentation/37029447_137937197/image-35.jpg) НОМЕНКЛАТУРА (ИЮПАК) КС [Co(en)3]Cl 3 – хлорид трис(этилендиамин)кобальта(III) [(NH 3)5 Cr O Cr(NH 3)5]Cl 4 – хлорид ( -оксо)бис(пентаамминхрома(III))
НОМЕНКЛАТУРА (ИЮПАК) КС [Co(en)3]Cl 3 – хлорид трис(этилендиамин)кобальта(III) [(NH 3)5 Cr O Cr(NH 3)5]Cl 4 – хлорид ( -оксо)бис(пентаамминхрома(III))
 ИЗОМЕРИЯ КС Геометрическая изомерия цис- (cis-) ос- (mer-) транс- (trans-) гран- (fac-)
ИЗОМЕРИЯ КС Геометрическая изомерия цис- (cis-) ос- (mer-) транс- (trans-) гран- (fac-)
 Геометрическая изомерия
Геометрическая изомерия
 Определение строения изомеров Рентгеноструктурный анализ, ЯМР спектроскопия и другие методы.
Определение строения изомеров Рентгеноструктурный анализ, ЯМР спектроскопия и другие методы.
 Ионизационная изомерия КС Лиганды во внутренней и внешней координационной сфере меняются местами. [Co(NH 3)5 Cl]CN – пентаамминхлорокобальт(II) цианид [Co(NH 3)5 СN]Cl – пентаамминцианокобальт(II) хлорид Частный случай ионизационной изомерии – гидратная изомерия Cr. Cl 3. 6 H 2 O – три изомера Соединение Цвет [Cr(H 2 O)6]Cl 3 фиолетовый [Cr(H 2 O)5 Cl]Cl 2. H 2 O Светло-зеленый [Cr(H 2 O)4 Cl 2]Cl. 2 H 2 O Темно-зеленый
Ионизационная изомерия КС Лиганды во внутренней и внешней координационной сфере меняются местами. [Co(NH 3)5 Cl]CN – пентаамминхлорокобальт(II) цианид [Co(NH 3)5 СN]Cl – пентаамминцианокобальт(II) хлорид Частный случай ионизационной изомерии – гидратная изомерия Cr. Cl 3. 6 H 2 O – три изомера Соединение Цвет [Cr(H 2 O)6]Cl 3 фиолетовый [Cr(H 2 O)5 Cl]Cl 2. H 2 O Светло-зеленый [Cr(H 2 O)4 Cl 2]Cl. 2 H 2 O Темно-зеленый
 Связевая изомерия Характерна для комплексов с амбидентатными лигандами Нитро- нитрито-
Связевая изомерия Характерна для комплексов с амбидентатными лигандами Нитро- нитрито-
 Координационная изомерия для комплексных соединений, в которых и катион и анион являются комплексными [Cu(NH 3)4][Pt. Cl 4] – фиолетовый цвет [Pt(NH 3)4][Cu. Cl 4] – желто-коричневый цвет
Координационная изомерия для комплексных соединений, в которых и катион и анион являются комплексными [Cu(NH 3)4][Pt. Cl 4] – фиолетовый цвет [Pt(NH 3)4][Cu. Cl 4] – желто-коричневый цвет
![Координационная полимерия связана с изменением молекулярной массы комплексного соединения [Pt(NH 3)2 Cl 2] – Координационная полимерия связана с изменением молекулярной массы комплексного соединения [Pt(NH 3)2 Cl 2] –](https://present5.com/presentation/37029447_137937197/image-42.jpg) Координационная полимерия связана с изменением молекулярной массы комплексного соединения [Pt(NH 3)2 Cl 2] – один атом платины, оба изомера (цис- и транс) желтого цвета [Pt(NH 3)4][Pt. Cl 4] – два атома платины, зеленая соль Магнуса [Pt(NH 3)3 Cl]2[Pt. Cl 4] – три атома платины, золотистый цвет
Координационная полимерия связана с изменением молекулярной массы комплексного соединения [Pt(NH 3)2 Cl 2] – один атом платины, оба изомера (цис- и транс) желтого цвета [Pt(NH 3)4][Pt. Cl 4] – два атома платины, зеленая соль Магнуса [Pt(NH 3)3 Cl]2[Pt. Cl 4] – три атома платины, золотистый цвет
 Хиральность и оптическая изомерия Хиральный комплекс - изображение в зеркале не совпадает с оригиналом (как правая и левая рука). Два зеркальных изомера образуют пару энантиомеров. Хиральные комплексы, если они стабильны и не переходят быстро друг в друга, являются оптически активными – вращают плоскость поляризации света в разных направлениях
Хиральность и оптическая изомерия Хиральный комплекс - изображение в зеркале не совпадает с оригиналом (как правая и левая рука). Два зеркальных изомера образуют пару энантиомеров. Хиральные комплексы, если они стабильны и не переходят быстро друг в друга, являются оптически активными – вращают плоскость поляризации света в разных направлениях
![ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА КОМПЛЕКСОВ Cd 2+ + CN- = [Cd(CN)+] K 1 = [Cd(CN)+]/[Cd 2+][CN-] ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА КОМПЛЕКСОВ Cd 2+ + CN- = [Cd(CN)+] K 1 = [Cd(CN)+]/[Cd 2+][CN-]](https://present5.com/presentation/37029447_137937197/image-44.jpg) ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА КОМПЛЕКСОВ Cd 2+ + CN- = [Cd(CN)+] K 1 = [Cd(CN)+]/[Cd 2+][CN-] [Cd(CN)]+ + CN- = [Cd(CN)2] K 2 = [Cd(CN)2]/[ Cd(CN)+][CN-] [Cd(CN)2] + CN- = [Cd(CN)3]- K 3 = [Cd(CN)3 -]/[Cd(CN)2][CN-] [Cd(CN)3]- + CN- = [Cd(CN)4]2 - K 4 = [Cd(CN)42 -]/[ Cd(CN)3 -][CN-] К 1, K 2 и т. д. – константы ступенчатого комплексообразования βi - суммарная (полная) константа образования β 1 = K 1 ; β 2 = K 1 K 2 ; β 3 = K 1 K 2 K 3 ; β 4 = K 1 K 2 K 3 K 4 ΔG = -RTln. K ΔG < 0 – условие протекания реакции как самопроизвольного процесса
ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА КОМПЛЕКСОВ Cd 2+ + CN- = [Cd(CN)+] K 1 = [Cd(CN)+]/[Cd 2+][CN-] [Cd(CN)]+ + CN- = [Cd(CN)2] K 2 = [Cd(CN)2]/[ Cd(CN)+][CN-] [Cd(CN)2] + CN- = [Cd(CN)3]- K 3 = [Cd(CN)3 -]/[Cd(CN)2][CN-] [Cd(CN)3]- + CN- = [Cd(CN)4]2 - K 4 = [Cd(CN)42 -]/[ Cd(CN)3 -][CN-] К 1, K 2 и т. д. – константы ступенчатого комплексообразования βi - суммарная (полная) константа образования β 1 = K 1 ; β 2 = K 1 K 2 ; β 3 = K 1 K 2 K 3 ; β 4 = K 1 K 2 K 3 K 4 ΔG = -RTln. K ΔG < 0 – условие протекания реакции как самопроизвольного процесса
 Константа образования характеризует устойчивость комплексов (в водных растворах). Константа образования характеризует прочность связывания лиганда с металлом по сравнению с прочностью связывания воды с металлом. ОБЫЧНО: К 1> К 2 > К 3 и так далее [M(H 2 O)5 L] + L = [M(H 2 O)4 L 2] + H 2 O [M(H 2 O)4 L 2] + L = [M(H 2 O)3 L 3] + H 2 O Статистический фактор!!!
Константа образования характеризует устойчивость комплексов (в водных растворах). Константа образования характеризует прочность связывания лиганда с металлом по сравнению с прочностью связывания воды с металлом. ОБЫЧНО: К 1> К 2 > К 3 и так далее [M(H 2 O)5 L] + L = [M(H 2 O)4 L 2] + H 2 O [M(H 2 O)4 L 2] + L = [M(H 2 O)3 L 3] + H 2 O Статистический фактор!!!
 ХЕЛАТНЫЙ ЭФФЕКТ Большая устойчивость хелатных комплексов по сравнению с их нехелатными аналогами. [Ni(H 2 O)6]2+ + 6 NH 3 = [Ni(NH 3)6]2+ + 6 H 2 O β 6 = 108, 6 [Ni(H 2 O)6]2+ + 3 en = [Ni(en)3]2+ + 6 H 2 O β 3 = 1018, 3 Энтропийный фактор: Δr. G = Δr. H -TΔr. S = -RTln. K
ХЕЛАТНЫЙ ЭФФЕКТ Большая устойчивость хелатных комплексов по сравнению с их нехелатными аналогами. [Ni(H 2 O)6]2+ + 6 NH 3 = [Ni(NH 3)6]2+ + 6 H 2 O β 6 = 108, 6 [Ni(H 2 O)6]2+ + 3 en = [Ni(en)3]2+ + 6 H 2 O β 3 = 1018, 3 Энтропийный фактор: Δr. G = Δr. H -TΔr. S = -RTln. K
 Ряд устойчивости Ирвинга-Вильямса
Ряд устойчивости Ирвинга-Вильямса
 Кинетическая устойчивость комплексов Термодинамика отражает только тот факт, что комплекс может получиться. Кинетика показывает быстро или медленно может получиться комплекс. Лабильные комплексы – подвергаются превращениям с большой скоростью. Инертные комплексы – подвергаются превращениям с малой скоростью.
Кинетическая устойчивость комплексов Термодинамика отражает только тот факт, что комплекс может получиться. Кинетика показывает быстро или медленно может получиться комплекс. Лабильные комплексы – подвергаются превращениям с большой скоростью. Инертные комплексы – подвергаются превращениям с малой скоростью.
![Инертные и лабильные комплексы [Fe(H 2 O)6]3+ и [Cr(H 2 O)6]3+ имеют высокие значения Инертные и лабильные комплексы [Fe(H 2 O)6]3+ и [Cr(H 2 O)6]3+ имеют высокие значения](https://present5.com/presentation/37029447_137937197/image-49.jpg) Инертные и лабильные комплексы [Fe(H 2 O)6]3+ и [Cr(H 2 O)6]3+ имеют высокие значения константы образования и, значит, приблизительно одинаковую термодинамическую стабильность [M(H 2 O)6]3+ + H 2 O* = [M(H 2 O)5(H 2 O*)]3+ + H 2 O t 1/2 – время полуреакции Для Fe 3+, t 1/2 = 1 сек – лабильный комплекс Для Cr 3+, t 1/2 = 10000 сек – инертный комплекс
Инертные и лабильные комплексы [Fe(H 2 O)6]3+ и [Cr(H 2 O)6]3+ имеют высокие значения константы образования и, значит, приблизительно одинаковую термодинамическую стабильность [M(H 2 O)6]3+ + H 2 O* = [M(H 2 O)5(H 2 O*)]3+ + H 2 O t 1/2 – время полуреакции Для Fe 3+, t 1/2 = 1 сек – лабильный комплекс Для Cr 3+, t 1/2 = 10000 сек – инертный комплекс
![Инертные и лабильные комплексы [Ni(CN)4]2 - β 4 = 1022, термодинамически очень стабилен [Ni(CN)4]2 Инертные и лабильные комплексы [Ni(CN)4]2 - β 4 = 1022, термодинамически очень стабилен [Ni(CN)4]2](https://present5.com/presentation/37029447_137937197/image-50.jpg) Инертные и лабильные комплексы [Ni(CN)4]2 - β 4 = 1022, термодинамически очень стабилен [Ni(CN)4]2 - + 4 CN-* = [Ni(CN*)4]2 - + 4 CNОчень быстрая реакция, кинетически лабильный комплекс [Co(NH 3)6]3+ + 6 H 3 O+ = [Co(H 2 O)6]3+ + 6 NH 4+ K = 1025, но аммиачный комплекс кинетически инертен и может быть выделен из растворов в концентрированной HCl
Инертные и лабильные комплексы [Ni(CN)4]2 - β 4 = 1022, термодинамически очень стабилен [Ni(CN)4]2 - + 4 CN-* = [Ni(CN*)4]2 - + 4 CNОчень быстрая реакция, кинетически лабильный комплекс [Co(NH 3)6]3+ + 6 H 3 O+ = [Co(H 2 O)6]3+ + 6 NH 4+ K = 1025, но аммиачный комплекс кинетически инертен и может быть выделен из растворов в концентрированной HCl
 Инертные и лабильные аквакомплексы
Инертные и лабильные аквакомплексы
 Механизмы реакций замещения лигандов Диссоциативный Взаимного обмена Ассоциативный
Механизмы реакций замещения лигандов Диссоциативный Взаимного обмена Ассоциативный
 Теория кристаллического поля Электронная пара лиганда рассматривается как точечный отрицательный заряд, который отталкивается электронами на d-орбиталях металла. Теория хорошо объясняет магнитные свойства комплексов, ЭСП и др.
Теория кристаллического поля Электронная пара лиганда рассматривается как точечный отрицательный заряд, который отталкивается электронами на d-орбиталях металла. Теория хорошо объясняет магнитные свойства комплексов, ЭСП и др.
 Октаэдрические комплексы Сферическое окружение Октаэдрическое окружение eg t 2 g Δo – параметр расщепления полем лиганда
Октаэдрические комплексы Сферическое окружение Октаэдрическое окружение eg t 2 g Δo – параметр расщепления полем лиганда
![Электронные спектры поглощения (окраска) d 1 комплекс [Ti(H 2 O)6]3+ фиолетовый цвет eg t Электронные спектры поглощения (окраска) d 1 комплекс [Ti(H 2 O)6]3+ фиолетовый цвет eg t](https://present5.com/presentation/37029447_137937197/image-55.jpg) Электронные спектры поглощения (окраска) d 1 комплекс [Ti(H 2 O)6]3+ фиолетовый цвет eg t 2 g
Электронные спектры поглощения (окраска) d 1 комплекс [Ti(H 2 O)6]3+ фиолетовый цвет eg t 2 g

 Спектрохимический ряд лигандов (Р. Цусида) Лиганды располагают в порядке возрастания энергии перехода в ЭСП комплексов I- Br- Cl- F- OH- H 2 O Py NH 3 en CN- CO Лиганды слабого поля [Co. X(NH 3)5]2+: Лиганды сильного поля X = I, красно-фиолетовый цвет X = Cl, розовый цвет X = NH 3, желтый цвет
Спектрохимический ряд лигандов (Р. Цусида) Лиганды располагают в порядке возрастания энергии перехода в ЭСП комплексов I- Br- Cl- F- OH- H 2 O Py NH 3 en CN- CO Лиганды слабого поля [Co. X(NH 3)5]2+: Лиганды сильного поля X = I, красно-фиолетовый цвет X = Cl, розовый цвет X = NH 3, желтый цвет
 Спектрохимический ряд металлов Mn 2+ Ni 2+ Co 2+ Fe 2+ Fe 3+ Co 3+ Mn 4+ Rh 3+ Pd 4+ Pt 4+ Δo возрастает при увеличении степени окисления металла (меньше размер катиона, короче длина связи M-L) Δo возрастает по группе при увеличении ат. номера (4 d, 5 d орбитали более диффузные, чем 3 d орбитали).
Спектрохимический ряд металлов Mn 2+ Ni 2+ Co 2+ Fe 2+ Fe 3+ Co 3+ Mn 4+ Rh 3+ Pd 4+ Pt 4+ Δo возрастает при увеличении степени окисления металла (меньше размер катиона, короче длина связи M-L) Δo возрастает по группе при увеличении ат. номера (4 d, 5 d орбитали более диффузные, чем 3 d орбитали).
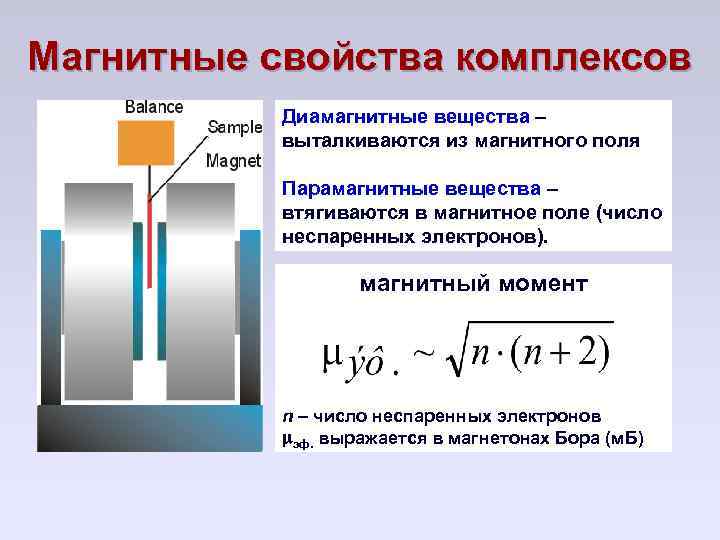 Магнитные свойства комплексов Диамагнитные вещества – выталкиваются из магнитного поля Парамагнитные вещества – втягиваются в магнитное поле (число неспаренных электронов). магнитный момент n – число неспаренных электронов эф. выражается в магнетонах Бора (м. Б)
Магнитные свойства комплексов Диамагнитные вещества – выталкиваются из магнитного поля Парамагнитные вещества – втягиваются в магнитное поле (число неспаренных электронов). магнитный момент n – число неспаренных электронов эф. выражается в магнетонах Бора (м. Б)
![3 d 2, [Ti(H 2 O)6]2+ 3 d 3, [V(H 2 O)6]2+ два неспаренных 3 d 2, [Ti(H 2 O)6]2+ 3 d 3, [V(H 2 O)6]2+ два неспаренных](https://present5.com/presentation/37029447_137937197/image-60.jpg) 3 d 2, [Ti(H 2 O)6]2+ 3 d 3, [V(H 2 O)6]2+ два неспаренных электрона три неспаренных электрона
3 d 2, [Ti(H 2 O)6]2+ 3 d 3, [V(H 2 O)6]2+ два неспаренных электрона три неспаренных электрона
 Сильное поле d 4 два неспаренных электрона Слабое поле d 4 четыре неспаренных электрона
Сильное поле d 4 два неспаренных электрона Слабое поле d 4 четыре неспаренных электрона
 Для 3 d 5, 3 d 6, 3 d 7 существуют высокоспиновые и низкоспиновые комплексы. Для 3 d 8, 3 d 9, 3 d 10 – нет выбора, все однозначно (термины высокоспиновый, низкоспиновый не применимы!) 4 d и 5 d комплексы, как правило, низкоспиновые. Δo возрастает по группе при увеличении атомного номера (4 d, 5 d орбитали более диффузные, чем 3 d орбитали). 4 d 4, [Ru. Cl 6]2 -, низкоспиновый, а лиганд слабого поля [Ru(ox)3]3 -, t 2 g 5 – низкоспиновый [Fe(ox)3]3 -, t 2 g 3 eg 2 – высокоспиновый
Для 3 d 5, 3 d 6, 3 d 7 существуют высокоспиновые и низкоспиновые комплексы. Для 3 d 8, 3 d 9, 3 d 10 – нет выбора, все однозначно (термины высокоспиновый, низкоспиновый не применимы!) 4 d и 5 d комплексы, как правило, низкоспиновые. Δo возрастает по группе при увеличении атомного номера (4 d, 5 d орбитали более диффузные, чем 3 d орбитали). 4 d 4, [Ru. Cl 6]2 -, низкоспиновый, а лиганд слабого поля [Ru(ox)3]3 -, t 2 g 5 – низкоспиновый [Fe(ox)3]3 -, t 2 g 3 eg 2 – высокоспиновый
 Тетраэдрические комплексы t 2 e e t 2 Δт Δ o
Тетраэдрические комплексы t 2 e e t 2 Δт Δ o
 Методы синтеза КС 1) Реакции обмена в водных растворах 2) Реакции обмена в неводных растворах 3) Окислительно-восстановительные реакции в растворах Реакция Cu. SO 4 в воде с аммиаком [Cu(H 2 O)4]2+ + 4 NH 3 = [Cu(NH 3)4]2+ + 4 H 2 O голубой р-р темно-синий р-р Добавление этанола приводит к осаждению кристаллов [Cu(NH 3)4]SO 4
Методы синтеза КС 1) Реакции обмена в водных растворах 2) Реакции обмена в неводных растворах 3) Окислительно-восстановительные реакции в растворах Реакция Cu. SO 4 в воде с аммиаком [Cu(H 2 O)4]2+ + 4 NH 3 = [Cu(NH 3)4]2+ + 4 H 2 O голубой р-р темно-синий р-р Добавление этанола приводит к осаждению кристаллов [Cu(NH 3)4]SO 4
![Реакция Ni. Cl 2 в воде с аммиаком [Ni(H 2 O)6]2+ + 6 NH Реакция Ni. Cl 2 в воде с аммиаком [Ni(H 2 O)6]2+ + 6 NH](https://present5.com/presentation/37029447_137937197/image-65.jpg) Реакция Ni. Cl 2 в воде с аммиаком [Ni(H 2 O)6]2+ + 6 NH 3 = [Ni(NH 3)6]2+ + 6 H 2 O зеленый р-р фиолетовый р-р Высаливание: добавление NH 4 Cl приводит к осаждению кристаллов [Ni(NH 3)6]Cl 2 K 3[Rh. Cl 6] + 3 K 2 C 2 O 4 = K 3[Rh(C 2 O 4)3] + 6 KCl красный р-р желтый осадок Кипячение в воде 2 часа приводит к образованию кристаллов K 3[Rh(C 2 O 4)3]
Реакция Ni. Cl 2 в воде с аммиаком [Ni(H 2 O)6]2+ + 6 NH 3 = [Ni(NH 3)6]2+ + 6 H 2 O зеленый р-р фиолетовый р-р Высаливание: добавление NH 4 Cl приводит к осаждению кристаллов [Ni(NH 3)6]Cl 2 K 3[Rh. Cl 6] + 3 K 2 C 2 O 4 = K 3[Rh(C 2 O 4)3] + 6 KCl красный р-р желтый осадок Кипячение в воде 2 часа приводит к образованию кристаллов K 3[Rh(C 2 O 4)3]
![Реакции синтеза в неводных растворах [Cr(H 2 O)6]3+ + 3 en = Cr(OH)3 + Реакции синтеза в неводных растворах [Cr(H 2 O)6]3+ + 3 en = Cr(OH)3 +](https://present5.com/presentation/37029447_137937197/image-66.jpg) Реакции синтеза в неводных растворах [Cr(H 2 O)6]3+ + 3 en = Cr(OH)3 + 3 en. H+ + 3 H 2 O фиолетовый р-р осадок Реакция в воде приводит к гидролизу! Cr. Cl 3(безводный) + 3 en = [Cr(en)3]Cl 3 пурпурный желтый Реакция в диэтиловом эфире приводит к получению комплекса
Реакции синтеза в неводных растворах [Cr(H 2 O)6]3+ + 3 en = Cr(OH)3 + 3 en. H+ + 3 H 2 O фиолетовый р-р осадок Реакция в воде приводит к гидролизу! Cr. Cl 3(безводный) + 3 en = [Cr(en)3]Cl 3 пурпурный желтый Реакция в диэтиловом эфире приводит к получению комплекса
 Окислительновосстановительные реакции в растворах Комплексы Co 3+ кинетически инертны, поэтому их часто получают окислением соответствующих комплексов Co 2+: Co. Cl 2. 6 H 2 O + водный аммиак + кислород воздуха (или пероксид водорода): получают [Co(NH 3)6]Cl 3 K 2[Ni(CN)4] + 2 K = K 4[Ni(CN)4] Ni 2+ Ni 0 Реакцию восстановления проводят в жидком аммиаке
Окислительновосстановительные реакции в растворах Комплексы Co 3+ кинетически инертны, поэтому их часто получают окислением соответствующих комплексов Co 2+: Co. Cl 2. 6 H 2 O + водный аммиак + кислород воздуха (или пероксид водорода): получают [Co(NH 3)6]Cl 3 K 2[Ni(CN)4] + 2 K = K 4[Ni(CN)4] Ni 2+ Ni 0 Реакцию восстановления проводят в жидком аммиаке
 Транс-влияние Н. С. Курнаков, Л. А. Чугаев, И. И. Черняев В квадратных комплексах Pt(II) некоторые лиганды облегчают замещение других лигандов, находящихся в трансположении. Thio> I- >Br->Cl->NH 3>H 2 O
Транс-влияние Н. С. Курнаков, Л. А. Чугаев, И. И. Черняев В квадратных комплексах Pt(II) некоторые лиганды облегчают замещение других лигандов, находящихся в трансположении. Thio> I- >Br->Cl->NH 3>H 2 O
 Thio> I- >Br->Cl->NH 3>H 2 O + NH 3 - Cl- Cl- + NH 3 - Cl- + Cl- NH 3 … + NH 3
Thio> I- >Br->Cl->NH 3>H 2 O + NH 3 - Cl- Cl- + NH 3 - Cl- + Cl- NH 3 … + NH 3
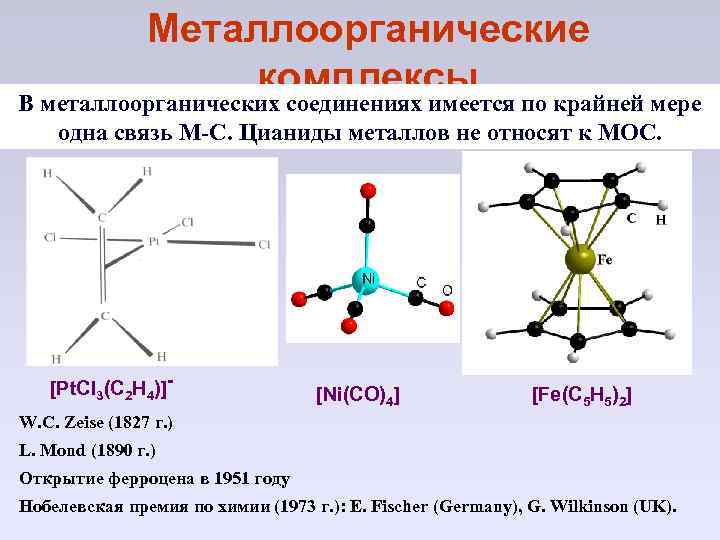 Металлоорганические комплексы В металлоорганических соединениях имеется по крайней мере одна связь M-C. Цианиды металлов не относят к МОС. [Pt. Cl 3(C 2 H 4)]- [Ni(CO)4] [Fe(C 5 H 5)2] W. C. Zeise (1827 г. ) L. Mond (1890 г. ) Открытие ферроцена в 1951 году Нобелевская премия по химии (1973 г. ): E. Fischer (Germany), G. Wilkinson (UK).
Металлоорганические комплексы В металлоорганических соединениях имеется по крайней мере одна связь M-C. Цианиды металлов не относят к МОС. [Pt. Cl 3(C 2 H 4)]- [Ni(CO)4] [Fe(C 5 H 5)2] W. C. Zeise (1827 г. ) L. Mond (1890 г. ) Открытие ферроцена в 1951 году Нобелевская премия по химии (1973 г. ): E. Fischer (Germany), G. Wilkinson (UK).
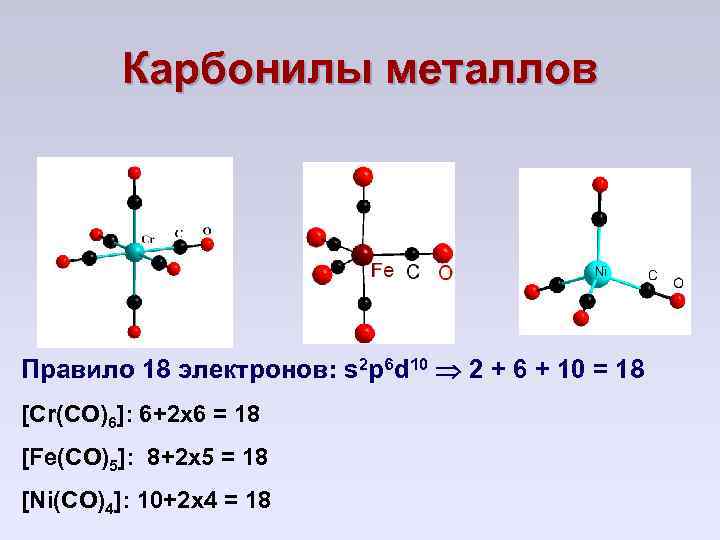 Карбонилы металлов Правило 18 электронов: s 2 p 6 d 10 2 + 6 + 10 = 18 [Cr(CO)6]: 6+2 x 6 = 18 [Fe(CO)5]: 8+2 x 5 = 18 [Ni(CO)4]: 10+2 x 4 = 18
Карбонилы металлов Правило 18 электронов: s 2 p 6 d 10 2 + 6 + 10 = 18 [Cr(CO)6]: 6+2 x 6 = 18 [Fe(CO)5]: 8+2 x 5 = 18 [Ni(CO)4]: 10+2 x 4 = 18
 Молекулярные орбитали СО 2 py 2 px 2 pz 1 2 2 2 1 4 3 2 Кр. св. = (8 -2)/2 = 3
Молекулярные орбитали СО 2 py 2 px 2 pz 1 2 2 2 1 4 3 2 Кр. св. = (8 -2)/2 = 3
 Электронное строение карбонилов металлов
Электронное строение карбонилов металлов
![Олефиновые комплексы [Pt. Cl 3( 2 -C 2 H 4)]- Олефиновые комплексы [Pt. Cl 3( 2 -C 2 H 4)]-](https://present5.com/presentation/37029447_137937197/image-74.jpg) Олефиновые комплексы [Pt. Cl 3( 2 -C 2 H 4)]-
Олефиновые комплексы [Pt. Cl 3( 2 -C 2 H 4)]-
![Строение металлоценов [Fe( 5 -C 5 H 5)2] – ферроцен (сэндвич) Получение ферроцена: C Строение металлоценов [Fe( 5 -C 5 H 5)2] – ферроцен (сэндвич) Получение ферроцена: C](https://present5.com/presentation/37029447_137937197/image-75.jpg) Строение металлоценов [Fe( 5 -C 5 H 5)2] – ферроцен (сэндвич) Получение ферроцена: C 5 H 6 + Na = Na+(C 5 H 5)- + ½ H 2 Fe. Cl 2 + 2 Na+(C 5 H 5)- = [Fe(C 5 H 5)2] + 2 Na. Cl Растворители: эфир, тетрагидрофуран; инертная атмосфера
Строение металлоценов [Fe( 5 -C 5 H 5)2] – ферроцен (сэндвич) Получение ферроцена: C 5 H 6 + Na = Na+(C 5 H 5)- + ½ H 2 Fe. Cl 2 + 2 Na+(C 5 H 5)- = [Fe(C 5 H 5)2] + 2 Na. Cl Растворители: эфир, тетрагидрофуран; инертная атмосфера
![Ареновые комплексы [Cr(C 6 H 6)2] Ареновые комплексы [Cr(C 6 H 6)2]](https://present5.com/presentation/37029447_137937197/image-76.jpg) Ареновые комплексы [Cr(C 6 H 6)2]
Ареновые комплексы [Cr(C 6 H 6)2]
![Полиядерные и кластерные комплексы [Mn 2(CO)10]: 7 x 2 + 2 x 10 + Полиядерные и кластерные комплексы [Mn 2(CO)10]: 7 x 2 + 2 x 10 +](https://present5.com/presentation/37029447_137937197/image-77.jpg) Полиядерные и кластерные комплексы [Mn 2(CO)10]: 7 x 2 + 2 x 10 + 1 x 2(Mn-Mn) = 36; 36/2 = 18 [Os 3(CO)12]: 8 x 3 + 2 x 12 + 3 x 2(Os-Os) = 54; 54/3 = 18
Полиядерные и кластерные комплексы [Mn 2(CO)10]: 7 x 2 + 2 x 10 + 1 x 2(Mn-Mn) = 36; 36/2 = 18 [Os 3(CO)12]: 8 x 3 + 2 x 12 + 3 x 2(Os-Os) = 54; 54/3 = 18
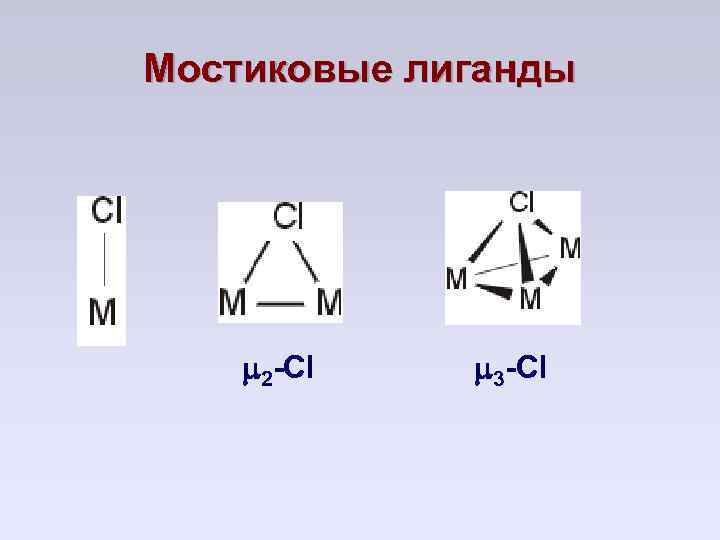 Мостиковые лиганды 2 -Cl 3 -Cl
Мостиковые лиганды 2 -Cl 3 -Cl
![Примеры кластерных комплексов [M 6 X 14]2 -: M = Mo, W; X = Примеры кластерных комплексов [M 6 X 14]2 -: M = Mo, W; X =](https://present5.com/presentation/37029447_137937197/image-79.jpg) Примеры кластерных комплексов [M 6 X 14]2 -: M = Mo, W; X = Cl, Br, I [M 6( 3 -X)8 X 6]2 - [M 6 X 18]2+: M = Nb, Ta; X = Cl, Br, I [M 6( 2 -X)12 X 6]2+
Примеры кластерных комплексов [M 6 X 14]2 -: M = Mo, W; X = Cl, Br, I [M 6( 3 -X)8 X 6]2 - [M 6 X 18]2+: M = Nb, Ta; X = Cl, Br, I [M 6( 2 -X)12 X 6]2+
![Кратные связи М-М Восстановление солей Re(VII) [Re. O 4]приводит к получению комплекса Re(III) [Re Кратные связи М-М Восстановление солей Re(VII) [Re. O 4]приводит к получению комплекса Re(III) [Re](https://present5.com/presentation/37029447_137937197/image-80.jpg) Кратные связи М-М Восстановление солей Re(VII) [Re. O 4]приводит к получению комплекса Re(III) [Re 2 Cl 8]2 - d(Re-Re) = 2, 24 Å
Кратные связи М-М Восстановление солей Re(VII) [Re. O 4]приводит к получению комплекса Re(III) [Re 2 Cl 8]2 - d(Re-Re) = 2, 24 Å
 Кратные связи М-М dz 2 dyz dx 2 y 2 Кратность связи M-M = 4: 1 + 2 + 1
Кратные связи М-М dz 2 dyz dx 2 y 2 Кратность связи M-M = 4: 1 + 2 + 1


