Кондукто- Кулоно-Вольтамперометрия.ppt
- Количество слайдов: 15
 КОНДУКТОМЕТРИЯ (КОНДУКТОМЕТРИЧЕСКИЙ АНАЛИЗ) Фридрих Кольрауш (1885 г. ) В кондуктометрии аналитическим сигналом является электропроводность. Электропроводность растворов обусловлена диссоциацией растворенного вещества и миграцией образующихся ионов под действием внешнего источника напряжения. Движущиеся ионы в поле электрического тока испытывают тормозящее действие со стороны молекул растворителя (релаксационный эффект) и со стороны противоположно заряженных ионов (электрофоретический эффект). В результате этих торможений раствор оказывает сопротивление прохождению электрического тока. Электропроводность (W) – величина, обратная сопротивлению R: W = 1/R, сименс (См = Ом -1, обратный Ом). Зависимость электропроводности от концентрации: где K – коэффициент пропорциональности; S – площадь электродов; с – концентрация ионов; λ – подвижность ионов; L – расстояние между электродами. Для данной пары электродов при L, S = const : W = K· c· λ
КОНДУКТОМЕТРИЯ (КОНДУКТОМЕТРИЧЕСКИЙ АНАЛИЗ) Фридрих Кольрауш (1885 г. ) В кондуктометрии аналитическим сигналом является электропроводность. Электропроводность растворов обусловлена диссоциацией растворенного вещества и миграцией образующихся ионов под действием внешнего источника напряжения. Движущиеся ионы в поле электрического тока испытывают тормозящее действие со стороны молекул растворителя (релаксационный эффект) и со стороны противоположно заряженных ионов (электрофоретический эффект). В результате этих торможений раствор оказывает сопротивление прохождению электрического тока. Электропроводность (W) – величина, обратная сопротивлению R: W = 1/R, сименс (См = Ом -1, обратный Ом). Зависимость электропроводности от концентрации: где K – коэффициент пропорциональности; S – площадь электродов; с – концентрация ионов; λ – подвижность ионов; L – расстояние между электродами. Для данной пары электродов при L, S = const : W = K· c· λ
 • Удельная электропроводность (æ) – это электропроводность 1 см 3 раствора, находящегося между электродами площадью 1 см 2 каждый, расположенными на расстоянии 1 см друг от друга. Размерность: См/см. • Эквивалентная электропроводность (λ) – это электропроводность 1 н раствора электролита, измеренная при расстоянии L = 1 см. Размерность: См·моль-1·см 2 (или См·г-экв-1·см 2) • Молярная электропроводность (µ) электролита определяется аналогично эквивалентной электропроводности где с – молярная концентрация эквивалента молярная концентрация). В соответствии с законом независимого движения ионов Кольрауша эквивалентная электропроводность раствора электролита при бесконечном разбавлении λ∞ (или λ 0)равна сумме предельных подвижностей катиона λ 0+ и аниона λ 0 -, т. е. их подвижностей при бесконечном разбавлении раствора: λ∞ = λ 0+ + λ 0 Предельная подвижность иона в данном растворителе при заданной температуре – экстраполированная величина. Она является константой, характеризующей электрическую подвижность данного иона. Подвижность ионов λ в растворе с конечной концентрацией не является постоянной и зависит от концентрации раствора: с ростом концентрации раствора подвижность ионов уменьшается.
• Удельная электропроводность (æ) – это электропроводность 1 см 3 раствора, находящегося между электродами площадью 1 см 2 каждый, расположенными на расстоянии 1 см друг от друга. Размерность: См/см. • Эквивалентная электропроводность (λ) – это электропроводность 1 н раствора электролита, измеренная при расстоянии L = 1 см. Размерность: См·моль-1·см 2 (или См·г-экв-1·см 2) • Молярная электропроводность (µ) электролита определяется аналогично эквивалентной электропроводности где с – молярная концентрация эквивалента молярная концентрация). В соответствии с законом независимого движения ионов Кольрауша эквивалентная электропроводность раствора электролита при бесконечном разбавлении λ∞ (или λ 0)равна сумме предельных подвижностей катиона λ 0+ и аниона λ 0 -, т. е. их подвижностей при бесконечном разбавлении раствора: λ∞ = λ 0+ + λ 0 Предельная подвижность иона в данном растворителе при заданной температуре – экстраполированная величина. Она является константой, характеризующей электрическую подвижность данного иона. Подвижность ионов λ в растворе с конечной концентрацией не является постоянной и зависит от концентрации раствора: с ростом концентрации раствора подвижность ионов уменьшается.
 Прямая кондуктометрия. Измеряют электропроводность исследуемого раствора и по градуировочному графику, построенному в тех же условиях для стандартных растворов, определяют концентрацию исследуемого раствора. Ограничения: метод неселективен, т. е. электропроводность – величина аддитивная, обусловленная присутствием всех ионов. Метод применим для анализа разбавленных растворов: с ростом концентрации электропроводность вначале растет, а при более высоких концентрациях (> 3 М) резко уменьшается. Применение: для непрерывного контроля качества пищевых продуктов, определения влажности различных материалов (бумаги, газов, зерна, текстильных материалов), определения общего солевого состава воды (речной, минеральной, дистиллированной); для определения растворимости малорастворимых электролитов; определения констант диссоциации электролитов в том числе комплексных соединений. Сочетают с другими методами, такими как потенциометрия, рефрактометрия, хроматография. Кондуктометрическое титрование. Точку стехиометричности определяют по резкому излому кривой зависимости электропроводности от объема титранта. Используют все типы реакций (нейтрализации, осаждения, комплексообразования), при которых достаточно резко изменяется электропроводность. Для получения надежных результатов следует учитывать различные факторы, влияющие на электропроводность (константа диссоциации, подвижность ионов, ионная сила раствора и т. д. ). Достоинства: возможность раздельного определения смесей кислот и оснований, титрование мутных и окрашенных растворов при точности 2 %.
Прямая кондуктометрия. Измеряют электропроводность исследуемого раствора и по градуировочному графику, построенному в тех же условиях для стандартных растворов, определяют концентрацию исследуемого раствора. Ограничения: метод неселективен, т. е. электропроводность – величина аддитивная, обусловленная присутствием всех ионов. Метод применим для анализа разбавленных растворов: с ростом концентрации электропроводность вначале растет, а при более высоких концентрациях (> 3 М) резко уменьшается. Применение: для непрерывного контроля качества пищевых продуктов, определения влажности различных материалов (бумаги, газов, зерна, текстильных материалов), определения общего солевого состава воды (речной, минеральной, дистиллированной); для определения растворимости малорастворимых электролитов; определения констант диссоциации электролитов в том числе комплексных соединений. Сочетают с другими методами, такими как потенциометрия, рефрактометрия, хроматография. Кондуктометрическое титрование. Точку стехиометричности определяют по резкому излому кривой зависимости электропроводности от объема титранта. Используют все типы реакций (нейтрализации, осаждения, комплексообразования), при которых достаточно резко изменяется электропроводность. Для получения надежных результатов следует учитывать различные факторы, влияющие на электропроводность (константа диссоциации, подвижность ионов, ионная сила раствора и т. д. ). Достоинства: возможность раздельного определения смесей кислот и оснований, титрование мутных и окрашенных растворов при точности 2 %.
 КУЛОНОМЕТРИЯ В основе метода – определение концентрации исследуемого вещества путем регистрации количества электричества, затраченного на электролиз вещества при потенциале электрода, равном потенциалу выделения анализируемого вещества. В соответствии с объединенным законом М. Фарадея масса вещества (m, г), прореагировавшего при электролизе в электрохимической ячейке, и количество электричества (Q, кулон) находятся в зависимости, выраженной уравнением где M – молярная масса вещества, г/моль; n – число электронов, участвующих в реакции; F – число Фарадея, равное 96487 Кл/моль. Количество электричества Q (в Кл), прошедшее при электролизе через электрохимическую ячейку, равно произведению электрического тока i (А) на время электролиза τ (с): Q= i · τ Если измерено количество электричества, то можно рассчитать массу. Это справедливо в том случае, когда все количество электричества, прошедшее при электролизе через ячейку, израсходовано только на электролиз данного вещества.
КУЛОНОМЕТРИЯ В основе метода – определение концентрации исследуемого вещества путем регистрации количества электричества, затраченного на электролиз вещества при потенциале электрода, равном потенциалу выделения анализируемого вещества. В соответствии с объединенным законом М. Фарадея масса вещества (m, г), прореагировавшего при электролизе в электрохимической ячейке, и количество электричества (Q, кулон) находятся в зависимости, выраженной уравнением где M – молярная масса вещества, г/моль; n – число электронов, участвующих в реакции; F – число Фарадея, равное 96487 Кл/моль. Количество электричества Q (в Кл), прошедшее при электролизе через электрохимическую ячейку, равно произведению электрического тока i (А) на время электролиза τ (с): Q= i · τ Если измерено количество электричества, то можно рассчитать массу. Это справедливо в том случае, когда все количество электричества, прошедшее при электролизе через ячейку, израсходовано только на электролиз данного вещества.
 • Кулонометрический анализ проводится как при контролируемом постоянном потенциале рабочего электрода, так и при контролируемом токе прошедшего через электролитическую ячейку. При этом важно: все электричество должно тратится на основной электрохимический процесс; точно проводить определение количества электричества (Q). • Прямая кулонометрия - при постоянном токе (редко), чаще - при контролируемом постоянном потенциале рабочего электрода (чаще всего платинового). • Кулонометрическое титрование – при постоянном токе. Роль титранта играет вещество, непрерывно образующееся на генераторном электроде при электролизе вспомогательного вещества и реагирующее с анализируемым веществом. Окончание титрования - момент, когда все определяемое вещество полностью прореагировало с генерируемым титрантом, - фиксируют либо визуально, либо с помощью инструментальных методов.
• Кулонометрический анализ проводится как при контролируемом постоянном потенциале рабочего электрода, так и при контролируемом токе прошедшего через электролитическую ячейку. При этом важно: все электричество должно тратится на основной электрохимический процесс; точно проводить определение количества электричества (Q). • Прямая кулонометрия - при постоянном токе (редко), чаще - при контролируемом постоянном потенциале рабочего электрода (чаще всего платинового). • Кулонометрическое титрование – при постоянном токе. Роль титранта играет вещество, непрерывно образующееся на генераторном электроде при электролизе вспомогательного вещества и реагирующее с анализируемым веществом. Окончание титрования - момент, когда все определяемое вещество полностью прореагировало с генерируемым титрантом, - фиксируют либо визуально, либо с помощью инструментальных методов.
 Определение массы тиосульфата натрия в растворе методом кулонометрического титрования. Генераторный сосуд Электролитический мостик Вспомогательный сосуд Анализируемый раствор Na 2 S 2 O 3 Вспомогательный реагент – KI в избытке Индикатор – крахмал Платиновый генераторный электрод (анод) Сильный электролит Индифферентный сильный электролит Платиновый катод При электролизе иодид-ионы вспомогательного реагента разряжаются на аноде: 2 I- – 2 e = I 2 При этом генерируется «титрант» I 2, вступающий в реакцию с тиосульфат-ионами: I 2 + 2 S 2 O 32 - = 2 I- + S 4 O 62 На вспомогательном платиновом катоде протекает электродная реакция: 2 Н 2 О + 2 е = Н 2↑+ 2 ОН- Конец «титрования» фиксируют по появлению синей окраски в результате образования комплекса крахмала с избыточной каплей иода. Электрическую цепь размыкают. Зная время τ (в с), затраченное на титрование и величину тока i , рассчитывают количество электричества Q ( в Кл) и массу тиосульфата в граммах, учитывая, что n=1.
Определение массы тиосульфата натрия в растворе методом кулонометрического титрования. Генераторный сосуд Электролитический мостик Вспомогательный сосуд Анализируемый раствор Na 2 S 2 O 3 Вспомогательный реагент – KI в избытке Индикатор – крахмал Платиновый генераторный электрод (анод) Сильный электролит Индифферентный сильный электролит Платиновый катод При электролизе иодид-ионы вспомогательного реагента разряжаются на аноде: 2 I- – 2 e = I 2 При этом генерируется «титрант» I 2, вступающий в реакцию с тиосульфат-ионами: I 2 + 2 S 2 O 32 - = 2 I- + S 4 O 62 На вспомогательном платиновом катоде протекает электродная реакция: 2 Н 2 О + 2 е = Н 2↑+ 2 ОН- Конец «титрования» фиксируют по появлению синей окраски в результате образования комплекса крахмала с избыточной каплей иода. Электрическую цепь размыкают. Зная время τ (в с), затраченное на титрование и величину тока i , рассчитывают количество электричества Q ( в Кл) и массу тиосульфата в граммах, учитывая, что n=1.
 ВОЛЬТАМПЕРОМЕТРИЯ Ø Вольтамперометрические методы анализа основаны на изучении зависимости силы тока от налагаемого на электролитическую ячейку внешнего напряжения. Ø В вольтамперометрии используют два электрода: Ø Рабочий поляризуемый электрод с малой поверхностью (микроэлектрод) – индикаторный электрод, на котором происходит электровосстановление или электроокисление. Ø Неполяризуемый электрод сравнения, потенциал которого остается постоянным.
ВОЛЬТАМПЕРОМЕТРИЯ Ø Вольтамперометрические методы анализа основаны на изучении зависимости силы тока от налагаемого на электролитическую ячейку внешнего напряжения. Ø В вольтамперометрии используют два электрода: Ø Рабочий поляризуемый электрод с малой поверхностью (микроэлектрод) – индикаторный электрод, на котором происходит электровосстановление или электроокисление. Ø Неполяризуемый электрод сравнения, потенциал которого остается постоянным.
 Полярография 1920 -е гг. - Я. Гейровский – 1959 г. Нобелевская премия • В полярографии осуществляют регистрацию тока как функции линейно-меняющегося потенциала, наложенного на электрохимическую ячейку специальной конструкции. Графическое изображение этой зависимости представляет собой вольтамперную кривую, называемую полярограммой • Полярографическая ячейка состоит из: индикаторного ртутно -капающего электрода (катода), электрода сравнения (анода) и анализируемого раствора (деполяризатора). • Для подавления миграционного тока в раствор вводят индифферентный (не принимающий участие в электродной реакции) фоновый электролит, катионы которого экранируют электрод, уменьшая движущую силу миграции под действием электрического поля практически до нуля.
Полярография 1920 -е гг. - Я. Гейровский – 1959 г. Нобелевская премия • В полярографии осуществляют регистрацию тока как функции линейно-меняющегося потенциала, наложенного на электрохимическую ячейку специальной конструкции. Графическое изображение этой зависимости представляет собой вольтамперную кривую, называемую полярограммой • Полярографическая ячейка состоит из: индикаторного ртутно -капающего электрода (катода), электрода сравнения (анода) и анализируемого раствора (деполяризатора). • Для подавления миграционного тока в раствор вводят индифферентный (не принимающий участие в электродной реакции) фоновый электролит, катионы которого экранируют электрод, уменьшая движущую силу миграции под действием электрического поля практически до нуля.
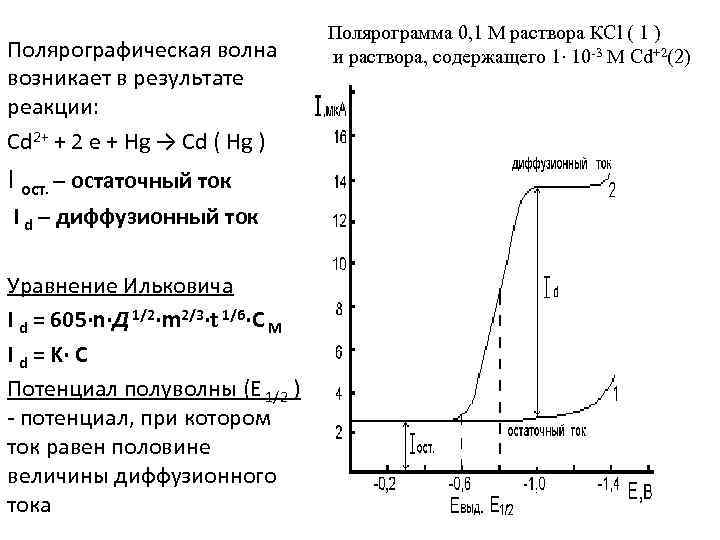 Полярографическая волна возникает в результате реакции: Cd 2+ + 2 e + Hg → Сd ( Hg ) I ост. – остаточный ток I d – диффузионный ток Уравнение Ильковича I d = 605·n·Д 1/2·m 2/3·t 1/6·C M I d = K· C Потенциал полуволны (Е 1/2 ) - потенциал, при котором ток равен половине величины диффузионного тока Полярограмма 0, 1 М раствора КСl ( 1 ) и раствора, содержащего 1· 10 -3 М Сd+2(2)
Полярографическая волна возникает в результате реакции: Cd 2+ + 2 e + Hg → Сd ( Hg ) I ост. – остаточный ток I d – диффузионный ток Уравнение Ильковича I d = 605·n·Д 1/2·m 2/3·t 1/6·C M I d = K· C Потенциал полуволны (Е 1/2 ) - потенциал, при котором ток равен половине величины диффузионного тока Полярограмма 0, 1 М раствора КСl ( 1 ) и раствора, содержащего 1· 10 -3 М Сd+2(2)
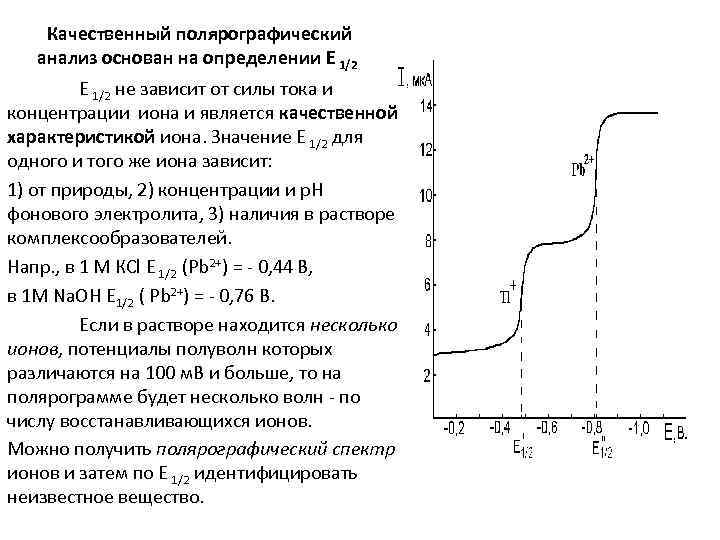 Качественный полярографический анализ основан на определении Е 1/2 не зависит от силы тока и концентрации иона и является качественной характеристикой иона. Значение Е 1/2 для одного и того же иона зависит: 1) от природы, 2) концентрации и р. Н фонового электролита, 3) наличия в растворе комплексообразователей. Напр. , в 1 М КСl E 1/2 (Pb 2+) = - 0, 44 B, в 1 М Na. OH E 1/2 ( Pb 2+) = - 0, 76 В. Если в растворе находится несколько ионов, потенциалы полуволн которых различаются на 100 м. B и больше, то на полярограмме будет несколько волн - по числу восстанавливающихся ионов. Можно получить полярографический спектр ионов и затем по Е 1/2 идентифицировать неизвестное вещество.
Качественный полярографический анализ основан на определении Е 1/2 не зависит от силы тока и концентрации иона и является качественной характеристикой иона. Значение Е 1/2 для одного и того же иона зависит: 1) от природы, 2) концентрации и р. Н фонового электролита, 3) наличия в растворе комплексообразователей. Напр. , в 1 М КСl E 1/2 (Pb 2+) = - 0, 44 B, в 1 М Na. OH E 1/2 ( Pb 2+) = - 0, 76 В. Если в растворе находится несколько ионов, потенциалы полуволн которых различаются на 100 м. B и больше, то на полярограмме будет несколько волн - по числу восстанавливающихся ионов. Можно получить полярографический спектр ионов и затем по Е 1/2 идентифицировать неизвестное вещество.
 Количественный анализ в полярографии основан на уравнении Ильковича • Градуировочный график строят по данным полярографирования нескольких стандартных растворов. На оси ординат откладывают величину I d (высота волны), по оси абсцисс - концентрацию анализируемого вещества. • Метод стандартных растворов - в строго одинаковых условиях снимают полярограммы стандартного и анализируемого растворов и рассчитывают неизвестную концентрацию Сx по уравнению : Сст - концентрация стандартного раствора; hx , hcт - высоты волн анализируемого и стандартного растворов. • Метод добавок. Сначала регистрируется полярограмма исследуемого раствора, затем к раствору добавляется известное количество стандартного раствора Сст и снова регистрируется полярограмма. Концентрация исследуемого раствора Сx находится по уравнению: hx - высота волны исследуемого раствора; hx + ст - высота волны исследуемого раствора с добавкой стандартного вещества.
Количественный анализ в полярографии основан на уравнении Ильковича • Градуировочный график строят по данным полярографирования нескольких стандартных растворов. На оси ординат откладывают величину I d (высота волны), по оси абсцисс - концентрацию анализируемого вещества. • Метод стандартных растворов - в строго одинаковых условиях снимают полярограммы стандартного и анализируемого растворов и рассчитывают неизвестную концентрацию Сx по уравнению : Сст - концентрация стандартного раствора; hx , hcт - высоты волн анализируемого и стандартного растворов. • Метод добавок. Сначала регистрируется полярограмма исследуемого раствора, затем к раствору добавляется известное количество стандартного раствора Сст и снова регистрируется полярограмма. Концентрация исследуемого раствора Сx находится по уравнению: hx - высота волны исследуемого раствора; hx + ст - высота волны исследуемого раствора с добавкой стандартного вещества.
 Применение метода полярографии • Определение катионов металлов : Cu 2+, Cd 2+, Pb 2+, Zn 2+, Tl+, Fe 3+ и др. ; анионов : Br -, IO 3 -, Cr 2 O 72 -, VO 3 -, NO 2 - и т. д. ; органических соединений, содержащих функциональные группы (карбонильные, перекисные, нитро-, нитрозо, азогруппы), галогенсодержащих органических соединений, гидрохинонов, меркаптанов и др. • Диапазон концентраций: 10 -6 - 10 -3 М (наиболее - 10 -4 - 10 -3 М). • Погрешность полярографического анализа составляет 2 %. • Определение металлов в рудах, концентратах, сплавах и иных природных и технических объектах. • Существенное практическое значение имеет определение Cr. O 42 -, IO 3 -, Mo. O 42 - - ионов, а также многих органических соединений. • Широко используется полярографический метод для анализа биологических материалов: крови, сыворотки и т. д.
Применение метода полярографии • Определение катионов металлов : Cu 2+, Cd 2+, Pb 2+, Zn 2+, Tl+, Fe 3+ и др. ; анионов : Br -, IO 3 -, Cr 2 O 72 -, VO 3 -, NO 2 - и т. д. ; органических соединений, содержащих функциональные группы (карбонильные, перекисные, нитро-, нитрозо, азогруппы), галогенсодержащих органических соединений, гидрохинонов, меркаптанов и др. • Диапазон концентраций: 10 -6 - 10 -3 М (наиболее - 10 -4 - 10 -3 М). • Погрешность полярографического анализа составляет 2 %. • Определение металлов в рудах, концентратах, сплавах и иных природных и технических объектах. • Существенное практическое значение имеет определение Cr. O 42 -, IO 3 -, Mo. O 42 - - ионов, а также многих органических соединений. • Широко используется полярографический метод для анализа биологических материалов: крови, сыворотки и т. д.
 АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ • В процессе титрования после прибавления отдельных порций реактива регистрируют величину диффузионного тока при постоянном потенциале индикаторного электрода и строят кривую амперометрического титрования в координатах: сила тока - объем титранта ( Id - V ). По графику находят ТС. • В качестве индикаторных электродов в амперометрическом титровании применяют платиновые, графитовые и др. твердые электроды • Необходимо различать электрохимическую реакцию, протекающую на границе раздела электрод-раствор, и химическую реакцию, протекающую в растворе между определяемым веществом и титрантом.
АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ • В процессе титрования после прибавления отдельных порций реактива регистрируют величину диффузионного тока при постоянном потенциале индикаторного электрода и строят кривую амперометрического титрования в координатах: сила тока - объем титранта ( Id - V ). По графику находят ТС. • В качестве индикаторных электродов в амперометрическом титровании применяют платиновые, графитовые и др. твердые электроды • Необходимо различать электрохимическую реакцию, протекающую на границе раздела электрод-раствор, и химическую реакцию, протекающую в растворе между определяемым веществом и титрантом.
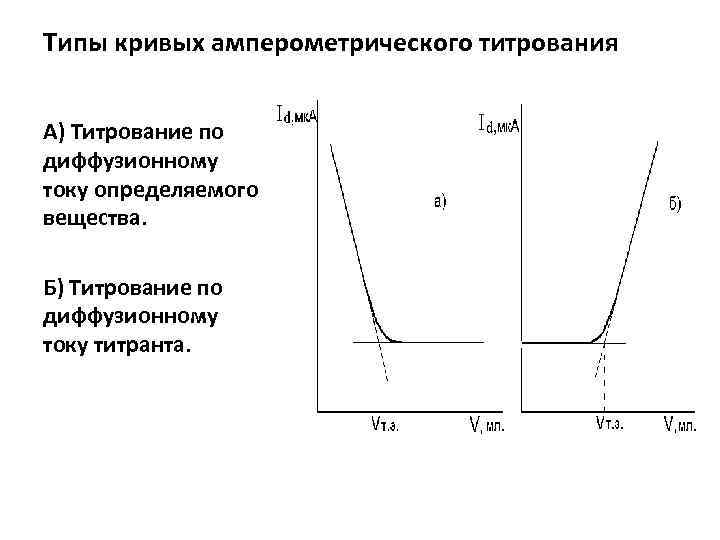 Типы кривых амперометрического титрования А) Титрование по диффузионному току определяемого вещества. Б) Титрование по диффузионному току титранта.
Типы кривых амперометрического титрования А) Титрование по диффузионному току определяемого вещества. Б) Титрование по диффузионному току титранта.
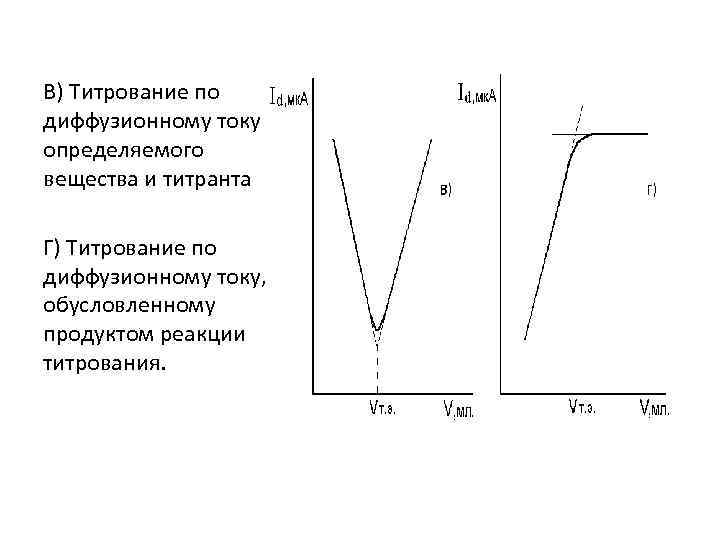 В) Титрование по диффузионному току определяемого вещества и титранта Г) Титрование по диффузионному току, обусловленному продуктом реакции титрования.
В) Титрование по диффузионному току определяемого вещества и титранта Г) Титрование по диффузионному току, обусловленному продуктом реакции титрования.


