кондуктометрия.ppt
- Количество слайдов: 56
 КОНДУКТОМЕТРИЯ И ВЫСОКОЧАСТОТНОЕ ТИТРОВАНИЕ
КОНДУКТОМЕТРИЯ И ВЫСОКОЧАСТОТНОЕ ТИТРОВАНИЕ
 • Кондуктометрия (от англ. conductivity – электропроводность и греч. metreo измеряю) - совокупность электрохимических методов анализа, основанных на измерении электропроводности в жидких электролитах, которая пропорциональна их концентрации.
• Кондуктометрия (от англ. conductivity – электропроводность и греч. metreo измеряю) - совокупность электрохимических методов анализа, основанных на измерении электропроводности в жидких электролитах, которая пропорциональна их концентрации.
 2 проводника 1 рода помещают в раствор – проводник второго рода, сила тока будет прямо пропорциональна напряжению и обратно пропорциональна сопротивлению раствора, находящегося между электродами I = U/R R= ρ l / S æ = 1 / ρ - зависит от геометрических размеров и концентрации вещества
2 проводника 1 рода помещают в раствор – проводник второго рода, сила тока будет прямо пропорциональна напряжению и обратно пропорциональна сопротивлению раствора, находящегося между электродами I = U/R R= ρ l / S æ = 1 / ρ - зависит от геометрических размеров и концентрации вещества
 Задачи, решаемые методом: • установление физических и физикохимических постоянных вещества, растворов, исследовнаие кинетики физико-химических процессов; • прямая кондуктометрия, ; • косвенная кондуктометрия (титрование), включая автоматические методы титрования, .
Задачи, решаемые методом: • установление физических и физикохимических постоянных вещества, растворов, исследовнаие кинетики физико-химических процессов; • прямая кондуктометрия, ; • косвенная кондуктометрия (титрование), включая автоматические методы титрования, .
 • Удельная электропроводность (æ) электропроводность 1 м 3 раствора, заключенного между плоскими электродами площадью 1 м 2 на расстоянии 1 м друг от друга. Т. е. это электропроводность электрического проводника площадью сечения 1 м 2 и длиной 1 м. Единица измерения – См/м, Ом-1 м-1
• Удельная электропроводность (æ) электропроводность 1 м 3 раствора, заключенного между плоскими электродами площадью 1 м 2 на расстоянии 1 м друг от друга. Т. е. это электропроводность электрического проводника площадью сечения 1 м 2 и длиной 1 м. Единица измерения – См/м, Ом-1 м-1
 • Эквивалентная электропроводность (λ, Ом-1 • см 2 /моль) - удельная электропроводность раствора, содержащего 1 моль-экв вещества, находящегося между двумя параллельными электродами, рассотяние между которыми 1 см. Значения æ и λ взаимосвязаны формулой: λ = 1000æ/с , где с – концентрация раствора, моль/дм 3.
• Эквивалентная электропроводность (λ, Ом-1 • см 2 /моль) - удельная электропроводность раствора, содержащего 1 моль-экв вещества, находящегося между двумя параллельными электродами, рассотяние между которыми 1 см. Значения æ и λ взаимосвязаны формулой: λ = 1000æ/с , где с – концентрация раствора, моль/дм 3.
 Эквивалентная электропроводность при бесконечно большом разбавлении, т. е. когда концентрация становится бесконечно малой, стремится к некоторому постоянному значению, не зависящему от изменения концентрации электролита, но зависящему только от температуры и природы электролита. Она называется предельной электропроводностью и обозначается λ∞. В разбавленных растворах электропроводность прямо пропорциональна количеству заряженных частиц (ионов).
Эквивалентная электропроводность при бесконечно большом разбавлении, т. е. когда концентрация становится бесконечно малой, стремится к некоторому постоянному значению, не зависящему от изменения концентрации электролита, но зависящему только от температуры и природы электролита. Она называется предельной электропроводностью и обозначается λ∞. В разбавленных растворах электропроводность прямо пропорциональна количеству заряженных частиц (ионов).
 • При малых концентрациях зависимость эквивалентной электропроводности сильного электролита от концентрации выражается формулой Кольрауша (носит эмпирический характер): • где α – коэффициент, зависящий от природы растворов.
• При малых концентрациях зависимость эквивалентной электропроводности сильного электролита от концентрации выражается формулой Кольрауша (носит эмпирический характер): • где α – коэффициент, зависящий от природы растворов.
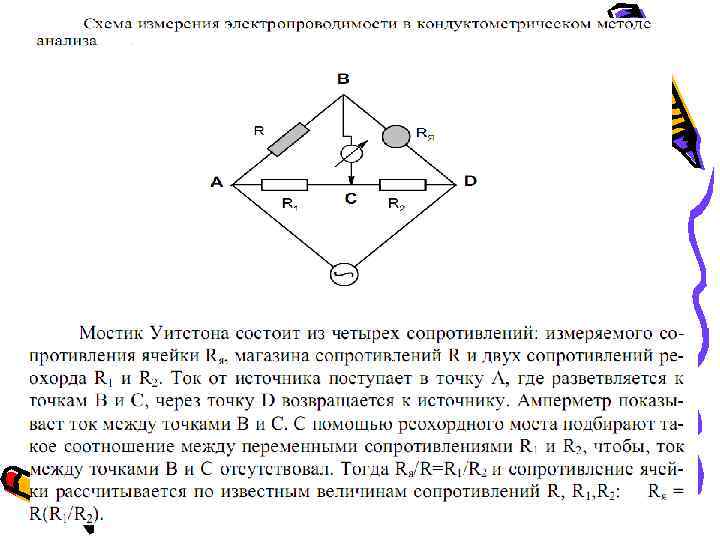
 Фридрих Вильгельм Георг Кольрауш (нем. Friedrich Wilhelm Georg Kohlrausch 14 октября 1840, Ринтельн, Нижняя Саксония — 17 января 1910, Марбург) — немецкий физик и электротехник. • В 1878— 1883 был ассистентом профессора Кундта в Страсбурге, затем там же читал лекции по теоретической физике. К этому времени относятся и некоторые его теоретические работы по оптике, акустике и магнетизму. Позже Кольрауш обратил своё внимание на техническое применение электричества и в 1884 занял только что основанную кафедру электротехники в технической школе в Ганновере; с 1892 он был её ректором. После смерти Г. Гельмгольца — директор Физико-технического института в Берлине (1895— 1905). • Научные работы Кольрауша относились, главным образом, к области электричества, магнетизма, оптики; занимался также электротехническими измерениями и теорией конструкции динамо-машин. Разработал метод измерения электрического тока в абсолютных единицах и метод измерения электрического сопротивления электролитов (мостик Кольрауша), методы и приборы для регистрации изменений магнитного поля Земли. • Выполнил ряд работ в области физикохимии растворов. Предложил способ определения электрического сопротивления электролитов, установил закон независимости движения ионов в электролитах (Закон Кольрауша).
Фридрих Вильгельм Георг Кольрауш (нем. Friedrich Wilhelm Georg Kohlrausch 14 октября 1840, Ринтельн, Нижняя Саксония — 17 января 1910, Марбург) — немецкий физик и электротехник. • В 1878— 1883 был ассистентом профессора Кундта в Страсбурге, затем там же читал лекции по теоретической физике. К этому времени относятся и некоторые его теоретические работы по оптике, акустике и магнетизму. Позже Кольрауш обратил своё внимание на техническое применение электричества и в 1884 занял только что основанную кафедру электротехники в технической школе в Ганновере; с 1892 он был её ректором. После смерти Г. Гельмгольца — директор Физико-технического института в Берлине (1895— 1905). • Научные работы Кольрауша относились, главным образом, к области электричества, магнетизма, оптики; занимался также электротехническими измерениями и теорией конструкции динамо-машин. Разработал метод измерения электрического тока в абсолютных единицах и метод измерения электрического сопротивления электролитов (мостик Кольрауша), методы и приборы для регистрации изменений магнитного поля Земли. • Выполнил ряд работ в области физикохимии растворов. Предложил способ определения электрического сопротивления электролитов, установил закон независимости движения ионов в электролитах (Закон Кольрауша).
 Предельная эквивалентная электропроводность λ∞ может быть экспериментально определена интерполяцией зависимости λ – ƒ(С). При бесконечном разбавлении λ∞ раствора электролита равна сумме эквивалентных электропроводностей (подвижностей) катиона и аниона, входящих в состав электролита: λ∞ = λ - + λ+ Пользуясь этим определением, легко предсказать электропроводность любого раствора с концентрацией С: æ = (λ- + λ+) С Электропроводность раствора, состоящего из смеси различных ионов, рассчитывается по формуле: æ = ∑λi • Сi.
Предельная эквивалентная электропроводность λ∞ может быть экспериментально определена интерполяцией зависимости λ – ƒ(С). При бесконечном разбавлении λ∞ раствора электролита равна сумме эквивалентных электропроводностей (подвижностей) катиона и аниона, входящих в состав электролита: λ∞ = λ - + λ+ Пользуясь этим определением, легко предсказать электропроводность любого раствора с концентрацией С: æ = (λ- + λ+) С Электропроводность раствора, состоящего из смеси различных ионов, рассчитывается по формуле: æ = ∑λi • Сi.
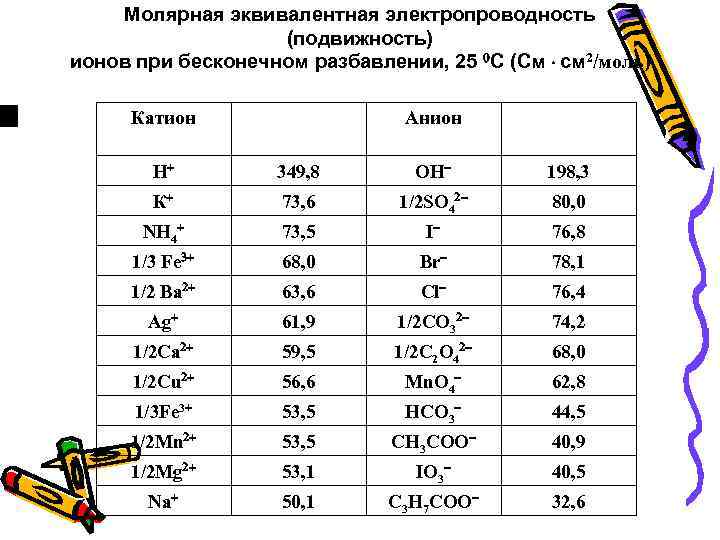 Молярная эквивалентная электропроводность (подвижность) ионов при бесконечном разбавлении, 25 С (См см 2/моль) Катион Анион Н 349, 8 OH 198, 3 К 73, 6 1/2 SO 4 80, 0 NH 4 73, 5 I 76, 8 1/3 Fe 68, 0 Br 78, 1 1/2 Вa 63, 6 Cl 76, 4 Ag 61, 9 1/2 CO 3 74, 2 1/2 Ca 59, 5 1/2 C 2 O 4 68, 0 1/2 Cu 56, 6 Mn. O 4 62, 8 1/3 Fe 3 53, 5 HCO 3 44, 5 1/2 Mn 53, 5 CH 3 COO 40, 9 1/2 Mg 53, 1 IO 3 40, 5 Na 50, 1 C 3 H 7 COO 32, 6
Молярная эквивалентная электропроводность (подвижность) ионов при бесконечном разбавлении, 25 С (См см 2/моль) Катион Анион Н 349, 8 OH 198, 3 К 73, 6 1/2 SO 4 80, 0 NH 4 73, 5 I 76, 8 1/3 Fe 68, 0 Br 78, 1 1/2 Вa 63, 6 Cl 76, 4 Ag 61, 9 1/2 CO 3 74, 2 1/2 Ca 59, 5 1/2 C 2 O 4 68, 0 1/2 Cu 56, 6 Mn. O 4 62, 8 1/3 Fe 3 53, 5 HCO 3 44, 5 1/2 Mn 53, 5 CH 3 COO 40, 9 1/2 Mg 53, 1 IO 3 40, 5 Na 50, 1 C 3 H 7 COO 32, 6
 • Природа электролита и растворителя оказывают большое влияние на подвижность ионов. Эквивалентные электропроводности подавляющего числа ионов близки друг к другу по величине. • Исключение - ионы Н+ , ОН-, электропроводности которых аномально высоки
• Природа электролита и растворителя оказывают большое влияние на подвижность ионов. Эквивалентные электропроводности подавляющего числа ионов близки друг к другу по величине. • Исключение - ионы Н+ , ОН-, электропроводности которых аномально высоки

 Прямая кондуктометрия Основана на зависимости электропроводности от концентрации ионов. Используя стандартные растворы, строят графики зависимости λ = ƒ(C), по которым затем находят концентрацию по измеренной электропроводности. Однако, электропроводность – величина аддитивная, т. е. равна сумме вкладов всех электропроводящих компонентов системы. Метод используют в аналитических лабораториях лишь для определения некоторых компонентов, например, SO 42 -. Чаще измерение электропроводности проводят для характеристики общего солесодержания растворов, а также для контроля качества дистиллированной воды, для которой нормой, установленной ГОСТом, является электропроводность не выше 0, 005 м. См/см.
Прямая кондуктометрия Основана на зависимости электропроводности от концентрации ионов. Используя стандартные растворы, строят графики зависимости λ = ƒ(C), по которым затем находят концентрацию по измеренной электропроводности. Однако, электропроводность – величина аддитивная, т. е. равна сумме вкладов всех электропроводящих компонентов системы. Метод используют в аналитических лабораториях лишь для определения некоторых компонентов, например, SO 42 -. Чаще измерение электропроводности проводят для характеристики общего солесодержания растворов, а также для контроля качества дистиллированной воды, для которой нормой, установленной ГОСТом, является электропроводность не выше 0, 005 м. См/см.

 Кондуктометрическое титрование • метод анализа, в котором точку эквивалентности устанавливают по резкому изменению электропроводности при титровании. Кондуктометрическое титрование обладает большими аналитическими возможностями. • В титровании используются реакции нейтрализации, осаждения, реже окисления – восстановления, комплексообразования.
Кондуктометрическое титрование • метод анализа, в котором точку эквивалентности устанавливают по резкому изменению электропроводности при титровании. Кондуктометрическое титрование обладает большими аналитическими возможностями. • В титровании используются реакции нейтрализации, осаждения, реже окисления – восстановления, комплексообразования.
 • Изменение электропроводности при титровании изображают графически в виде кондуктометрических кривых. • Вид кривой титрования зависит от природы взаимодействующих электролитов и подвижности ионов в растворе.
• Изменение электропроводности при титровании изображают графически в виде кондуктометрических кривых. • Вид кривой титрования зависит от природы взаимодействующих электролитов и подвижности ионов в растворе.
 Титрование слабой кислоты
Титрование слабой кислоты
 Титрование смеси кислот
Титрование смеси кислот
 Условия выполнения анализа
Условия выполнения анализа


 Высокочастотная неконтактная кондуктометрия В растворах, помещенных в электромагнитное поле, согласно теории Максвелла, протекает два тока - ток проводимости и ток смещения. Первый из них, в основном вызывается перемещением ионов в направлении поля, а второй - их обратимым колебательным движением. Возможность использования этих двух видов тока для анализа веществ обусловила возникновение двух самостоятельных видов высокочастотного титрования: • кондуктометрическое высокочастотное титрование, ВЧТ, • диэлькометрическое титрование.
Высокочастотная неконтактная кондуктометрия В растворах, помещенных в электромагнитное поле, согласно теории Максвелла, протекает два тока - ток проводимости и ток смещения. Первый из них, в основном вызывается перемещением ионов в направлении поля, а второй - их обратимым колебательным движением. Возможность использования этих двух видов тока для анализа веществ обусловила возникновение двух самостоятельных видов высокочастотного титрования: • кондуктометрическое высокочастотное титрование, ВЧТ, • диэлькометрическое титрование.
 • Неконтактные методы разработаны с целью устранения поляризационных явлений на электродах, являющихся следствием протекания электрического тока через поверхность раздела электрод-раствор. • Они применяются для анализа концентрированных растворов и для измерений в агрессивных и летучих средах, а также при работе с окрашенными и темными растворами, при образовании осадков и титровании взвесей и эмульсий. • Метод удобен в тех случаях, когда реакцию следует проводить в герметичной аппаратуре или в таких условиях, когда контакт электродов с раствором недопустим вследствие, например, возможности катализа и других осложняющих обстоятельств.
• Неконтактные методы разработаны с целью устранения поляризационных явлений на электродах, являющихся следствием протекания электрического тока через поверхность раздела электрод-раствор. • Они применяются для анализа концентрированных растворов и для измерений в агрессивных и летучих средах, а также при работе с окрашенными и темными растворами, при образовании осадков и титровании взвесей и эмульсий. • Метод удобен в тех случаях, когда реакцию следует проводить в герметичной аппаратуре или в таких условиях, когда контакт электродов с раствором недопустим вследствие, например, возможности катализа и других осложняющих обстоятельств.
 Преимущества неконтактных методов : • отсутствие возможности взаимодействия между исследуемой системой и материалом электродов и невозможность механического загрязнения электродов (это особенно важно в случае проточной ячейки применении метода для контроля производственных процессов); • возможность исследования процессов, происходящих в системе, находящейся в запаянной ампуле при высокой или низкой температуре, при исследовании фазовых переходов и т. д.
Преимущества неконтактных методов : • отсутствие возможности взаимодействия между исследуемой системой и материалом электродов и невозможность механического загрязнения электродов (это особенно важно в случае проточной ячейки применении метода для контроля производственных процессов); • возможность исследования процессов, происходящих в системе, находящейся в запаянной ампуле при высокой или низкой температуре, при исследовании фазовых переходов и т. д.
 Недостаток неконтактных методов • Нет возможности производить непосредственные отсчет величин измеренной электропроводности, поэтому часто применяются только для определения относительных изменений величины электропроводности.
Недостаток неконтактных методов • Нет возможности производить непосредственные отсчет величин измеренной электропроводности, поэтому часто применяются только для определения относительных изменений величины электропроводности.
 • При высокочастотном титровании электродов нет вообще, и этим полностью снимается проблема учета или уменьшения электродной поляризации. Ячейку с титруемым раствором и стеклянной мешалкой помещают либо внутрь катушкиу индуктивности, либо в конденсатор колебательного контура высокочастотного генератора и в процессе титрования записывают показания прибора
• При высокочастотном титровании электродов нет вообще, и этим полностью снимается проблема учета или уменьшения электродной поляризации. Ячейку с титруемым раствором и стеклянной мешалкой помещают либо внутрь катушкиу индуктивности, либо в конденсатор колебательного контура высокочастотного генератора и в процессе титрования записывают показания прибора
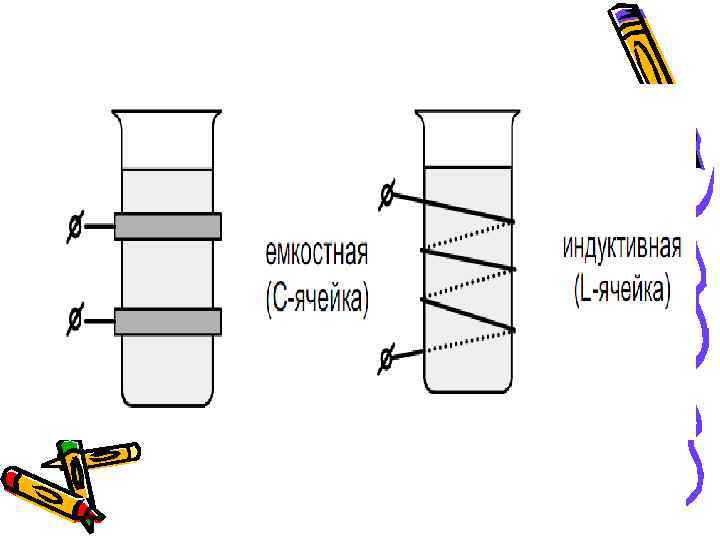
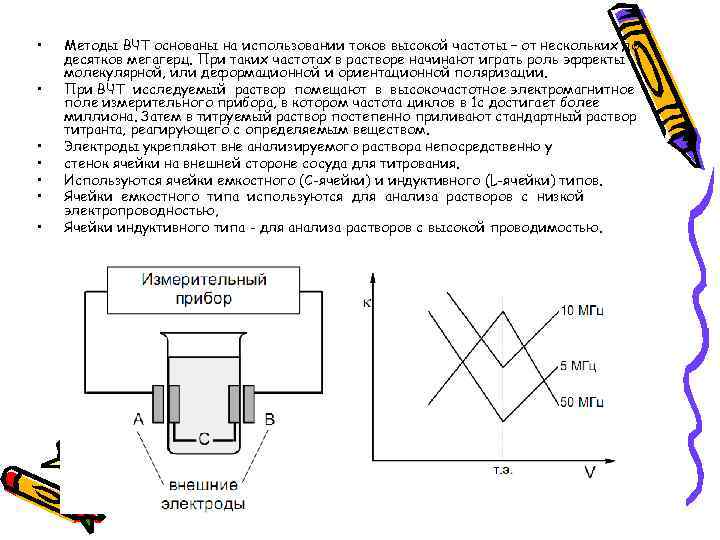 • • Методы ВЧТ основаны на использовании токов высокой частоты – от нескольких до десятков мегагерц. При таких частотах в растворе начинают играть роль эффекты молекулярной, или деформационной и ориентационной поляризации. При ВЧТ исследуемый раствор помещают в высокочастотное электромагнитное поле измерительного прибора, в котором частота циклов в 1 с достигает более миллиона. Затем в титруемый раствор постепенно приливают стандартный раствор титранта, реагирующего с определяемым веществом. Электроды укрепляют вне анализируемого раствора непосредственно у стенок ячейки на внешней стороне сосуда для титрования. Используются ячейки емкостного (С-ячейки) и индуктивного (L-ячейки) типов. Ячейки емкостного типа используются для анализа растворов с низкой электропроводностью, Ячейки индуктивного типа - для анализа растворов с высокой проводимостью.
• • Методы ВЧТ основаны на использовании токов высокой частоты – от нескольких до десятков мегагерц. При таких частотах в растворе начинают играть роль эффекты молекулярной, или деформационной и ориентационной поляризации. При ВЧТ исследуемый раствор помещают в высокочастотное электромагнитное поле измерительного прибора, в котором частота циклов в 1 с достигает более миллиона. Затем в титруемый раствор постепенно приливают стандартный раствор титранта, реагирующего с определяемым веществом. Электроды укрепляют вне анализируемого раствора непосредственно у стенок ячейки на внешней стороне сосуда для титрования. Используются ячейки емкостного (С-ячейки) и индуктивного (L-ячейки) типов. Ячейки емкостного типа используются для анализа растворов с низкой электропроводностью, Ячейки индуктивного типа - для анализа растворов с высокой проводимостью.
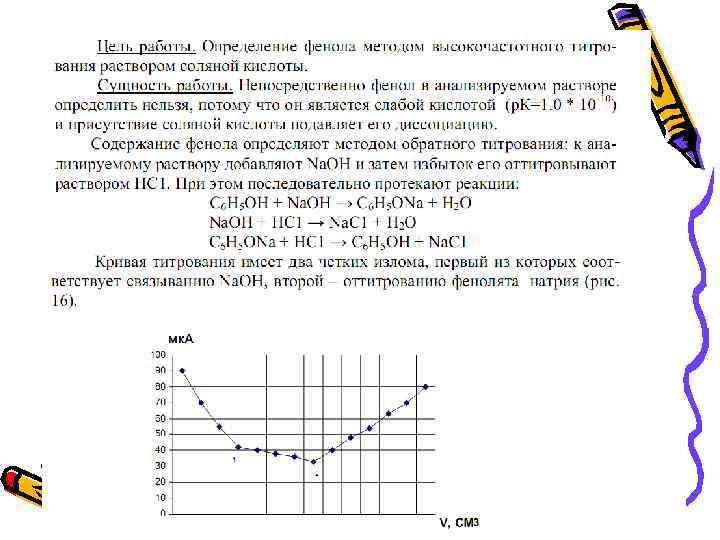
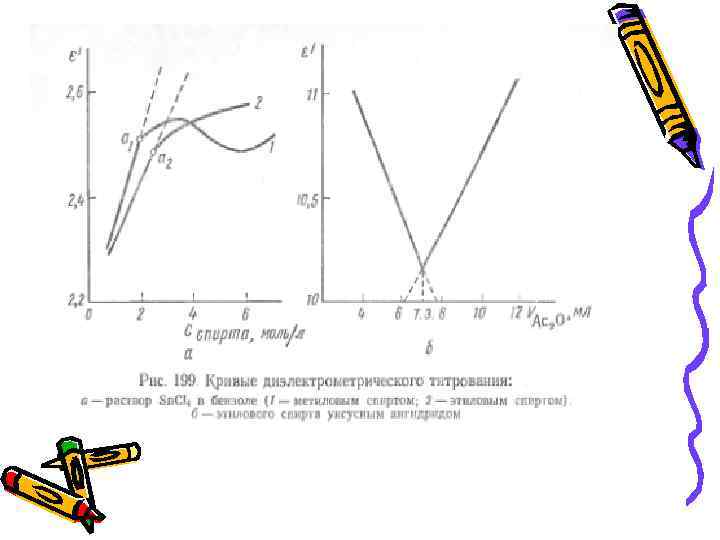
 Диэлектрометрия • Диэлектрометрия объединяет методы анализа, основанные на измерении диэлектрической проницаемости вещества, обусловленной ориентацией в электрическом поле частиц (молекул, ионов), обладающих дипольным моментом. Методы диэлектрометрии применяют для контроля чистоты диэлектриков, например для определения малых количеств влаги. Диэлектрометрическое титрование используют для анализа растворов.
Диэлектрометрия • Диэлектрометрия объединяет методы анализа, основанные на измерении диэлектрической проницаемости вещества, обусловленной ориентацией в электрическом поле частиц (молекул, ионов), обладающих дипольным моментом. Методы диэлектрометрии применяют для контроля чистоты диэлектриков, например для определения малых количеств влаги. Диэлектрометрическое титрование используют для анализа растворов.
 история • Своми корнями диэлектрометрия уходит в конец 19 века к работам Фарадея, который обнаружил, что отношение емкостей заполненного и пустого конденсатора является постоянной характеристикой заполняющего конденсатор вещества, которая получила название диэлектрической проницаемости ( ε), а само вещество - название диэлектрика
история • Своми корнями диэлектрометрия уходит в конец 19 века к работам Фарадея, который обнаружил, что отношение емкостей заполненного и пустого конденсатора является постоянной характеристикой заполняющего конденсатор вещества, которая получила название диэлектрической проницаемости ( ε), а само вещество - название диэлектрика
 ФАРАДЕЙ, МАЙКЛ (Faraday, Michael) (1791– 1867), английский физик, основоположник учения об электромагнетизме. Родился 22 сентября 1791 в предместье Лондона в семье кузнеца. Смог получить лишь начальное образование. С 12 лет работал разносчиком газет, затем был учеником в переплетной мастерской. Получив право работать по найму, продолжал совершенствоваться в своем ремесле и одновременно занимался самообразованием, читая книги по химии и электричеству. В 1813 один из заказчиков подарил Фарадею пригласительные билеты на лекции Г. Дэви в Королевском институте. Эти лекции сыграли большую роль в решении Фарадея посвятить себя науке. Он обратился к Дэви с просьбой принять его на работу и получил место ассистента в Королевском институте. В 1813– 1815, путешествуя вместе с Дэви по Европе, Фарадей посетил лаборатории ряда стран. Помогал Дэви в химических экспериментах, затем начал самостоятельные исследования по химии. Его наивысшие достижения в этой области – ожижение газов и получение бензола. В 1821 впервые осуществил вращение магнита вокруг проводника с током и проводника с током вокруг магнита, создав первую модель электродвигателя. В течение последующих 10 лет занимался исследованием связи между электрическими и магнитными явлениями и в 1831 открыл электромагнитную индукцию, лежащую в основе работы всех электрогенераторов постоянного и переменного тока.
ФАРАДЕЙ, МАЙКЛ (Faraday, Michael) (1791– 1867), английский физик, основоположник учения об электромагнетизме. Родился 22 сентября 1791 в предместье Лондона в семье кузнеца. Смог получить лишь начальное образование. С 12 лет работал разносчиком газет, затем был учеником в переплетной мастерской. Получив право работать по найму, продолжал совершенствоваться в своем ремесле и одновременно занимался самообразованием, читая книги по химии и электричеству. В 1813 один из заказчиков подарил Фарадею пригласительные билеты на лекции Г. Дэви в Королевском институте. Эти лекции сыграли большую роль в решении Фарадея посвятить себя науке. Он обратился к Дэви с просьбой принять его на работу и получил место ассистента в Королевском институте. В 1813– 1815, путешествуя вместе с Дэви по Европе, Фарадей посетил лаборатории ряда стран. Помогал Дэви в химических экспериментах, затем начал самостоятельные исследования по химии. Его наивысшие достижения в этой области – ожижение газов и получение бензола. В 1821 впервые осуществил вращение магнита вокруг проводника с током и проводника с током вокруг магнита, создав первую модель электродвигателя. В течение последующих 10 лет занимался исследованием связи между электрическими и магнитными явлениями и в 1831 открыл электромагнитную индукцию, лежащую в основе работы всех электрогенераторов постоянного и переменного тока.
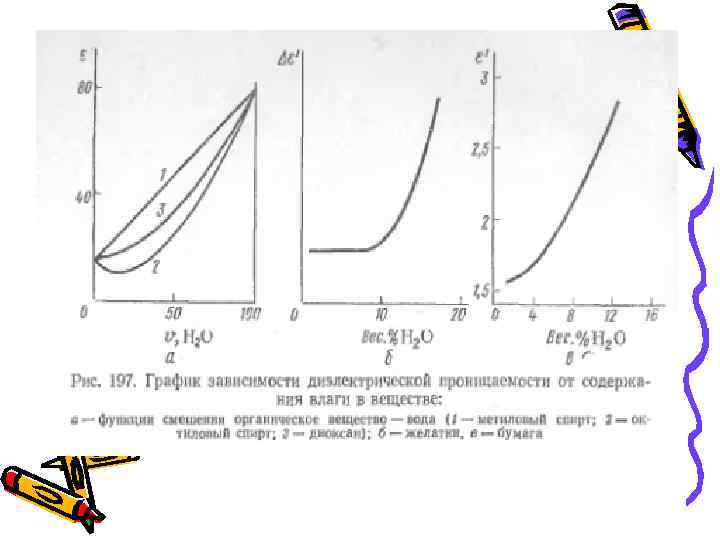
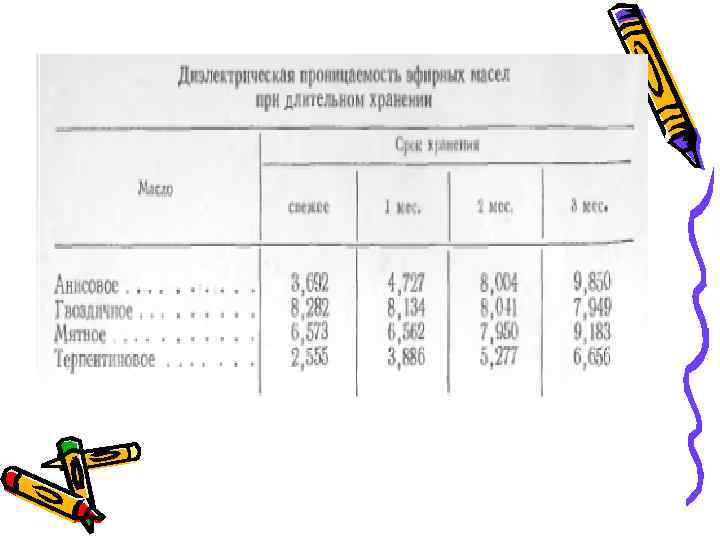
 Акваметрия • В основе возможности определения содержания воды путем измерения диэлектрической проницаемости находится тот факт, что диэлектрическая проницаемость большинства веществ намного меньше соответствующего значения для воды.
Акваметрия • В основе возможности определения содержания воды путем измерения диэлектрической проницаемости находится тот факт, что диэлектрическая проницаемость большинства веществ намного меньше соответствующего значения для воды.


 КУЛОНОМЕТРИЯ Кулонометрические методы основаны на • измерении количества электричества, затраченного на электропревращение определяемого вещества (прямая кулонометрия) • получении промежуточного реагента, который количественно реагирует с определяемым веществом (косвенная кулонометрия).
КУЛОНОМЕТРИЯ Кулонометрические методы основаны на • измерении количества электричества, затраченного на электропревращение определяемого вещества (прямая кулонометрия) • получении промежуточного реагента, который количественно реагирует с определяемым веществом (косвенная кулонометрия).
 законы электролиза Фарадея • • Количество (масса) вещества, выделившегося при электролизе, пропорциональна количеству электричества, прошедшего через раствор. При прохождении через раствор одного и того же количества электричества, на электродах выделяется одно и то же количество эквивалента вещества. где m – масса вещества, выделившегося при электролизе, г; Q ‑ количество электричества, Кл; Мэ ‑ молярная масса эквивалента, г/моль-экв; F ‑ число Фарадея: F = 96500 Кл/моль-экв; I ‑ сила тока, А; t ‑ время электролиза, с.
законы электролиза Фарадея • • Количество (масса) вещества, выделившегося при электролизе, пропорциональна количеству электричества, прошедшего через раствор. При прохождении через раствор одного и того же количества электричества, на электродах выделяется одно и то же количество эквивалента вещества. где m – масса вещества, выделившегося при электролизе, г; Q ‑ количество электричества, Кл; Мэ ‑ молярная масса эквивалента, г/моль-экв; F ‑ число Фарадея: F = 96500 Кл/моль-экв; I ‑ сила тока, А; t ‑ время электролиза, с.
 Обязательное условие • электропревращение вещества на электроде происходит со 100 %-ной эффективностью, т. е. со 100%-ным выходом по току, что возможно только в отсутствие побочных процессов (разложение воды, окисление или восстановление примесей, участие материала электрода в электрохимической реакции и др. ) Электролиз в кулонометрической ячейке можно проводить либо при постоянной силе тока (гальваностатическая кулонометрия), либо при постоянном потенциале (потенциостатическая кулонометрия).
Обязательное условие • электропревращение вещества на электроде происходит со 100 %-ной эффективностью, т. е. со 100%-ным выходом по току, что возможно только в отсутствие побочных процессов (разложение воды, окисление или восстановление примесей, участие материала электрода в электрохимической реакции и др. ) Электролиз в кулонометрической ячейке можно проводить либо при постоянной силе тока (гальваностатическая кулонометрия), либо при постоянном потенциале (потенциостатическая кулонометрия).
 Прямая кулонометрия • определяют только электроактивные вещества, в основе находится непосредственное электропревращение вещества на электроде. измерения можно проводить, поддерживая постоянной либо силу тока (необходимо иметь гальваностат), либо потенциал рабочего электрода (необходимо иметь потенциостат).
Прямая кулонометрия • определяют только электроактивные вещества, в основе находится непосредственное электропревращение вещества на электроде. измерения можно проводить, поддерживая постоянной либо силу тока (необходимо иметь гальваностат), либо потенциал рабочего электрода (необходимо иметь потенциостат).
 • Если электоролиз проводят при постоянной силе тока (гальваностатическая кулонометрия), то количество электричества (Q) за время электролиза t. Э, при постоянном токе I равно: Погрешность измерения Q зависит от точности измерения времени, поскольку современные приборы позволяют очень точно измерять даже небольшие токи. Прямая кулонометрия при постоянной силе тока является более простым, но менее селективным способом, поскольку в определенный момент времени может пойти реакция с участием мешающих веществ, фонового электролита или растворителя, и выход по току начинает уменьшаться по экспоненциальному закону.
• Если электоролиз проводят при постоянной силе тока (гальваностатическая кулонометрия), то количество электричества (Q) за время электролиза t. Э, при постоянном токе I равно: Погрешность измерения Q зависит от точности измерения времени, поскольку современные приборы позволяют очень точно измерять даже небольшие токи. Прямая кулонометрия при постоянной силе тока является более простым, но менее селективным способом, поскольку в определенный момент времени может пойти реакция с участием мешающих веществ, фонового электролита или растворителя, и выход по току начинает уменьшаться по экспоненциальному закону.
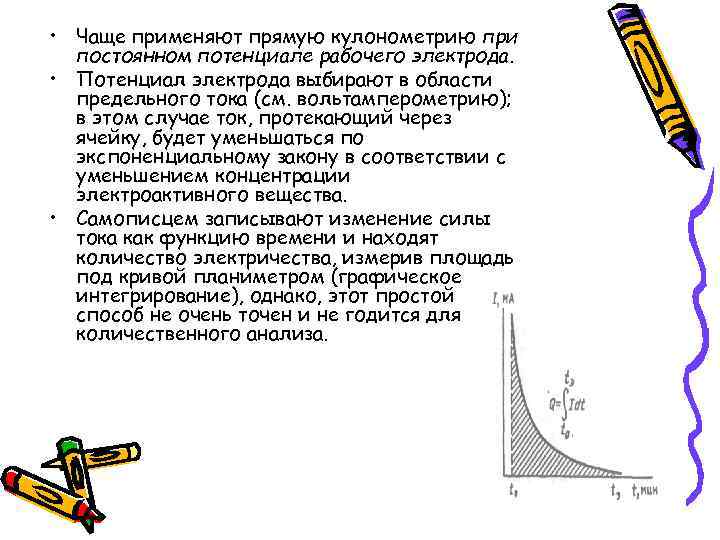 • Чаще применяют прямую кулонометрию при постоянном потенциале рабочего электрода. • Потенциал электрода выбирают в области предельного тока (см. вольтамперометрию); в этом случае ток, протекающий через ячейку, будет уменьшаться по экспоненциальному закону в соответствии с уменьшением концентрации электроактивного вещества. • Самописцем записывают изменение силы тока как функцию времени и находят количество электричества, измерив площадь под кривой планиметром (графическое интегрирование), однако, этот простой способ не очень точен и не годится для количественного анализа.
• Чаще применяют прямую кулонометрию при постоянном потенциале рабочего электрода. • Потенциал электрода выбирают в области предельного тока (см. вольтамперометрию); в этом случае ток, протекающий через ячейку, будет уменьшаться по экспоненциальному закону в соответствии с уменьшением концентрации электроактивного вещества. • Самописцем записывают изменение силы тока как функцию времени и находят количество электричества, измерив площадь под кривой планиметром (графическое интегрирование), однако, этот простой способ не очень точен и не годится для количественного анализа.
 Кулонометрическое титрование • • Титрование проводят, поддерживая постоянной силу тока. Метод применяется для определения и электроактивных и электронеактивных веществ. • В процессе титрования определяемое вещество реагирует с титрантом, образующимся в результате электрохимической реакции на электроде. Такой титрант называют электрогенерированным кулонометрическим титрантом, а электрод, на котором его получают – генераторным. Вторым электродом схемы генерации является так называемый вспомогательный электрод. Его обычно изолируют от анализируемого раствора, помещая в трубку с дном из пористого стекла, так как продукт реакции на вспомогательном электроде нередко мешает кулонометрическому определению. Индикаторными электродами могут быть два платиновых или золотых электрода, если для индикации применяется амперометрический метод, или платиновый и каломельный или хлоридсеребряный, если используется потенциометрическая индикация.
Кулонометрическое титрование • • Титрование проводят, поддерживая постоянной силу тока. Метод применяется для определения и электроактивных и электронеактивных веществ. • В процессе титрования определяемое вещество реагирует с титрантом, образующимся в результате электрохимической реакции на электроде. Такой титрант называют электрогенерированным кулонометрическим титрантом, а электрод, на котором его получают – генераторным. Вторым электродом схемы генерации является так называемый вспомогательный электрод. Его обычно изолируют от анализируемого раствора, помещая в трубку с дном из пористого стекла, так как продукт реакции на вспомогательном электроде нередко мешает кулонометрическому определению. Индикаторными электродами могут быть два платиновых или золотых электрода, если для индикации применяется амперометрический метод, или платиновый и каломельный или хлоридсеребряный, если используется потенциометрическая индикация.
 Электрогенерированный титрант • можно получать из воды (ОН‾ при восстановлении ее на катоде или Н+ при окислении на аноде), • растворов солей, кислот, • вспомогательных реагентов (например, при окислении KI можно получить I 2), • твердых электроактивных рабочих электродов.
Электрогенерированный титрант • можно получать из воды (ОН‾ при восстановлении ее на катоде или Н+ при окислении на аноде), • растворов солей, кислот, • вспомогательных реагентов (например, при окислении KI можно получить I 2), • твердых электроактивных рабочих электродов.
 Электрогенерированный титрант можно получать : • непосредственно в ячейке для кулонометрического титрования (внутренняя генерация) • в отдельном устройстве (внешняя генерация), а затем вводить его в кулонометрическую ячейку.
Электрогенерированный титрант можно получать : • непосредственно в ячейке для кулонометрического титрования (внутренняя генерация) • в отдельном устройстве (внешняя генерация), а затем вводить его в кулонометрическую ячейку.
 Электрогенерированные кулонометрические титранты Титрант Вспомогательный реагент Реакции на генераторном электроде Применение Кислотно–основное титрование ОН‾ H 2 O Титрование кислот Н+ H 2 O Титрование оснований Осадительное титрование Ag+ Ag-анод Титрование Cl‾, Br‾, I‾, органических серосодержащих веществ Окислительно–восстановительное титрование Титрование Fe (II), H 2 C 2 O 4 Mn 3+ Mn. SO 4 Br 2 Br‾ Cu. Cl 3‾ Cu. Cl 2 KCl Титрование I‾, As (III) I 2 KI Титрование S 2 O 32‾, As (III) Титрование I‾, As (III), фенолов Титрование Cr (VI), IO 3‾
Электрогенерированные кулонометрические титранты Титрант Вспомогательный реагент Реакции на генераторном электроде Применение Кислотно–основное титрование ОН‾ H 2 O Титрование кислот Н+ H 2 O Титрование оснований Осадительное титрование Ag+ Ag-анод Титрование Cl‾, Br‾, I‾, органических серосодержащих веществ Окислительно–восстановительное титрование Титрование Fe (II), H 2 C 2 O 4 Mn 3+ Mn. SO 4 Br 2 Br‾ Cu. Cl 3‾ Cu. Cl 2 KCl Титрование I‾, As (III) I 2 KI Титрование S 2 O 32‾, As (III) Титрование I‾, As (III), фенолов Титрование Cr (VI), IO 3‾
 • В качестве химической реакции между кулонометрическим титрантом и определяемым веществом может быть использована любая химическая реакция, применяемая в титриметрии – реакции кислотно -основного взаимодействия, окисления-восстановления, осаждения, комплексообразования. • Для определения конца кулонометрического титрования пригодны практически все способы установления конечной точки в титриметрии: • использование визуальных индикаторов (крахмала, фенолфталеина) и инструментальных методов. Наибольшее распространение получили потенциометрический и амперометрический методы с двумя индикаторными электродами.
• В качестве химической реакции между кулонометрическим титрантом и определяемым веществом может быть использована любая химическая реакция, применяемая в титриметрии – реакции кислотно -основного взаимодействия, окисления-восстановления, осаждения, комплексообразования. • Для определения конца кулонометрического титрования пригодны практически все способы установления конечной точки в титриметрии: • использование визуальных индикаторов (крахмала, фенолфталеина) и инструментальных методов. Наибольшее распространение получили потенциометрический и амперометрический методы с двумя индикаторными электродами.
 Преимущества • нет необходимости в приготовлении, стандартизации и хранении титранта, т. к. он образуется в процессе титрования и сразу же расходуется • при электрогенерации можно получать титранты, крайне неустойчивые в обычных условиях хранения, например, стандартные растворы Cu(1), Cr(П), Ag(Ш), или легколетучие вещества - Cl 2 , Br 2 • регулируя силу тока, можно прибавлять титрант сколь угодно малыми порциями, что более удобно, чем при использовании обычной бюретки • метод кулонометрического титрования характеризуется высокой чувствительностью и точностью (0, 05 -0, 1%), прямым титрованием определяют вещества в растворе при концентрации до 10 -6 моль/л. • легко автоматизируется.
Преимущества • нет необходимости в приготовлении, стандартизации и хранении титранта, т. к. он образуется в процессе титрования и сразу же расходуется • при электрогенерации можно получать титранты, крайне неустойчивые в обычных условиях хранения, например, стандартные растворы Cu(1), Cr(П), Ag(Ш), или легколетучие вещества - Cl 2 , Br 2 • регулируя силу тока, можно прибавлять титрант сколь угодно малыми порциями, что более удобно, чем при использовании обычной бюретки • метод кулонометрического титрования характеризуется высокой чувствительностью и точностью (0, 05 -0, 1%), прямым титрованием определяют вещества в растворе при концентрации до 10 -6 моль/л. • легко автоматизируется.
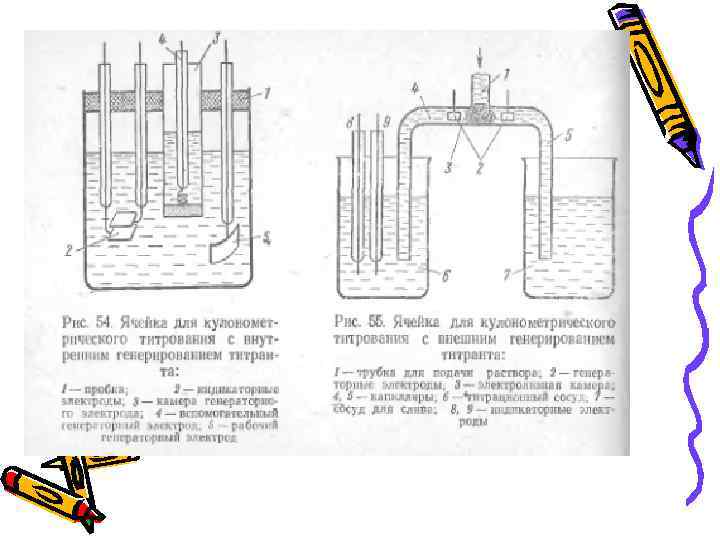
 В титриметрическую ячейку с вмонтированным генераторным и индикаторным электродами помещают электролит, содержащий сравнительно большое количество компонента, окислением или восстановлением которого можно получить необходимый титрант. Раствор в ячейки перемешивают, вводят определенный объем анализируемого раствора. Включая ток, начинают генерировать титрующее вещество или ион. Пуск секундомера и включение генераторной цепи проводится одновременно.
В титриметрическую ячейку с вмонтированным генераторным и индикаторным электродами помещают электролит, содержащий сравнительно большое количество компонента, окислением или восстановлением которого можно получить необходимый титрант. Раствор в ячейки перемешивают, вводят определенный объем анализируемого раствора. Включая ток, начинают генерировать титрующее вещество или ион. Пуск секундомера и включение генераторной цепи проводится одновременно.




