Кондуктометрия .ppt
- Количество слайдов: 30
 КОНДУКТОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА 1
КОНДУКТОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА 1
 Кондуктометрия Основные понятия Метод основан на использовании зависимости электрической проводимости растворов электролитов от их концентрации. 2
Кондуктометрия Основные понятия Метод основан на использовании зависимости электрической проводимости растворов электролитов от их концентрации. 2
 Кондуктометрия Основные понятия Основатель этого метода – немецкий физик Кольрауш, который впервые в 1885 г. предложил уравнение зависимости электропроводности растворов сильных электролитов от концентрации. Электропроводность растворов обусловлена диссоциацией растворенного вещества и миграцией образующихся ионов под действием внешнего источника напряжения. 3
Кондуктометрия Основные понятия Основатель этого метода – немецкий физик Кольрауш, который впервые в 1885 г. предложил уравнение зависимости электропроводности растворов сильных электролитов от концентрации. Электропроводность растворов обусловлена диссоциацией растворенного вещества и миграцией образующихся ионов под действием внешнего источника напряжения. 3
 Кондуктометрия Основные понятия Движущиеся ионы в поле электрического тока испытывают тормозящее действие со стороны молекул растворителя – релаксационный эффект – и со стороны противоположно заряженных ионов – электрофоретический эффект. В результате этих торможений раствор оказывает сопротивление прохождению электрического тока. То есть электропроводность (W) – это величина обратная сопротивлению: W =1/R , Ом-1. 4
Кондуктометрия Основные понятия Движущиеся ионы в поле электрического тока испытывают тормозящее действие со стороны молекул растворителя – релаксационный эффект – и со стороны противоположно заряженных ионов – электрофоретический эффект. В результате этих торможений раствор оказывает сопротивление прохождению электрического тока. То есть электропроводность (W) – это величина обратная сопротивлению: W =1/R , Ом-1. 4
 Кондуктометрия Основные понятия Удельная электропроводность (χ): электропроводность 1 см 3 раствора, находящегося между электродами площадью 1 см 2 каждый, расположенными на расстоянии 1 см друг от друга. Размерность: См/м (См – сименс). 1 См=Ом-1 5
Кондуктометрия Основные понятия Удельная электропроводность (χ): электропроводность 1 см 3 раствора, находящегося между электродами площадью 1 см 2 каждый, расположенными на расстоянии 1 см друг от друга. Размерность: См/м (См – сименс). 1 См=Ом-1 5
 Кондуктометрия Основные понятия Удельная электропроводность раствора электролита, как правило, возрастает с увеличением концентрации до известного предела, а затем снижается, то есть проходит через максимум. Это объясняется уменьшением подвижности ионов при возрастании их концентрации вследствие существования «ионной атмосферы» , которая влияет на его подвижность в электрическом поле. 6
Кондуктометрия Основные понятия Удельная электропроводность раствора электролита, как правило, возрастает с увеличением концентрации до известного предела, а затем снижается, то есть проходит через максимум. Это объясняется уменьшением подвижности ионов при возрастании их концентрации вследствие существования «ионной атмосферы» , которая влияет на его подвижность в электрическом поле. 6
 Кондуктометрия Основные понятия Более удобной характеристикой раствора электролита является его эквивалентная электропроводность (λ): проводимость слоя электролита толщиной 1 см, помещенного между электродами такой площади, чтобы объем электролита между ними содержал 1 моль растворенного вещества. 7
Кондуктометрия Основные понятия Более удобной характеристикой раствора электролита является его эквивалентная электропроводность (λ): проводимость слоя электролита толщиной 1 см, помещенного между электродами такой площади, чтобы объем электролита между ними содержал 1 моль растворенного вещества. 7
 Кондуктометрия Основные понятия Кондуктометрический анализ основан на измерении удельной или эквивалентной электропроводности, которые связаны с концентрацией соотношением: где С – концентрация электролита, моль/дм 3; V – объем раствора, в котором находится 1 моль вещества, см 3. 8
Кондуктометрия Основные понятия Кондуктометрический анализ основан на измерении удельной или эквивалентной электропроводности, которые связаны с концентрацией соотношением: где С – концентрация электролита, моль/дм 3; V – объем раствора, в котором находится 1 моль вещества, см 3. 8
 Кондуктометрия Основные понятия Зависимость электропроводности от температуры: Обычно при повышении температуры раствора происходит уменьшение его вязкости и увеличение подвижности ионов, что приводит к росту χ и λ. Поэтому кондуктометрические измерения проводят в термостатических условиях. 9
Кондуктометрия Основные понятия Зависимость электропроводности от температуры: Обычно при повышении температуры раствора происходит уменьшение его вязкости и увеличение подвижности ионов, что приводит к росту χ и λ. Поэтому кондуктометрические измерения проводят в термостатических условиях. 9
 Кондуктометрия Классификация • прямая кондуктометрия; • кондуктометрическое титрование; • хронокондуктометрическое титрование – основано на определении содержания вещества по затраченному на титрование времени, автоматически фиксируемого на диаграммной ленте регистратора кривой титрования. 10
Кондуктометрия Классификация • прямая кондуктометрия; • кондуктометрическое титрование; • хронокондуктометрическое титрование – основано на определении содержания вещества по затраченному на титрование времени, автоматически фиксируемого на диаграммной ленте регистратора кривой титрования. 10
 Кондуктометрия Классификация Прямая кондуктометрия: метод, позволяющий непосредственно определять концентрацию электролита путем измерения электропроводности раствора с известным качественным составом. Шкала приборов – солемеров откалибрована в единицах концентрации и это позволяет прямо определять солесодержание раствора. 11
Кондуктометрия Классификация Прямая кондуктометрия: метод, позволяющий непосредственно определять концентрацию электролита путем измерения электропроводности раствора с известным качественным составом. Шкала приборов – солемеров откалибрована в единицах концентрации и это позволяет прямо определять солесодержание раствора. 11
 Кондуктометрия Классификация Прямая кондуктометрия: метод применим при малом содержании ионов в растворе, так как в этом случае его электрическая проводимость пропорциональна концентрации. Когда испытуемый объект содержит большие количества различных солей, прямой кондуктометрический анализ невозможен. Используют косвенный метод анализа – кондуктометрическое титрование. 12
Кондуктометрия Классификация Прямая кондуктометрия: метод применим при малом содержании ионов в растворе, так как в этом случае его электрическая проводимость пропорциональна концентрации. Когда испытуемый объект содержит большие количества различных солей, прямой кондуктометрический анализ невозможен. Используют косвенный метод анализа – кондуктометрическое титрование. 12
 Кондуктометрия Классификация Кондуктометрическое титрование: метод анализа, основанный на определении содержания вещества по излому кривой титрования. При добавлении одного электролита к другому в результате протекающей химической реакции изменяется ионный состав раствора, что приводит к изменению электрической проводимости. 13
Кондуктометрия Классификация Кондуктометрическое титрование: метод анализа, основанный на определении содержания вещества по излому кривой титрования. При добавлении одного электролита к другому в результате протекающей химической реакции изменяется ионный состав раствора, что приводит к изменению электрической проводимости. 13
 Кондуктометрия Кондуктометрическое титрование: Графики кондуктометрического титрования строят в координатах «объем приливаемого титранта – удельная электрическая проводимость раствора. Кривые кондуктометрического титрования имеют излом, соответствующий точке эквивалентности, по которому можно установить объем титранта, израсходованного на титрование, и рассчитать концентрацию анализируемого раствора» 14
Кондуктометрия Кондуктометрическое титрование: Графики кондуктометрического титрования строят в координатах «объем приливаемого титранта – удельная электрическая проводимость раствора. Кривые кондуктометрического титрования имеют излом, соответствующий точке эквивалентности, по которому можно установить объем титранта, израсходованного на титрование, и рассчитать концентрацию анализируемого раствора» 14
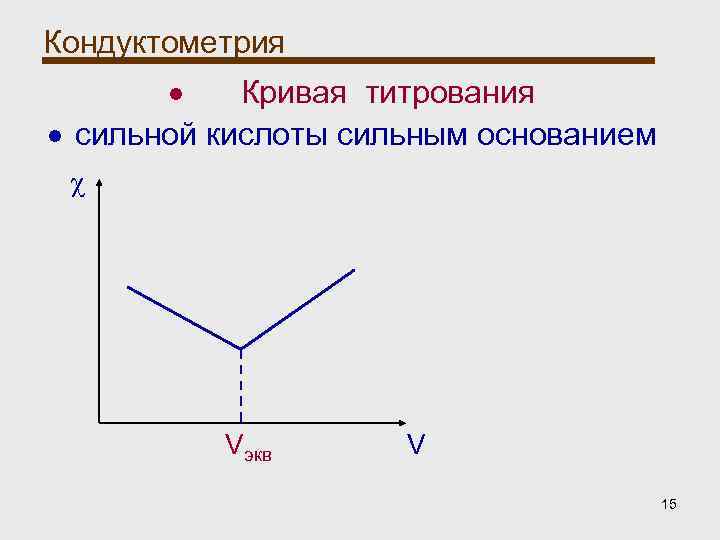 Кондуктометрия Кривая титрования сильной кислоты сильным основанием χ Vэкв V 15
Кондуктометрия Кривая титрования сильной кислоты сильным основанием χ Vэкв V 15
 Кондуктометрия Кондуктометрическое титрование: При титровании слабых кислот характер кривых зависит от концентрации раствора, что влияет на степень диссоциации кислот и, соответственно, их электрическую проводимость. 16
Кондуктометрия Кондуктометрическое титрование: При титровании слабых кислот характер кривых зависит от концентрации раствора, что влияет на степень диссоциации кислот и, соответственно, их электрическую проводимость. 16
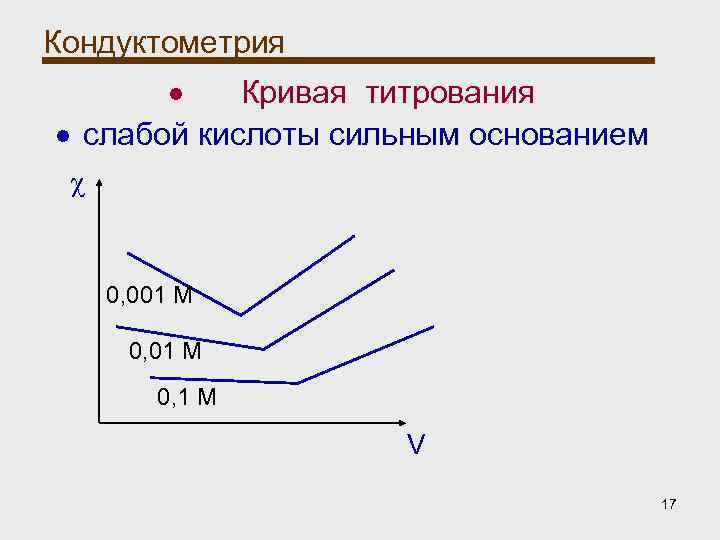 Кондуктометрия Кривая титрования слабой кислоты сильным основанием χ 0, 001 М 0, 1 М V 17
Кондуктометрия Кривая титрования слабой кислоты сильным основанием χ 0, 001 М 0, 1 М V 17
 Кондуктометрия Кондуктометрическое титрование: Для использования реакций окислениявосстановления применяют умеренно кислые или щелочные растворы, т. к. участие в реакции водородных или гидроксильных ионов способствует резкому изменению электрической проводимости. 18
Кондуктометрия Кондуктометрическое титрование: Для использования реакций окислениявосстановления применяют умеренно кислые или щелочные растворы, т. к. участие в реакции водородных или гидроксильных ионов способствует резкому изменению электрической проводимости. 18
 Кондуктометрия Кондуктометрическое титрование: При использовании реакций комплексообразования наиболее широко применяют комплексон III (двунатриевая соль этилендиаминтетрауксусной кислоты). При реакции катионов с комплексоном III в водных растворах увеличивается концентрация ионов водорода, что приводит к увеличению электрической проводимости раствора. 19
Кондуктометрия Кондуктометрическое титрование: При использовании реакций комплексообразования наиболее широко применяют комплексон III (двунатриевая соль этилендиаминтетрауксусной кислоты). При реакции катионов с комплексоном III в водных растворах увеличивается концентрация ионов водорода, что приводит к увеличению электрической проводимости раствора. 19
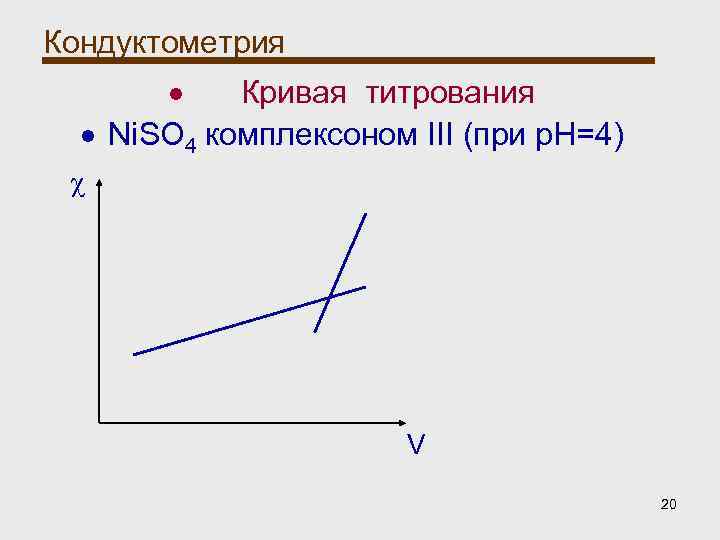 Кондуктометрия Кривая титрования Ni. SO 4 комплексоном III (при p. H=4) χ V 20
Кондуктометрия Кривая титрования Ni. SO 4 комплексоном III (при p. H=4) χ V 20
 Кондуктометрия Кондуктометрическое титрование: При использовании реакций осаждения кривые титрования могут искажаться вследствие растворимости образующегося осадка. Для уменьшения растворимости осадка к раствору добавляют этиловый спирт. 21
Кондуктометрия Кондуктометрическое титрование: При использовании реакций осаждения кривые титрования могут искажаться вследствие растворимости образующегося осадка. Для уменьшения растворимости осадка к раствору добавляют этиловый спирт. 21
 Кондуктометрия Кондуктометрическое титрование: При титровании хлорида бария сульфатом натрия ионы бария связываются с сульфат-ионами. Характер изменения электрической проводимости зависит от сравнительной подвижности ионов. Подвижность ионов бария выше, чем ионов натрия, поэтому до точки эквивалентности электрическая проводимость падает, а после – возрастает (избыток сульфат-ионов). 22
Кондуктометрия Кондуктометрическое титрование: При титровании хлорида бария сульфатом натрия ионы бария связываются с сульфат-ионами. Характер изменения электрической проводимости зависит от сравнительной подвижности ионов. Подвижность ионов бария выше, чем ионов натрия, поэтому до точки эквивалентности электрическая проводимость падает, а после – возрастает (избыток сульфат-ионов). 22
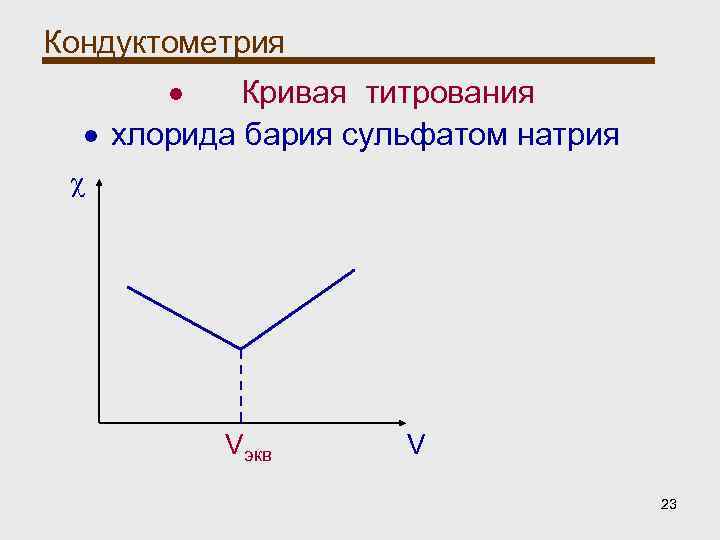 Кондуктометрия Кривая титрования хлорида бария сульфатом натрия χ Vэкв V 23
Кондуктометрия Кривая титрования хлорида бария сульфатом натрия χ Vэкв V 23
 Кондуктометрия Кондуктометрическое титрование: При титровании слабой кислоты слабым основанием (и наоборот) электрическая проводимость вначале растет вследствие образования соли, а после прибавления избытка реагента остается постоянной, т. к. слабая кислота (или основание) мало изменяют электрическую проводимость. 24
Кондуктометрия Кондуктометрическое титрование: При титровании слабой кислоты слабым основанием (и наоборот) электрическая проводимость вначале растет вследствие образования соли, а после прибавления избытка реагента остается постоянной, т. к. слабая кислота (или основание) мало изменяют электрическую проводимость. 24
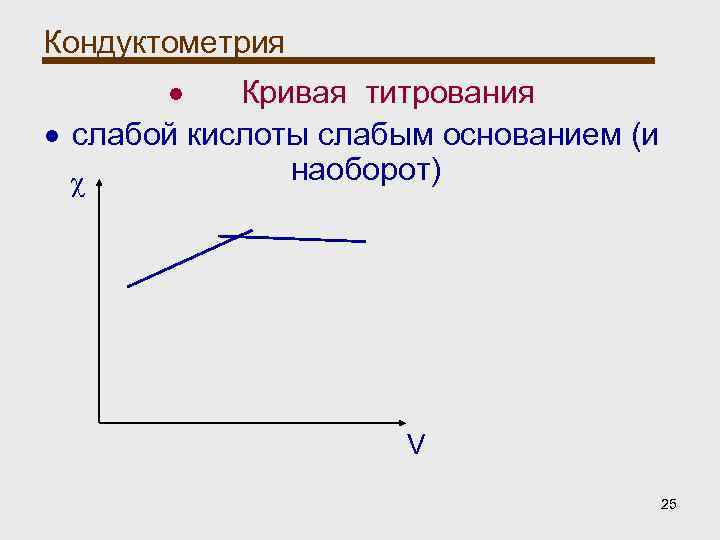 Кондуктометрия Кривая титрования слабой кислоты слабым основанием (и наоборот) χ V 25
Кондуктометрия Кривая титрования слабой кислоты слабым основанием (и наоборот) χ V 25
 Кондуктометрия Кондуктометрическое титрование: При титровании смеси сильной и слабой кислот на кривой получается две точки пересечения, что соответствует моменту эквивалентности титрования HCl и CH 3 COOH. 26
Кондуктометрия Кондуктометрическое титрование: При титровании смеси сильной и слабой кислот на кривой получается две точки пересечения, что соответствует моменту эквивалентности титрования HCl и CH 3 COOH. 26
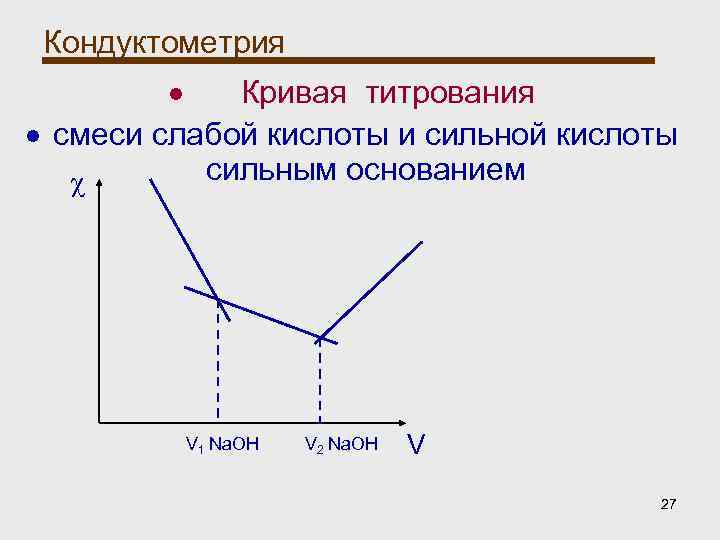 Кондуктометрия Кривая титрования смеси слабой кислоты и сильной кислоты сильным основанием χ V 1 Na. OH V 27
Кондуктометрия Кривая титрования смеси слабой кислоты и сильной кислоты сильным основанием χ V 1 Na. OH V 27
 Кондуктометрия Особенности кондуктометрических методов анализа • Возможность проводить определение не только в прозрачных, но и в окрашенных и мутных растворах, а также в присутствии окислителей, восстановителей, органических веществ; • возможность определения различных неорганических индивидуальных соединений; 28
Кондуктометрия Особенности кондуктометрических методов анализа • Возможность проводить определение не только в прозрачных, но и в окрашенных и мутных растворах, а также в присутствии окислителей, восстановителей, органических веществ; • возможность определения различных неорганических индивидуальных соединений; 28
 Кондуктометрия • • Особенности кондуктометрических методов анализа высокая чувствительность метода, позволяющая работать с разбавленными растворами; анализ водных и органических растворов; возможность автоматизации процесса (хронокондуктометрия); использование разнообразных типов реакций; 29
Кондуктометрия • • Особенности кондуктометрических методов анализа высокая чувствительность метода, позволяющая работать с разбавленными растворами; анализ водных и органических растворов; возможность автоматизации процесса (хронокондуктометрия); использование разнообразных типов реакций; 29
 Кондуктометрия Особенности кондуктометрических методов анализа • во многих случаях отсутствие необходимости проводить предварительную пробоподготовку; • простота определения конечной точки титрования по пересечению прямых; • возможность проведения дифференцированного титрования смесей электролитов, что невозможно при титровании с визуальной индикацией конечной точки титрования. 30
Кондуктометрия Особенности кондуктометрических методов анализа • во многих случаях отсутствие необходимости проводить предварительную пробоподготовку; • простота определения конечной точки титрования по пересечению прямых; • возможность проведения дифференцированного титрования смесей электролитов, что невозможно при титровании с визуальной индикацией конечной точки титрования. 30


