КОНФ. 22.03.14.ОКС.СТРЕСС.ppt
- Количество слайдов: 44
 Концепция развития патохимических реакций при гипоксических состояниях. Докладчик: Разин А. Ю.
Концепция развития патохимических реакций при гипоксических состояниях. Докладчик: Разин А. Ю.

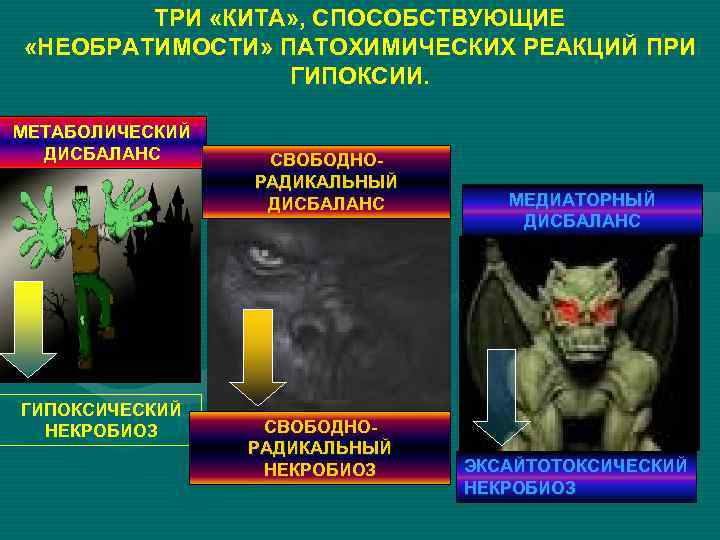 ТРИ «КИТА» , СПОСОБСТВУЮЩИЕ «НЕОБРАТИМОСТИ» ПАТОХИМИЧЕСКИХ РЕАКЦИЙ ПРИ ГИПОКСИИ. МЕТАБОЛИЧЕСКИЙ ДИСБАЛАНС ГИПОКСИЧЕСКИЙ НЕКРОБИОЗ СВОБОДНОРАДИКАЛЬНЫЙ ДИСБАЛАНС СВОБОДНОРАДИКАЛЬНЫЙ НЕКРОБИОЗ МЕДИАТОРНЫЙ ДИСБАЛАНС ЭКСАЙТОТОКСИЧЕСКИЙ НЕКРОБИОЗ
ТРИ «КИТА» , СПОСОБСТВУЮЩИЕ «НЕОБРАТИМОСТИ» ПАТОХИМИЧЕСКИХ РЕАКЦИЙ ПРИ ГИПОКСИИ. МЕТАБОЛИЧЕСКИЙ ДИСБАЛАНС ГИПОКСИЧЕСКИЙ НЕКРОБИОЗ СВОБОДНОРАДИКАЛЬНЫЙ ДИСБАЛАНС СВОБОДНОРАДИКАЛЬНЫЙ НЕКРОБИОЗ МЕДИАТОРНЫЙ ДИСБАЛАНС ЭКСАЙТОТОКСИЧЕСКИЙ НЕКРОБИОЗ
 Последствия патохимических реакций гипоксии. 1. МЕТАБОЛИЧЕСКИЙ ДИСБАЛАНС (дефицит энергии) -снижение скорости окислительного фосфорилирования -сдвиг равновесия НАД+/НАДН вправо (изменение поляризации клеточных мембран ). -несостоятельность альтернативных путей образования АТФ - внутриклеточный ацидоз (МК, С 02, протоны) 2. ОКСИДАТИВНЫЙ ДИСБАЛАНС (образование АФК): -нарушение композиции клеточных мембран 3. МЕДИАТОРНЫЙ ДИСБАЛАНС (эксайтотоксичность). 4. Цитокиновый дисбаланс 5. Транскрипционный дисбаланс. -нарушение кальциевого гомеостаза клетки. -эксайтотоксичность Нарушение гомеостаза клеточного кластера
Последствия патохимических реакций гипоксии. 1. МЕТАБОЛИЧЕСКИЙ ДИСБАЛАНС (дефицит энергии) -снижение скорости окислительного фосфорилирования -сдвиг равновесия НАД+/НАДН вправо (изменение поляризации клеточных мембран ). -несостоятельность альтернативных путей образования АТФ - внутриклеточный ацидоз (МК, С 02, протоны) 2. ОКСИДАТИВНЫЙ ДИСБАЛАНС (образование АФК): -нарушение композиции клеточных мембран 3. МЕДИАТОРНЫЙ ДИСБАЛАНС (эксайтотоксичность). 4. Цитокиновый дисбаланс 5. Транскрипционный дисбаланс. -нарушение кальциевого гомеостаза клетки. -эксайтотоксичность Нарушение гомеостаза клеточного кластера
 СВОБОДНО-РАДИКАЛЬНЫЙ НЕКРОБИОЗ (ОКСИДАТИВНЫЙ ДИСБАЛАНС).
СВОБОДНО-РАДИКАЛЬНЫЙ НЕКРОБИОЗ (ОКСИДАТИВНЫЙ ДИСБАЛАНС).
 Реакции с участием О 2 в живой клетке протекают в активных центрах оксидаз или оксигеназ (два пути окисления) 1. оксидазный 2. оксигеназный
Реакции с участием О 2 в живой клетке протекают в активных центрах оксидаз или оксигеназ (два пути окисления) 1. оксидазный 2. оксигеназный
 ОКСИДАЗНЫЙ ПУТЬ. 80% кислорода потребляемого клеткой, используется в митохондриях с участием цитохромоксидазы- дающий клетке энергию в виде АТФ. Оксидазы ФМН и ФАД –зависимые катализируют реакции окисления веществ с образованием перекиси водорода.
ОКСИДАЗНЫЙ ПУТЬ. 80% кислорода потребляемого клеткой, используется в митохондриях с участием цитохромоксидазы- дающий клетке энергию в виде АТФ. Оксидазы ФМН и ФАД –зависимые катализируют реакции окисления веществ с образованием перекиси водорода.
 Процесс полного восстановления О 2 до Н 2 О более энергозависимый, чем процессы неполного восстановления, и осуществляется конечным ферментом дыхательной цепи митохондрий - цитохромоксидазой.
Процесс полного восстановления О 2 до Н 2 О более энергозависимый, чем процессы неполного восстановления, и осуществляется конечным ферментом дыхательной цепи митохондрий - цитохромоксидазой.
 Оксигеназный путь окисления. 1. Не дает клетке энергии. 2. Происходит на мембранах эндоплазматического ретикулума(микросомах). 3. Микросомальным окислением осуществляется альфа-гамма окисление ЖК, синтез ненасыщенных ЖК, стероидов, обезвреживание ксенобиотиков. 4. О 2 включается в субстрат с образованием гидроксильной или карбоксильной групп.
Оксигеназный путь окисления. 1. Не дает клетке энергии. 2. Происходит на мембранах эндоплазматического ретикулума(микросомах). 3. Микросомальным окислением осуществляется альфа-гамма окисление ЖК, синтез ненасыщенных ЖК, стероидов, обезвреживание ксенобиотиков. 4. О 2 включается в субстрат с образованием гидроксильной или карбоксильной групп.
 -Выделяют 2 вида оксигеназ. 1. диоксигеназы –включающие в молекулу субстрата два атома молекулы О 2. монооксигеназы(гидроксилазы)один атом молекулы О 2 включается в субстрат, а второй атом восстанавливается до воды. (гидроксилирование ксенобиотиков). Активатором О 2 при этом является цитохром Р 450
-Выделяют 2 вида оксигеназ. 1. диоксигеназы –включающие в молекулу субстрата два атома молекулы О 2. монооксигеназы(гидроксилазы)один атом молекулы О 2 включается в субстрат, а второй атом восстанавливается до воды. (гидроксилирование ксенобиотиков). Активатором О 2 при этом является цитохром Р 450
 Свободные радикалы - это атомы или группы химически связанных атомов или молекулы которые имеют неспаренные электроны на внешний валентной орбитали, то есть свободные валентности, наличие которых определяет их высокую химическую реакционную способность и магнитный момент(магнетизм). Процессы, в которых участвуют эти свободные радикалы, являются обязательным атрибутом нормального аэробного метаболизма.
Свободные радикалы - это атомы или группы химически связанных атомов или молекулы которые имеют неспаренные электроны на внешний валентной орбитали, то есть свободные валентности, наличие которых определяет их высокую химическую реакционную способность и магнитный момент(магнетизм). Процессы, в которых участвуют эти свободные радикалы, являются обязательным атрибутом нормального аэробного метаболизма.
 - О 2 - - супероксидный радикал - НО 2 - - гидроперекисный радикал - ОН - - гидроксильный радикал - Н 2 О 2 - пероксид водорода Эти соединения обладают высокой реакционной способностью и получили название активных форм кислорода (АФК).
- О 2 - - супероксидный радикал - НО 2 - - гидроперекисный радикал - ОН - - гидроксильный радикал - Н 2 О 2 - пероксид водорода Эти соединения обладают высокой реакционной способностью и получили название активных форм кислорода (АФК).
 АФК образуются 1. Внутриклеточно (в митохондриях , микросомах, перосисомах). 2. Внеклеточно (в процессе фагоцитоза).
АФК образуются 1. Внутриклеточно (в митохондриях , микросомах, перосисомах). 2. Внеклеточно (в процессе фагоцитоза).
 АФК - нестабильные соединения. Известно, что время жизни АФК в биологических системах очень коротко. Соответственно времени жизни изменяется и величина диффузии каждого из них в живых организмах.
АФК - нестабильные соединения. Известно, что время жизни АФК в биологических системах очень коротко. Соответственно времени жизни изменяется и величина диффузии каждого из них в живых организмах.
 Кроме продуктов восстановления кислорода, к АФК относят также: - молекулы кислорода в синглетном состоянии (1 О 2) - окисел азота (NО) - пероксинитрит (ОNОО) - гипогалогениты (НОСl, НОВг, НОJ) - а также продукты перекисного окисления липидов (ПОЛ) - перекисные (RО 2 -) и алкоксильные (RО) радикалы.
Кроме продуктов восстановления кислорода, к АФК относят также: - молекулы кислорода в синглетном состоянии (1 О 2) - окисел азота (NО) - пероксинитрит (ОNОО) - гипогалогениты (НОСl, НОВг, НОJ) - а также продукты перекисного окисления липидов (ПОЛ) - перекисные (RО 2 -) и алкоксильные (RО) радикалы.
 Свободнорадикальные реакции, которые происходят в организме, непосредственно ведут к образованию эндогенного кислорода. Такой механизм ведёт к постоянному поддержанию в клетках высокого напряжения кислорода, что стимулирует работу митохондрий, поддерживает кислородный гомеостаз и обеспечивает высокую интенсивность аэробного метаболизма.
Свободнорадикальные реакции, которые происходят в организме, непосредственно ведут к образованию эндогенного кислорода. Такой механизм ведёт к постоянному поддержанию в клетках высокого напряжения кислорода, что стимулирует работу митохондрий, поддерживает кислородный гомеостаз и обеспечивает высокую интенсивность аэробного метаболизма.
 В условиях нормально функционирующего организма ПОЛ является физиологическим процессом, способствующим обновлению клеточных мембран и внутриклеточных структур. Поддержание оптимального уровня перекисных процессов осуществляется с помощью ферментативного и неферментативного компонентов антиоксидантной системы.
В условиях нормально функционирующего организма ПОЛ является физиологическим процессом, способствующим обновлению клеточных мембран и внутриклеточных структур. Поддержание оптимального уровня перекисных процессов осуществляется с помощью ферментативного и неферментативного компонентов антиоксидантной системы.
 Ферментативная защита клеток. 1. Супероксиддисмутазыпревращение супероксидного радикала в перекись водорода. 2. Каталазы(разложение перекиси водорода на Н 2 О и О 2).
Ферментативная защита клеток. 1. Супероксиддисмутазыпревращение супероксидного радикала в перекись водорода. 2. Каталазы(разложение перекиси водорода на Н 2 О и О 2).
 3. Глутатионпероксидазы – главная система защиты эритроцитов от разрушительного действия Н 2 О 2. В качестве кофермента – глутатионпероксидазы выступает трипептид-глутатион.
3. Глутатионпероксидазы – главная система защиты эритроцитов от разрушительного действия Н 2 О 2. В качестве кофермента – глутатионпероксидазы выступает трипептид-глутатион.
 Неферментативная защита. 1. Вит. Е – защита ненасыщенных ЖК клеточных мембран от перекисного окисления , SH-групп мембранных белков, двойных связей кротинов и Вит. А
Неферментативная защита. 1. Вит. Е – защита ненасыщенных ЖК клеточных мембран от перекисного окисления , SH-групп мембранных белков, двойных связей кротинов и Вит. А
 2. Вит Е – (с Вит. С) способствует включению селена в состав активного центра глутатионпероксидазы – контролирующей синтез гема и цитохромов, стабилизирующей биологические мембраны.
2. Вит Е – (с Вит. С) способствует включению селена в состав активного центра глутатионпероксидазы – контролирующей синтез гема и цитохромов, стабилизирующей биологические мембраны.
 При глубоких дистрофических энергодефицитных состояниях эти процессы угнетаются, что ведёт к появлению токсических концентраций недоокисленных метаболитов.
При глубоких дистрофических энергодефицитных состояниях эти процессы угнетаются, что ведёт к появлению токсических концентраций недоокисленных метаболитов.
 Кислородные свободные радикалы принимают участие: - в метаболизме ксенобиотиков в организме; - при повреждениях, вызванных ишемией и реперфузией; - в онтогенезе и в клеточной пролиферации; - в регуляции тонуса сосудов; - при воспалении; - при бактериальных и вирусных инфекциях; - в регуляции метаболических процессов как внутриклеточные мессенджеры; - в канцерогенезе; - в атерогенезе; - при старении и т. д.
Кислородные свободные радикалы принимают участие: - в метаболизме ксенобиотиков в организме; - при повреждениях, вызванных ишемией и реперфузией; - в онтогенезе и в клеточной пролиферации; - в регуляции тонуса сосудов; - при воспалении; - при бактериальных и вирусных инфекциях; - в регуляции метаболических процессов как внутриклеточные мессенджеры; - в канцерогенезе; - в атерогенезе; - при старении и т. д.
 В человеческом организме выявлено много систем, которые продуцируют активные формы кислорода, как в физиологических условиях, так и в патологических. Это образование кислородных свободных радикалов: - в дыхательной цепи митохондрий; - в электронно-транспортной цепи микросом; - путём перехода оксигемоглобина в метгемоглобин; - во время метаболизма арахидоновой кислоты; - в реакции гипоксантин-ксантиноксидаза; - при биосинтезе и окислении катехоламинов; - под воздействием ионизирующего излучения, озона, NO 2; - при фотолизе и функциональной активности фагоцитирующих клеток крови (нейтрофилов, моноцитов, макрофагов.
В человеческом организме выявлено много систем, которые продуцируют активные формы кислорода, как в физиологических условиях, так и в патологических. Это образование кислородных свободных радикалов: - в дыхательной цепи митохондрий; - в электронно-транспортной цепи микросом; - путём перехода оксигемоглобина в метгемоглобин; - во время метаболизма арахидоновой кислоты; - в реакции гипоксантин-ксантиноксидаза; - при биосинтезе и окислении катехоламинов; - под воздействием ионизирующего излучения, озона, NO 2; - при фотолизе и функциональной активности фагоцитирующих клеток крови (нейтрофилов, моноцитов, макрофагов.
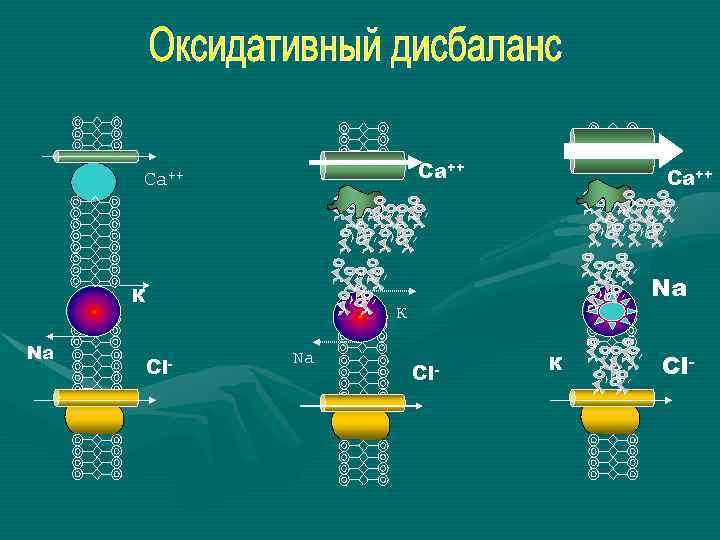 Са++ К Na Са++ Na К Сl- Na Сl- К Сl-
Са++ К Na Са++ Na К Сl- Na Сl- К Сl-
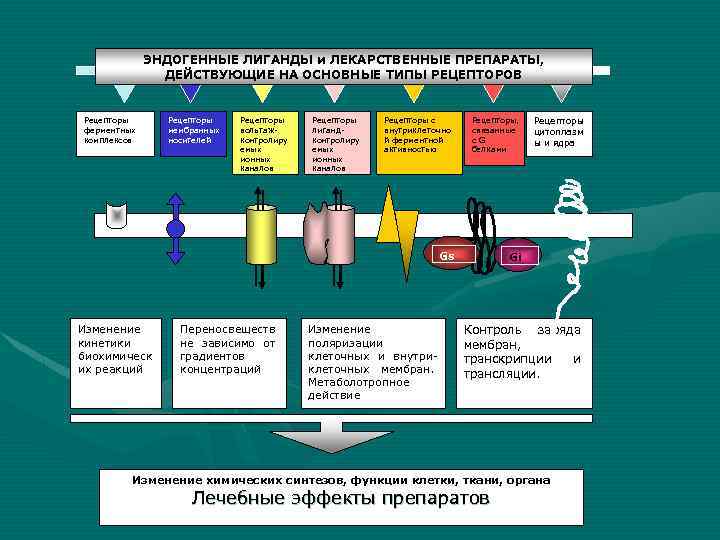 ЭНДОГЕННЫЕ ЛИГАНДЫ и ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ДЕЙСТВУЮЩИЕ НА ОСНОВНЫЕ ТИПЫ РЕЦЕПТОРОВ Рецепторы ферментных комплексов Рецепторы мембранных носителей Рецепторы вольтажконтролиру емых ионных каналов Рецепторы лигандконтролиру емых ионных каналов Рецепторы с внутриклеточно й ферментной активностью Рецепторы, связанные с. G белками Gs Изменение кинетики биохимическ их реакций Переносвеществ не зависимо от градиентов концентраций Изменение поляризации клеточных и внутриклеточных мембран. Метаболотропное действие Рецепторы цитоплазм ы и ядра Gi Контроль заряда мембран, транскрипции и трансляции. Изменение химических синтезов, функции клетки, ткани, органа Лечебные эффекты препаратов
ЭНДОГЕННЫЕ ЛИГАНДЫ и ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, ДЕЙСТВУЮЩИЕ НА ОСНОВНЫЕ ТИПЫ РЕЦЕПТОРОВ Рецепторы ферментных комплексов Рецепторы мембранных носителей Рецепторы вольтажконтролиру емых ионных каналов Рецепторы лигандконтролиру емых ионных каналов Рецепторы с внутриклеточно й ферментной активностью Рецепторы, связанные с. G белками Gs Изменение кинетики биохимическ их реакций Переносвеществ не зависимо от градиентов концентраций Изменение поляризации клеточных и внутриклеточных мембран. Метаболотропное действие Рецепторы цитоплазм ы и ядра Gi Контроль заряда мембран, транскрипции и трансляции. Изменение химических синтезов, функции клетки, ткани, органа Лечебные эффекты препаратов
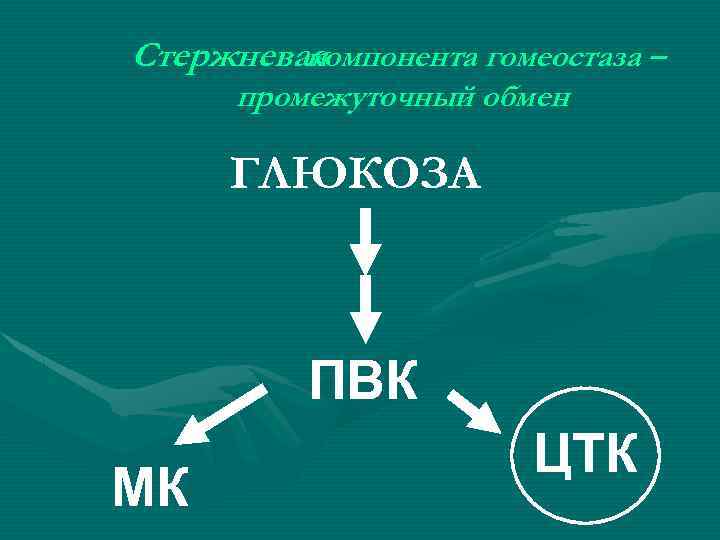 Стержневая компонента гомеостаза – промежуточный обмен ГЛЮКОЗА ПВК МК ЦТК
Стержневая компонента гомеостаза – промежуточный обмен ГЛЮКОЗА ПВК МК ЦТК
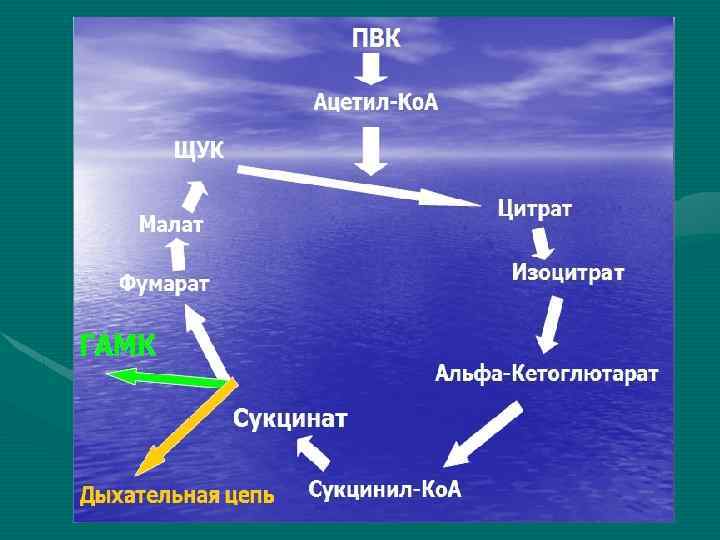
 Сопряжение окисления и фосфорилирования
Сопряжение окисления и фосфорилирования
 ОКИСЛЕНИЕ Н+ О 2 ФОСФОРИЛИРОВАНИЕ Н+ НРО 3
ОКИСЛЕНИЕ Н+ О 2 ФОСФОРИЛИРОВАНИЕ Н+ НРО 3
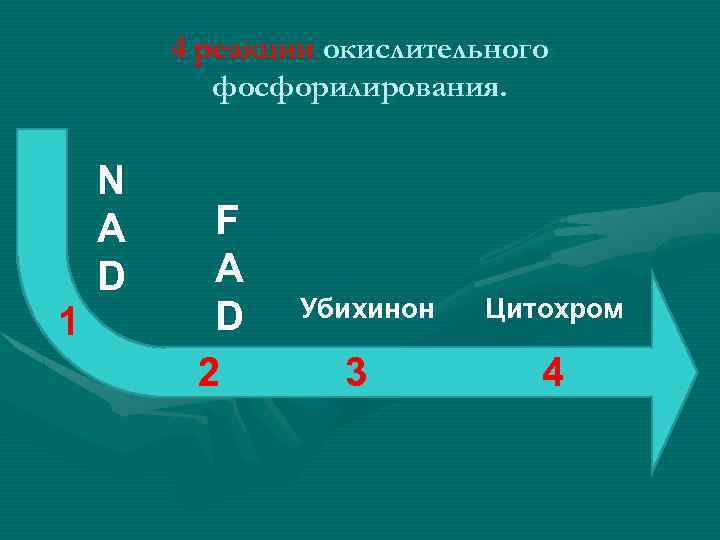 4 реакции окислительного фосфорилирования. 1 N A D F A D 2 Убихинон 3 Цитохром 4
4 реакции окислительного фосфорилирования. 1 N A D F A D 2 Убихинон 3 Цитохром 4
 Гипоксия снижает активность цитохромов дыхательной цепи митохондрий, происходит неполное электронное восстановление О 2 с образованием Н 2 О 2 – ключевого момента автоматического запуска перекисных процессов.
Гипоксия снижает активность цитохромов дыхательной цепи митохондрий, происходит неполное электронное восстановление О 2 с образованием Н 2 О 2 – ключевого момента автоматического запуска перекисных процессов.
 Развивается неконтролируемый рост концентрации АФК. Этот процесс поддерживается одновременным ингибированием ферментативного компонента антиоксидантной системы.
Развивается неконтролируемый рост концентрации АФК. Этот процесс поддерживается одновременным ингибированием ферментативного компонента антиоксидантной системы.
 Снижение выхода АТФ НАРУШЕНИЕ РАБОТЫ БЕЛКОВПЕРЕНОСЧИКОВ КАТИОННЫХ КАНАЛОВ. 1. К-Na АТФ-азы 2. Са –зависимой АТФ-азы 3. Протонной помпы
Снижение выхода АТФ НАРУШЕНИЕ РАБОТЫ БЕЛКОВПЕРЕНОСЧИКОВ КАТИОННЫХ КАНАЛОВ. 1. К-Na АТФ-азы 2. Са –зависимой АТФ-азы 3. Протонной помпы
 Са внутри клетки 10(-7) Са в межклеточном пространстве 10(-3) ВЫРАВНИВАНИЕ КОНЦЕНТРАЦИЙ ВВИДУ НЕХВАТКИ ЭНЕРГИИ И ОБРАЗОВАНИЯ ДОПОЛНИТЕЛЬНЫХ КАНАЛОВ ПУТЕМ ПРОСТОЙ ДИФФУЗИИ, ПО ГРАДИЕНТУ КОНЦЕНТРАЦИИ.
Са внутри клетки 10(-7) Са в межклеточном пространстве 10(-3) ВЫРАВНИВАНИЕ КОНЦЕНТРАЦИЙ ВВИДУ НЕХВАТКИ ЭНЕРГИИ И ОБРАЗОВАНИЯ ДОПОЛНИТЕЛЬНЫХ КАНАЛОВ ПУТЕМ ПРОСТОЙ ДИФФУЗИИ, ПО ГРАДИЕНТУ КОНЦЕНТРАЦИИ.
 Са внутриклеточно связываясь в избытке со специфическим белком – кальмодулином блокирует внутриклеточный метаболизм + вызывает вазоконстрикцию.
Са внутриклеточно связываясь в избытке со специфическим белком – кальмодулином блокирует внутриклеточный метаболизм + вызывает вазоконстрикцию.
 Наростание внутриклеточно ионов Са и ионов Сl приводит к образованию хлорида кальция – обладающегодополнительным некротическим действием.
Наростание внутриклеточно ионов Са и ионов Сl приводит к образованию хлорида кальция – обладающегодополнительным некротическим действием.
 Н 2 О 2 – ЗЛЕЙШИЙ ВРАГ ЭРИТРОЦИТТОВ. Ввиду переменной валентности железа. Fe 2+ + H 2 O 2 = OH- +. OH + Fe 3+
Н 2 О 2 – ЗЛЕЙШИЙ ВРАГ ЭРИТРОЦИТТОВ. Ввиду переменной валентности железа. Fe 2+ + H 2 O 2 = OH- +. OH + Fe 3+
 Следовательно, активация окислительновосстановительных процессов, с одной стороны, обеспечивает кислородный обмен и высокий субстратный потенциал, а с другой - эффективную утилизацию недоокисленных субстратов и мобилизацию их в окислительных процессах, что ведёт к высокой интенсивности окислительновосстановительных реакций, к синтезу макроэргических интермедиатов и активности анаболического обмена, который, собственно, и поддерживает высокую эффективность ферментативной антиоксидантной защиты.
Следовательно, активация окислительновосстановительных процессов, с одной стороны, обеспечивает кислородный обмен и высокий субстратный потенциал, а с другой - эффективную утилизацию недоокисленных субстратов и мобилизацию их в окислительных процессах, что ведёт к высокой интенсивности окислительновосстановительных реакций, к синтезу макроэргических интермедиатов и активности анаболического обмена, который, собственно, и поддерживает высокую эффективность ферментативной антиоксидантной защиты.
 Принципиальный поход к цитопротекции ЛЮБОГО ГЕНЕЗА Мембраны клеток: нарушение композиции липидного слоя мембран Цитоскелет: бимолеклярного ↑Н+ ацидоз, отек, ишемия, эксайтотоксичность, накопление МНи. СММ образование АФК ↑ свободных радикалов сдвиг НАД+/НАДН 1 Лечение метаболических нарушений 2 Лечение цитокинового дисбаланса Лечение оксидативного стресса 4 Лечение эксайтотоксичности Лечение транскрипционных нарушений 5 3
Принципиальный поход к цитопротекции ЛЮБОГО ГЕНЕЗА Мембраны клеток: нарушение композиции липидного слоя мембран Цитоскелет: бимолеклярного ↑Н+ ацидоз, отек, ишемия, эксайтотоксичность, накопление МНи. СММ образование АФК ↑ свободных радикалов сдвиг НАД+/НАДН 1 Лечение метаболических нарушений 2 Лечение цитокинового дисбаланса Лечение оксидативного стресса 4 Лечение эксайтотоксичности Лечение транскрипционных нарушений 5 3
 ИДЕАЛЬНЫЙ ЦИТОПРОТЕКТОР ДОЛЖНЕН ОКАЗЫВАТЬ СЛЕДУЮЩИЕ ВИДЫ ДЕЙСТВИЯ: Ш СНИЖАТЬ КИСЛОРОДНЫЙ ЗАПРОС КЛЕТОК И ТКАНЕЙ, УВЕЛИЧИВАТЬ КПД ТКАНЕВОГО ДЫХАНИЯ Ш ПОДДЕРЖИВАТЬ И «РАСТОРМАЖИВАТЬ» ГЛИКОЛИЗ «НА ВЫХОДЕ» Ш АКТИВИРОВАТЬ ГЛЮКОНЕОГЕНЕЗ (В АСТРОЦИТАХ) Ш СНИЖАТЬ ЛАКТАТ-АЦИДОЗ Ш ЗАМЕДЛЯТЬ НЕФОСФОРИЛИРУЮЩИЕ ВИДЫ ОКИСЛЕНИЯ (свободно-радикальное окисдение) Ш ЛИМИТИРОВАТЬ ЭКСАЙТОТОКСИЧНОСТЬ И «ВТОРИЧНЫЕ КАСКАДЫ» ИШЕМИИ Ш СОХРАНЯТЬ ХИМИЧЕСКИЕ СИНТЕЗЫ РНК
ИДЕАЛЬНЫЙ ЦИТОПРОТЕКТОР ДОЛЖНЕН ОКАЗЫВАТЬ СЛЕДУЮЩИЕ ВИДЫ ДЕЙСТВИЯ: Ш СНИЖАТЬ КИСЛОРОДНЫЙ ЗАПРОС КЛЕТОК И ТКАНЕЙ, УВЕЛИЧИВАТЬ КПД ТКАНЕВОГО ДЫХАНИЯ Ш ПОДДЕРЖИВАТЬ И «РАСТОРМАЖИВАТЬ» ГЛИКОЛИЗ «НА ВЫХОДЕ» Ш АКТИВИРОВАТЬ ГЛЮКОНЕОГЕНЕЗ (В АСТРОЦИТАХ) Ш СНИЖАТЬ ЛАКТАТ-АЦИДОЗ Ш ЗАМЕДЛЯТЬ НЕФОСФОРИЛИРУЮЩИЕ ВИДЫ ОКИСЛЕНИЯ (свободно-радикальное окисдение) Ш ЛИМИТИРОВАТЬ ЭКСАЙТОТОКСИЧНОСТЬ И «ВТОРИЧНЫЕ КАСКАДЫ» ИШЕМИИ Ш СОХРАНЯТЬ ХИМИЧЕСКИЕ СИНТЕЗЫ РНК
 ВЫВОД : АНТИГИПОКСАНТ ДОЛЖЕН ПРЕПЯТСТВОВАТЬ РАЗВИТИЮ: – ВНУТРИКЛЕТОЧНОГО АЦИДОЗА И ЛЮБЫМ ПУТЕМ АКТИВИРОВАТЬ ГЛИКОЛИЗ – ОКСИДАТИВНОГО СТРЕССА – МЕДИАТОРНОГО СДВИГА – ЦИТОКИНОВОГО ДИСБАЛАНСА ЭТО ОЗНАЧАЕТ, ЧТО ЭФФЕКТИВНЫЙ «АНТИГИПОКСАНТ» ДОЛЖЕН ВОЗДЕЙСТВОВАТЬ КАК МИНИМУМ НА 4 КАСКАДА ГИПОКСИИ, Т. Е. БЫТЬ КОМБИНАЦИЕЙ ВЕЩЕСТВ, ингредиенты которой должны назначаться в определенной последовательности
ВЫВОД : АНТИГИПОКСАНТ ДОЛЖЕН ПРЕПЯТСТВОВАТЬ РАЗВИТИЮ: – ВНУТРИКЛЕТОЧНОГО АЦИДОЗА И ЛЮБЫМ ПУТЕМ АКТИВИРОВАТЬ ГЛИКОЛИЗ – ОКСИДАТИВНОГО СТРЕССА – МЕДИАТОРНОГО СДВИГА – ЦИТОКИНОВОГО ДИСБАЛАНСА ЭТО ОЗНАЧАЕТ, ЧТО ЭФФЕКТИВНЫЙ «АНТИГИПОКСАНТ» ДОЛЖЕН ВОЗДЕЙСТВОВАТЬ КАК МИНИМУМ НА 4 КАСКАДА ГИПОКСИИ, Т. Е. БЫТЬ КОМБИНАЦИЕЙ ВЕЩЕСТВ, ингредиенты которой должны назначаться в определенной последовательности



