5-7 гр. НСL.ppt
- Количество слайдов: 12

КОМУНАЛЬНИЙ ЗАКЛАД «БЕРДЯНСЬКИЙ МЕДИЧНИЙ КОЛЕДЖ» ЗАПОРІЗЬКОЇ ОБЛАСНОЇ РАДИ ЛЕКЦІЯ З ФАРМАЦЕВТИЧНОЇ ХІМІЇ НА ТЕМУ: «VІІ ГРУПА ПЕРІОДИЧНОЇ СИСТЕМИ. ЗАГАЛЬНА ХАРАКТЕРИСТИКА ГРУПИ. ЛІКАРСЬКІ ЗАСОБИ ГАЛОГЕНІВ ТА ЇХ СПОЛУК: ХЛОРОВОДНЕВА КИСЛОТА, . » РОЗРОБЛЕНО: БОНДАРЕНКО О. І. , СПЕЦІАЛІСТОМ ПЕРШОЇ КАТЕГОРІЇ, ВИКЛАДАЧЕМ ФАРМАЦЕВТИЧНОЇ ХІМІЇ 2013 Р.

До головної підгрупи VІІ групи періодичної системи входять галогени: фтор, хлор, бром, йод. Вони зустрічаються у природі. Фтор, бром, йод у числі 15 мікроелементів входять в состав нашого організму. У молекулярній формі жоден з галогенів в природі не зустрічається, тому що їх молекули мають дуже високу реакційну здатність. У більшості своїх сполучень галогени одновалентні. Являються окисниками. По мірі зростання атомної маси зменшуються окисні здібності. Будучи окисниками, галогени застосовуються в медицині як дезінфікуючі речовини. Однак фтор і бром дуже токсичні і в медицині не застосовуються.

Хлор застосовують для обеззараження води. Йод ─ єдиний з галогенів є фармацевтичним препаратом і у вигляді спиртових розчинів (5 і 10 %) застосовується у медицині. Всі галогени мають дуже різкий, подразнюючий запах. Частіше галогени застосовується у медицині у вигляді сполучень з іншими елементами. З цих сполучень значення для медицини мають: Сполучення галогенів з воднем ─ галогеноводні кислоти (HCl, HBr, HI). Значення для медицини має хлороводнева (соляна) кислота. Це єдина мінеральна кислота, яка постійно є у вільному стані в шлунковому соку людини та тварин, де її концентрація близько 0, 3 %. Вона перетворює фермент ─ пепсин в активну форму, знищує патогенні та гнилісні бактерії.

Сполучення галогенів з киснем загальної формули Х 2 О, тобто оксиди , які з водою дають відповідно хлорнуватисту, бромнуватисту, йоднуватисту кислоти: Cl 2 O 2 HCl. O Br 2 O + H 2 O 2 HBr. O I 2 O 2 HIO Cолі цих кислот, головним чином хлорнуватистої (Na. OCl, KOCl) являються фармацевтичними препаратами і називаються гіпохлоритами. Сполучення галогенів з лужними металами ─ галогениди (Na. Cl, KCl, Na. Br, KBr, Na. I, KI).

Кислота хлороводнева концентрована (ДФУ) (Acidum hydrochloridum concentratum) Кислота хлористоводнева розведена (Eur. Ph. ) (Acidum hydrochloridum dilutum) Кислота хлоридна HC 1 М. м. 36, 46

Добування. Промисловий спосіб: прямий синтез з водню та хлору, які утворюються при електролізі розчину натрію хлориду: Схему процесу електролізу можна подати рівнянням: Обидва гази (водень і хлор) спалюють у контактних печах: Отриманий хлороводень НС 1 пропускають крізь поглинальні башти з водою, в результаті чого утворюється хлороводнева кислота з концентрацією 35— 36 % (яка димить).

Властивості. Обидві речовини — безбарвні прозорі рідини, зі своєрідним запахом, кислим смаком; змішуються з водою та спиртом у всіх співвідношеннях з утворенням розчинів сильно кислої реакції. Маючи однакові властивості, розрізняються лише за вмістом хлороводню й відповідно за густиною. Кислота хлористоводнева концентрована повинна містити хлоровод ню межах 35, 0 39, 0 %, відносна густина в становить близько 1, 18. Кислота хлористоводнева розведена містить хлороводню в межах 9, 5 10, 5 %.

Ідентифікація. 1. Розчин лікарської речовини дає характерну реакцію на хлорид іони: Білий осад аргентуму хлориду розчиняється в розчині амоніаку: 2. При нагріванні лікарського засобу з мангану диоксидом виділяється вільний хлор, який виявляють за запахом: 3. Водний розчин субстанції повинен мати сильно кислу реакцію (за кольором індикатора). 4. Реакція сухої речовини з калію дихроматом і кислотою сульфатною папір, просочений розчином дифенілкарбазиду, забарвлюється у фіолетово червоний колір.
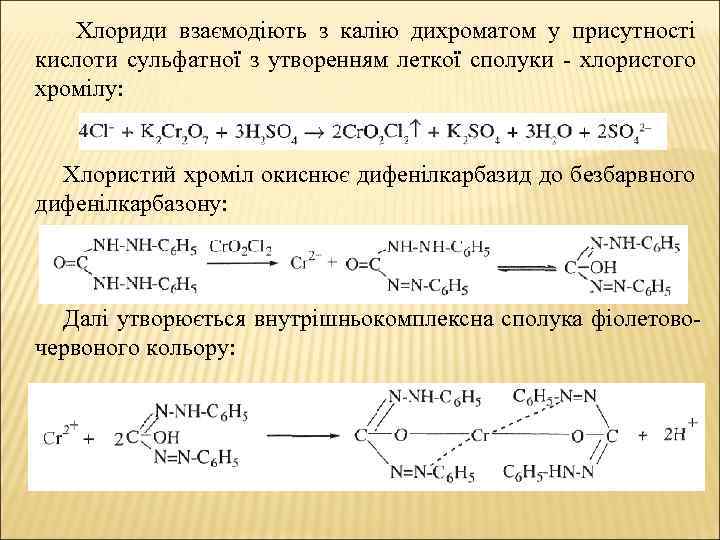
Хлориди взаємодіють з калію дихроматом у присутності кислоти сульфатної з утворенням леткої сполуки хлористого хромілу: Хлористий хроміл окиснює дифенілкарбазид до безбарвного дифенілкарбазону: Далі утворюється внутрішньокомплексна сполука фіолетово червоного кольору:

Специфічні домішки. Вільний хлор. визначають за реакцією з калію йодидом у присутності розчину крохмалю: Протягом 2 хвилин блакитне забарвлення розчину має зникати при додаванні 0, 2 мл 0, 01 М розчину натрію тіосульфату. Сульфати. Субстанцію упарюють насухо з натрію гідрокарбонатом, після чого проводять випробування на сульфати.

Кількісне визначення. 1. Алкаліметрія, пряме титрування, індикатор — метиловий червоний, Е= М. м. : 2. Кількісний вміст хлороводню можна визначити також за густиною. Зберігання. У склянках з притертими пробками при кімнатній температурі. Застосування. Внутрішньо в краплях або у вигляді мікстури (частіше з пепсином) при недостатній кислотності шлункового соку.

Дякую за увагу !
5-7 гр. НСL.ppt