L_5_Komplx_t-e.ppt
- Количество слайдов: 61
 Комплексометрия (основные понятия) n Комплексометрия основана на реакциях образования комплексов. M + L ↔ ML ML + L ↔ ML 2. . . . MLn-1 + L MLn Hg. Cl 2 – меркуриметрия MF 6 n- (M – Al(III), Zr(IV), Th (IV) – фторидометрия M(CN)42 - (M – Co(II), Ni(II), Hg(II), Cu(II) – цианидометрия
Комплексометрия (основные понятия) n Комплексометрия основана на реакциях образования комплексов. M + L ↔ ML ML + L ↔ ML 2. . . . MLn-1 + L MLn Hg. Cl 2 – меркуриметрия MF 6 n- (M – Al(III), Zr(IV), Th (IV) – фторидометрия M(CN)42 - (M – Co(II), Ni(II), Hg(II), Cu(II) – цианидометрия
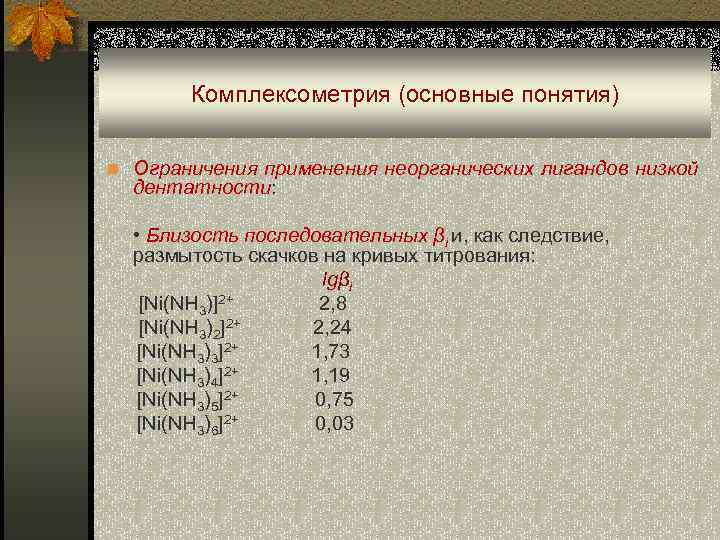 Комплексометрия (основные понятия) n Ограничения применения неорганических лигандов низкой дентатности: • Близость последовательных βi и, как следствие, размытость скачков на кривых титрования: lgβi [Ni(NH 3)]2+ 2, 8 [Ni(NH 3)2]2+ 2, 24 [Ni(NH 3)3]2+ 1, 73 [Ni(NH 3)4]2+ 1, 19 [Ni(NH 3)5]2+ 0, 75 [Ni(NH 3)6]2+ 0, 03
Комплексометрия (основные понятия) n Ограничения применения неорганических лигандов низкой дентатности: • Близость последовательных βi и, как следствие, размытость скачков на кривых титрования: lgβi [Ni(NH 3)]2+ 2, 8 [Ni(NH 3)2]2+ 2, 24 [Ni(NH 3)3]2+ 1, 73 [Ni(NH 3)4]2+ 1, 19 [Ni(NH 3)5]2+ 0, 75 [Ni(NH 3)6]2+ 0, 03
 Комплексометрия (основные понятия) n Ограничения применения неорганических лигандов низкой дентатности: • Нарушение стехиометричности титранта и титруемого вещества в т. э. Cd(H 2 O)4 Cl 2 + NH 3 ↔ [Cd(H 2 O)3 NH 3]2+ ÷ [Cd(NH 3)4]2+ в 1 М NH 3 содержание [Cd(NH 3)4]2+ составляет ~ 85, 4 %. n Наибольшее применение в комплексометрии нашли полидентатные хелатообразующие титранты – комплексоны, которые образуют с ионами металлов устойчивые комплексы чаще всего в стехиометрическом соотношении 1 : 1.
Комплексометрия (основные понятия) n Ограничения применения неорганических лигандов низкой дентатности: • Нарушение стехиометричности титранта и титруемого вещества в т. э. Cd(H 2 O)4 Cl 2 + NH 3 ↔ [Cd(H 2 O)3 NH 3]2+ ÷ [Cd(NH 3)4]2+ в 1 М NH 3 содержание [Cd(NH 3)4]2+ составляет ~ 85, 4 %. n Наибольшее применение в комплексометрии нашли полидентатные хелатообразующие титранты – комплексоны, которые образуют с ионами металлов устойчивые комплексы чаще всего в стехиометрическом соотношении 1 : 1.
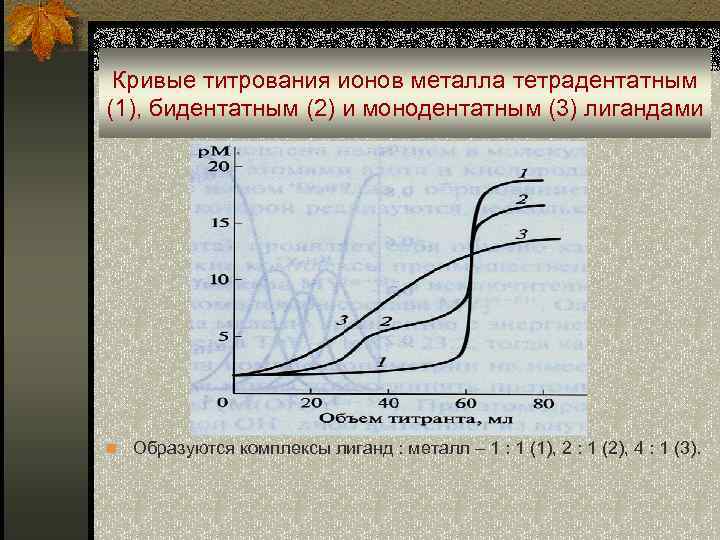 Кривые титрования ионов металла тетрадентатным (1), бидентатным (2) и монодентатным (3) лигандами n Образуются комплексы лиганд : металл – 1 : 1 (1), 2 : 1 (2), 4 : 1 (3).
Кривые титрования ионов металла тетрадентатным (1), бидентатным (2) и монодентатным (3) лигандами n Образуются комплексы лиганд : металл – 1 : 1 (1), 2 : 1 (2), 4 : 1 (3).
 Комплексометрия (основные понятия) n Титрование с использованием комплексонов (полидентатных органических реагентов) называют комплексонометрией. n Комплексоны (Герольд Шварценбах, 1945 г. ) – группа полиаминополиуксусных кислот, содержащих иминодиацетатные фрагменты – N(CH 2 COOH)2, связанные с различными алифатическими и ароматическими радикалами. n Тридентатные – иминодиуксусная (ИДА) и метиламинодиуксусная (МИДА) кислота
Комплексометрия (основные понятия) n Титрование с использованием комплексонов (полидентатных органических реагентов) называют комплексонометрией. n Комплексоны (Герольд Шварценбах, 1945 г. ) – группа полиаминополиуксусных кислот, содержащих иминодиацетатные фрагменты – N(CH 2 COOH)2, связанные с различными алифатическими и ароматическими радикалами. n Тридентатные – иминодиуксусная (ИДА) и метиламинодиуксусная (МИДА) кислота
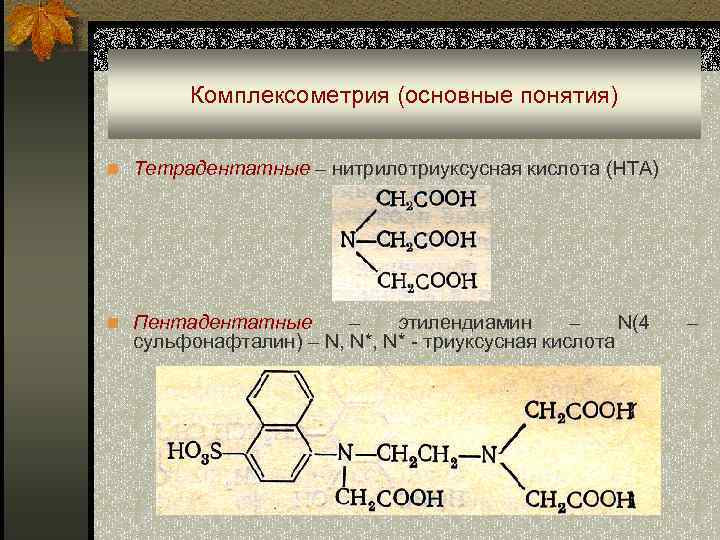 Комплексометрия (основные понятия) n Тетрадентатные – нитрилотриуксусная кислота (НТА) n Пентадентатные – этилендиамин – N(4 сульфонафталин) – N, N* - триуксусная кислота –
Комплексометрия (основные понятия) n Тетрадентатные – нитрилотриуксусная кислота (НТА) n Пентадентатные – этилендиамин – N(4 сульфонафталин) – N, N* - триуксусная кислота –
 Комплексометрия (основные понятия) n Гексадентатные – этиледиамин – N, N, N* тетрауксусная кислота (ЭДТА) n Октадентатные – диэтилентриамин – N, N, N*, N* - пентауксусная кислота (ДТПА)
Комплексометрия (основные понятия) n Гексадентатные – этиледиамин – N, N, N* тетрауксусная кислота (ЭДТА) n Октадентатные – диэтилентриамин – N, N, N*, N* - пентауксусная кислота (ДТПА)
 Комплексометрия (основные понятия) n На практике наиболее часто применяют ЭДТА (Н 4 Y) или ее хорошо растворимую динатриевую соль Na 2 H 2 Y • 2 H 2 O. n ЭДТА – белое кристаллическое вещество, малорастворимое в воде (при температуре 20 0 С растворимость ее составляет 28, 3 мг в 100 мл воды). n Динатриевая соль Na 2 H 2 Y • 2 H 2 O при 22 0 С растворяется до концентрации 108 г/л.
Комплексометрия (основные понятия) n На практике наиболее часто применяют ЭДТА (Н 4 Y) или ее хорошо растворимую динатриевую соль Na 2 H 2 Y • 2 H 2 O. n ЭДТА – белое кристаллическое вещество, малорастворимое в воде (при температуре 20 0 С растворимость ее составляет 28, 3 мг в 100 мл воды). n Динатриевая соль Na 2 H 2 Y • 2 H 2 O при 22 0 С растворяется до концентрации 108 г/л.
 Этилендиаминтетрауксусная кислота (комплексон III)
Этилендиаминтетрауксусная кислота (комплексон III)
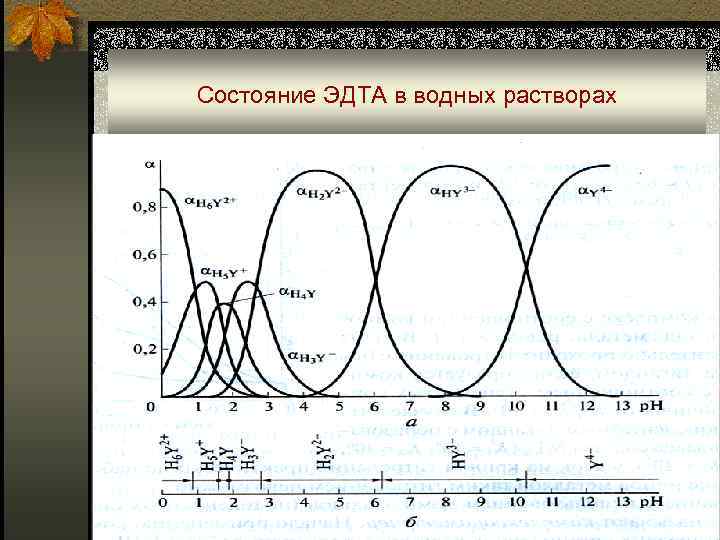 Состояние ЭДТА в водных растворах
Состояние ЭДТА в водных растворах
 Состояние ЭДТА в водных растворах
Состояние ЭДТА в водных растворах
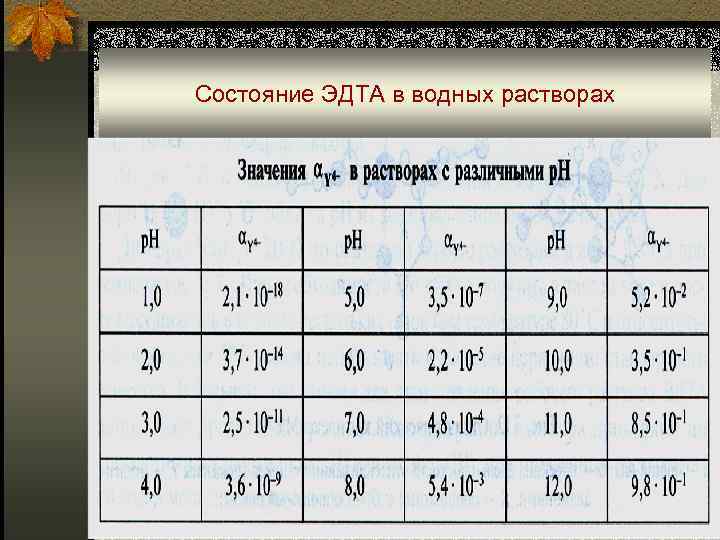 Состояние ЭДТА в водных растворах
Состояние ЭДТА в водных растворах
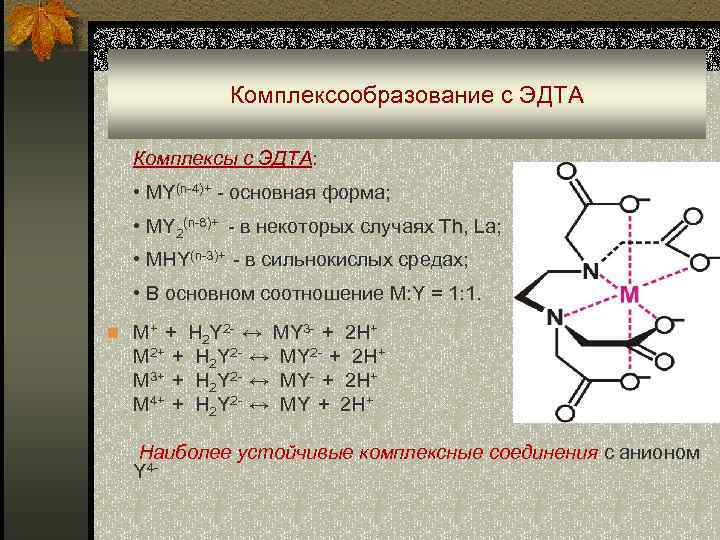 Комплексообразование с ЭДТА Комплексы с ЭДТА: • MY(n-4)+ - основная форма; • MY 2(n-8)+ - в некоторых случаях Th, La; • MHY(n-3)+ - в сильнокислых средах; • В основном соотношение M: Y = 1: 1. n M+ + H 2 Y 2 - ↔ MY 3 - + 2 H+ M 2+ + H 2 Y 2 - ↔ MY 2 - + 2 H+ M 3+ + H 2 Y 2 - ↔ MY- + 2 H+ M 4+ + H 2 Y 2 - ↔ MY + 2 H+ Наиболее устойчивые комплексные соединения с анионом Y 4 -
Комплексообразование с ЭДТА Комплексы с ЭДТА: • MY(n-4)+ - основная форма; • MY 2(n-8)+ - в некоторых случаях Th, La; • MHY(n-3)+ - в сильнокислых средах; • В основном соотношение M: Y = 1: 1. n M+ + H 2 Y 2 - ↔ MY 3 - + 2 H+ M 2+ + H 2 Y 2 - ↔ MY 2 - + 2 H+ M 3+ + H 2 Y 2 - ↔ MY- + 2 H+ M 4+ + H 2 Y 2 - ↔ MY + 2 H+ Наиболее устойчивые комплексные соединения с анионом Y 4 -
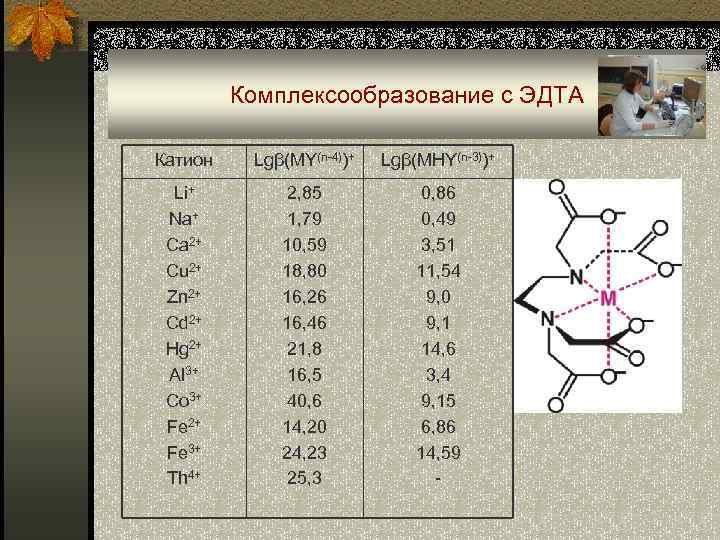 Комплексообразование с ЭДТА Катион Lgβ(MY(n-4))+ Lgβ(MHY(n-3))+ Li+ Na+ Ca 2+ Cu 2+ Zn 2+ Cd 2+ Hg 2+ Al 3+ Co 3+ Fe 2+ Fe 3+ Th 4+ 2, 85 1, 79 10, 59 18, 80 16, 26 16, 46 21, 8 16, 5 40, 6 14, 20 24, 23 25, 3 0, 86 0, 49 3, 51 11, 54 9, 0 9, 1 14, 6 3, 4 9, 15 6, 86 14, 59 -
Комплексообразование с ЭДТА Катион Lgβ(MY(n-4))+ Lgβ(MHY(n-3))+ Li+ Na+ Ca 2+ Cu 2+ Zn 2+ Cd 2+ Hg 2+ Al 3+ Co 3+ Fe 2+ Fe 3+ Th 4+ 2, 85 1, 79 10, 59 18, 80 16, 26 16, 46 21, 8 16, 5 40, 6 14, 20 24, 23 25, 3 0, 86 0, 49 3, 51 11, 54 9, 0 9, 1 14, 6 3, 4 9, 15 6, 86 14, 59 -
 Комплексообразование с ЭДТА Ионы определяемого металла часто присутствуют в титруемом растворе не только в виде свободных ионов Мn+ или комплекса с ЭДТА MY(n – 4)+ , но и в виде комплексов с компонентами буферного раствора или гидроксокомплексов. В этом случае общая концентрация иона металла (С/М запишется: Величина αМ рассчитывается по уравнению
Комплексообразование с ЭДТА Ионы определяемого металла часто присутствуют в титруемом растворе не только в виде свободных ионов Мn+ или комплекса с ЭДТА MY(n – 4)+ , но и в виде комплексов с компонентами буферного раствора или гидроксокомплексов. В этом случае общая концентрация иона металла (С/М запишется: Величина αМ рассчитывается по уравнению
 Комплексообразование с ЭДТА n Условную константу (β|MY) с учетом конкурирующих реакций можно рассчитать, умножив αМ на термодинамическую константу устойчивости комплекса MY(n – 4)+ : n Условную константу (β|MY) устойчивости с учетом конкурирующих реакций иона металла и лиганда рассчитывают:
Комплексообразование с ЭДТА n Условную константу (β|MY) с учетом конкурирующих реакций можно рассчитать, умножив αМ на термодинамическую константу устойчивости комплекса MY(n – 4)+ : n Условную константу (β|MY) устойчивости с учетом конкурирующих реакций иона металла и лиганда рассчитывают:
 Комплексообразование с ЭДТА n Комплексообразование учетом всех конкурирующих реакций: комплекса, протолитических по лиганду и образования гидроксокомплексов по металлу
Комплексообразование с ЭДТА n Комплексообразование учетом всех конкурирующих реакций: комплекса, протолитических по лиганду и образования гидроксокомплексов по металлу
 Комплексообразование с ЭДТА n Комплексообразование учетом всех конкурирующих реакций: комплекса, протолитических по лиганду и образования гидроксокомплексов по металлу
Комплексообразование с ЭДТА n Комплексообразование учетом всех конкурирующих реакций: комплекса, протолитических по лиганду и образования гидроксокомплексов по металлу
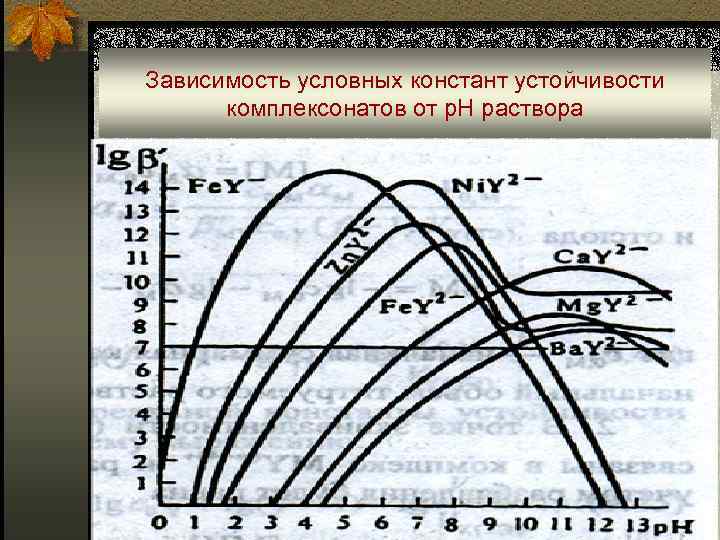 Зависимость условных констант устойчивости комплексонатов от р. Н раствора
Зависимость условных констант устойчивости комплексонатов от р. Н раствора
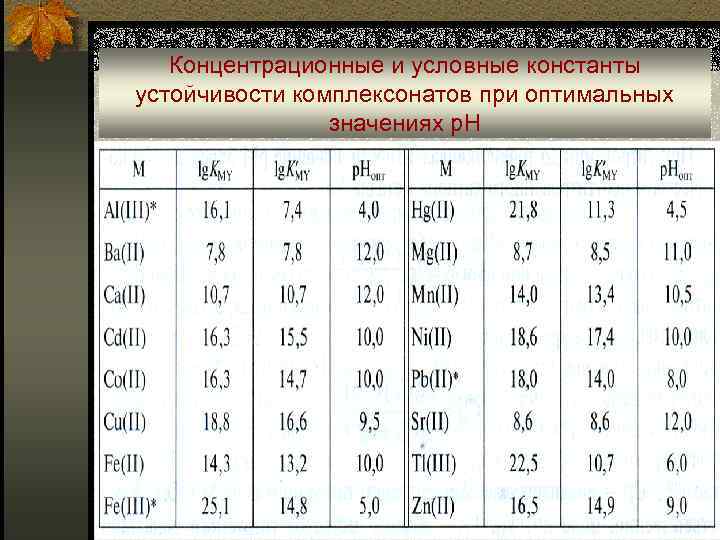 Концентрационные и условные константы устойчивости комплексонатов при оптимальных значениях р. Н
Концентрационные и условные константы устойчивости комплексонатов при оптимальных значениях р. Н
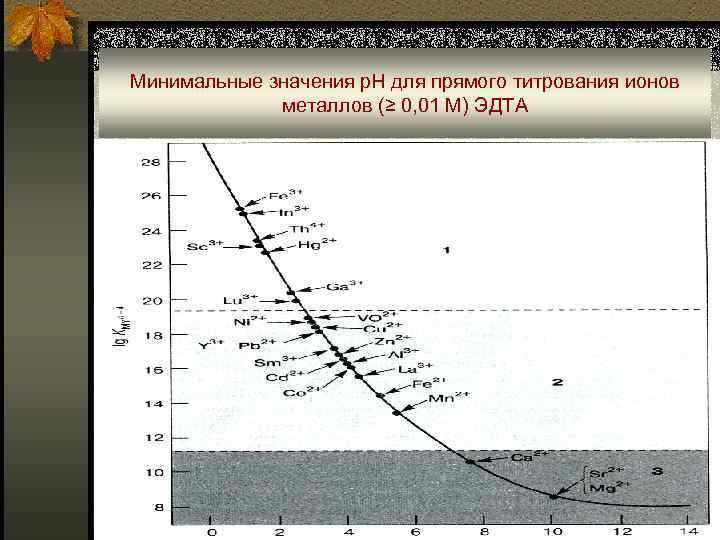 Минимальные значения р. Н для прямого титрования ионов металлов (≥ 0, 01 M) ЭДТА
Минимальные значения р. Н для прямого титрования ионов металлов (≥ 0, 01 M) ЭДТА
 Кривые комплексонометрического титрования p. M = f(τ); M + Y ↔ MY; fi = 1; I = 1; C(M)0 = C(Y)0 ~ [MY] Этапы т - я Состав р - а Уравнение I, 0 ≤ τ <1 M, MY p. M = - lg. C(M)o – lg(τ – 1) II, τ=1 MY C(M)0 βт. MY = ——— [M]2 [M] = (C(M)0/ βт. MY)½ p. M = ½ lg βт. MY - ½ lg (C(M)0
Кривые комплексонометрического титрования p. M = f(τ); M + Y ↔ MY; fi = 1; I = 1; C(M)0 = C(Y)0 ~ [MY] Этапы т - я Состав р - а Уравнение I, 0 ≤ τ <1 M, MY p. M = - lg. C(M)o – lg(τ – 1) II, τ=1 MY C(M)0 βт. MY = ——— [M]2 [M] = (C(M)0/ βт. MY)½ p. M = ½ lg βт. MY - ½ lg (C(M)0
 Кривые комплексонометрического титрования p. M = f(τ); M + Y ↔ MY; fi = 1; I = 1; C(M)0 = C(Y)0 ~ [MY] Этапы т - я Состав р - а III, τ>1 MY, Y Уравнение C(M)0 βт. MY = ———— [M] C(M)0 (τ – 1) 1 [M] = ————— βт. MY (τ – 1) p. M = lg βт. MY + lg (τ – 1)
Кривые комплексонометрического титрования p. M = f(τ); M + Y ↔ MY; fi = 1; I = 1; C(M)0 = C(Y)0 ~ [MY] Этапы т - я Состав р - а III, τ>1 MY, Y Уравнение C(M)0 βт. MY = ———— [M] C(M)0 (τ – 1) 1 [M] = ————— βт. MY (τ – 1) p. M = lg βт. MY + lg (τ – 1)
 Кривые комплексонометрического титрования (реальные условия) n i ≠ 1; βт. MY → βу. MY; p. M → p. C(M); [M]/C(M) = M; p. M = p. C(M) - lg M; p. C(M) = p. M + lg M. I этап: p. C(M) = p. M + lg M = - lg. C(M)o – lg(τ – 1); p. M = - lg. C(M)o – lg M – lg(τ – 1). II этап: p. C(M) = p. M + lg M = ½ lg βу. MY - ½ lg (C(M)0; p. M = ½ lgβт. MY + ½ lg M + ½ lg Y - lg M - ½ lg (C(M)0 = ½ lgβт. MY + ½ lg Y - ½ lg M - ½ lg (C(M)0.
Кривые комплексонометрического титрования (реальные условия) n i ≠ 1; βт. MY → βу. MY; p. M → p. C(M); [M]/C(M) = M; p. M = p. C(M) - lg M; p. C(M) = p. M + lg M. I этап: p. C(M) = p. M + lg M = - lg. C(M)o – lg(τ – 1); p. M = - lg. C(M)o – lg M – lg(τ – 1). II этап: p. C(M) = p. M + lg M = ½ lg βу. MY - ½ lg (C(M)0; p. M = ½ lgβт. MY + ½ lg M + ½ lg Y - lg M - ½ lg (C(M)0 = ½ lgβт. MY + ½ lg Y - ½ lg M - ½ lg (C(M)0.
 Кривые комплексонометрического титрования (реальные условия) n i ≠ 1; βт. MY → βу. MY; p. M → p. C(M); [M]/C(M) = M; p. M = p. C(M) - lg M; p. C(M) = p. M + lg M. III этап: p. C(M) = p. M + lg M = lg βу. MY + lg(τ – 1); p. M = lgβт. MY + lg M + lg Y - lg M + lg(τ – 1); p. M = lgβт. MY + lg(τ – 1). ∆ p. M = lgβт. MY + lg M + lg C(M)0 - 4; ∆ p. M = lgβу. MY + lg C(M)0 - 4.
Кривые комплексонометрического титрования (реальные условия) n i ≠ 1; βт. MY → βу. MY; p. M → p. C(M); [M]/C(M) = M; p. M = p. C(M) - lg M; p. C(M) = p. M + lg M. III этап: p. C(M) = p. M + lg M = lg βу. MY + lg(τ – 1); p. M = lgβт. MY + lg M + lg Y - lg M + lg(τ – 1); p. M = lgβт. MY + lg(τ – 1). ∆ p. M = lgβт. MY + lg M + lg C(M)0 - 4; ∆ p. M = lgβу. MY + lg C(M)0 - 4.
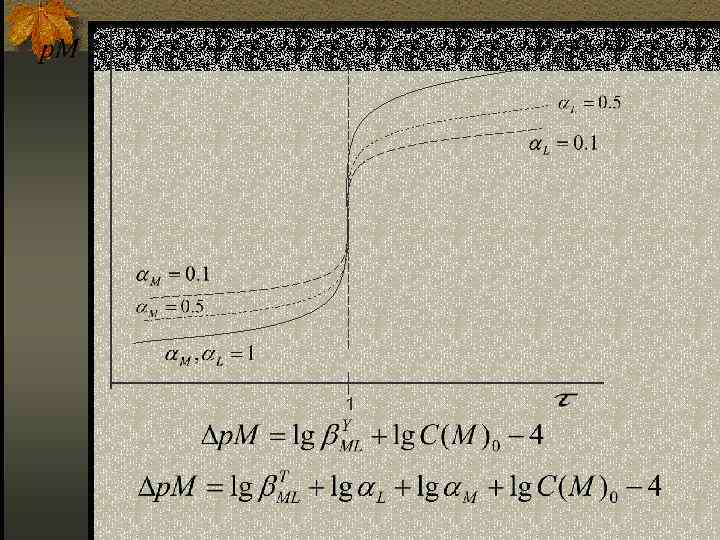 1
1
 Кривые комплексонометрического титрования (реальные условия) n Задача: оценить возможность комплексонометрического титрования в системе Ni(II) – ЭДТА – NH 3 С(Ni 2+) = C(ЭДТА) = C(NH 3) = 0, 1 М; lg βт. Ni. ЭДТА=18, 62; ∆ p. M = lgβт. MY + lg M + lg C(M)0 - 4; 1 Ni(II) = ———————————— = 1+ 0, 1 102, 79 + 0, 12 105, 03 + 0, 13 106, 76+ 0, 14 107, 95 + 0, 15 108, 70 + 0, 16 108, 73 ~ 6, 6 10 -4; lg Ni(II) = -3, 18; Y = 3, 9 10 -2; lg Y = -1, 40; ∆p. M = 18, 62 – 3, 18 -1, 40 -1 -4 = 9, 04 >>0
Кривые комплексонометрического титрования (реальные условия) n Задача: оценить возможность комплексонометрического титрования в системе Ni(II) – ЭДТА – NH 3 С(Ni 2+) = C(ЭДТА) = C(NH 3) = 0, 1 М; lg βт. Ni. ЭДТА=18, 62; ∆ p. M = lgβт. MY + lg M + lg C(M)0 - 4; 1 Ni(II) = ———————————— = 1+ 0, 1 102, 79 + 0, 12 105, 03 + 0, 13 106, 76+ 0, 14 107, 95 + 0, 15 108, 70 + 0, 16 108, 73 ~ 6, 6 10 -4; lg Ni(II) = -3, 18; Y = 3, 9 10 -2; lg Y = -1, 40; ∆p. M = 18, 62 – 3, 18 -1, 40 -1 -4 = 9, 04 >>0
 Кривые комплексонометрического титрования n Кривые комплексонометрического титрования представляют собой зависимости р. М = - lg [M] от степени оттитрованности f. n Равновесные концентрации ионов металла в любой точке рассчитывают с помощью αМ и αY 4 - и соответствующей условной константы устойчивости:
Кривые комплексонометрического титрования n Кривые комплексонометрического титрования представляют собой зависимости р. М = - lg [M] от степени оттитрованности f. n Равновесные концентрации ионов металла в любой точке рассчитывают с помощью αМ и αY 4 - и соответствующей условной константы устойчивости:
 Кривые комплексонометрического титрования n До точки эквивалентности (0 ≤ f < 1) равновесную концентрацию неоттитрованных ионов металла при наличии конкурирующих реакций рассчитывают по уравнениям: n где С 0, М – начальная суммарная концентрация титруемых ионов; V 0, М - начальный объем титруемого раствора; VY – объем раствора ЭДТА.
Кривые комплексонометрического титрования n До точки эквивалентности (0 ≤ f < 1) равновесную концентрацию неоттитрованных ионов металла при наличии конкурирующих реакций рассчитывают по уравнениям: n где С 0, М – начальная суммарная концентрация титруемых ионов; V 0, М - начальный объем титруемого раствора; VY – объем раствора ЭДТА.
 Кривые комплексонометрического титрования n В точке эквивалентности (f = 1) фактически все ионы металла связаны в комплекс MY(n-4)+ и его равновесная концентрация равна: n С учетом того, что С(М) = С(Y), получим:
Кривые комплексонометрического титрования n В точке эквивалентности (f = 1) фактически все ионы металла связаны в комплекс MY(n-4)+ и его равновесная концентрация равна: n С учетом того, что С(М) = С(Y), получим:
 Кривые комплексонометрического титрования n После точки уравнения: эквивалентности (f > 1) используем
Кривые комплексонометрического титрования n После точки уравнения: эквивалентности (f > 1) используем
 Кривые комплексонометрического титрования n После точки уравнения: эквивалентности (f > 1) используем
Кривые комплексонометрического титрования n После точки уравнения: эквивалентности (f > 1) используем
 Кривые комплексонометрического титрования
Кривые комплексонометрического титрования
 Кривые комплексонометрического титрования
Кривые комплексонометрического титрования
 Кривые комплексонометрического титрования
Кривые комплексонометрического титрования
 Кривые комплексонометрического титрования
Кривые комплексонометрического титрования
 Кривые комплексонометрического титрования
Кривые комплексонометрического титрования
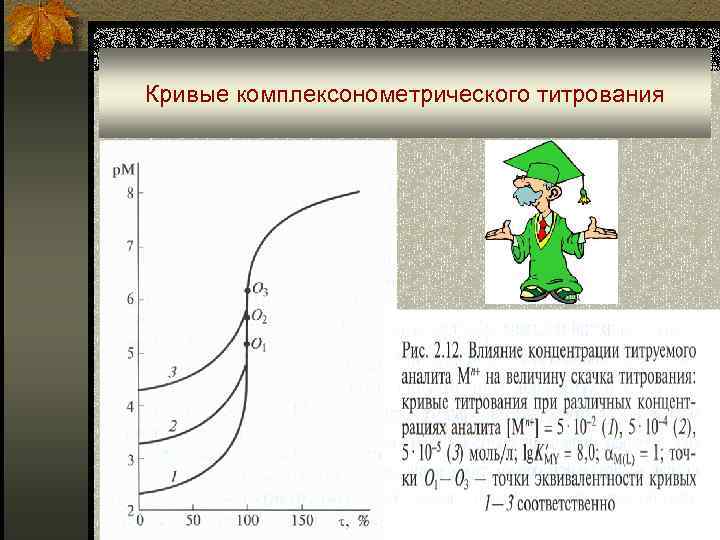 Кривые комплексонометрического титрования
Кривые комплексонометрического титрования
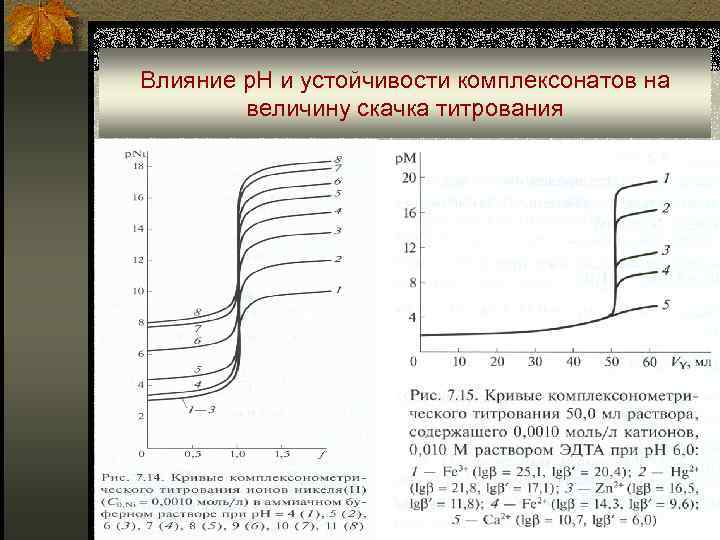 Влияние р. Н и устойчивости комплексонатов на величину скачка титрования
Влияние р. Н и устойчивости комплексонатов на величину скачка титрования
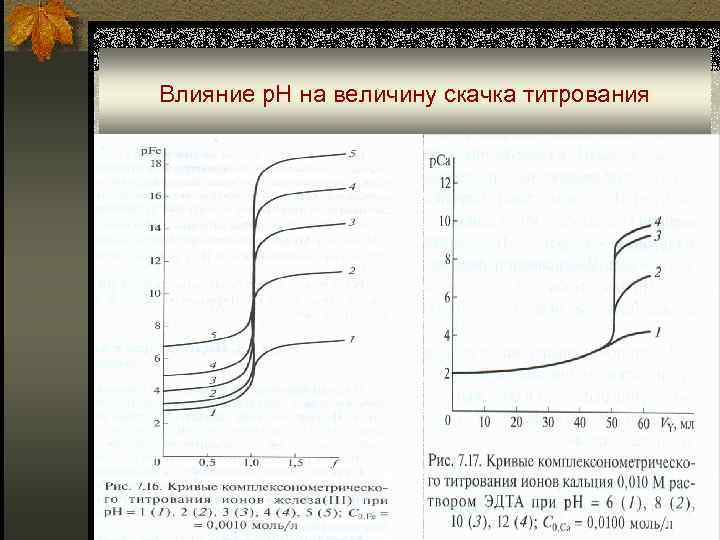 Влияние р. Н на величину скачка титрования
Влияние р. Н на величину скачка титрования
 Индикаторы в комплексонометрии n В комплексонометрии конечную точку титрования устанавливают как визуально, так и с использованием инструментальных методов. n При визуальном способе применяют металлоиндикаторы, которые изменяют окраску в зависимости от концентрации иона металла. n Металлоиндикаторы делят на две группы: • к I группе относятся соединения, которые сами не имеют окраски, но образуют с ионами металлов окрашенные комплексы; • ко II наиболее многочисленной группе относят окрашенные соединения, которые образую с ионами металлов комплексы, отличающиеся по цвету.
Индикаторы в комплексонометрии n В комплексонометрии конечную точку титрования устанавливают как визуально, так и с использованием инструментальных методов. n При визуальном способе применяют металлоиндикаторы, которые изменяют окраску в зависимости от концентрации иона металла. n Металлоиндикаторы делят на две группы: • к I группе относятся соединения, которые сами не имеют окраски, но образуют с ионами металлов окрашенные комплексы; • ко II наиболее многочисленной группе относят окрашенные соединения, которые образую с ионами металлов комплексы, отличающиеся по цвету.
 Металлоиндикаторы I группы: салициловая кислота
Металлоиндикаторы I группы: салициловая кислота
 Металлоиндикаторы I группы: сульфосалициловая кислота
Металлоиндикаторы I группы: сульфосалициловая кислота
 Металлоиндикаторы I группы: тиомочевина
Металлоиндикаторы I группы: тиомочевина
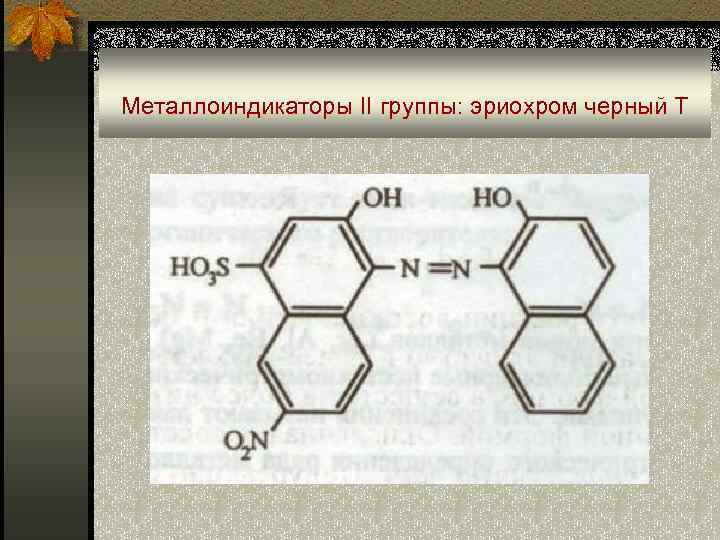 Металлоиндикаторы II группы: эриохром черный Т
Металлоиндикаторы II группы: эриохром черный Т
![Металлоиндикаторы II группы: ПАН [1 -(2 пиридилазо)-2 -нафтол] Металлоиндикаторы II группы: ПАН [1 -(2 пиридилазо)-2 -нафтол]](https://present5.com/presentation/11359852_132090148/image-46.jpg) Металлоиндикаторы II группы: ПАН [1 -(2 пиридилазо)-2 -нафтол]
Металлоиндикаторы II группы: ПАН [1 -(2 пиридилазо)-2 -нафтол]
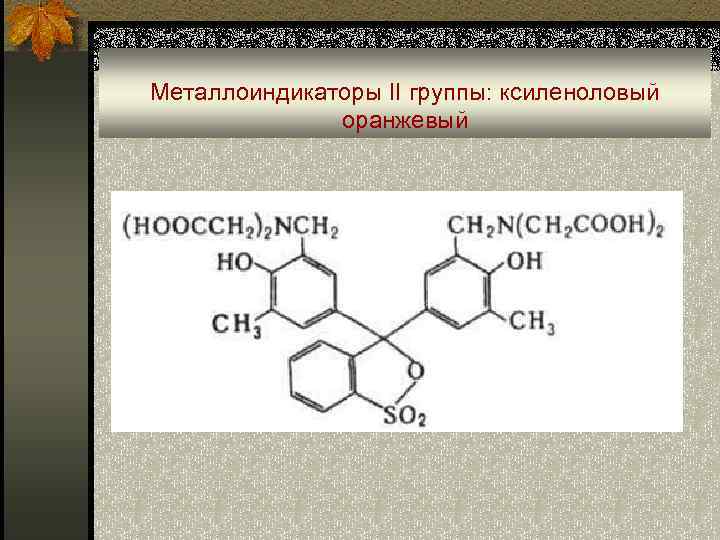 Металлоиндикаторы II группы: ксиленоловый оранжевый
Металлоиндикаторы II группы: ксиленоловый оранжевый
 Индикаторы в комплексонометрии n К металлоиндикаторам предъявляют ряд требований: • образование к. с. M : Jnd, равным 1 : 1 с соотношением условных констант устойчивости 10 < βy. MY/ βy. MInd < 104; • MJnd – кинетическая лабильность, быстрое разрушение с ЭДТА; • изменение окраски индикатора в к. т. т. должно быть контрастным. [MJnd] M + Jnd ↔ MJnd; βу. MJnd = —————; [M] = ———————; [M] C(Jnd) βу. MJnd C(Jnd) p. M = lg βу. MJnd + lg ————; Δp. M = lg βу. MJnd ± 1; [MJnd]
Индикаторы в комплексонометрии n К металлоиндикаторам предъявляют ряд требований: • образование к. с. M : Jnd, равным 1 : 1 с соотношением условных констант устойчивости 10 < βy. MY/ βy. MInd < 104; • MJnd – кинетическая лабильность, быстрое разрушение с ЭДТА; • изменение окраски индикатора в к. т. т. должно быть контрастным. [MJnd] M + Jnd ↔ MJnd; βу. MJnd = —————; [M] = ———————; [M] C(Jnd) βу. MJnd C(Jnd) p. M = lg βу. MJnd + lg ————; Δp. M = lg βу. MJnd ± 1; [MJnd]
 Погрешности комплексонометрического титрования n В общем случае погрешность титрования можно легко найти, зная общие концентрации ионов металла или ЭДТА в конечной точке титрования, степень оттитрованности f и условную константу устойчивости комплекса MY(n-4)+. n Если конечная точка титрования наступает раньше точки эквивалентности, то общая концентрация ионов металла, за исключением связанных в комплекс MY(n-4)+, равна: n Полагаем, что [MY] = Co, M, следовательно:
Погрешности комплексонометрического титрования n В общем случае погрешность титрования можно легко найти, зная общие концентрации ионов металла или ЭДТА в конечной точке титрования, степень оттитрованности f и условную константу устойчивости комплекса MY(n-4)+. n Если конечная точка титрования наступает раньше точки эквивалентности, то общая концентрация ионов металла, за исключением связанных в комплекс MY(n-4)+, равна: n Полагаем, что [MY] = Co, M, следовательно:
 Погрешности комплексонометрического титрования n После подстановки выражения преобразования получаем: для n Тогда погрешность титрования равна: величины С/Y и
Погрешности комплексонометрического титрования n После подстановки выражения преобразования получаем: для n Тогда погрешность титрования равна: величины С/Y и
 Погрешности комплексонометрического титрования n Если конечная точка титрования находится после точки эквивалентности, то общую концентрацию незакомплексованной ЭДТА находим по формуле: n Подставляя значение С/Y в выражение для константы устойчивости получаем: n Учитывая, что [MY] = Co, M, после преобразования имеем:
Погрешности комплексонометрического титрования n Если конечная точка титрования находится после точки эквивалентности, то общую концентрацию незакомплексованной ЭДТА находим по формуле: n Подставляя значение С/Y в выражение для константы устойчивости получаем: n Учитывая, что [MY] = Co, M, после преобразования имеем:
 Погрешности комплексонометрического титрования
Погрешности комплексонометрического титрования
 Погрешности комплексонометрического титрования
Погрешности комплексонометрического титрования
 Погрешности комплексонометрического титрования
Погрешности комплексонометрического титрования
 Погрешности комплексонометрического титрования
Погрешности комплексонометрического титрования
 Погрешности комплексонометрического титрования
Погрешности комплексонометрического титрования
 Проведение комплексонометрического титрования n Прямое титрование. Большинство (около 30) ионов металлов можно определять прямым титрованием раствором ЭДТА в присутствии металлоиндикатора. n При прямом титровании необходимо выполнение следующих условий: • комплексы иона металла с ЭДТА и с металлохромными индикаторами должны быть лабильными; • значения lg βy. MY должны быть не менее 8 (С 0, М = 0, 1 моль/л), погрешность титрования 0, 1 %; • изменение окраски индикатора должно быть контрастным, а интервал его перехода должен укладываться в диапазон р. М скачка на кривой титрования.
Проведение комплексонометрического титрования n Прямое титрование. Большинство (около 30) ионов металлов можно определять прямым титрованием раствором ЭДТА в присутствии металлоиндикатора. n При прямом титровании необходимо выполнение следующих условий: • комплексы иона металла с ЭДТА и с металлохромными индикаторами должны быть лабильными; • значения lg βy. MY должны быть не менее 8 (С 0, М = 0, 1 моль/л), погрешность титрования 0, 1 %; • изменение окраски индикатора должно быть контрастным, а интервал его перехода должен укладываться в диапазон р. М скачка на кривой титрования.
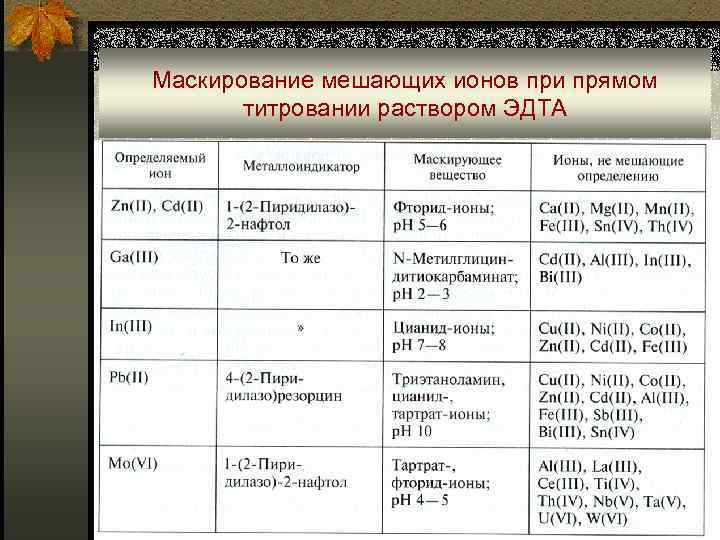 Маскирование мешающих ионов при прямом титровании раствором ЭДТА
Маскирование мешающих ионов при прямом титровании раствором ЭДТА
 Обратное титрование ионов металлов раствором ЭДТА n Обратное титрование применяют в тех случаях, когда невозможно прямое титрование, а именно: • ионы металлов (Co 2+, AI 3+, Cr 3+, Ni 2+ и др. ) очень медленно взаимодействуют с ЭДТА; • в оптимальном для титрования интервале р. Н образуются осадки гидроксидов металлов; • отсутствует подходящий индикатор для фиксирования к. т. т. ; • анализируемые соединения мало растворимы в воде, но хорошо растворимы в ЭДТА (Pb. SO 4, Ca. C 2 O 4, Ca. CO 3, Sr. SO 3 и др. ).
Обратное титрование ионов металлов раствором ЭДТА n Обратное титрование применяют в тех случаях, когда невозможно прямое титрование, а именно: • ионы металлов (Co 2+, AI 3+, Cr 3+, Ni 2+ и др. ) очень медленно взаимодействуют с ЭДТА; • в оптимальном для титрования интервале р. Н образуются осадки гидроксидов металлов; • отсутствует подходящий индикатор для фиксирования к. т. т. ; • анализируемые соединения мало растворимы в воде, но хорошо растворимы в ЭДТА (Pb. SO 4, Ca. C 2 O 4, Ca. CO 3, Sr. SO 3 и др. ).
 Вытеснительное титрование ионов металлов раствором ЭДТА n Этот способ основан на реакции, при которой определяемый ион металла М 1 n+ вытесняет ион металла М 2 m+ из его менее устойчивого комплекса с ЭДТА: М 1 n+ + М 2 Y(4 -m)+ ↔ М 1 Y(4 -n)+ + М 2 m+. n Выделяющиеся ионы металла М 2 m+ в количестве, эквивалентном М 1 n+, титруют раствором ЭДТА в присутствии подходящего индикатора. n Например, вытесняют ионы цинка (II), а затем оттитровывют их в аммиачном буферном растворе с р. Н ≤ 10.
Вытеснительное титрование ионов металлов раствором ЭДТА n Этот способ основан на реакции, при которой определяемый ион металла М 1 n+ вытесняет ион металла М 2 m+ из его менее устойчивого комплекса с ЭДТА: М 1 n+ + М 2 Y(4 -m)+ ↔ М 1 Y(4 -n)+ + М 2 m+. n Выделяющиеся ионы металла М 2 m+ в количестве, эквивалентном М 1 n+, титруют раствором ЭДТА в присутствии подходящего индикатора. n Например, вытесняют ионы цинка (II), а затем оттитровывют их в аммиачном буферном растворе с р. Н ≤ 10.
 Косвенное титрование ионов металлов раствором ЭДТА n Данный способ основан применяют для определения соединений, не образующих комплексы с ЭДТА. n При определении анионов, например, сульфид -, сульфат -, фосфат - ионов, их осаждают избытком стандартного раствора ионов какого-либо металла, осадок отделяют и в фильтрате титруют раствором ЭДТА избыток ионов металлов, не осадившихся определяемым ионом (анионом). n Можно определять ионы по количеству другого иона после растворения осадка, например, ионы натрия по ионам цинка Na. Zn(UO 2)3(CH 3 COO)9 • 6 H 2 O или фосфат - ионы по количеству ионов магния Mg. NH 4 PO 4 • 6 H 2 O.
Косвенное титрование ионов металлов раствором ЭДТА n Данный способ основан применяют для определения соединений, не образующих комплексы с ЭДТА. n При определении анионов, например, сульфид -, сульфат -, фосфат - ионов, их осаждают избытком стандартного раствора ионов какого-либо металла, осадок отделяют и в фильтрате титруют раствором ЭДТА избыток ионов металлов, не осадившихся определяемым ионом (анионом). n Можно определять ионы по количеству другого иона после растворения осадка, например, ионы натрия по ионам цинка Na. Zn(UO 2)3(CH 3 COO)9 • 6 H 2 O или фосфат - ионы по количеству ионов магния Mg. NH 4 PO 4 • 6 H 2 O.


