 КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
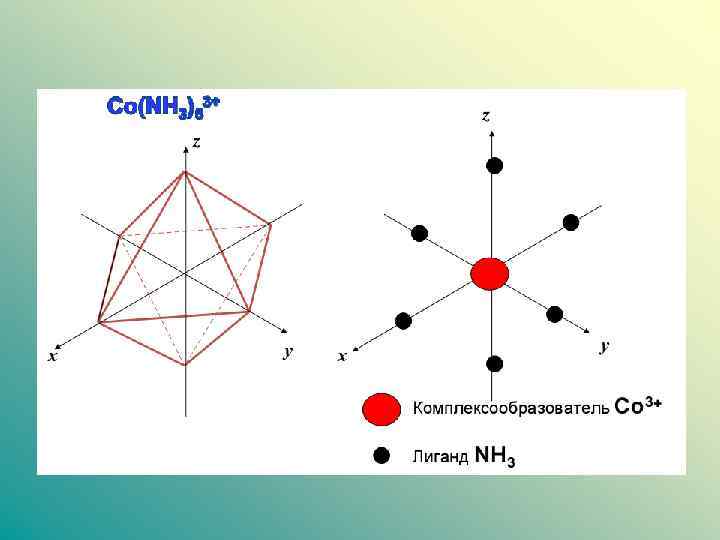
 Заряд комплексного иона (КИ) определяется алгебраической суммой заряда комплексообразователя и зарядов всех лигандов. Различают КИ • катионные ([Co(NH 3)6]3+ [Al(H 2 O)5 OH]2+ ; • анионные ([Fe(CN)6]4 - , [Zn(OH)4]2 - • нейтральные ([Ni(CO)4]0, Co(NH 3)3 Cl 3]0
Заряд комплексного иона (КИ) определяется алгебраической суммой заряда комплексообразователя и зарядов всех лигандов. Различают КИ • катионные ([Co(NH 3)6]3+ [Al(H 2 O)5 OH]2+ ; • анионные ([Fe(CN)6]4 - , [Zn(OH)4]2 - • нейтральные ([Ni(CO)4]0, Co(NH 3)3 Cl 3]0
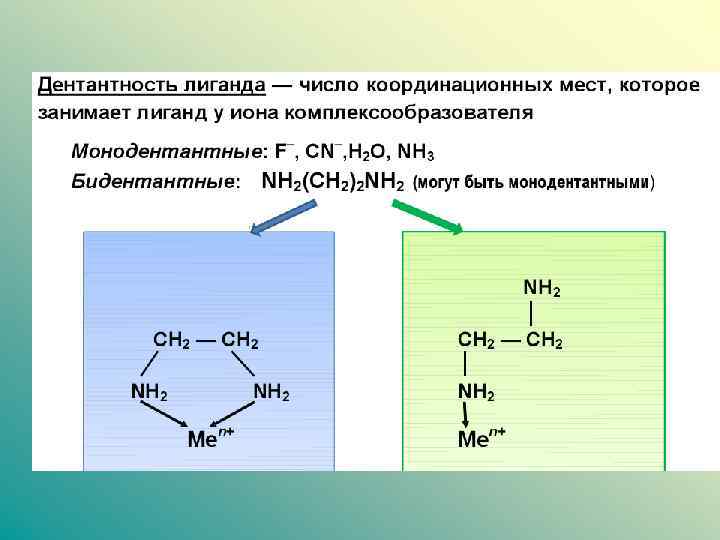
 Лиганды - Простые и сложные ионы - Нейтральные неорганические и органические вещества Координационная емкость – число мест, занимаемых каждым лигандом во внутренней сфере комплекса. Моно, би- и полидентантные лиганды
Лиганды - Простые и сложные ионы - Нейтральные неорганические и органические вещества Координационная емкость – число мест, занимаемых каждым лигандом во внутренней сфере комплекса. Моно, би- и полидентантные лиганды
![>Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl >Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl](https://present5.com/presentation/3/49895079_62241281.pdf-img/49895079_62241281.pdf-4.jpg) Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl • Гидроксокомплексы (Na 2[Zn(ОН 4)]) • Ацидокомплексы (K 4[Fe(CN)6]) • Комплексные соединения смешанного типа [Co(NH 3)4 Cl 2] O C O • Хелатные комплексы M O C O
Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl • Гидроксокомплексы (Na 2[Zn(ОН 4)]) • Ацидокомплексы (K 4[Fe(CN)6]) • Комплексные соединения смешанного типа [Co(NH 3)4 Cl 2] O C O • Хелатные комплексы M O C O
 Положения теории координационной связи • Метод валентных связей Взаимодействие между комплексообразователем и лигандами – донорно-акцепторное. Центральный атом подвергается гибридизации, которая определяет геометрию комплекса. Парамагнетизм объясняется наличием неспаренных электронов.
Положения теории координационной связи • Метод валентных связей Взаимодействие между комплексообразователем и лигандами – донорно-акцепторное. Центральный атом подвергается гибридизации, которая определяет геометрию комплекса. Парамагнетизм объясняется наличием неспаренных электронов.
 Теория кристаллического поля (ТПК) Взаимодействие между комплексообразователем и лигандами – подчиняется закону Кулона. Все частицы- недеформированные шары с определенным зарядом и радиусом. Поле лигандов влияет на энергетическое состояние комплексообразователя. При увеличении вклада доли ковалентной связи взаимодействие описывается на основе метода молекулярных орбиталей
Теория кристаллического поля (ТПК) Взаимодействие между комплексообразователем и лигандами – подчиняется закону Кулона. Все частицы- недеформированные шары с определенным зарядом и радиусом. Поле лигандов влияет на энергетическое состояние комплексообразователя. При увеличении вклада доли ковалентной связи взаимодействие описывается на основе метода молекулярных орбиталей
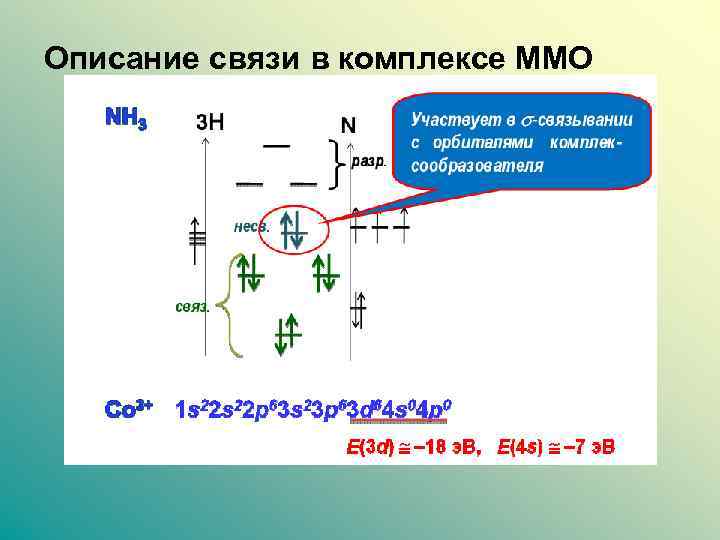
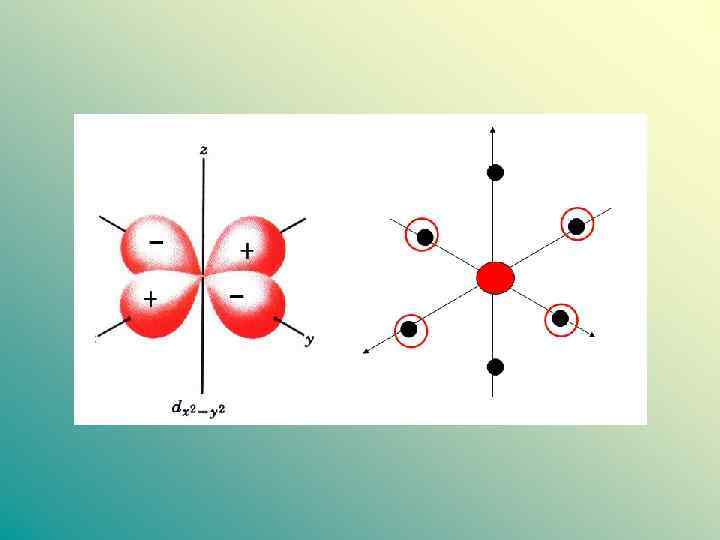
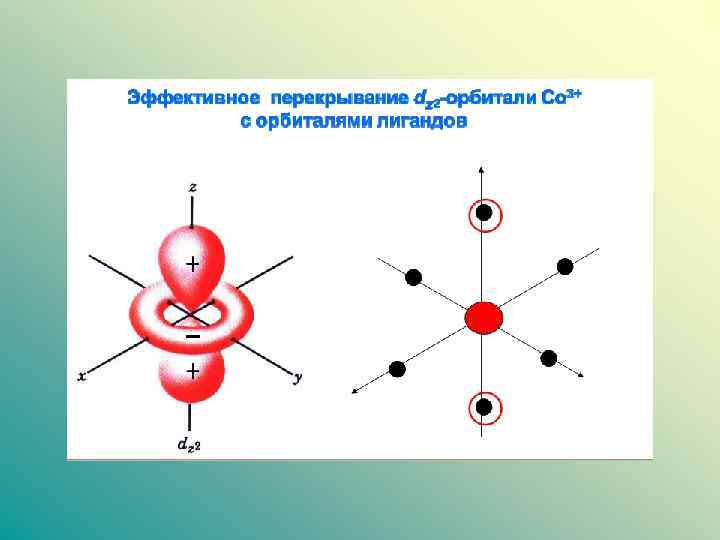
 Описание связи в комплексе ММО
Описание связи в комплексе ММО
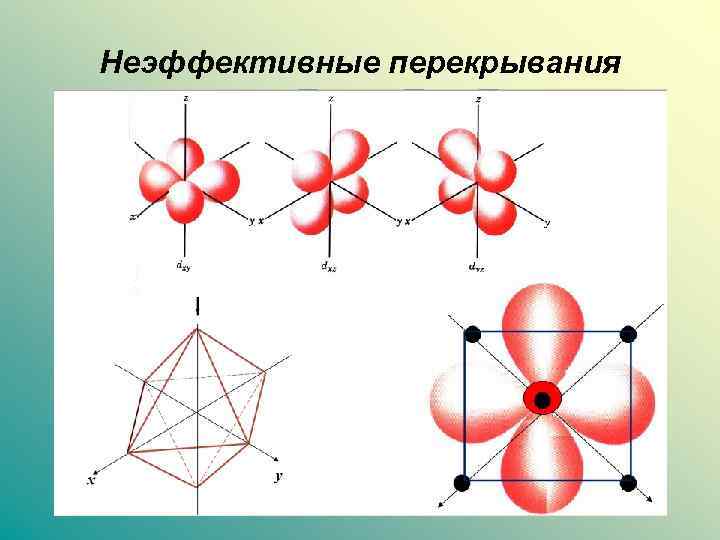
 Неэффективные перекрывания
Неэффективные перекрывания
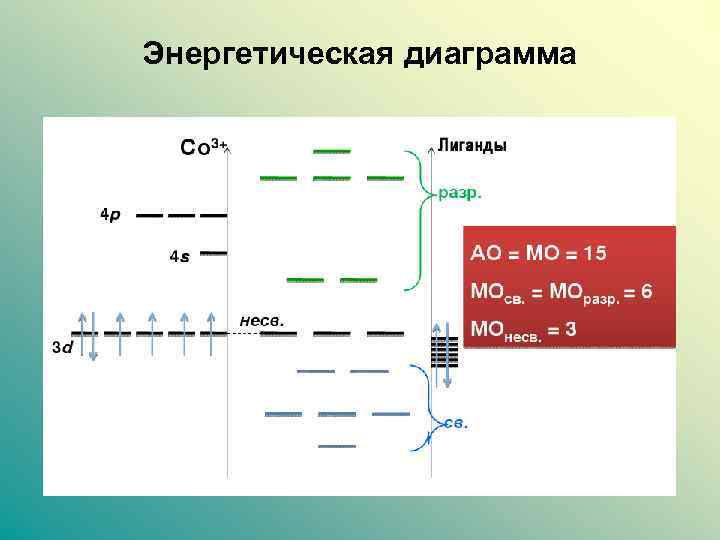
 Энергетическая диаграмма
Энергетическая диаграмма
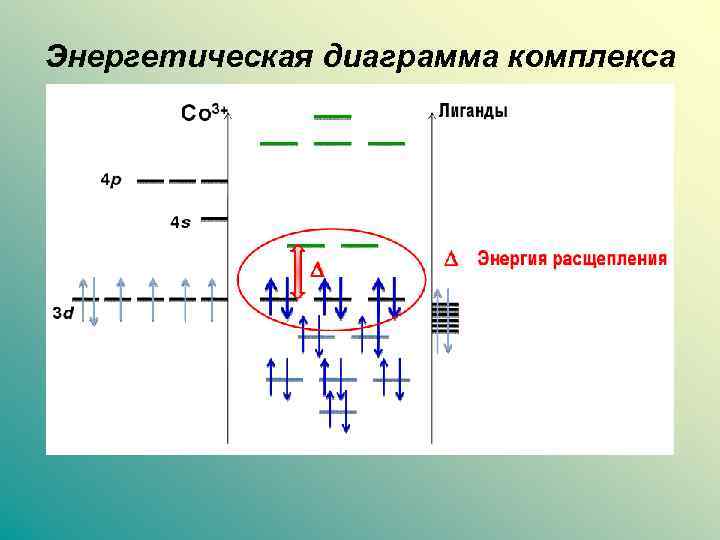
 Энергетическая диаграмма комплекса
Энергетическая диаграмма комплекса
![>Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ + >Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ +](https://present5.com/presentation/3/49895079_62241281.pdf-img/49895079_62241281.pdf-11.jpg) Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ + Cl- Вторичная: [Ag(NН 3)2]+ = Ag+ + 2 NH 3 Константа нестойкости
Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ + Cl- Вторичная: [Ag(NН 3)2]+ = Ag+ + 2 NH 3 Константа нестойкости




![Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl](https://present5.com/presentation/3/49895079_62241281.pdf-img/49895079_62241281.pdf-4.jpg)






![Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ + Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ +](https://present5.com/presentation/3/49895079_62241281.pdf-img/49895079_62241281.pdf-11.jpg)













![Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl Классификация комплексных соединений • Аквакомплексы ([Cr(Н 2 О)6]Cl 3 • Аммиакаты (Ag(NН 3)2]Cl](https://present5.com/presentation/3/49895079_62241281.pdf-img/49895079_62241281.pdf-4.jpg)






![Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ + Устойчивость комплексных соединений Диссоциация первичная (сильный электролит): [Ag(NН 3)2]Cl = [Ag(NН 3)2]+ +](https://present5.com/presentation/3/49895079_62241281.pdf-img/49895079_62241281.pdf-11.jpg)
















