КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ в аналитике.ppt
- Количество слайдов: 40
 Комплексные соединения в аналитической химии
Комплексные соединения в аналитической химии
 План 1. Общие положения и понятия комплексных соединений. Номенклатура комплексных соединений 2. Виды комплексных соединений 3. Способы получения комплексных соединений. 4. Диссоциация комплексных соединений в растворах 5. Равновесие в растворах комплексных соединений. 6. Устойчивость комплексных соединений Литература: Харитонов Ю. Я. т. 1, гл. 7, § 7. 1 -7. 9, стр. 179 -223
План 1. Общие положения и понятия комплексных соединений. Номенклатура комплексных соединений 2. Виды комплексных соединений 3. Способы получения комплексных соединений. 4. Диссоциация комплексных соединений в растворах 5. Равновесие в растворах комплексных соединений. 6. Устойчивость комплексных соединений Литература: Харитонов Ю. Я. т. 1, гл. 7, § 7. 1 -7. 9, стр. 179 -223
 1. Общие положения и понятия комплексных соединений. Номенклатура комплексных соединений Комплексные соединения – устойчивые химические соединения сложного состава, в которых обязательно имеется хотя бы одна связь, образованная по донорно – акцепторному механизму.
1. Общие положения и понятия комплексных соединений. Номенклатура комплексных соединений Комплексные соединения – устойчивые химические соединения сложного состава, в которых обязательно имеется хотя бы одна связь, образованная по донорно – акцепторному механизму.
 Комплексные соединения (лат. complexus — сочетание, обхват), или координационные соединения (лат. co — «вместе» иordinatio — «упорядочение» ) — частицы (нейтральные молекулы или ионы), которые образуются в результате присоединения к данному иону (или атому), называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами. Теория комплексных соединений (координационная теория) была в 1893 г. А. предложена Вернером.
Комплексные соединения (лат. complexus — сочетание, обхват), или координационные соединения (лат. co — «вместе» иordinatio — «упорядочение» ) — частицы (нейтральные молекулы или ионы), которые образуются в результате присоединения к данному иону (или атому), называемому комплексообразователем, нейтральных молекул или других ионов, называемых лигандами. Теория комплексных соединений (координационная теория) была в 1893 г. А. предложена Вернером.
 Швейцарский химик Альфред Вернер (1866 -1919). Координационная теория Вернера 1893 года была первой попыткой объяснить структуру комплексных соединений. Эта теория была предложена до открытия электрона Томсоном в 1896 году, и до разработки электронной теории валентности. Вернер не имел в своём распоряжении никаких инструментальных методов исследований, а все его исследования были сделаны интерпретацией простых химических реакций.
Швейцарский химик Альфред Вернер (1866 -1919). Координационная теория Вернера 1893 года была первой попыткой объяснить структуру комплексных соединений. Эта теория была предложена до открытия электрона Томсоном в 1896 году, и до разработки электронной теории валентности. Вернер не имел в своём распоряжении никаких инструментальных методов исследований, а все его исследования были сделаны интерпретацией простых химических реакций.
 Характерная особенность комплексных соединений – наличие в них химической связи, возникшей по донорно-акцепторному механизму: М(□)n + n↑↓L → [М (↓↑L)n] комплексообразователь лиганды Комплексная частица – сложная частица, способная к самостоятельному существованию в кристалле или растворе, образованная из других, более простых частиц, также способных к самостоятельному существованию. Иногда комплексными частицами называют сложные химические частицы, все или часть связей в которых образованы подонорноакцепторному механизму.
Характерная особенность комплексных соединений – наличие в них химической связи, возникшей по донорно-акцепторному механизму: М(□)n + n↑↓L → [М (↓↑L)n] комплексообразователь лиганды Комплексная частица – сложная частица, способная к самостоятельному существованию в кристалле или растворе, образованная из других, более простых частиц, также способных к самостоятельному существованию. Иногда комплексными частицами называют сложные химические частицы, все или часть связей в которых образованы подонорноакцепторному механизму.
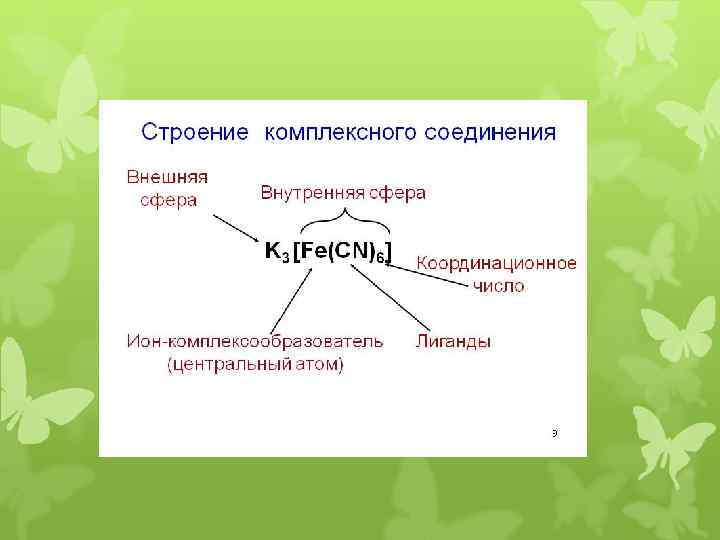
 Комплексообразователь – это центральный атом или ион, который является акцептором электронных пар, предоставляя свободные АО, и занимает центральное положение в комплексном соединении. Обычно комплексообразователь – атом элемента, образующего металл, но это может быть и атом кислорода, азота, серы, йода и других элементов, образующих неметаллы. Комплексообразователь обычно положительно заряжен и в таком случае именуется в современной научной литературе металлоцентром; заряд комплексообразователя может быть также отрицательным или равным нулю. Лиганды – это молекулы или ионы, которые являются донорами электронных пар и непосредственно связанные с комплексообразователем.
Комплексообразователь – это центральный атом или ион, который является акцептором электронных пар, предоставляя свободные АО, и занимает центральное положение в комплексном соединении. Обычно комплексообразователь – атом элемента, образующего металл, но это может быть и атом кислорода, азота, серы, йода и других элементов, образующих неметаллы. Комплексообразователь обычно положительно заряжен и в таком случае именуется в современной научной литературе металлоцентром; заряд комплексообразователя может быть также отрицательным или равным нулю. Лиганды – это молекулы или ионы, которые являются донорами электронных пар и непосредственно связанные с комплексообразователем.
 Обычно лигандами являются ионы или молекулы, содержащие неподеленные электронные пары или достаточно подвижные π-электронные пары.
Обычно лигандами являются ионы или молекулы, содержащие неподеленные электронные пары или достаточно подвижные π-электронные пары.
 Внутренняя сфера комплексного соединения – центральный атом со связанными с ним лигандами, то есть, собственно, комплексная частица. Заряд комплексного иона равен алгебраической сумме зарядов центрального иона и лигандов. Например, заряд комплексного иона Fe(CN)64 - равен (2+) + (6 -) = 4 -, т. к. заряд иона-комплексообразователя 2+, суммарный заряд лигандов 6 -. Следовательно, ион Fe(CN)64 - - комплексный анион. Внешняя сфера комплексного соединения – остальные частицы, связанные с комплексной частицей ионной или межмолекулярными связями, включая водородные. Дентатность лиганда определяется числом координационных мест, занимаемых лигандом в координационной сфере комплексообразователя. Различают монодентатные (унидентатные) лиганды, связанные с центральным атомом через один из своих атомов, то есть одной ковалентной связью), бидентатные (связанные с центральным атомом через два своих атома, то есть, двумя связями), три- , тетрадентатные и т. д.
Внутренняя сфера комплексного соединения – центральный атом со связанными с ним лигандами, то есть, собственно, комплексная частица. Заряд комплексного иона равен алгебраической сумме зарядов центрального иона и лигандов. Например, заряд комплексного иона Fe(CN)64 - равен (2+) + (6 -) = 4 -, т. к. заряд иона-комплексообразователя 2+, суммарный заряд лигандов 6 -. Следовательно, ион Fe(CN)64 - - комплексный анион. Внешняя сфера комплексного соединения – остальные частицы, связанные с комплексной частицей ионной или межмолекулярными связями, включая водородные. Дентатность лиганда определяется числом координационных мест, занимаемых лигандом в координационной сфере комплексообразователя. Различают монодентатные (унидентатные) лиганды, связанные с центральным атомом через один из своих атомов, то есть одной ковалентной связью), бидентатные (связанные с центральным атомом через два своих атома, то есть, двумя связями), три- , тетрадентатные и т. д.
 Координационное число (КЧ) – число - связей, образуемых центральным атомом с лигандами. Для комплексных соединений с монодентантными лигандами КЧ равно числу лигандов, а в случае полидентантных лигандов - числу таких лигандов, умноженному на дентатность. Различают характеристическое и максимальное координационные числа. Максимальное координационное число (м. к. ч. ), определяется свойствами центрального атома и не зависит от природы лиганда. Оно может быть равно 4 или 6 и более, если позволяет пространство. Характеристическое координационное число (х. к. ч. ) в основном определяется природой лиганда. Так, ионы серебра и ртути (II) в аммиакатах, галогенидах и гидроксокомплексах имеют характеристическое координационное число равное 2 и максимальное координационное число равное 4.
Координационное число (КЧ) – число - связей, образуемых центральным атомом с лигандами. Для комплексных соединений с монодентантными лигандами КЧ равно числу лигандов, а в случае полидентантных лигандов - числу таких лигандов, умноженному на дентатность. Различают характеристическое и максимальное координационные числа. Максимальное координационное число (м. к. ч. ), определяется свойствами центрального атома и не зависит от природы лиганда. Оно может быть равно 4 или 6 и более, если позволяет пространство. Характеристическое координационное число (х. к. ч. ) в основном определяется природой лиганда. Так, ионы серебра и ртути (II) в аммиакатах, галогенидах и гидроксокомплексах имеют характеристическое координационное число равное 2 и максимальное координационное число равное 4.
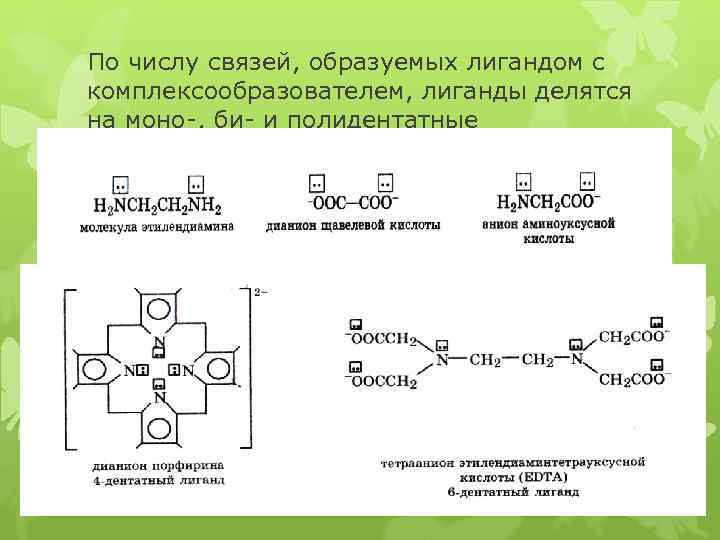 По числу связей, образуемых лигандом с комплексообразователем, лиганды делятся на моно-, би- и полидентатные
По числу связей, образуемых лигандом с комплексообразователем, лиганды делятся на моно-, би- и полидентатные
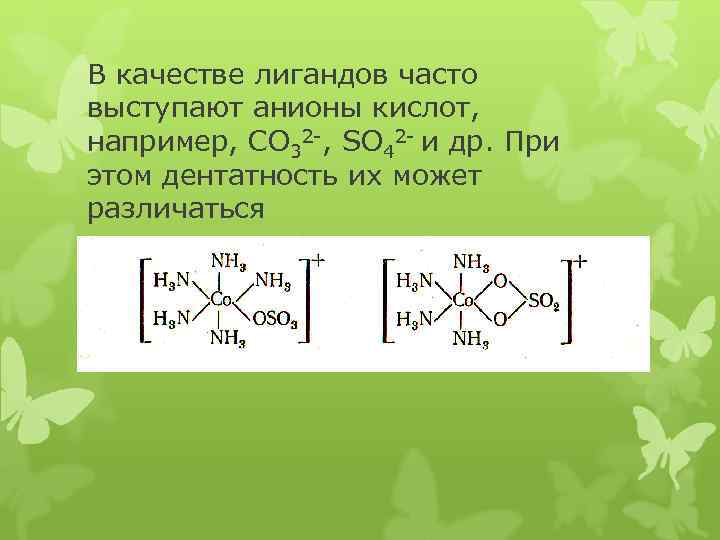 В качестве лигандов часто выступают анионы кислот, например, CO 32 -, SO 42 - и др. При этом дентатность их может различаться
В качестве лигандов часто выступают анионы кислот, например, CO 32 -, SO 42 - и др. При этом дентатность их может различаться
 2. Виды комплексных соединений Существует несколько классификации комплексных соединений в основу которых положены различные принципы. I. В зависимости от заряда внутренней сферы комплексные соединения подразделяются на анионные, катионные и нейтральные комплексы. 1) Катионные комплексы образованы в результате координации вокруг положительного иона нейтральных молекул (H 2 O, NH 3 и др. ). [(Zn(NH 3)4)]Cl 2 — хлорид тетраамминцинка(II) [Co(NH 3)6]Cl 3 — хлорид гексаамминкобальта(II) 2) Анионные комплексы: в роли комплексообразователя выступает атом с положительной степенью окисления, а лигандами являются простые или сложные анионы. K 2[Be. F 4] — тетрафторобериллат(II) калия Li[Al. H 4] — тетрагидридоалюминат(III) лития K 3[Fe(CN)6] — гексацианоферрат(III) калия 3) Нейтральные комплексы образуются при координации молекул вокруг нейтрального атома, а так же при одновременной координации вокруг положительного иона — комплексообразователя отрицательных ионов и молекул. [Ni(CO)4] — тетракарбонилникель [Pt(NH 3)2 Cl 2] — дихлородиамминплатина (II)
2. Виды комплексных соединений Существует несколько классификации комплексных соединений в основу которых положены различные принципы. I. В зависимости от заряда внутренней сферы комплексные соединения подразделяются на анионные, катионные и нейтральные комплексы. 1) Катионные комплексы образованы в результате координации вокруг положительного иона нейтральных молекул (H 2 O, NH 3 и др. ). [(Zn(NH 3)4)]Cl 2 — хлорид тетраамминцинка(II) [Co(NH 3)6]Cl 3 — хлорид гексаамминкобальта(II) 2) Анионные комплексы: в роли комплексообразователя выступает атом с положительной степенью окисления, а лигандами являются простые или сложные анионы. K 2[Be. F 4] — тетрафторобериллат(II) калия Li[Al. H 4] — тетрагидридоалюминат(III) лития K 3[Fe(CN)6] — гексацианоферрат(III) калия 3) Нейтральные комплексы образуются при координации молекул вокруг нейтрального атома, а так же при одновременной координации вокруг положительного иона — комплексообразователя отрицательных ионов и молекул. [Ni(CO)4] — тетракарбонилникель [Pt(NH 3)2 Cl 2] — дихлородиамминплатина (II)
 II. По природе лиганда 1) Аммиакаты — комплексы, в которых лигандами служат молекулы аммиака, например: [Cu(NH 3)4]SO 4, [Co(NH 3)6]Cl 3, [Pt(NH 3)6]Cl 4 и др. 2) Аквакомплексы — в которых лигандом выступает вода: [Co(H 2 O)6]Cl 2, [Al(H 2 O)6]Cl 3 и др. 3) Карбонилы — комплексные соединения, в которых лигандами являются молекулы оксида углерода (II): [Fe(CO)5], [Ni(CO)4]. 4) Ацидокомплексы — комплексы, в которых лигандами являются кислотные остатки. К ним относятся комплексные соли: K 2[Pt. Cl 4], комплексные кислоты: H 2[Co. Cl 4], H 2[Si. F 6]. 5) Гидроксокомплексы — комплексные соединения, в которых в качестве лигандов выступают гидроксид-ионы: Na 2[Zn(OH)4], Na 2[Sn(OH)6] и др.
II. По природе лиганда 1) Аммиакаты — комплексы, в которых лигандами служат молекулы аммиака, например: [Cu(NH 3)4]SO 4, [Co(NH 3)6]Cl 3, [Pt(NH 3)6]Cl 4 и др. 2) Аквакомплексы — в которых лигандом выступает вода: [Co(H 2 O)6]Cl 2, [Al(H 2 O)6]Cl 3 и др. 3) Карбонилы — комплексные соединения, в которых лигандами являются молекулы оксида углерода (II): [Fe(CO)5], [Ni(CO)4]. 4) Ацидокомплексы — комплексы, в которых лигандами являются кислотные остатки. К ним относятся комплексные соли: K 2[Pt. Cl 4], комплексные кислоты: H 2[Co. Cl 4], H 2[Si. F 6]. 5) Гидроксокомплексы — комплексные соединения, в которых в качестве лигандов выступают гидроксид-ионы: Na 2[Zn(OH)4], Na 2[Sn(OH)6] и др.
 III. По числу мест занимаемых лигандами в координационной сфере 1) Монодентатные лиганды. Такие лиганды бывают нейтральными (молекулы Н 2 О, NH 3, CO, NO и др. ) и заряженными (ионы CN−, F−, Cl−, OH−, SCN−, S 2 O 32− и др. ). 2) Бидентатные лиганды. Примерами служат лиганды: ион аминоуксусной кислоты H 2 N — CH 2 — COO−, оксалатный ион −O — CO — O−, карбонат-ион СО 32−, сульфат-ион SO 42−. 3) Полидентатные лиганды. Например, комплексоны - органические лиганды, содержащие в своем составе несколько групп −С≡N или −COOH (этилендиаминтетрауксусная кислота — ЭДТА). Циклические комплексы, образуемые некоторыми полидентатными лигандами, относят к хелатным (гемоглобин и др. ).
III. По числу мест занимаемых лигандами в координационной сфере 1) Монодентатные лиганды. Такие лиганды бывают нейтральными (молекулы Н 2 О, NH 3, CO, NO и др. ) и заряженными (ионы CN−, F−, Cl−, OH−, SCN−, S 2 O 32− и др. ). 2) Бидентатные лиганды. Примерами служат лиганды: ион аминоуксусной кислоты H 2 N — CH 2 — COO−, оксалатный ион −O — CO — O−, карбонат-ион СО 32−, сульфат-ион SO 42−. 3) Полидентатные лиганды. Например, комплексоны - органические лиганды, содержащие в своем составе несколько групп −С≡N или −COOH (этилендиаминтетрауксусная кислота — ЭДТА). Циклические комплексы, образуемые некоторыми полидентатными лигандами, относят к хелатным (гемоглобин и др. ).


 3. Способы получения комплексных соединений. 1. По типу присоединения: Bi. I 3 + KI → K[Bi. I 4] тетрайодовисмутат (III) калия 2. По типу внедрения: Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 сульфат тетрааминмеди (II) 3. Растворение металла в смеси: 3 Pt + 4 HNO 3 + 18 HCl → 4 NO + 3 H 2[Pt. Cl 6] + 8 H 2 O гексахлороплатинат (IV) водорода 4. По способу вытеснения: Na 3[Co(NO 2)6] + H 2 C 2 O 4 → Na 3[Co(C 2 O 4)(NO 2)4] + 2 HNO 2 тетранитритомонооксалатокобальтат (III) натрия 5. В случае окислительно-восстановительных реакций: Сo. Cl 2+7 Na. NO 2+2 CH 3 COOH→Na 3[Co(NO 2)6]+2 Na. Cl+2 CH 3 COONa+CO 2+ H 2 O 1.
3. Способы получения комплексных соединений. 1. По типу присоединения: Bi. I 3 + KI → K[Bi. I 4] тетрайодовисмутат (III) калия 2. По типу внедрения: Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 сульфат тетрааминмеди (II) 3. Растворение металла в смеси: 3 Pt + 4 HNO 3 + 18 HCl → 4 NO + 3 H 2[Pt. Cl 6] + 8 H 2 O гексахлороплатинат (IV) водорода 4. По способу вытеснения: Na 3[Co(NO 2)6] + H 2 C 2 O 4 → Na 3[Co(C 2 O 4)(NO 2)4] + 2 HNO 2 тетранитритомонооксалатокобальтат (III) натрия 5. В случае окислительно-восстановительных реакций: Сo. Cl 2+7 Na. NO 2+2 CH 3 COOH→Na 3[Co(NO 2)6]+2 Na. Cl+2 CH 3 COONa+CO 2+ H 2 O 1.
 4. Диссоциация комплексных соединений в растворах Комплексные соединения - неэлектролиты в водных растворах диссоциации не подвергаются. У них отсутствует внешняя сфера комплекса, например: [Zn(NH 3)2 Cl 2] [Co(NH 3)3(NO 3)3] [Pt(NH 3)2 Cl 2] дихлородиаминоцинк тринитротриаминокобальт дихлородиаминоплатина В водной среде такие молекулы гидратируются как единое соединение. Комплексные соединения - электролиты при диссоциации в водных растворах образуют комплексные ионы: [Ag(NH 3)2]Cl ↔ [Ag(NH 3)2]+ + Cl- K[Ag(CN)2] ↔ K+ + [Ag(CN)2]- Такая диссоциация протекает полностью, ионы гидратируются.
4. Диссоциация комплексных соединений в растворах Комплексные соединения - неэлектролиты в водных растворах диссоциации не подвергаются. У них отсутствует внешняя сфера комплекса, например: [Zn(NH 3)2 Cl 2] [Co(NH 3)3(NO 3)3] [Pt(NH 3)2 Cl 2] дихлородиаминоцинк тринитротриаминокобальт дихлородиаминоплатина В водной среде такие молекулы гидратируются как единое соединение. Комплексные соединения - электролиты при диссоциации в водных растворах образуют комплексные ионы: [Ag(NH 3)2]Cl ↔ [Ag(NH 3)2]+ + Cl- K[Ag(CN)2] ↔ K+ + [Ag(CN)2]- Такая диссоциация протекает полностью, ионы гидратируются.
![Комплексные ионы, в свою очередь, подвергаются вторичной диссоциации: [Ag(NH 3)2]+ ↔ Ag+ + 2 Комплексные ионы, в свою очередь, подвергаются вторичной диссоциации: [Ag(NH 3)2]+ ↔ Ag+ + 2](https://present5.com/presentation/208984867_428488258/image-21.jpg) Комплексные ионы, в свою очередь, подвергаются вторичной диссоциации: [Ag(NH 3)2]+ ↔ Ag+ + 2 NH 3 (a) [Ag(CN)2]- ↔ Ag+ + 2 CN- (б) Однако эта диссоциация обычно протекает в незначительной степени. В растворах комплексные соединения могут подвергаться первичной и вторичной диссоциации.
Комплексные ионы, в свою очередь, подвергаются вторичной диссоциации: [Ag(NH 3)2]+ ↔ Ag+ + 2 NH 3 (a) [Ag(CN)2]- ↔ Ag+ + 2 CN- (б) Однако эта диссоциация обычно протекает в незначительной степени. В растворах комплексные соединения могут подвергаться первичной и вторичной диссоциации.
 Первичная диссоциация комплексного соединения - это его распад на комплексный ион, образованный внутренней сферой и ионы внешней сферы. В водных растворах первичная диссоциация комплексных соединений обусловлена разрывом ионной связи между внутренней и внешней сферами, она практически необратима: K 3[Fe(CN)6] ® 3 K+ + [Fe(CN)6]3– [Cu(NH 3)4]SO 4 ® [Cu(NH 3)4]2+ + SO 42– Образующийся комплексный ион ведет себя как целая самостоятельная частица с характерными для нее свойствами. Поэтому в водных растворах комплексных соединений, как правило, нельзя обнаружить присутствие ионов или молекул, входящих в состав внутренней сферы.
Первичная диссоциация комплексного соединения - это его распад на комплексный ион, образованный внутренней сферой и ионы внешней сферы. В водных растворах первичная диссоциация комплексных соединений обусловлена разрывом ионной связи между внутренней и внешней сферами, она практически необратима: K 3[Fe(CN)6] ® 3 K+ + [Fe(CN)6]3– [Cu(NH 3)4]SO 4 ® [Cu(NH 3)4]2+ + SO 42– Образующийся комплексный ион ведет себя как целая самостоятельная частица с характерными для нее свойствами. Поэтому в водных растворах комплексных соединений, как правило, нельзя обнаружить присутствие ионов или молекул, входящих в состав внутренней сферы.
 Вторичная диссоциация комплексного соединения – это распад внутренней сферы комплекса на составляющие ее компоненты. Так как при этом разрушаются не ионные, а ковалентные связи комплексообразователя с лигандами, этот процесс затруднен и обратим. Он происходит ступенчато: [Ag(NH 3)2]+ → [Ag(NH 3)]+ + NH 3 1 -ая ступень [Ag(NH 3)]+ → Ag+ + NH 3 2 -ая ступень Вторичная диссоциация характеризуется константой равновесия, причем для каждой из стадий можно вычислить свою константу. Для количественной оценки устойчивости внутренней сферы комплексного соединения используют константу равновесия, описывающую полную ее диссоциацию. Эту константу называют константой нестойкости комплекса Кнест. В соответствии с законом действующих масс для приведенного выше примера диссоциации иона диамминсеребра выражение для константы нестойкости принимает вид:
Вторичная диссоциация комплексного соединения – это распад внутренней сферы комплекса на составляющие ее компоненты. Так как при этом разрушаются не ионные, а ковалентные связи комплексообразователя с лигандами, этот процесс затруднен и обратим. Он происходит ступенчато: [Ag(NH 3)2]+ → [Ag(NH 3)]+ + NH 3 1 -ая ступень [Ag(NH 3)]+ → Ag+ + NH 3 2 -ая ступень Вторичная диссоциация характеризуется константой равновесия, причем для каждой из стадий можно вычислить свою константу. Для количественной оценки устойчивости внутренней сферы комплексного соединения используют константу равновесия, описывающую полную ее диссоциацию. Эту константу называют константой нестойкости комплекса Кнест. В соответствии с законом действующих масс для приведенного выше примера диссоциации иона диамминсеребра выражение для константы нестойкости принимает вид:
 Чем ниже Kнест, тем прочнее и стабильнее внутренняя сфера комплексного соединения, тем в меньшей мере происходит вторичная диссоциация комплексного соединения в растворе. Сравните устойчивость комплексных соединений, используя таблицу 1. Таблица 1 Константы нестойкости некоторых комплексных ионов Комплексный ион [Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ Kнест 7, 75 • 10– 6 9, 31 • 10– 8 2, 14 • 10– 13 Комплексный ион [Zn(OH)4]2– [Fe(CN)6]3– [Fe(CN)6]4– Kнест 3, 6 • 10– 16 1, 0 • 10– 31 1, 0 • 10– 36
Чем ниже Kнест, тем прочнее и стабильнее внутренняя сфера комплексного соединения, тем в меньшей мере происходит вторичная диссоциация комплексного соединения в растворе. Сравните устойчивость комплексных соединений, используя таблицу 1. Таблица 1 Константы нестойкости некоторых комплексных ионов Комплексный ион [Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ Kнест 7, 75 • 10– 6 9, 31 • 10– 8 2, 14 • 10– 13 Комплексный ион [Zn(OH)4]2– [Fe(CN)6]3– [Fe(CN)6]4– Kнест 3, 6 • 10– 16 1, 0 • 10– 31 1, 0 • 10– 36
 5. Равновесие в растворах комплексных соединений. Комплексообразование в водных растворах Равновесные процессы образования и диссоциации могут происходить не только с участием ионов Н+ и анионов, но и при участии других ионов и молекул в растворе. Пусть в растворе присутствуют катионы М и анионы L (или молекулы), способные образовывать соединения: М + L → МL Эти соединения в какой-то степени способны диссоциировать с образованием исходных ионов М и L: МL → М + L В результате в растворе устанавливается равновесие с участием ионов М и L и соединения МL: М + L ↔ МL
5. Равновесие в растворах комплексных соединений. Комплексообразование в водных растворах Равновесные процессы образования и диссоциации могут происходить не только с участием ионов Н+ и анионов, но и при участии других ионов и молекул в растворе. Пусть в растворе присутствуют катионы М и анионы L (или молекулы), способные образовывать соединения: М + L → МL Эти соединения в какой-то степени способны диссоциировать с образованием исходных ионов М и L: МL → М + L В результате в растворе устанавливается равновесие с участием ионов М и L и соединения МL: М + L ↔ МL
 Ионы металлов в водном растворе сильно гидратированы. Поскольку некоторое число молекул воды координационно связано с металлом, образование комплекса можно рассматривать как реакцию обмена лигандов: М(ОН 2)n + п. HL = MLn + n. H 3 O+ Если уравнение расчленить на его составляющие, получим следующие уравнения: 1)М + п. L ↔ MLn; 3) М + п. Н 2 О ↔ М(ОН 2)n; 2) H+ + L ↔ НL; 4) Н+ + Н 2 О ↔ H 3 O+ Приведенные реакции существуют одновременно, и преобладающим в результате суммарной реакции окажется тот продукт, который имеет наибольшую константу образования.
Ионы металлов в водном растворе сильно гидратированы. Поскольку некоторое число молекул воды координационно связано с металлом, образование комплекса можно рассматривать как реакцию обмена лигандов: М(ОН 2)n + п. HL = MLn + n. H 3 O+ Если уравнение расчленить на его составляющие, получим следующие уравнения: 1)М + п. L ↔ MLn; 3) М + п. Н 2 О ↔ М(ОН 2)n; 2) H+ + L ↔ НL; 4) Н+ + Н 2 О ↔ H 3 O+ Приведенные реакции существуют одновременно, и преобладающим в результате суммарной реакции окажется тот продукт, который имеет наибольшую константу образования.
 6. Устойчивость комплексных соединений Количественной характеристикой устойчивости комплексных соединений является константа образования, т. е. константа равновесия М + п. L ↔ MLn Большинство равновесий комплексообразования реализуется ступенчато. Каждая ступень при этом имеет свою константу образования: [ML] М + L ↔ ML; K 1 = -----; β 1 = ----; [M][L] [ML 2] МL + L ↔ ML 2; K 2 = -----; β 2 = ----; . [ML][L] [M][L]2 [MLn] МLn-1 + L ↔ MLn; Kn = ------; βn = -----; [MLn-1][L] [M][L] n где K 1, K 2, . . , Kn – ступенчатые константы образования (или ступенчатые константы устойчивости); β 1, β 2, βn – общие константы образования (устойчивости). Значение констант β определяется как произведения констант K.
6. Устойчивость комплексных соединений Количественной характеристикой устойчивости комплексных соединений является константа образования, т. е. константа равновесия М + п. L ↔ MLn Большинство равновесий комплексообразования реализуется ступенчато. Каждая ступень при этом имеет свою константу образования: [ML] М + L ↔ ML; K 1 = -----; β 1 = ----; [M][L] [ML 2] МL + L ↔ ML 2; K 2 = -----; β 2 = ----; . [ML][L] [M][L]2 [MLn] МLn-1 + L ↔ MLn; Kn = ------; βn = -----; [MLn-1][L] [M][L] n где K 1, K 2, . . , Kn – ступенчатые константы образования (или ступенчатые константы устойчивости); β 1, β 2, βn – общие константы образования (устойчивости). Значение констант β определяется как произведения констант K.
 Чем больше константа устойчивости, тем прочнее комплекс в растворе, тем полнее ионы металла М связываются в комплекс. Реакция диссоциации комплекса в общем виде MLn = М + п. L характеризуется полной истинной термодинамической константой равновесия – константой нестойкости, константой неустойчивости или константой диссоциации комплекса Kн: a(M) a(L)n Kн = ------a(MLn)
Чем больше константа устойчивости, тем прочнее комплекс в растворе, тем полнее ионы металла М связываются в комплекс. Реакция диссоциации комплекса в общем виде MLn = М + п. L характеризуется полной истинной термодинамической константой равновесия – константой нестойкости, константой неустойчивости или константой диссоциации комплекса Kн: a(M) a(L)n Kн = ------a(MLn)
 Аналогично для ступенчатых констант нестойкости: MLn = М + п. L 1 a(МLn-1) a(L)n Kн, n = ----------βn a(MLn) МLn-1 = MLn-2 + L 1 a(МLn-2) a(L) Kн, n-1 = ----------βn-1 a(МLn-1) В общем виде: МL = M + L 1 a(М) a(L) Kн, 1 = ---------β 1 a(МL) Константа устойчивости есть величина обратная константе нестойкости: β = 1/ Kн Произведение всех ступенчатых констант настойкости равно полной константе нестойкости комплекса: Kн, 1 Kн, 2∙∙∙ Kн, n = Kн
Аналогично для ступенчатых констант нестойкости: MLn = М + п. L 1 a(МLn-1) a(L)n Kн, n = ----------βn a(MLn) МLn-1 = MLn-2 + L 1 a(МLn-2) a(L) Kн, n-1 = ----------βn-1 a(МLn-1) В общем виде: МL = M + L 1 a(М) a(L) Kн, 1 = ---------β 1 a(МL) Константа устойчивости есть величина обратная константе нестойкости: β = 1/ Kн Произведение всех ступенчатых констант настойкости равно полной константе нестойкости комплекса: Kн, 1 Kн, 2∙∙∙ Kн, n = Kн


 Значение комплексных соединений в аналитической химии Реакции комплексообразования широко применяются в качественном и в количественном анализе. Рассмотрим основные направления использования комплексов в качественном анализе. 1. Огромное число характерных реакций на те или иные ионы основано на комплексообразовании. Например, по образованию характерно окрашенного комплекса ионов никеля и диметилглиоксимом (реакция Чугаева) можно сделать вывод о наличии ионов никеля в растворе. 2. Комплексообразование имеет значение не только при обнаружении отдельных ионов, но и для их разделения. Например, для разделения ионов Al 3+ и Zn 2+ используется раствор аммиака. Ионы алюминия переходят в осадок Al(OH)3, а ионы цинка образуют аммиачный комплекс [Zn(NH 3)6]2+.
Значение комплексных соединений в аналитической химии Реакции комплексообразования широко применяются в качественном и в количественном анализе. Рассмотрим основные направления использования комплексов в качественном анализе. 1. Огромное число характерных реакций на те или иные ионы основано на комплексообразовании. Например, по образованию характерно окрашенного комплекса ионов никеля и диметилглиоксимом (реакция Чугаева) можно сделать вывод о наличии ионов никеля в растворе. 2. Комплексообразование имеет значение не только при обнаружении отдельных ионов, но и для их разделения. Например, для разделения ионов Al 3+ и Zn 2+ используется раствор аммиака. Ионы алюминия переходят в осадок Al(OH)3, а ионы цинка образуют аммиачный комплекс [Zn(NH 3)6]2+.
 3. Комплексообразование используют для маскировки отдельных ионов. Например, присутствие в растворе ионов Fe 3+ мешает обнаружению ионов Co 2+. Чтобы значительно снизить концентрацию ионов Fe 3+ и обнаружить ионы кобальта, можно внести в раствор фторид аммония. Образуется прочный комплекс [Fe. F 6]3–, и концентрация ионов Fe 3+ снижается настолько, что оказывается возможным обнаружить ион Co 2+. 4. Комплексообразование используется для перевода в раствор некоторых малорастворимых веществ. Например, хлорид серебра растворяется при добавлении раствора аммиака, так как образуется комплексное соединение: Ag. Cl + 2 NH 3∙H 2 O = [Ag(NH 3)2]Cl + 2 H 2 O.
3. Комплексообразование используют для маскировки отдельных ионов. Например, присутствие в растворе ионов Fe 3+ мешает обнаружению ионов Co 2+. Чтобы значительно снизить концентрацию ионов Fe 3+ и обнаружить ионы кобальта, можно внести в раствор фторид аммония. Образуется прочный комплекс [Fe. F 6]3–, и концентрация ионов Fe 3+ снижается настолько, что оказывается возможным обнаружить ион Co 2+. 4. Комплексообразование используется для перевода в раствор некоторых малорастворимых веществ. Например, хлорид серебра растворяется при добавлении раствора аммиака, так как образуется комплексное соединение: Ag. Cl + 2 NH 3∙H 2 O = [Ag(NH 3)2]Cl + 2 H 2 O.
 Различают несколько типов комплексных соединений: 1) хелатные 2) макроциклические 3) полиядерные Хелаты – устойчивые комплексы металлов с полидентатными лигандами, в которых центральный атом является компонентом циклической структуры.
Различают несколько типов комплексных соединений: 1) хелатные 2) макроциклические 3) полиядерные Хелаты – устойчивые комплексы металлов с полидентатными лигандами, в которых центральный атом является компонентом циклической структуры.
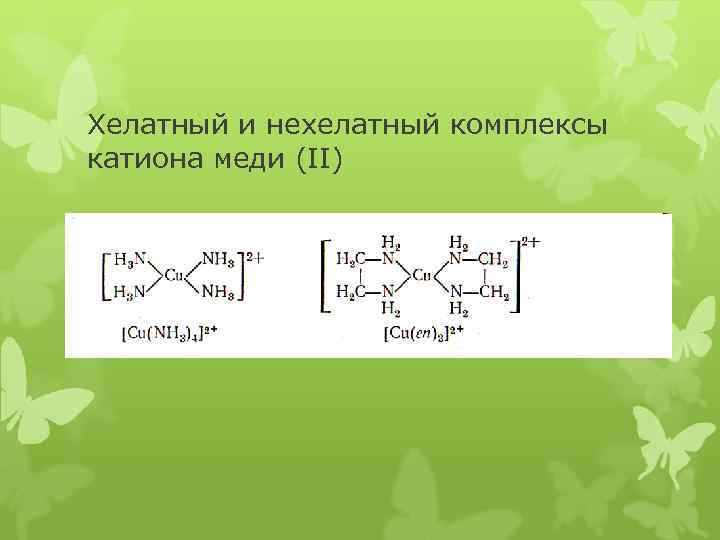 Хелатный и нехелатный комплексы катиона меди (II)
Хелатный и нехелатный комплексы катиона меди (II)
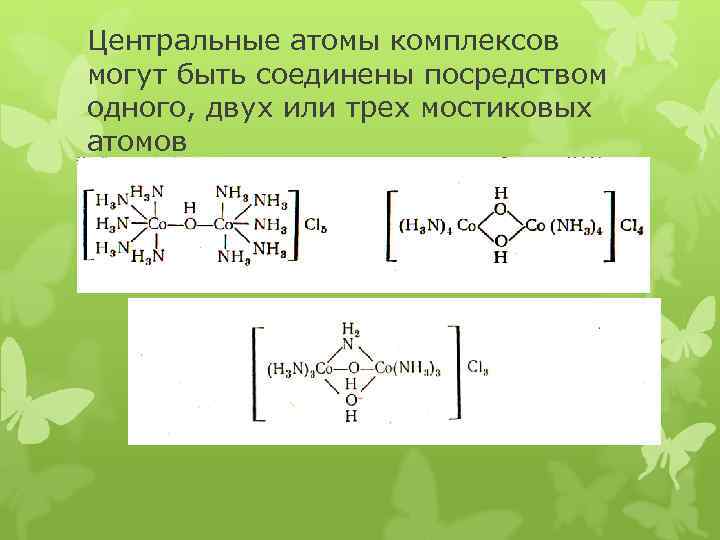 Центральные атомы комплексов могут быть соединены посредством одного, двух или трех мостиковых атомов
Центральные атомы комплексов могут быть соединены посредством одного, двух или трех мостиковых атомов
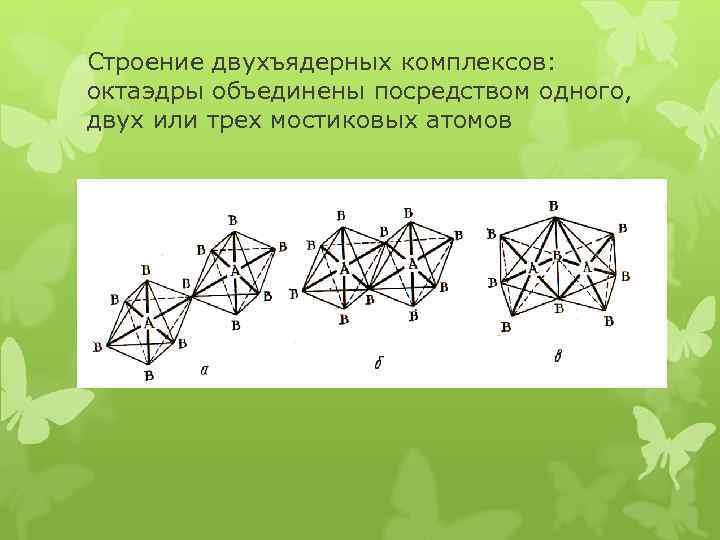 Строение двухъядерных комплексов: октаэдры объединены посредством одного, двух или трех мостиковых атомов
Строение двухъядерных комплексов: октаэдры объединены посредством одного, двух или трех мостиковых атомов
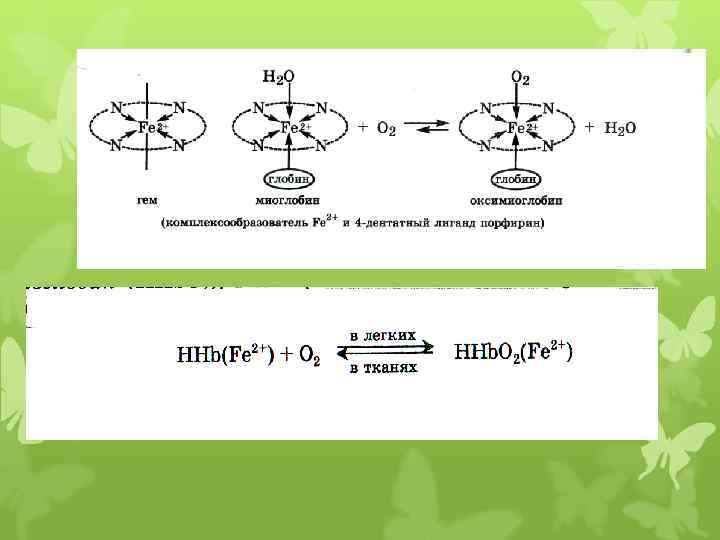
 Под действием окислителей: нитратов, нитритов, Н 2 О 2, О 3 и др. , гемоглобин в результате окисления катиона железа и отрыва протона превращается в метгемоглобин: ННb(Fe 2+) → мет. ННb(Fe 3+) + Н+ + е. Метгемоглобин не способен переносить кислород, поэтому его появление уменьшает кислородную емкость крови.
Под действием окислителей: нитратов, нитритов, Н 2 О 2, О 3 и др. , гемоглобин в результате окисления катиона железа и отрыва протона превращается в метгемоглобин: ННb(Fe 2+) → мет. ННb(Fe 3+) + Н+ + е. Метгемоглобин не способен переносить кислород, поэтому его появление уменьшает кислородную емкость крови.
 химических превращений. Попадая в организм, нитраты легко восстанавливаются до нитритов: NO 3 - + 2 H+ + 2 e-→ NO 2 - + H 2 O Нитриты чрезвычайно легко окисляют гемоглобин в метгемоглобин , образуя оксид азота (II): HHb(Fe 2+) + NO 2 - + 2 H+ → мет. HHb(Fe 3+) + NO + Н 2 О Образовавшийся оксид азота (II) связывает гемоглобин в прочный комплекс – нитрозогемоглобин HHb + NO → HHb. NO
химических превращений. Попадая в организм, нитраты легко восстанавливаются до нитритов: NO 3 - + 2 H+ + 2 e-→ NO 2 - + H 2 O Нитриты чрезвычайно легко окисляют гемоглобин в метгемоглобин , образуя оксид азота (II): HHb(Fe 2+) + NO 2 - + 2 H+ → мет. HHb(Fe 3+) + NO + Н 2 О Образовавшийся оксид азота (II) связывает гемоглобин в прочный комплекс – нитрозогемоглобин HHb + NO → HHb. NO


