Комплексы.ppt
- Количество слайдов: 38
 Комплексные соединения
Комплексные соединения
 УМК «ХИМИЯ» Тема лекции: Комплексные соединения Лектор – Иванов М. Г.
УМК «ХИМИЯ» Тема лекции: Комплексные соединения Лектор – Иванов М. Г.
 Цель лекции: изложение основных понятий химии координационных соединений в рамках современной химической теории Компетенции, формируемые у студента: Умения: q прогнозировать на основе положения элементов в Периодической системе, а также современных представлений о строении атомов и химической связи, свойства, строение и поведение в растворах комплексных соединений p-, d –элементов.
Цель лекции: изложение основных понятий химии координационных соединений в рамках современной химической теории Компетенции, формируемые у студента: Умения: q прогнозировать на основе положения элементов в Периодической системе, а также современных представлений о строении атомов и химической связи, свойства, строение и поведение в растворах комплексных соединений p-, d –элементов.
 СОДЕРЖАНИЕ Основные понятия Классификация Номенклатура Изомерия Геометрическая Оптическая Связевые изомеры Гидратные и ионизационные изомеры Конформационные изомеры Лиганды Хелатные комплексы Макроциклические Сэндвичевые комплексы Многоядерные комплексы Строение комплексов Метод ВС Теория кристаллического поля Расщепление d-орбиталей Сильное и слабое поле Устойчивость комплексов Литература
СОДЕРЖАНИЕ Основные понятия Классификация Номенклатура Изомерия Геометрическая Оптическая Связевые изомеры Гидратные и ионизационные изомеры Конформационные изомеры Лиганды Хелатные комплексы Макроциклические Сэндвичевые комплексы Многоядерные комплексы Строение комплексов Метод ВС Теория кристаллического поля Расщепление d-орбиталей Сильное и слабое поле Устойчивость комплексов Литература
 Основные понятия содержание Комплексными (координационными) называют соединения стехиометрически достоверные, устойчивые в растворе и твердом состоянии , состоящие их центрального атома и координированных вокруг него лигандов. Основные понятия: q Центральный атом q Лиганды q Координационное число q Внутрення и внешняя сфеда q Дентатаность
Основные понятия содержание Комплексными (координационными) называют соединения стехиометрически достоверные, устойчивые в растворе и твердом состоянии , состоящие их центрального атома и координированных вокруг него лигандов. Основные понятия: q Центральный атом q Лиганды q Координационное число q Внутрення и внешняя сфеда q Дентатаность
 Классификация содержание А. Вернер (1866 -1919) Согласно теории Вернера – Миолати существует три типа классических комплексов: q Координационные ацидосоединения, во внутренней сфере которых содержатся только кислотные остатки; q Молекулярные координационные соединения, во внутренней сфере которых содержатся только лиганды в молекулярной форме; q Смешанные ацидо-молекулярные координационные соединения.
Классификация содержание А. Вернер (1866 -1919) Согласно теории Вернера – Миолати существует три типа классических комплексов: q Координационные ацидосоединения, во внутренней сфере которых содержатся только кислотные остатки; q Молекулярные координационные соединения, во внутренней сфере которых содержатся только лиганды в молекулярной форме; q Смешанные ацидо-молекулярные координационные соединения.
![Номенклатура содержание q Традиционные названия: [Pt(NH 3)4][Pt. Cl 4] – соль Магнуса K 3[Fe(CN)6] Номенклатура содержание q Традиционные названия: [Pt(NH 3)4][Pt. Cl 4] – соль Магнуса K 3[Fe(CN)6]](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-7.jpg) Номенклатура содержание q Традиционные названия: [Pt(NH 3)4][Pt. Cl 4] – соль Магнуса K 3[Fe(CN)6] – красная кровяная соль цис-[Pt(NH 3)2 Cl 2] – соль Пейроне q Формула по ЮПАК: квадратные скобки –центральный атом –анионные лиганды по алфавиту –нейтральные лиганды по алфавиту Na[Ag(CN)2] K 2[Pt. Cl 6] K 3[Ga. F 6] [Cu(NH 3)4]SO 4 – дицианоаргентат(I) натрия – тетрахлороплатинат(IV) калия – гексафторогаллат(III) калия – сульфат тетрааминмеди(II)
Номенклатура содержание q Традиционные названия: [Pt(NH 3)4][Pt. Cl 4] – соль Магнуса K 3[Fe(CN)6] – красная кровяная соль цис-[Pt(NH 3)2 Cl 2] – соль Пейроне q Формула по ЮПАК: квадратные скобки –центральный атом –анионные лиганды по алфавиту –нейтральные лиганды по алфавиту Na[Ag(CN)2] K 2[Pt. Cl 6] K 3[Ga. F 6] [Cu(NH 3)4]SO 4 – дицианоаргентат(I) натрия – тетрахлороплатинат(IV) калия – гексафторогаллат(III) калия – сульфат тетрааминмеди(II)
 Изомерия q Пространственная: геометрическая и оптическая q Ионизационная q Гидратная q Связевая q Спиновая q Конформационная содержание
Изомерия q Пространственная: геометрическая и оптическая q Ионизационная q Гидратная q Связевая q Спиновая q Конформационная содержание
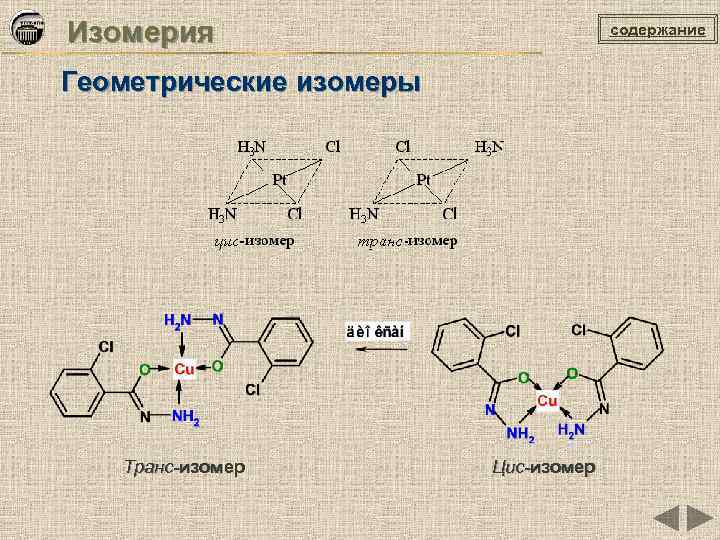 Изомерия содержание Геометрические изомеры Транс-изомер Цис-изомер
Изомерия содержание Геометрические изомеры Транс-изомер Цис-изомер
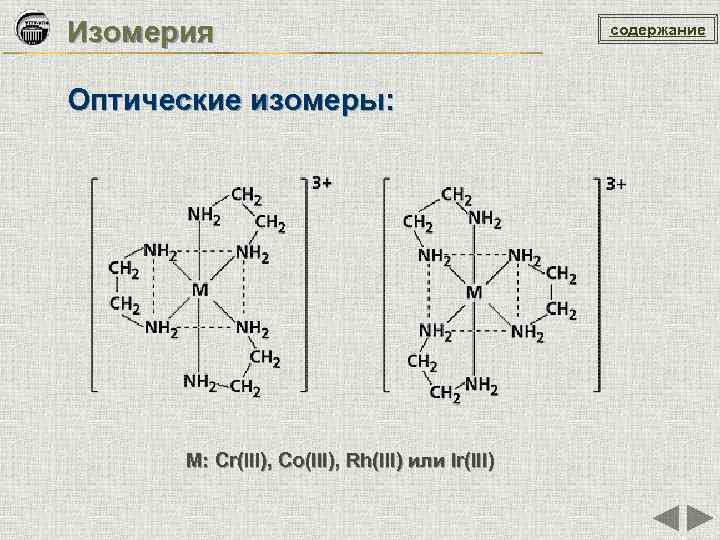 Изомерия Оптические изомеры: M: Cr(III), Co(III), Rh(III) или Ir(III) содержание
Изомерия Оптические изомеры: M: Cr(III), Co(III), Rh(III) или Ir(III) содержание
![Изомерия содержание Связевые изомеры: [(CO)5 Mn—SCN] и [(CO)5 Mn—NCS] [Co. NO 2(NH 3)5]Cl 2 Изомерия содержание Связевые изомеры: [(CO)5 Mn—SCN] и [(CO)5 Mn—NCS] [Co. NO 2(NH 3)5]Cl 2](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-11.jpg) Изомерия содержание Связевые изомеры: [(CO)5 Mn—SCN] и [(CO)5 Mn—NCS] [Co. NO 2(NH 3)5]Cl 2 и Co(ONO)(NH 3)5]Cl 2
Изомерия содержание Связевые изомеры: [(CO)5 Mn—SCN] и [(CO)5 Mn—NCS] [Co. NO 2(NH 3)5]Cl 2 и Co(ONO)(NH 3)5]Cl 2
![Изомерия содержание Гидратные и ионизационные изомеры [Co. Br(NH 3)5]SO 4 - фиолетовый [Co. SO Изомерия содержание Гидратные и ионизационные изомеры [Co. Br(NH 3)5]SO 4 - фиолетовый [Co. SO](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-12.jpg) Изомерия содержание Гидратные и ионизационные изомеры [Co. Br(NH 3)5]SO 4 - фиолетовый [Co. SO 4(NH 3)5]Br - красно-фиолетовый [Co. Cl(H 2 O)5]Cl 2·H 2 O [Co. Cl 2(H 2 O)4]Cl· 2 H 2 O
Изомерия содержание Гидратные и ионизационные изомеры [Co. Br(NH 3)5]SO 4 - фиолетовый [Co. SO 4(NH 3)5]Br - красно-фиолетовый [Co. Cl(H 2 O)5]Cl 2·H 2 O [Co. Cl 2(H 2 O)4]Cl· 2 H 2 O
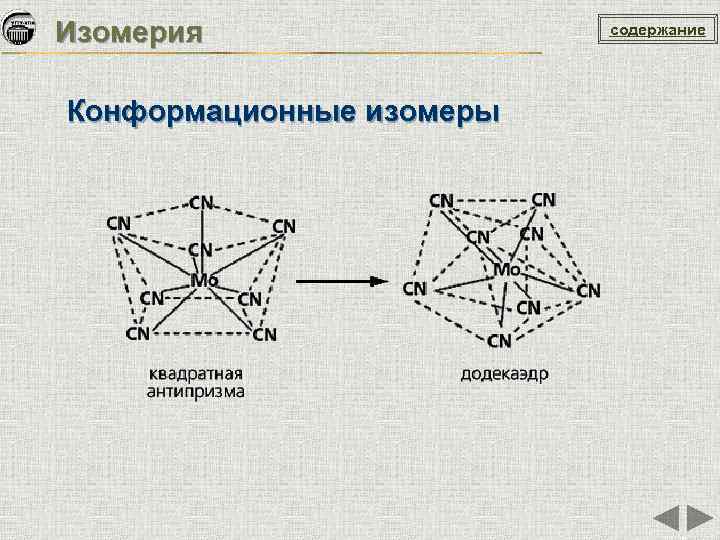 Изомерия Конформационные изомеры содержание
Изомерия Конформационные изомеры содержание
 Лиганды содержание Типы: нейтральные: H 2 O, NH 3, CO, Н 2 N-CH 2 -NH 2 нейтральные: анионы: Cl-, OH-, CN-, F-, оксалат-ион- С 2 O 42 - Дентатность: Монодентатные: H 2 O, NH 3, CO, Cl-, OH-, CN-, F- Полидентатные: Н 2 N-CH 2 -NH 2, С 2 O 42 -
Лиганды содержание Типы: нейтральные: H 2 O, NH 3, CO, Н 2 N-CH 2 -NH 2 нейтральные: анионы: Cl-, OH-, CN-, F-, оксалат-ион- С 2 O 42 - Дентатность: Монодентатные: H 2 O, NH 3, CO, Cl-, OH-, CN-, F- Полидентатные: Н 2 N-CH 2 -NH 2, С 2 O 42 -
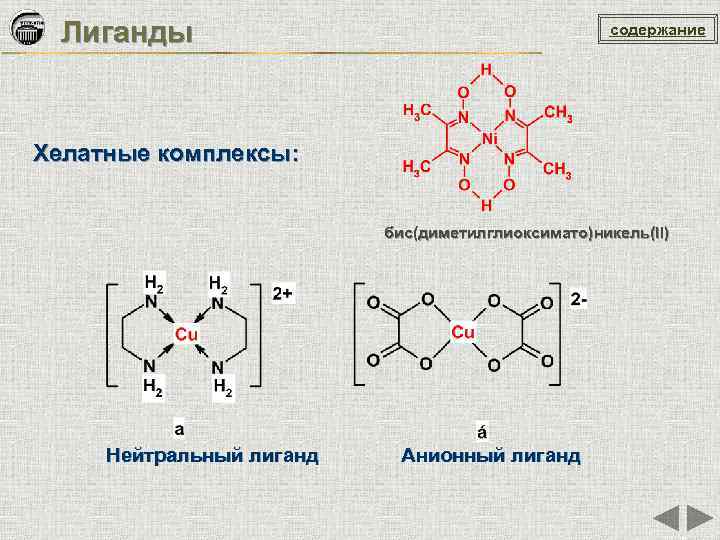 Лиганды содержание Хелатные комплексы: бис(диметилглиоксимато)никель(II) Нейтральный лиганд Анионный лиганд
Лиганды содержание Хелатные комплексы: бис(диметилглиоксимато)никель(II) Нейтральный лиганд Анионный лиганд
![Лиганды содержание Макроциклический [Ni(H 2 O)6]2+ + n L [Ni(L)n(H 2 O)2]2+ + 4 Лиганды содержание Макроциклический [Ni(H 2 O)6]2+ + n L [Ni(L)n(H 2 O)2]2+ + 4](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-16.jpg) Лиганды содержание Макроциклический [Ni(H 2 O)6]2+ + n L [Ni(L)n(H 2 O)2]2+ + 4 H 2 O L= NH 3 n= 4 lg n= 8, 12 en 2 13, 5 trien 2 -3 -2 1 1 13, 8 14, 6
Лиганды содержание Макроциклический [Ni(H 2 O)6]2+ + n L [Ni(L)n(H 2 O)2]2+ + 4 H 2 O L= NH 3 n= 4 lg n= 8, 12 en 2 13, 5 trien 2 -3 -2 1 1 13, 8 14, 6
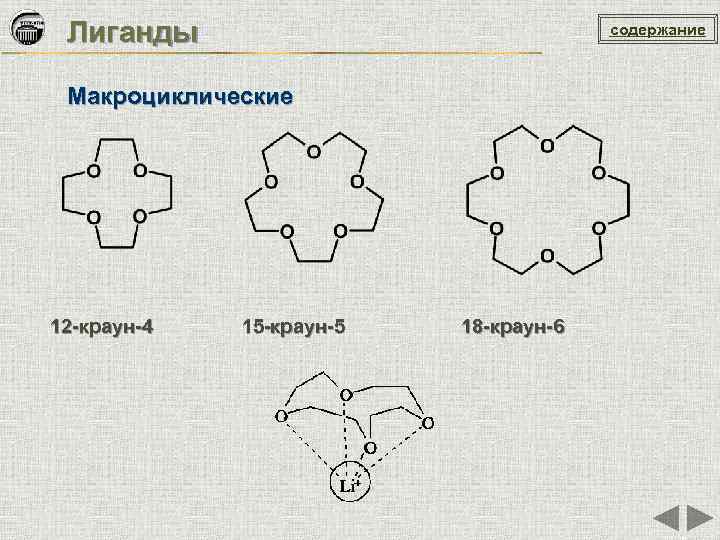 Лиганды содержание Макроциклические 12 -краун-4 15 -краун-5 18 -краун-6
Лиганды содержание Макроциклические 12 -краун-4 15 -краун-5 18 -краун-6
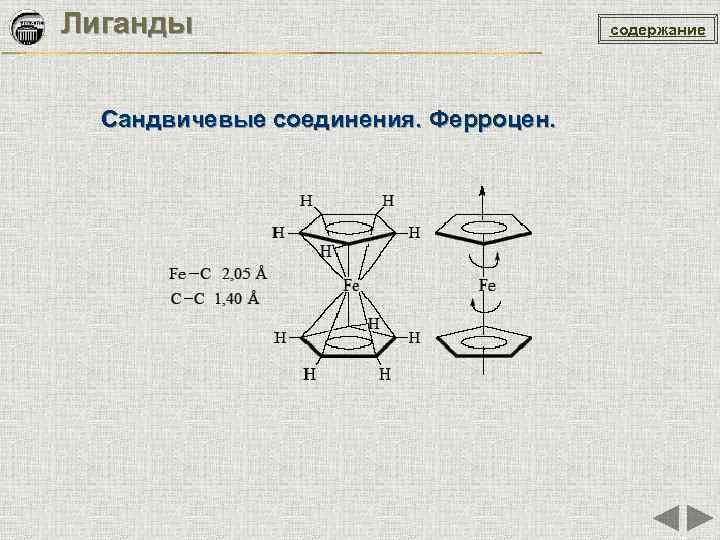 Лиганды Сандвичевые соединения. Ферроцен. содержание
Лиганды Сандвичевые соединения. Ферроцен. содержание
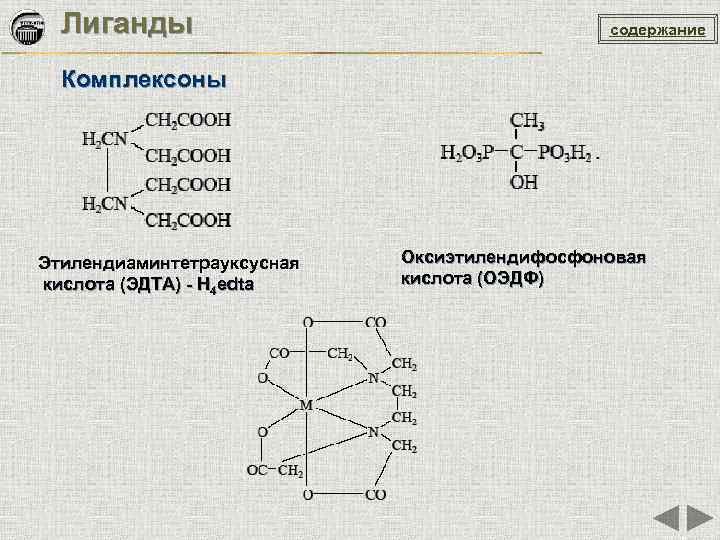 Лиганды содержание Комплексоны Этилендиаминтетрауксусная кислота (ЭДТА) - H 4 edta Оксиэтилендифосфоновая кислота (ОЭДФ)
Лиганды содержание Комплексоны Этилендиаминтетрауксусная кислота (ЭДТА) - H 4 edta Оксиэтилендифосфоновая кислота (ОЭДФ)
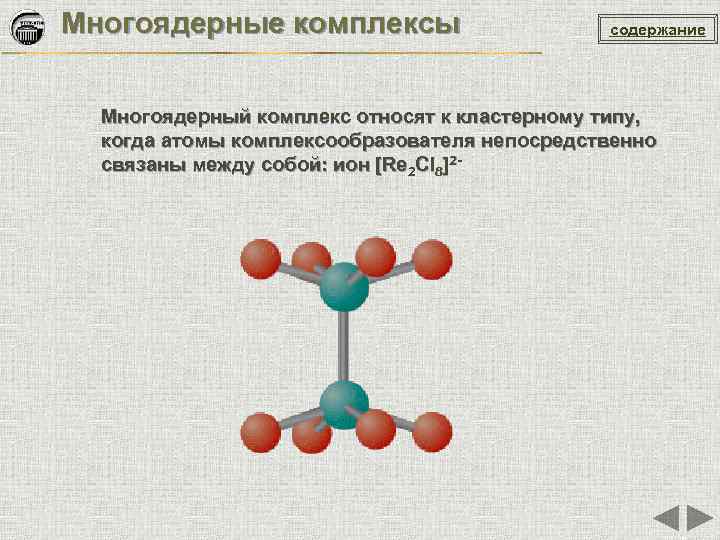 Многоядерные комплексы содержание Многоядерный комплекс относят к кластерному типу, когда атомы комплексообразователя непосредственно связаны между собой: ион [Re 2 Cl 8]2 -
Многоядерные комплексы содержание Многоядерный комплекс относят к кластерному типу, когда атомы комплексообразователя непосредственно связаны между собой: ион [Re 2 Cl 8]2 -
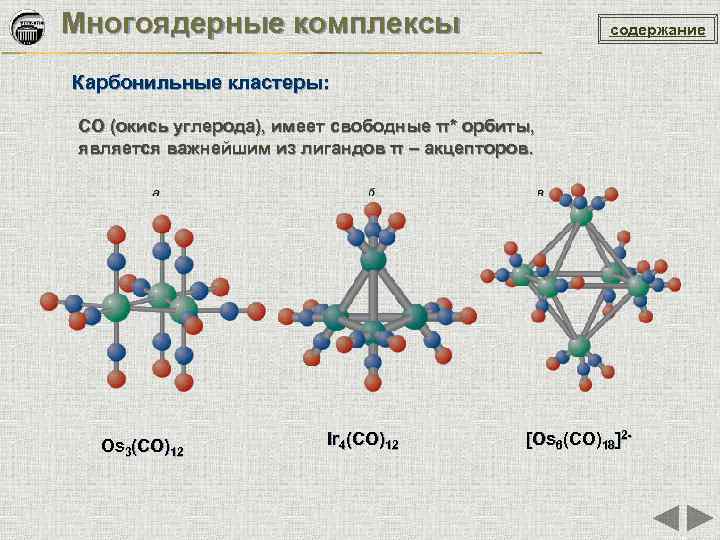 Многоядерные комплексы содержание Карбонильные кластеры: CO (окись углерода), имеет свободные π* орбиты, является важнейшим из лигандов π – акцепторов. Os 3(CO)12 Ir 4(CO)12 [Os 6(CO)18]2 -
Многоядерные комплексы содержание Карбонильные кластеры: CO (окись углерода), имеет свободные π* орбиты, является важнейшим из лигандов π – акцепторов. Os 3(CO)12 Ir 4(CO)12 [Os 6(CO)18]2 -
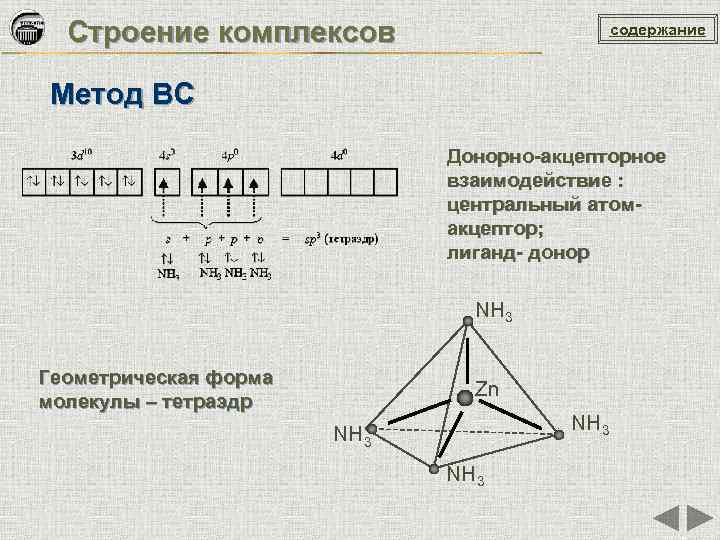 Строение комплексов содержание Метод ВС Донорно-акцепторное взаимодействие : центральный атомакцептор; лиганд- донор NH 3 Геометрическая форма молекулы – тетраэдр Zn NH 3
Строение комплексов содержание Метод ВС Донорно-акцепторное взаимодействие : центральный атомакцептор; лиганд- донор NH 3 Геометрическая форма молекулы – тетраэдр Zn NH 3
 Строение комплексов Недостатки метода ВС q Не объясняет магнитные свойства комплексов q Не объясняет окраску комплексов q Не учитывает π-связывание q Не объясняет различную устойчивость комплексов содержание
Строение комплексов Недостатки метода ВС q Не объясняет магнитные свойства комплексов q Не объясняет окраску комплексов q Не учитывает π-связывание q Не объясняет различную устойчивость комплексов содержание
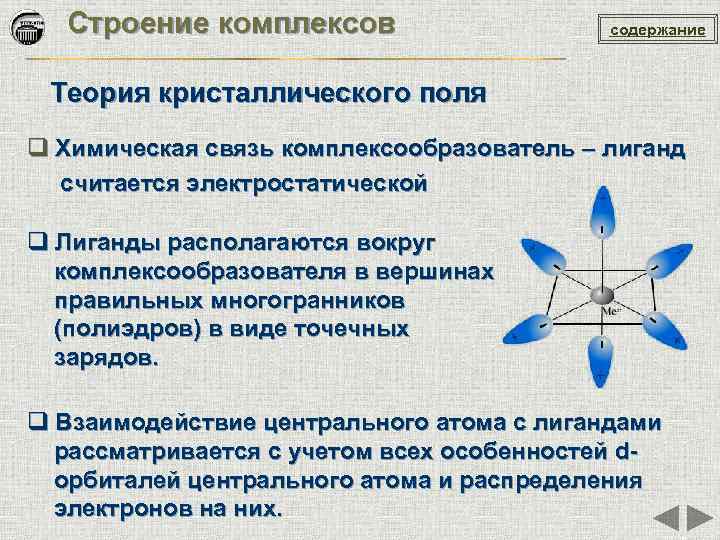 Строение комплексов содержание Теория кристаллического поля q Химическая связь комплексообразователь – лиганд считается электростатической q Лиганды располагаются вокруг комплексообразователя в вершинах правильных многогранников (полиэдров) в виде точечных зарядов. q Взаимодействие центрального атома с лигандами рассматривается с учетом всех особенностей dорбиталей центрального атома и распределения электронов на них.
Строение комплексов содержание Теория кристаллического поля q Химическая связь комплексообразователь – лиганд считается электростатической q Лиганды располагаются вокруг комплексообразователя в вершинах правильных многогранников (полиэдров) в виде точечных зарядов. q Взаимодействие центрального атома с лигандами рассматривается с учетом всех особенностей dорбиталей центрального атома и распределения электронов на них.
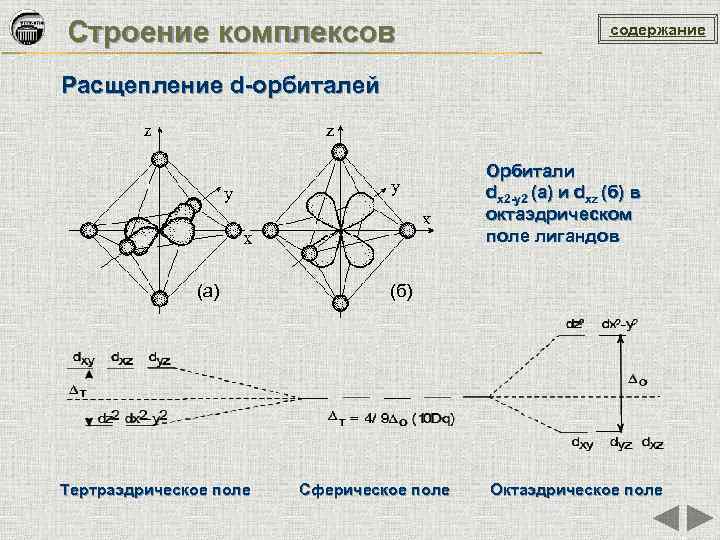 Строение комплексов содержание Расщепление d-орбиталей Орбитали dх2 -у2 (а) и dxz (б) в октаэдрическом поле лигандов (а) Тертраэдрическое поле (б) Сферическое поле Октаэдрическое поле
Строение комплексов содержание Расщепление d-орбиталей Орбитали dх2 -у2 (а) и dxz (б) в октаэдрическом поле лигандов (а) Тертраэдрическое поле (б) Сферическое поле Октаэдрическое поле
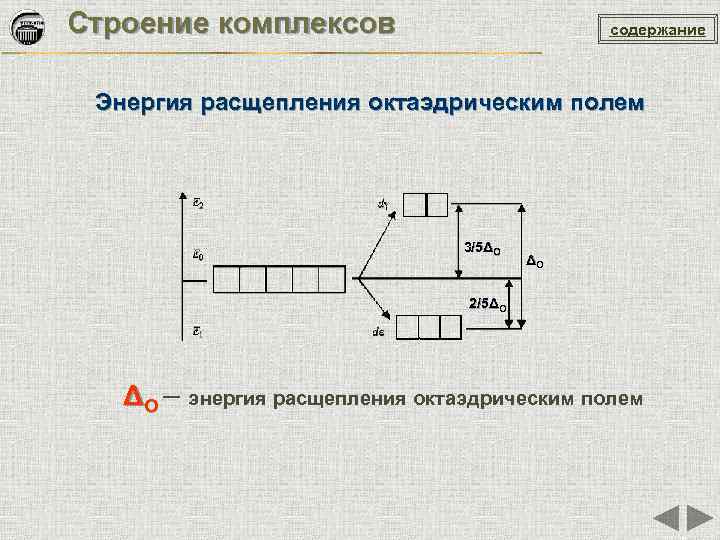 Строение комплексов содержание Энергия расщепления октаэдрическим полем 3/5ΔO ΔO 2/5ΔO ΔO – энергия расщепления октаэдрическим полем
Строение комплексов содержание Энергия расщепления октаэдрическим полем 3/5ΔO ΔO 2/5ΔO ΔO – энергия расщепления октаэдрическим полем
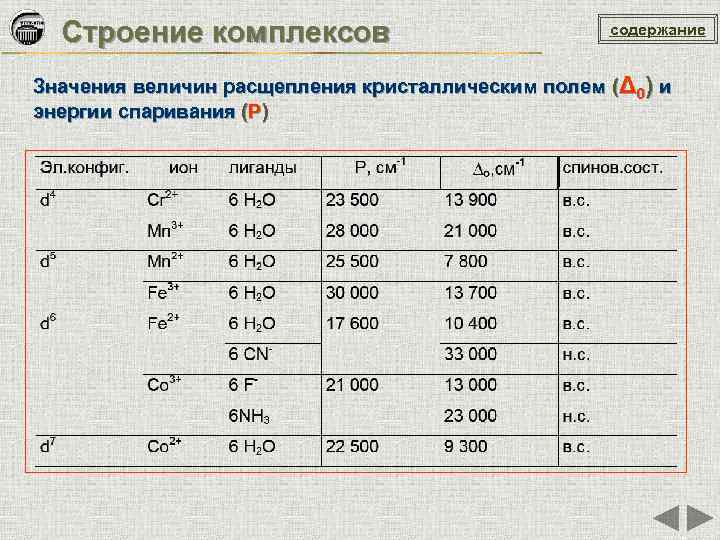 Строение комплексов содержание Значения величин расщепления кристаллическим полем (Δ 0) и энергии спаривания (P)
Строение комплексов содержание Значения величин расщепления кристаллическим полем (Δ 0) и энергии спаривания (P)
![Строение комплексов содержание Сильное и слабое поле [Fe(CN)6]4 - 3 d 6 ΔO = Строение комплексов содержание Сильное и слабое поле [Fe(CN)6]4 - 3 d 6 ΔO =](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-28.jpg) Строение комплексов содержание Сильное и слабое поле [Fe(CN)6]4 - 3 d 6 ΔO = 33000 cm-1 ΔO > P (энергии спаривания электронов) – комплекс низкоспиновый (сильное поле)
Строение комплексов содержание Сильное и слабое поле [Fe(CN)6]4 - 3 d 6 ΔO = 33000 cm-1 ΔO > P (энергии спаривания электронов) – комплекс низкоспиновый (сильное поле)
![Строение комплексов содержание Сильное и слабое поле [Fe(H 2 O)6]2+ 3 d 6 ΔO Строение комплексов содержание Сильное и слабое поле [Fe(H 2 O)6]2+ 3 d 6 ΔO](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-29.jpg) Строение комплексов содержание Сильное и слабое поле [Fe(H 2 O)6]2+ 3 d 6 ΔO = 10400 cm-1 ΔO < P (энергии спаривания электронов) – комплекс высокоспиновый (слабое поле)
Строение комплексов содержание Сильное и слабое поле [Fe(H 2 O)6]2+ 3 d 6 ΔO = 10400 cm-1 ΔO < P (энергии спаривания электронов) – комплекс высокоспиновый (слабое поле)
![Магнитные свойства содержание μэфф = 2 [S(S+1)]1/2 = [n(n+2)]1/2 (магнетон Бора) S –суммарный спин Магнитные свойства содержание μэфф = 2 [S(S+1)]1/2 = [n(n+2)]1/2 (магнетон Бора) S –суммарный спин](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-30.jpg) Магнитные свойства содержание μэфф = 2 [S(S+1)]1/2 = [n(n+2)]1/2 (магнетон Бора) S –суммарный спин n–число неспаренных электронов
Магнитные свойства содержание μэфф = 2 [S(S+1)]1/2 = [n(n+2)]1/2 (магнетон Бора) S –суммарный спин n–число неспаренных электронов
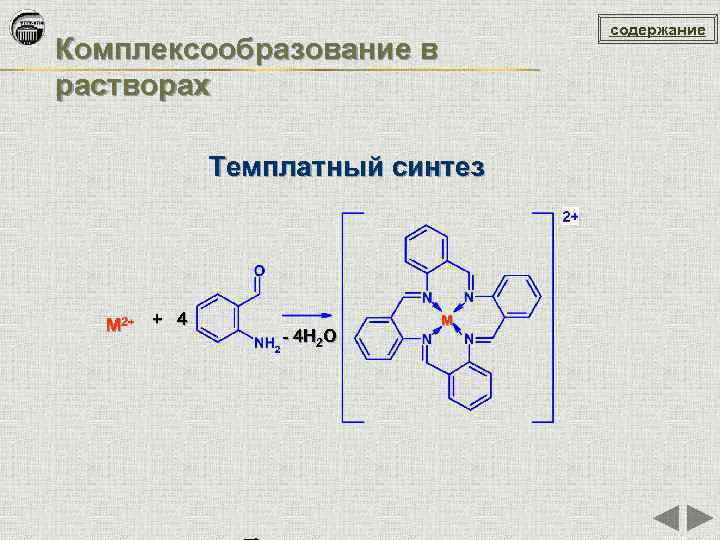 содержание Комплексообразование в растворах Темплатный синтез M 2+ + 4 - 4 H 2 O M
содержание Комплексообразование в растворах Темплатный синтез M 2+ + 4 - 4 H 2 O M
![Устойчивость комплексов содержание [М(H 2 O)6]n+ + m L [M(L)m(H 2 O)k]n+ + (6 Устойчивость комплексов содержание [М(H 2 O)6]n+ + m L [M(L)m(H 2 O)k]n+ + (6](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-32.jpg) Устойчивость комплексов содержание [М(H 2 O)6]n+ + m L [M(L)m(H 2 O)k]n+ + (6 -k)H 2 O Куст = [ M ( L ) m n + ] Кнест = [Mn+] [L]m 1 Куст
Устойчивость комплексов содержание [М(H 2 O)6]n+ + m L [M(L)m(H 2 O)k]n+ + (6 -k)H 2 O Куст = [ M ( L ) m n + ] Кнест = [Mn+] [L]m 1 Куст
![Устойчивость комплексов содержание [М]n+ + L [ML]n+ ; [МL] n+ + L [ML 2]n+ Устойчивость комплексов содержание [М]n+ + L [ML]n+ ; [МL] n+ + L [ML 2]n+](https://present5.com/presentation/3/192625256_324668178.pdf-img/192625256_324668178.pdf-33.jpg) Устойчивость комплексов содержание [М]n+ + L [ML]n+ ; [МL] n+ + L [ML 2]n+ К 1 = К 2 = [MLn+] [Mn+] [L] [ML 2 n+] [MLn+] [L] = К 1 К 2…Km ΔG 0 = –RT ln(β)
Устойчивость комплексов содержание [М]n+ + L [ML]n+ ; [МL] n+ + L [ML 2]n+ К 1 = К 2 = [MLn+] [Mn+] [L] [ML 2 n+] [MLn+] [L] = К 1 К 2…Km ΔG 0 = –RT ln(β)
 Разрушение комплексов содержание
Разрушение комплексов содержание
 Устойчивость комплексов содержание Константы нестойкости некоторых комплексов Комплексн ый ион Kнест [Co(NH 3)6 7, 75 • 10– 6 [Zn(OH)4] 3, 6 • 10– 16 2– 2+ ] [Ag(NH 3)2 1, 07 • 10– 7 [Fe(CN)6]3 1, 0 • 10– 31 – ]+ [Cu(NH 3)4 2, 14 • 10– [Fe(CN)6]4 1, 0 • 10– 36 13 – ]2+
Устойчивость комплексов содержание Константы нестойкости некоторых комплексов Комплексн ый ион Kнест [Co(NH 3)6 7, 75 • 10– 6 [Zn(OH)4] 3, 6 • 10– 16 2– 2+ ] [Ag(NH 3)2 1, 07 • 10– 7 [Fe(CN)6]3 1, 0 • 10– 31 – ]+ [Cu(NH 3)4 2, 14 • 10– [Fe(CN)6]4 1, 0 • 10– 36 13 – ]2+
 Инертность и стабильность содержание Кинетическая стабильность комплекса характеризуется терминами: q лабильный: время жизни комплекса в 0. 1 М растворе > 1 с q инертный время жизни комплекса в 0. 1 М растворе < 1 с константа скорости изотопного обмена молекул воды во внутренней координационной сфере для инертного комплекса [Ni(H 2 O)6]2+ равна 3, 3. 104 с-1, а для лабильного [Сr(Н 2 О)6]3+ – 5. 10 -7 с-1.
Инертность и стабильность содержание Кинетическая стабильность комплекса характеризуется терминами: q лабильный: время жизни комплекса в 0. 1 М растворе > 1 с q инертный время жизни комплекса в 0. 1 М растворе < 1 с константа скорости изотопного обмена молекул воды во внутренней координационной сфере для инертного комплекса [Ni(H 2 O)6]2+ равна 3, 3. 104 с-1, а для лабильного [Сr(Н 2 О)6]3+ – 5. 10 -7 с-1.
 Выводы и заключения содержание Химия комплексных соединений важнейшей является частью неорганической химии. Знание о природе взаимодействия атомов металла и лигандов в комплексе, позволяет представить механизм образования, строение и реакционную способность комплексных соединений.
Выводы и заключения содержание Химия комплексных соединений важнейшей является частью неорганической химии. Знание о природе взаимодействия атомов металла и лигандов в комплексе, позволяет представить механизм образования, строение и реакционную способность комплексных соединений.
 Список литературы n n n n содержание Кукушкин Ю. Н. Химия координационных соединений. М. : Высшая школа, 1985. Гринберг А. А. Введение в химию комплексных соединений. М. ; Л. : Химия, 1966. Вернер А. Новые воззрения в области неорганической химии. Л. : ОНТИ, 1936. Коттон Ф. , Уилкинсон Дж. Современная неорганическая химия. М. : Мир, 1969. Дятлова Н. М. , Темкина В. Я. , Попов К. И. Комплексоны и комплексонаты металлов. М. : Химия, 1988. О. В. Михайлов. Многоликая изомерия координационных соединений //Природа, 2002, № 5. О. В. Михайлов. Что такое темплатный синтез// Соросвский образовательный журнал, 1999, № 10.
Список литературы n n n n содержание Кукушкин Ю. Н. Химия координационных соединений. М. : Высшая школа, 1985. Гринберг А. А. Введение в химию комплексных соединений. М. ; Л. : Химия, 1966. Вернер А. Новые воззрения в области неорганической химии. Л. : ОНТИ, 1936. Коттон Ф. , Уилкинсон Дж. Современная неорганическая химия. М. : Мир, 1969. Дятлова Н. М. , Темкина В. Я. , Попов К. И. Комплексоны и комплексонаты металлов. М. : Химия, 1988. О. В. Михайлов. Многоликая изомерия координационных соединений //Природа, 2002, № 5. О. В. Михайлов. Что такое темплатный синтез// Соросвский образовательный журнал, 1999, № 10.


