комплексные соединения.ppt
- Количество слайдов: 38
![Комплексные соединения Na 3[Co(NO 2)6] [Cu(NH 3)4]2+ Содержание • Проблемный подход к изучению комплексных Комплексные соединения Na 3[Co(NO 2)6] [Cu(NH 3)4]2+ Содержание • Проблемный подход к изучению комплексных](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-1.jpg) Комплексные соединения Na 3[Co(NO 2)6] [Cu(NH 3)4]2+ Содержание • Проблемный подход к изучению комплексных соединений • Исторические предпосылки возникновения координационной теории • Координационная теория А. Вернера • Основы номенклатуры комплексных соединений • Строение комплексных соединений • Растворы комплексных соединений • Хелатные комплексы • Альфред Вернер K 3[Fe(CN)6] 1
Комплексные соединения Na 3[Co(NO 2)6] [Cu(NH 3)4]2+ Содержание • Проблемный подход к изучению комплексных соединений • Исторические предпосылки возникновения координационной теории • Координационная теория А. Вернера • Основы номенклатуры комплексных соединений • Строение комплексных соединений • Растворы комплексных соединений • Хелатные комплексы • Альфред Вернер K 3[Fe(CN)6] 1
 Проблема «дополнительных валентностей» n n n Cu. SO 4. 4 NH 3 – Андрей Либавий, 1597 г. Ag. Cl. 2 NH 3 – И. Глаубер, 1648 г. Co. Cl 3. 6 NH 3 – Тассер, 1798 г. 1704 г. Дисбах – получил берлинскую лазурь KCN. Fe(CN)2. Fe(CN)3 1749 -1753 гг. Пьер Жозеф Макер получил красную кровяную соль. 2
Проблема «дополнительных валентностей» n n n Cu. SO 4. 4 NH 3 – Андрей Либавий, 1597 г. Ag. Cl. 2 NH 3 – И. Глаубер, 1648 г. Co. Cl 3. 6 NH 3 – Тассер, 1798 г. 1704 г. Дисбах – получил берлинскую лазурь KCN. Fe(CN)2. Fe(CN)3 1749 -1753 гг. Пьер Жозеф Макер получил красную кровяную соль. 2
 Двойная соль или комплексное соединение? KCr(SO 4)2∙ 12 H 2 O – хромокалиевые квасцы KCr(SO 4)2∙ 12 H 2 O = = K+ + Cr 3+ + 2 SO 42 - + 12 H 2 O Fe(CN)3. 3 KCN = 3 K+ + Fe 3+ + 6 CNКрасная кровяная соль не определяются в растворе 3
Двойная соль или комплексное соединение? KCr(SO 4)2∙ 12 H 2 O – хромокалиевые квасцы KCr(SO 4)2∙ 12 H 2 O = = K+ + Cr 3+ + 2 SO 42 - + 12 H 2 O Fe(CN)3. 3 KCN = 3 K+ + Fe 3+ + 6 CNКрасная кровяная соль не определяются в растворе 3
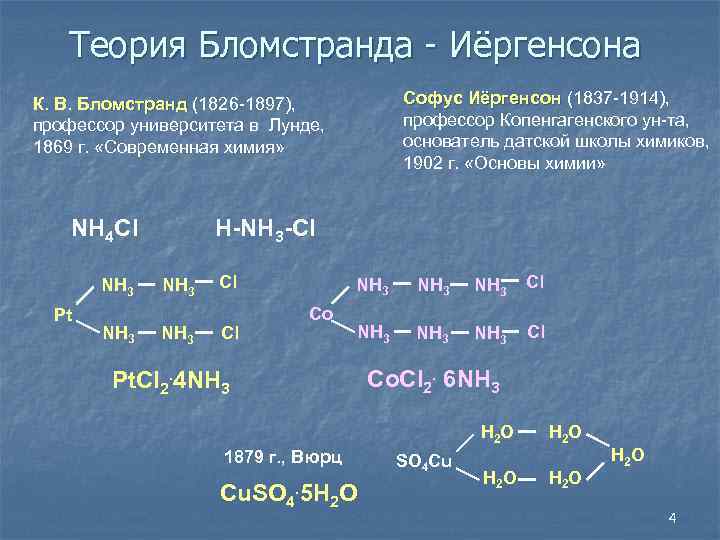 Теория Бломстранда - Иёргенсона Софус Иёргенсон (1837 -1914), профессор Копенгагенского ун-та, основатель датской школы химиков, 1902 г. «Основы химии» К. В. Бломстранд (1826 -1897), профессор университета в Лунде, 1869 г. «Современная химия» NH 4 Cl NH 3 Pt NH 3 H-NH 3 -Cl NH 3 Cl Cl Co NH 3 Cl NH 3 Cl Co. Cl 2. 6 NH 3 Pt. Cl 2. 4 NH 3 H 2 O 1879 г. , Вюрц Cu. SO 4 . 5 H 2 O SO 4 Cu H 2 O 4
Теория Бломстранда - Иёргенсона Софус Иёргенсон (1837 -1914), профессор Копенгагенского ун-та, основатель датской школы химиков, 1902 г. «Основы химии» К. В. Бломстранд (1826 -1897), профессор университета в Лунде, 1869 г. «Современная химия» NH 4 Cl NH 3 Pt NH 3 H-NH 3 -Cl NH 3 Cl Cl Co NH 3 Cl NH 3 Cl Co. Cl 2. 6 NH 3 Pt. Cl 2. 4 NH 3 H 2 O 1879 г. , Вюрц Cu. SO 4 . 5 H 2 O SO 4 Cu H 2 O 4
 Валентность постоянная или переменная? «Соединительная сила» «Атомность» Эдуард Франкланд, 1852 г. «Валентность» Г. Вихельгауз, 1868 г. Эдуард Франкланд (1825 -1899) Valencia - сила Фридрих Август Кекуле (1829 – 1896) 5
Валентность постоянная или переменная? «Соединительная сила» «Атомность» Эдуард Франкланд, 1852 г. «Валентность» Г. Вихельгауз, 1868 г. Эдуард Франкланд (1825 -1899) Valencia - сила Фридрих Август Кекуле (1829 – 1896) 5
 n Цепь аммиаков может быть, по-видимому, беспредельна, и, нам кажется, наиболее существенный недостаток такого представления и состоит именно в том, что оно не указывает вовсе на число аммиаков, могущих удерживаться платиной. Притом допустить связь азота с азотом в столь прочных телах едва ли возможно. Д. И. Менделеев 6
n Цепь аммиаков может быть, по-видимому, беспредельна, и, нам кажется, наиболее существенный недостаток такого представления и состоит именно в том, что оно не указывает вовсе на число аммиаков, могущих удерживаться платиной. Притом допустить связь азота с азотом в столь прочных телах едва ли возможно. Д. И. Менделеев 6
 Рождение координационной теории Альфред Вернер «К вопросу о строении неорганических соединений» . 1893 г. 1. 2. 3. 4. Главная и побочная валентности Принцип координации Внутренняя и внешняя сферы Пространственное строение комплексных ионов 1905 г. «Новые воззрения в области неорганической химии» 7
Рождение координационной теории Альфред Вернер «К вопросу о строении неорганических соединений» . 1893 г. 1. 2. 3. 4. Главная и побочная валентности Принцип координации Внутренняя и внешняя сферы Пространственное строение комплексных ионов 1905 г. «Новые воззрения в области неорганической химии» 7
 Главная и побочная валентности Pt. Cl 4. 2 NH 3 Cl Cl Cl Pt Cl NH 3 [Pt(NH 3)2 Cl 4] Главная валентность соответствует обычной валентности элемента, закономерности которой находят отражение в ПСХЭ Побочная валентность – дополнительная, остаточная валентность, которую атомы проявляют после насыщения главной 8
Главная и побочная валентности Pt. Cl 4. 2 NH 3 Cl Cl Cl Pt Cl NH 3 [Pt(NH 3)2 Cl 4] Главная валентность соответствует обычной валентности элемента, закономерности которой находят отражение в ПСХЭ Побочная валентность – дополнительная, остаточная валентность, которую атомы проявляют после насыщения главной 8
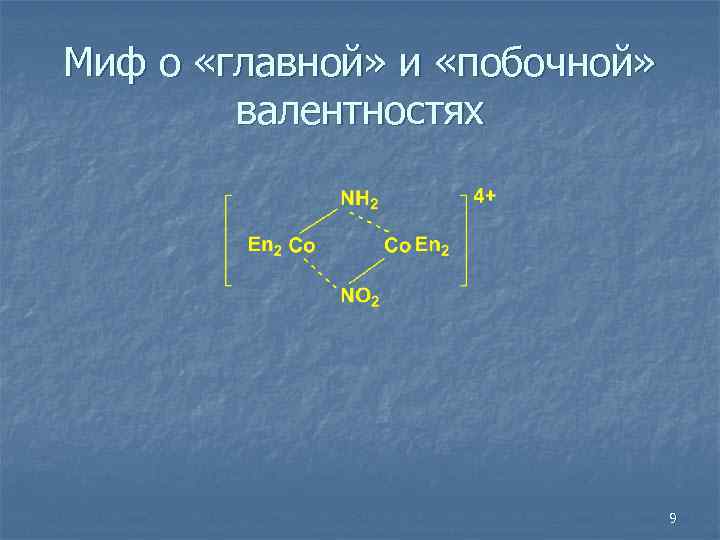 Миф о «главной» и «побочной» валентностях 9
Миф о «главной» и «побочной» валентностях 9
![Строение комплексного соединения Внешняя сфера Внутренняя сфера K 3 [Fe(CN)6] Ион. Координационное число Комплексообразователь Строение комплексного соединения Внешняя сфера Внутренняя сфера K 3 [Fe(CN)6] Ион. Координационное число Комплексообразователь](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-10.jpg) Строение комплексного соединения Внешняя сфера Внутренняя сфера K 3 [Fe(CN)6] Ион. Координационное число Комплексообразователь Лиганды [Cu(NH 3)4]Cl 2 Внутренняя сфера Внешняя сфера 10
Строение комплексного соединения Внешняя сфера Внутренняя сфера K 3 [Fe(CN)6] Ион. Координационное число Комплексообразователь Лиганды [Cu(NH 3)4]Cl 2 Внутренняя сфера Внешняя сфера 10
 Рождение стереохимии 1874 г. Якоб Вант-Гофф (1852 — 1912) «Предложение применять в пространстве современные структурно-химические формулы вместе с примечанием об отношении между оптической вращательной способностью и химической конструкцией органических соединений» «Фантастическая чепуха, Г. Кольбе напрочь лишенная какого бы то ни было фактического основания и совершенно непонятная серьезному исследователю» 11
Рождение стереохимии 1874 г. Якоб Вант-Гофф (1852 — 1912) «Предложение применять в пространстве современные структурно-химические формулы вместе с примечанием об отношении между оптической вращательной способностью и химической конструкцией органических соединений» «Фантастическая чепуха, Г. Кольбе напрочь лишенная какого бы то ни было фактического основания и совершенно непонятная серьезному исследователю» 11
![Строение комплексного соединения K 3 [Fe(CN)6] [Cu(NH 3)4]Cl 2 [Zn(NH 3)4]Cl 2 12 Строение комплексного соединения K 3 [Fe(CN)6] [Cu(NH 3)4]Cl 2 [Zn(NH 3)4]Cl 2 12](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-12.jpg) Строение комплексного соединения K 3 [Fe(CN)6] [Cu(NH 3)4]Cl 2 [Zn(NH 3)4]Cl 2 12
Строение комплексного соединения K 3 [Fe(CN)6] [Cu(NH 3)4]Cl 2 [Zn(NH 3)4]Cl 2 12
![Номенклатура комплексных соединений +3 n K 3 [Fe(CN)6] Гексацианоферрат(III) калия +2 n [Cu(NH 3)4]Cl Номенклатура комплексных соединений +3 n K 3 [Fe(CN)6] Гексацианоферрат(III) калия +2 n [Cu(NH 3)4]Cl](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-13.jpg) Номенклатура комплексных соединений +3 n K 3 [Fe(CN)6] Гексацианоферрат(III) калия +2 n [Cu(NH 3)4]Cl 2 Хлорид тетраамминмеди(II) 1 – моно 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса H 2 O – аква NH 3 – аммин Cl- – хлоро. NO 2 - - нитро CN- - циано. SCN- - родано- Порядок перечисления лиганд: 1. Анионные: H-, O 2 -, OH-, простые анионы, многоатомные анионы, органические в алфавитном порядке 1. Нейтральные: NH 3, H 2 O и т. д. - -о 2. Катионные: N 2 H 5+ и т. д. + -иум 13
Номенклатура комплексных соединений +3 n K 3 [Fe(CN)6] Гексацианоферрат(III) калия +2 n [Cu(NH 3)4]Cl 2 Хлорид тетраамминмеди(II) 1 – моно 2 – ди 3 – три 4 – тетра 5 – пента 6 – гекса H 2 O – аква NH 3 – аммин Cl- – хлоро. NO 2 - - нитро CN- - циано. SCN- - родано- Порядок перечисления лиганд: 1. Анионные: H-, O 2 -, OH-, простые анионы, многоатомные анионы, органические в алфавитном порядке 1. Нейтральные: NH 3, H 2 O и т. д. - -о 2. Катионные: N 2 H 5+ и т. д. + -иум 13
2 Соль Чугаева [Pt. Упражнение 1 n n n n Первое основание Рейзе [Pt(NH 3)4](OH)2 Соль Чугаева [Pt.](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-14.jpg) Упражнение 1 n n n n Первое основание Рейзе [Pt(NH 3)4](OH)2 Соль Чугаева [Pt. Cl(NH 3)5]Cl 3 Соль Цейзе K[Pt. Cl 3 C 2 H 4] Пурпуреосоль [Co. Cl(NH 3)5]Cl 2 Кроцеосоль [Co(NO 2)2(NH 3)4]Cl Соль Рейнеке NH 4[Cr(SCN)4(NH 3)2] Соль Магнуса [Pt(NH 3)4][Pt. Cl 4] 14
Упражнение 1 n n n n Первое основание Рейзе [Pt(NH 3)4](OH)2 Соль Чугаева [Pt. Cl(NH 3)5]Cl 3 Соль Цейзе K[Pt. Cl 3 C 2 H 4] Пурпуреосоль [Co. Cl(NH 3)5]Cl 2 Кроцеосоль [Co(NO 2)2(NH 3)4]Cl Соль Рейнеке NH 4[Cr(SCN)4(NH 3)2] Соль Магнуса [Pt(NH 3)4][Pt. Cl 4] 14
![Упражнение 2 n n Гексанитрокобальтат(III) натрия Na 3[Co(NO 2)6] Гидроксид диамминсеребра(I) [Ag(NH 3)2]OH реактив Упражнение 2 n n Гексанитрокобальтат(III) натрия Na 3[Co(NO 2)6] Гидроксид диамминсеребра(I) [Ag(NH 3)2]OH реактив](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-15.jpg) Упражнение 2 n n Гексанитрокобальтат(III) натрия Na 3[Co(NO 2)6] Гидроксид диамминсеребра(I) [Ag(NH 3)2]OH реактив Толленса Тетраиодомеркурат(II) калия K 2[Hg. I 4] реактив Несслера Тетрароданомеркурат(II) аммония (NH 4)2[Hg(SCN)4] 15
Упражнение 2 n n Гексанитрокобальтат(III) натрия Na 3[Co(NO 2)6] Гидроксид диамминсеребра(I) [Ag(NH 3)2]OH реактив Толленса Тетраиодомеркурат(II) калия K 2[Hg. I 4] реактив Несслера Тетрароданомеркурат(II) аммония (NH 4)2[Hg(SCN)4] 15
 16
16
 Вернер подтверждает Вернера 1893 -4 гг. не были периодом утверждения теории. Вернер 20 лет не оставлял лаборатории Для установления состава соединений Вернер использовал: 1. Химический метод 2. Измерение электропроводности Химический метод При действии Ag. NO 3 на 1 моль Cr. Cl 3. 6 NH 3 осаждается 3 моль Cl[Cr(NH 3)6]Cl 3 на 1 моль Cr. Cl 3. 5 NH 3 осаждается 2 моль Cl[Cr(NH 3)5 Cl]Cl 2 на 1 моль Cr. Cl 3. 4 NH 3 осаждается 1 моль Cl[Cr(NH 3)4 Cl 2]Cl 17
Вернер подтверждает Вернера 1893 -4 гг. не были периодом утверждения теории. Вернер 20 лет не оставлял лаборатории Для установления состава соединений Вернер использовал: 1. Химический метод 2. Измерение электропроводности Химический метод При действии Ag. NO 3 на 1 моль Cr. Cl 3. 6 NH 3 осаждается 3 моль Cl[Cr(NH 3)6]Cl 3 на 1 моль Cr. Cl 3. 5 NH 3 осаждается 2 моль Cl[Cr(NH 3)5 Cl]Cl 2 на 1 моль Cr. Cl 3. 4 NH 3 осаждается 1 моль Cl[Cr(NH 3)4 Cl 2]Cl 17
![Ряды Вернера - Миолати 3 4 5 6 7 [Pt(NH 3)4 Cl 2]Cl 2 Ряды Вернера - Миолати 3 4 5 6 7 [Pt(NH 3)4 Cl 2]Cl 2](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-18.jpg) Ряды Вернера - Миолати 3 4 5 6 7 [Pt(NH 3)4 Cl 2]Cl 2 [Pt(NH 3)3 Cl 3]Cl [Pt(NH 3)2 Cl 4] K[Pt(NH 3)Cl 5] K 2[Pt. Cl 6] , Ом-1. см 2. моль-1 Диаграмма молярной электропроводности соединений В 1893 г. А. Вернер совместно с А. Миолати, используя метод измерения молярной электропроводности установили закономерности ее изменения в ряду комплексных соединений. 1 [Pt(NH 3)6]Cl В основе метода 4 способность электролитов проводить эл. ток – 2 в зависимости. Cl]Cl 3 [Pt(NH 3)5 от наличия свободных ионов в растворе 18
Ряды Вернера - Миолати 3 4 5 6 7 [Pt(NH 3)4 Cl 2]Cl 2 [Pt(NH 3)3 Cl 3]Cl [Pt(NH 3)2 Cl 4] K[Pt(NH 3)Cl 5] K 2[Pt. Cl 6] , Ом-1. см 2. моль-1 Диаграмма молярной электропроводности соединений В 1893 г. А. Вернер совместно с А. Миолати, используя метод измерения молярной электропроводности установили закономерности ее изменения в ряду комплексных соединений. 1 [Pt(NH 3)6]Cl В основе метода 4 способность электролитов проводить эл. ток – 2 в зависимости. Cl]Cl 3 [Pt(NH 3)5 от наличия свободных ионов в растворе 18
![Изомерия комплексов Pt. Cl 2. 2 NH 3 [Pt(NH 3)2 Cl 2] Цис-изомер Cl Изомерия комплексов Pt. Cl 2. 2 NH 3 [Pt(NH 3)2 Cl 2] Цис-изомер Cl](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-19.jpg) Изомерия комплексов Pt. Cl 2. 2 NH 3 [Pt(NH 3)2 Cl 2] Цис-изомер Cl NH 3 Pt Cl Транс-изомер Cl NH 3 Pt NH 3 Соль Пейроне NH 3 Cl Хлорид второго основания Рейзе 1844 г. М. Пейроне Оранжево-желтый Светло-желтый Противоопухолевая активность! Мичиганский ун-т, д-р Барнетт Розенберг 19
Изомерия комплексов Pt. Cl 2. 2 NH 3 [Pt(NH 3)2 Cl 2] Цис-изомер Cl NH 3 Pt Cl Транс-изомер Cl NH 3 Pt NH 3 Соль Пейроне NH 3 Cl Хлорид второго основания Рейзе 1844 г. М. Пейроне Оранжево-желтый Светло-желтый Противоопухолевая активность! Мичиганский ун-т, д-р Барнетт Розенберг 19
![Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr(H 2 O)5 Cl]Cl 2 Светло-зеленый [Cr(H Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr(H 2 O)5 Cl]Cl 2 Светло-зеленый [Cr(H](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-20.jpg) Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr(H 2 O)5 Cl]Cl 2 Светло-зеленый [Cr(H 2 O)4 Cl 2]Cl Темно-зеленый 20
Сольватная изомерия [Cr(H 2 O)6]Cl 3 Фиолетовый [Cr(H 2 O)5 Cl]Cl 2 Светло-зеленый [Cr(H 2 O)4 Cl 2]Cl Темно-зеленый 20
![Механизм образования комплексного иона [Al(OH)4]- 21 Механизм образования комплексного иона [Al(OH)4]- 21](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-21.jpg) Механизм образования комплексного иона [Al(OH)4]- 21
Механизм образования комплексного иона [Al(OH)4]- 21
![Комплексные соединения в растворах Первичная диссоциация комплексных соединений K 3[Fe(CN)6] = 3 K+ + Комплексные соединения в растворах Первичная диссоциация комплексных соединений K 3[Fe(CN)6] = 3 K+ +](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-22.jpg) Комплексные соединения в растворах Первичная диссоциация комплексных соединений K 3[Fe(CN)6] = 3 K+ + [Fe(CN)6]3[Cu(NH 3)4]SO 4 = [Cu(NH 3)4]2+ + SO 42[Ag(NH 3)2]Cl = [Ag(NH 3)2]+ + Cl- 22
Комплексные соединения в растворах Первичная диссоциация комплексных соединений K 3[Fe(CN)6] = 3 K+ + [Fe(CN)6]3[Cu(NH 3)4]SO 4 = [Cu(NH 3)4]2+ + SO 42[Ag(NH 3)2]Cl = [Ag(NH 3)2]+ + Cl- 22
![Вторичная диссоциация комплексов [Ag(NH 3)2]+ [Ag(NH 3)]+ + NH 3 Ag+ + NH 3 Вторичная диссоциация комплексов [Ag(NH 3)2]+ [Ag(NH 3)]+ + NH 3 Ag+ + NH 3](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-23.jpg) Вторичная диссоциация комплексов [Ag(NH 3)2]+ [Ag(NH 3)]+ + NH 3 Ag+ + NH 3 [Ag(NH 3)2]+ Ag+ + 2 NH 3 KH = [Ag+] [NH 3]2 = 9, 3. 10 -8 [ [Ag(NH 3)2]+ ] Диссоциация комплексов (или реакции обмена лигандов на молекулы растворителя) количественно характеризуется константами нестойкости комплексов Kн. 23
Вторичная диссоциация комплексов [Ag(NH 3)2]+ [Ag(NH 3)]+ + NH 3 Ag+ + NH 3 [Ag(NH 3)2]+ Ag+ + 2 NH 3 KH = [Ag+] [NH 3]2 = 9, 3. 10 -8 [ [Ag(NH 3)2]+ ] Диссоциация комплексов (или реакции обмена лигандов на молекулы растворителя) количественно характеризуется константами нестойкости комплексов Kн. 23
![Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа](https://present5.com/presentation/3/53657083_136923441.pdf-img/53657083_136923441.pdf-24.jpg) Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа нестойкости 1, 0. 10– 31 1, 0. 10– 36 7, 75. 10– 6 9, 31. 10– 8 2, 14. 10– 13 3, 6. 10– 16 24
Константы нестойкости некоторых комплексов Комплексный ион [Fe(CN)6]3[Fe(CN)6]4[Co(NH 3)6]2+ [Ag(NH 3)2]+ [Cu(NH 3)4]2+ [Zn(OH)4]2– Константа нестойкости 1, 0. 10– 31 1, 0. 10– 36 7, 75. 10– 6 9, 31. 10– 8 2, 14. 10– 13 3, 6. 10– 16 24
 Что же такое комплексы? Комплексные соединения – вещества, существующие как в кристаллическом состоянии, так и в растворе, особенностью которых является наличие центрального атома (акцептора электронов), окруженного лигандами (донорами электронов). В растворе лиганды способны ступенчато и обратимо отщепляться от центрального атома по гетеролитическому типу. n 25
Что же такое комплексы? Комплексные соединения – вещества, существующие как в кристаллическом состоянии, так и в растворе, особенностью которых является наличие центрального атома (акцептора электронов), окруженного лигандами (донорами электронов). В растворе лиганды способны ступенчато и обратимо отщепляться от центрального атома по гетеролитическому типу. n 25
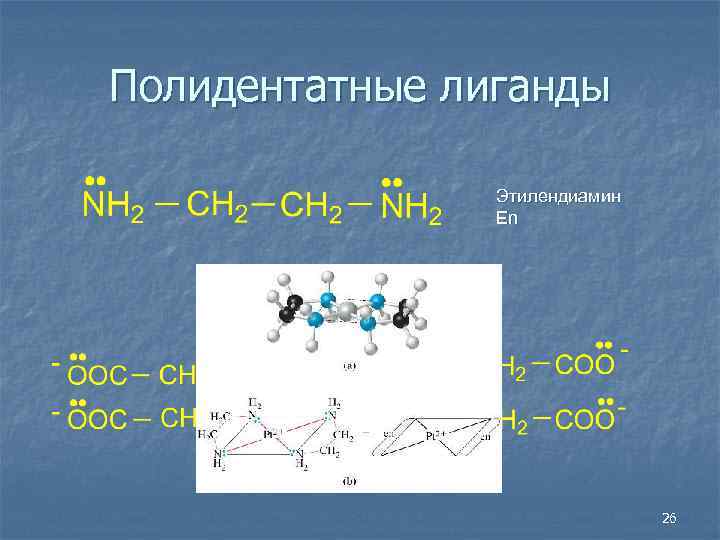 Полидентатные лиганды Этилендиамин En ЭДТА 26
Полидентатные лиганды Этилендиамин En ЭДТА 26
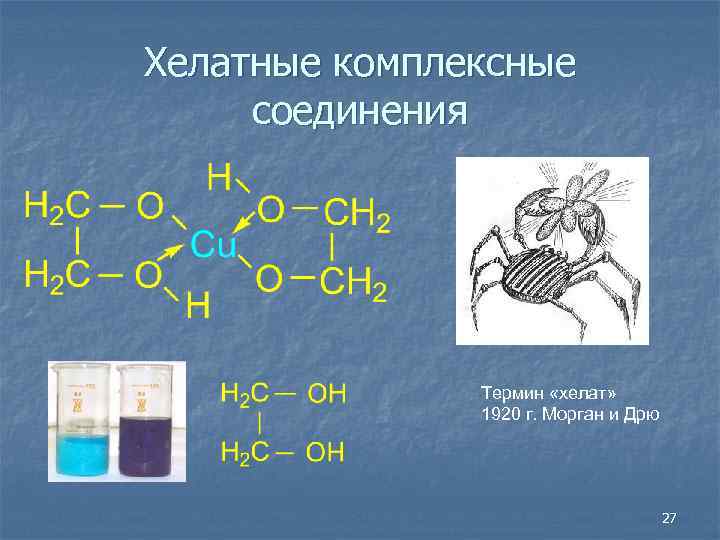 Хелатные комплексные соединения Термин «хелат» 1920 г. Морган и Дрю 27
Хелатные комплексные соединения Термин «хелат» 1920 г. Морган и Дрю 27
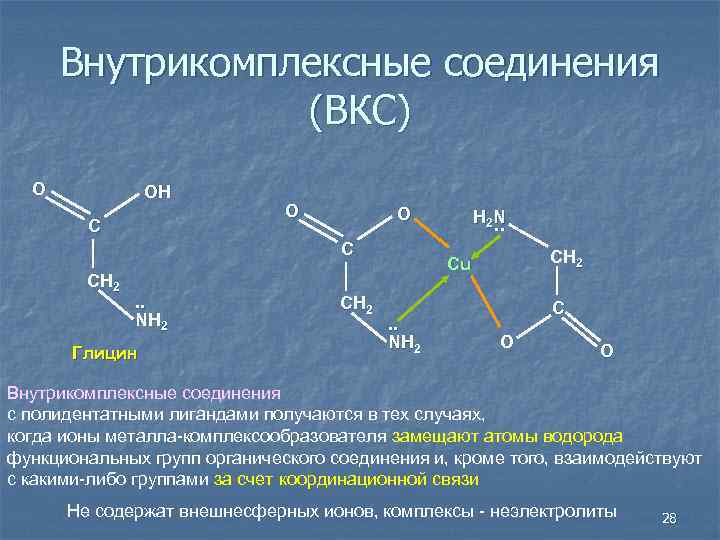 Внутрикомплексные соединения (ВКС) O OH С O O С CH 2 . . NH 2 Глицин CH 2 N. . CH 2 Cu . . NH 2 С O O Внутрикомплексные соединения с полидентатными лигандами получаются в тех случаях, когда ионы металла-комплексообразователя замещают атомы водорода функциональных групп органического соединения и, кроме того, взаимодействуют с какими-либо группами за счет координационной связи Не содержат внешнесферных ионов, комплексы - неэлектролиты 28
Внутрикомплексные соединения (ВКС) O OH С O O С CH 2 . . NH 2 Глицин CH 2 N. . CH 2 Cu . . NH 2 С O O Внутрикомплексные соединения с полидентатными лигандами получаются в тех случаях, когда ионы металла-комплексообразователя замещают атомы водорода функциональных групп органического соединения и, кроме того, взаимодействуют с какими-либо группами за счет координационной связи Не содержат внешнесферных ионов, комплексы - неэлектролиты 28
 Качественная реакция на Ni 2+ c диметилглиоксимом Реактив Чугаева Лев Александрович Чугаев (1873 -1922) 29
Качественная реакция на Ni 2+ c диметилглиоксимом Реактив Чугаева Лев Александрович Чугаев (1873 -1922) 29
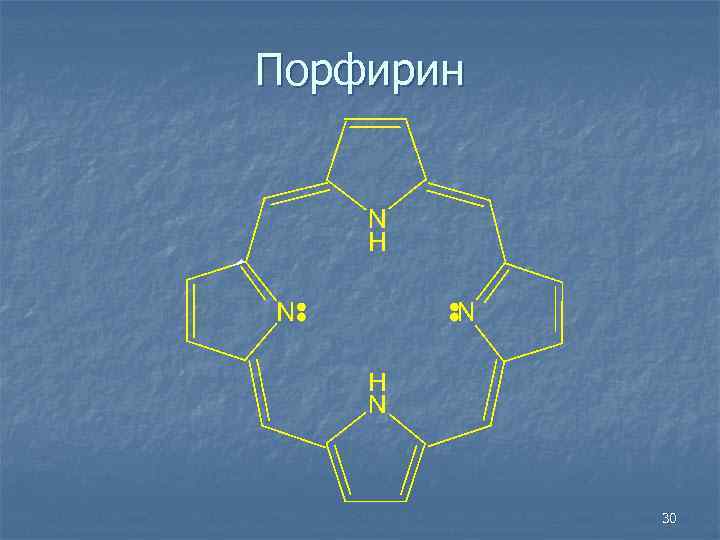 Порфирин 30
Порфирин 30
 Хлорофилл 31
Хлорофилл 31
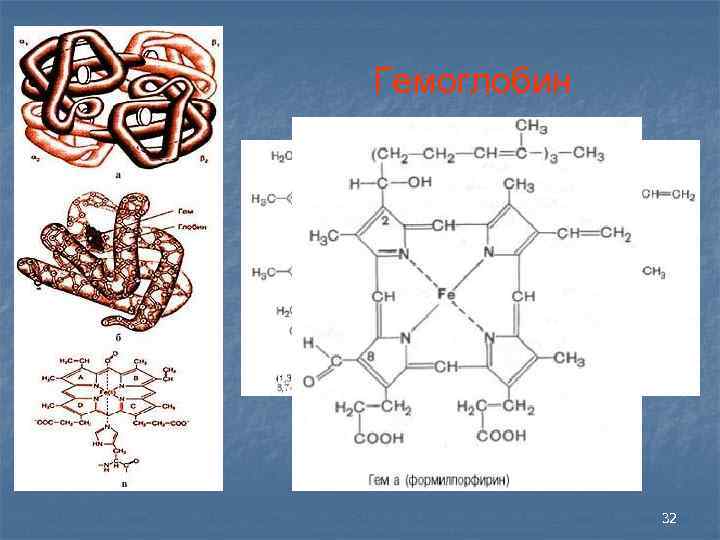 Гемоглобин 32
Гемоглобин 32
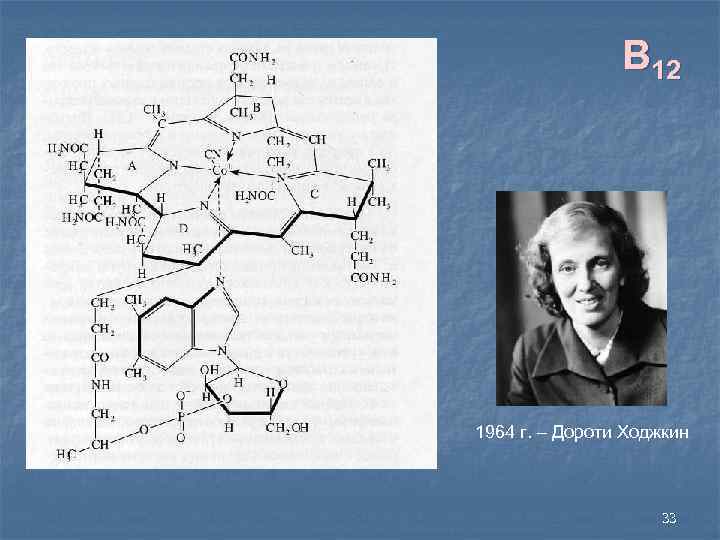 B 12 1964 г. – Дороти Ходжкин 33
B 12 1964 г. – Дороти Ходжкин 33
 Альфред Вернер 1866 -1919 1866 г. – родился в Мюлузе (Эльзас) 34
Альфред Вернер 1866 -1919 1866 г. – родился в Мюлузе (Эльзас) 34
 1885 г. – служба в армии в Карлсруэ С 1886 г. – Цюрих. 1886 г. – 1889 г. Цюрихский политехникум. Профессор Артур Ганч 1890 г. «О пространственном расположении атомов в азотсодержащих молекулах» 1891 г. – конкурсная работа на звание приват-доцента «К теории сродства и валентности» 1891 г – стажировка в лаборатории Марселена Бертло 1892 г. -1893 г. – статья «О строении неорганических соединений» 35
1885 г. – служба в армии в Карлсруэ С 1886 г. – Цюрих. 1886 г. – 1889 г. Цюрихский политехникум. Профессор Артур Ганч 1890 г. «О пространственном расположении атомов в азотсодержащих молекулах» 1891 г. – конкурсная работа на звание приват-доцента «К теории сродства и валентности» 1891 г – стажировка в лаборатории Марселена Бертло 1892 г. -1893 г. – статья «О строении неорганических соединений» 35
 Альфред Вернер 1866 -1919 В 1913 г. шведский король Густав V вручил Альфреду Вернеру золотую медаль лауреата Нобелевской премии и диплом, "в признание его работ о природе связей в молекулах, которыми он по-новому осветил старые проблемы и открыл новые области для исследований, особенно в неорганической химии". "Меня часто охватывает экстаз пред красотой моей науки. Чем дальше я погружаюсь в ее тайны, тем более она кажется мне огромной, величественной, слишком красивой для простого смертного" 36
Альфред Вернер 1866 -1919 В 1913 г. шведский король Густав V вручил Альфреду Вернеру золотую медаль лауреата Нобелевской премии и диплом, "в признание его работ о природе связей в молекулах, которыми он по-новому осветил старые проблемы и открыл новые области для исследований, особенно в неорганической химии". "Меня часто охватывает экстаз пред красотой моей науки. Чем дальше я погружаюсь в ее тайны, тем более она кажется мне огромной, величественной, слишком красивой для простого смертного" 36
 Спасибо за внимание! 37
Спасибо за внимание! 37
 Литература • Кукушкин Ю. Н. Химия координационных соединений. М. : Высшая школа, 1985. • Кукушкин Ю. Н. Соединения высшего порядка. Л. : Химия, 1991. • Макашев Ю. А. , Замяткина В. М. Соединения в квадратных скобках. Л. : Химия, 1976. • Степин Б. Д. , Аликберова Л. Ю. Книга по химии для домашнего чтения. М. : Химия, 1994. • Беликова М. Ю. Чудесные секреты Мастера Турнбуля // Химия в школе. – № 4. – 1998. – С. 27 -37 • Федоренко Н. В. Вернер: изучение сочетаний атомов в молекуле // Химия в школе. – № 4. – 1998. – С. 79 -83 http: //www. alhimik. ru/compl_soed/content. htm http: //www. chem. msu. su/rus/school/zhukov/welcome. html 38
Литература • Кукушкин Ю. Н. Химия координационных соединений. М. : Высшая школа, 1985. • Кукушкин Ю. Н. Соединения высшего порядка. Л. : Химия, 1991. • Макашев Ю. А. , Замяткина В. М. Соединения в квадратных скобках. Л. : Химия, 1976. • Степин Б. Д. , Аликберова Л. Ю. Книга по химии для домашнего чтения. М. : Химия, 1994. • Беликова М. Ю. Чудесные секреты Мастера Турнбуля // Химия в школе. – № 4. – 1998. – С. 27 -37 • Федоренко Н. В. Вернер: изучение сочетаний атомов в молекуле // Химия в школе. – № 4. – 1998. – С. 79 -83 http: //www. alhimik. ru/compl_soed/content. htm http: //www. chem. msu. su/rus/school/zhukov/welcome. html 38


