комплексные соедин.ppt
- Количество слайдов: 31
 Комплексные соединения N Mg N О О N N О О O 11 класс естественнонаучный
Комплексные соединения N Mg N О О N N О О O 11 класс естественнонаучный
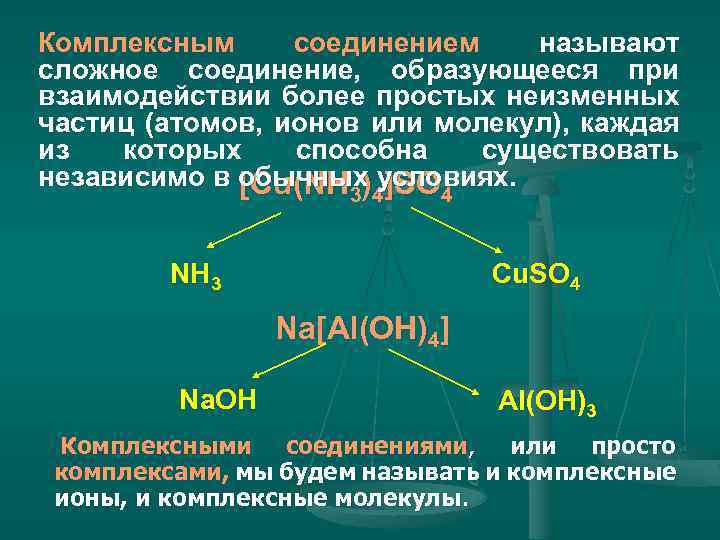 Комплексным соединением называют сложное соединение, образующееся при взаимодействии более простых неизменных частиц (атомов, ионов или молекул), каждая из которых способна существовать независимо в обычных условиях. [Cu(NH ) ]SO 3 4 4 NH 3 Cu. SO 4 Na[Al(OH)4] Na. OH Al(OH)3 Комплексными соединениями, или просто комплексами, мы будем называть и комплексные ионы, и комплексные молекулы.
Комплексным соединением называют сложное соединение, образующееся при взаимодействии более простых неизменных частиц (атомов, ионов или молекул), каждая из которых способна существовать независимо в обычных условиях. [Cu(NH ) ]SO 3 4 4 NH 3 Cu. SO 4 Na[Al(OH)4] Na. OH Al(OH)3 Комплексными соединениями, или просто комплексами, мы будем называть и комплексные ионы, и комплексные молекулы.
 Наиболее удачно строение и свойства таких соединений объясняет координационная теория. Предложена в 1893 г. швейцарским химиком, лауреатом Нобелевской премии, профессором Цюрихского университета Альфредом Вернером и дополненная русскими учёными Л. А Чугаевым, И. Л. Черняевым и А. А. Гринбергом. (1866 – 1919)
Наиболее удачно строение и свойства таких соединений объясняет координационная теория. Предложена в 1893 г. швейцарским химиком, лауреатом Нобелевской премии, профессором Цюрихского университета Альфредом Вернером и дополненная русскими учёными Л. А Чугаевым, И. Л. Черняевым и А. А. Гринбергом. (1866 – 1919)
 Основные положения координационной теории 1 Комплексообразователь (центральный катион) - катион металла, который обладает вакантными орбиталями. Катионы: nметаллов (d-элементов): Сu+2, Co+3, Fe+3, Hg+2 и др. n(реже р-элементы): Al+3 n(иногда неметаллы): В+3, Si+4. + +3 K[Fe(CN)6] Fe
Основные положения координационной теории 1 Комплексообразователь (центральный катион) - катион металла, который обладает вакантными орбиталями. Катионы: nметаллов (d-элементов): Сu+2, Co+3, Fe+3, Hg+2 и др. n(реже р-элементы): Al+3 n(иногда неметаллы): В+3, Si+4. + +3 K[Fe(CN)6] Fe
 Основные положения координационной теории 2. Вокруг комплексообразователя расположены лиганды – частицы, обладающие неподеленными электронными парами. Молекулы: . . H 2 O, NH 3, . . Анионы: CN-, OH-, Cl-, Br-, NO 2 -
Основные положения координационной теории 2. Вокруг комплексообразователя расположены лиганды – частицы, обладающие неподеленными электронными парами. Молекулы: . . H 2 O, NH 3, . . Анионы: CN-, OH-, Cl-, Br-, NO 2 -
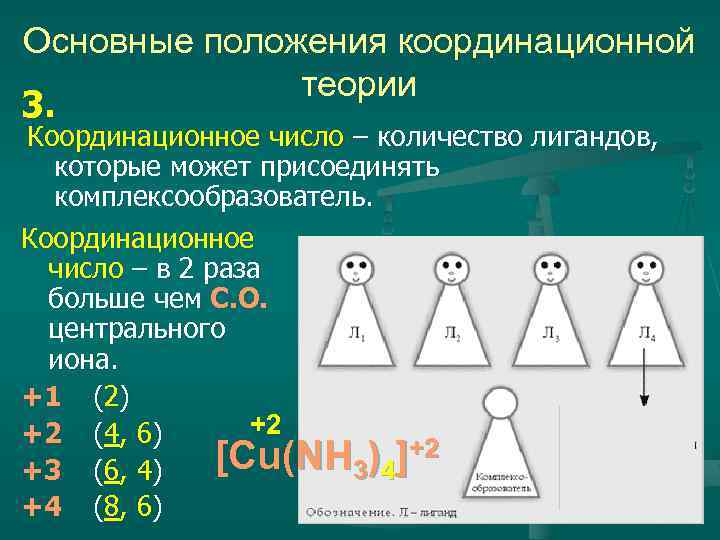 Основные положения координационной теории 3. Координационное число – количество лигандов, которые может присоединять комплексообразователь. Координационное число – в 2 раза больше чем С. О. центрального иона. +1 (2) +2 +2 (4, 6) [Cu(NH 3)4]+2 +3 (6, 4) +4 (8, 6)
Основные положения координационной теории 3. Координационное число – количество лигандов, которые может присоединять комплексообразователь. Координационное число – в 2 раза больше чем С. О. центрального иона. +1 (2) +2 +2 (4, 6) [Cu(NH 3)4]+2 +3 (6, 4) +4 (8, 6)
 Основные положения координационной теории 4. Комплексообразователь и лиганды составляют внутреннюю сферу комплекса. [Cu(NH ) ]+2 3 4 Как определить суммарный заряд внутренней сферы?
Основные положения координационной теории 4. Комплексообразователь и лиганды составляют внутреннюю сферу комплекса. [Cu(NH ) ]+2 3 4 Как определить суммарный заряд внутренней сферы?
![РАССТАВЬТЕ СТЕПЕНЬ ОКИСЛЕНИЯ ИОНА КОМПЛЕКСООБРАЗОВАТЕЛЯ: Na 3[Al. F 6] Ответ: Na+3[Al+3 F-6] K[Mg. Cl РАССТАВЬТЕ СТЕПЕНЬ ОКИСЛЕНИЯ ИОНА КОМПЛЕКСООБРАЗОВАТЕЛЯ: Na 3[Al. F 6] Ответ: Na+3[Al+3 F-6] K[Mg. Cl](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-8.jpg) РАССТАВЬТЕ СТЕПЕНЬ ОКИСЛЕНИЯ ИОНА КОМПЛЕКСООБРАЗОВАТЕЛЯ: Na 3[Al. F 6] Ответ: Na+3[Al+3 F-6] K[Mg. Cl 3] Ответ: K+[Mg+2 Cl-3] Na[Al(OH)4] Ответ: Na+[Al+3(OH)-4] Na 4[Fe(CN)6] Ответ: Na+4[Fe+2(CN)-6] Na 3[Al(OH)6] Ответ: Na+3[Al+3(OH)-6] [Cu(NH 3)4]Cl 2 Ответ: [Cu+2(NH 3)04]Cl-2
РАССТАВЬТЕ СТЕПЕНЬ ОКИСЛЕНИЯ ИОНА КОМПЛЕКСООБРАЗОВАТЕЛЯ: Na 3[Al. F 6] Ответ: Na+3[Al+3 F-6] K[Mg. Cl 3] Ответ: K+[Mg+2 Cl-3] Na[Al(OH)4] Ответ: Na+[Al+3(OH)-4] Na 4[Fe(CN)6] Ответ: Na+4[Fe+2(CN)-6] Na 3[Al(OH)6] Ответ: Na+3[Al+3(OH)-6] [Cu(NH 3)4]Cl 2 Ответ: [Cu+2(NH 3)04]Cl-2
![КОМПЛЕКСНЫЙ ИОН СТРОЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Cu(NH 3)4]Cl 2 КОМПЛЕКСООБРАЗОВАТЕЛЬ ЛИГАНДЫ КООРДИНАЦИОННОЕ ЧИСЛО - 4 КОМПЛЕКСНЫЙ ИОН СТРОЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Cu(NH 3)4]Cl 2 КОМПЛЕКСООБРАЗОВАТЕЛЬ ЛИГАНДЫ КООРДИНАЦИОННОЕ ЧИСЛО - 4](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-9.jpg) КОМПЛЕКСНЫЙ ИОН СТРОЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Cu(NH 3)4]Cl 2 КОМПЛЕКСООБРАЗОВАТЕЛЬ ЛИГАНДЫ КООРДИНАЦИОННОЕ ЧИСЛО - 4 ВНУТРЕННЯЯ СФЕРА ВНЕШНЯЯ СФЕРА
КОМПЛЕКСНЫЙ ИОН СТРОЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ [Cu(NH 3)4]Cl 2 КОМПЛЕКСООБРАЗОВАТЕЛЬ ЛИГАНДЫ КООРДИНАЦИОННОЕ ЧИСЛО - 4 ВНУТРЕННЯЯ СФЕРА ВНЕШНЯЯ СФЕРА
 Строение комплексных соединений n n Координационные соединения образованы металлами побочных подгрупп, имеющими, как правило, незавершенный d - уровень. Метод валентных связей (ВС) принимает во внимание донорно-акцепторное происхождение связей в комплексных соединениях. Образование комплексного иона можно объяснить наличием у катионов d-металлов вакантных орбиталей на s-, p-, d- и f- подуровнях: Co 0 Co 3+ 4 s 4 s 4 р 4 р 3 d 3 d
Строение комплексных соединений n n Координационные соединения образованы металлами побочных подгрупп, имеющими, как правило, незавершенный d - уровень. Метод валентных связей (ВС) принимает во внимание донорно-акцепторное происхождение связей в комплексных соединениях. Образование комплексного иона можно объяснить наличием у катионов d-металлов вакантных орбиталей на s-, p-, d- и f- подуровнях: Co 0 Co 3+ 4 s 4 s 4 р 4 р 3 d 3 d
 Строение комплексных соединений n Для образования прочных связей внутри комплексного соединения энергетически выгодно освободить две d-орбитали спариванием электронов: Co 3+ n 4 s 4 р 3 d Свободные орбитали атомов кобальта, в свою очередь, являются вакансиями для неподелённой электронной пары азота в молекуле аммиака. Так происходит образование внутренней координационной сферы комплексного соединения: Co 3+ . . NH NH NH . . NH
Строение комплексных соединений n Для образования прочных связей внутри комплексного соединения энергетически выгодно освободить две d-орбитали спариванием электронов: Co 3+ n 4 s 4 р 3 d Свободные орбитали атомов кобальта, в свою очередь, являются вакансиями для неподелённой электронной пары азота в молекуле аммиака. Так происходит образование внутренней координационной сферы комплексного соединения: Co 3+ . . NH NH NH . . NH
 Классификация комплексных соединений Комплексные соединения классифицируют по заряду комплекса по виду лигандов по составу внешней сферы
Классификация комплексных соединений Комплексные соединения классифицируют по заряду комплекса по виду лигандов по составу внешней сферы
![Классификация По заряду комплекса Катионные Нейтральные [Cr(H 2 O)4]3+Cl 3 [Pt. Cl 4(NH 3)2] Классификация По заряду комплекса Катионные Нейтральные [Cr(H 2 O)4]3+Cl 3 [Pt. Cl 4(NH 3)2]](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-13.jpg) Классификация По заряду комплекса Катионные Нейтральные [Cr(H 2 O)4]3+Cl 3 [Pt. Cl 4(NH 3)2] Катионно анионные [Cu(NH 3)4]2+[Pt. Cl 4]2 - Анионные K 2[Pt. Cl 6]2 -
Классификация По заряду комплекса Катионные Нейтральные [Cr(H 2 O)4]3+Cl 3 [Pt. Cl 4(NH 3)2] Катионно анионные [Cu(NH 3)4]2+[Pt. Cl 4]2 - Анионные K 2[Pt. Cl 6]2 -
![Классификация По составу внешней сферы Кислоты H 2[Pt. Cl 6] Основания [Ag(NH 3)2]OH Соли Классификация По составу внешней сферы Кислоты H 2[Pt. Cl 6] Основания [Ag(NH 3)2]OH Соли](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-14.jpg) Классификация По составу внешней сферы Кислоты H 2[Pt. Cl 6] Основания [Ag(NH 3)2]OH Соли Na 3[Al. F 6] Неэлектролиты [Pt(NH 3)2 Cl 2]
Классификация По составу внешней сферы Кислоты H 2[Pt. Cl 6] Основания [Ag(NH 3)2]OH Соли Na 3[Al. F 6] Неэлектролиты [Pt(NH 3)2 Cl 2]
![Классификация По виду лигандов Аквакомплексные [Fe(H 2 O)6]SO 4 Смешанные [Co. Cl(NH 3)3(H 2 Классификация По виду лигандов Аквакомплексные [Fe(H 2 O)6]SO 4 Смешанные [Co. Cl(NH 3)3(H 2](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-15.jpg) Классификация По виду лигандов Аквакомплексные [Fe(H 2 O)6]SO 4 Смешанные [Co. Cl(NH 3)3(H 2 O)2](NO 3)2 Ацидокомплексные K[Au(CN)4] Аминокомплексные [Zn(NH 3)4]Cl 2
Классификация По виду лигандов Аквакомплексные [Fe(H 2 O)6]SO 4 Смешанные [Co. Cl(NH 3)3(H 2 O)2](NO 3)2 Ацидокомплексные K[Au(CN)4] Аминокомплексные [Zn(NH 3)4]Cl 2
 Комплексные соединения N Mg N О О N N О О O 11 класс естественнонаучный
Комплексные соединения N Mg N О О N N О О O 11 класс естественнонаучный
 НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ ЧИСЛИТЕЛЬН НАЗВАНИЯ ЫЕ: 2 - ди- ЛИГАНДОВ: H 2 O - аква 3 - три- NH 3 - амин 4 - тетра- СO - карбонил 5 - пента- OН- - гидроксо- 6 - гекса- (СN)- - циано (NO 2)- - нитро F-, Cl-, Br-, I- - фторо-, хлоро-, бромо-, йодо-
НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ ЧИСЛИТЕЛЬН НАЗВАНИЯ ЫЕ: 2 - ди- ЛИГАНДОВ: H 2 O - аква 3 - три- NH 3 - амин 4 - тетра- СO - карбонил 5 - пента- OН- - гидроксо- 6 - гекса- (СN)- - циано (NO 2)- - нитро F-, Cl-, Br-, I- - фторо-, хлоро-, бромо-, йодо-
 НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ НАЗВАНИЯ КОМПЛЕКСНЫХ АНИОНОВ: +3 Fe - феррат +2 Cu - купрат + Ag - аргентат +3 Au - аурат +2 Hg - меркурат +2 Zn - цинкат +3 Al - алюминат От латинского названия комплексообразовате ля с добавлением суффикса ат
НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ НАЗВАНИЯ КОМПЛЕКСНЫХ АНИОНОВ: +3 Fe - феррат +2 Cu - купрат + Ag - аргентат +3 Au - аурат +2 Hg - меркурат +2 Zn - цинкат +3 Al - алюминат От латинского названия комплексообразовате ля с добавлением суффикса ат
![НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2[Zn+2 (OH)-4] тетра гидроксо натрия цинкат [Cr+3(H 2 O)06] Cl-3 хлорид НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2[Zn+2 (OH)-4] тетра гидроксо натрия цинкат [Cr+3(H 2 O)06] Cl-3 хлорид](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-19.jpg) НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2[Zn+2 (OH)-4] тетра гидроксо натрия цинкат [Cr+3(H 2 O)06] Cl-3 хлорид гексааква xрома (III) K+2 [Hg+2 I- 4] тетрайодомеркурат(II) калия
НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2[Zn+2 (OH)-4] тетра гидроксо натрия цинкат [Cr+3(H 2 O)06] Cl-3 хлорид гексааква xрома (III) K+2 [Hg+2 I- 4] тетрайодомеркурат(II) калия
![НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Na 3[Al. F 6] Гексафтороалюминат натрия Na[Al(OH)4] Тетрагидроксоалюминат натрия K 4[Fe(CN)6] НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Na 3[Al. F 6] Гексафтороалюминат натрия Na[Al(OH)4] Тетрагидроксоалюминат натрия K 4[Fe(CN)6]](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-20.jpg) НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Na 3[Al. F 6] Гексафтороалюминат натрия Na[Al(OH)4] Тетрагидроксоалюминат натрия K 4[Fe(CN)6] Гексационоферрат (II) калия
НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Na 3[Al. F 6] Гексафтороалюминат натрия Na[Al(OH)4] Тетрагидроксоалюминат натрия K 4[Fe(CN)6] Гексационоферрат (II) калия
![НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ [Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Ag(NH 3)2]Cl Хлорид диамминсеребра [Cr(H НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ [Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Ag(NH 3)2]Cl Хлорид диамминсеребра [Cr(H](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-21.jpg) НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ [Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Ag(NH 3)2]Cl Хлорид диамминсеребра [Cr(H 2 O)6]Cl 3 Хлорид гексааквахрома (III)
НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ [Cu(NH 3)4]SO 4 Сульфат тетраамминмеди (II) [Ag(NH 3)2]Cl Хлорид диамминсеребра [Cr(H 2 O)6]Cl 3 Хлорид гексааквахрома (III)
![СОСТАВЬТЕ ФОРМУЛЫ ВЕЩЕСТВ Гексахлороплатинат (IV) калия Ответ: K 2[Pt. Cl 6] Нитрат хлоронитротетраамминкобальта (III) СОСТАВЬТЕ ФОРМУЛЫ ВЕЩЕСТВ Гексахлороплатинат (IV) калия Ответ: K 2[Pt. Cl 6] Нитрат хлоронитротетраамминкобальта (III)](https://present5.com/presentation/3/273166396_343277026.pdf-img/273166396_343277026.pdf-22.jpg) СОСТАВЬТЕ ФОРМУЛЫ ВЕЩЕСТВ Гексахлороплатинат (IV) калия Ответ: K 2[Pt. Cl 6] Нитрат хлоронитротетраамминкобальта (III) Ответ: [Co(NH 3)4(NO 2)Cl]NO 3 Гексагидроксохромат (III) натрия Ответ: Na 3[Cr(OH)6] Нитрат гексаамминникеля (II) Ответ: [Ni(NH 3)6](NO 3)2
СОСТАВЬТЕ ФОРМУЛЫ ВЕЩЕСТВ Гексахлороплатинат (IV) калия Ответ: K 2[Pt. Cl 6] Нитрат хлоронитротетраамминкобальта (III) Ответ: [Co(NH 3)4(NO 2)Cl]NO 3 Гексагидроксохромат (III) натрия Ответ: Na 3[Cr(OH)6] Нитрат гексаамминникеля (II) Ответ: [Ni(NH 3)6](NO 3)2
 Лабораторная работа Получение и свойства комплексных соединений Оборудование и посуда: пробирки планшет Реактивы: HCl, Cu. SO 4, NH 4 OH, K 3[Fe(CN)6], Fe. SO 4, [Ag(NH 3)]NO 3, [Co(H 2 O)6]SO 4.
Лабораторная работа Получение и свойства комплексных соединений Оборудование и посуда: пробирки планшет Реактивы: HCl, Cu. SO 4, NH 4 OH, K 3[Fe(CN)6], Fe. SO 4, [Ag(NH 3)]NO 3, [Co(H 2 O)6]SO 4.
 Опыт № 1 ПОЛУЧЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Получение гидроксида тетраамминмеди (II) Cu. SO 4+ NH 4 OH → Cu(OH)2 + 4 NH 3 → Получение хлорида диамминсеребра (I) Ag. Cl+ NH 4 OH →
Опыт № 1 ПОЛУЧЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Получение гидроксида тетраамминмеди (II) Cu. SO 4+ NH 4 OH → Cu(OH)2 + 4 NH 3 → Получение хлорида диамминсеребра (I) Ag. Cl+ NH 4 OH →
 Подсказка Cu. SO 4+NH 4 OH → Cu(OH)2↓+(NH 4)2 SO 4 Cu(OH)2 + 4 NH 3 → [Cu(NH 3)4](OH)2
Подсказка Cu. SO 4+NH 4 OH → Cu(OH)2↓+(NH 4)2 SO 4 Cu(OH)2 + 4 NH 3 → [Cu(NH 3)4](OH)2
 Опыт № 2. ХИМИЧЕСКИЕ СВОЙСТВА n 1. Реакции по внешней сфере Fe. SO 4+K 3[Fe(CN)6]→ n 2. Реакции с участием лигандов [Cu(NH 3)4]SO 4+ 4 HCl→ n 3. Реакции по центральному иону [Ag(NH 3)2]NO 3 + HCl → n 4. Разрушение комплексов: [Co(H 2 O)6]SO 4· H 2 O→
Опыт № 2. ХИМИЧЕСКИЕ СВОЙСТВА n 1. Реакции по внешней сфере Fe. SO 4+K 3[Fe(CN)6]→ n 2. Реакции с участием лигандов [Cu(NH 3)4]SO 4+ 4 HCl→ n 3. Реакции по центральному иону [Ag(NH 3)2]NO 3 + HCl → n 4. Разрушение комплексов: [Co(H 2 O)6]SO 4· H 2 O→
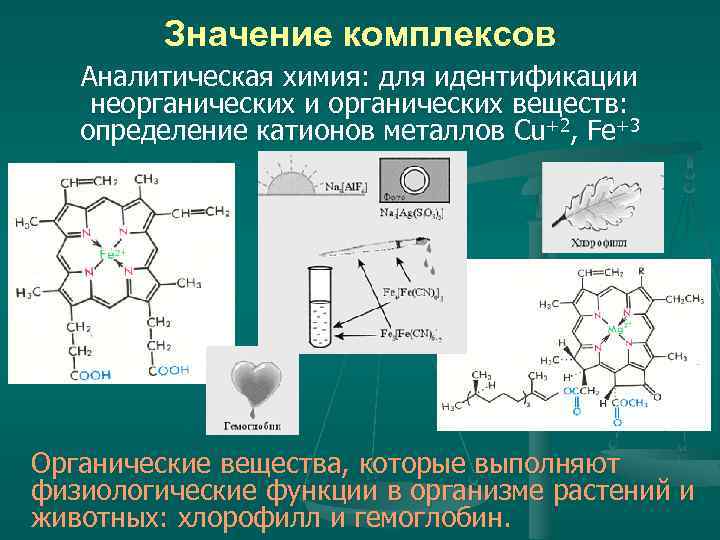 Значение комплексов Аналитическая химия: для идентификации неорганических и органических веществ: определение катионов металлов Cu+2, Fe+3 Органические вещества, которые выполняют физиологические функции в организме растений и животных: хлорофилл и гемоглобин.
Значение комплексов Аналитическая химия: для идентификации неорганических и органических веществ: определение катионов металлов Cu+2, Fe+3 Органические вещества, которые выполняют физиологические функции в организме растений и животных: хлорофилл и гемоглобин.
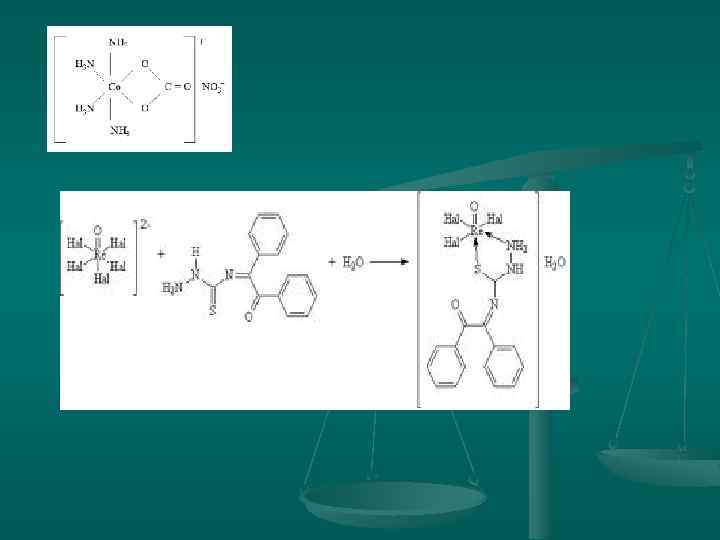
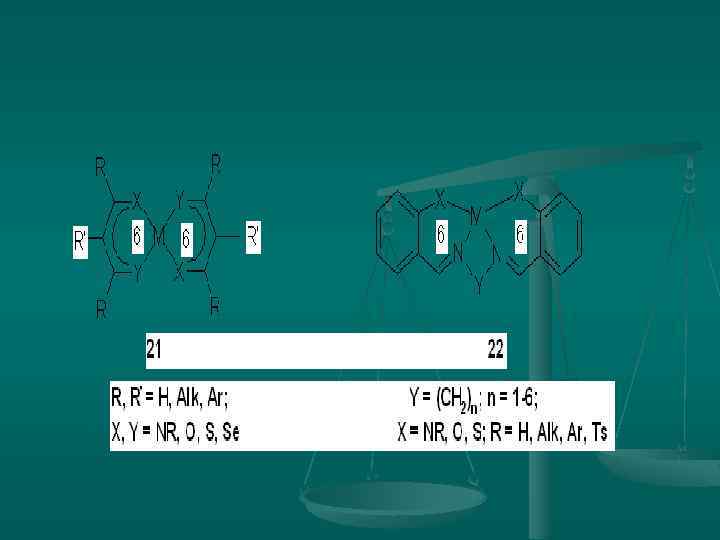
 n n Лиганды, занимающие во внутренней сфере одно место называются монодентантными, а а занимающие два, три и более местполидентантными. (привести примеры)
n n Лиганды, занимающие во внутренней сфере одно место называются монодентантными, а а занимающие два, три и более местполидентантными. (привести примеры)
 Спасибо за внимание! Данная презентация была создана с использованием ресурсов ИНТЕРНЕТ (презентация учителя химии СОШ № 9 г. Аши Челябинсткой области Сагадеевой Г. А. ).
Спасибо за внимание! Данная презентация была создана с использованием ресурсов ИНТЕРНЕТ (презентация учителя химии СОШ № 9 г. Аши Челябинсткой области Сагадеевой Г. А. ).


