получение комплексных соединений.ppt
- Количество слайдов: 21
 Комплексные соединения Методы получения и разрушения. Решение задач
Комплексные соединения Методы получения и разрушения. Решение задач
![Типы комплексных соединений. 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H Типы комплексных соединений. 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-2.jpg) Типы комплексных соединений. 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H 2 O)6]3+ • [Cr(H 2 O)6]3+ … Кристаллогидраты: • [Be(H 2 O)4]SO 4 • [Al(H 2 O)6]Cl 3 • [K(H 2 O)6][Cr(H 2 O)6](SO 4)2 • [Cu(H 2 O)4]SO 4·H 2 O • [Ni(H 2 O)6]SO 4·H 2 O M : OH 2
Типы комплексных соединений. 1. Аквакомплексы В водных растворах: • [Be(H 2 O)4]2+ • [Al(H 2 O)6]3+ • [Cr(H 2 O)6]3+ … Кристаллогидраты: • [Be(H 2 O)4]SO 4 • [Al(H 2 O)6]Cl 3 • [K(H 2 O)6][Cr(H 2 O)6](SO 4)2 • [Cu(H 2 O)4]SO 4·H 2 O • [Ni(H 2 O)6]SO 4·H 2 O M : OH 2
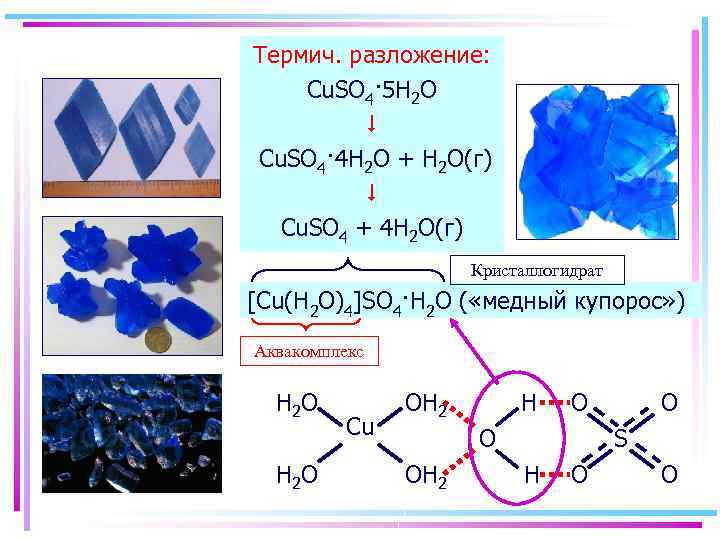 Аквакомплексы Термич. разложение: Cu. SO 4· 5 H 2 O Cu. SO 4· 4 H 2 O + H 2 O(г) Cu. SO 4 + 4 H 2 O(г) Кристаллогидрат [Cu(H 2 O)4]SO 4·H 2 O ( «медный купорос» ) Аквакомплекс H 2 O Cu OH 2 H O O OH 2 O S H O O
Аквакомплексы Термич. разложение: Cu. SO 4· 5 H 2 O Cu. SO 4· 4 H 2 O + H 2 O(г) Cu. SO 4 + 4 H 2 O(г) Кристаллогидрат [Cu(H 2 O)4]SO 4·H 2 O ( «медный купорос» ) Аквакомплекс H 2 O Cu OH 2 H O O OH 2 O S H O O
![Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-4.jpg) Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H 2 O Fe OH 2 H O O OH 2 O S H O O
Аквакомплексы Кристаллогидрат [Fe(H 2 O)6]SO 4·H 2 O ( «железный купорос» ) Аквакомплекс H 2 O Fe OH 2 H O O OH 2 O S H O O
![Гидроксокомплексы M : OH– Получение: • Zn(OH)2 + 2 OH–(изб. ) = [Zn(OH)4]2–; p. Гидроксокомплексы M : OH– Получение: • Zn(OH)2 + 2 OH–(изб. ) = [Zn(OH)4]2–; p.](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-5.jpg) Гидроксокомплексы M : OH– Получение: • Zn(OH)2 + 2 OH–(изб. ) = [Zn(OH)4]2–; p. H >> 7 Разрушение: • [Zn(OH)4]2– (+H 3 O+) • + CH 3 COOH; CO 2; NH 4+ (сл. к-ты, p. H 7) • Zn(OH)2(т) • + H 3 O+ (сильн. к-ты, p. H < 7) • [Zn(H 2 O)4]2+ • Образование гидроксокомплексов характерно для амфотерных элементов.
Гидроксокомплексы M : OH– Получение: • Zn(OH)2 + 2 OH–(изб. ) = [Zn(OH)4]2–; p. H >> 7 Разрушение: • [Zn(OH)4]2– (+H 3 O+) • + CH 3 COOH; CO 2; NH 4+ (сл. к-ты, p. H 7) • Zn(OH)2(т) • + H 3 O+ (сильн. к-ты, p. H < 7) • [Zn(H 2 O)4]2+ • Образование гидроксокомплексов характерно для амфотерных элементов.
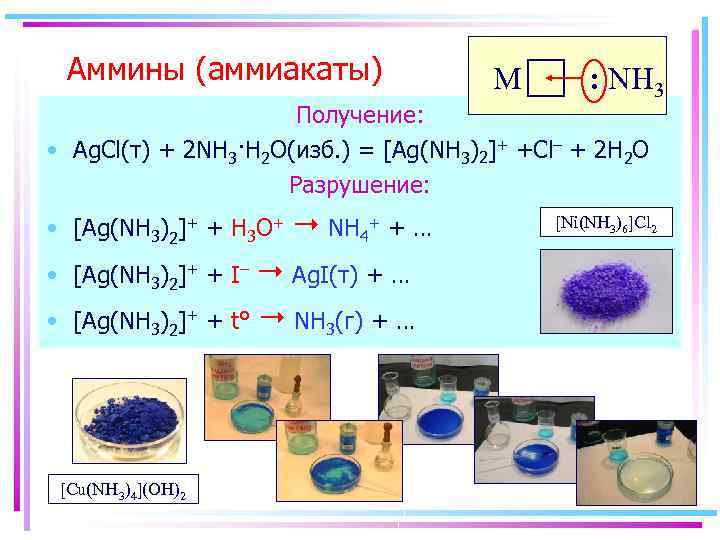 Аммины (аммиакаты) M : NH 3 Получение: • Ag. Cl(т) + 2 NH 3·H 2 O(изб. ) = [Ag(NH 3)2]+ +Cl– + 2 H 2 O Разрушение: • [Ag(NH 3)2]+ + H 3 O+ Ag. I(т) + … [Ag(NH 3)2]+ + t° NH 3(г) + … • [Ag(NH 3)2]+ + I– • NH 4+ + … [Cu(NH 3)4](OH)2 [Ni(NH 3)6]Cl 2
Аммины (аммиакаты) M : NH 3 Получение: • Ag. Cl(т) + 2 NH 3·H 2 O(изб. ) = [Ag(NH 3)2]+ +Cl– + 2 H 2 O Разрушение: • [Ag(NH 3)2]+ + H 3 O+ Ag. I(т) + … [Ag(NH 3)2]+ + t° NH 3(г) + … • [Ag(NH 3)2]+ + I– • NH 4+ + … [Cu(NH 3)4](OH)2 [Ni(NH 3)6]Cl 2
 Ацидокомплексы • • M : Х– Получение: Hg. I 2(т) + 2 I–(изб. ) = [Hg. I 4]2– [Fe(H 2 O)6]3+ + 6 NCS−=[Fe(NCS)6]3− + 6 H 2 O Разрушение: [Hg. I 4]2– + S 2– = Hg. S(т) + 4 I– [Fe(NCS)6]3− + 4 F− = [Fe. F 4]− + 6 NCS− Получение и разрушение тиоцианатного к-са Fe(III) K 3[Fe(CN)6] K 4[Fe(CN)6]
Ацидокомплексы • • M : Х– Получение: Hg. I 2(т) + 2 I–(изб. ) = [Hg. I 4]2– [Fe(H 2 O)6]3+ + 6 NCS−=[Fe(NCS)6]3− + 6 H 2 O Разрушение: [Hg. I 4]2– + S 2– = Hg. S(т) + 4 I– [Fe(NCS)6]3− + 4 F− = [Fe. F 4]− + 6 NCS− Получение и разрушение тиоцианатного к-са Fe(III) K 3[Fe(CN)6] K 4[Fe(CN)6]
 Гидридокомплексы • • • M : H– Получение: 4 Na. H + B(OCH 3)3 = Na[BH 4] + 3 CH 3 ONa (при 250 °C) 4 Li. H + Al. Cl 3 = Li[Al. H 4] + 3 Li. Cl 3 Li[BH 4] + Al. Cl 3 = Al[BH 4]3 + 3 Li. Cl Разрушение: Na[Al. H 4] + 4 H 2 O = Na. OH + Al(OH)3 + 4 H 2 (ОВР) 2 Na[BH 4] + H 2 SO 4 = Na 2 SO 4 + B 2 H 6 2 H 2 (ОВР) + Li[Al. H 4] Na[BH 4]
Гидридокомплексы • • • M : H– Получение: 4 Na. H + B(OCH 3)3 = Na[BH 4] + 3 CH 3 ONa (при 250 °C) 4 Li. H + Al. Cl 3 = Li[Al. H 4] + 3 Li. Cl 3 Li[BH 4] + Al. Cl 3 = Al[BH 4]3 + 3 Li. Cl Разрушение: Na[Al. H 4] + 4 H 2 O = Na. OH + Al(OH)3 + 4 H 2 (ОВР) 2 Na[BH 4] + H 2 SO 4 = Na 2 SO 4 + B 2 H 6 2 H 2 (ОВР) + Li[Al. H 4] Na[BH 4]
![Анионгалогенаты M[ЭГ¢m. Г²n] (Э, Г¢ и Г² – галогены) Получение: • KI + I Анионгалогенаты M[ЭГ¢m. Г²n] (Э, Г¢ и Г² – галогены) Получение: • KI + I](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-9.jpg) Анионгалогенаты M[ЭГ¢m. Г²n] (Э, Г¢ и Г² – галогены) Получение: • KI + I 2 = K[I(I)2]; Cs. Cl + IBr = Cs[I(Br)(Cl)] Разрушение: • K[I(I)2] + t° = KI + I 2(г) • Cs[I(Br)(Cl)] + t° = Cs. Cl + IBr(г) 7. Катионгалогены [ЭГ¢m. Г²n]Z (Э, Г¢ и Г² – галогены) Получение: • ICl 3 + Sb. Cl 5 = [ICl 2][Sb. Cl 6]; Br. F 3 + As. F 5 = [Br. F 2][As. F 6] Свойства: • Ag[Br. F 4](s) + [Br. F 2][Sb. F 6](s) = Ag[Sb. F 6](s) + 2 Br. F 3(ж) в среде Br. F 3(ж)
Анионгалогенаты M[ЭГ¢m. Г²n] (Э, Г¢ и Г² – галогены) Получение: • KI + I 2 = K[I(I)2]; Cs. Cl + IBr = Cs[I(Br)(Cl)] Разрушение: • K[I(I)2] + t° = KI + I 2(г) • Cs[I(Br)(Cl)] + t° = Cs. Cl + IBr(г) 7. Катионгалогены [ЭГ¢m. Г²n]Z (Э, Г¢ и Г² – галогены) Получение: • ICl 3 + Sb. Cl 5 = [ICl 2][Sb. Cl 6]; Br. F 3 + As. F 5 = [Br. F 2][As. F 6] Свойства: • Ag[Br. F 4](s) + [Br. F 2][Sb. F 6](s) = Ag[Sb. F 6](s) + 2 Br. F 3(ж) в среде Br. F 3(ж)
 (ниже 50 Карбонилы M : CO Получение: • Ni(т) + 4 CO(г) = [Ni(CO)4](ж) (ниже 50](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-10.jpg) Карбонилы M : CO Получение: • Ni(т) + 4 CO(г) = [Ni(CO)4](ж) (ниже 50 °С) тетракарбонилникель(0) Разрушение: • [Ni(CO)4](ж) + t° = Ni(т) + 4 CO(г) (выше 200 °С) • [Ni(CO)4] + H 2 SO 4(разб. ) = Ni. SO 4 + 4 CO + H 2 Высокочистое железо (карбонильный метод очистки) Состав карбонильных комплексов: [Cr(CO)6], [Mn 2(CO)10], [Fe(CO)5], [Co 2(CO)8] и др.
Карбонилы M : CO Получение: • Ni(т) + 4 CO(г) = [Ni(CO)4](ж) (ниже 50 °С) тетракарбонилникель(0) Разрушение: • [Ni(CO)4](ж) + t° = Ni(т) + 4 CO(г) (выше 200 °С) • [Ni(CO)4] + H 2 SO 4(разб. ) = Ni. SO 4 + 4 CO + H 2 Высокочистое железо (карбонильный метод очистки) Состав карбонильных комплексов: [Cr(CO)6], [Mn 2(CO)10], [Fe(CO)5], [Co 2(CO)8] и др.
 Правило Сиджвика для определения состава комплексов • Устойчивым является комплекс, в котором реализована 18 -эл-ная оболочка из s-, p- и d-электронов М и x эл. пар лигандов (L) • Н. -В. Сиджвик (1873 – 1952) 26 Fe 0 [Ar]3 d 64 s 2 || • 18 – 8 = 10 e 36 Kr – • или 36 – 26 = 10 e – • x = 10/2 = 5 эл. пар (5 молекул CO) • [Fe(CO)5] пентакарбонилжелезо
Правило Сиджвика для определения состава комплексов • Устойчивым является комплекс, в котором реализована 18 -эл-ная оболочка из s-, p- и d-электронов М и x эл. пар лигандов (L) • Н. -В. Сиджвик (1873 – 1952) 26 Fe 0 [Ar]3 d 64 s 2 || • 18 – 8 = 10 e 36 Kr – • или 36 – 26 = 10 e – • x = 10/2 = 5 эл. пар (5 молекул CO) • [Fe(CO)5] пентакарбонилжелезо
![Правило Сиджвика (примеры) * * * Co 0 [Ar]3 d 74 s 2 || Правило Сиджвика (примеры) * * * Co 0 [Ar]3 d 74 s 2 ||](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-12.jpg) Правило Сиджвика (примеры) * * * Co 0 [Ar]3 d 74 s 2 || 36 Kr 27 18 – 9 = 9 e –; х = 9/2 = 4, 5 (? ) радикал [·Co(CO)4] тетракарбонилкобальт (неуст. ) * димер [Co 2(CO)8] (уст. ) октакарбонилдикобальт • 23 V 0 [Ar]3 d 34 s 2 || 36 Kr • 18– 5 = 13 e –; • х = 13/2 = 6, 5 (? ) • радикал [·V(CO)6] (неуст. ) • или компл. соединение состава K[: V–I(CO)6] гексакарбонилванадат(-I) калия (уст. )
Правило Сиджвика (примеры) * * * Co 0 [Ar]3 d 74 s 2 || 36 Kr 27 18 – 9 = 9 e –; х = 9/2 = 4, 5 (? ) радикал [·Co(CO)4] тетракарбонилкобальт (неуст. ) * димер [Co 2(CO)8] (уст. ) октакарбонилдикобальт • 23 V 0 [Ar]3 d 34 s 2 || 36 Kr • 18– 5 = 13 e –; • х = 13/2 = 6, 5 (? ) • радикал [·V(CO)6] (неуст. ) • или компл. соединение состава K[: V–I(CO)6] гексакарбонилванадат(-I) калия (уст. )
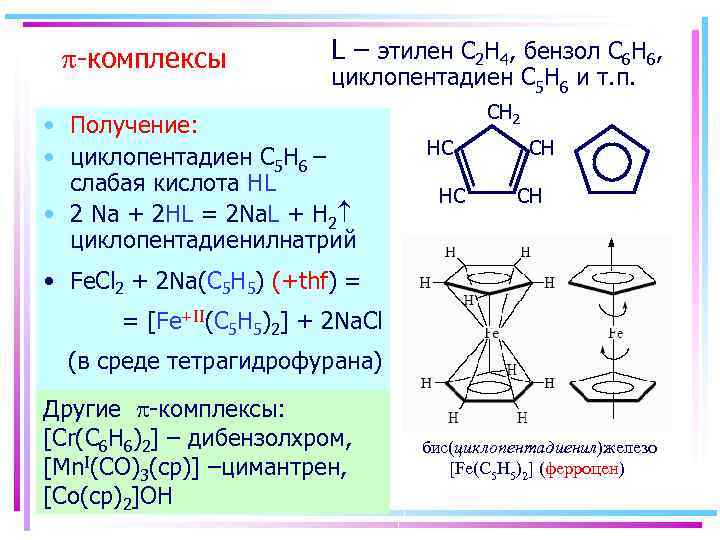 -комплексы L – этилен C 2 H 4, бензол C 6 H 6, циклопентадиен С 5 H 6 и т. п. • Получение: • циклопентадиен С 5 H 6 – слабая кислота HL • 2 Na + 2 HL = 2 Na. L + H 2 циклопентадиенилнатрий CH 2 HC HC CH CH • Fe. Cl 2 + 2 Na(C 5 H 5) (+thf) = = [Fe+II(C 5 H 5)2] + 2 Na. Cl (в среде тетрагидрофурана) Другие -комплексы: [Cr(C 6 H 6)2] – дибензолхром, [Mn. I(CO)3(cp)] –цимантрен, [Co(cp)2]OH бис(циклопентадиенил)железо [Fe(C 5 H 5)2] (ферроцен)
-комплексы L – этилен C 2 H 4, бензол C 6 H 6, циклопентадиен С 5 H 6 и т. п. • Получение: • циклопентадиен С 5 H 6 – слабая кислота HL • 2 Na + 2 HL = 2 Na. L + H 2 циклопентадиенилнатрий CH 2 HC HC CH CH • Fe. Cl 2 + 2 Na(C 5 H 5) (+thf) = = [Fe+II(C 5 H 5)2] + 2 Na. Cl (в среде тетрагидрофурана) Другие -комплексы: [Cr(C 6 H 6)2] – дибензолхром, [Mn. I(CO)3(cp)] –цимантрен, [Co(cp)2]OH бис(циклопентадиенил)железо [Fe(C 5 H 5)2] (ферроцен)
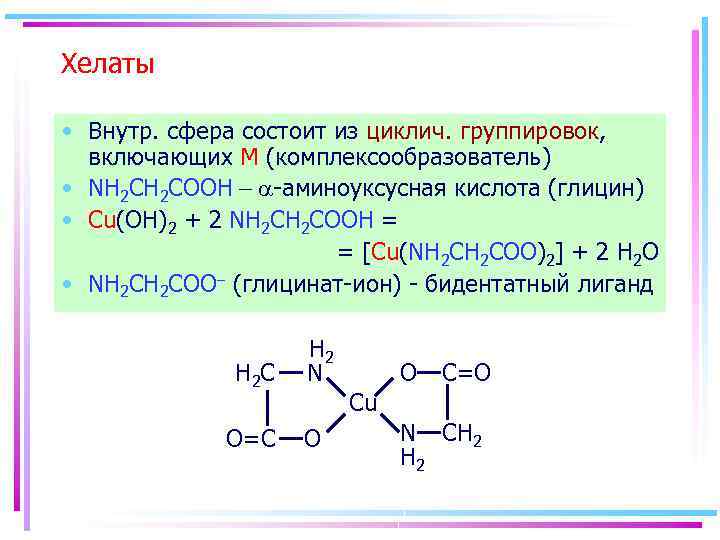 Хелаты • Внутр. сфера состоит из циклич. группировок, включающих M (комплексообразователь) • NH 2 COOH - a-аминоуксусная кислота (глицин) • Cu(OH)2 + 2 NH 2 COOH = = [Cu(NH 2 COO)2] + 2 H 2 O • NH 2 COO- (глицинат-ион) - бидентатный лиганд H 2 C O=C H 2 N O C=O Cu O N CH 2
Хелаты • Внутр. сфера состоит из циклич. группировок, включающих M (комплексообразователь) • NH 2 COOH - a-аминоуксусная кислота (глицин) • Cu(OH)2 + 2 NH 2 COOH = = [Cu(NH 2 COO)2] + 2 H 2 O • NH 2 COO- (глицинат-ион) - бидентатный лиганд H 2 C O=C H 2 N O C=O Cu O N CH 2
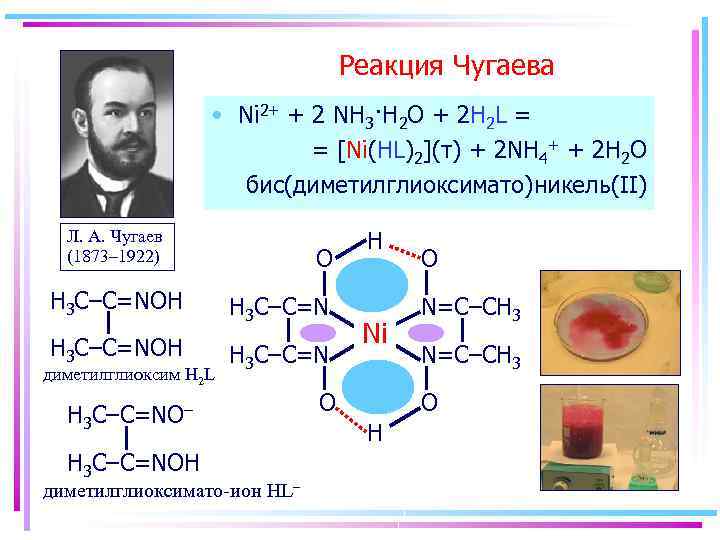 Реакция Чугаева • Ni 2+ + 2 NH 3·H 2 O + 2 H 2 L = = [Ni(HL)2](т) + 2 NH 4+ + 2 H 2 O бис(диметилглиоксимато)никель(II) Л. А. Чугаев (1873– 1922) O H 3 C–C=NOH H 3 C–C=N диметилглиоксим H 2 L H 3 C–C=NO– H 3 C–C=NOH диметилглиоксимато-ион HL– H Ni O O N=C–CH 3 O H
Реакция Чугаева • Ni 2+ + 2 NH 3·H 2 O + 2 H 2 L = = [Ni(HL)2](т) + 2 NH 4+ + 2 H 2 O бис(диметилглиоксимато)никель(II) Л. А. Чугаев (1873– 1922) O H 3 C–C=NOH H 3 C–C=N диметилглиоксим H 2 L H 3 C–C=NO– H 3 C–C=NOH диметилглиоксимато-ион HL– H Ni O O N=C–CH 3 O H
 Методы синтеза комплексных соединений • Реакция обмена лигандов А) в водном растворе ( обр, принцип Ле Шателье): • [Сu(H 2 O)4]2+ + 4 NH 3·H 2 O = [Cu(NH 3)4]2+ + 8 H 2 O (обр. прод. ) > (обр. исх. реаг. ) Б) в неводном растворителе: • [Al(H 2 O)6]3+ + NH 3·H 2 O • [Al(H 2 O)6]3+(s) + 6 NH 3(ж) = [Al(NH 3)6]3+(s) + 6 H 2 O(s) В) без растворителя: • [Ni(H 2 O)6]Cl 2(т) + 6 NH 3(г) = [Ni(NH 3)6]Cl 2(т) +6 H 2 O(г) Г) внутримол. обмен лигандов в тв. фазе: • 2[Co(H 2 O)6]Cl 2(т) + t° = Co[Co. Cl 4](т) + 12 H 2 O розовый синий
Методы синтеза комплексных соединений • Реакция обмена лигандов А) в водном растворе ( обр, принцип Ле Шателье): • [Сu(H 2 O)4]2+ + 4 NH 3·H 2 O = [Cu(NH 3)4]2+ + 8 H 2 O (обр. прод. ) > (обр. исх. реаг. ) Б) в неводном растворителе: • [Al(H 2 O)6]3+ + NH 3·H 2 O • [Al(H 2 O)6]3+(s) + 6 NH 3(ж) = [Al(NH 3)6]3+(s) + 6 H 2 O(s) В) без растворителя: • [Ni(H 2 O)6]Cl 2(т) + 6 NH 3(г) = [Ni(NH 3)6]Cl 2(т) +6 H 2 O(г) Г) внутримол. обмен лигандов в тв. фазе: • 2[Co(H 2 O)6]Cl 2(т) + t° = Co[Co. Cl 4](т) + 12 H 2 O розовый синий
 Методы синтеза комплексных соединений Д) ОВР + реакции обмена лигандов +Ок. + L • [Сo. II(H 2 O)6]2+ [Сo. IIIL 6]3+ • Ок. : H 2 O 2, KNO 2 … L – NH 3, NO 2– … • Примеры: • 2 Co. IICl 2 + 12 NH 3 + H 2 O 2 = 2[Co. III(NH 3)6](OH)Cl 2 • Co. IICl 2 + 7 KNO 2 + 2 CH 3 COOH = = K 3[Co. III(NO 2)6] + NO + 2 KCl + 2 CH 3 COOK + H 2 O + Вс • [Ni. II(CN)4]2– [Ni 0(CN)4]4–
Методы синтеза комплексных соединений Д) ОВР + реакции обмена лигандов +Ок. + L • [Сo. II(H 2 O)6]2+ [Сo. IIIL 6]3+ • Ок. : H 2 O 2, KNO 2 … L – NH 3, NO 2– … • Примеры: • 2 Co. IICl 2 + 12 NH 3 + H 2 O 2 = 2[Co. III(NH 3)6](OH)Cl 2 • Co. IICl 2 + 7 KNO 2 + 2 CH 3 COOH = = K 3[Co. III(NO 2)6] + NO + 2 KCl + 2 CH 3 COOK + H 2 O + Вс • [Ni. II(CN)4]2– [Ni 0(CN)4]4–
 Решение задач. 1. Растворение осадка при комплексообразовании • Ag. Br(т) Ag+ + Br – ; ПРAg. Br = 7, 7· 10– 13 • Ag+ + 2 SO 3 S 2– [Ag(SO 3 S)2]3– ; обр = 4· 1013 • Ag. Br(т) + 2 SO 3 S 2– [Ag(SO 3 S)2]3– + Br –; • Kc = ? Kc = [Ag(SO 3 S)23–][Br –] [Ag+] [SO 3 S 2–]2 [Ag+] = ПРAg. Br обр Kc = ПРAg. Br обр = 7, 7· 10– 13 4· 1013 = 30, 8 >> 1 Наблюдается растворение осадка (смещение равновесия вправо )
Решение задач. 1. Растворение осадка при комплексообразовании • Ag. Br(т) Ag+ + Br – ; ПРAg. Br = 7, 7· 10– 13 • Ag+ + 2 SO 3 S 2– [Ag(SO 3 S)2]3– ; обр = 4· 1013 • Ag. Br(т) + 2 SO 3 S 2– [Ag(SO 3 S)2]3– + Br –; • Kc = ? Kc = [Ag(SO 3 S)23–][Br –] [Ag+] [SO 3 S 2–]2 [Ag+] = ПРAg. Br обр Kc = ПРAg. Br обр = 7, 7· 10– 13 4· 1013 = 30, 8 >> 1 Наблюдается растворение осадка (смещение равновесия вправо )
![Решение задач. 2. Реакция обмена лигандов • [Co(NH 3)6]3+ + 6 CN– [Co(CN)6]3– + Решение задач. 2. Реакция обмена лигандов • [Co(NH 3)6]3+ + 6 CN– [Co(CN)6]3– +](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-19.jpg) Решение задач. 2. Реакция обмена лигандов • [Co(NH 3)6]3+ + 6 CN– [Co(CN)6]3– + 6 NH 3 ; • Kc = ? • Co 3+ + 6 NH 3 [Co(NH 3)6]3+ ; обр(1) = 1, 6· 1035 • Co 3+ + 6 CN– [Co(CN)6]3– ; обр(2) = 1, 0· 1064 Kc = [Co(CN)63–] [NH 3]6 [Co 3+] [Co(NH 3)6 3+] [CN–]6 [Co 3+] = обр(2) обр(1) Kc = обр(2) / обр(1) = (1, 0· 1064)/(1, 6· 1035) = 6, 2· 1029 >> 1 Наблюдается смещение равновесия вправо
Решение задач. 2. Реакция обмена лигандов • [Co(NH 3)6]3+ + 6 CN– [Co(CN)6]3– + 6 NH 3 ; • Kc = ? • Co 3+ + 6 NH 3 [Co(NH 3)6]3+ ; обр(1) = 1, 6· 1035 • Co 3+ + 6 CN– [Co(CN)6]3– ; обр(2) = 1, 0· 1064 Kc = [Co(CN)63–] [NH 3]6 [Co 3+] [Co(NH 3)6 3+] [CN–]6 [Co 3+] = обр(2) обр(1) Kc = обр(2) / обр(1) = (1, 0· 1064)/(1, 6· 1035) = 6, 2· 1029 >> 1 Наблюдается смещение равновесия вправо
![Решение задач. 3. Разрушение комплекса • [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H Решение задач. 3. Разрушение комплекса • [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H](https://present5.com/presentation/3/121486170_172709327.pdf-img/121486170_172709327.pdf-20.jpg) Решение задач. 3. Разрушение комплекса • [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H 2 O)4]2+ + 4 NH 4+ ; • Kc = ? • Cu 2+ + 4 NH 3 [Cu(NH 3)4]2+ ; обр = 7, 9· 1012 • NH 4+ + 2 H 2 O NH 3·H 2 O + H 3 O+ ; Kк = 5, 75· 10– 10 Kc = [Cu 2+] [NH 4+]4 [NH 3]4 [Cu(NH 3)4 2+] [H 3 O +] 4 [NH 3 ]4 = 1 обр Kк 4 Kc = 1 / (7, 9· 1012· 5, 754· 10– 40 ) = 1, 16· 1020 >> 1 Наблюдается разрушение аммиачного комплекса в кислотной среде (смещение равновесия вправо )
Решение задач. 3. Разрушение комплекса • [Cu(NH 3)4]2+ + 4 H 3 O+ [Cu(H 2 O)4]2+ + 4 NH 4+ ; • Kc = ? • Cu 2+ + 4 NH 3 [Cu(NH 3)4]2+ ; обр = 7, 9· 1012 • NH 4+ + 2 H 2 O NH 3·H 2 O + H 3 O+ ; Kк = 5, 75· 10– 10 Kc = [Cu 2+] [NH 4+]4 [NH 3]4 [Cu(NH 3)4 2+] [H 3 O +] 4 [NH 3 ]4 = 1 обр Kк 4 Kc = 1 / (7, 9· 1012· 5, 754· 10– 40 ) = 1, 16· 1020 >> 1 Наблюдается разрушение аммиачного комплекса в кислотной среде (смещение равновесия вправо )
 Решение задач. 4. Направление реакции • Cu. CN(т) + H 2 O + HCN [Cu(CN)2]– + H 3 O+ • Kc = ? • Cu+ + 2 CN– [Cu(CN)2]– ; обр = 1, 0· 1024 • HCN + H 2 O CN– + H 3 O+ ; Kк = = 4, 93· 10– 10 • Cu. CN(т) Cu+ + CN– ; ПРCu. CN = 3, 2· 10– 20 Kc = [Cu(CN)2–][H 3 O+] [CN–][Cu+][CN–] [HCN] [CN–]2 [Cu+] = обр·Kк·ПРCu. CN Kc = 1, 0· 1024 · 4, 93· 10– 10 · 3, 2· 10– 20 = 1, 6· 10– 6 << 1 Растворение осадка не наблюдается (равновесие смещено влево )
Решение задач. 4. Направление реакции • Cu. CN(т) + H 2 O + HCN [Cu(CN)2]– + H 3 O+ • Kc = ? • Cu+ + 2 CN– [Cu(CN)2]– ; обр = 1, 0· 1024 • HCN + H 2 O CN– + H 3 O+ ; Kк = = 4, 93· 10– 10 • Cu. CN(т) Cu+ + CN– ; ПРCu. CN = 3, 2· 10– 20 Kc = [Cu(CN)2–][H 3 O+] [CN–][Cu+][CN–] [HCN] [CN–]2 [Cu+] = обр·Kк·ПРCu. CN Kc = 1, 0· 1024 · 4, 93· 10– 10 · 3, 2· 10– 20 = 1, 6· 10– 6 << 1 Растворение осадка не наблюдается (равновесие смещено влево )


