Комплексные соединения.ppt
- Количество слайдов: 23

Комплексные соединения Лектор: ассистент каф. общей и биоорганической химии Литов Константин Михайлович

Г. Томас Л. А. Чугаев К. Гофман А. Вернер К. Б. Яцимирский И. И. Черняев

Тассер – французский химик, получивший в лаборатории комплексное соединение üCu. SO 4. 4 NH 3 – Андрей Либавий, 1597 г. üAg. Cl. 2 NH 3 – И. Глаубер, 1648 г. üCo. Cl 3. 6 NH 3 – Тассер, 1798 г. [Co(NH 3)6]Cl 3 ü 1704 г. Дисбах – получил берлинскую лазурь KCN. Fe(CN)2. Fe(CN)3 ü 1749 -1753 гг. Пьер Жозеф Макер получил красную кровяную соль.
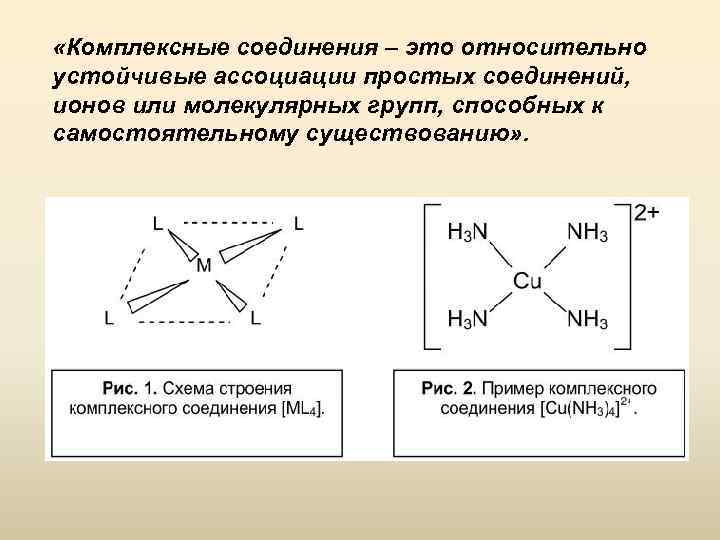
«Комплексные соединения – это относительно устойчивые ассоциации простых соединений, ионов или молекулярных групп, способных к самостоятельному существованию» .

Суммарный заряд комплексообразователя и лигандов формирует заряд внутренней сферы и, следовательно, внутренняя сфера может иметь положительный ([МLn]ν+) или отрицательный заряд ([МLn]ν-), а может быть нейтральной ([МLn]0) и тогда внешней сферы нет совсем. Варианты строения комплексных соединений: 1) [МLn] ν+X νПримеры: [Ni(NH 3)4]2+Cl 2 -, [Al(H 2 O)6]3+Cl 3 -. 2) X ν+ [МLn] νПримеры: K 4+[Fe(CN)6]4 -, K 2+[Hg(SO 3)2]2 -. 3) [МLn]0 Примеры: [Sn(H 2 O)Cl 2]0. [Os(CO)5]0, 4) [МLn] ν+ [МLn] νПримеры: [PCl 4]+[Au. Cl 4]-, [Pt(NH 3)4]2+[Cu. Cl 4]2 -.
![монодентатность [Be(OH)4]2 - [Pt. Br 4]2 - [Zn(NH 3)2 Cl 2] [Pt(NH 3)2(N 2 монодентатность [Be(OH)4]2 - [Pt. Br 4]2 - [Zn(NH 3)2 Cl 2] [Pt(NH 3)2(N 2](https://present5.com/presentation/3/139798218_182267296.pdf-img/139798218_182267296.pdf-6.jpg)
монодентатность [Be(OH)4]2 - [Pt. Br 4]2 - [Zn(NH 3)2 Cl 2] [Pt(NH 3)2(N 2 H 4)2]2+ бидентатность [Zn(NH 2 CH 2 NH 2)2]2+ [Cu(NH 2 COO)2] [Co(NH 2 CH 2 NH 2)2 Cl 2]+
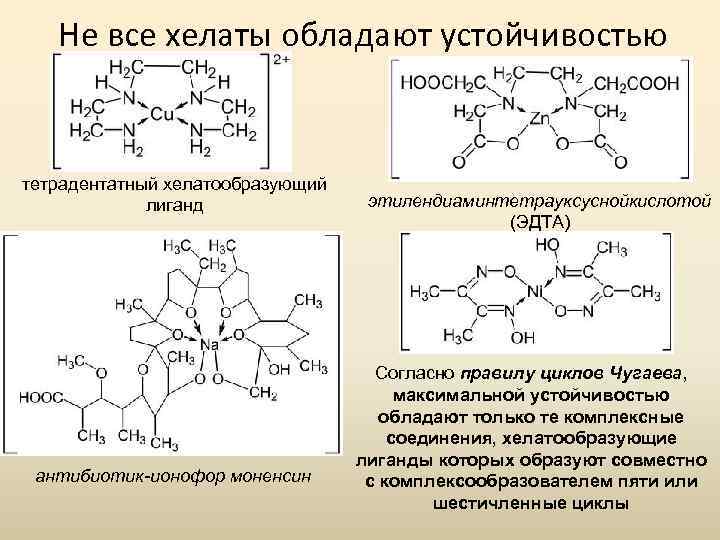
Не все хелаты обладают устойчивостью тетрадентатный хелатообразующий лиганд антибиотик-ионофор моненсин этилендиаминтетрауксуснойкислотой (ЭДТА) Согласно правилу циклов Чугаева, максимальной устойчивостью обладают только те комплексные соединения, хелатообразующие лиганды которых образуют совместно с комплексообразователем пяти или шестичленные циклы
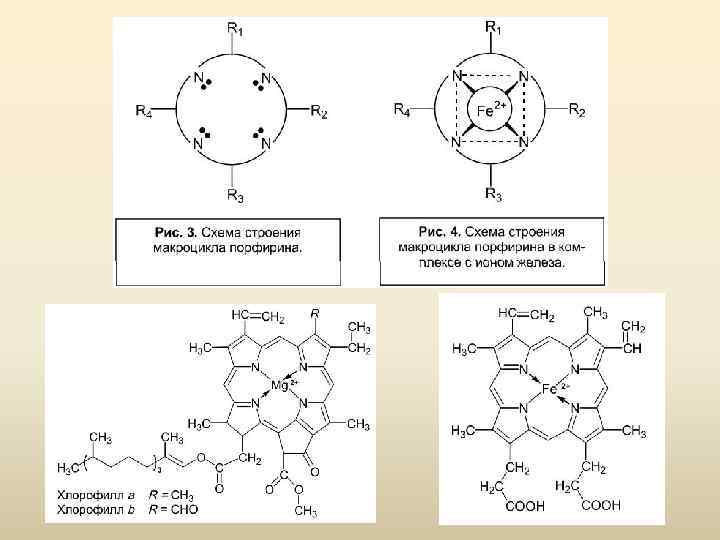

Важной характеристикой комплексообразователя в комплексных соединениях является координационное число. Различают характеристическое и максимальное координационные числа комплексообразователя. Характеристическим координационным числом комплексообразователя называют общее число σ-связей, образующихся между комплексообразователем и лигандами в конкретном комплексном соединении. Характеристическое координационное число (КЧ) зависит от природы лигандов. Максимальное координационное число (МКЧ) определяет максимально возможное число связей, которое может предоставить комплексообразователь. Максимальное координационное число не зависит от природы лигандов, оно полностью определяется электронным строением самого комплексообразователя. Примеры: [Co(H 2 O)(NH 3)4 Cl]Cl 2, [Pt(NH 3)5(OH)]Br 3, K[Ag(CN)2], КЧ=6; КЧ=2;

Номенклатура комплексных соединений Числовые приставки Умножающие приставки 1 – моно 4 – тетра 7 – гепта 10 – дека 2 – ди 5 – пента 8 – окта 11 – ундека 3 – три 6 – гекса 9 – нона 12 – додека 2 – бис 4 – тетракис 3 – трис 5 – пентакис Анионные лиганды Нейтральные лиганды Н 2 О – аква CO – карбонил NH 3 – аммин NO – нитрозил F– – фторо, Сl– – хлоро, O 2– – оксо, S 2– – тио, N 3– – азидо, NO 2– – нитро, OH– – гидроксо, СN– – циано, NCS– – тиоцианато, CO 32– – карбонато, C 2 O 42– – оксалато, SO 32– – сульфито, SO 3 S 2– – тиосульфато, C 5 H 5– – циклопентадиенил. Катионные лиганды Ag – аргенат As – арс, арсен Au – аур С – карб, карбон Cu – купр Fe – ферр Hg – меркур Mn – манган N – нитр Ni – никкол Pb – плюмб S – сульф Sb – стиб Si – сил, силик Sn – станн

ХАРАКТЕРИСТИКА ХИМИЧЕСКИХ СВЯЗЕЙ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ Частицы внешней сферы удерживаются за счет сил электростатического ион-ионного взаимодействия С точки зрения метода валентных связей между комплексообразователем и лигандом возникает ковалентная двухцентровая двухэлектронная связь по донорноакцепторному механизму Влияние типа гибридизации валентных орбиталей на геометрию комплексных соединений Тип комплекса ML 2 ML 3 ML 4 ML 5 ML 6 Тип гибридизации sp sp 2 sp 3, sd 3 dsp 2 spd 3, sp 3 d sp 2 d 2 sp 3 d 2 Конфигурация Линейная Треугольная Тетраэдрическая Плоскоквадратная Тригональнобипирамидальная Тетрагональнопирамидальная Октаэдрическая
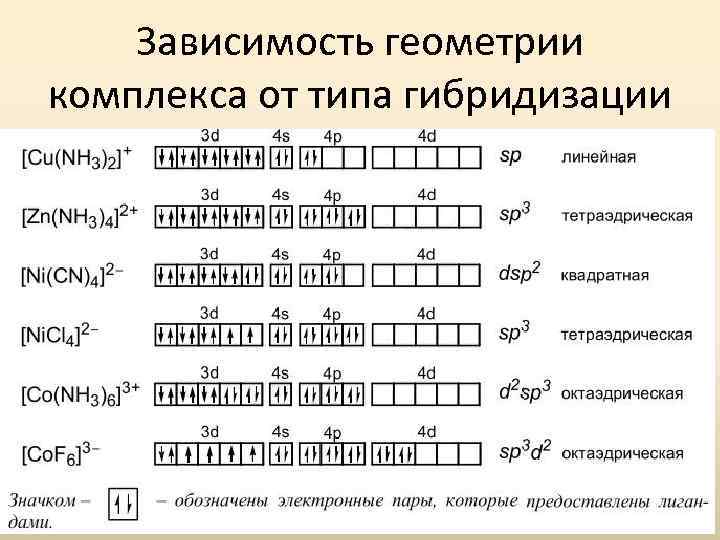
Зависимость геометрии комплекса от типа гибридизации
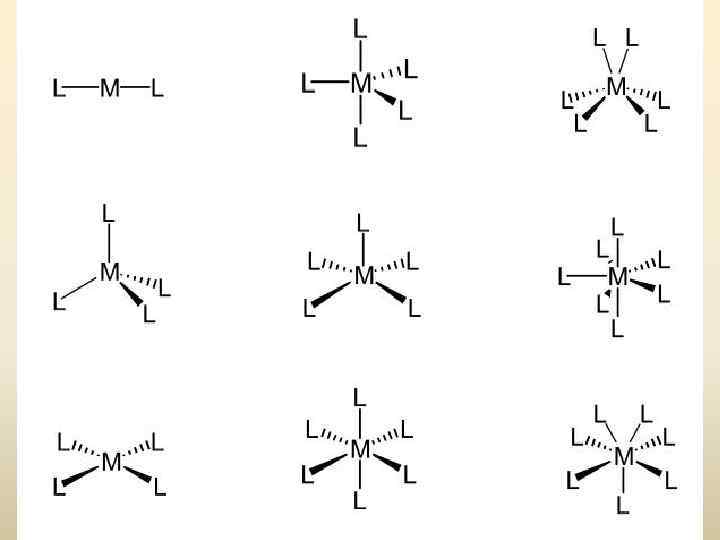
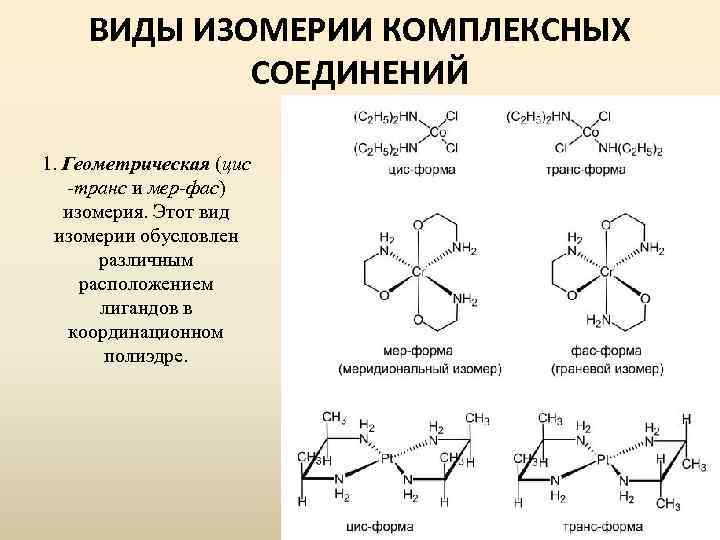
ВИДЫ ИЗОМЕРИИ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ 1. Геометрическая (цис -транс и мер-фас) изомерия. Этот вид изомерии обусловлен различным расположением лигандов в координационном полиэдре.
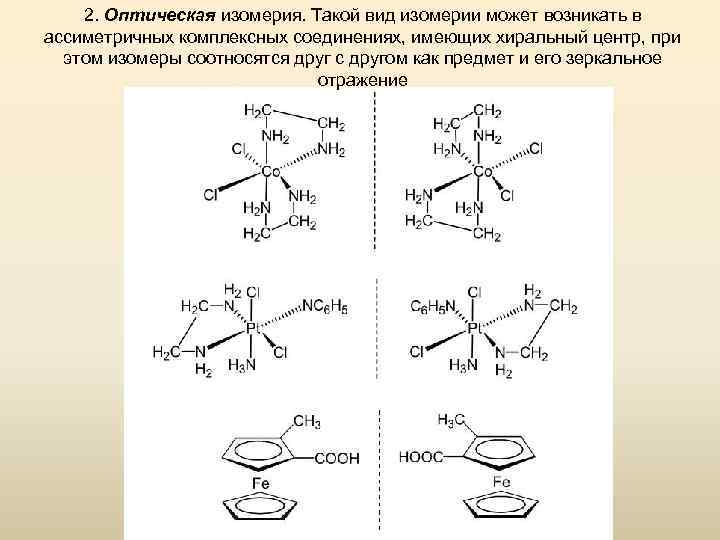
2. Оптическая изомерия. Такой вид изомерии может возникать в ассиметричных комплексных соединениях, имеющих хиральный центр, при этом изомеры соотносятся друг с другом как предмет и его зеркальное отражение

3. Сольватная изомерия связана с перераспределением молекул растворителя между внешней и внутренней сферами. Если в качестве растворителя выступает вода, то такой вид сольватной изомерии называют гидратной. Примеры: [Cr(H 2 O)6]Cl 3 [Cr(H 2 O)5 Cl]Cl 2·H 2 O, [Co(en)2(H 2 O)Cl]Cl 2 [Co(en)2 Cl 2]Cl·H 2 O, [Cr(py)2(H 2 O)2 Cl 2]Cl [Cr(py)2(H 2 O)Cl 3]·H 2 O. 4. Ионизационная изомерия встречается только в комплексах катионного типа и обусловлена различным распределением частиц внешней сферы и лигандов. Примеры: [Pt(NH 3)4 Cl 2]Br 2 [Pt(NH 3)4 Br 2]Cl 2, [Pt(NH 3)4 Br]NO 2 [Pt(NH 3)4(NO 2)]Br 2, [Co(en)2(NCS)2]Cl [Co(en)2 Cl(NCS)]NCS. 5. Связевая (солевая) изомерия. Подобная изомерия возможна для комплексных соединений, имеющих в своем составе амбидентатные лиганды. Связевая изомерия объясняется возможностью амбидентатных лигандов координироваться с комплексообразователем разными способами. Примеры: K 3[Co(-ONO)6] К 3[Co(-NO 2)6], [Pt(NH 3)2(-NCS)2] [Pt(NH 3)2(-SCN)2], Na 3[Ir(H 2 O)3(-SO 3)3] Na 3[Ir(H 2 O)3(-OSO 2)3].

6. Координационная изомерия возникает в комплексных соединениях, которые состоят из комплексного катиона и комплексного аниона, имеющих разные комплексообразователи. Обусловлен такой вид изомерии различным распределением лигандов между комплексообразователями катионного и анионного комплексов. Примеры: [Pt(NH 3)4][Pd. IICl 4] [Pd(NH 3)4][Pt. IICl 4], [Co(en)2(ox)][Cr. III(en)(ox)2] [Cr(en)2(ox)][Co. III(en)(ox)2], [Rh(en)3][Ir. IIICl 6] [Rh(en)2 Cl 2][Ir. III(en)Cl 4]. 7. Координационная полимерия. Связана с возможностью образования поликомплексных соединений, которые имеют одинаковый состав, но разное химическое строение. Примеры: [Pt(NH 3)4][Pt. IVCl 4(OH)2] [Pt(NH 3)4(OH)2][Pt. IICl 4], [Pt(NH 3)4][Pt. II(NH 3)Cl 3]2 [Pt(NH 3)3 Cl]2[Pt. IICl 4], [Cr(H 2 O)4 F 2][Cr. III(H 2 O)2 F 4] [Cr(H 2 O)6][Cr. IIIF 6]. 8. Трансформационная изомерия. Такой вид изомерии связан с возможностью химического превращения лигандов. Причем для подобных изомеров различается и способ координации лигандов (σ – π). Примеры: [Pt. H(C 2 H 4)(P(Ph)3)2 Cl. O 4] [Pt(C 2 H 5)(P(Ph)3)2 Cl. O 4], [Pt. Cl(CCl=CCl 2)(P(Ph)3)2] [Pt(CCl 2=CCl 2)(P(Ph)3)2], [Pt. Br(CF=CF 2)(As(Ph)3)2] [Pt (CFBr=CF 2)(As(Ph)3)2].

9. Конформационная изомерия обусловлена свободным вращением, которое допускает одинарная σ-связь, при этом за счет теплового вращения молекула может менять свою форму. Пример: 10. Формальная изомерия обусловлена существованием комплексных соединений с одинаковым составом, но генетически не связанных друг с другом и не способных переходить одно в другое. Пример: [Pt(NH 3)(NH 2 C 2 H 5)Cl 2] [Pt(NH 2 CH 3)2 Cl 2]
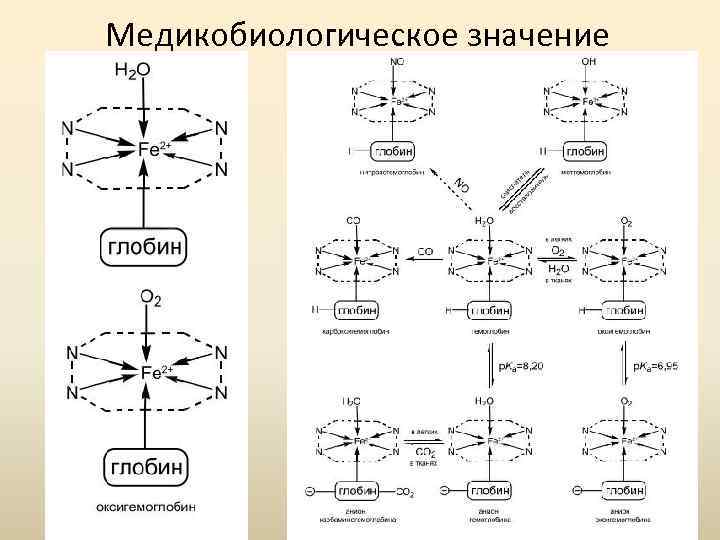
Медикобиологическое значение
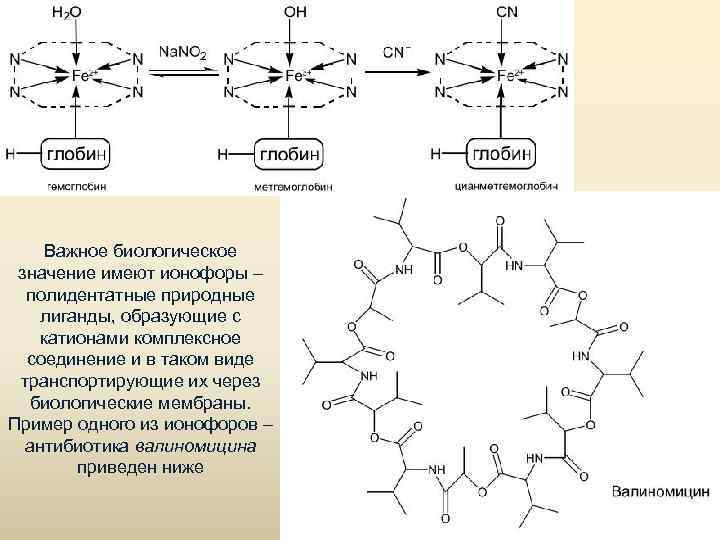
Важное биологическое значение имеют ионофоры – полидентатные природные лиганды, образующие с катионами комплексное соединение и в таком виде транспортирующие их через биологические мембраны. Пример одного из ионофоров – антибиотика валиномицина приведен ниже
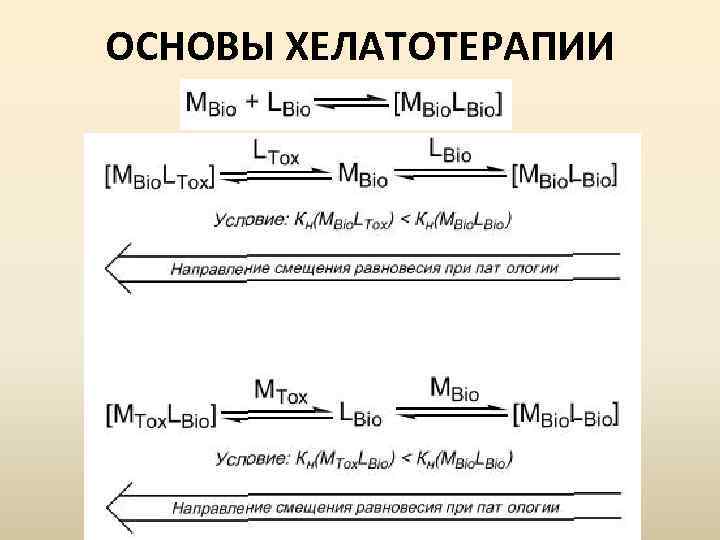
ОСНОВЫ ХЕЛАТОТЕРАПИИ

При отборе лигандов, которые планируется использовать для хелатотерапии, руководствуются четырьмя основными принципами: 1) лиганд-препарат не должен быть токсичным для организма; 2) лиганд-препарат не должен разрушаться или модифицироваться в биологической среде; 3) лиганд-препарат должен обладать высоким сродством к токсическим комплексообразователям; 4) лиганд-препарат должен обладать низким сродством к биокомплексообразователям. В качестве лигандовпрепаратов для хелатотерапии эффективно используются следующие препараты: трилон Б, тетацин, пентацин, дефероксамин, пеницилламин, британский антилюизит (БАЛ), унитиол, криптанид, алюминон и ряд других

Спасибо за внимание!
Комплексные соединения.ppt