Комплексные соединения.ppt
- Количество слайдов: 14
 Комплексные соединения L L А L L
Комплексные соединения L L А L L
 Комплексные соединения Взаимодействие между молекулами часто приводит к образованию более сложных молекул. Любое вещество в какой-либо мере растворимо в другом веществе. Происходит координация взаимодействующих частиц (при этом может протекать комплексообразование). Основополагающие представления о комплексных соединениях ввел в науку швейцарский ученый Альфред Вернер в 1892 г. разработав координационную теорию. А. Вернер (1866 – 1919 гг. ) В 1913 г. А. Вернеру была присуждена Нобелевская премия по химии за выдающиеся исследования в области координационной химии. В дальнейшем в развитии комплексных соединений большую роль сыграли труды Л. А. Чугаева и его учеников. Чугаев Л. А. (1873 – 1922 гг. )
Комплексные соединения Взаимодействие между молекулами часто приводит к образованию более сложных молекул. Любое вещество в какой-либо мере растворимо в другом веществе. Происходит координация взаимодействующих частиц (при этом может протекать комплексообразование). Основополагающие представления о комплексных соединениях ввел в науку швейцарский ученый Альфред Вернер в 1892 г. разработав координационную теорию. А. Вернер (1866 – 1919 гг. ) В 1913 г. А. Вернеру была присуждена Нобелевская премия по химии за выдающиеся исследования в области координационной химии. В дальнейшем в развитии комплексных соединений большую роль сыграли труды Л. А. Чугаева и его учеников. Чугаев Л. А. (1873 – 1922 гг. )
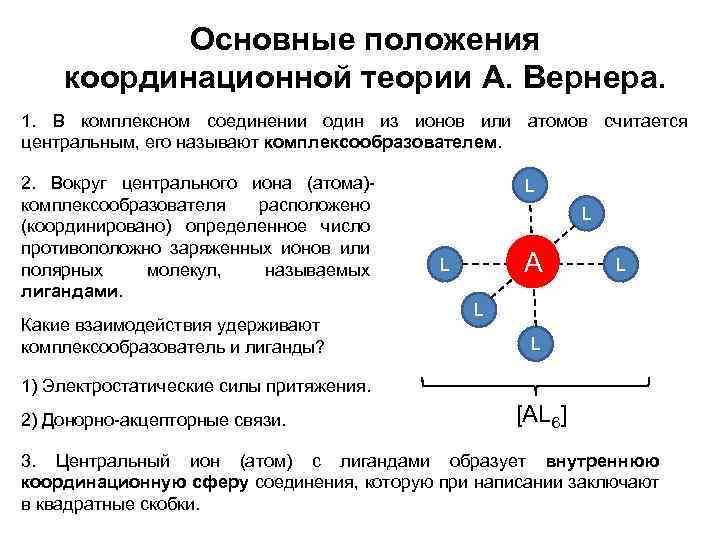 Основные положения координационной теории А. Вернера. 1. В комплексном соединении один из ионов или атомов считается центральным, его называют комплексообразователем. 2. Вокруг центрального иона (атома)комплексообразователя расположено (координировано) определенное число противоположно заряженных ионов или полярных молекул, называемых лигандами. Какие взаимодействия удерживают комплексообразователь и лиганды? L L А L L 1) Электростатические силы притяжения. 2) Донорно-акцепторные связи. [AL 6] 3. Центральный ион (атом) с лигандами образует внутреннюю координационную сферу соединения, которую при написании заключают в квадратные скобки.
Основные положения координационной теории А. Вернера. 1. В комплексном соединении один из ионов или атомов считается центральным, его называют комплексообразователем. 2. Вокруг центрального иона (атома)комплексообразователя расположено (координировано) определенное число противоположно заряженных ионов или полярных молекул, называемых лигандами. Какие взаимодействия удерживают комплексообразователь и лиганды? L L А L L 1) Электростатические силы притяжения. 2) Донорно-акцепторные связи. [AL 6] 3. Центральный ион (атом) с лигандами образует внутреннюю координационную сферу соединения, которую при написании заключают в квадратные скобки.
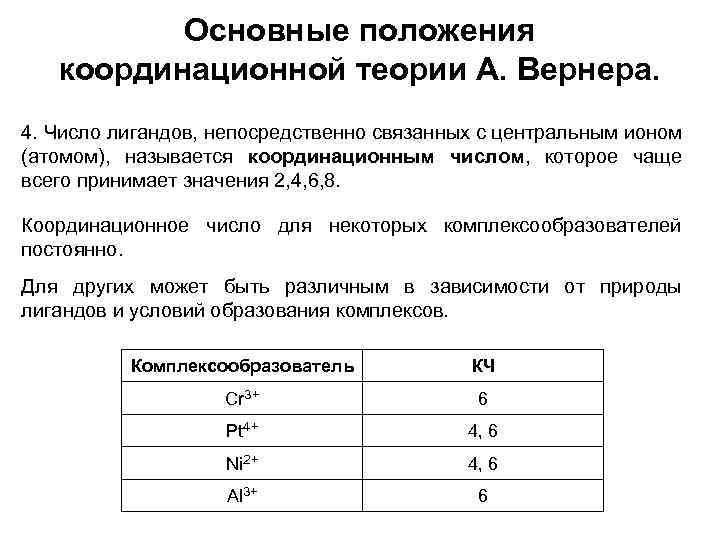 Основные положения координационной теории А. Вернера. 4. Число лигандов, непосредственно связанных с центральным ионом (атомом), называется координационным числом, которое чаще всего принимает значения 2, 4, 6, 8. Координационное число для некоторых комплексообразователей постоянно. Для других может быть различным в зависимости от природы лигандов и условий образования комплексов. Комплексообразователь КЧ Cr 3+ 6 Pt 4+ 4, 6 Ni 2+ 4, 6 Al 3+ 6
Основные положения координационной теории А. Вернера. 4. Число лигандов, непосредственно связанных с центральным ионом (атомом), называется координационным числом, которое чаще всего принимает значения 2, 4, 6, 8. Координационное число для некоторых комплексообразователей постоянно. Для других может быть различным в зависимости от природы лигандов и условий образования комплексов. Комплексообразователь КЧ Cr 3+ 6 Pt 4+ 4, 6 Ni 2+ 4, 6 Al 3+ 6
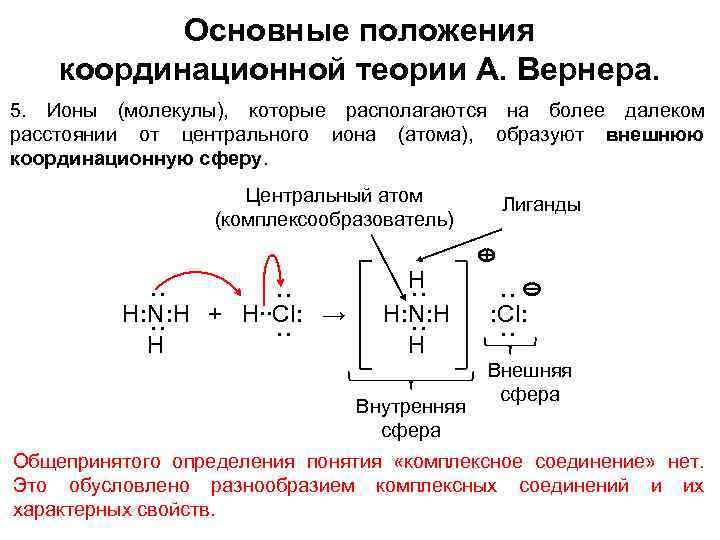 Основные положения координационной теории А. Вернера. 5. Ионы (молекулы), которые располагаются на более далеком расстоянии от центрального иона (атома), образуют внешнюю координационную сферу. : : : : Cl: Внутренняя сфера : : H: N: H + H∙∙Cl: → H H H: N: H H Лиганды : : : Центральный атом (комплексообразователь) Внешняя сфера Общепринятого определения понятия «комплексное соединение» нет. Это обусловлено разнообразием комплексных соединений и их характерных свойств.
Основные положения координационной теории А. Вернера. 5. Ионы (молекулы), которые располагаются на более далеком расстоянии от центрального иона (атома), образуют внешнюю координационную сферу. : : : : Cl: Внутренняя сфера : : H: N: H + H∙∙Cl: → H H H: N: H H Лиганды : : : Центральный атом (комплексообразователь) Внешняя сфера Общепринятого определения понятия «комплексное соединение» нет. Это обусловлено разнообразием комплексных соединений и их характерных свойств.
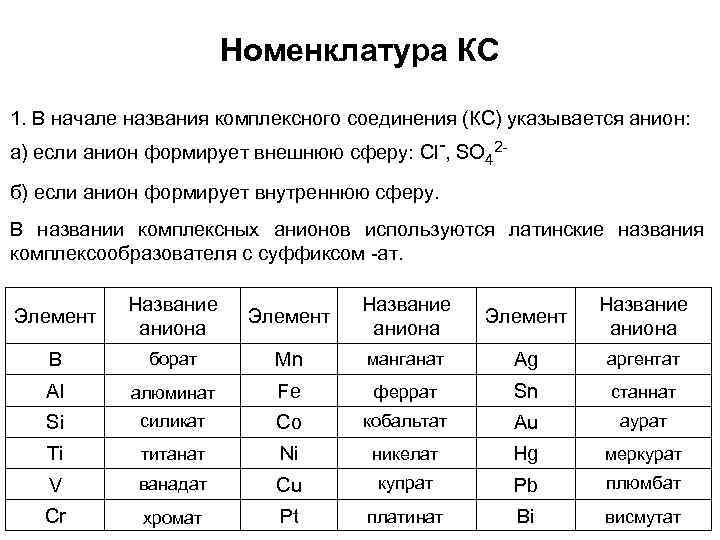 Номенклатура КС 1. В начале названия комплексного соединения (КС) указывается анион: а) если анион формирует внешнюю сферу: Cl-, SO 42 б) если анион формирует внутреннюю сферу. В названии комплексных анионов используются латинские названия комплексообразователя с суффиксом -ат. Элемент Название аниона B борат Mn манганат Ag аргентат Al алюминат Fe феррат Sn станнат Si силикат Co кобальтат Au аурат Ti титанат Ni никелат Hg меркурат V ванадат Cu купрат Pb плюмбат Cr хромат Pt платинат Bi висмутат
Номенклатура КС 1. В начале названия комплексного соединения (КС) указывается анион: а) если анион формирует внешнюю сферу: Cl-, SO 42 б) если анион формирует внутреннюю сферу. В названии комплексных анионов используются латинские названия комплексообразователя с суффиксом -ат. Элемент Название аниона B борат Mn манганат Ag аргентат Al алюминат Fe феррат Sn станнат Si силикат Co кобальтат Au аурат Ti титанат Ni никелат Hg меркурат V ванадат Cu купрат Pb плюмбат Cr хромат Pt платинат Bi висмутат
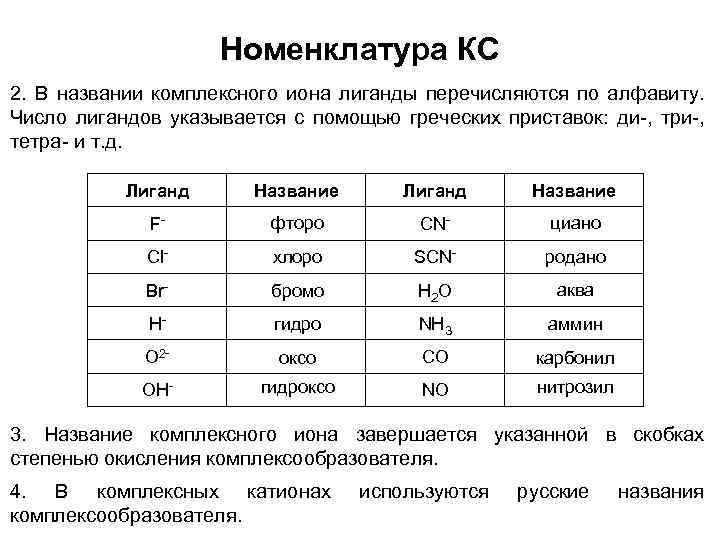 Номенклатура КС 2. В названии комплексного иона лиганды перечисляются по алфавиту. Число лигандов указывается с помощью греческих приставок: ди-, три-, тетра- и т. д. Лиганд Название F- фторо CN- циано Cl- хлоро SCN- родано Br- бромо H 2 O аква H- гидро NH 3 аммин O 2 - оксо CO карбонил OH- гидроксо NO нитрозил 3. Название комплексного иона завершается указанной в скобках степенью окисления комплексообразователя. 4. В комплексных катионах комплексообразователя. используются русские названия
Номенклатура КС 2. В названии комплексного иона лиганды перечисляются по алфавиту. Число лигандов указывается с помощью греческих приставок: ди-, три-, тетра- и т. д. Лиганд Название F- фторо CN- циано Cl- хлоро SCN- родано Br- бромо H 2 O аква H- гидро NH 3 аммин O 2 - оксо CO карбонил OH- гидроксо NO нитрозил 3. Название комплексного иона завершается указанной в скобках степенью окисления комплексообразователя. 4. В комплексных катионах комплексообразователя. используются русские названия
 Классификация КС I. Классификация по знаку заряда внутренней сферы комплекса: 1) Катионные комплексы: [Al(H 2 O)6]Cl 3 хлорид гексаакваалюминия гидрат [Zn(NH 3)4]Cl 2 хлорид тетраамминцинка аммиакат 2) Анионные комплексы: K[Al(OH)4] тетрагидроксоалюминат калия Na 2[SO 4] тетраоксосульфат (VI) натрия K 2[Be(SO 4)2] дисульфатобериллат калия 3) Нейтральные комплексы (не имеют внешней сферы): [Pt(NH 3)2 Cl 2] дихлородиаммин платины (II) [Ni(CO)4] тетракарбонил никеля
Классификация КС I. Классификация по знаку заряда внутренней сферы комплекса: 1) Катионные комплексы: [Al(H 2 O)6]Cl 3 хлорид гексаакваалюминия гидрат [Zn(NH 3)4]Cl 2 хлорид тетраамминцинка аммиакат 2) Анионные комплексы: K[Al(OH)4] тетрагидроксоалюминат калия Na 2[SO 4] тетраоксосульфат (VI) натрия K 2[Be(SO 4)2] дисульфатобериллат калия 3) Нейтральные комплексы (не имеют внешней сферы): [Pt(NH 3)2 Cl 2] дихлородиаммин платины (II) [Ni(CO)4] тетракарбонил никеля
![Классификация КС II. Классификация по проводимости электрического тока: Электролиты Кислоты Основания H[Au. Cl 4] Классификация КС II. Классификация по проводимости электрического тока: Электролиты Кислоты Основания H[Au. Cl 4]](https://present5.com/presentation/3/15129394_135573696.pdf-img/15129394_135573696.pdf-9.jpg) Классификация КС II. Классификация по проводимости электрического тока: Электролиты Кислоты Основания H[Au. Cl 4] [Ag(NH 3)2]OH [Ni(NH 3)6](NO 3)2 тетрахлороаурат (III) водорода гидроксид диамминсеребра (I) нитрат гексаамминникеля (II) H 2[SO 4] [Cu(NH 3)4](OH)2 Na 3[Al. F 6] тетраоксосульфат (VI) водорода гидроксид тетраамминмеди (II) Соли гексафтороалюминат натрия Диссоциируют на внутреннюю и внешнюю сферы: K 3[Al(OH)6] 3 K+ + [Al(OH)6]3 - Неэлектролиты: дихлородиаммин платины (II) [Pt(NH 3)2 Cl 2]
Классификация КС II. Классификация по проводимости электрического тока: Электролиты Кислоты Основания H[Au. Cl 4] [Ag(NH 3)2]OH [Ni(NH 3)6](NO 3)2 тетрахлороаурат (III) водорода гидроксид диамминсеребра (I) нитрат гексаамминникеля (II) H 2[SO 4] [Cu(NH 3)4](OH)2 Na 3[Al. F 6] тетраоксосульфат (VI) водорода гидроксид тетраамминмеди (II) Соли гексафтороалюминат натрия Диссоциируют на внутреннюю и внешнюю сферы: K 3[Al(OH)6] 3 K+ + [Al(OH)6]3 - Неэлектролиты: дихлородиаммин платины (II) [Pt(NH 3)2 Cl 2]
![Упражнения [Ag(NH 3)2]Cl [Co. Cl 2(NH 3)4]NO 3 хлорид диамминсеребра (I) нитрат тетраамминдихлорокобальта (III) Упражнения [Ag(NH 3)2]Cl [Co. Cl 2(NH 3)4]NO 3 хлорид диамминсеребра (I) нитрат тетраамминдихлорокобальта (III)](https://present5.com/presentation/3/15129394_135573696.pdf-img/15129394_135573696.pdf-10.jpg) Упражнения [Ag(NH 3)2]Cl [Co. Cl 2(NH 3)4]NO 3 хлорид диамминсеребра (I) нитрат тетраамминдихлорокобальта (III) [Cr(H 2 O)6]Cl 3 K 3[Fe(CN)6] хлорид гексааквахрома (III) гексацианоферрат (III) калия Na 2[Zn(OH)4] K 4[Fe(CN)6] тетрагидроксоцинкат натрия гексацианоферрат (II) калия [Fe(OH)2(H 2 O)4]Cl [Co(NH 3)4(NO 2)2]Cl хлорид тетрааквадигидроксожелеза (III) Na 3[Co(NO 2)6] гексанитрокобальтат (III) натрия хлорид тетраамминдинитрокобальта (III) Fe 3[Fe(CN)6]2 гексацианоферрат (III) железа (II)
Упражнения [Ag(NH 3)2]Cl [Co. Cl 2(NH 3)4]NO 3 хлорид диамминсеребра (I) нитрат тетраамминдихлорокобальта (III) [Cr(H 2 O)6]Cl 3 K 3[Fe(CN)6] хлорид гексааквахрома (III) гексацианоферрат (III) калия Na 2[Zn(OH)4] K 4[Fe(CN)6] тетрагидроксоцинкат натрия гексацианоферрат (II) калия [Fe(OH)2(H 2 O)4]Cl [Co(NH 3)4(NO 2)2]Cl хлорид тетрааквадигидроксожелеза (III) Na 3[Co(NO 2)6] гексанитрокобальтат (III) натрия хлорид тетраамминдинитрокобальта (III) Fe 3[Fe(CN)6]2 гексацианоферрат (III) железа (II)
![Упражнения Na 2[Cu. Cl 4] K 2[Pt. Cl 6] тетрахлорокупрат (II) натрия гексахлороплатинат (IV) Упражнения Na 2[Cu. Cl 4] K 2[Pt. Cl 6] тетрахлорокупрат (II) натрия гексахлороплатинат (IV)](https://present5.com/presentation/3/15129394_135573696.pdf-img/15129394_135573696.pdf-11.jpg) Упражнения Na 2[Cu. Cl 4] K 2[Pt. Cl 6] тетрахлорокупрат (II) натрия гексахлороплатинат (IV) калия Na 2[Cu(OH)4] тетрагидроксокупрат (II) натрия [Cr(H 2 O)6]Cl 3 хлорид гексааквахрома (III) [Fe(NH 3)6]Br 2 [Pt(NH 3)2 Cl 2] бромид гексаамминжелеза (II) дихлородиааминплатина (II) Fe 4[Fe(CN)6]3 гексацианоферрат (II) железа (III) [Cu(NH 3)4]SO 4 сульфат тетраамминмеди (II) [Co(NH 3)4(NO 2)Cl]Cl. O 4 перхлорат нитрохлоротетраамминкобальта (III) K 2[Zn(OH)4] тетрагидроксоцинкат (II) калия
Упражнения Na 2[Cu. Cl 4] K 2[Pt. Cl 6] тетрахлорокупрат (II) натрия гексахлороплатинат (IV) калия Na 2[Cu(OH)4] тетрагидроксокупрат (II) натрия [Cr(H 2 O)6]Cl 3 хлорид гексааквахрома (III) [Fe(NH 3)6]Br 2 [Pt(NH 3)2 Cl 2] бромид гексаамминжелеза (II) дихлородиааминплатина (II) Fe 4[Fe(CN)6]3 гексацианоферрат (II) железа (III) [Cu(NH 3)4]SO 4 сульфат тетраамминмеди (II) [Co(NH 3)4(NO 2)Cl]Cl. O 4 перхлорат нитрохлоротетраамминкобальта (III) K 2[Zn(OH)4] тетрагидроксоцинкат (II) калия
 Получение комплексных солей 1. амфотерный раствор + гидроксид щелочи = комплексная соль Be(OH)2 + Na. OH = Cr(OH)3 + KOH = 2. амфотерный раствор + вода + оксид щелочи = комплексная соль Zn. O + KOH + H 2 O = Al 2 O 3 + Na. OH + H 2 O = 3. Некоторые металлы (Zn, Be, Al) + раствор щелочи Be + Na. OH + H 2 O = Zn + KOH + H 2 O = Al + Na. OH + H 2 O = + вода = комплексная + водород соль
Получение комплексных солей 1. амфотерный раствор + гидроксид щелочи = комплексная соль Be(OH)2 + Na. OH = Cr(OH)3 + KOH = 2. амфотерный раствор + вода + оксид щелочи = комплексная соль Zn. O + KOH + H 2 O = Al 2 O 3 + Na. OH + H 2 O = 3. Некоторые металлы (Zn, Be, Al) + раствор щелочи Be + Na. OH + H 2 O = Zn + KOH + H 2 O = Al + Na. OH + H 2 O = + вода = комплексная + водород соль
![Разрушение гидроксокомплексов 1. Действие избытка сильной кислоты: Na[Al(OH)4] + HCl = K 3[Cr(OH)6] + Разрушение гидроксокомплексов 1. Действие избытка сильной кислоты: Na[Al(OH)4] + HCl = K 3[Cr(OH)6] +](https://present5.com/presentation/3/15129394_135573696.pdf-img/15129394_135573696.pdf-13.jpg) Разрушение гидроксокомплексов 1. Действие избытка сильной кислоты: Na[Al(OH)4] + HCl = K 3[Cr(OH)6] + HNO 3 = 2. Действие недостатка сильной кислоты: Na[Al(OH)4] + HCl = K 3[Cr(OH)6] + HNO 3 = 3. Действие слабой кислоты: Na[Al(OH)4] + H 2 S = K 3[Cr(OH)6] + CH 3 COOH =
Разрушение гидроксокомплексов 1. Действие избытка сильной кислоты: Na[Al(OH)4] + HCl = K 3[Cr(OH)6] + HNO 3 = 2. Действие недостатка сильной кислоты: Na[Al(OH)4] + HCl = K 3[Cr(OH)6] + HNO 3 = 3. Действие слабой кислоты: Na[Al(OH)4] + H 2 S = K 3[Cr(OH)6] + CH 3 COOH =
![Разрушение гидроксокомплексов 4. Действие углекислого газа и сернистого газа: Na[Al(OH)4] + СO 2 = Разрушение гидроксокомплексов 4. Действие углекислого газа и сернистого газа: Na[Al(OH)4] + СO 2 =](https://present5.com/presentation/3/15129394_135573696.pdf-img/15129394_135573696.pdf-14.jpg) Разрушение гидроксокомплексов 4. Действие углекислого газа и сернистого газа: Na[Al(OH)4] + СO 2 = K 3[Cr(OH)6] + SO 2 = 5. Действие солей железа (III), хрома (III), алюминия и сильных кислот: Na[Al(OH)4] + Fe. Cl 3 = K 3[Cr(OH)6] + Al(NO 3) = 6. Нагревание гидроксокомплексов ЩМ: t˚ Na[Al(OH)4] = t˚ K 3[Cr(OH)6] =
Разрушение гидроксокомплексов 4. Действие углекислого газа и сернистого газа: Na[Al(OH)4] + СO 2 = K 3[Cr(OH)6] + SO 2 = 5. Действие солей железа (III), хрома (III), алюминия и сильных кислот: Na[Al(OH)4] + Fe. Cl 3 = K 3[Cr(OH)6] + Al(NO 3) = 6. Нагревание гидроксокомплексов ЩМ: t˚ Na[Al(OH)4] = t˚ K 3[Cr(OH)6] =


