Комплексные соединения.ppt
- Количество слайдов: 28
 Комплексные соединения
Комплексные соединения
 • Комплексными называют соединения, содержащие в своем составе сложную молекулярную частицу (комплексную частицу), состоящую из центрального атома (комплексообразователя) и лигандов.
• Комплексными называют соединения, содержащие в своем составе сложную молекулярную частицу (комплексную частицу), состоящую из центрального атома (комплексообразователя) и лигандов.
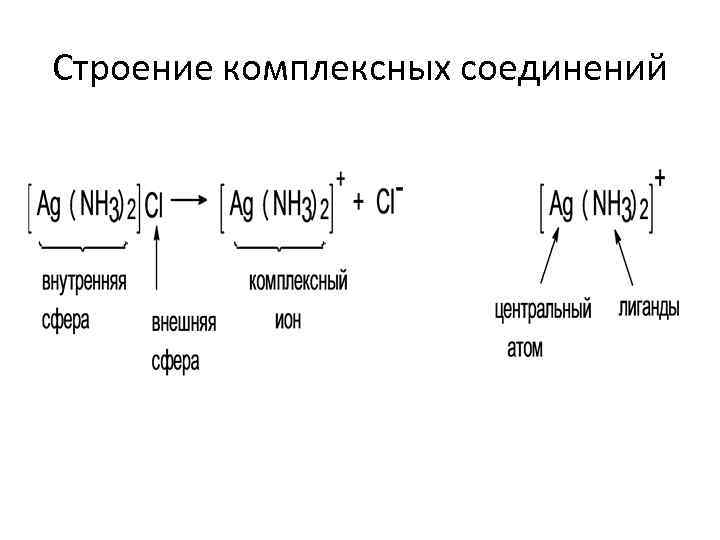 Строение комплексных соединений
Строение комплексных соединений
 • Координационное число комплексообразователя – это число связей, которые центральный атом образует с лигандами. • Дентатность лиганда определяется числом донорных атомов, доступных для координации.
• Координационное число комплексообразователя – это число связей, которые центральный атом образует с лигандами. • Дентатность лиганда определяется числом донорных атомов, доступных для координации.
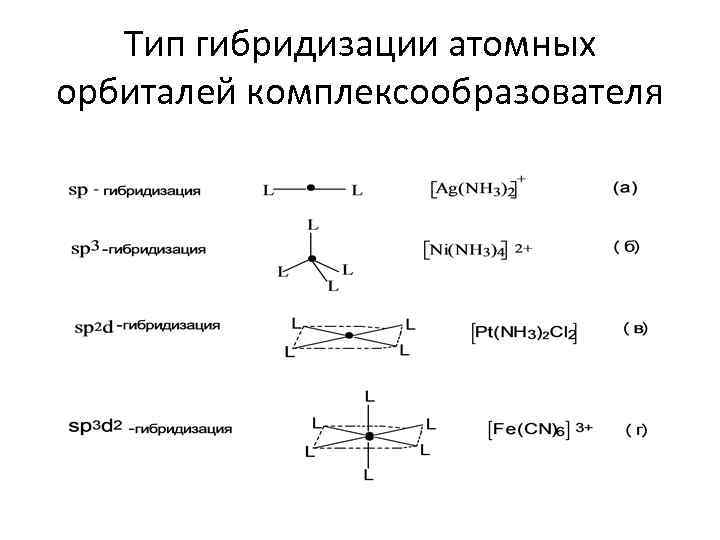 Тип гибридизации атомных орбиталей комплексообразователя
Тип гибридизации атомных орбиталей комплексообразователя
 Характеристика лигандов • Лиганды могут быть нейтральными молекулами ( H 2 O, NH 3, CO, амины RNH 2, пиридин C 6 H 5 N и т. д. ) или анионами (Cl-, F-, OH-, NO 2 -, CN- и т. д. ), имеющими в своем составе донорные атомы • По числу донорных атомов лиганды подразделяют на моно-, би- и полидентатные •
Характеристика лигандов • Лиганды могут быть нейтральными молекулами ( H 2 O, NH 3, CO, амины RNH 2, пиридин C 6 H 5 N и т. д. ) или анионами (Cl-, F-, OH-, NO 2 -, CN- и т. д. ), имеющими в своем составе донорные атомы • По числу донорных атомов лиганды подразделяют на моно-, би- и полидентатные •
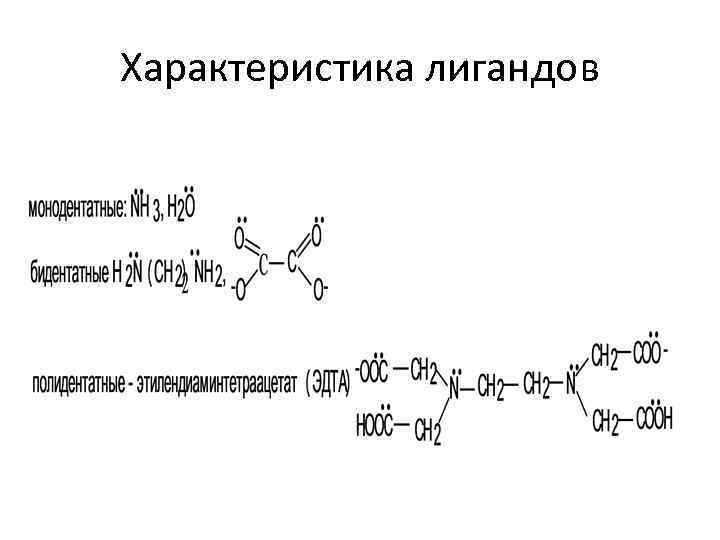 Характеристика лигандов
Характеристика лигандов
 Хелатные комплексы • Бидентатные и полидентатные лиганды (чаще органические молекулы) при соединении с центральным атомом могут образовывать циклические группировки атомов, включающие атом металлакомплексообразователя. Такие циклические структуры называют хелатными (или внутрициклическими) комплексами
Хелатные комплексы • Бидентатные и полидентатные лиганды (чаще органические молекулы) при соединении с центральным атомом могут образовывать циклические группировки атомов, включающие атом металлакомплексообразователя. Такие циклические структуры называют хелатными (или внутрициклическими) комплексами
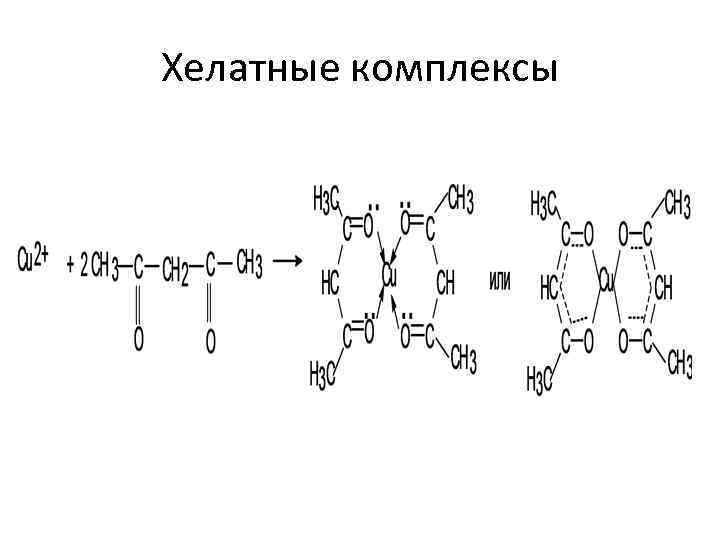 Хелатные комплексы
Хелатные комплексы
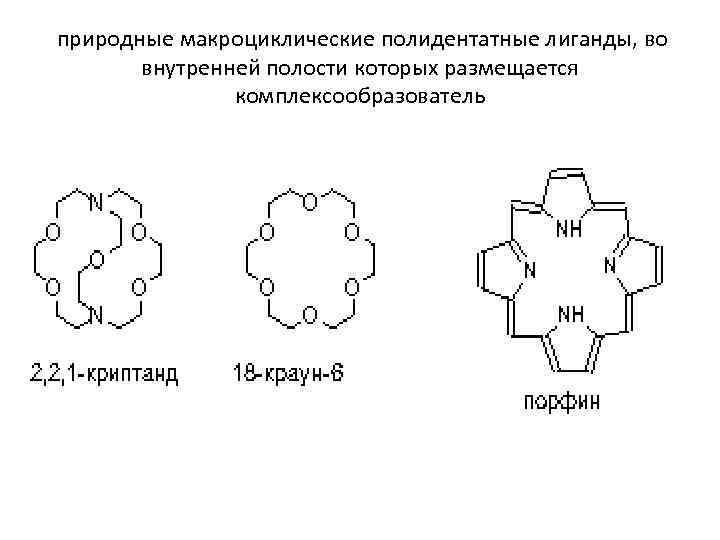 природные макроциклические полидентатные лиганды, во внутренней полости которых размещается комплексообразователь
природные макроциклические полидентатные лиганды, во внутренней полости которых размещается комплексообразователь
 По характеру электрического заряда комплексной частицы различают: • - катионные комплексы – • ион тетрааквацинка [Zn(H 2 O)4]2+, • ион дис(этилендиаммин) меди (II) [Cu(H 2 NCH 2 NH 2)2]2+ ; • - анионные комплексы – • гексацианоферрат (III)-ион [Fe(CN)6]3 -, триоксалатоманганат (III)-ион[Mn(C 2 O 4)3]3 -; • - нейтральные комплексы дихлородиамминплатина [Pt(NH 3)2 Cl 2], тетракарбонилникель [Ni(CO)4].
По характеру электрического заряда комплексной частицы различают: • - катионные комплексы – • ион тетрааквацинка [Zn(H 2 O)4]2+, • ион дис(этилендиаммин) меди (II) [Cu(H 2 NCH 2 NH 2)2]2+ ; • - анионные комплексы – • гексацианоферрат (III)-ион [Fe(CN)6]3 -, триоксалатоманганат (III)-ион[Mn(C 2 O 4)3]3 -; • - нейтральные комплексы дихлородиамминплатина [Pt(NH 3)2 Cl 2], тетракарбонилникель [Ni(CO)4].
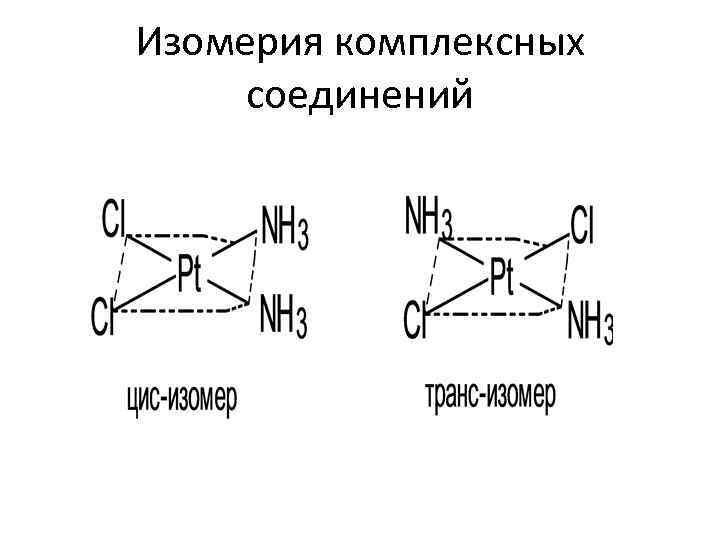
 Изомерия комплексных соединений • геометрическая (цис-, транс-) изомерия возможна в квадратных и октаэдрических комплексах при наличии двух одинаковых лигандов. Например, соединение дихлордиамминплатина [Pt(NH 3)2 Cl 2] может иметь:
Изомерия комплексных соединений • геометрическая (цис-, транс-) изомерия возможна в квадратных и октаэдрических комплексах при наличии двух одинаковых лигандов. Например, соединение дихлордиамминплатина [Pt(NH 3)2 Cl 2] может иметь:
 Изомерия комплексных соединений
Изомерия комплексных соединений
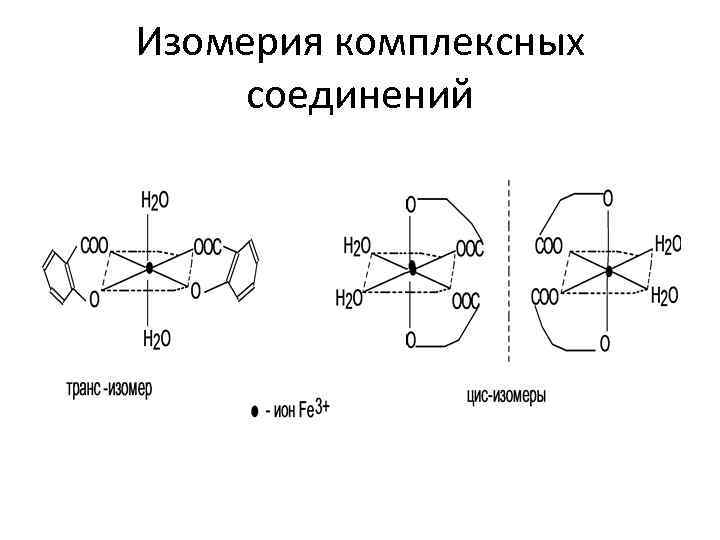
 Изомерия комплексных соединений • оптическая изомерия характерна для тетраэдрических комплексов с четырьмя различными лигандами и октаэдрических комплексов с бидентатными лигандами. По направлению вращения плоскости поляризованного света различают левовращающие и правовращающие комплексы. Такие оптические изомеры называют энантиомерами. Например, ион дисалицилатодиакваферрат (III) может существовать в виде трех пространственных изомеров (цис-изомер имеет два оптических изомера)
Изомерия комплексных соединений • оптическая изомерия характерна для тетраэдрических комплексов с четырьмя различными лигандами и октаэдрических комплексов с бидентатными лигандами. По направлению вращения плоскости поляризованного света различают левовращающие и правовращающие комплексы. Такие оптические изомеры называют энантиомерами. Например, ион дисалицилатодиакваферрат (III) может существовать в виде трех пространственных изомеров (цис-изомер имеет два оптических изомера)
 Изомерия комплексных соединений
Изомерия комплексных соединений
 Изомерия комплексных соединений • ионизационная изомерия – обмен частицами между внешней и внутренней координационной сферой (частный случай – гидратная изомерия), например: • [Cr(H 2 O)6]Cl 3 • [Cr. Cl(H 2 O)5]Cl 2 ∙ H 2 O • [Cr. Cl 2(H 2 O)4]Cl ∙ 2 H 2 O
Изомерия комплексных соединений • ионизационная изомерия – обмен частицами между внешней и внутренней координационной сферой (частный случай – гидратная изомерия), например: • [Cr(H 2 O)6]Cl 3 • [Cr. Cl(H 2 O)5]Cl 2 ∙ H 2 O • [Cr. Cl 2(H 2 O)4]Cl ∙ 2 H 2 O
![Химические свойства • H 2[Pt. Cl 6] + 2 KCl = K 2[Pt. Cl Химические свойства • H 2[Pt. Cl 6] + 2 KCl = K 2[Pt. Cl](https://present5.com/presentation/3/-42654335_139024246.pdf-img/-42654335_139024246.pdf-17.jpg) Химические свойства • H 2[Pt. Cl 6] + 2 KCl = K 2[Pt. Cl 6]↓ + 2 HCl • 2 K 4[Fe(CN)6] + Br 2 = 2 K 3[Fe(CN)6] + 2 KBr • K 2[Pt. Cl 6] + K 2 C 2 O 4 = K 2[Pt. Cl 4] + 2 KCl + 2 CO 2 • цис-[Pt(NH 3)2 Cl 2] + 2 NH 3 = [Pt(NH 3)4]2+ + 2 Cl–
Химические свойства • H 2[Pt. Cl 6] + 2 KCl = K 2[Pt. Cl 6]↓ + 2 HCl • 2 K 4[Fe(CN)6] + Br 2 = 2 K 3[Fe(CN)6] + 2 KBr • K 2[Pt. Cl 6] + K 2 C 2 O 4 = K 2[Pt. Cl 4] + 2 KCl + 2 CO 2 • цис-[Pt(NH 3)2 Cl 2] + 2 NH 3 = [Pt(NH 3)4]2+ + 2 Cl–
![Ионизация комплексных соединений • [Co(NH 3)6]Cl 3 = [Co(NH 3)6]3+ + 3 Cl– • Ионизация комплексных соединений • [Co(NH 3)6]Cl 3 = [Co(NH 3)6]3+ + 3 Cl– •](https://present5.com/presentation/3/-42654335_139024246.pdf-img/-42654335_139024246.pdf-18.jpg) Ионизация комплексных соединений • [Co(NH 3)6]Cl 3 = [Co(NH 3)6]3+ + 3 Cl– • • K 2[Pt. Cl 4] = 2 K+ + [Pt. Cl 4]2–
Ионизация комплексных соединений • [Co(NH 3)6]Cl 3 = [Co(NH 3)6]3+ + 3 Cl– • • K 2[Pt. Cl 4] = 2 K+ + [Pt. Cl 4]2–
![Ионизация комплексных ионов • • • [Zn(NH 3)4]2+ = [Zn(NH 3)3]2+ + NH 3, Ионизация комплексных ионов • • • [Zn(NH 3)4]2+ = [Zn(NH 3)3]2+ + NH 3,](https://present5.com/presentation/3/-42654335_139024246.pdf-img/-42654335_139024246.pdf-19.jpg) Ионизация комплексных ионов • • • [Zn(NH 3)4]2+ = [Zn(NH 3)3]2+ + NH 3, K 1 = 1, 1∙ 10– 3 [Zn(NH 3)3]2+ = [Zn(NH 3)2]2+ + NH 3, K 2 = 4, 9∙ 10– 3 [Zn(NH 3)2]2+ = [Zn(NH 3)]2+ + NH 3, K 3 = 5, 6∙ 10– 3 [Zn(NH 3)]2+ = Zn 2+ + NH 3, K 4 = 6, 6∙ 10– 3 [Zn(NH 3)4]2+ = Zn 2+ + 4 NH 3, Kн = K 1∙K 2∙K 3∙K 4 = 2, 0∙ 10– 10
Ионизация комплексных ионов • • • [Zn(NH 3)4]2+ = [Zn(NH 3)3]2+ + NH 3, K 1 = 1, 1∙ 10– 3 [Zn(NH 3)3]2+ = [Zn(NH 3)2]2+ + NH 3, K 2 = 4, 9∙ 10– 3 [Zn(NH 3)2]2+ = [Zn(NH 3)]2+ + NH 3, K 3 = 5, 6∙ 10– 3 [Zn(NH 3)]2+ = Zn 2+ + NH 3, K 4 = 6, 6∙ 10– 3 [Zn(NH 3)4]2+ = Zn 2+ + 4 NH 3, Kн = K 1∙K 2∙K 3∙K 4 = 2, 0∙ 10– 10
 Ионизация комплексных ионов • Рассчитайте концентрацию свободных ионов цинка в растворе нитрата татраамминцинка с концентрацией 0, 1 моль/л, содержащем также избыток аммиака 0, 5 моль/л.
Ионизация комплексных ионов • Рассчитайте концентрацию свободных ионов цинка в растворе нитрата татраамминцинка с концентрацией 0, 1 моль/л, содержащем также избыток аммиака 0, 5 моль/л.
![Конкурирующие процессы • [Zn(NH 3)4]2+ + 4 CN– = [Zn(CN)4]2– + 4 NH 3 Конкурирующие процессы • [Zn(NH 3)4]2+ + 4 CN– = [Zn(CN)4]2– + 4 NH 3](https://present5.com/presentation/3/-42654335_139024246.pdf-img/-42654335_139024246.pdf-21.jpg) Конкурирующие процессы • [Zn(NH 3)4]2+ + 4 CN– = [Zn(CN)4]2– + 4 NH 3
Конкурирующие процессы • [Zn(NH 3)4]2+ + 4 CN– = [Zn(CN)4]2– + 4 NH 3
 Комплексообразование и комплексные соединения в медицине. • Комплексные соединения применяются для корректировки обмена веществ (витамин В 12), терапии (комплексы платины), для детоксикации.
Комплексообразование и комплексные соединения в медицине. • Комплексные соединения применяются для корректировки обмена веществ (витамин В 12), терапии (комплексы платины), для детоксикации.
 принципы выведения из организма токсических ионов • применяется комплексонат кальция Na 2[Ca( –O CCH ) NCH CH N(CH CO –) ]. Препарат 2 2 2 2 получил название тетацин-кальций. Коротко обозначим комплексный ион Ca. Y 2. Рассмотрим возможность выведения с его помошью ионов Cr 3+. • Ca. Y 2 + Cr 3+ = Ca 2+ + Cr. Y Kн 2, 6 10 11 4 10 24
принципы выведения из организма токсических ионов • применяется комплексонат кальция Na 2[Ca( –O CCH ) NCH CH N(CH CO –) ]. Препарат 2 2 2 2 получил название тетацин-кальций. Коротко обозначим комплексный ион Ca. Y 2. Рассмотрим возможность выведения с его помошью ионов Cr 3+. • Ca. Y 2 + Cr 3+ = Ca 2+ + Cr. Y Kн 2, 6 10 11 4 10 24
 принципы выведения из организма токсических ионов • Рассмотрим пример потери активности карбоангидразы (КА) вследствие замещения нативного иона Zn 2+ ионами ртути: • КА Zn 2+ + Hg 2+ = КА Hg 2+ + Zn 2+ • Kн 3 10 11 3, 2 10 22 • K = 3 10 11/3, 2 10 22 = 9, 4 1010 • Активность можно восстановить, вводя в качестве антидота тиосульфат натрия • КА Hg 2+ + 2 S 2 O 32 = КА + [Hg(S 2 O 3)2]2 • Kн 3, 2 10 22 2, 4 10 34 • K = 3, 2 10 22/2, 4 10 34 = 1, 3 1012
принципы выведения из организма токсических ионов • Рассмотрим пример потери активности карбоангидразы (КА) вследствие замещения нативного иона Zn 2+ ионами ртути: • КА Zn 2+ + Hg 2+ = КА Hg 2+ + Zn 2+ • Kн 3 10 11 3, 2 10 22 • K = 3 10 11/3, 2 10 22 = 9, 4 1010 • Активность можно восстановить, вводя в качестве антидота тиосульфат натрия • КА Hg 2+ + 2 S 2 O 32 = КА + [Hg(S 2 O 3)2]2 • Kн 3, 2 10 22 2, 4 10 34 • K = 3, 2 10 22/2, 4 10 34 = 1, 3 1012
 Комплексные соединения как лекарства • • Комплексные соединения железа(II) применяются при пониженном содержании железа: цитрат, фумарат, лактат, глицерофосфат и др. • Миокризин Cl Au S(CH 2 COONa)2 при артритах (в настоящее время не применяется, но есть и другие препараты) • Тетрасукцинимидозолото(III) Au (NCOCH 2 CO)4 • Детоксиканты • БАЛ CH 2 CHCH 2 и унитиол CH 2 CHCH 2 SO 3 Na • І І І • SH SH OH SH SH
Комплексные соединения как лекарства • • Комплексные соединения железа(II) применяются при пониженном содержании железа: цитрат, фумарат, лактат, глицерофосфат и др. • Миокризин Cl Au S(CH 2 COONa)2 при артритах (в настоящее время не применяется, но есть и другие препараты) • Тетрасукцинимидозолото(III) Au (NCOCH 2 CO)4 • Детоксиканты • БАЛ CH 2 CHCH 2 и унитиол CH 2 CHCH 2 SO 3 Na • І І І • SH SH OH SH SH
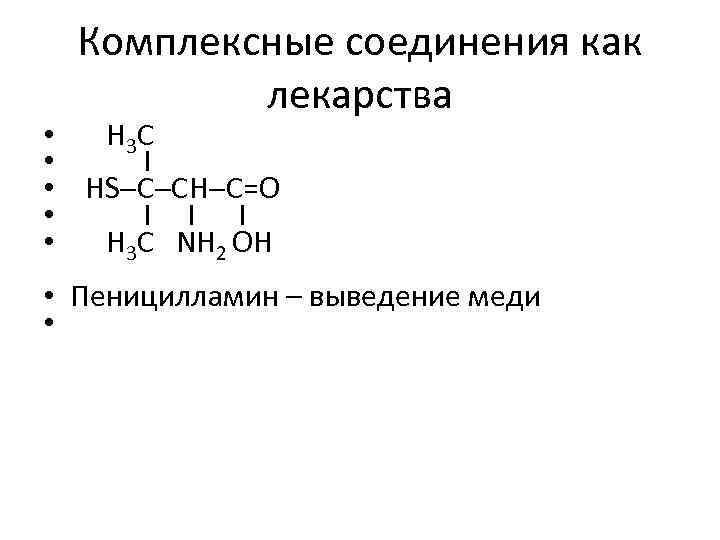 Комплексные соединения как лекарства • H 3 C • І • HS C CH C=O • І І І • H 3 C NH 2 OH • Пеницилламин – выведение меди •
Комплексные соединения как лекарства • H 3 C • І • HS C CH C=O • І І І • H 3 C NH 2 OH • Пеницилламин – выведение меди •
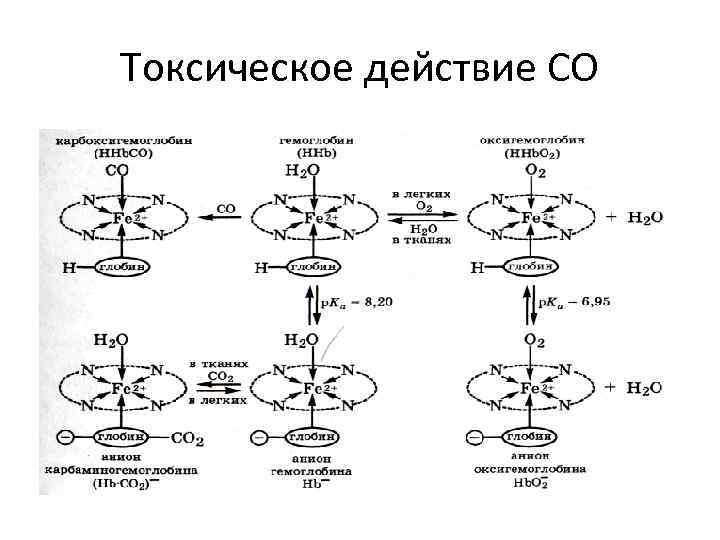 Токсическое действие СО
Токсическое действие СО
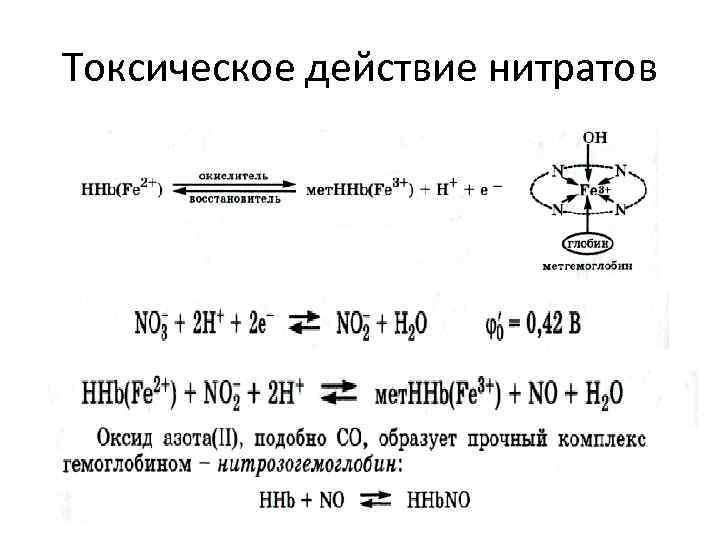 Токсическое действие нитратов
Токсическое действие нитратов


