Материаловедение.ppt
- Количество слайдов: 154



 Компетенции, формируемые в рамках дисциплины «Материаловедение» • • • использует основные законы естественнонаучных дисциплин в профессиональной деятельности, применяет методы математического анализа и моделирования, теоретического и экспериментального исследования; умеет выбирать основные и вспомогательные материалы и способы реализации основных технологических процессов и применять прогрессивные методы эксплуатации технологического оборудования при изготовлении изделий машиностроения; умеет применять методы стандартных испытаний по определению физико механических свойств и технологических показателей используемых материалов и готовых изделий; участвует во внедрении технологических процессов наукоемкого производства, контроля качества материалов, процессов повышения надежности и износостойкости элементов и узлов машин и установок, механических систем различного назначения; способен участвовать в организации эффективного контроля качества материалов, технологических процессов, готовой машиностроительной продукции.
Компетенции, формируемые в рамках дисциплины «Материаловедение» • • • использует основные законы естественнонаучных дисциплин в профессиональной деятельности, применяет методы математического анализа и моделирования, теоретического и экспериментального исследования; умеет выбирать основные и вспомогательные материалы и способы реализации основных технологических процессов и применять прогрессивные методы эксплуатации технологического оборудования при изготовлении изделий машиностроения; умеет применять методы стандартных испытаний по определению физико механических свойств и технологических показателей используемых материалов и готовых изделий; участвует во внедрении технологических процессов наукоемкого производства, контроля качества материалов, процессов повышения надежности и износостойкости элементов и узлов машин и установок, механических систем различного назначения; способен участвовать в организации эффективного контроля качества материалов, технологических процессов, готовой машиностроительной продукции.
 Вещества в газообразном состоянии не имеют формы, заполняют весь возможный объем; имеют меньшие плотности, чем твердые тела и жидкости. При обычных температурах газы – хорошие диэлектрики. Жидкости подобно твердым телам обладают малой сжимаемостью и большой плотностью, подобно газам не обладают упругостью формы и легко текут. Имеет место «ближний порядок» , т. е. в среднем для каждой молекулы жидкости число ближайших соседей и их взаимное расположение одинаковы.
Вещества в газообразном состоянии не имеют формы, заполняют весь возможный объем; имеют меньшие плотности, чем твердые тела и жидкости. При обычных температурах газы – хорошие диэлектрики. Жидкости подобно твердым телам обладают малой сжимаемостью и большой плотностью, подобно газам не обладают упругостью формы и легко текут. Имеет место «ближний порядок» , т. е. в среднем для каждой молекулы жидкости число ближайших соседей и их взаимное расположение одинаковы.
 Твердое состояние тела характеризуются стабильностью формы, малой сжимаемостью и большой плотностью. Частицы твердого тела расположены друг от друга на расстоянии, не превышающем их габариты, поэтому они практически лишены возможности совершать относительное перемещение. Единственное движение, которое им доступно – колебание вокруг состояния равновесия. Плазма частично или полностью ионизированный газ, образованный из нейтральных атомов (или молекул) и заряженных частиц (ионов и электронов). Присутствие свободных электрических зарядов делает плазму проводящей средой, что обуславливает её заметно большее (по сравнению с другими агрегатными состояниями вещества) взаимодействие с магнитным и электрическим полями.
Твердое состояние тела характеризуются стабильностью формы, малой сжимаемостью и большой плотностью. Частицы твердого тела расположены друг от друга на расстоянии, не превышающем их габариты, поэтому они практически лишены возможности совершать относительное перемещение. Единственное движение, которое им доступно – колебание вокруг состояния равновесия. Плазма частично или полностью ионизированный газ, образованный из нейтральных атомов (или молекул) и заряженных частиц (ионов и электронов). Присутствие свободных электрических зарядов делает плазму проводящей средой, что обуславливает её заметно большее (по сравнению с другими агрегатными состояниями вещества) взаимодействие с магнитным и электрическим полями.
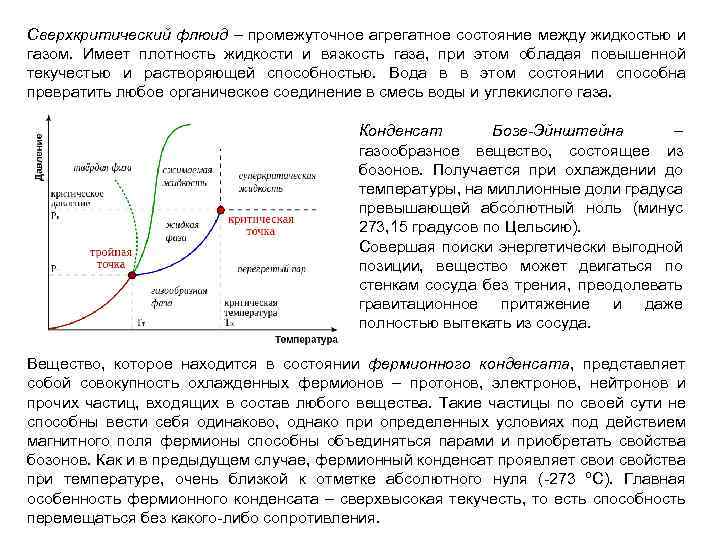 Сверхкритический флюид – промежуточное агрегатное состояние между жидкостью и газом. Имеет плотность жидкости и вязкость газа, при этом обладая повышенной текучестью и растворяющей способностью. Вода в в этом состоянии способна превратить любое органическое соединение в смесь воды и углекислого газа. Конденсат Бозе-Эйнштейна – газообразное вещество, состоящее из бозонов. Получается при охлаждении до температуры, на миллионные доли градуса превышающей абсолютный ноль (минус 273, 15 градусов по Цельсию). Совершая поиски энергетически выгодной позиции, вещество может двигаться по стенкам сосуда без трения, преодолевать гравитационное притяжение и даже полностью вытекать из сосуда. Вещество, которое находится в состоянии фермионного конденсата, представляет собой совокупность охлажденных фермионов – протонов, электронов, нейтронов и прочих частиц, входящих в состав любого вещества. Такие частицы по своей сути не способны вести себя одинаково, однако при определенных условиях под действием магнитного поля фермионы способны объединяться парами и приобретать свойства бозонов. Как и в предыдущем случае, фермионный конденсат проявляет свои свойства при температуре, очень близкой к отметке абсолютного нуля ( 273 ºС). Главная особенность фермионного конденсата – сверхвысокая текучесть, то есть способность перемещаться без какого либо сопротивления.
Сверхкритический флюид – промежуточное агрегатное состояние между жидкостью и газом. Имеет плотность жидкости и вязкость газа, при этом обладая повышенной текучестью и растворяющей способностью. Вода в в этом состоянии способна превратить любое органическое соединение в смесь воды и углекислого газа. Конденсат Бозе-Эйнштейна – газообразное вещество, состоящее из бозонов. Получается при охлаждении до температуры, на миллионные доли градуса превышающей абсолютный ноль (минус 273, 15 градусов по Цельсию). Совершая поиски энергетически выгодной позиции, вещество может двигаться по стенкам сосуда без трения, преодолевать гравитационное притяжение и даже полностью вытекать из сосуда. Вещество, которое находится в состоянии фермионного конденсата, представляет собой совокупность охлажденных фермионов – протонов, электронов, нейтронов и прочих частиц, входящих в состав любого вещества. Такие частицы по своей сути не способны вести себя одинаково, однако при определенных условиях под действием магнитного поля фермионы способны объединяться парами и приобретать свойства бозонов. Как и в предыдущем случае, фермионный конденсат проявляет свои свойства при температуре, очень близкой к отметке абсолютного нуля ( 273 ºС). Главная особенность фермионного конденсата – сверхвысокая текучесть, то есть способность перемещаться без какого либо сопротивления.
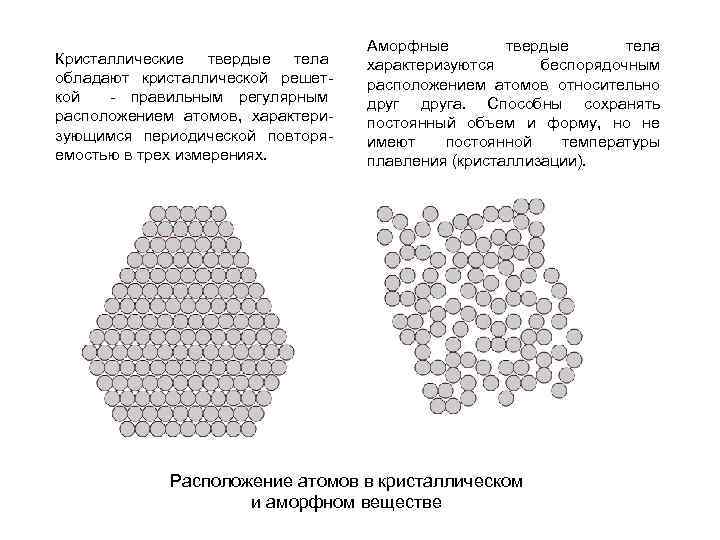 Кристаллические твердые тела обладают кристаллической решет кой правильным регулярным расположением атомов, характери зующимся периодической повторя емостью в трех измерениях. Аморфные твердые тела характеризуются беспорядочным расположением атомов относительно друга. Способны сохранять постоянный объем и форму, но не имеют постоянной температуры плавления (кристаллизации). Расположение атомов в кристаллическом и аморфном веществе
Кристаллические твердые тела обладают кристаллической решет кой правильным регулярным расположением атомов, характери зующимся периодической повторя емостью в трех измерениях. Аморфные твердые тела характеризуются беспорядочным расположением атомов относительно друга. Способны сохранять постоянный объем и форму, но не имеют постоянной температуры плавления (кристаллизации). Расположение атомов в кристаллическом и аморфном веществе
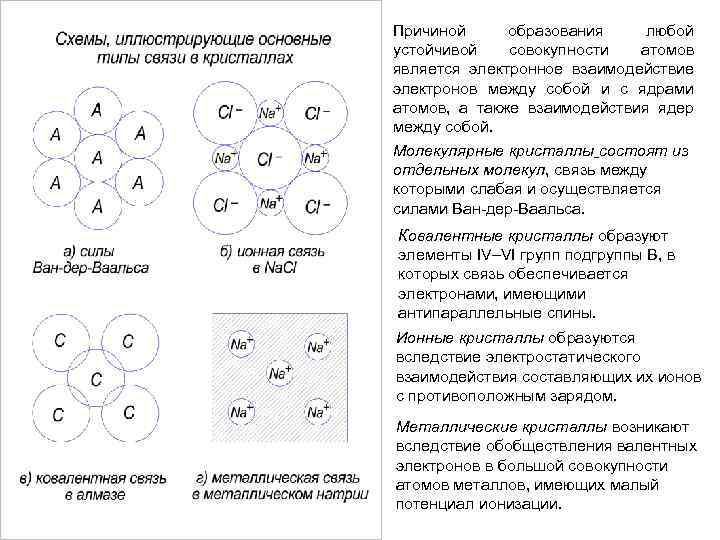 Причиной образования любой устойчивой совокупности атомов является электронное взаимодействие электронов между собой и с ядрами атомов, а также взаимодействия ядер между собой. Молекулярные кристаллы состоят из отдельных молекул, связь между которыми слабая и осуществляется силами Ван дер Ваальса. Ковалентные кристаллы образуют элементы IV–VI групп подгруппы В, в которых связь обеспечивается электронами, имеющими антипараллельные спины. Ионные кристаллы образуются вследствие электростатического взаимодействия составляющих их ионов с противоположным зарядом. Металлические кристаллы возникают вследствие обобществления валентных электронов в большой совокупности атомов металлов, имеющих малый потенциал ионизации.
Причиной образования любой устойчивой совокупности атомов является электронное взаимодействие электронов между собой и с ядрами атомов, а также взаимодействия ядер между собой. Молекулярные кристаллы состоят из отдельных молекул, связь между которыми слабая и осуществляется силами Ван дер Ваальса. Ковалентные кристаллы образуют элементы IV–VI групп подгруппы В, в которых связь обеспечивается электронами, имеющими антипараллельные спины. Ионные кристаллы образуются вследствие электростатического взаимодействия составляющих их ионов с противоположным зарядом. Металлические кристаллы возникают вследствие обобществления валентных электронов в большой совокупности атомов металлов, имеющих малый потенциал ионизации.
 Металлы – вещества, которые в твердом состоянии обладают рядом характерных свойств: • высокой тепло и электропроводностью; • положительным температурным коэффициентом электросопротивления (с повышением температуры электросопротивление чистых металлов возрастает; большое число металлов обладает сверхпроводимостью – у этих металлов при температуре, близкой к абсолютному нулю, электросопротивление падает скачкообразно практически до нуля); • термоэлектронной эмиссией, т. е. способностью испускать электроны при нагреве; • хорошей отражательной способностью (металлы непрозрачны и обладают металлическим блеском); • повышенной способностью к пластической деформации. Свойства металлов обусловлены металлической связью взаимодействием между периодически расположенными и положительно заряженными ионами и электронным газом внешними валентными электронами.
Металлы – вещества, которые в твердом состоянии обладают рядом характерных свойств: • высокой тепло и электропроводностью; • положительным температурным коэффициентом электросопротивления (с повышением температуры электросопротивление чистых металлов возрастает; большое число металлов обладает сверхпроводимостью – у этих металлов при температуре, близкой к абсолютному нулю, электросопротивление падает скачкообразно практически до нуля); • термоэлектронной эмиссией, т. е. способностью испускать электроны при нагреве; • хорошей отражательной способностью (металлы непрозрачны и обладают металлическим блеском); • повышенной способностью к пластической деформации. Свойства металлов обусловлены металлической связью взаимодействием между периодически расположенными и положительно заряженными ионами и электронным газом внешними валентными электронами.
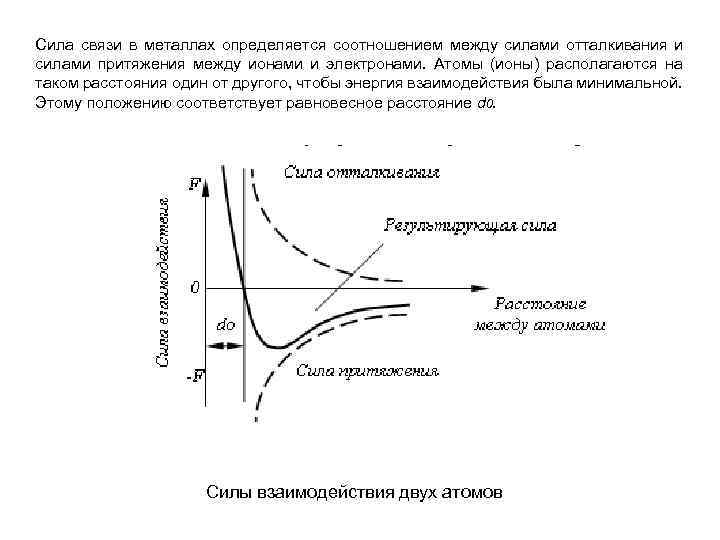 Сила связи в металлах определяется соотношением между силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстояния один от другого, чтобы энергия взаимодействия была минимальной. Этому положению соответствует равновесное расстояние d 0. Силы взаимодействия двух атомов
Сила связи в металлах определяется соотношением между силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстояния один от другого, чтобы энергия взаимодействия была минимальной. Этому положению соответствует равновесное расстояние d 0. Силы взаимодействия двух атомов
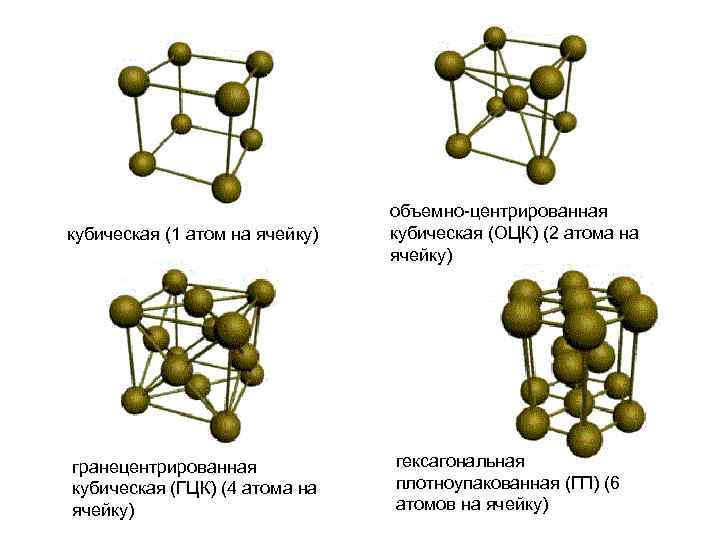 кубическая (1 атом на ячейку) гранецентрированная кубическая (ГЦК) (4 атома на ячейку) объемно центрированная кубическая (ОЦК) (2 атома на ячейку) гексагональная плотноупакованная (ГП) (6 атомов на ячейку)
кубическая (1 атом на ячейку) гранецентрированная кубическая (ГЦК) (4 атома на ячейку) объемно центрированная кубическая (ОЦК) (2 атома на ячейку) гексагональная плотноупакованная (ГП) (6 атомов на ячейку)
 Параметр решетки − это расстояние между атомами по ребру элементарной ячейки. Параметры решетки измеряется в нанометрах (1 нм = 10 9 м = 10 Å). Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а. Для характеристики гексагональной решетки принимают два параметра сторону шестигранника а и высоту призмы с. Когда отношение с/а = 1, 633, то атомы упакованы наиболее плотно, и решетка называется гексагональной плотноупакованной. Базис кристаллической решетки - число атомов, принадлежащих каждой элементарной ячейке. Коэффициент компактности – отношение объема всех частиц, приходящихся на одну элементарную ячейку, ко всему объему элементарной ячейки. Под координационным числом понимается количество ближайших соседей данного атома.
Параметр решетки − это расстояние между атомами по ребру элементарной ячейки. Параметры решетки измеряется в нанометрах (1 нм = 10 9 м = 10 Å). Параметры кубических решеток характеризуются длиной ребра куба и обозначаются буквой а. Для характеристики гексагональной решетки принимают два параметра сторону шестигранника а и высоту призмы с. Когда отношение с/а = 1, 633, то атомы упакованы наиболее плотно, и решетка называется гексагональной плотноупакованной. Базис кристаллической решетки - число атомов, принадлежащих каждой элементарной ячейке. Коэффициент компактности – отношение объема всех частиц, приходящихся на одну элементарную ячейку, ко всему объему элементарной ячейки. Под координационным числом понимается количество ближайших соседей данного атома.
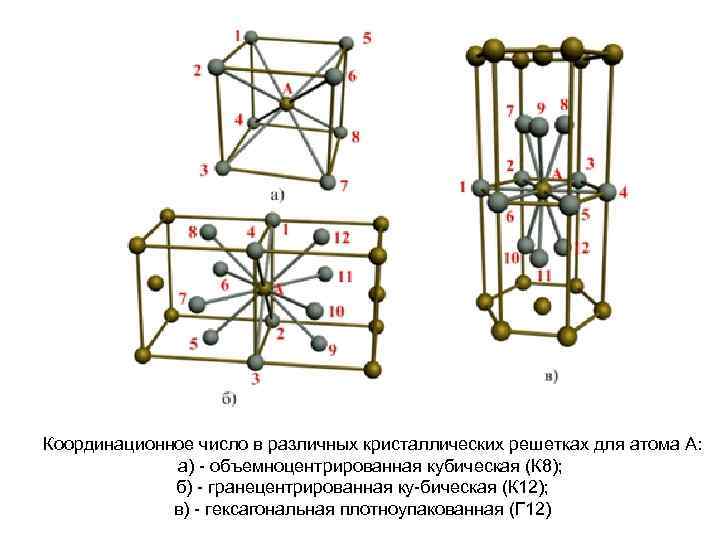 Координационное число в различных кристаллических решетках для атома А: а) объемноцентрированная кубическая (К 8); б) гранецентрированная ку бическая (К 12); в) гексагональная плотноупакованная (Г 12)
Координационное число в различных кристаллических решетках для атома А: а) объемноцентрированная кубическая (К 8); б) гранецентрированная ку бическая (К 12); в) гексагональная плотноупакованная (Г 12)
![Кристаллографические направления и плоскости в кристаллической решетке: основные направления [001]; основные плоскости (001) [001] Кристаллографические направления и плоскости в кристаллической решетке: основные направления [001]; основные плоскости (001) [001]](https://present5.com/presentation/3/144759616_437878692.pdf-img/144759616_437878692.pdf-17.jpg) Кристаллографические направления и плоскости в кристаллической решетке: основные направления [001]; основные плоскости (001) [001] z z (111) (110) (010) [010] y y [100] x x (100) [110] Упорядоченность кристаллического строения в пространственной решетке позволяет выделить отдельные кристаллографические направления и плоскости. Кристаллографические направления − это характерные прямые линии, выходящие из точки отсчета, вдоль которых в кристаллической решетке располагаются атомы. Точками отсчета, могут служить вершины куба, а кристаллографическими направлениями его ребра и диагонали, а также диагонали граней
Кристаллографические направления и плоскости в кристаллической решетке: основные направления [001]; основные плоскости (001) [001] z z (111) (110) (010) [010] y y [100] x x (100) [110] Упорядоченность кристаллического строения в пространственной решетке позволяет выделить отдельные кристаллографические направления и плоскости. Кристаллографические направления − это характерные прямые линии, выходящие из точки отсчета, вдоль которых в кристаллической решетке располагаются атомы. Точками отсчета, могут служить вершины куба, а кристаллографическими направлениями его ребра и диагонали, а также диагонали граней
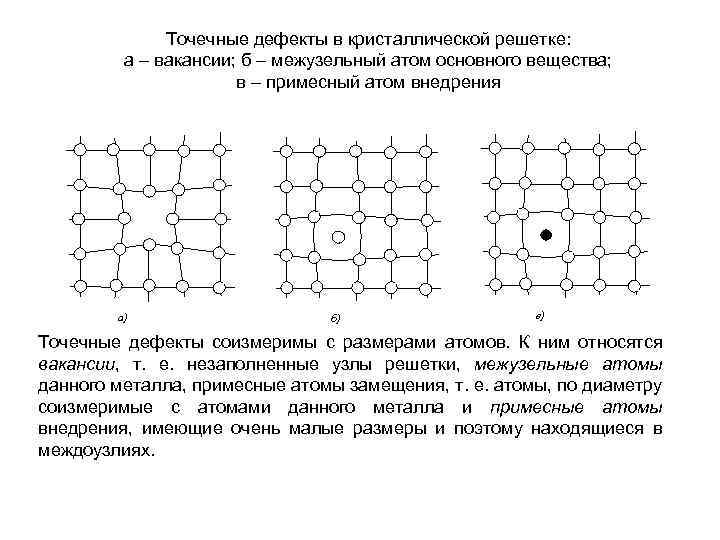 Точечные дефекты в кристаллической решетке: а – вакансии; б – межузельный атом основного вещества; в – примесный атом внедрения а) б) в) Точечные дефекты соизмеримы с размерами атомов. К ним относятся вакансии, т. е. незаполненные узлы решетки, межузельные атомы данного металла, примесные атомы замещения, т. е. атомы, по диаметру соизмеримые с атомами данного металла и примесные атомы внедрения, имеющие очень малые размеры и поэтому находящиеся в междоузлиях.
Точечные дефекты в кристаллической решетке: а – вакансии; б – межузельный атом основного вещества; в – примесный атом внедрения а) б) в) Точечные дефекты соизмеримы с размерами атомов. К ним относятся вакансии, т. е. незаполненные узлы решетки, межузельные атомы данного металла, примесные атомы замещения, т. е. атомы, по диаметру соизмеримые с атомами данного металла и примесные атомы внедрения, имеющие очень малые размеры и поэтому находящиеся в междоузлиях.
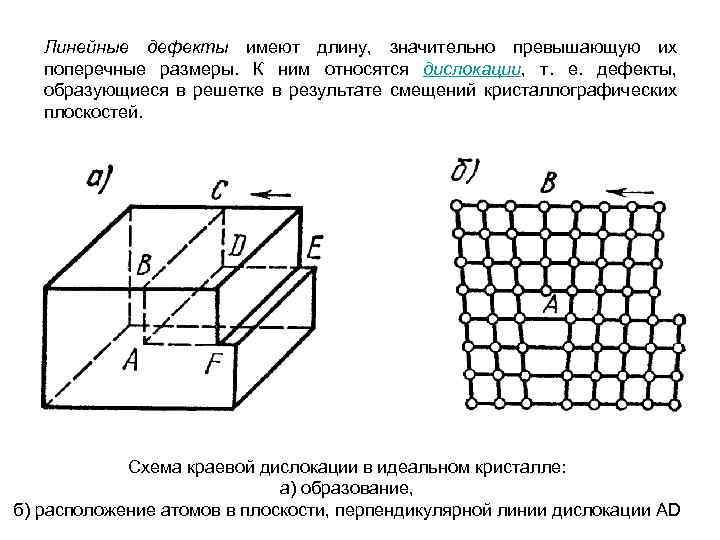 Линейные дефекты имеют длину, значительно превышающую их поперечные размеры. К ним относятся дислокации, т. е. дефекты, образующиеся в решетке в результате смещений кристаллографических плоскостей. Схема краевой дислокации в идеальном кристалле: а) образование, б) расположение атомов в плоскости, перпендикулярной линии дислокации AD
Линейные дефекты имеют длину, значительно превышающую их поперечные размеры. К ним относятся дислокации, т. е. дефекты, образующиеся в решетке в результате смещений кристаллографических плоскостей. Схема краевой дислокации в идеальном кристалле: а) образование, б) расположение атомов в плоскости, перпендикулярной линии дислокации AD
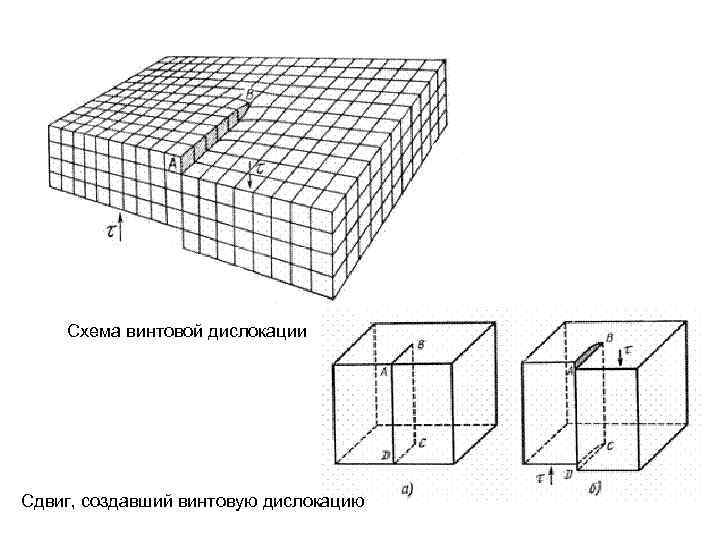 Схема винтовой дислокации Сдвиг, создавший винтовую дислокацию
Схема винтовой дислокации Сдвиг, создавший винтовую дислокацию
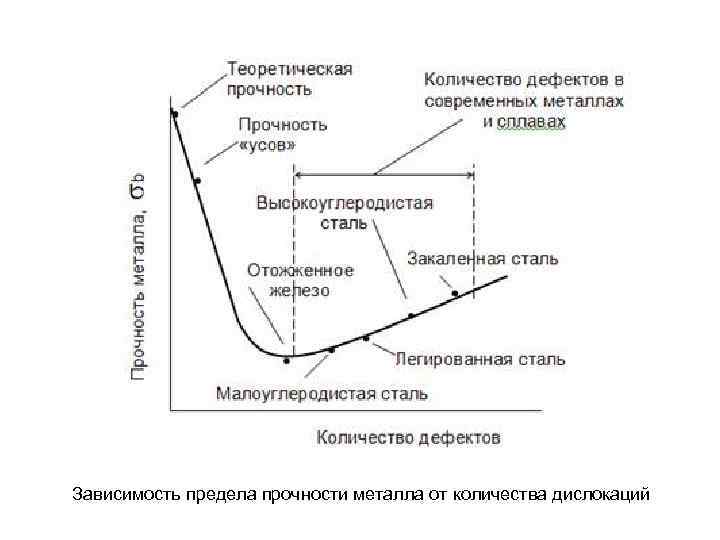 Зависимость предела прочности металла от количества дислокаций
Зависимость предела прочности металла от количества дислокаций
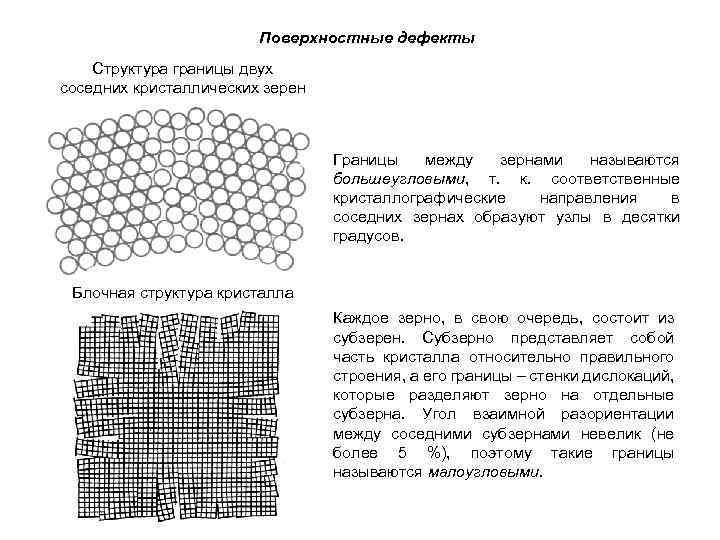 Поверхностные дефекты Структура границы двух соседних кристаллических зерен Границы между зернами называются большеугловыми, т. к. соответственные кристаллографические направления в соседних зернах образуют узлы в десятки градусов. Блочная структура кристалла Каждое зерно, в свою очередь, состоит из субзерен. Субзерно представляет собой часть кристалла относительно правильного строения, а его границы – стенки дислокаций, которые разделяют зерно на отдельные субзерна. Угол взаимной разориентации между соседними субзернами невелик (не более 5 %), поэтому такие границы называются малоугловыми.
Поверхностные дефекты Структура границы двух соседних кристаллических зерен Границы между зернами называются большеугловыми, т. к. соответственные кристаллографические направления в соседних зернах образуют узлы в десятки градусов. Блочная структура кристалла Каждое зерно, в свою очередь, состоит из субзерен. Субзерно представляет собой часть кристалла относительно правильного строения, а его границы – стенки дислокаций, которые разделяют зерно на отдельные субзерна. Угол взаимной разориентации между соседними субзернами невелик (не более 5 %), поэтому такие границы называются малоугловыми.
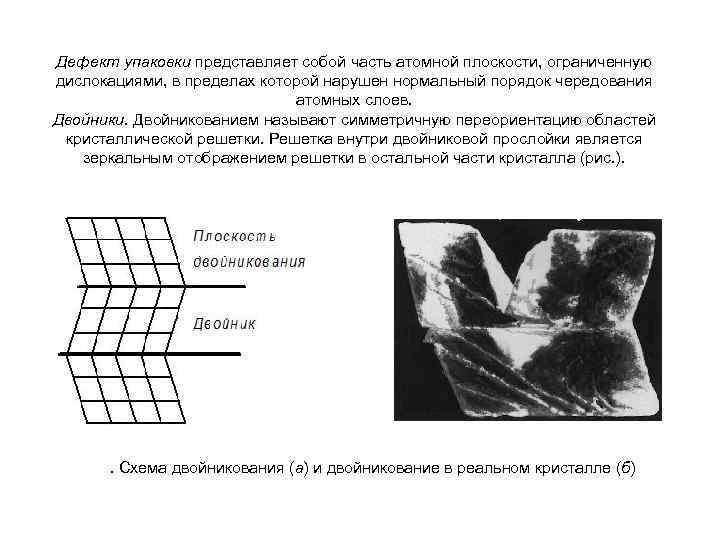 Дефект упаковки представляет собой часть атомной плоскости, ограниченную дислокациями, в пределах которой нарушен нормальный порядок чередования атомных слоев. Двойники. Двойникованием называют симметричную переориентацию областей кристаллической решетки. Решетка внутри двойниковой прослойки является зеркальным отображением решетки в остальной части кристалла (рис. ). . Схема двойникования (а) и двойникование в реальном кристалле (б)
Дефект упаковки представляет собой часть атомной плоскости, ограниченную дислокациями, в пределах которой нарушен нормальный порядок чередования атомных слоев. Двойники. Двойникованием называют симметричную переориентацию областей кристаллической решетки. Решетка внутри двойниковой прослойки является зеркальным отображением решетки в остальной части кристалла (рис. ). . Схема двойникования (а) и двойникование в реальном кристалле (б)
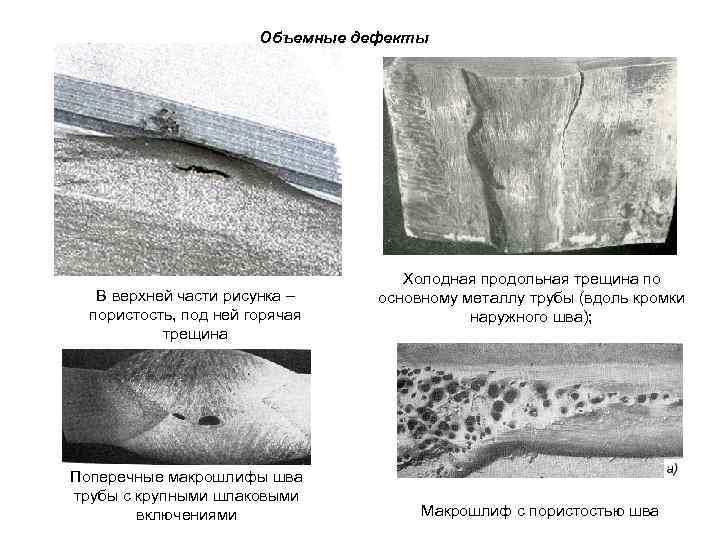 Объемные дефекты В верхней части рисунка – пористость, под ней горячая трещина Поперечные макрошлифы шва трубы с крупными шлаковыми включениями Холодная продольная трещина по основному металлу трубы (вдоль кромки наружного шва); Макрошлиф с пористостью шва
Объемные дефекты В верхней части рисунка – пористость, под ней горячая трещина Поперечные макрошлифы шва трубы с крупными шлаковыми включениями Холодная продольная трещина по основному металлу трубы (вдоль кромки наружного шва); Макрошлиф с пористостью шва
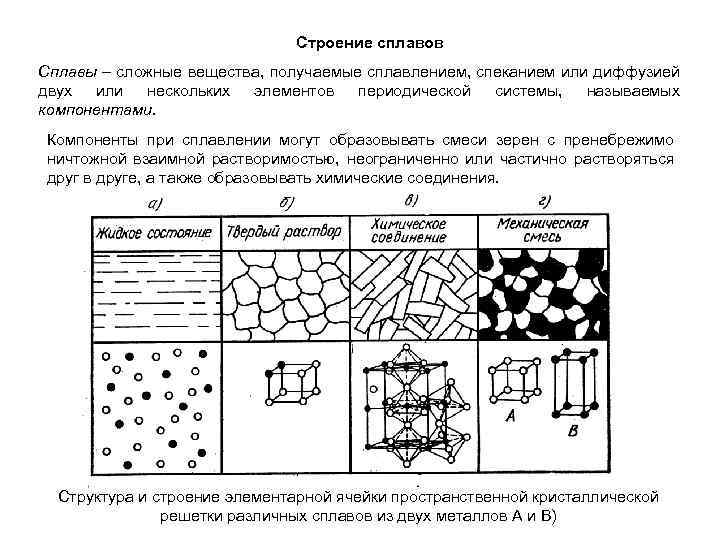 Строение сплавов Сплавы – сложные вещества, получаемые сплавлением, спеканием или диффузией двух или нескольких элементов периодической системы, называемых компонентами. Компоненты при сплавлении могут образовывать смеси зерен с пренебрежимо ничтожной взаимной растворимостью, неограниченно или частично растворяться друг в друге, а также образовывать химические соединения. Структура и строение элементарной ячейки пространственной кристаллической решетки различных сплавов из двух металлов А и В)
Строение сплавов Сплавы – сложные вещества, получаемые сплавлением, спеканием или диффузией двух или нескольких элементов периодической системы, называемых компонентами. Компоненты при сплавлении могут образовывать смеси зерен с пренебрежимо ничтожной взаимной растворимостью, неограниченно или частично растворяться друг в друге, а также образовывать химические соединения. Структура и строение элементарной ячейки пространственной кристаллической решетки различных сплавов из двух металлов А и В)
 Смесь образуется при взаимодействии компонентов, не способных к взаимному растворению в твердом состоянии и не вступающих в химическую реакцию с образованием соединения. Химическое соединение представляет собой зерна со специфической кристаллической решеткой, отличной от решеток обоих компонентов. Химические соединения являются очень твердыми и хрупкими веществами. Твердый раствор образуется при растворении компонентов друге, является однофазным, состоит из одного вида кристаллов, имеет одну кристаллическую решетку и существует в интервале концентраций. Обозначаются твердые растворы буквами греческого алфавита: α, β, γ и т. д. А А А С В В а) б) в) Кристаллическая решетка ОЦК: а – неограниченный твердый раствор замещения; б – ограниченный твердый раствор замещения; в – твердый раствор внедрения
Смесь образуется при взаимодействии компонентов, не способных к взаимному растворению в твердом состоянии и не вступающих в химическую реакцию с образованием соединения. Химическое соединение представляет собой зерна со специфической кристаллической решеткой, отличной от решеток обоих компонентов. Химические соединения являются очень твердыми и хрупкими веществами. Твердый раствор образуется при растворении компонентов друге, является однофазным, состоит из одного вида кристаллов, имеет одну кристаллическую решетку и существует в интервале концентраций. Обозначаются твердые растворы буквами греческого алфавита: α, β, γ и т. д. А А А С В В а) б) в) Кристаллическая решетка ОЦК: а – неограниченный твердый раствор замещения; б – ограниченный твердый раствор замещения; в – твердый раствор внедрения
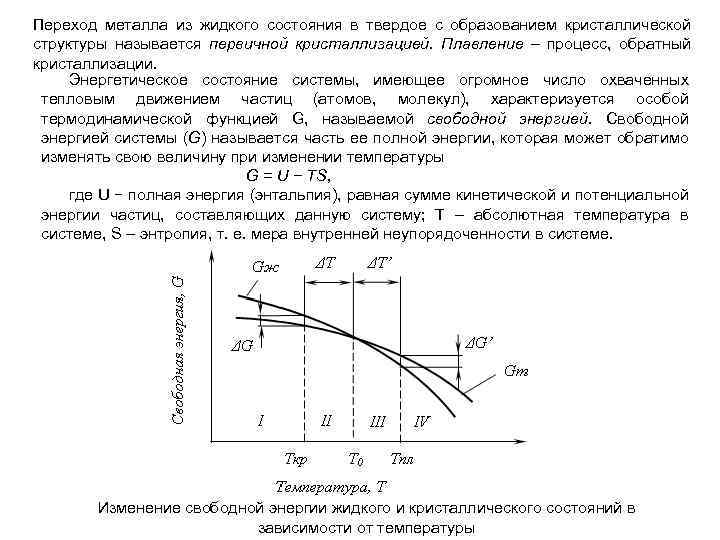 Переход металла из жидкого состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Плавление – процесс, обратный кристаллизации. Энергетическое состояние системы, имеющее огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией G, называемой свободной энергией. Свободной энергией системы (G) называется часть ее полной энергии, которая может обратимо изменять свою величину при изменении температуры G = U − TS, где U − полная энергия (энтальпия), равная сумме кинетической и потенциальной энергии частиц, составляющих данную систему; Т – абсолютная температура в системе, S – энтропия, т. е. мера внутренней неупорядоченности в системе. Изменение свободной энергии жидкого и кристаллического состояний в зависимости от температуры
Переход металла из жидкого состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Плавление – процесс, обратный кристаллизации. Энергетическое состояние системы, имеющее огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией G, называемой свободной энергией. Свободной энергией системы (G) называется часть ее полной энергии, которая может обратимо изменять свою величину при изменении температуры G = U − TS, где U − полная энергия (энтальпия), равная сумме кинетической и потенциальной энергии частиц, составляющих данную систему; Т – абсолютная температура в системе, S – энтропия, т. е. мера внутренней неупорядоченности в системе. Изменение свободной энергии жидкого и кристаллического состояний в зависимости от температуры
 Кривые охлаждения при кристаллизации
Кривые охлаждения при кристаллизации
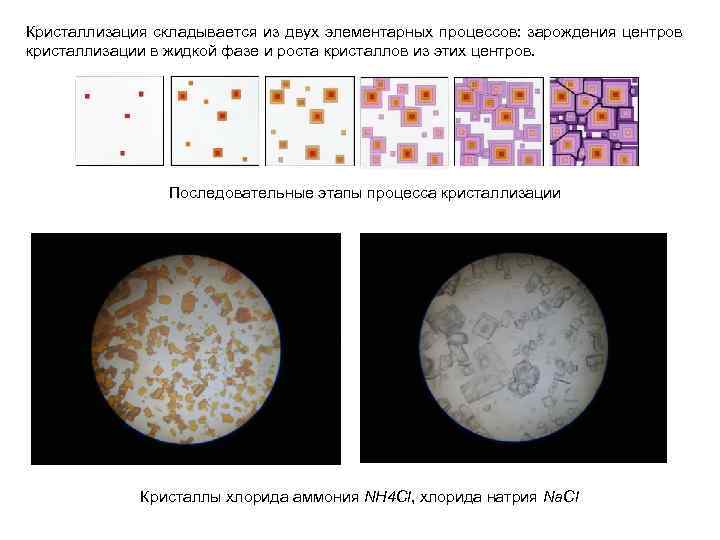 Кристаллизация складывается из двух элементарных процессов: зарождения центров кристаллизации в жидкой фазе и роста кристаллов из этих центров. Последовательные этапы процесса кристаллизации Кристаллы хлорида аммония NH 4 Cl, хлорида натрия Na. Cl
Кристаллизация складывается из двух элементарных процессов: зарождения центров кристаллизации в жидкой фазе и роста кристаллов из этих центров. Последовательные этапы процесса кристаллизации Кристаллы хлорида аммония NH 4 Cl, хлорида натрия Na. Cl
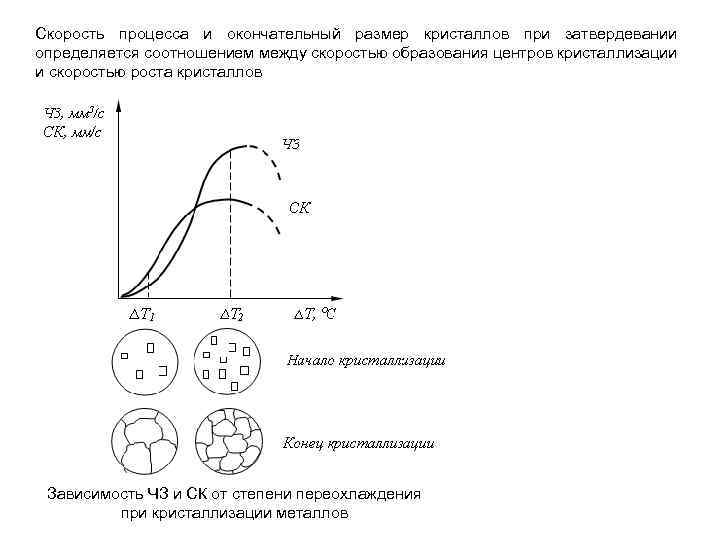 Скорость процесса и окончательный размер кристаллов при затвердевании определяется соотношением между скоростью образования центров кристаллизации и скоростью роста кристаллов Зависимость ЧЗ и СК от степени переохлаждения при кристаллизации металлов
Скорость процесса и окончательный размер кристаллов при затвердевании определяется соотношением между скоростью образования центров кристаллизации и скоростью роста кристаллов Зависимость ЧЗ и СК от степени переохлаждения при кристаллизации металлов
 Форма растущих кристаллов определяется не только условиями их столкновений между собой, но и составом сплава, наличием примесей и условиями охлаждения: • условиями их столкновений (образование зерен); • составом сплава (зерна из тугоплавкого вещества кристаллизуется в первую очередь и поэтому более крупные); • наличием примесей (получение более мелкозернистой структуры); • условиями охлаждения (столбчатые или равноосные кристаллы). Дендриты окислов марганца в халцедоне Схема строения дендрита: 1– 3 – оси первого, второго и третьего порядка
Форма растущих кристаллов определяется не только условиями их столкновений между собой, но и составом сплава, наличием примесей и условиями охлаждения: • условиями их столкновений (образование зерен); • составом сплава (зерна из тугоплавкого вещества кристаллизуется в первую очередь и поэтому более крупные); • наличием примесей (получение более мелкозернистой структуры); • условиями охлаждения (столбчатые или равноосные кристаллы). Дендриты окислов марганца в халцедоне Схема строения дендрита: 1– 3 – оси первого, второго и третьего порядка
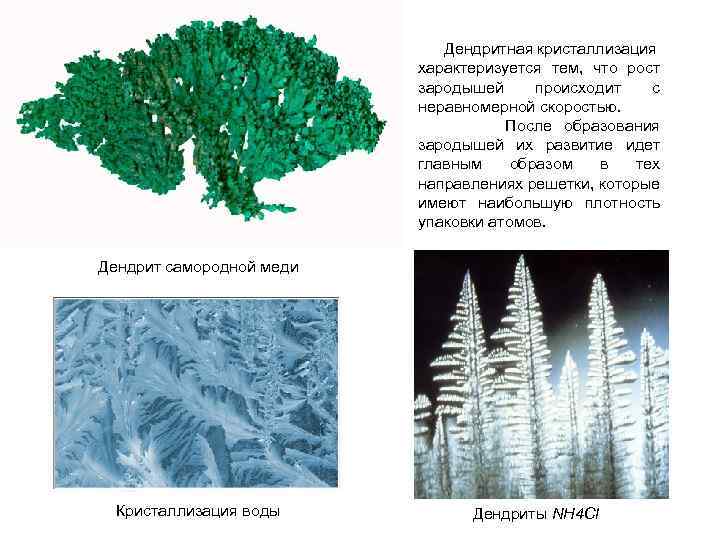 Дендритная кристаллизация характеризуется тем, что рост зародышей происходит с неравномерной скоростью. После образования зародышей их развитие идет главным образом в тех направлениях решетки, которые имеют наибольшую плотность упаковки атомов. Дендрит самородной меди Кристаллизация воды Дендриты NH 4 Cl
Дендритная кристаллизация характеризуется тем, что рост зародышей происходит с неравномерной скоростью. После образования зародышей их развитие идет главным образом в тех направлениях решетки, которые имеют наибольшую плотность упаковки атомов. Дендрит самородной меди Кристаллизация воды Дендриты NH 4 Cl
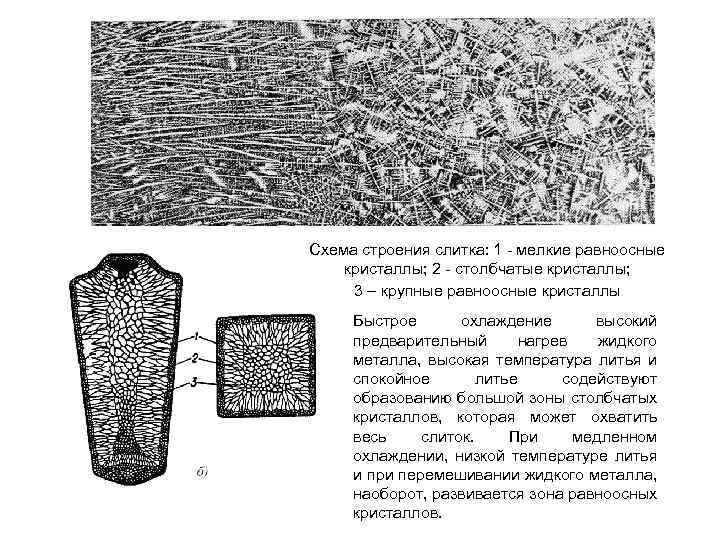 Схема строения слитка: 1 мелкие равноосные кристаллы; 2 столбчатые кристаллы; 3 – крупные равноосные кристаллы Быстрое охлаждение высокий предварительный нагрев жидкого металла, высокая температура литья и спокойное литье содействуют образованию большой зоны столбчатых кристаллов, которая может охватить весь слиток. При медленном охлаждении, низкой температуре литья и при перемешивании жидкого металла, наоборот, развивается зона равноосных кристаллов.
Схема строения слитка: 1 мелкие равноосные кристаллы; 2 столбчатые кристаллы; 3 – крупные равноосные кристаллы Быстрое охлаждение высокий предварительный нагрев жидкого металла, высокая температура литья и спокойное литье содействуют образованию большой зоны столбчатых кристаллов, которая может охватить весь слиток. При медленном охлаждении, низкой температуре литья и при перемешивании жидкого металла, наоборот, развивается зона равноосных кристаллов.
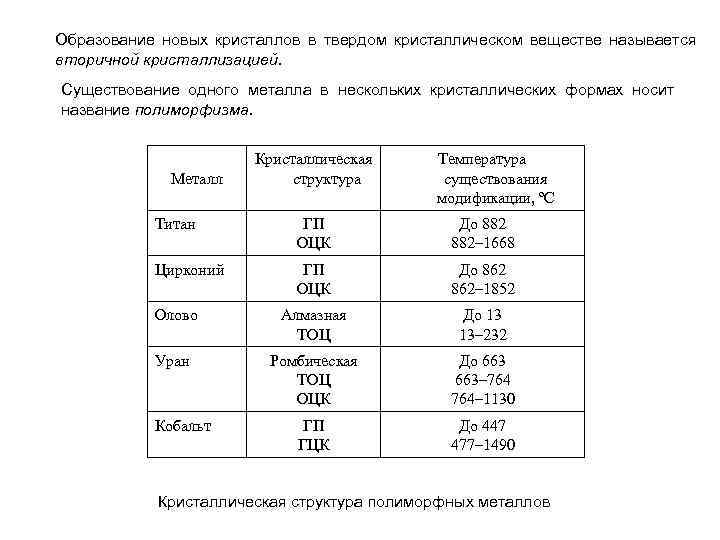 Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. Существование одного металла в нескольких кристаллических формах носит название полиморфизма. Металл Кристаллическая структура Температура существования модификации, ºС Титан ГП ОЦК До 882– 1668 Цирконий ГП ОЦК До 862– 1852 Олово Алмазная ТОЦ До 13 13– 232 Уран Ромбическая ТОЦ ОЦК До 663– 764– 1130 ГП ГЦК До 447 477– 1490 Кобальт Кристаллическая структура полиморфных металлов
Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. Существование одного металла в нескольких кристаллических формах носит название полиморфизма. Металл Кристаллическая структура Температура существования модификации, ºС Титан ГП ОЦК До 882– 1668 Цирконий ГП ОЦК До 862– 1852 Олово Алмазная ТОЦ До 13 13– 232 Уран Ромбическая ТОЦ ОЦК До 663– 764– 1130 ГП ГЦК До 447 477– 1490 Кобальт Кристаллическая структура полиморфных металлов
 Т, о. С Ж Ж+Feδ 1539 1392 Feδ+Feγ Feγ+Feβ 911 Feβ+Feα 768 Feα Время Кривая охлаждения железа
Т, о. С Ж Ж+Feδ 1539 1392 Feδ+Feγ Feγ+Feβ 911 Feβ+Feα 768 Feα Время Кривая охлаждения железа
 Фаза - однородная часть равновесной системы с определённым химическим составом и термодинамическими свойствами отделённая от других частей системы поверхностью раздела. Компонент – это простые и сложные вещества, составляющие систему. Независимые компоненты – это вещества, наименьшее число которых достаточно для образования как всей системы, так и любой её фазы. Величины, характеризующие состояние системы называются параметрами её состояния. Это температура, давление, магнитное поле и др. ; концентрация (при условии 2 х или более компонентов в системе). Числом степеней свободы (вариантностью) называется число тех переменных (давление, температура, концентрация), которые можно изменять произвольно без изменения числа фаз. Правило фаз Гиббса: предсказывает возможность изменения числа фаз в системе, в зависимости от числа компонентов и от изменения внешних условий. В равновесной многофазной системе число независимых компонентов равно числу степеней свободы плюс два минус число фаз Ф, если на систему из внешних факторов влияют только давление и температура. С = К + 2 – Ф, где С – степень свободы, К – число независимых компонентов, Ф – число фаз.
Фаза - однородная часть равновесной системы с определённым химическим составом и термодинамическими свойствами отделённая от других частей системы поверхностью раздела. Компонент – это простые и сложные вещества, составляющие систему. Независимые компоненты – это вещества, наименьшее число которых достаточно для образования как всей системы, так и любой её фазы. Величины, характеризующие состояние системы называются параметрами её состояния. Это температура, давление, магнитное поле и др. ; концентрация (при условии 2 х или более компонентов в системе). Числом степеней свободы (вариантностью) называется число тех переменных (давление, температура, концентрация), которые можно изменять произвольно без изменения числа фаз. Правило фаз Гиббса: предсказывает возможность изменения числа фаз в системе, в зависимости от числа компонентов и от изменения внешних условий. В равновесной многофазной системе число независимых компонентов равно числу степеней свободы плюс два минус число фаз Ф, если на систему из внешних факторов влияют только давление и температура. С = К + 2 – Ф, где С – степень свободы, К – число независимых компонентов, Ф – число фаз.
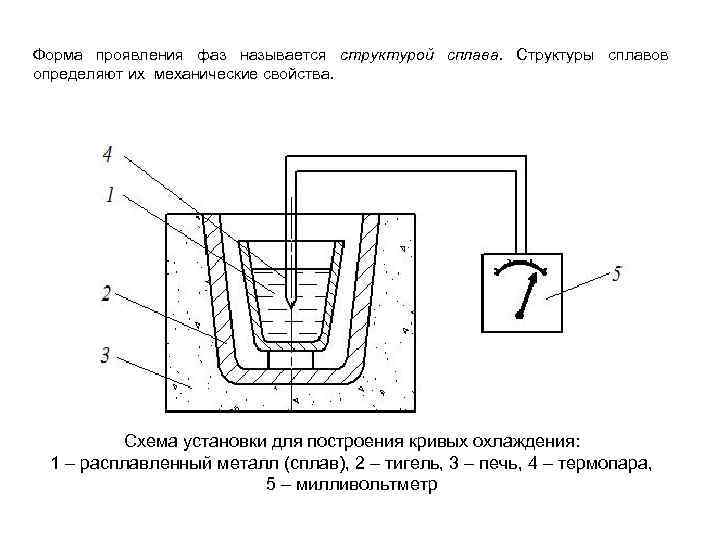 Форма проявления фаз называется структурой сплава. Структуры сплавов определяют их механические свойства. Схема установки для построения кривых охлаждения: 1 – расплавленный металл (сплав), 2 – тигель, 3 – печь, 4 – термопара, 5 – милливольтметр
Форма проявления фаз называется структурой сплава. Структуры сплавов определяют их механические свойства. Схема установки для построения кривых охлаждения: 1 – расплавленный металл (сплав), 2 – тигель, 3 – печь, 4 – термопара, 5 – милливольтметр
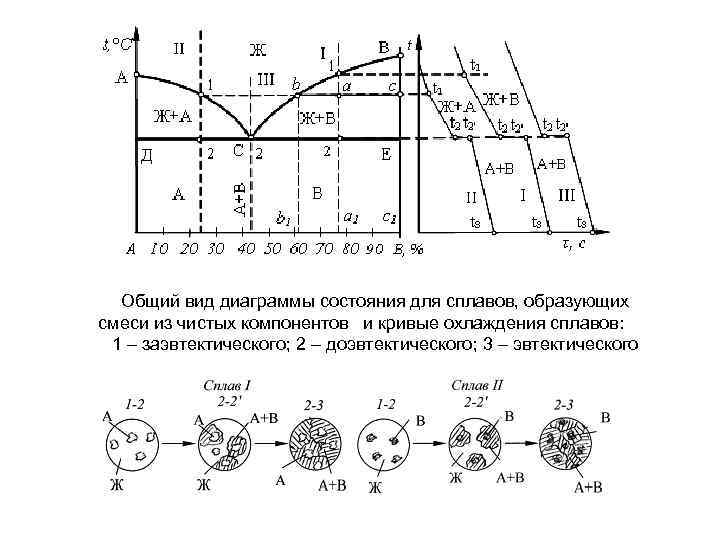 Общий вид диаграммы состояния для сплавов, образующих смеси из чистых компонентов и кривые охлаждения сплавов: 1 – заэвтектического; 2 – доэвтектического; 3 – эвтектического
Общий вид диаграммы состояния для сплавов, образующих смеси из чистых компонентов и кривые охлаждения сплавов: 1 – заэвтектического; 2 – доэвтектического; 3 – эвтектического
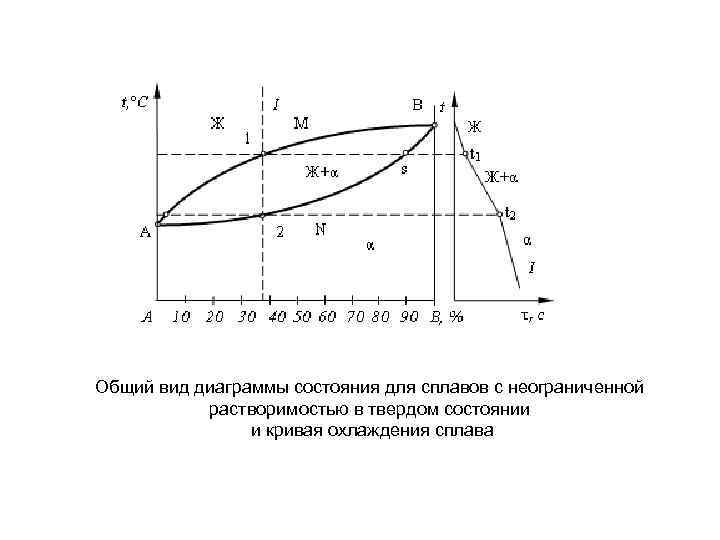 Общий вид диаграммы состояния для сплавов с неограниченной растворимостью в твердом состоянии и кривая охлаждения сплава
Общий вид диаграммы состояния для сплавов с неограниченной растворимостью в твердом состоянии и кривая охлаждения сплава
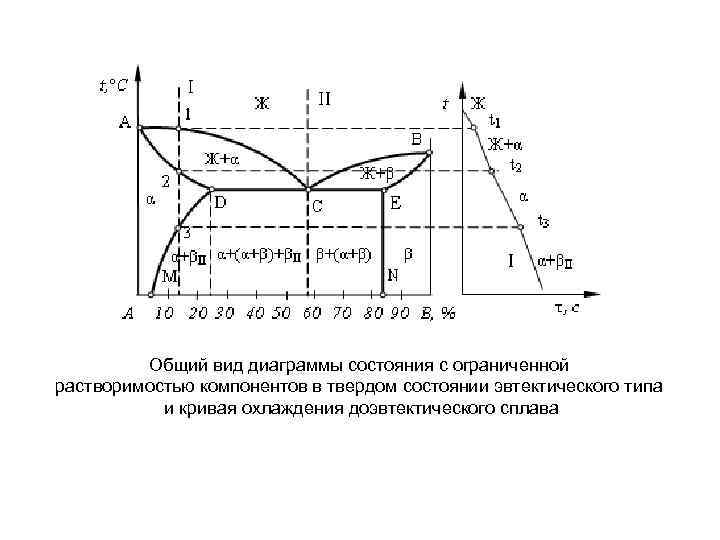 Общий вид диаграммы состояния с ограниченной растворимостью компонентов в твердом состоянии эвтектического типа и кривая охлаждения доэвтектического сплава
Общий вид диаграммы состояния с ограниченной растворимостью компонентов в твердом состоянии эвтектического типа и кривая охлаждения доэвтектического сплава
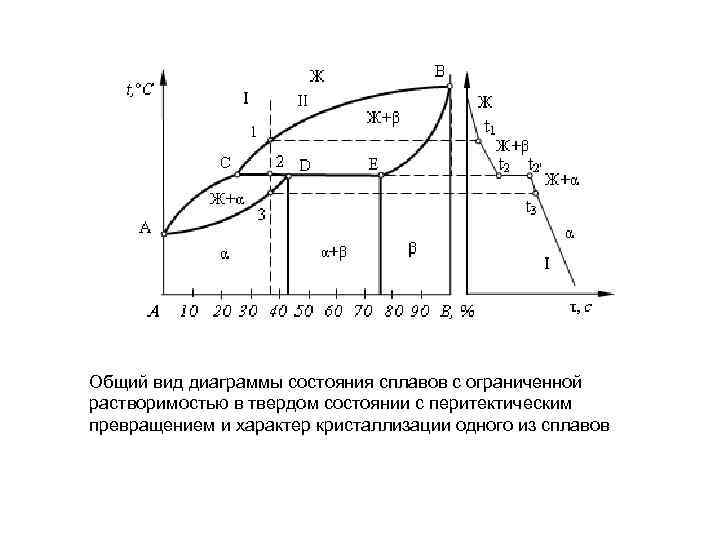 Общий вид диаграммы состояния сплавов с ограниченной растворимостью в твердом состоянии с перитектическим превращением и характер кристаллизации одного из сплавов
Общий вид диаграммы состояния сплавов с ограниченной растворимостью в твердом состоянии с перитектическим превращением и характер кристаллизации одного из сплавов
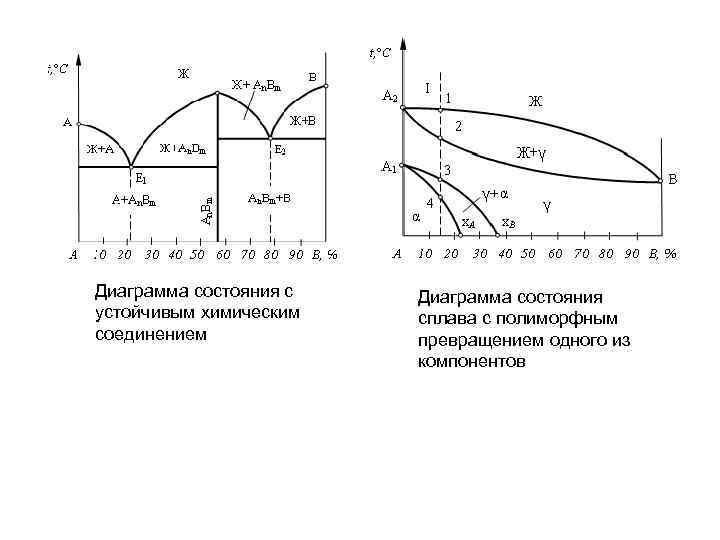 Диаграмма состояния с устойчивым химическим соединением Диаграмма состояния сплава с полиморфным превращением одного из компонентов
Диаграмма состояния с устойчивым химическим соединением Диаграмма состояния сплава с полиморфным превращением одного из компонентов
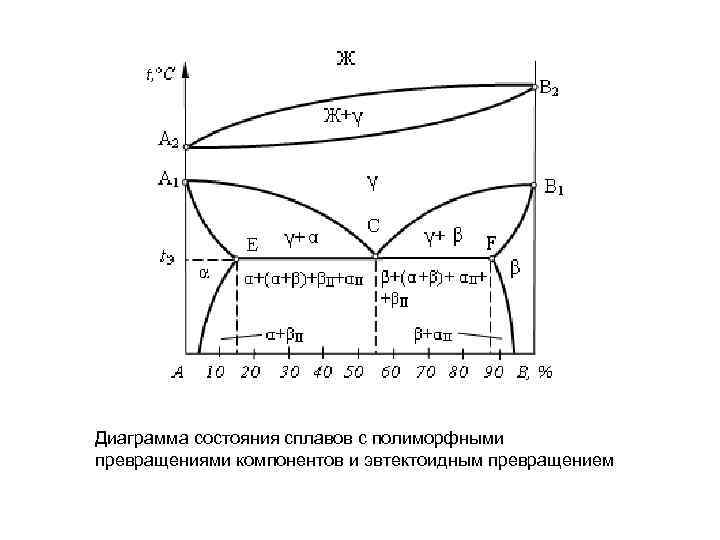 Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением
Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением
 Так как вид диаграммы, также как и свойства сплава, зависит от того, какие соединения или какие фазы образовали компоненты сплава, то между ними должна существовать определенная связь. Эта зависимость установлена Курнаковым Н. С. 1. При образовании механических смесей свойства изменяются по линейному закону. Значения характеристик свойств сплава находятся в интервале между характеристиками чистых компонентов. 2. При образовании твердых растворов с неограниченной растворимостью свойства сплавов изменяются по криволинейной зависимости, причем некоторые свойства, например, электросопротивление, могут значительно отличаться от свойств компонентов. 3. При образовании твердых растворов с ограниченной растворимостью свойства в интервале концентраций, отвечающих однофазным твердым растворам, изменяются по криволинейному закону, а в двухфазной области – по линейному закону. Причем крайние точки на прямой являются свойствами чистых фаз, предельно насыщенных твердых растворов, образующих данную смесь. 4. При образовании химических соединений концентрация химического соединения отвечает максимуму на кривой. Эта точка перелома, соответствующая химическому соединению, называется сингулярной точкой.
Так как вид диаграммы, также как и свойства сплава, зависит от того, какие соединения или какие фазы образовали компоненты сплава, то между ними должна существовать определенная связь. Эта зависимость установлена Курнаковым Н. С. 1. При образовании механических смесей свойства изменяются по линейному закону. Значения характеристик свойств сплава находятся в интервале между характеристиками чистых компонентов. 2. При образовании твердых растворов с неограниченной растворимостью свойства сплавов изменяются по криволинейной зависимости, причем некоторые свойства, например, электросопротивление, могут значительно отличаться от свойств компонентов. 3. При образовании твердых растворов с ограниченной растворимостью свойства в интервале концентраций, отвечающих однофазным твердым растворам, изменяются по криволинейному закону, а в двухфазной области – по линейному закону. Причем крайние точки на прямой являются свойствами чистых фаз, предельно насыщенных твердых растворов, образующих данную смесь. 4. При образовании химических соединений концентрация химического соединения отвечает максимуму на кривой. Эта точка перелома, соответствующая химическому соединению, называется сингулярной точкой.
 Свойства Т, о. С Типы диаграмм состояния и их связь с механическими свойствами сплавов
Свойства Т, о. С Типы диаграмм состояния и их связь с механическими свойствами сплавов
 Свойства материалов. Способность металла сопротивляться воздействию внешних сил характеризуется механическими свойствами. Поэтому при выборе металла для изготовления деталей машин необходимо знать его механические свойства: прочность, упругость, пластичность, ударную вязкость и выносливость. Эти свойства определяют по результатам механических испытаний, при которых металлы подвергаются воздействию внешних сил (нагрузок). Внешние силы могут быть статическими, динамическими или циклическими (знакопеременными). К основным физико химическим свойствам материалов относятся: температура плавления, плотность, электро и теплопроводность, коэффициенты линейного и объемного расширения и др. Технологические свойства металлов и сплавов характеризуют их способность поддаваться различным видам горячей и холодной обработки (получению деталей литьем, обработкой давлением, сваркой и резанием). Литейные свойства характеризуют способность металла или сплава заполнять литейную форму, обеспечивать получение отливки заданных размеров и конфигурации без пор и трещин во всех ее частях. К основным литейным свойствам сплавов относят: жидкотекучесть, усадку сплавов, склонность к образованию трещин, газопоглощение, ликвацию.
Свойства материалов. Способность металла сопротивляться воздействию внешних сил характеризуется механическими свойствами. Поэтому при выборе металла для изготовления деталей машин необходимо знать его механические свойства: прочность, упругость, пластичность, ударную вязкость и выносливость. Эти свойства определяют по результатам механических испытаний, при которых металлы подвергаются воздействию внешних сил (нагрузок). Внешние силы могут быть статическими, динамическими или циклическими (знакопеременными). К основным физико химическим свойствам материалов относятся: температура плавления, плотность, электро и теплопроводность, коэффициенты линейного и объемного расширения и др. Технологические свойства металлов и сплавов характеризуют их способность поддаваться различным видам горячей и холодной обработки (получению деталей литьем, обработкой давлением, сваркой и резанием). Литейные свойства характеризуют способность металла или сплава заполнять литейную форму, обеспечивать получение отливки заданных размеров и конфигурации без пор и трещин во всех ее частях. К основным литейным свойствам сплавов относят: жидкотекучесть, усадку сплавов, склонность к образованию трещин, газопоглощение, ликвацию.
 Обрабатываемость давлением оценивается различными технологическими пробами (на осадку, вытяжку сферической лунки и т. д. ), характеристиками пластичности, твердости. Среди характеристик обрабатываемости давлением используют понятие ковкости. Ковкость – способность металла или сплава деформироваться с минимальным сопротивлением под действием внешней приложенной нагрузки и принимать заданную форму. Ковкость зависит от многих внешних факторов, в частности, от температуры нагревания и схемы напряженного состояния. Свариваемостью называют способность материала образовывать неразъемные соединения с комплексом свойств, обеспечивающих работоспособность конструкции. Обрабатываемостью называют свойство металла поддаваться обработке резанием. Критериями обрабатываемости являются параметры режимов резания и качество поверхностного слоя.
Обрабатываемость давлением оценивается различными технологическими пробами (на осадку, вытяжку сферической лунки и т. д. ), характеристиками пластичности, твердости. Среди характеристик обрабатываемости давлением используют понятие ковкости. Ковкость – способность металла или сплава деформироваться с минимальным сопротивлением под действием внешней приложенной нагрузки и принимать заданную форму. Ковкость зависит от многих внешних факторов, в частности, от температуры нагревания и схемы напряженного состояния. Свариваемостью называют способность материала образовывать неразъемные соединения с комплексом свойств, обеспечивающих работоспособность конструкции. Обрабатываемостью называют свойство металла поддаваться обработке резанием. Критериями обрабатываемости являются параметры режимов резания и качество поверхностного слоя.
 Механические свойства материалов Механические свойства металлов определяют поведение материала при деформации и разрушении от действия внешних нагрузок. В зависимости от условий нагружения механические свой ства могут определяться при: • статическом нагружении, когда нагрузка на образец возрастает медленно и плавно; • динамическом нагружении, когда нагрузка воз растает с большой скоростью имеет ударный характер; • повторно переменном или циклическом нагружении, когда нагрузка в процессе испытания многократно изменяется по величине или по величине и направлению. Отношение максимальных касательных напряжений τmax к максимальным нормальным напряжениям σmax, действующим в детали, зависит от способа нагружения и называется коэффициентом жесткости нагружения α:
Механические свойства материалов Механические свойства металлов определяют поведение материала при деформации и разрушении от действия внешних нагрузок. В зависимости от условий нагружения механические свой ства могут определяться при: • статическом нагружении, когда нагрузка на образец возрастает медленно и плавно; • динамическом нагружении, когда нагрузка воз растает с большой скоростью имеет ударный характер; • повторно переменном или циклическом нагружении, когда нагрузка в процессе испытания многократно изменяется по величине или по величине и направлению. Отношение максимальных касательных напряжений τmax к максимальным нормальным напряжениям σmax, действующим в детали, зависит от способа нагружения и называется коэффициентом жесткости нагружения α:
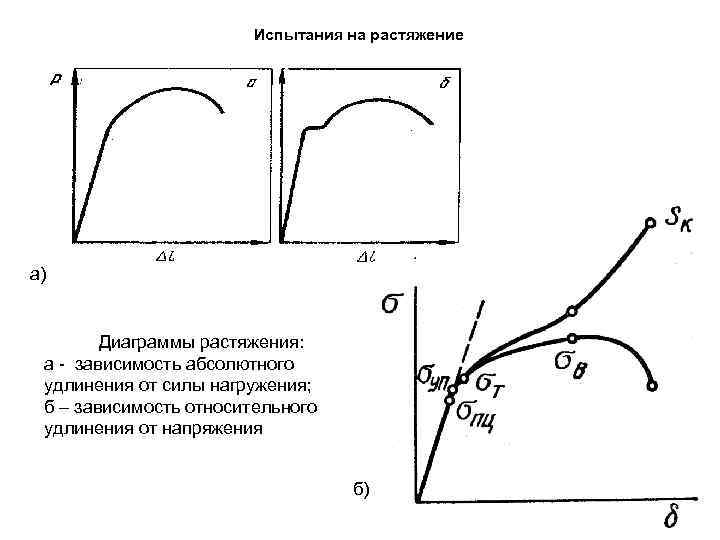 Испытания на растяжение а) Диаграммы растяжения: а зависимость абсолютного удлинения от силы нагружения; б – зависимость относительного удлинения от напряжения б)
Испытания на растяжение а) Диаграммы растяжения: а зависимость абсолютного удлинения от силы нагружения; б – зависимость относительного удлинения от напряжения б)
 Пластичность материала − это способность к значительной пластической деформации до окончательного разрушения. Прочность — способность материала сопротивляться разрушению под действием внутренних напряжений, возникающих под воздействием внешних сил. Участок до точки σпц на диаграмме растяжения соответствует упругой деформации материала, когда соблюдается закон Гука где Е − модуль упругости (модуль Юнга). Модуль упругости Е является константой материала, характеризующей его жесткость. Е = σ/δ = tg α, Напряжение, соответствующее предельной упругой деформа ции, называют пределом пропорциональности: σпц= Pпц/Fо, где Pпц нагрузка; Fо площадь поперечного сечения образца, мм. В СИ σпц выражается в МПа (1 кгс/мм 2~10 МПа). Пределом упругости считают напряжение, при котором остаточная деформация очень мала (например, 0, 05 % или меньше).
Пластичность материала − это способность к значительной пластической деформации до окончательного разрушения. Прочность — способность материала сопротивляться разрушению под действием внутренних напряжений, возникающих под воздействием внешних сил. Участок до точки σпц на диаграмме растяжения соответствует упругой деформации материала, когда соблюдается закон Гука где Е − модуль упругости (модуль Юнга). Модуль упругости Е является константой материала, характеризующей его жесткость. Е = σ/δ = tg α, Напряжение, соответствующее предельной упругой деформа ции, называют пределом пропорциональности: σпц= Pпц/Fо, где Pпц нагрузка; Fо площадь поперечного сечения образца, мм. В СИ σпц выражается в МПа (1 кгс/мм 2~10 МПа). Пределом упругости считают напряжение, при котором остаточная деформация очень мала (например, 0, 05 % или меньше).
 Напряжение σ0, 2, вызывающее остаточную деформацию δ=0, 2 %, принято называть условным пределом текучести: σ0, 2= P 0, 2/Fо, где Р 0, 2 сила, действующая на образец; Fo исходное сечение образца. Напряжение, соответствующее значительной пластической деформируется без увеличения нагрузки (напряжения), называют физическим пределом текучести и обозначают σт. Напряжение σв, соответствующее началу большой местной пластической деформации, называется пределом прочности или временным сопротивлением разрушению: σв= Рв/ Fo, где Рв нагрузка, соответствующая пределу прочности; Fo исходное поперечное сечение образца. Относительное удлинение δ представляет отношение прироста длины образца после растяжения к первоначальной длине (%): Относительное сужение ψ представляет отношение уменьшения площади поперечного сечения образца к первоначальной площади поперечного сечения (%)
Напряжение σ0, 2, вызывающее остаточную деформацию δ=0, 2 %, принято называть условным пределом текучести: σ0, 2= P 0, 2/Fо, где Р 0, 2 сила, действующая на образец; Fo исходное сечение образца. Напряжение, соответствующее значительной пластической деформируется без увеличения нагрузки (напряжения), называют физическим пределом текучести и обозначают σт. Напряжение σв, соответствующее началу большой местной пластической деформации, называется пределом прочности или временным сопротивлением разрушению: σв= Рв/ Fo, где Рв нагрузка, соответствующая пределу прочности; Fo исходное поперечное сечение образца. Относительное удлинение δ представляет отношение прироста длины образца после растяжения к первоначальной длине (%): Относительное сужение ψ представляет отношение уменьшения площади поперечного сечения образца к первоначальной площади поперечного сечения (%)
 Дислокационный механизм образования трещины
Дислокационный механизм образования трещины
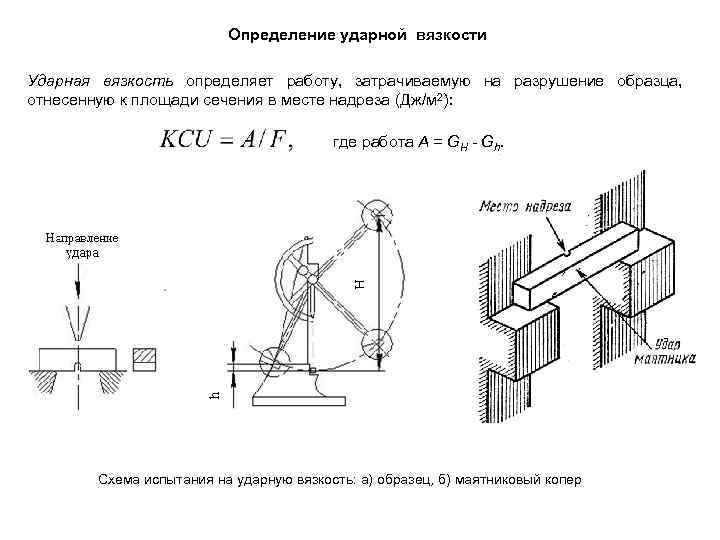 Определение ударной вязкости Ударная вязкость определяет работу, затрачиваемую на разрушение образца, отнесенную к площади сечения в месте надреза (Дж/м 2): где работа А = GH - Gh. Схема испытания на ударную вязкость: а) образец, б) маятниковый копер
Определение ударной вязкости Ударная вязкость определяет работу, затрачиваемую на разрушение образца, отнесенную к площади сечения в месте надреза (Дж/м 2): где работа А = GH - Gh. Схема испытания на ударную вязкость: а) образец, б) маятниковый копер
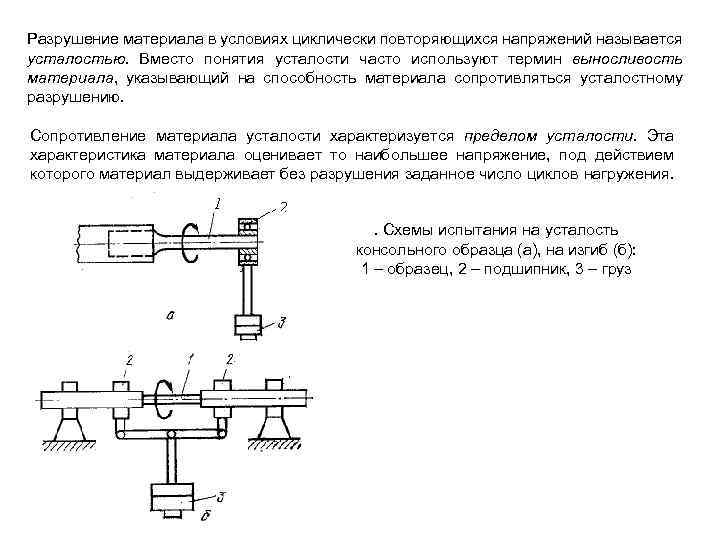 Разрушение материала в условиях циклически повторяющихся напряжений называется усталостью. Вместо понятия усталости часто используют термин выносливость материала, указывающий на способность материала сопротивляться усталостному разрушению. Сопротивление материала усталости характеризуется пределом усталости. Эта характеристика материала оценивает то наибольшее напряжение, под действием которого материал выдерживает без разрушения заданное число циклов нагружения. . Схемы испытания на усталость консольного образца (а), на изгиб (б): 1 – образец, 2 – подшипник, 3 – груз
Разрушение материала в условиях циклически повторяющихся напряжений называется усталостью. Вместо понятия усталости часто используют термин выносливость материала, указывающий на способность материала сопротивляться усталостному разрушению. Сопротивление материала усталости характеризуется пределом усталости. Эта характеристика материала оценивает то наибольшее напряжение, под действием которого материал выдерживает без разрушения заданное число циклов нагружения. . Схемы испытания на усталость консольного образца (а), на изгиб (б): 1 – образец, 2 – подшипник, 3 – груз
 Методы определение твердости Твердость – способность материала сопротивляться проникновению в него другого, более твердого, материала. 1. Определение твердости по Бринеллю Схема испытания твердости методом Бринелля где НВ – число твердости по Бринеллю; Р – нагрузка, Н; F – шаровая поверхность отпечатка (сегмента), мм 2. σВ(МПа) = 3, 3 HRC =0, 33 НВ – для стали; σВ = 0, 45 НВ – для медных сплавов; σВ = 0, 35 НВ – для алюминиевых сплавов.
Методы определение твердости Твердость – способность материала сопротивляться проникновению в него другого, более твердого, материала. 1. Определение твердости по Бринеллю Схема испытания твердости методом Бринелля где НВ – число твердости по Бринеллю; Р – нагрузка, Н; F – шаровая поверхность отпечатка (сегмента), мм 2. σВ(МПа) = 3, 3 HRC =0, 33 НВ – для стали; σВ = 0, 45 НВ – для медных сплавов; σВ = 0, 35 НВ – для алюминиевых сплавов.
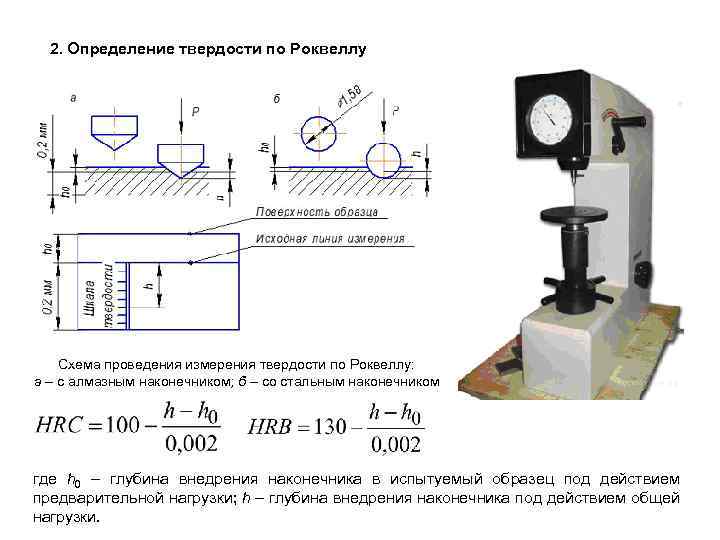 2. Определение твердости по Роквеллу Схема проведения измерения твердости по Роквеллу: а – с алмазным наконечником; б – со стальным наконечником где h 0 – глубина внедрения наконечника в испытуемый образец под действием предварительной нагрузки; h – глубина внедрения наконечника под действием общей нагрузки.
2. Определение твердости по Роквеллу Схема проведения измерения твердости по Роквеллу: а – с алмазным наконечником; б – со стальным наконечником где h 0 – глубина внедрения наконечника в испытуемый образец под действием предварительной нагрузки; h – глубина внедрения наконечника под действием общей нагрузки.
 3. Определение твердости по Виккерсу Схема измерения по Виккерсу где Р – нагрузка; a – угол между противоположными гранями пирамиды при вершине (136º), d – среднее арифметическое значение обеих диагоналей отпечатка после снятия нагрузки, мм.
3. Определение твердости по Виккерсу Схема измерения по Виккерсу где Р – нагрузка; a – угол между противоположными гранями пирамиды при вершине (136º), d – среднее арифметическое значение обеих диагоналей отпечатка после снятия нагрузки, мм.
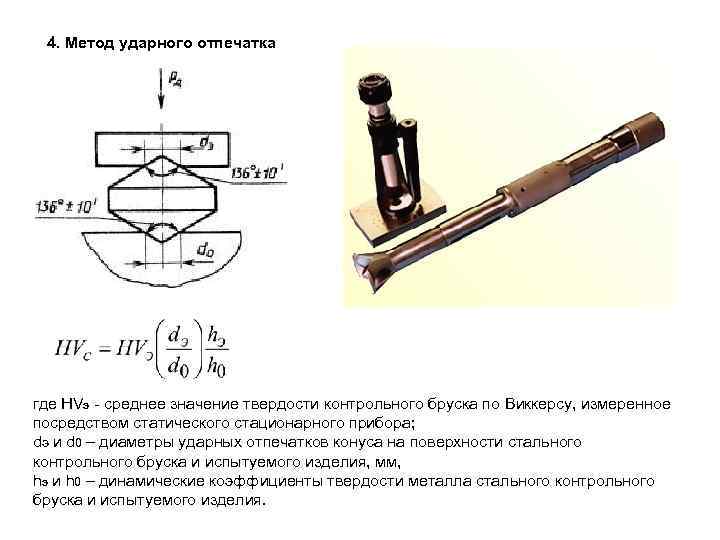 4. Метод ударного отпечатка где HVэ среднее значение твердости контрольного бруска по Виккерсу, измеренное посредством статического стационарного прибора; dэ и d 0 – диаметры ударных отпечатков конуса на поверхности стального контрольного бруска и испытуемого изделия, мм, hэ и h 0 – динамические коэффициенты твердости металла стального контрольного бруска и испытуемого изделия.
4. Метод ударного отпечатка где HVэ среднее значение твердости контрольного бруска по Виккерсу, измеренное посредством статического стационарного прибора; dэ и d 0 – диаметры ударных отпечатков конуса на поверхности стального контрольного бруска и испытуемого изделия, мм, hэ и h 0 – динамические коэффициенты твердости металла стального контрольного бруска и испытуемого изделия.
 4. Определение твердости царапаньем Набор напильников для измерения твердости металлов Твёрдость по Моосу Эталонный минерал 1 Тальк (Mg 3 Si 4 O 10(OH)2) Царапается ногтем Графит 2 Гипс (Ca. SO 4· 2 H 2 O) Царапается ногтем Слюда 3 Кальцит (Ca. CO 3) Царапается медью Биотит, золото, серебро 4 Флюорит (Ca. F 2) Легко царапается ножом, стеклом Доломит 5 Апатит (Ca 5(PO 4)3(OH-, Cl-, F-)) С усилием царапается ножом, оконным стеклом Гематит, лазурит 6 Ортоклаз (KAl. Si 3 O 8) Царапает стекло. Обрабатывается напильником Опал, рутил 7 Кварц (Si. O 2) Поддаётся обработке алмазом, царапает стекло Гранат, турмалин 8 Топаз (Al 2 Si. O 4(OH-, F-)2) Поддаётся обработке алмазом, царапает стекло Берилл, шпинель, аквамарин Корунд (Al 2 O 3) Поддаётся обработке алмазом, царапает стекло Сапфир, рубин, карбид вольфрама Алмаз (C) Режет стекло Эльбор 9 10 Другие минералы с аналогичной твердостью Обрабатываемость
4. Определение твердости царапаньем Набор напильников для измерения твердости металлов Твёрдость по Моосу Эталонный минерал 1 Тальк (Mg 3 Si 4 O 10(OH)2) Царапается ногтем Графит 2 Гипс (Ca. SO 4· 2 H 2 O) Царапается ногтем Слюда 3 Кальцит (Ca. CO 3) Царапается медью Биотит, золото, серебро 4 Флюорит (Ca. F 2) Легко царапается ножом, стеклом Доломит 5 Апатит (Ca 5(PO 4)3(OH-, Cl-, F-)) С усилием царапается ножом, оконным стеклом Гематит, лазурит 6 Ортоклаз (KAl. Si 3 O 8) Царапает стекло. Обрабатывается напильником Опал, рутил 7 Кварц (Si. O 2) Поддаётся обработке алмазом, царапает стекло Гранат, турмалин 8 Топаз (Al 2 Si. O 4(OH-, F-)2) Поддаётся обработке алмазом, царапает стекло Берилл, шпинель, аквамарин Корунд (Al 2 O 3) Поддаётся обработке алмазом, царапает стекло Сапфир, рубин, карбид вольфрама Алмаз (C) Режет стекло Эльбор 9 10 Другие минералы с аналогичной твердостью Обрабатываемость
 5. Определение твердости методом отскока (твёрдость по Шору) Твердость по Шору обозначается HSx, где H ‒ Hardness, S ‒ Shore и x ‒ латинская буква, обозначающая тип шкалы, использованной при измерении. Пример обозначения твердости данным методом – 85 HSh. D, что означает 85 единиц твердости по шкале D. Универсальный электронный динамический склероскоп
5. Определение твердости методом отскока (твёрдость по Шору) Твердость по Шору обозначается HSx, где H ‒ Hardness, S ‒ Shore и x ‒ латинская буква, обозначающая тип шкалы, использованной при измерении. Пример обозначения твердости данным методом – 85 HSh. D, что означает 85 единиц твердости по шкале D. Универсальный электронный динамический склероскоп
 6. Определение твердости методом вдавливания (твёрдость по Шору) Аналоговый дюрометр Шора Твердость по Шору А/15: 45, где A ‒ тип дюрометра, 15 ‒ время в секундах от момента приведения опорной поверхности в тесный контакт с образцом до момента снятия показания, 45 ‒ показания. Твердость по Шору D/1: 60 означает показание 60, полученное с помощью дюрометра типа D в течение 1 с или от максимального показания.
6. Определение твердости методом вдавливания (твёрдость по Шору) Аналоговый дюрометр Шора Твердость по Шору А/15: 45, где A ‒ тип дюрометра, 15 ‒ время в секундах от момента приведения опорной поверхности в тесный контакт с образцом до момента снятия показания, 45 ‒ показания. Твердость по Шору D/1: 60 означает показание 60, полученное с помощью дюрометра типа D в течение 1 с или от максимального показания.
 7. Ультразвуковой метод измерения твердости Этот метод измерения твердости называют методом ультразвукового контактного импеданса. Алмазную пирамидку прижимают к исследуемому образцу при постоянном усилии и возбуждают упругие колебания. Чем меньше твердость образца, тем больше индентор продавливает его поверхность, тем сильнее гасится звуковая волна. Прибор излучает звуковые волны, а затем регистрирует время их прохождения через исследуемый образец и преобразовывает полученные данные в значение твёрдости
7. Ультразвуковой метод измерения твердости Этот метод измерения твердости называют методом ультразвукового контактного импеданса. Алмазную пирамидку прижимают к исследуемому образцу при постоянном усилии и возбуждают упругие колебания. Чем меньше твердость образца, тем больше индентор продавливает его поверхность, тем сильнее гасится звуковая волна. Прибор излучает звуковые волны, а затем регистрирует время их прохождения через исследуемый образец и преобразовывает полученные данные в значение твёрдости
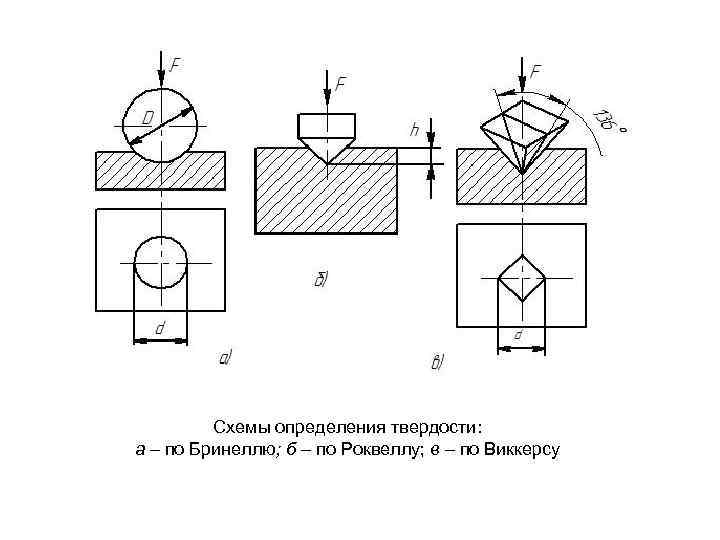 Схемы определения твердости: а – по Бринеллю; б – по Роквеллу; в – по Виккерсу
Схемы определения твердости: а – по Бринеллю; б – по Роквеллу; в – по Виккерсу
 В твердых телах различают упругую деформацию (исчезающую после устранения воздействия, вызвавшего ее) и пластическую (оставшуюся после удаления нагрузки). Схемы пластического сдвига: а) одновременным смещением одной части кристалла относительно другой; б) изменение в расположении атомов в процессе перемещения дислокации Схема пластической деформации скольжением (а) и двойникованием (б).
В твердых телах различают упругую деформацию (исчезающую после устранения воздействия, вызвавшего ее) и пластическую (оставшуюся после удаления нагрузки). Схемы пластического сдвига: а) одновременным смещением одной части кристалла относительно другой; б) изменение в расположении атомов в процессе перемещения дислокации Схема пластической деформации скольжением (а) и двойникованием (б).
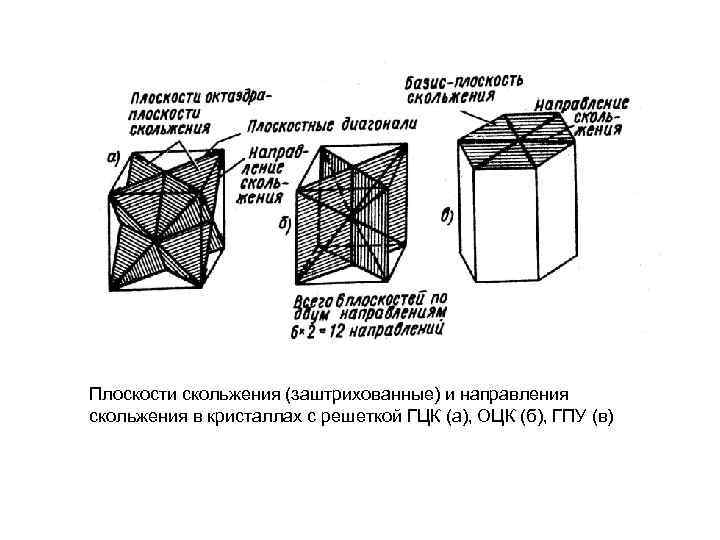 Плоскости скольжения (заштрихованные) и направления скольжения в кристаллах с решеткой ГЦК (а), ОЦК (б), ГПУ (в)
Плоскости скольжения (заштрихованные) и направления скольжения в кристаллах с решеткой ГЦК (а), ОЦК (б), ГПУ (в)
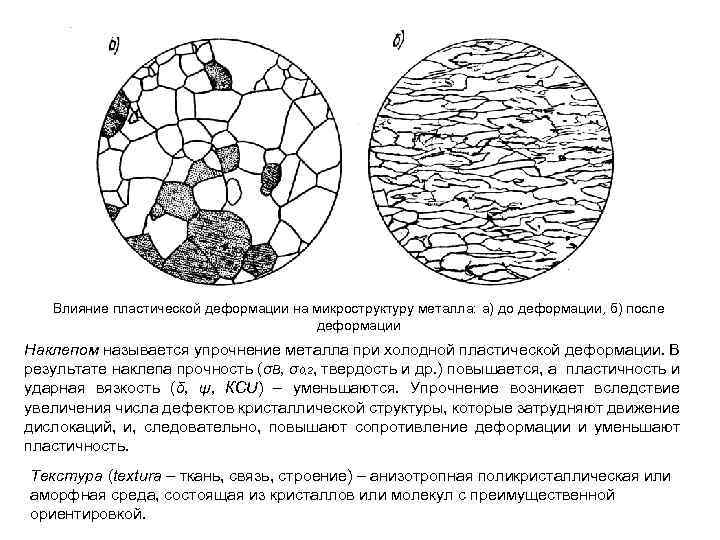 Влияние пластической деформации на микроструктуру металла: а) до деформации, б) после деформации Наклепом называется упрочнение металла при холодной пластической деформации. В результате наклепа прочность (σВ, σ0, 2, твердость и др. ) повышается, а пластичность и ударная вязкость (δ, ψ, КСU) – уменьшаются. Упрочнение возникает вследствие увеличения числа дефектов кристаллической структуры, которые затрудняют движение дислокаций, и, следовательно, повышают сопротивление деформации и уменьшают пластичность. Текстура (textura – ткань, связь, строение) – анизотропная поликристаллическая или аморфная среда, состоящая из кристаллов или молекул с преимущественной ориентировкой.
Влияние пластической деформации на микроструктуру металла: а) до деформации, б) после деформации Наклепом называется упрочнение металла при холодной пластической деформации. В результате наклепа прочность (σВ, σ0, 2, твердость и др. ) повышается, а пластичность и ударная вязкость (δ, ψ, КСU) – уменьшаются. Упрочнение возникает вследствие увеличения числа дефектов кристаллической структуры, которые затрудняют движение дислокаций, и, следовательно, повышают сопротивление деформации и уменьшают пластичность. Текстура (textura – ткань, связь, строение) – анизотропная поликристаллическая или аморфная среда, состоящая из кристаллов или молекул с преимущественной ориентировкой.
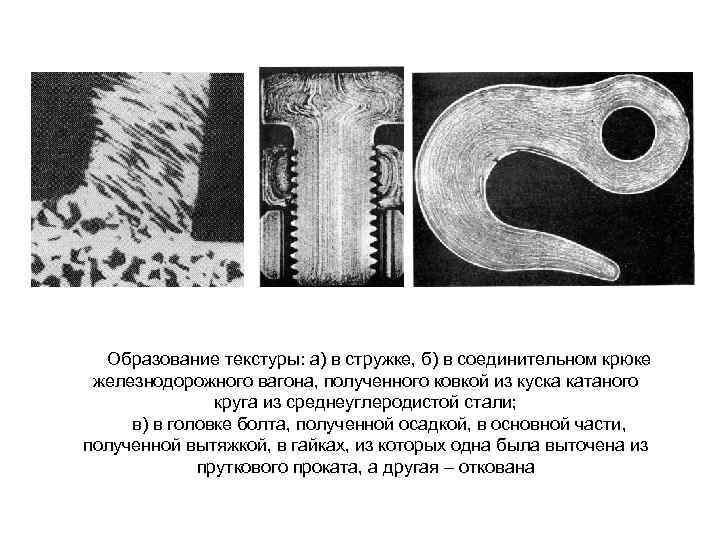 Образование текстуры: а) в стружке, б) в соединительном крюке железнодорожного вагона, полученного ковкой из куска катаного круга из среднеуглеродистой стали; в) в головке болта, полученной осадкой, в основной части, полученной вытяжкой, в гайках, из которых одна была выточена из пруткового проката, а другая – откована
Образование текстуры: а) в стружке, б) в соединительном крюке железнодорожного вагона, полученного ковкой из куска катаного круга из среднеуглеродистой стали; в) в головке болта, полученной осадкой, в основной части, полученной вытяжкой, в гайках, из которых одна была выточена из пруткового проката, а другая – откована
 а) зарождение новых мелких недеформированных зерен в) вторичная рекристаллизация Рекристаллизация холоднодеформированной стали б) конец первичной рекристаллизации
а) зарождение новых мелких недеформированных зерен в) вторичная рекристаллизация Рекристаллизация холоднодеформированной стали б) конец первичной рекристаллизации
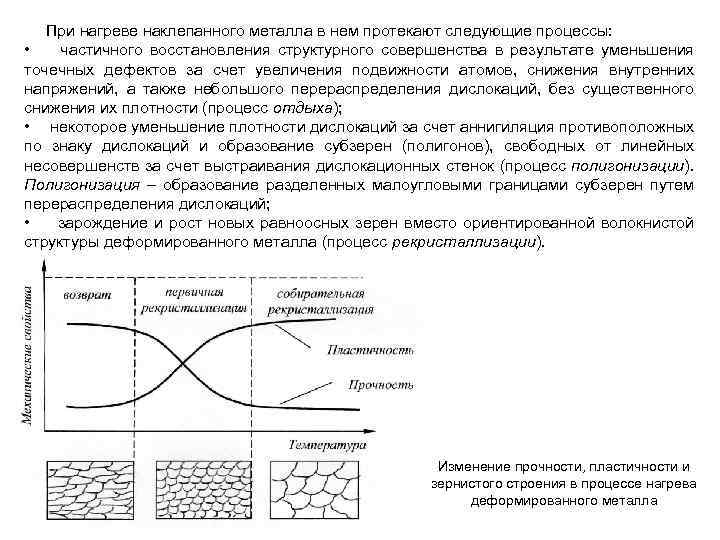 При нагреве наклепанного металла в нем протекают следующие процессы: • частичного восстановления структурного совершенства в результате уменьшения точечных дефектов за счет увеличения подвижности атомов, снижения внутренних напряжений, а также небольшого перераспределения дислокаций, без существенного снижения их плотности (процесс отдыха); • некоторое уменьшение плотности дислокаций за счет аннигиляция противоположных по знаку дислокаций и образование субзерен (полигонов), свободных от линейных несовершенств за счет выстраивания дислокационных стенок (процесс полигонизации). Полигонизация – образование разделенных малоугловыми границами субзерен путем перераспределения дислокаций; • зарождение и рост новых равноосных зерен вместо ориентированной волокнистой структуры деформированного металла (процесс рекристаллизации). Изменение прочности, пластичности и зернистого строения в процессе нагрева деформированного металла
При нагреве наклепанного металла в нем протекают следующие процессы: • частичного восстановления структурного совершенства в результате уменьшения точечных дефектов за счет увеличения подвижности атомов, снижения внутренних напряжений, а также небольшого перераспределения дислокаций, без существенного снижения их плотности (процесс отдыха); • некоторое уменьшение плотности дислокаций за счет аннигиляция противоположных по знаку дислокаций и образование субзерен (полигонов), свободных от линейных несовершенств за счет выстраивания дислокационных стенок (процесс полигонизации). Полигонизация – образование разделенных малоугловыми границами субзерен путем перераспределения дислокаций; • зарождение и рост новых равноосных зерен вместо ориентированной волокнистой структуры деформированного металла (процесс рекристаллизации). Изменение прочности, пластичности и зернистого строения в процессе нагрева деформированного металла
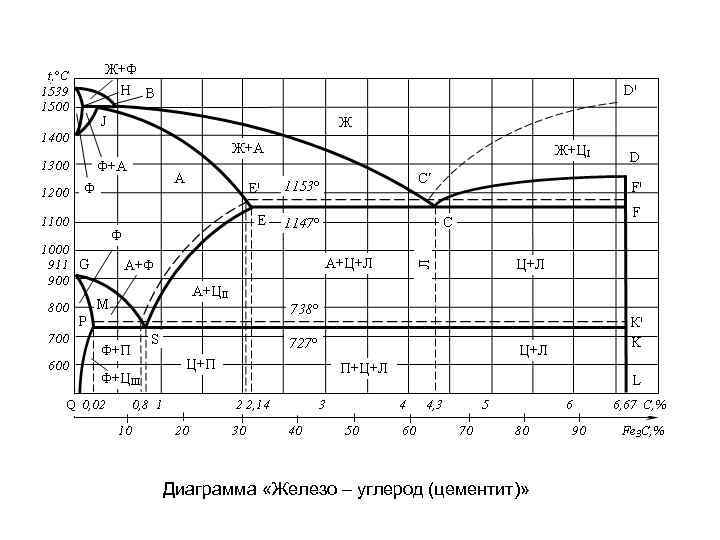 Диаграмма «Железо – углерод (цементит)»
Диаграмма «Железо – углерод (цементит)»
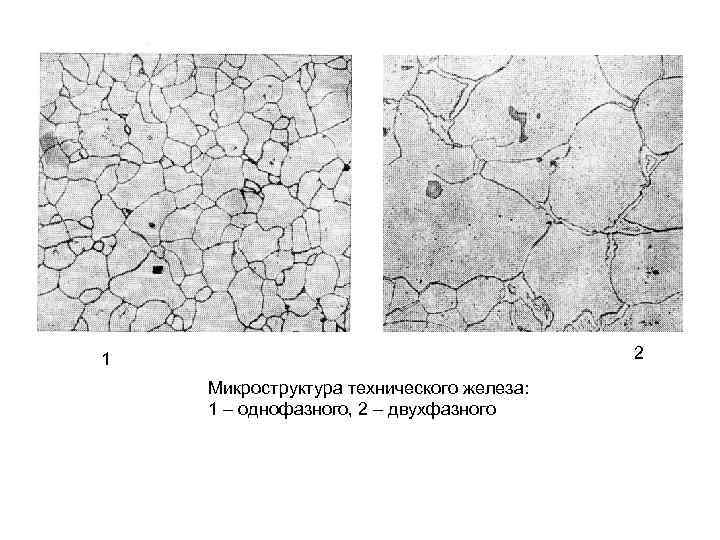 2 1 Микроструктура технического железа: 1 – однофазного, 2 – двухфазного
2 1 Микроструктура технического железа: 1 – однофазного, 2 – двухфазного
 а) б) Микроструктура доэвтектоидной стали: а) сталь 25; б) сталь 45
а) б) Микроструктура доэвтектоидной стали: а) сталь 25; б) сталь 45
 Микроструктура аустенита
Микроструктура аустенита
 а) Микроструктура эвтектоидной (а) и заэвтектоидной (б) стали б)
а) Микроструктура эвтектоидной (а) и заэвтектоидной (б) стали б)
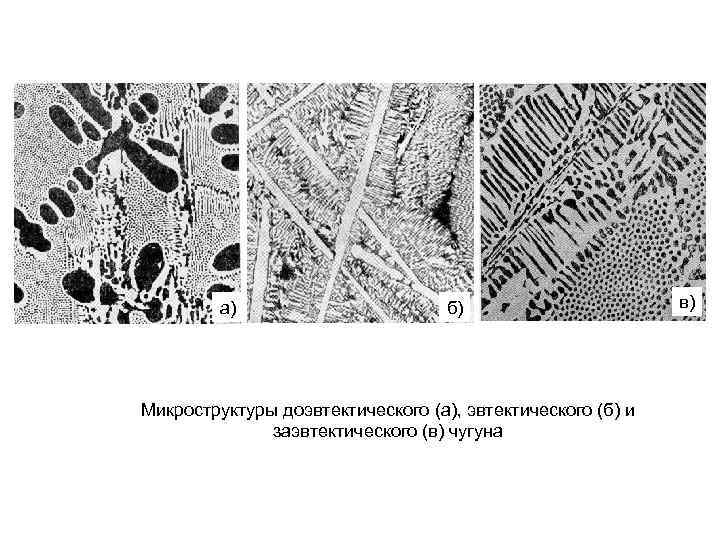 а) б) Микроструктуры доэвтектического (а), эвтектического (б) и заэвтектического (в) чугуна в)
а) б) Микроструктуры доэвтектического (а), эвтектического (б) и заэвтектического (в) чугуна в)
 Расшифруйте следующие марки стали: 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, сталь 2 кп, 40 ХН 2 МА, 35, 70 С 2 ХАБ, А 12, А 40 Г, сталь 4 сп, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
Расшифруйте следующие марки стали: 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, сталь 2 кп, 40 ХН 2 МА, 35, 70 С 2 ХАБ, А 12, А 40 Г, сталь 4 сп, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
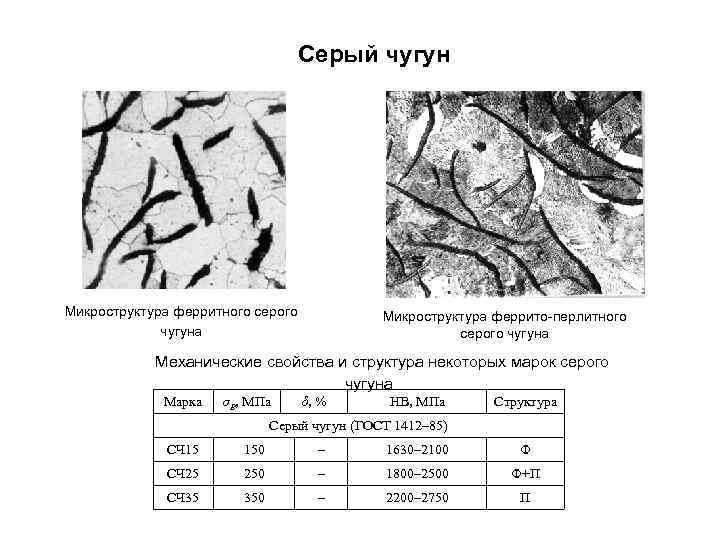 Серый чугун Микроструктура ферритного серого чугуна Микроструктура феррито перлитного серого чугуна Механические свойства и структура некоторых марок серого чугуна Марка σВ, МПа δ, % НВ, МПа Структура Серый чугун (ГОСТ 1412– 85) СЧ 15 150 – 1630– 2100 Ф СЧ 25 250 – 1800– 2500 Ф+П СЧ 35 350 – 2200– 2750 П
Серый чугун Микроструктура ферритного серого чугуна Микроструктура феррито перлитного серого чугуна Механические свойства и структура некоторых марок серого чугуна Марка σВ, МПа δ, % НВ, МПа Структура Серый чугун (ГОСТ 1412– 85) СЧ 15 150 – 1630– 2100 Ф СЧ 25 250 – 1800– 2500 Ф+П СЧ 35 350 – 2200– 2750 П
 Высокопрочный чугун Микроструктура феррито перлитного высокопрочного чугуна Микроструктура ферритного высокопрочного чугуна Механические свойства и структура некоторых марок высокопрочного чугуна Марка σв, МПа δ, % НВ, МПа Структура Высокопрочный чугун (ГОСТ 7293– 85) ВЧ 35 350 22 1400– 1700 Ф ВЧ 45 450 10 1400– 2250 Ф+П ВЧ 60 600 3 1920– 2270 Ф+П ВЧ 80 800 2 2480– 3510 П
Высокопрочный чугун Микроструктура феррито перлитного высокопрочного чугуна Микроструктура ферритного высокопрочного чугуна Механические свойства и структура некоторых марок высокопрочного чугуна Марка σв, МПа δ, % НВ, МПа Структура Высокопрочный чугун (ГОСТ 7293– 85) ВЧ 35 350 22 1400– 1700 Ф ВЧ 45 450 10 1400– 2250 Ф+П ВЧ 60 600 3 1920– 2270 Ф+П ВЧ 80 800 2 2480– 3510 П
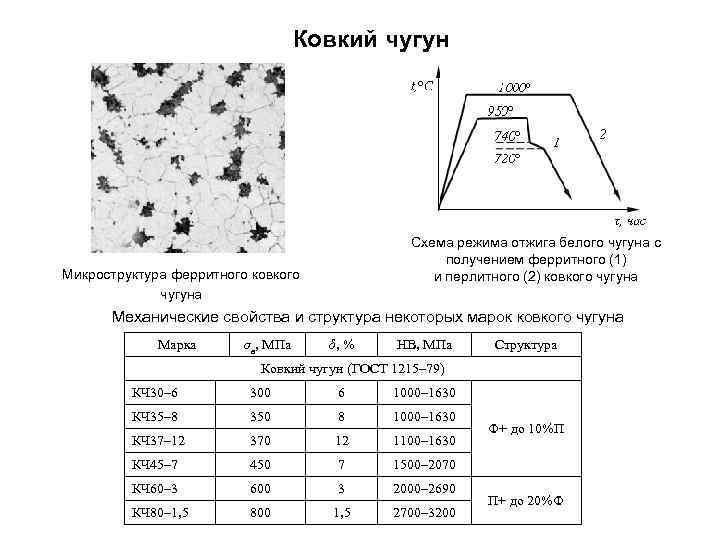 Ковкий чугун Схема режима отжига белого чугуна с получением ферритного (1) и перлитного (2) ковкого чугуна Микроструктура ферритного ковкого чугуна Механические свойства и структура некоторых марок ковкого чугуна Марка σв, МПа δ, % НВ, МПа Структура Ковкий чугун (ГОСТ 1215– 79) КЧ 30– 6 300 6 1000– 1630 КЧ 35– 8 350 8 1000– 1630 КЧ 37– 12 370 12 1100– 1630 КЧ 45– 7 450 7 1500– 2070 КЧ 60– 3 600 3 2000– 2690 КЧ 80– 1, 5 800 1, 5 2700– 3200 Ф+ до 10%П П+ до 20%Ф
Ковкий чугун Схема режима отжига белого чугуна с получением ферритного (1) и перлитного (2) ковкого чугуна Микроструктура ферритного ковкого чугуна Механические свойства и структура некоторых марок ковкого чугуна Марка σв, МПа δ, % НВ, МПа Структура Ковкий чугун (ГОСТ 1215– 79) КЧ 30– 6 300 6 1000– 1630 КЧ 35– 8 350 8 1000– 1630 КЧ 37– 12 370 12 1100– 1630 КЧ 45– 7 450 7 1500– 2070 КЧ 60– 3 600 3 2000– 2690 КЧ 80– 1, 5 800 1, 5 2700– 3200 Ф+ до 10%П П+ до 20%Ф
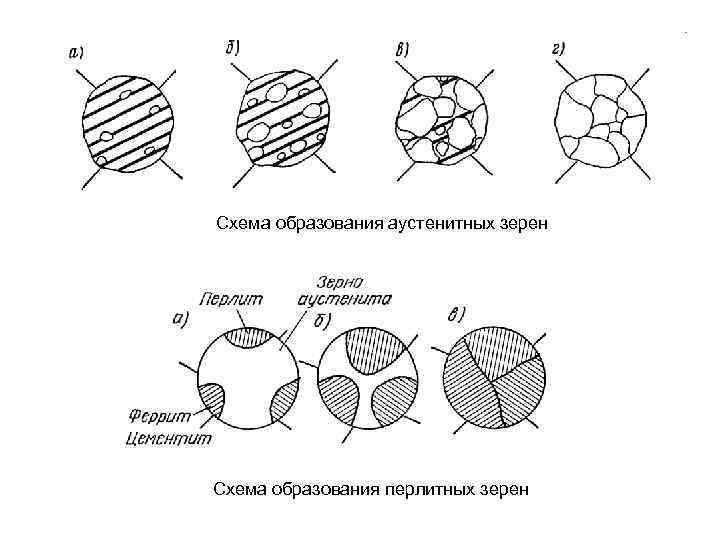 Схема образования аустенитных зерен Схема образования перлитных зерен
Схема образования аустенитных зерен Схема образования перлитных зерен
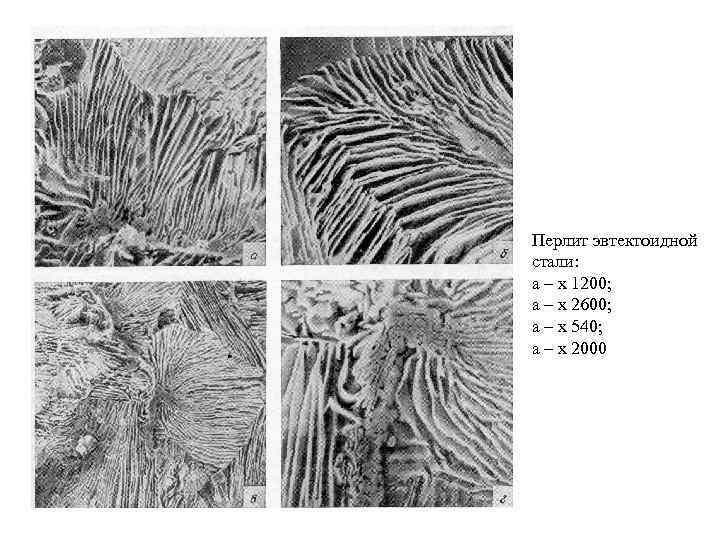 Перлит эвтектоидной стали: а – х 1200; а – х 2600; а – х 540; а – х 2000
Перлит эвтектоидной стали: а – х 1200; а – х 2600; а – х 540; а – х 2000
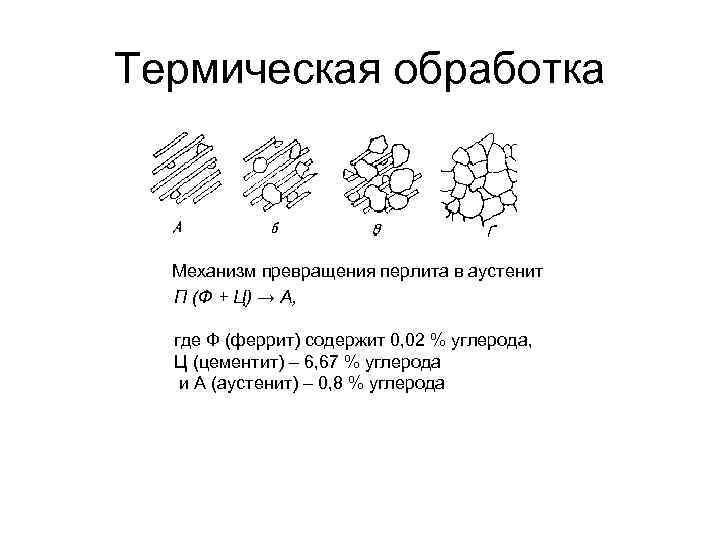 Термическая обработка Механизм превращения перлита в аустенит П (Ф + Ц) → А, где Ф (феррит) содержит 0, 02 % углерода, Ц (цементит) – 6, 67 % углерода и А (аустенит) – 0, 8 % углерода
Термическая обработка Механизм превращения перлита в аустенит П (Ф + Ц) → А, где Ф (феррит) содержит 0, 02 % углерода, Ц (цементит) – 6, 67 % углерода и А (аустенит) – 0, 8 % углерода
 а) б) Фотография (а) и схема (б) микроструктуры Видманштетта
а) б) Фотография (а) и схема (б) микроструктуры Видманштетта
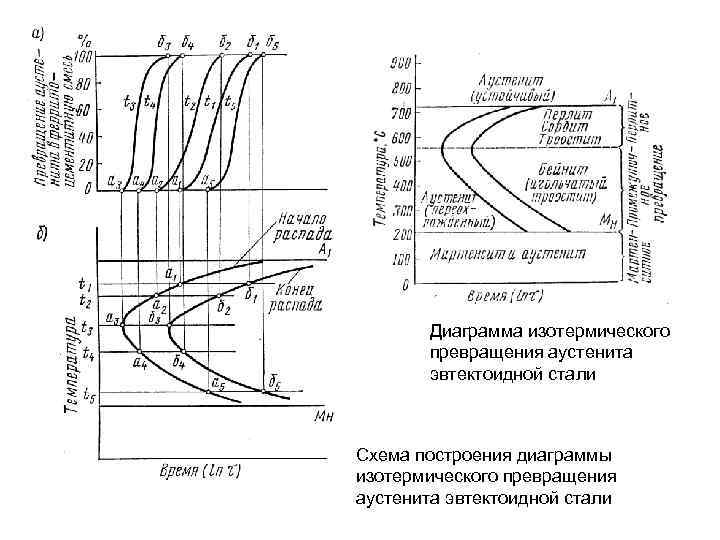 Диаграмма изотермического превращения аустенита эвтектоидной стали Схема построения диаграммы изотермического превращения аустенита эвтектоидной стали
Диаграмма изотермического превращения аустенита эвтектоидной стали Схема построения диаграммы изотермического превращения аустенита эвтектоидной стали
 Схема образования микроструктуры пластинчатого перлита Микроструктуры перлита, сорбита и троостита
Схема образования микроструктуры пластинчатого перлита Микроструктуры перлита, сорбита и троостита
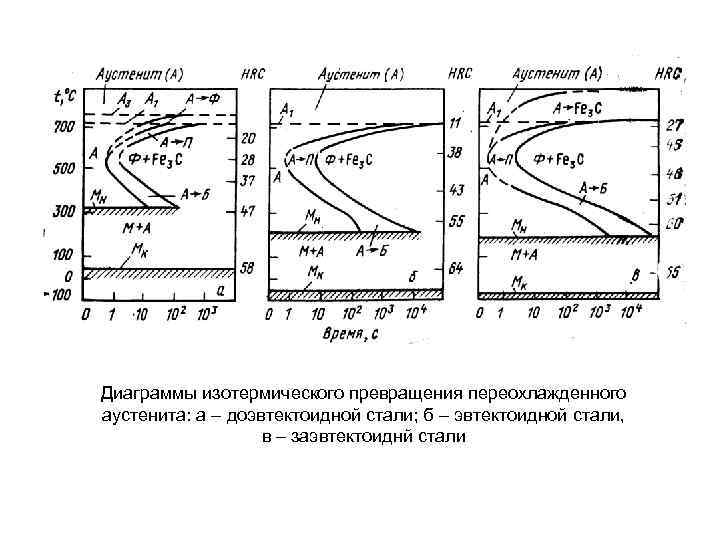 Диаграммы изотермического превращения переохлажденного аустенита: а – доэвтектоидной стали; б – эвтектоидной стали, в – заэвтектоиднй стали
Диаграммы изотермического превращения переохлажденного аустенита: а – доэвтектоидной стали; б – эвтектоидной стали, в – заэвтектоиднй стали
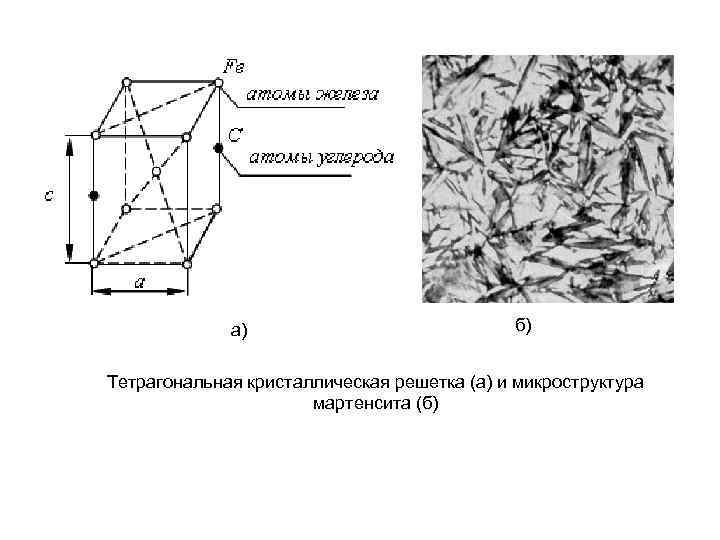 а) б) Тетрагональная кристаллическая решетка (а) и микроструктура мартенсита (б)
а) б) Тетрагональная кристаллическая решетка (а) и микроструктура мартенсита (б)
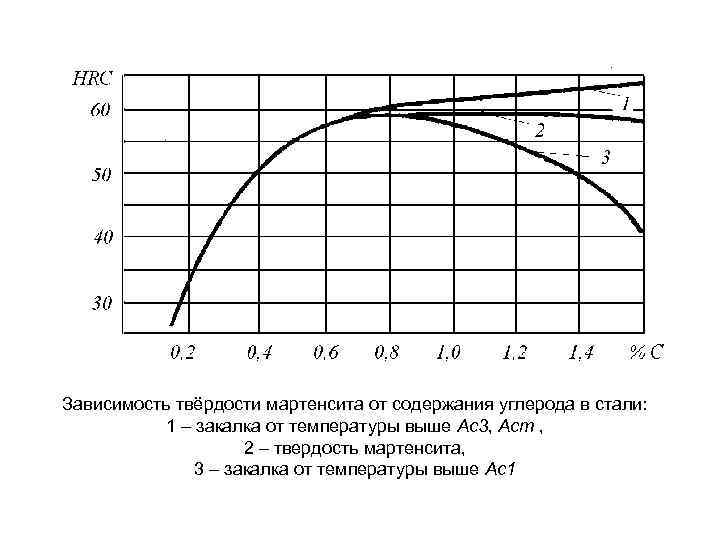 Зависимость твёрдости мартенсита от содержания углерода в стали: 1 – закалка от температуры выше Ас3, Аст , 2 – твердость мартенсита, 3 – закалка от температуры выше Ас1
Зависимость твёрдости мартенсита от содержания углерода в стали: 1 – закалка от температуры выше Ас3, Аст , 2 – твердость мартенсита, 3 – закалка от температуры выше Ас1
 Электронные микроструктуры бейнита (х15000): а) верхнего, б) нижнего
Электронные микроструктуры бейнита (х15000): а) верхнего, б) нижнего
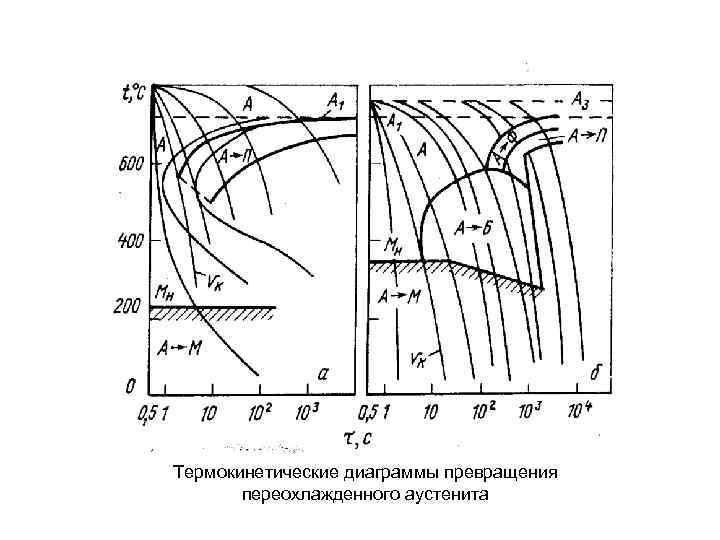 Термокинетические диаграммы превращения переохлажденного аустенита
Термокинетические диаграммы превращения переохлажденного аустенита
 Наложение кривых охлаждения на диаграмму изотермического распада аустенита
Наложение кривых охлаждения на диаграмму изотермического распада аустенита
 . Структура медно никелевого сплава а) литого, б) после диффузионного отжига
. Структура медно никелевого сплава а) литого, б) после диффузионного отжига
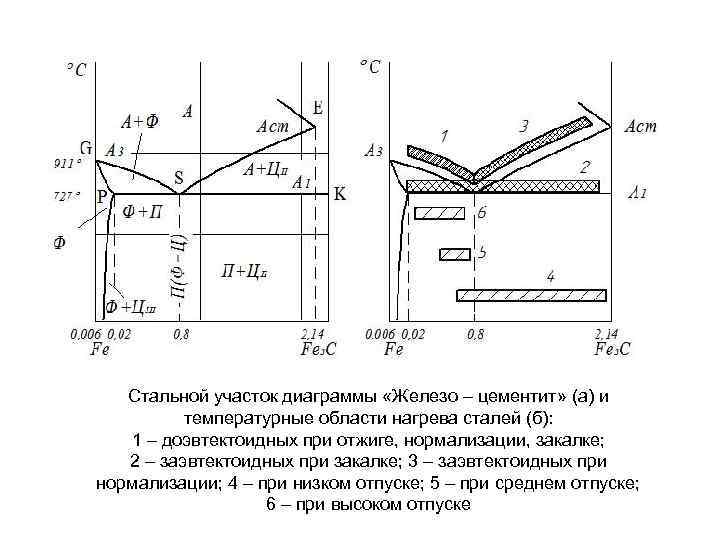 Стальной участок диаграммы «Железо – цементит» (а) и температурные области нагрева сталей (б): 1 – доэвтектоидных при отжиге, нормализации, закалке; 2 – заэвтектоидных при закалке; 3 – заэвтектоидных при нормализации; 4 – при низком отпуске; 5 – при среднем отпуске; 6 – при высоком отпуске
Стальной участок диаграммы «Железо – цементит» (а) и температурные области нагрева сталей (б): 1 – доэвтектоидных при отжиге, нормализации, закалке; 2 – заэвтектоидных при закалке; 3 – заэвтектоидных при нормализации; 4 – при низком отпуске; 5 – при среднем отпуске; 6 – при высоком отпуске
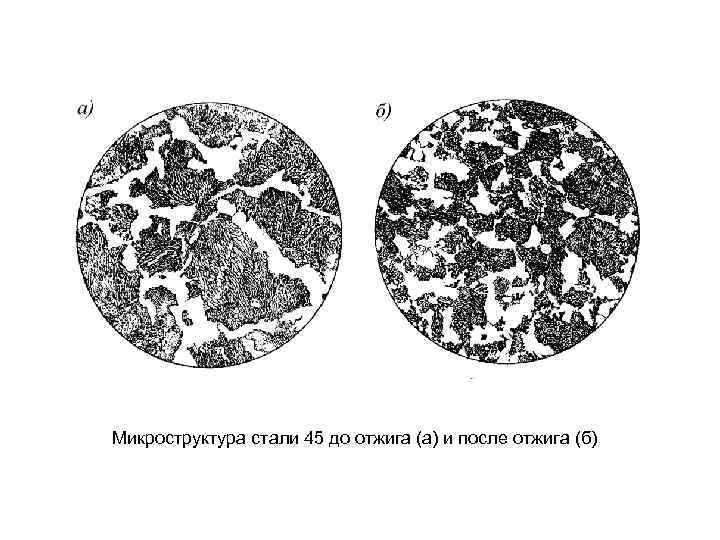 Микроструктура стали 45 до отжига (а) и после отжига (б)
Микроструктура стали 45 до отжига (а) и после отжига (б)
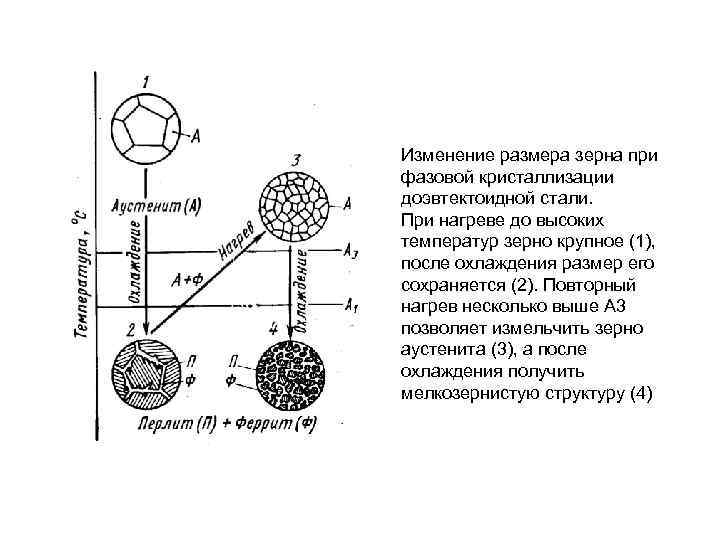 Изменение размера зерна при фазовой кристаллизации доэвтектоидной стали. При нагреве до высоких температур зерно крупное (1), после охлаждения размер его сохраняется (2). Повторный нагрев несколько выше А 3 позволяет измельчить зерно аустенита (3), а после охлаждения получить мелкозернистую структуру (4)
Изменение размера зерна при фазовой кристаллизации доэвтектоидной стали. При нагреве до высоких температур зерно крупное (1), после охлаждения размер его сохраняется (2). Повторный нагрев несколько выше А 3 позволяет измельчить зерно аустенита (3), а после охлаждения получить мелкозернистую структуру (4)
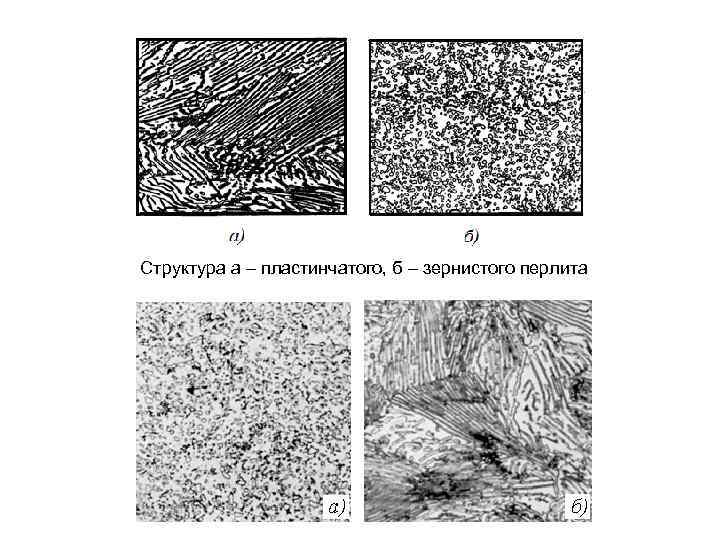 Структура а – пластинчатого, б – зернистого перлита
Структура а – пластинчатого, б – зернистого перлита

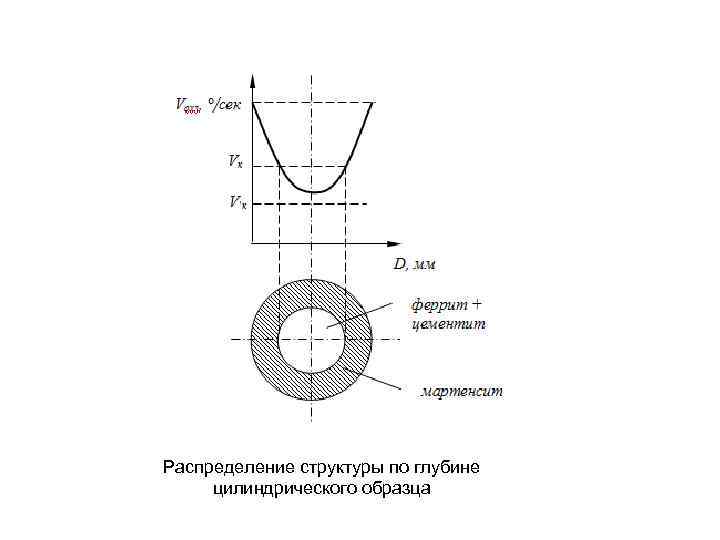 Распределение структуры по глубине цилиндрического образца
Распределение структуры по глубине цилиндрического образца
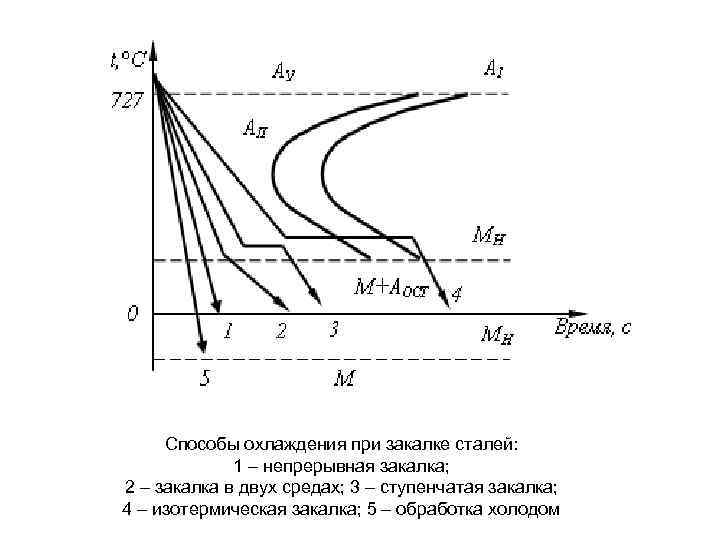 Способы охлаждения при закалке сталей: 1 – непрерывная закалка; 2 – закалка в двух средах; 3 – ступенчатая закалка; 4 – изотермическая закалка; 5 – обработка холодом
Способы охлаждения при закалке сталей: 1 – непрерывная закалка; 2 – закалка в двух средах; 3 – ступенчатая закалка; 4 – изотермическая закалка; 5 – обработка холодом
 Схемы структур стали У 8: а – мартенсит мелкоигольчатый; б – мартенсит крупноиголъчатый
Схемы структур стали У 8: а – мартенсит мелкоигольчатый; б – мартенсит крупноиголъчатый
 Диаграмма состояния сплава с переменной растворимостью компонента В в А
Диаграмма состояния сплава с переменной растворимостью компонента В в А
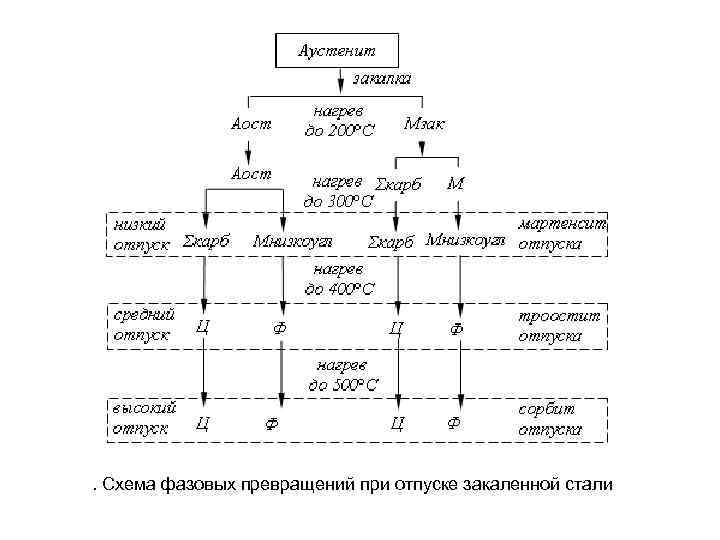 . Схема фазовых превращений при отпуске закаленной стали
. Схема фазовых превращений при отпуске закаленной стали
 Изменение строения и состава фаз при отпуске углеродистой стали (0, 8%)
Изменение строения и состава фаз при отпуске углеродистой стали (0, 8%)
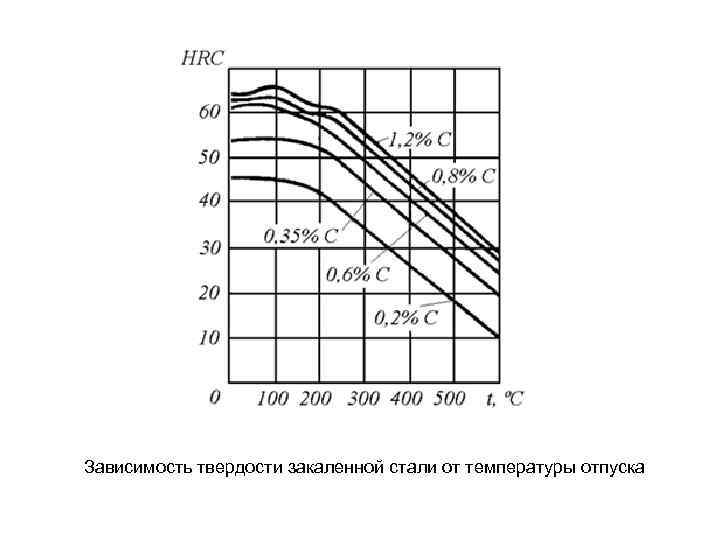 Зависимость твердости закаленной стали от температуры отпуска
Зависимость твердости закаленной стали от температуры отпуска
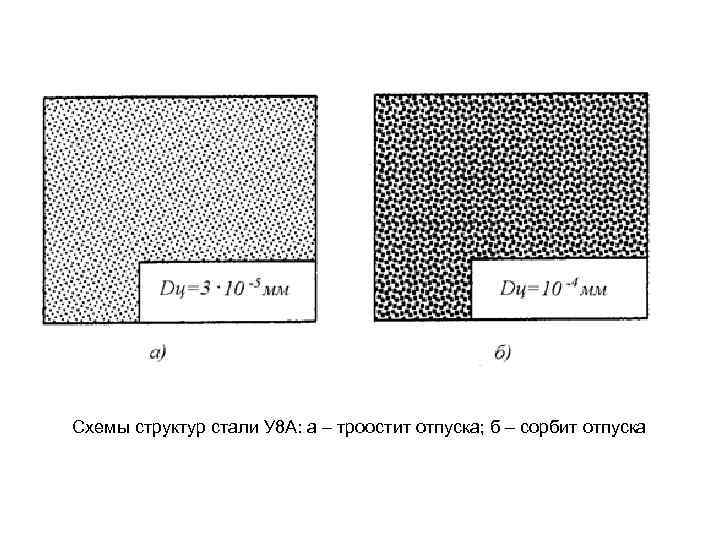 Схемы структур стали У 8 А: а – троостит отпуска; б – сорбит отпуска
Схемы структур стали У 8 А: а – троостит отпуска; б – сорбит отпуска
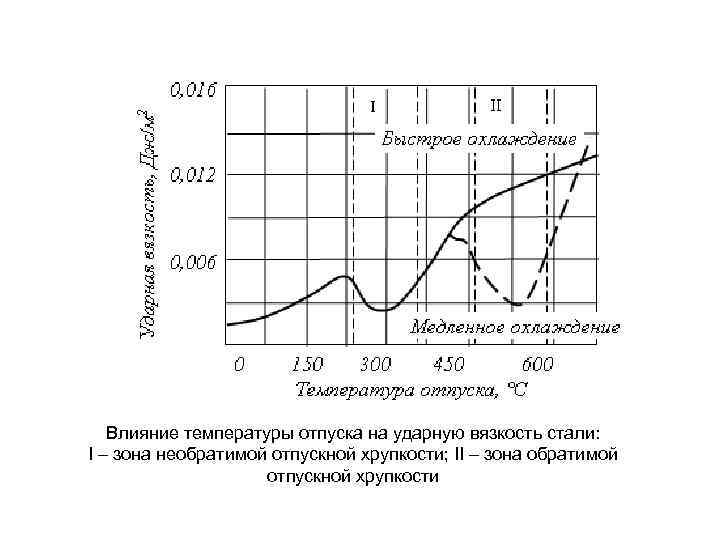 Влияние температуры отпуска на ударную вязкость стали: Ι – зона необратимой отпускной хрупкости; ΙΙ – зона обратимой отпускной хрупкости
Влияние температуры отпуска на ударную вязкость стали: Ι – зона необратимой отпускной хрупкости; ΙΙ – зона обратимой отпускной хрупкости
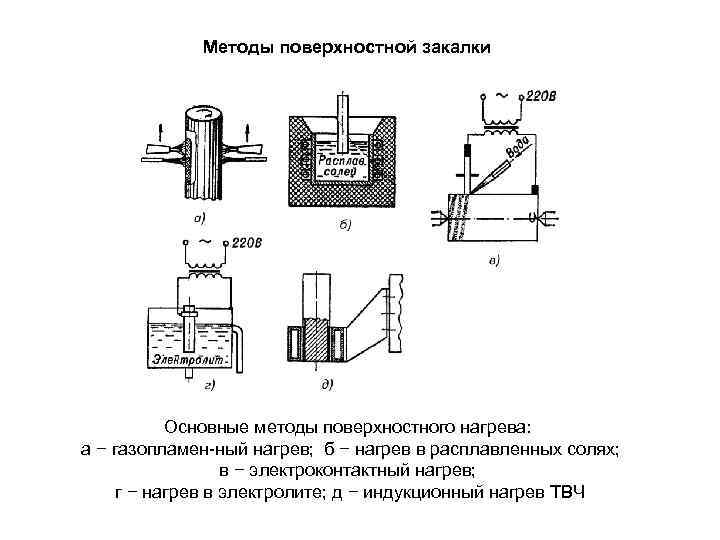 Методы поверхностной закалки Основные методы поверхностного нагрева: а − газопламен ный нагрев; б − нагрев в расплавленных солях; в − электроконтактный нагрев; г − нагрев в электролите; д − индукционный нагрев ТВЧ
Методы поверхностной закалки Основные методы поверхностного нагрева: а − газопламен ный нагрев; б − нагрев в расплавленных солях; в − электроконтактный нагрев; г − нагрев в электролите; д − индукционный нагрев ТВЧ
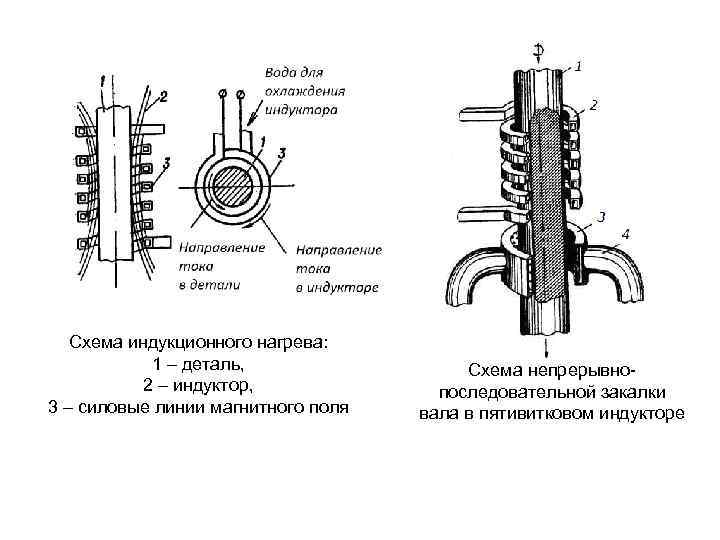 Схема индукционного нагрева: 1 – деталь, 2 – индуктор, 3 – силовые линии магнитного поля Схема непрерывно последовательной закалки вала в пятивитковом индукторе
Схема индукционного нагрева: 1 – деталь, 2 – индуктор, 3 – силовые линии магнитного поля Схема непрерывно последовательной закалки вала в пятивитковом индукторе
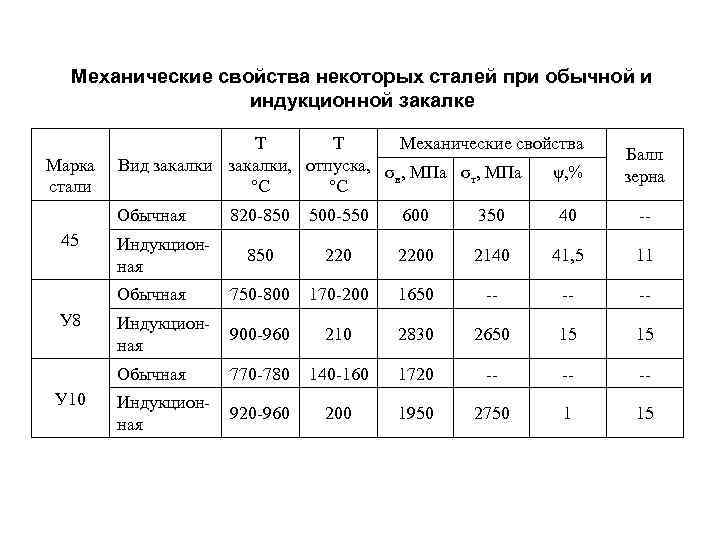 Механические свойства некоторых сталей при обычной и индукционной закалке Марка стали Т Т Механические свойства Вид закалки, отпуска, σ , МПа ψ, % в т °С °С Обычная Балл зерна У 10 600 350 40 -- 850 2200 2140 41, 5 11 750 -800 170 -200 1650 -- -- -- Индукционная 900 -960 210 2830 2650 15 15 Обычная У 8 500 -550 Обычная 45 820 -850 770 -780 140 -160 1720 -- -- -- Индукционная 920 -960 200 1950 2750 1 15 Индукционная
Механические свойства некоторых сталей при обычной и индукционной закалке Марка стали Т Т Механические свойства Вид закалки, отпуска, σ , МПа ψ, % в т °С °С Обычная Балл зерна У 10 600 350 40 -- 850 2200 2140 41, 5 11 750 -800 170 -200 1650 -- -- -- Индукционная 900 -960 210 2830 2650 15 15 Обычная У 8 500 -550 Обычная 45 820 -850 770 -780 140 -160 1720 -- -- -- Индукционная 920 -960 200 1950 2750 1 15 Индукционная
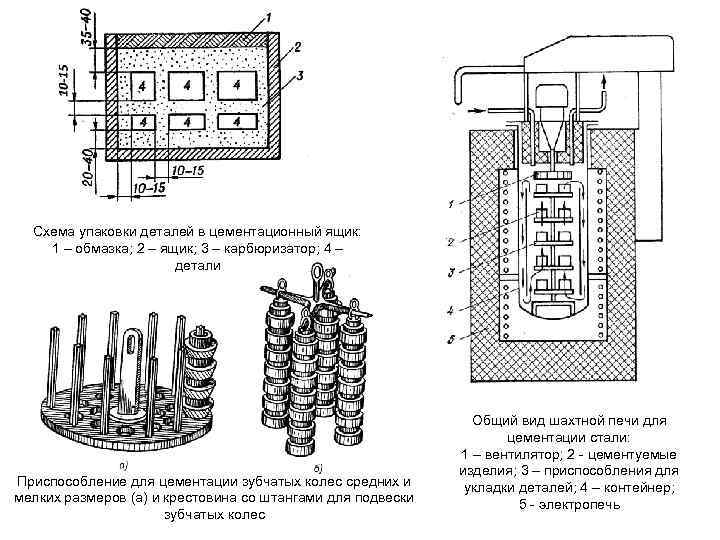 Схема упаковки деталей в цементационный ящик: 1 – обмазка; 2 – ящик; 3 – карбюризатор; 4 – детали Приспособление для цементации зубчатых колес средних и мелких размеров (а) и крестовина со штангами для подвески зубчатых колес Общий вид шахтной печи для цементации стали: 1 – вентилятор; 2 цементуемые изделия; 3 – приспособления для укладки деталей; 4 – контейнер; 5 электропечь
Схема упаковки деталей в цементационный ящик: 1 – обмазка; 2 – ящик; 3 – карбюризатор; 4 – детали Приспособление для цементации зубчатых колес средних и мелких размеров (а) и крестовина со штангами для подвески зубчатых колес Общий вид шахтной печи для цементации стали: 1 – вентилятор; 2 цементуемые изделия; 3 – приспособления для укладки деталей; 4 – контейнер; 5 электропечь
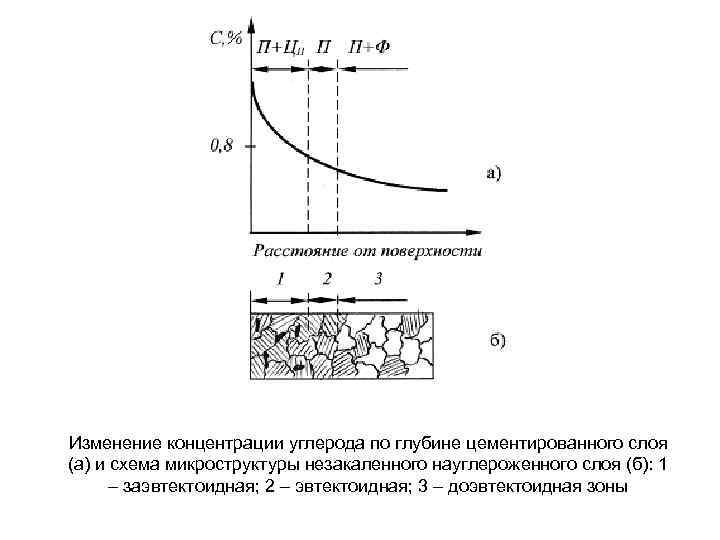 Изменение концентрации углерода по глубине цементированного слоя (а) и схема микроструктуры незакаленного науглероженного слоя (б): 1 – заэвтектоидная; 2 – эвтектоидная; 3 – доэвтектоидная зоны
Изменение концентрации углерода по глубине цементированного слоя (а) и схема микроструктуры незакаленного науглероженного слоя (б): 1 – заэвтектоидная; 2 – эвтектоидная; 3 – доэвтектоидная зоны
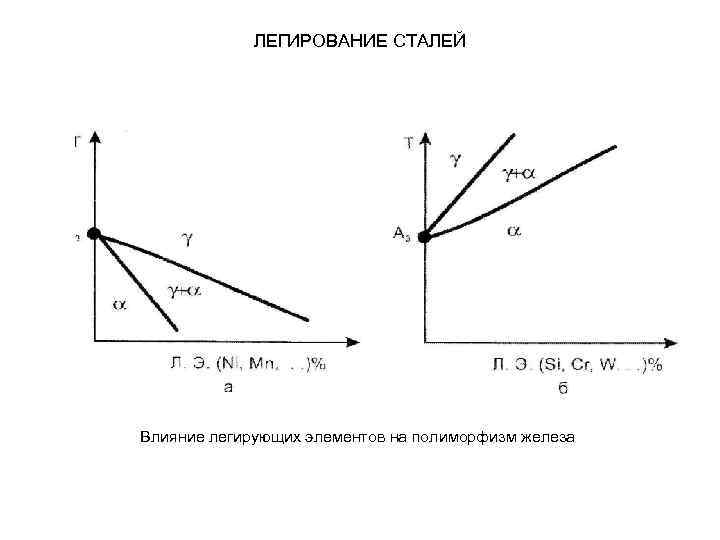 ЛЕГИРОВАНИЕ СТАЛЕЙ Влияние легирующих элементов на полиморфизм железа
ЛЕГИРОВАНИЕ СТАЛЕЙ Влияние легирующих элементов на полиморфизм железа
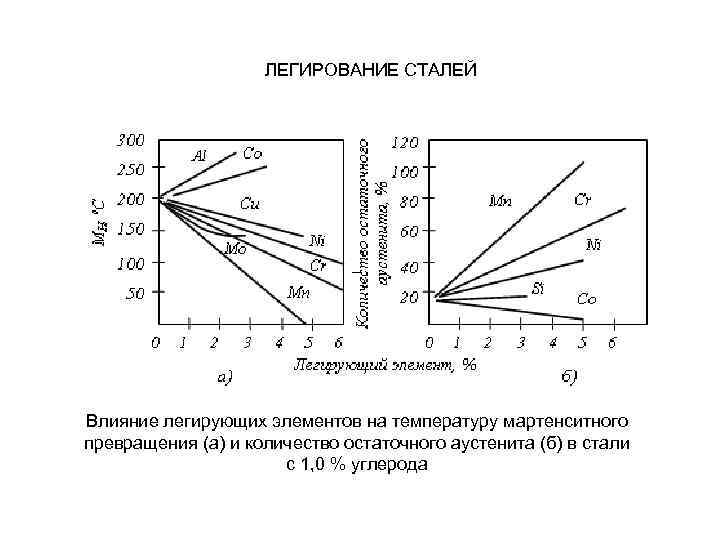 ЛЕГИРОВАНИЕ СТАЛЕЙ – Влияние легирующих элементов на температуру мартенситного превращения (а) и количество остаточного аустенита (б) в стали с 1, 0 % углерода
ЛЕГИРОВАНИЕ СТАЛЕЙ – Влияние легирующих элементов на температуру мартенситного превращения (а) и количество остаточного аустенита (б) в стали с 1, 0 % углерода
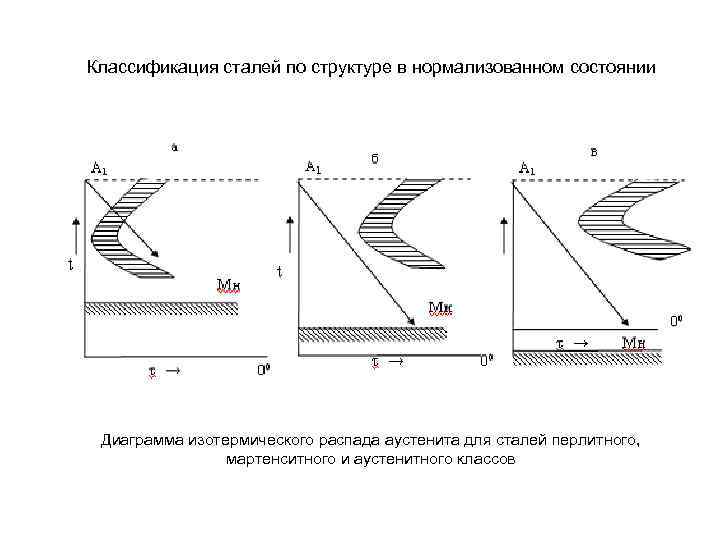 Классификация сталей по структуре в нормализованном состоянии Диаграмма изотермического распада аустенита для сталей перлитного, мартенситного и аустенитного классов
Классификация сталей по структуре в нормализованном состоянии Диаграмма изотермического распада аустенита для сталей перлитного, мартенситного и аустенитного классов
 Каждый легирующий элемент обозначается буквой: А – азот, Б – ниобий, В – вольфрам, Г – марганец, Д – медь, Е – селен, К –кобальт, Н – никель, М – молибден, П – фосфор, Р – бор, С – кремний, Т – титан, Ф – ванадий, Х – хром, Ц – цирконий, Ч – редкоземельные элементы, Ю – алюминий. 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, 40 ХН 2 МА, 35, 70 С 2 ХАБ ШХ 15, А 12, А 40 Г, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
Каждый легирующий элемент обозначается буквой: А – азот, Б – ниобий, В – вольфрам, Г – марганец, Д – медь, Е – селен, К –кобальт, Н – никель, М – молибден, П – фосфор, Р – бор, С – кремний, Т – титан, Ф – ванадий, Х – хром, Ц – цирконий, Ч – редкоземельные элементы, Ю – алюминий. 12 Х 2 НВФА, 14 Г 2, 10 ХСНД, 18 Г 2 С, 15, 20 Х, 15 ХФ, 20 Х 2 Н 4 А, 20 ХГНР, 40 ХН 2 МА, 35, 70 С 2 ХАБ ШХ 15, А 12, А 40 Г, 20 Х 12 ВНМФ, 40 Х 15 Н 7 Г 7 Ф 2 МС, У 12, У 10 А, ХВСГ
 Инструментальные стали б) а) Сталь Х для режущего инструмента (х1000): а) зернистый перлит после отжига, б) отпущенный мартенсит после закалки и отпуска
Инструментальные стали б) а) Сталь Х для режущего инструмента (х1000): а) зернистый перлит после отжига, б) отпущенный мартенсит после закалки и отпуска
 а) б) Быстрорежущая сталь Р 18 (х1000): а) литая, б) прокатанная и отожженная
а) б) Быстрорежущая сталь Р 18 (х1000): а) литая, б) прокатанная и отожженная
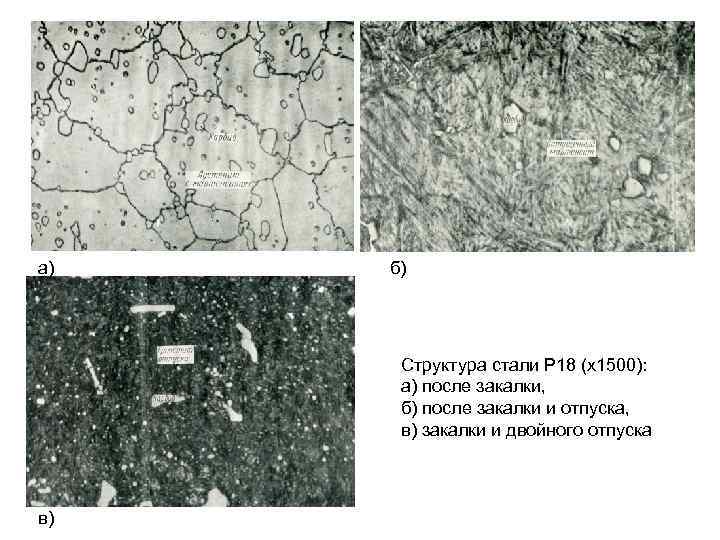 а) б) Структура стали Р 18 (х1500): а) после закалки, б) после закалки и отпуска, в) закалки и двойного отпуска в)
а) б) Структура стали Р 18 (х1500): а) после закалки, б) после закалки и отпуска, в) закалки и двойного отпуска в)
 а) б) Структура твердых сплавов а) мелкозернистого ВК 15, б) крупнозернистого ВК 15, в) Т 15 К 6)
а) б) Структура твердых сплавов а) мелкозернистого ВК 15, б) крупнозернистого ВК 15, в) Т 15 К 6)
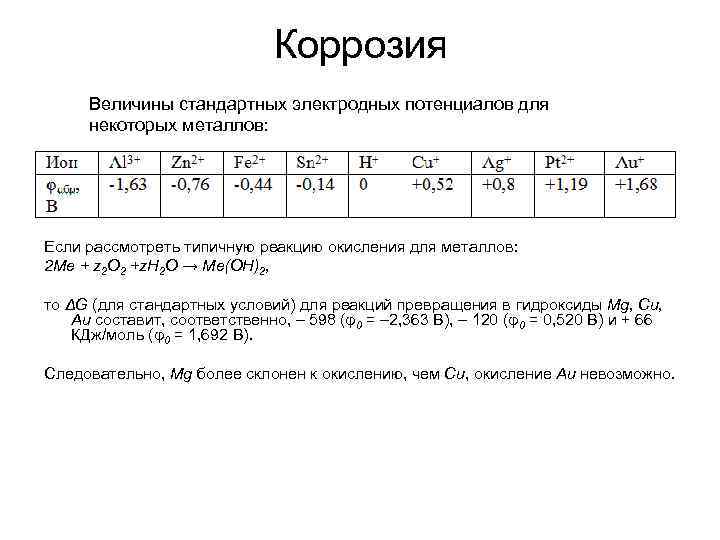 Коррозия Величины стандартных электродных потенциалов для некоторых металлов: Если рассмотреть типичную реакцию окисления для металлов: 2 Ме + z 2 O 2 +z. Н 2 O → Ме(OН)2, то ΔG (для стандартных условий) для реакций превращения в гидроксиды Мg, Cu, Аu составит, соответственно, – 598 (φ0 = – 2, 363 В), – 120 (φ0 = 0, 520 В) и + 66 КДж/моль (φ0 = 1, 692 В). Следовательно, Мg более склонен к окислению, чем Сu, окисление Аu невозможно.
Коррозия Величины стандартных электродных потенциалов для некоторых металлов: Если рассмотреть типичную реакцию окисления для металлов: 2 Ме + z 2 O 2 +z. Н 2 O → Ме(OН)2, то ΔG (для стандартных условий) для реакций превращения в гидроксиды Мg, Cu, Аu составит, соответственно, – 598 (φ0 = – 2, 363 В), – 120 (φ0 = 0, 520 В) и + 66 КДж/моль (φ0 = 1, 692 В). Следовательно, Мg более склонен к окислению, чем Сu, окисление Аu невозможно.
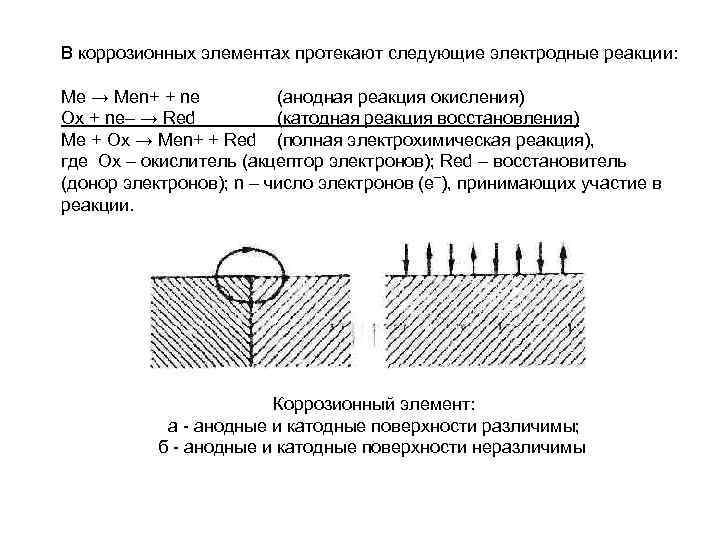 В коррозионных элементах протекают следующие электродные реакции: Ме → Меn+ + nе (анодная реакция окисления) Ох + ne– → Red (катодная реакция восстановления) Ме + Ох → Меn+ + Red (полная электрохимическая реакция), где Ох – окислитель (акцептор электронов); Red – восстановитель (донор электронов); n – число электронов (е–), принимающих участие в реакции. Коррозионный элемент: а анодные и катодные поверхности различимы; б анодные и катодные поверхности неразличимы
В коррозионных элементах протекают следующие электродные реакции: Ме → Меn+ + nе (анодная реакция окисления) Ох + ne– → Red (катодная реакция восстановления) Ме + Ох → Меn+ + Red (полная электрохимическая реакция), где Ох – окислитель (акцептор электронов); Red – восстановитель (донор электронов); n – число электронов (е–), принимающих участие в реакции. Коррозионный элемент: а анодные и катодные поверхности различимы; б анодные и катодные поверхности неразличимы
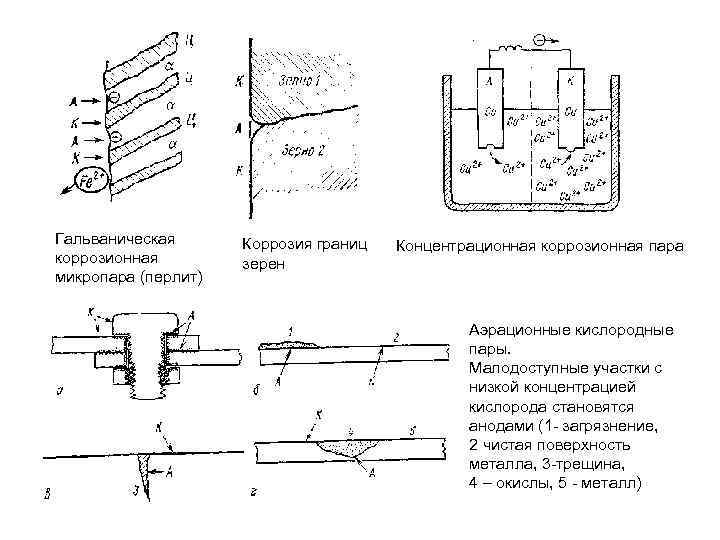 Гальваническая коррозионная микропара (перлит) Коррозия границ зерен Концентрационная коррозионная пара Аэрационные кислородные пары. Малодоступные участки с низкой концентрацией кислорода становятся анодами (1 загрязнение, 2 чистая поверхность металла, 3 трещина, 4 – окислы, 5 металл)
Гальваническая коррозионная микропара (перлит) Коррозия границ зерен Концентрационная коррозионная пара Аэрационные кислородные пары. Малодоступные участки с низкой концентрацией кислорода становятся анодами (1 загрязнение, 2 чистая поверхность металла, 3 трещина, 4 – окислы, 5 металл)
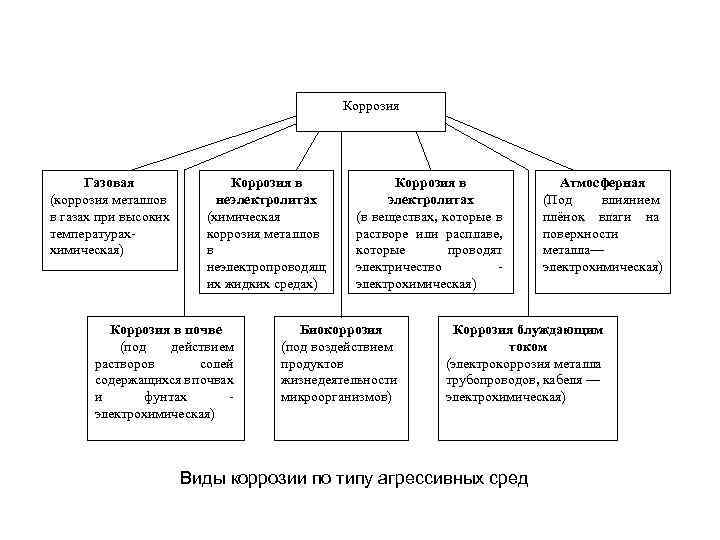 Коррозия Газовая (коррозия металлов в газах при высоких температурах- химическая) Коррозия в неэлектролитах (химическая коррозия металлов в неэлектропроводящ их жидких средах) Коррозия в почве (под действием растворов солей содержащихся в почвах и фунтах - электрохимическая) Коррозия в электролитах (в веществах, которые в растворе или расплаве, которые проводят электричество - электрохимическая) Биокоррозия (под воздействием продуктов жизнедеятельности микроорганизмов) Атмосферная (Под влиянием плёнок влаги на поверхности металла— электрохимическая) Коррозия блуждающим током (электрокоррозия металла трубопроводов, кабеля — электрохимическая) Виды коррозии по типу агрессивных сред
Коррозия Газовая (коррозия металлов в газах при высоких температурах- химическая) Коррозия в неэлектролитах (химическая коррозия металлов в неэлектропроводящ их жидких средах) Коррозия в почве (под действием растворов солей содержащихся в почвах и фунтах - электрохимическая) Коррозия в электролитах (в веществах, которые в растворе или расплаве, которые проводят электричество - электрохимическая) Биокоррозия (под воздействием продуктов жизнедеятельности микроорганизмов) Атмосферная (Под влиянием плёнок влаги на поверхности металла— электрохимическая) Коррозия блуждающим током (электрокоррозия металла трубопроводов, кабеля — электрохимическая) Виды коррозии по типу агрессивных сред
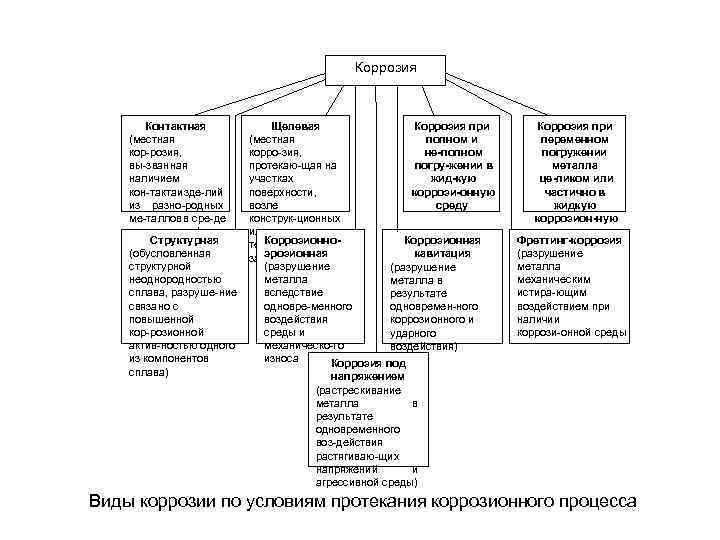 Коррозия Контактная (местная кор розия, вы званная наличием кон такта зде лий и из разно родных ме таллов сре де в электролите) Структурная (обусловленная структурной неоднородностью сплава, разруше ние связано с повышенной кор розионной актив ностью одного из компонентов сплава) Щелевая Коррозия при (местная полном и корро зия, не полном протекаю щая на погру жении в участках жид кую поверхности, коррози онную возле среду конструк ционных или Коррозионно Коррозионная технологических эрозионная кавитация зазоров) (разрушение металла в вследствие результате одновре менного одновремен ного воздействия коррозионного и среды и ударного механическо го воздействия) износа Коррозия под Коррозия при переменном погружении металла це ликом или частично в жидкую коррозион ную среду Фреттинг коррозия (разрушение металла механическим истира ющим воздействием при наличии коррози онной среды напряжением (растрескивание металла в результате одновременного воз действия растягиваю щих напряжений и агрессивной среды) Виды коррозии по условиям протекания коррозионного процесса
Коррозия Контактная (местная кор розия, вы званная наличием кон такта зде лий и из разно родных ме таллов сре де в электролите) Структурная (обусловленная структурной неоднородностью сплава, разруше ние связано с повышенной кор розионной актив ностью одного из компонентов сплава) Щелевая Коррозия при (местная полном и корро зия, не полном протекаю щая на погру жении в участках жид кую поверхности, коррози онную возле среду конструк ционных или Коррозионно Коррозионная технологических эрозионная кавитация зазоров) (разрушение металла в вследствие результате одновре менного одновремен ного воздействия коррозионного и среды и ударного механическо го воздействия) износа Коррозия под Коррозия при переменном погружении металла це ликом или частично в жидкую коррозион ную среду Фреттинг коррозия (разрушение металла механическим истира ющим воздействием при наличии коррози онной среды напряжением (растрескивание металла в результате одновременного воз действия растягиваю щих напряжений и агрессивной среды) Виды коррозии по условиям протекания коррозионного процесса
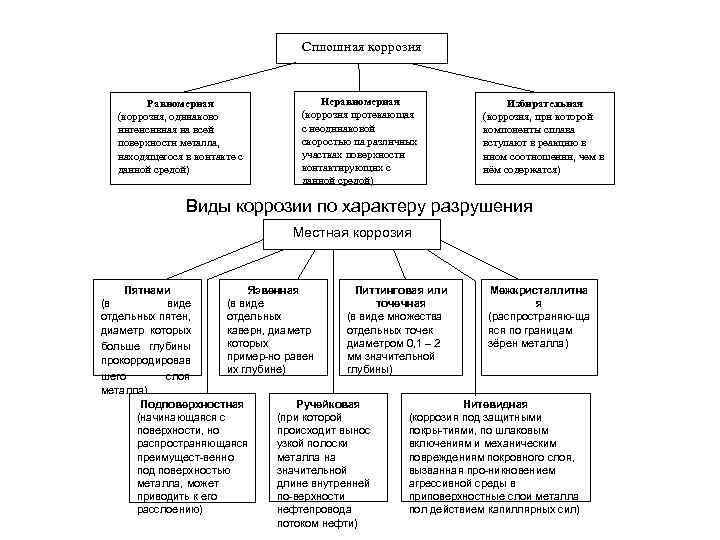 Сплошная коррозия Равномерная (коррозия, одинаково интенсивная на всей поверхности металла, находящегося в контакте с данной средой) Неравномерная (коррозия протекающая с неодинаковой скоростью па различных участках поверхности контактирующих с данной средой) Избирательная (коррозия, при которой компоненты сплава вступают в реакцию в ином соотношении, чем в нём содержатся) Виды коррозии по характеру разрушения Местная коррозия Пятнами Язвенная Питтинговая или Межкристаллитна (в виде точечная я отдельных пятен, отдельных (в виде множества (распространяю ща диаметр которых каверн, диаметр отдельных точек яся по границам которых диаметром 0, 1 – 2 зёрен металла) больше глубины пример но равен мм значительной прокорродировав их глубине) глубины) шего слоя металла) Подповерхностная Ручейковая Нитевидная (начинающаяся с (при которой (коррозия под защитными поверхности, но происходит вынос покры тиями, по шлаковым распространяющаяся узкой полоски включениям и механическим преимущест венно металла на повреждениям покровного слоя, под поверхностью значительной вызванная про никновением металла, может длине внутренней агрессивной среды в приводить к его по верхности приповерхностные слои металла расслоению) нефтепровода пол действием капиллярных сил) потоком нефти)
Сплошная коррозия Равномерная (коррозия, одинаково интенсивная на всей поверхности металла, находящегося в контакте с данной средой) Неравномерная (коррозия протекающая с неодинаковой скоростью па различных участках поверхности контактирующих с данной средой) Избирательная (коррозия, при которой компоненты сплава вступают в реакцию в ином соотношении, чем в нём содержатся) Виды коррозии по характеру разрушения Местная коррозия Пятнами Язвенная Питтинговая или Межкристаллитна (в виде точечная я отдельных пятен, отдельных (в виде множества (распространяю ща диаметр которых каверн, диаметр отдельных точек яся по границам которых диаметром 0, 1 – 2 зёрен металла) больше глубины пример но равен мм значительной прокорродировав их глубине) глубины) шего слоя металла) Подповерхностная Ручейковая Нитевидная (начинающаяся с (при которой (коррозия под защитными поверхности, но происходит вынос покры тиями, по шлаковым распространяющаяся узкой полоски включениям и механическим преимущест венно металла на повреждениям покровного слоя, под поверхностью значительной вызванная про никновением металла, может длине внутренней агрессивной среды в приводить к его по верхности приповерхностные слои металла расслоению) нефтепровода пол действием капиллярных сил) потоком нефти)
 Цветные металлы Магний и сплавы на его основе Физические и механические свойства магния: Температура плавления, °С 651 Плотность, кг/м 3 1740 t, ºC σB, МПа ψ, % +17 -196 -253 180 200 210 10 7 8
Цветные металлы Магний и сплавы на его основе Физические и механические свойства магния: Температура плавления, °С 651 Плотность, кг/м 3 1740 t, ºC σB, МПа ψ, % +17 -196 -253 180 200 210 10 7 8
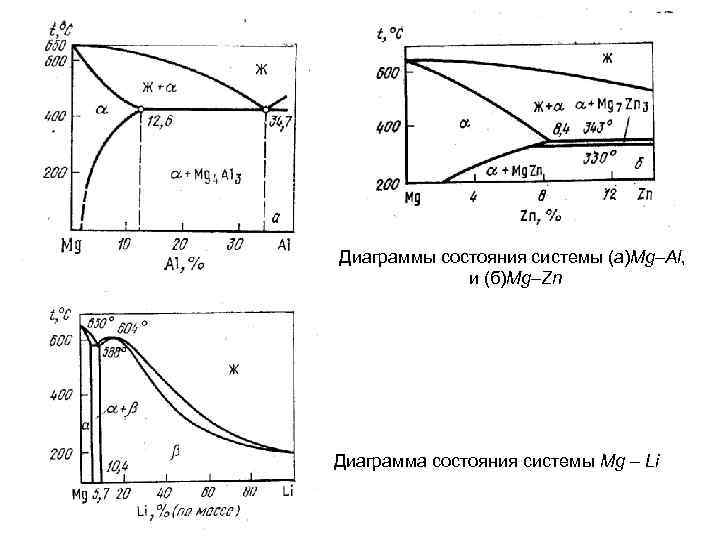 Диаграммы состояния системы (a)Mg–Al, и (б)Mg–Zn Диаграмма состояния системы Mg – Li
Диаграммы состояния системы (a)Mg–Al, и (б)Mg–Zn Диаграмма состояния системы Mg – Li
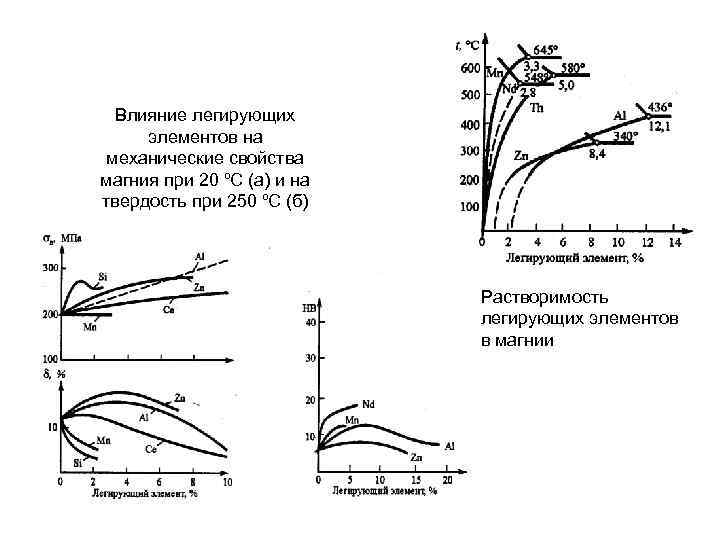 Влияние легирующих элементов на механические свойства магния при 20 ºС (а) и на твердость при 250 ºС (б) Растворимость легирующих элементов в магнии
Влияние легирующих элементов на механические свойства магния при 20 ºС (а) и на твердость при 250 ºС (б) Растворимость легирующих элементов в магнии
 Бериллий и сплавы на его основе Физические свойства бериллия: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) теплоемкость удельная, Дж/(кг·К) температурный коэффициент линейного расширения, К− 1 1283 1844, 8 150 1674 13 модуль нормальной упругости, ГПа 310
Бериллий и сплавы на его основе Физические свойства бериллия: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) теплоемкость удельная, Дж/(кг·К) температурный коэффициент линейного расширения, К− 1 1283 1844, 8 150 1674 13 модуль нормальной упругости, ГПа 310
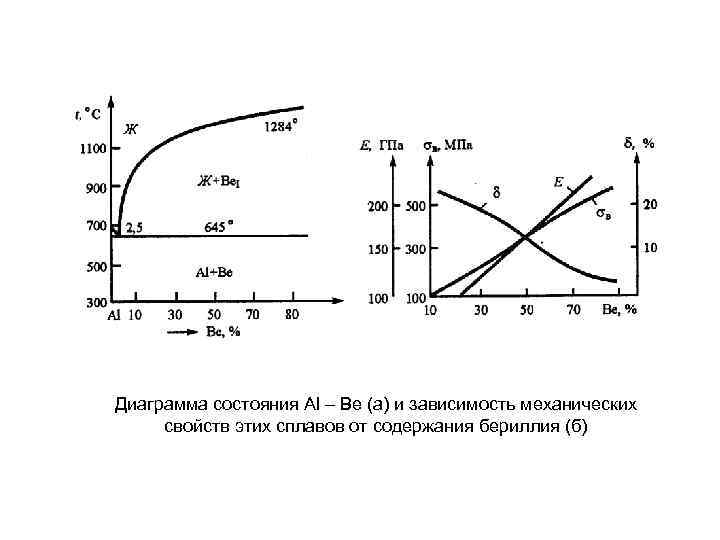 Диаграмма состояния Al – Be (а) и зависимость механических свойств этих сплавов от содержания бериллия (б)
Диаграмма состояния Al – Be (а) и зависимость механических свойств этих сплавов от содержания бериллия (б)
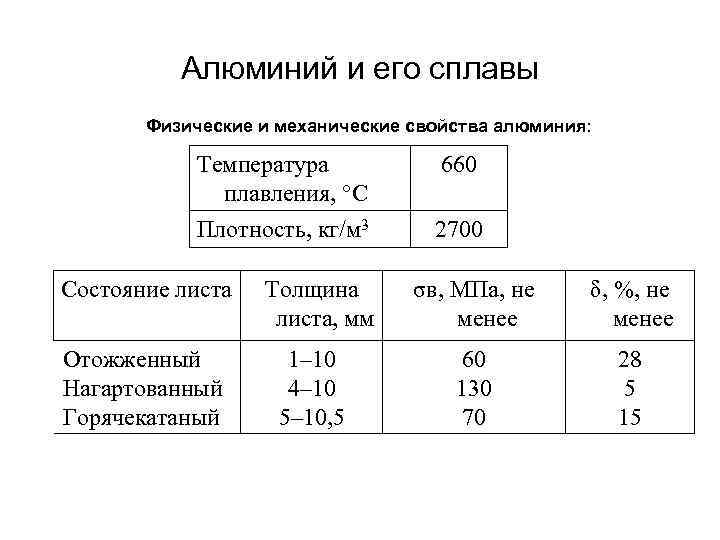 Алюминий и его сплавы Физические и механические свойства алюминия: Температура плавления, °С 660 Плотность, кг/м 3 2700 Состояние листа Отожженный Нагартованный Горячекатаный Толщина листа, мм 1– 10 4– 10 5– 10, 5 σв, МПа, не менее δ, %, не менее 60 130 70 28 5 15
Алюминий и его сплавы Физические и механические свойства алюминия: Температура плавления, °С 660 Плотность, кг/м 3 2700 Состояние листа Отожженный Нагартованный Горячекатаный Толщина листа, мм 1– 10 4– 10 5– 10, 5 σв, МПа, не менее δ, %, не менее 60 130 70 28 5 15
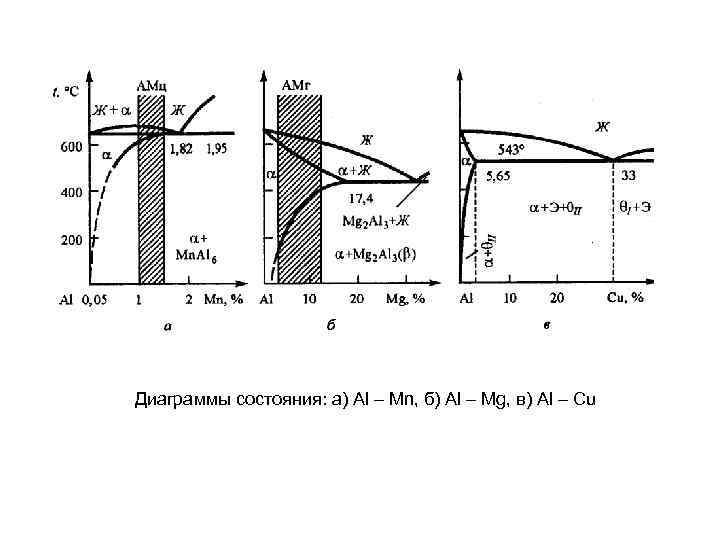 Диаграммы состояния: а) Al – Mn, б) Al – Mg, в) Al – Cu
Диаграммы состояния: а) Al – Mn, б) Al – Mg, в) Al – Cu
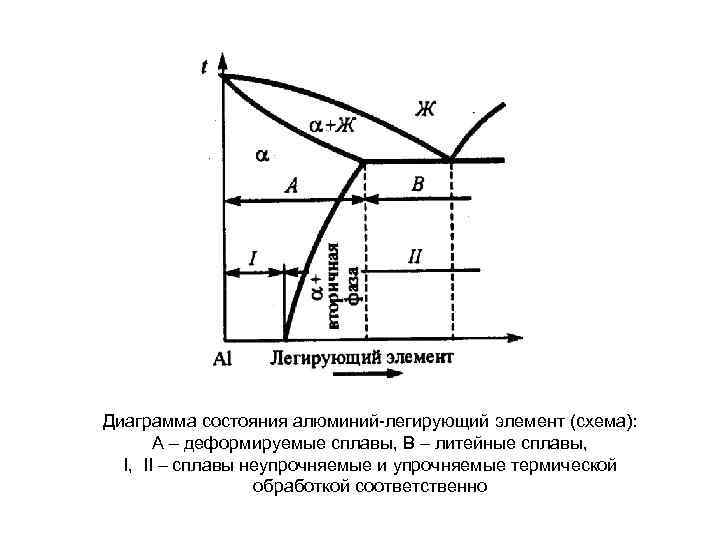 Диаграмма состояния алюминий легирующий элемент (схема): А – деформируемые сплавы, В – литейные сплавы, II – сплавы неупрочняемые и упрочняемые термической обработкой соответственно
Диаграмма состояния алюминий легирующий элемент (схема): А – деформируемые сплавы, В – литейные сплавы, II – сплавы неупрочняемые и упрочняемые термической обработкой соответственно
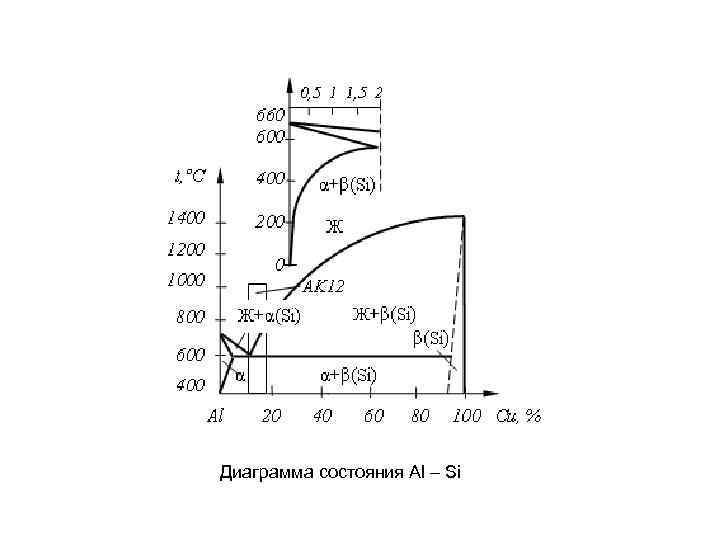 Диаграмма состояния Al – Si
Диаграмма состояния Al – Si
 Титан и сплавы на его основе Физические свойства титана: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) температурный коэффициент линейного расширения, К− 1 1700 4500 18, 85 8, 15 модуль нормальной упругости, ГПа 112
Титан и сплавы на его основе Физические свойства титана: температура плавления, °С плотность, кг/м 3 теплопроводность, Вт/(м·К) температурный коэффициент линейного расширения, К− 1 1700 4500 18, 85 8, 15 модуль нормальной упругости, ГПа 112
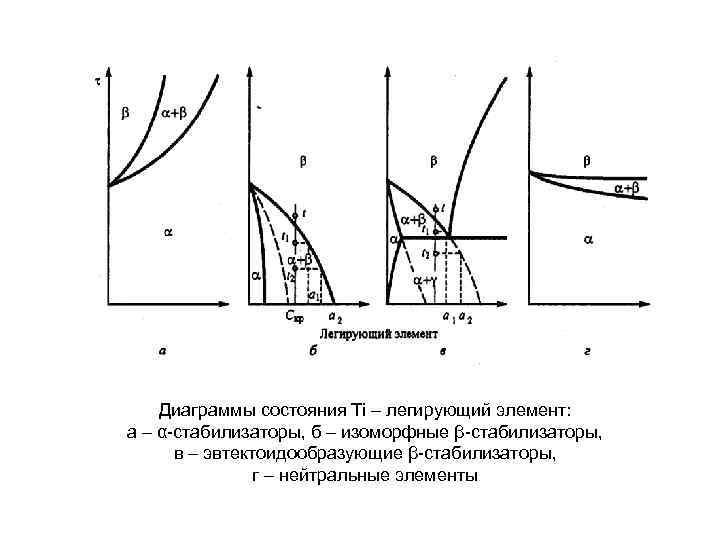 Диаграммы состояния Тi – легирующий элемент: а – α стабилизаторы, б – изоморфные β стабилизаторы, в – эвтектоидообразующие β стабилизаторы, г – нейтральные элементы
Диаграммы состояния Тi – легирующий элемент: а – α стабилизаторы, б – изоморфные β стабилизаторы, в – эвтектоидообразующие β стабилизаторы, г – нейтральные элементы
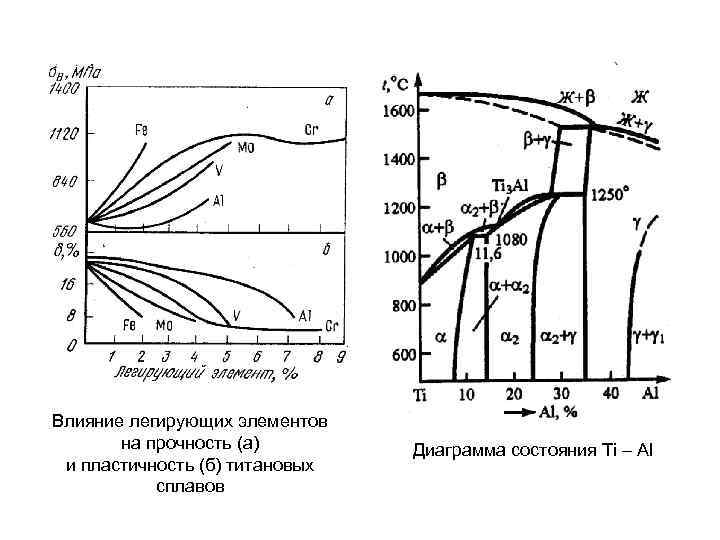 Влияние легирующих элементов на прочность (а) и пластичность (б) титановых сплавов Диаграмма состояния Ti – Al
Влияние легирующих элементов на прочность (а) и пластичность (б) титановых сплавов Диаграмма состояния Ti – Al
 Медь и ее сплавы Физические и механические свойства меди: Температура плавления, ºС 1083 Плотность, кг/м 3 8940 Предел прочности, МПа 200– 250 Относительное удлинение, % 40– 50
Медь и ее сплавы Физические и механические свойства меди: Температура плавления, ºС 1083 Плотность, кг/м 3 8940 Предел прочности, МПа 200– 250 Относительное удлинение, % 40– 50
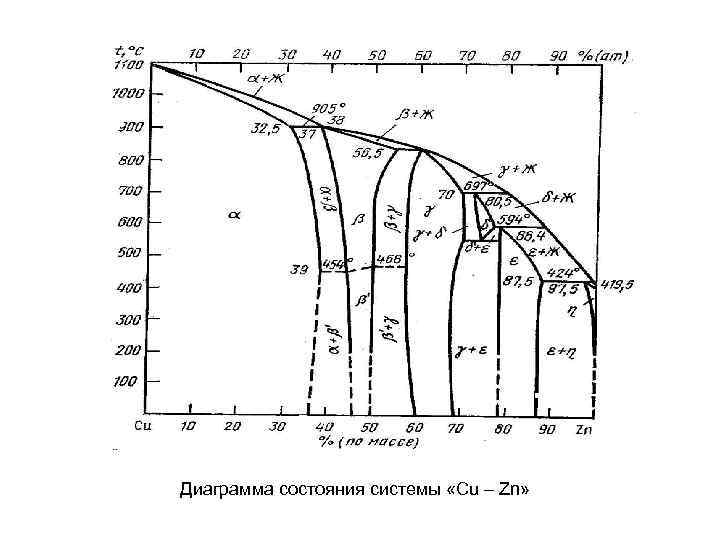 Диаграмма состояния системы «Cu – Zn»
Диаграмма состояния системы «Cu – Zn»
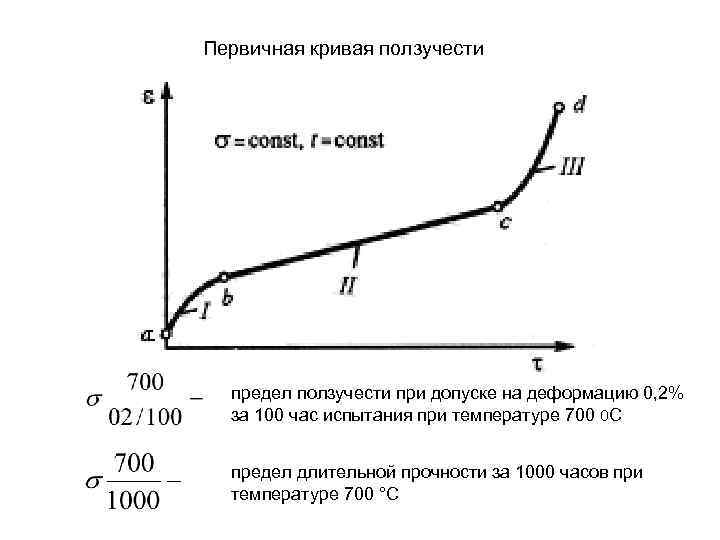 Первичная кривая ползучести предел ползучести при допуске на деформацию 0, 2% за 100 час испытания при температуре 700 0 С предел длительной прочности за 1000 часов при температуре 700 °С
Первичная кривая ползучести предел ползучести при допуске на деформацию 0, 2% за 100 час испытания при температуре 700 0 С предел длительной прочности за 1000 часов при температуре 700 °С
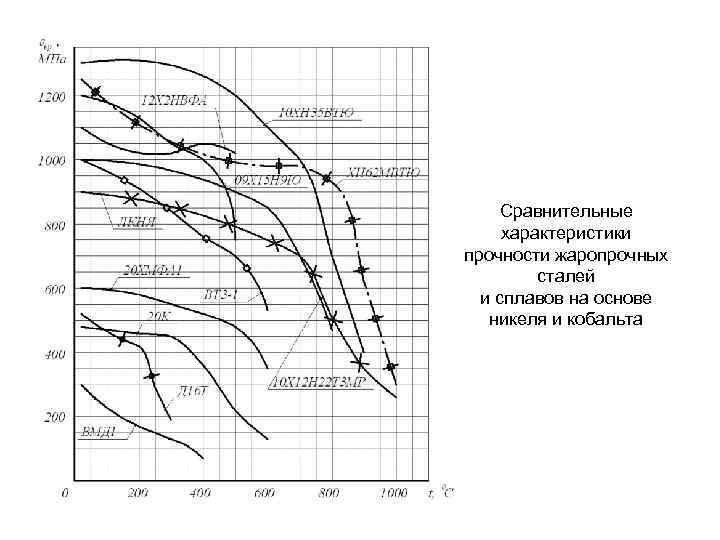 Сравнительные характеристики прочности жаропрочных сталей и сплавов на основе никеля и кобальта
Сравнительные характеристики прочности жаропрочных сталей и сплавов на основе никеля и кобальта
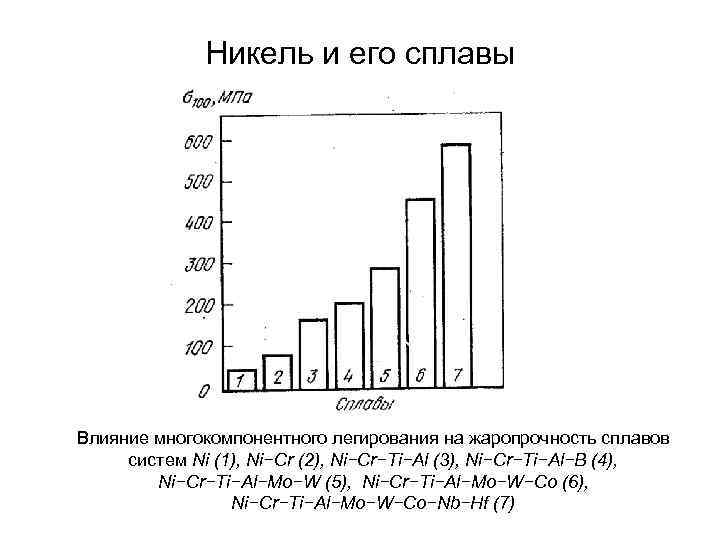 Никель и его сплавы Влияние многокомпонентного легирования на жаропрочность сплавов систем Ni (1), Ni−Cr (2), Ni−Cr−Ti−Al (3), Ni−Cr−Ti−Al−B (4), Ni−Cr−Ti−Al−Mo−W (5), Ni−Cr−Ti−Al−Mo−W−Co (6), Ni−Cr−Ti−Al−Mo−W−Co−Nb−Hf (7)
Никель и его сплавы Влияние многокомпонентного легирования на жаропрочность сплавов систем Ni (1), Ni−Cr (2), Ni−Cr−Ti−Al (3), Ni−Cr−Ti−Al−B (4), Ni−Cr−Ti−Al−Mo−W (5), Ni−Cr−Ti−Al−Mo−W−Co (6), Ni−Cr−Ti−Al−Mo−W−Co−Nb−Hf (7)
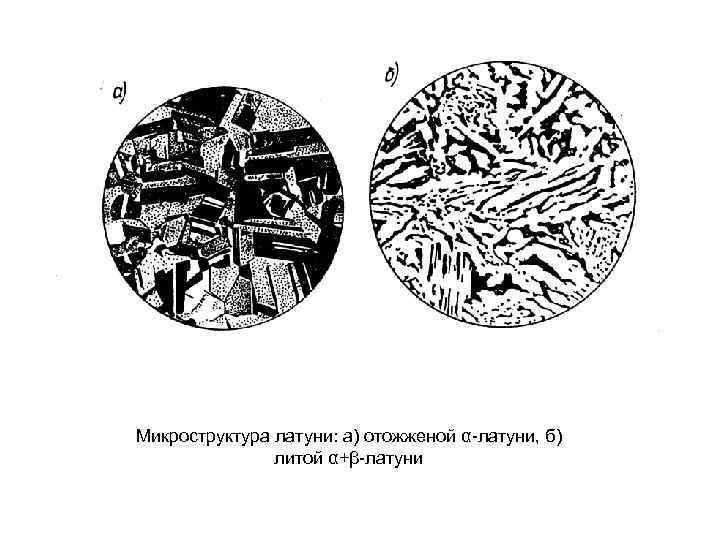 Микроструктура латуни: а) отожженой α латуни, б) литой α+β латуни
Микроструктура латуни: а) отожженой α латуни, б) литой α+β латуни
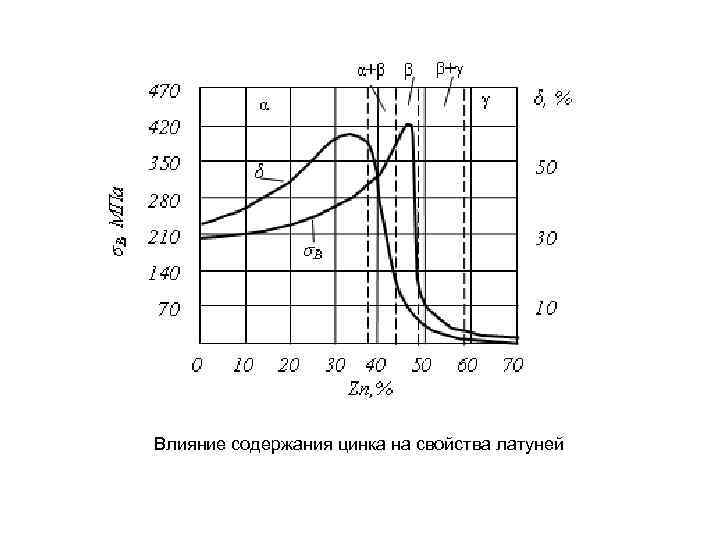 Влияние содержания цинка на свойства латуней
Влияние содержания цинка на свойства латуней
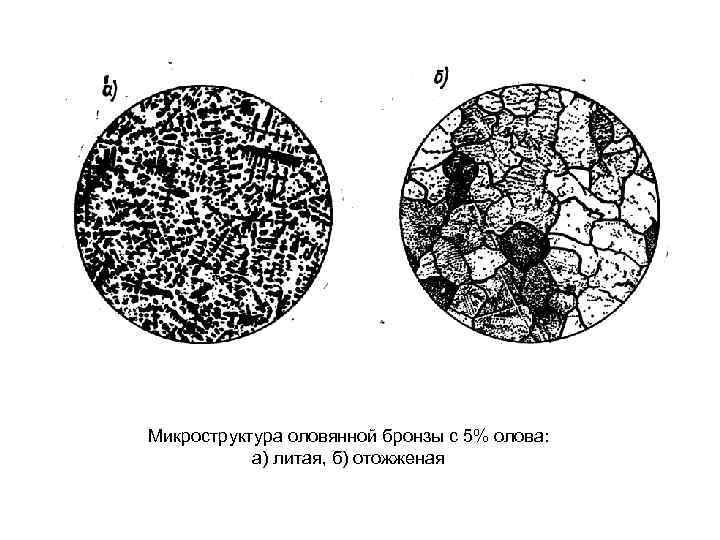 Микроструктура оловянной бронзы с 5% олова: а) литая, б) отожженая
Микроструктура оловянной бронзы с 5% олова: а) литая, б) отожженая
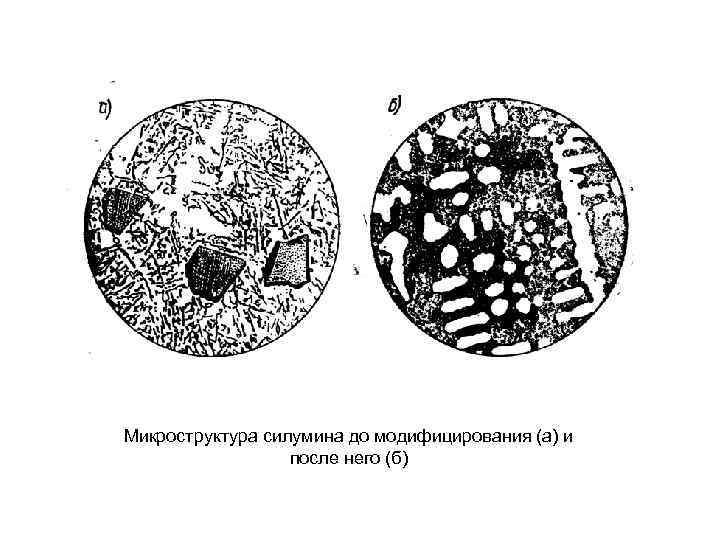 Микроструктура силумина до модифицирования (а) и после него (б)
Микроструктура силумина до модифицирования (а) и после него (б)
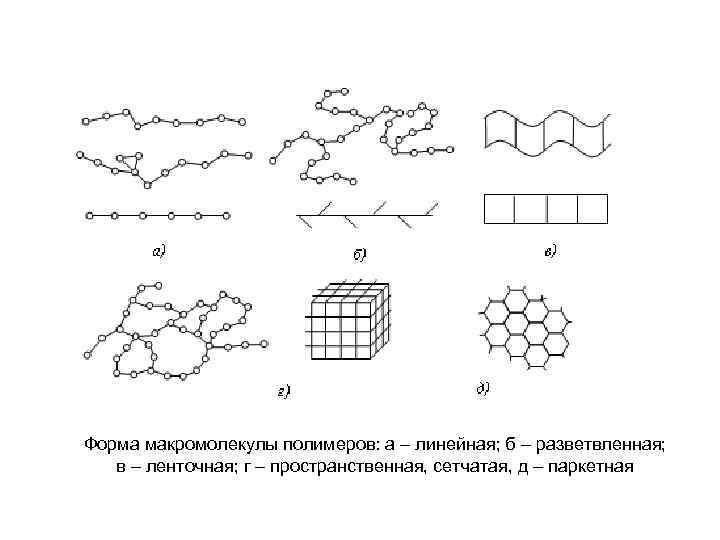 Форма макромолекулы полимеров: а – линейная; б – разветвленная; в – ленточная; г – пространственная, сетчатая, д – паркетная
Форма макромолекулы полимеров: а – линейная; б – разветвленная; в – ленточная; г – пространственная, сетчатая, д – паркетная
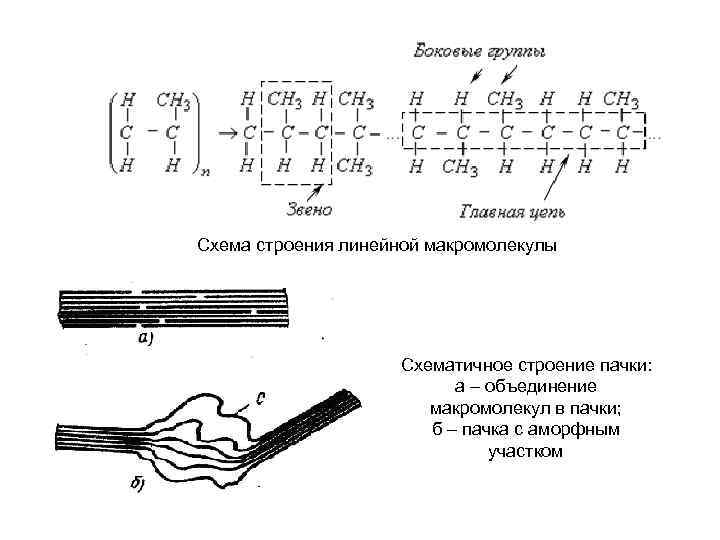 Схема строения линейной макромолекулы Схематичное строение пачки: а – объединение макромолекул в пачки; б – пачка с аморфным участком
Схема строения линейной макромолекулы Схематичное строение пачки: а – объединение макромолекул в пачки; б – пачка с аморфным участком
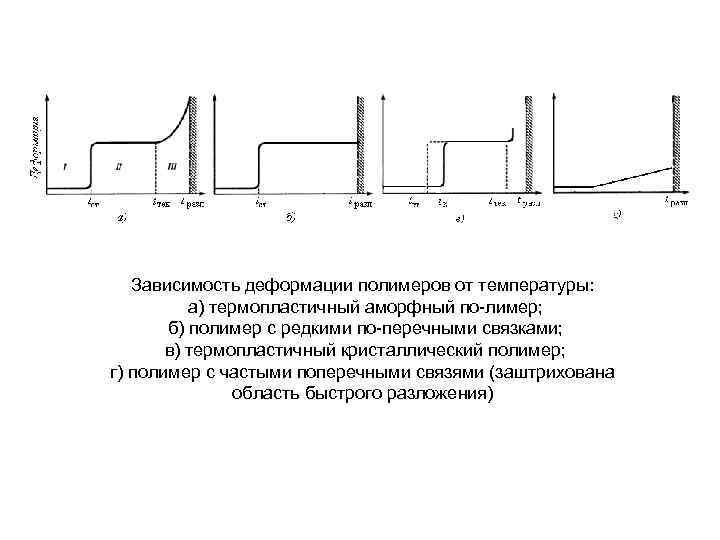 Зависимость деформации полимеров от температуры: а) термопластичный аморфный по лимер; б) полимер с редкими по перечными связками; в) термопластичный кристаллический полимер; г) полимер с частыми поперечными связями (заштрихована область быстрого разложения)
Зависимость деформации полимеров от температуры: а) термопластичный аморфный по лимер; б) полимер с редкими по перечными связками; в) термопластичный кристаллический полимер; г) полимер с частыми поперечными связями (заштрихована область быстрого разложения)
 Схематичное изображение молекулярных процессов при деформации: 1 – упругое, 2 – высокоэластичное, 3 – вязкое
Схематичное изображение молекулярных процессов при деформации: 1 – упругое, 2 – высокоэластичное, 3 – вязкое
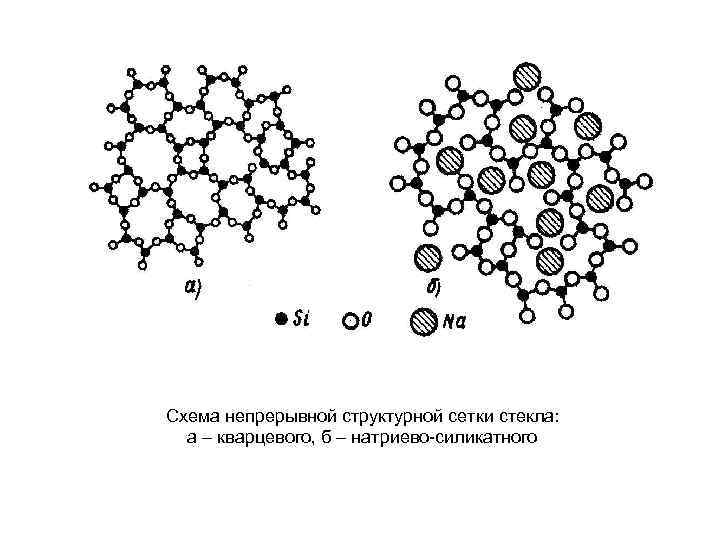 Схема непрерывной структурной сетки стекла: а – кварцевого, б – натриево силикатного
Схема непрерывной структурной сетки стекла: а – кварцевого, б – натриево силикатного
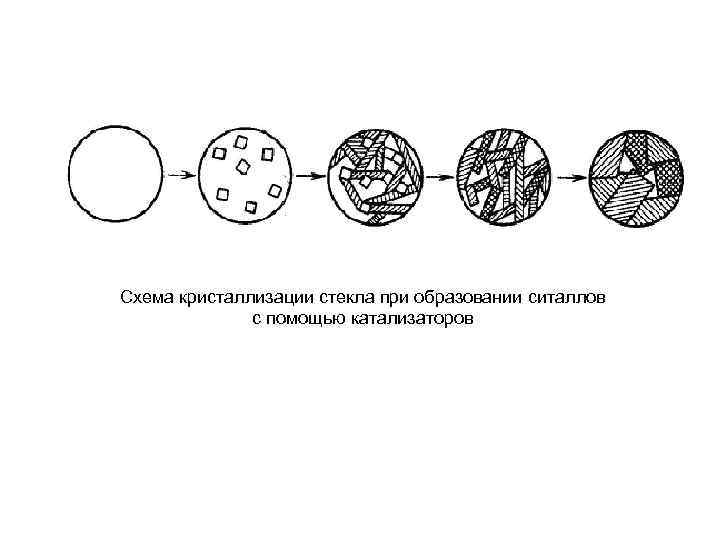 Схема кристаллизации стекла при образовании ситаллов с помощью катализаторов
Схема кристаллизации стекла при образовании ситаллов с помощью катализаторов
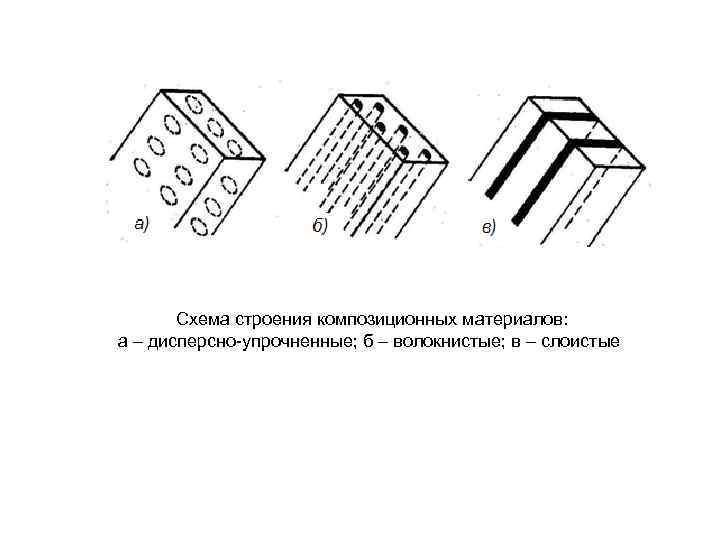 Схема строения композиционных материалов: а – дисперсно упрочненные; б – волокнистые; в – слоистые
Схема строения композиционных материалов: а – дисперсно упрочненные; б – волокнистые; в – слоистые
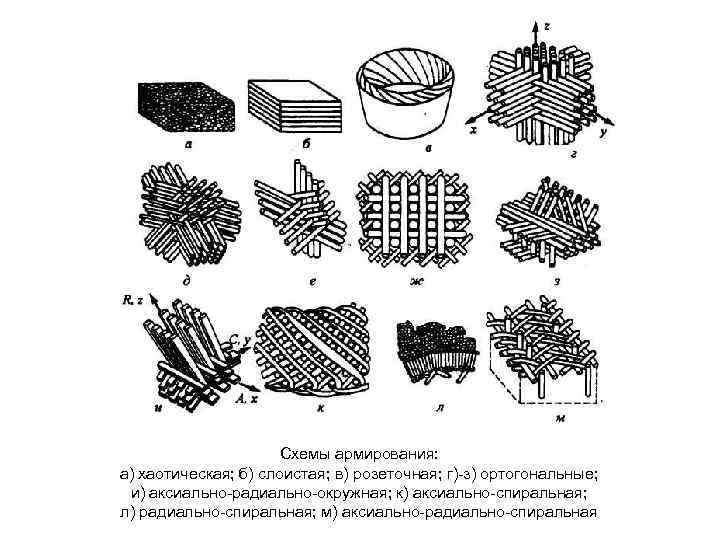 Схемы армирования: а) хаотическая; б) слоистая; в) розеточная; г) з) ортогональные; и) аксиально радиально окружная; к) аксиально спиральная; л) радиально спиральная; м) аксиально радиально спиральная
Схемы армирования: а) хаотическая; б) слоистая; в) розеточная; г) з) ортогональные; и) аксиально радиально окружная; к) аксиально спиральная; л) радиально спиральная; м) аксиально радиально спиральная


