КОЛОРЕКТАЛЬНЫЙ РАК.ppt
- Количество слайдов: 93

КОЛОРЕКТАЛЬНЫЙ РАК Кафедра онкологии СПб. ГМУ им. акад. И. П. Павлова д. м. н. В. В. Семиглазов к. м. н. В. В. Корхов И. Ю. Малых
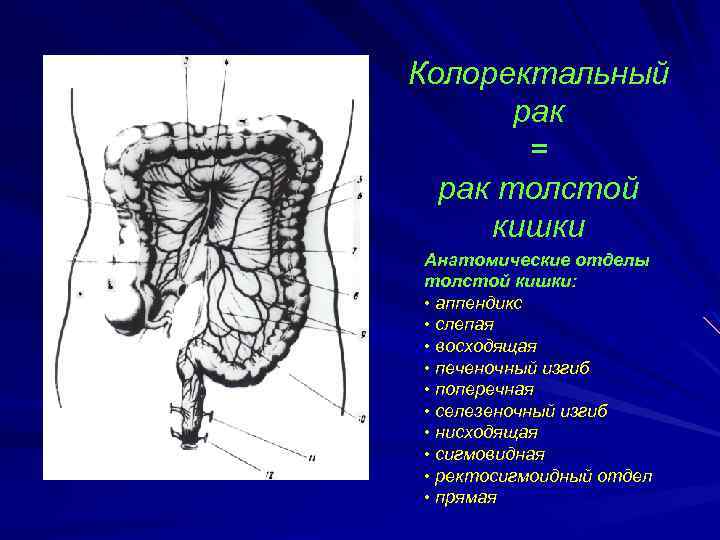
Колоректальный рак = рак толстой кишки Анатомические отделы толстой кишки: • аппендикс • слепая • восходящая • печеночный изгиб • поперечная • селезеночный изгиб • нисходящая • сигмовидная • ректосигмоидный отдел • прямая

Ежегодно в мире регистрируется более 600 тысяч случаев рака толстой кишки. Накопленный контингент составляет более 3, 5 млн человек. В США рак ободочной кишки встречается в 2 раза чаще, чем рак прямой кишки. В США рак толстой кишки вышел на первое место. В России рак толстой кишки занимает 3 место. Частота рака ободочной кишки составляет 11, 6 у мужчин и 9, 2 у женщин на 100 000 тыс. населения. Заболеваемость раком прямой кишки среди мужчин 11, 0, среди женщин 7, 1. В Москве за 15 лет рак толстой кишки возрос с 10, 2 до 17, 2. Наиболее часто рак толстой кишки выявляется у лиц старше 50 лет.

Около 80% новообразований локализуется в ампулярной части прямой кишки. Почти одинаково часто ( 24 27% ) пораженными оказываются верхняя, средняя и нижняя треть. Приблизительно в 10% случаев опухоли занимают всю ампулу прямой кишки или большую ее часть. В ректосигмоидном отделе новообразования встречаются с частотой, не превышающей 10%. Промежностный отдел оказывается местом возникновения опухолей в 3 4 % случаев Первично множественный рак обнаруживают у 2 12 % больных.

По С. А. Холдину выделяют: 1) Экзофитные опухоли, растущие в просвет кишки в виде полипообразных, капустообразных или несколько более уплощенных форм, иногда с изъязвленной поверхностью, 2) Эндофитные раки в виде язвы, проникающей в стенку кишки, иногда с утолщенными валикообразно выступающими плотными краями, 3) Диффузные инфильтрирующие опухоли, распространяющиеся в толще кишечной стенки и приводящие ее к уплотнению и утолщению. 4) Плоскостные раки в виде язвы со слегка утолщенными краями, обычно в аноперинеалыюй области.

Международная гистологическая классификация: 1) аденокарцинома (высоко. умеренно и низко дифференцированная), 2) слизистая аденокарцинома ( мукоидный, слизистый, коллоидный рак), 3) перстневидно клеточный рак ( мукоцеллюлярный ), 4) плоскоклеточный рак, 5) железисто плоскоклеточный рак 6) недиффернцированный рак 7) неклассифицируемый рак Чаще всего ( 90% ) встречаются аденокарциномы различной степени дифференцировки. Частота плоскоклеточных опухолей не превышает 5 6%.

Размеры новообразований колеблются в широких пределах. При экзофитных раках распространение опухоли в стенке прямой кишки не выходит заметно за пределы макроскопически определяемых краев. При эндофитных раках, напротив, более, чем в 1/2 случаев выявляется распространение за пределы макроскопических краев, в большей степени в проксимальном направлении. При язвенно ипфильтративиых опухолях оно составляет 1, 5 2 см, а при диффузных достигает 6 7 см. Длительное наблюдение за больными, отказавшимися от лечения, показало, что распространение опухоли на 1/4 окружности происходит приблизительно за 6 месяцев. В толще стенки кишки опухоль растет в виде конуса с основанием в слизисто подслизистом слое и верхушкой, направленной к серозному покрову.

Внекишечное распространение рака прямой кишки происходит, в основном, лимфогепным путем. При раке ректосигмоидного и верхнеампулярного отделов чаще поражаются верхние прямокишечные забрюшинные лимфатические узлы. Рак среднеампулярного отдела метастазирует в этот же лимфоколлектор, а также в подвздошные лимфатические узлы на боковых стенках таза, реже в паховые. При раке нижнеампулярного и промежностного отделов метастазы наблюдаются в паховых, наружных и общих подвздошных лимфатических узлах. Наиболее склонны к метастазированию низкодифференцированные аденокарциномы солидные и плоскоклеточные раки. Частота метастазов в лимфатических узлах регионарных зон колеблется от 31 до 61% . Ретроградное метастазирование отмечено сравнительно редко и составляет не более 1, 3%. При гематогенном метастазировании чаще всего поражается печень ( по данным В. Д. Федорова 13, 4% ), реже легкие, головной мозг, кости. Имплантационные метастазы распространяются по брюшине. Отдаленные метастазы обнаруживаются почти у каждого третьего больного, умершего от рака прямой кишки.

В соответствии с официальными указаниями Минздрава оценка степени распространения рака прямой кишки сводится к IV стадиям: Международная классификация TNM (шестое издание, 2003 г. ) Прямая и ободочная кишка T Первичная опухоль TХ Недостаточно данных для оценки первичной опухоли Т 0 Первичная опухоль не определяется Tis Интраэпителиальная или с инвазией в слизистой оболочки ичная опухоль T 1 С инфильтрацией стенки кишки до подслизистой оболочки опухоль T 2 – С инфильтрацией мышечного слоя T 3 – С инфильтрацией субсерозы или неперитонизированных участков кишки Т 4 – С прорастанием висцеральной брюшины или распространением на соседние органы и структуры

N – Регионарные лимфатические узлы NХ Недостаточно данных для оценки регионарных узлов N 0 – Нет признаков метастатического поражения узлов N 1 – Метастазы в 1 3 регионарных узлах N 2 Метастазы в 4 и более регионарных узлах

М – отдаленные метастазы p. N 0 – при гистологическом анализе должно исследоваться не менее 12 лимфатических узлов
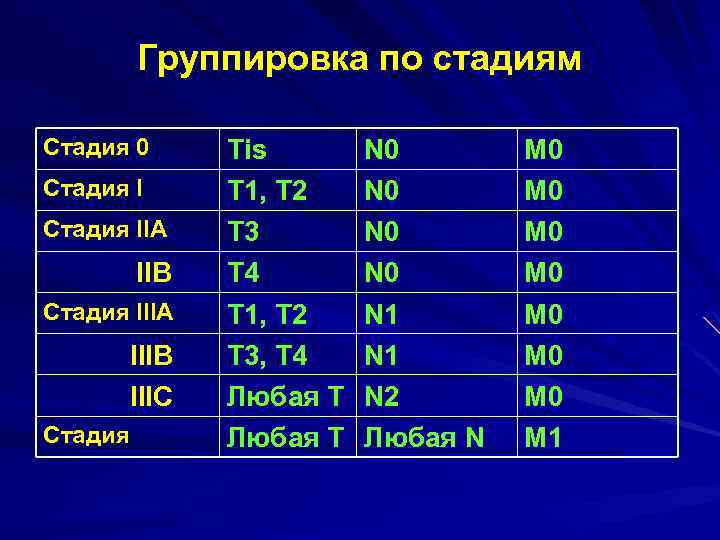
Группировка по стадиям Стадия 0 Стадия IIA IIB Стадия IIIA IIIB IIIC Стадия Tis T 1, T 2 T 3 T 4 T 1, T 2 T 3, T 4 Любая Т N 0 N 0 N 1 N 2 Любая N M 0 M 0 M 1

Анальный канал T Первичная опухоль TХ Недостаточно данных для оценки первичной опухоли Т 0 Первичная опухоль не определяется Tis Преинвазивная опухоль ( Carcinoma in situ) T 1 Опухоль до 2 см в наибольшем измерении T 2 – Опухоль до 5 см в наибольшем измерении T 3 – Опухоль более 5 см в наибольшем измерении Т 4 – Опухоль любого размера, прорастающая соседние органы: влагалище, мочеиспускательный канал, мочевой пузырь

N – Регионарные лимфатические узлы NХ Недостаточно данных для оценки регионарных узлов N 0 – Нет признаков метастатического поражения узлов N 1 – Метастазы в околопрямокишечных лимфатических(ом) узлах(е) N 2 Метастазы в подвздошных или паховых лимфатических(ом) узлах(е) N 3 Метастазы в околопрямокишечных и паховых лимфатических узлах и/или в подвздошных и/или паховых с обеих сторон М – отдаленные метастазы
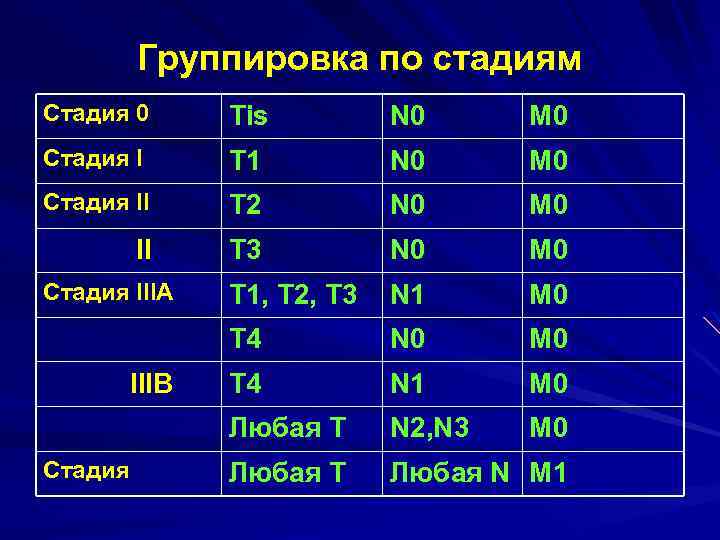
Группировка по стадиям Стадия 0 Tis N 0 M 0 Стадия I T 1 N 0 M 0 Стадия II T 2 N 0 M 0 II T 3 N 0 M 0 Стадия IIIA T 1, T 2, Т 3 N 1 M 0 T 4 N 0 M 0 Т 4 N 1 M 0 Любая Т N 2, N 3 M 0 Любая Т Любая N M 1 IIIB Стадия

Классификация Дюкса (Dukes) Группа А опухоль, прорастающая только стенку кишки, без метастазов в регионарных лимфатических узлах Гриппа В опухоль, прорастающая в параректальную жировую клетчатку, без метастазов в регионарных лимфатических узлах Группа С опухоль, прорастающая параректальную жировую клетчатку, метастазами в регионарных лимфоузлах в с
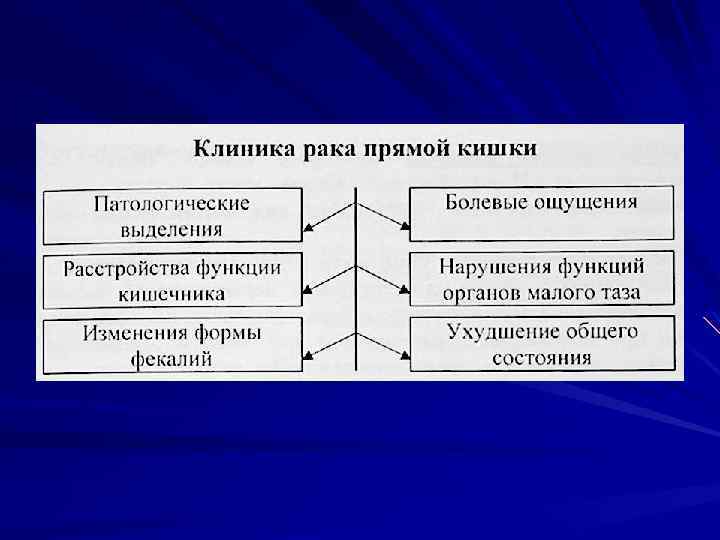

Патологические выделения появляются в сравнительно раннем периоде рака прямой кишки. Наиболее частое явление — примесь крови, которая при опухолях ампулы достигает 80 90%. Кровь обычно предшествует каловым массам, как правило, бывает измененной, но иногда, в виде полоски или отдельных капелек располагается на одной из сторон фекалий в зависимости от места опухоли. Изредка могут возникать массивные кровотечения. Слизь чаще наблюдается в смеси с другими выделениями, например, с кровью, приблизительно у 1/3 больных. Она выделяется небольшими скоплениями или хлопьями, в основном, при проксимально расположенных опухолях. Распад и изъязвление новообразования могут повлечь развитие ректита на почве вторичной инфекции с выделением гноя.

Функциональные расстройства разнообразны и менее специфичны. Причина в рефлекторных раздражениях. Не менее 3/4 больных жалуются на нарушения ритмичной деятельности кишечника. Около 1/3 отмечают задержку стула, а у 1/5, напротив, встречаются поносы. Тенезмы констатированы у каждого пятого больного, иногда до 15 20 раз в сутки, чаще и интенсивнее при опухолях ректосигмоидного и верхнеампулярного отделов. Выраженные в той или иной степени нарушения проходимости на почве рака прямой кишки наблюдаются в 20% случаев. Недержание газов и кала наступает при непосредственной инфильтрации сфиктера опухолью. Однако, вначале характерно судорожное сокращение сфинктера из за резкой болезненности (2 3% больных).

Изменения формы фекалий при раке прямой кишки встречаются редко ( 5% ). Каловые массы могут оказаться стющенными. иметь округлый . шаровидный вид, форму тонких нитей или тяжей. Боль не относится к ранним симптомам ( 60% больных). При раке ректосигмоидного отдела она связана с перистальтикой и вначале кратковременна. При раке ампулы боль постоянная, ноющая, усиливается при дефекации, иррадиирует в низ живота, задний проход, копчик, обусловлена прорастанием стенки кишки. Только при раке анального канала она появляется сравнительно рано и становится доминирующим симптомом, так как носит жгучий характер, еще больше усиливаясь при дефекации. Нарушения функции органов малого таза происходят при их вовлечении в опухолевый процесс (5% случаев). Это касается мочевыводящих путей. У женщин возможно прорастание опухоли прямой кишки в тело, шейку матки, заднюю стенку влагалища. Ухудшение общею состояния в виде анемизации, снижения аппетита, похудания, нарушения водно электролитного баланса, белкового обмена связано с более поздними проявлениями болезни.

Симптоматика рака прямой кишки определяется локализацией, формой роста и степенью распространения. Для эндофитных опухолей ректосигмоидного отдела характерны симптомы кишечной непроходимости. Основной симптом при ампулярном раке кровянисто слизистые выделения. При раке промежностного отдела наиболее выражены тенезмы и боли. Позднее появление болей в области малого таза с иррадиацией в нижние конечности свидетельствует о прорастании опухоли в параректальную клетчатку, стенки таза, крестец. Вместе с тем, приблизительно в 2 2, 2 % случаев можно констатировать отсутствие симптомов проявления болезни.
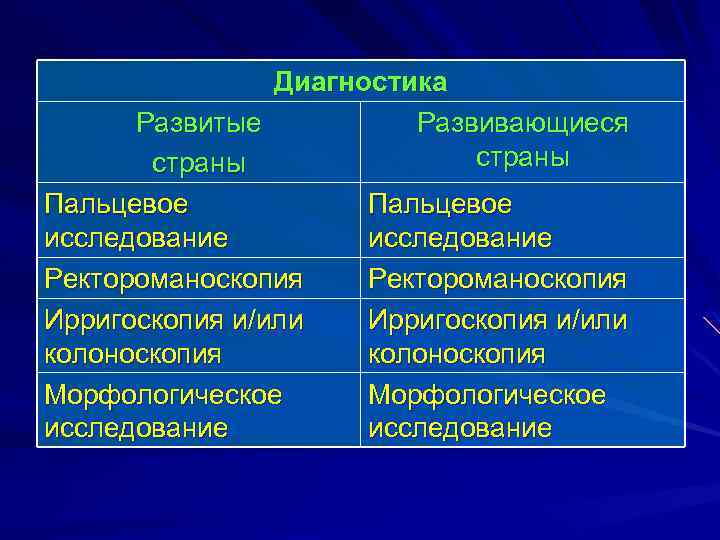
Диагностика Развитые Развивающиеся страны Пальцевое исследование Ректороманоскопия Ирригоскопия и/или колоноскопия Морфологическое исследование

Диагностика рака прямой кишки, в принципе, не представляет трудностей. Если врач, или сам больной подумали об опухолевой патологии, то в 30% случаев обеспечено установление диагноза. Практически достаточно только пальцевого исследования и ректороманоскопии для подтверждения предполагаемого диагноза.

При пальцевом исследовании после очистительной клизмы, последовательно ощупываются стенки прямой кишки. Это исследование должно проводиться в различных положениях больного: 1) на спине с умеренно согнутыми в коленных суставах ногами, 2) на спине с приведенными к животу ногами и с приподнятым тазом (у женщин бидигитально и бимануально), 3) в коленно локтевом положении при котором за счет перемещения кишечника к диафрагме создаются хорошие условия для пальпации органов и стенок малого таза, 4) на корточках, благодаря чему удается достигнуть опухоли даже на расстоянии более 9 см от заднего прохода. 5) на левом боку с приведенными к животу ногами для исследования опухоли на боковых стенках кишки.

Для рака характерны: 1) Плотная консистенция особенно в области основания опухоли 2) Изъязвление с четко определяемыми уплотненными и утолщенными, иногда валикообразными краями, 3) Инфильтрация стенки кишки без четких границ 4) Кольцевидное сужение просвета, 5) Ригидность стенки кишки с тенденцией к фиксации со смежными органами, 6) патологические выделения. При пальцевом исследовании возможно не менее, чем в 70% случаев диагностировать рак прямой кишки, а также выявить глубину прорастания опухоли, ее смещаемость, взаимоотношение со смежными органами, увеличенные лимфатические узлы на стенках таза, составив, тем самым, объективное представление о степени распространения процесса.

Ректороманоскопия позволяет осмотреть 30 см кишки. Подготовка больного требует назначения слабительных средств с очистительными клизмами. Ректороманоскопия, как правило, выполняется в коленно локтевом положении с прогнутой в поясничном отделе спиной. У ослабленных больных возможно положение на боку с приведенными к животу ногами. В металлический тубус ректороманоскопа вставляют обтуратор с закругленным концом, прибор смазывают вазелиновым маслом и вводят в кишку на глубину 5 6 см. Дальнейшее продвижение должно проводиться под контролем зрения с освещением и поддуванием воздуха. Направляя тубус ректороманоскопа в соответствии с анатомическими изгибами кишки, врач видит открывающийся просвет. Однако, в деталях слизистая оболочка осматривается при извлечении инструмента медленными винтообразными движениями. Рак прямой кишки имеет вид экзофитного или блюдцеобразного плотного бугристого образования темно красного цвета, легко кровоточащего с участками распада и фибринозными наслоениями. Эндофитные опухоли выглядят в виде белесоватого циркулярного сужения, иногда с плоским изъязвлением. Обнаружив опухоль, следует взять кусочек для гистологического и цитологического исследований. Биопсия производится специальными щипцами конхотомом из наиболее подозрительного периферического участка опухоли, граничащего со слизистой оболочкой кишки.

ИРРИГОСКОПИЯ имеет значение не только для диагностики опухоли, но и для выявления анатомофупкциональных особенностей толстой кишки. Подготовка к рентгенологическому исследованию предусматривает перевод больного на бесшлаковую диету в течении 2 3 дней, прием накануне однократной дозы касторового масла или сульфата магния, вечером и утром за 2 часа очистительные клизмы до чистой воды. Контрастную клизму приготавливают из расчета 400 г бариевой взвеси на 1 л воды. Заполнение кишки производят поэтапно с обязательным выполнением рентгенограмм. После опорожнения кишечника производится рентгенография рельефа слизистой оболочки, а затем выполняют обзорные и прицельные рентгенограммы в условиях двойного контрастирования, раздувая кишку воздухом. К прямым рентгенологическим признакам рака прямой кишки относятся дефект наполнения, изменение рельефа слизистой оболочки, ригидность стенки кишки, сужение просвета. К косвенным симптомам спазм стенки кишки, отсутствие гаустрации. расширение просвета проксимальнее и дистальнее пораженного участка, неполная эвакуация контрастного вещества после дефекации. Рентгеносемиотика рака прямой кишки зависит от размеров, локализации, анатомического типа опухоли, а также от сопутствующих изменений стенки органа.

Фиброколоноскопия в последнее время приобретает все большее значение. Подготовка к этому исследованию должна быть такой же тщательной, как и к ирригоскопии. Колоноскоп с управляемым дистальным концом и оптической системой прямого обзора позволяет осуществить осмотр слизистой оболочки практически на всем протяжении толстой кишки. Затруднения возникают из за петлеобразования, фиксации или стриктуры отдельных участков. Диагностическая ценность фиброколоноскопии повышается возможностью выполнения прицельной биопсии.

Стадирование Развитые страны Развивающиеся страны Трансректальное УЗИ печени и забрюшинных лимфоузлов КТ или ЯМР Рентген грудной клетки в/в урография УЗИ печени и забрюшинных лимфоузлов Рентген грудной клетки Кровь на РЭА


Хирургическое лечение рака прямой кишки предусматривает выполнение операций в соответствии с анатомической зональностью и футлярностыо, прежде всего, с учетом локализации опухоли.
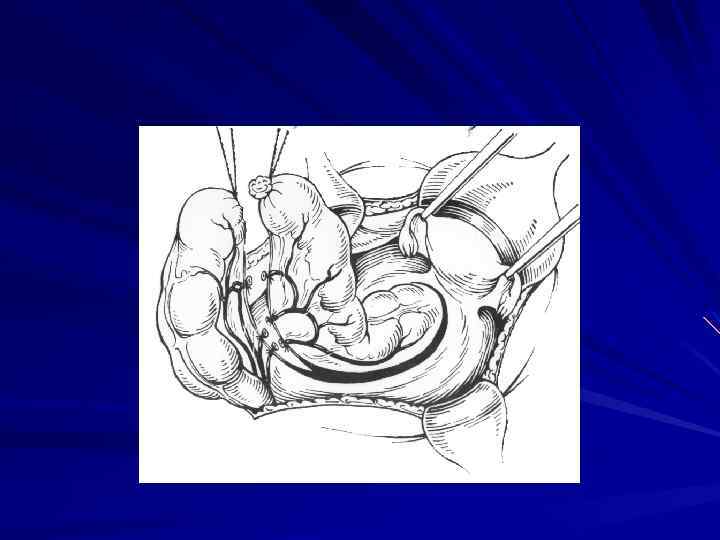
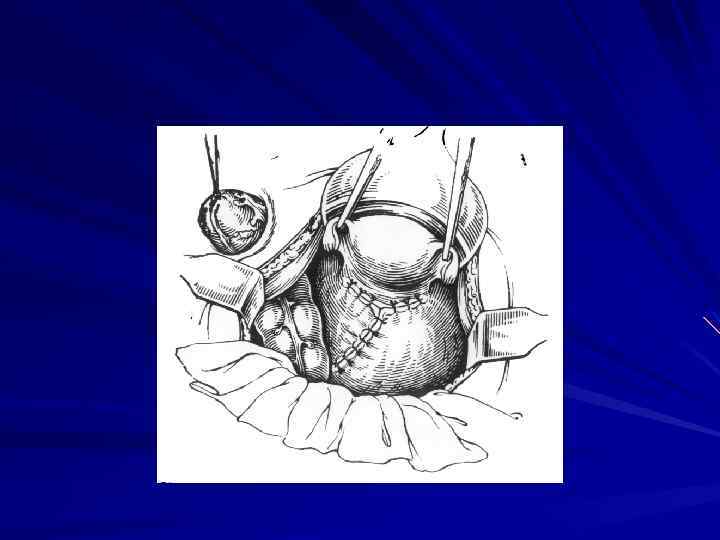
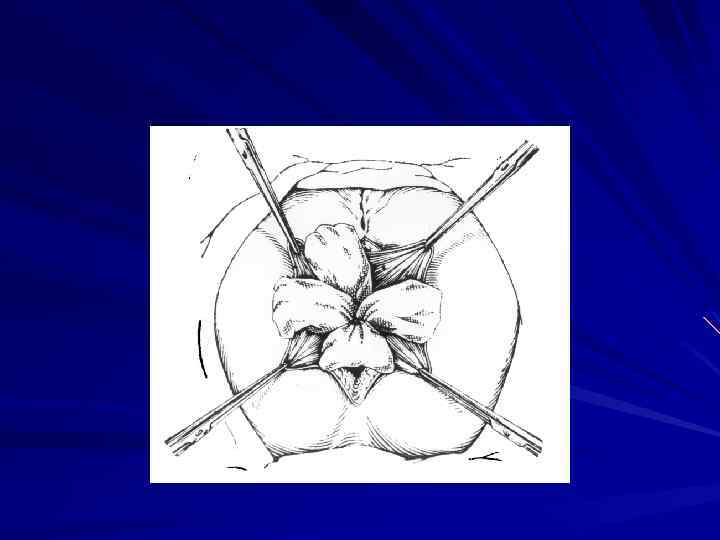
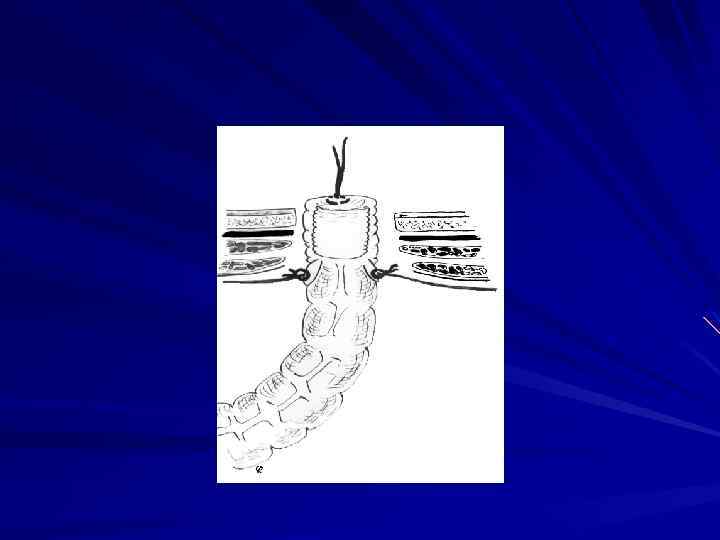
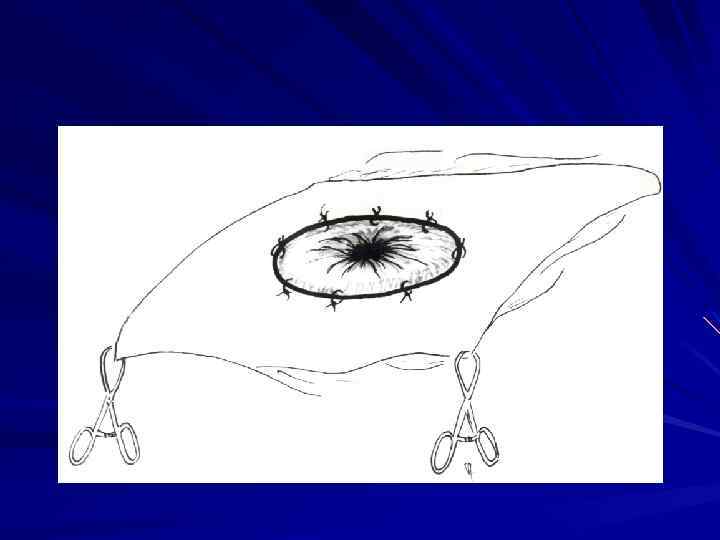
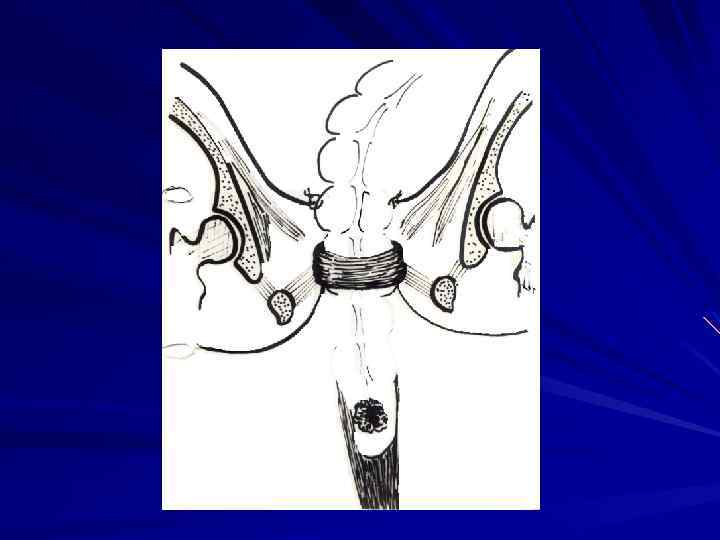
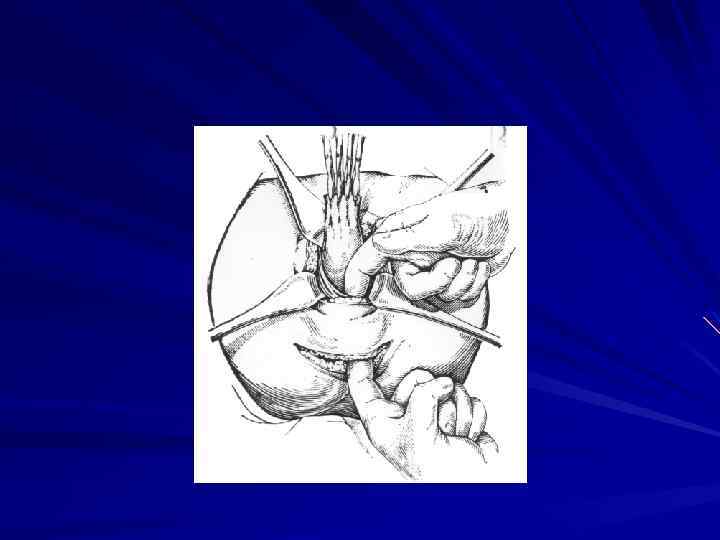

Местнораспространенные опухоли с вовлечением прилежащих тканей и органов или путей лимфооттока, например, подвздошных, паховых лимфатических узлов требуют применения расширенных и комбинированных операций (возможно, сфинктерсохраняющего характера).

Комбинированный метод является наиболее эффективным при раке прямой кишки II - Ш стадии. В современных схемах комбинированного лечения наряду с хирургическим компонентом применяется не только лучевая, но и химиотерапия. Химиолучевое лечение состоит из 2 фаз: совместное использование цитостатика и ионизирующей радиации с целью потенциирующего эффекта и последующих курсов химиотерапии с целью воздействия на микрометастазы. Однако, наиболее распространена комбинация операции с облучением, которое назначается или в пред - или в послеоперационном периодах. Хирургические вмешательства должны отвечать требованиям онкологического радикализма.

В предоперационном периоде в основном проводится дистанционное облучение: 1) СОД 40 50 Гр при разовых дозах 2 2, 5 Гр на протяжении 3 5 недель и операцией после 3 4 недельного перерыва, 2) разовые дозы 4 5 Гр, СОД 20 30 Гр или по 6, 5 Гр до 19, 5 Гр и операцией через I 3 дня, 3) укрупненная или крупная фракция облучения однократно накануне или в день операции. Реже используются сочетанные методики. После операции облучение применяется в режиме классического фракционирования с уровнем СОД 60 Гр, а при "сендвич" технике 30 Гр. Дальнейшее повышение эффективности лучевой терапии связано с нетрадиционными схемами фракционирования дозы и с дополнительным назначением радиомодификаторов.

Лучевая терапия, как радикальный метод, находит применение только при плоскоклеточном раке анального канала, доводя СОД до 70 Гр. В этих случаях обоснована сочетанная методика, при которой применяются разнообразные режимы дистанционного и внутриполостного облучения.

Хирургический компонент в виде брюшно промежностной экстирпации (БПЭ) прямой кишки применяется только в случаях частичного регресса, а также при возникновении рецидива опухоли. При развитии гнойно некротических осложнений возможно формирование колостомы или выполнение БПЭ прямой кишки.

Паллиативное лечение рака прямой кишки – хирургическое, лучевое, лекарственное. Хирургическое лечение при общем удовлетворительном состоянии больного возможно в объеме радикальных операций, но как правило, за исключением расширенных и комбинированных вмешательств.

Результаты радикалыюго лечения рака прямой кишки. Осложнения после радикальных операций на прямой кишке крайне разнообразны и возникают более, чем у половины больных. Летальность составляет 4 5% (после расширенных и комбинированных вмешательств 10 12% ). Сфинтерсохраняющие операции практически в 2. 5 раза менее опасны, чем экстирпация прямой кишки. Пятилетняя выживаемость достигает 45 65%. У больных, оперированных по поводу верхнеампулярпого рака прямой кишки, 5 летнее выздоровление наблюдается в 65% случаев, а при опухолях нижнеампулярного и промежностного отделов в 46 47%. По данным Московского НИОИ им. П. А. Герцена 5 лстияя выживаемость при поражении слизистой оболочки прямой кишки составляет 93%. при прорастании опухоли в подслизистый слой 57%. а при вовлечении параректальной клетчатки 37%. В случаях отсутствия регионарных метастазов 5 летняя выжи ваемость достигает 50 60%, а при их наличии снижается до 30%. По сравнению с хирургическим методом комбинированное лечение позволяет улучшить 5 летнюю выживаемость на 7 12% за счет уменьшения частоты рецидивов.

В отношении функциональных результатов даже после экстирпации прямой кишки большинство больных приспосаб ливаются к налаженному 1 2 кратному опорожнению кишечника в определенные часы. Изучение проблемы реабилитации показало, что почти 2/3 ольных после брюшно анальной резекции и У 3 после брюшно иромежностной экстирпации прямой кишки возобновляют трудовую леятельность на протяжении 3 6 месяцев.

Лечение рецидивов и метастазов рака прямой кишки Различаются локальные и регионарные рецидивы рака прямой кишки. Локальные рецидивы подразделяются на резидуальные и имплантационные и возникают в зоне опухоли или в непосредственной близости от операционного поля в стенке кишки, окружающей клетчатке, смежных органах. Регионарные рецидивы развиваются из неудаленных лимфатических узлов. Симптоматическая лекарственная терапия не является методом выбора в лечении рецидивов. При локальных рецидивах ведущая роль принадлежит хирургическому лечению, возможно в комбинации с лучевой терапией. В случаях регионарных рецидивов наряду с лучевой применяется химиотерапия с предварительным формированием при необходимости противоестественного заднего прохода. Методики лечения отдаленных метастазов рака прямой кишки, локализующихся преимущественно в печени, постоянно совершенствуются. При возможности целесобразно хирургическое удаление одиночных метастазов с последующей химиотерапией

СИМПТОМАТИЧЕСКОЕ лечение рака прямой кишки - хирургическое (противоестественный задний проход), - лучевое (обезболивающий и противовоспалительный эффект), - лекарственное (устранение симптомов заболевания и осложнений специфической терапии).

Скрининг рака ободочной кишки проводится с помощью следующих методов: • гемоккультного теста • сигмоидоскопии

При проведении скрининга среди формально здорового населения от 2 до 6% обследован ных имеют положительный гемоккульттест. При последующем обследовании лиц, имеющих положительный тест на наличие скрытой крови в кале, рак ободочной кишки выявляется в 5 – 10%, а железистые аденомы –в 20– 40% случаев. Следует подчеркнуть, что проведение гемоккультного теста имеет ряд ограничений. В нормальных условиях постоянная потеря крови из кишечника составляет 2 мл ежедневно. Для того, чтобы тест был надежноположительным, необходима ежедневная потеря крови не менее 20 мл.

Таким образом, в 50 -75% случаев тест бывает ложноположительным. Но главным недостатком этого метода является низкая специфичность - частота ложноотрицательных результатов при наличии рака может достигать 50%, а при аденомах ободочной кишки – 70% наблюдений.

Обследование лиц после положительных гемоккульттестов (в том числе при ложноположительных результатах) повышает частоту выявления аденом и опухолей толстой кишки на ранних стадиях

Риск развития колоректального рака в европейской популяции составляет 4 5% (в течение жизни 1 из 20 человек заболевает раком этой локализации).

Колоноскопия и рентгенологическое исследование толстой кишки являются более предпочтительными и точными методами скрининга, чем гемоккульттести сигм оидоскопия. Однако, возможность использования этих м етодик для широкого скрининга является сомн ительной изза их большей сложности и высокой стоимости (стоимость геммокульттеста – 15$; сигмоидоскопии – 325$; фиброколоноскопии 1300$)

В настоящее время различные методы скрининга рекомендуется проводить с разной периодичностью в зависимости от степени риска среди групп населения. Так, среди лиц старше 50 лет и не имеющих факторов риска развития колоректального рака, считается достаточным проведение гемоккульттеста 1 раз в год. Выполнение сигмоидоскопии гибким сигмоидоскопом в этой группе рекомендуется каждые 3– 5 лет. Рентгенологическое исследование толстой кишки с двойным контрастированием следует производить каждые 5– 10 лет, либо каждые 10 лет выполнять колоноскопию.

Скрининг среди лиц с факторами риска следует начинать в более раннем возрасте, и он должен быть основан на учете индивидуального риска развития рака. Группы населения, имеющие высокий риск развития рака, например, при наследственном неполипозном колоректальном раке или семейном диффузном полипозе, должны подвергаться генетическому консультированию д ля выявления других локализаций карцином и проведению более интенсивного скрининга, начиная с 35 – 40 летнего возраста. Сигмоидоскопия либо колоноскопия подобным п ациентам должна выполняться ежегодно

В нашей стране для раннего выявления рака пользуется идея формирования так называемых «групп риска» . С помощью специальных вопросников или компьютерных программ возможно выделение части популяции, в которой будет выявляться большинство опухолей. По замыслу исследователей это позволит ограничиться обследованием, например, 20% населения, а выявить не менее 80% всех раков. Проблема, однако, состоит в том, что до настоящего времени неизвестны факторы риска, которые обладали бы подобным относительным риском (они должны увеличивать вероятность развития заболевания в 100 раз и более). Наиболее значимые из известных факторов увеличивают этот показатель не более чем в 5– 10 раз.
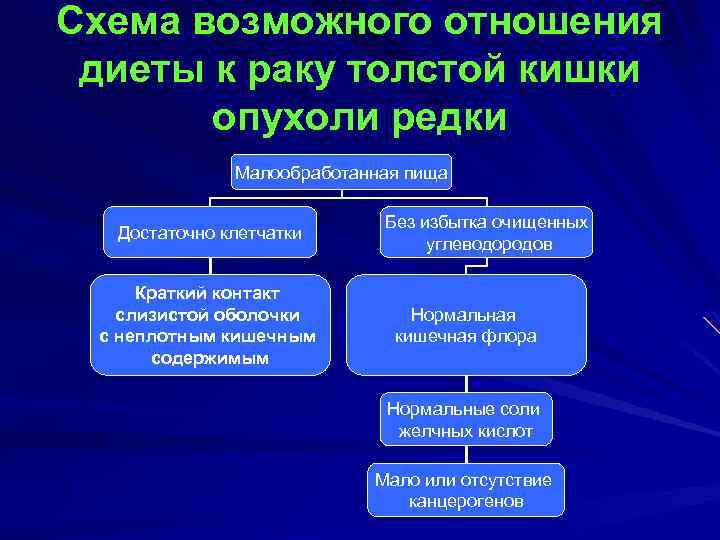
Схема возможного отношения диеты к раку толстой кишки опухоли редки Малообработанная пища Достаточно клетчатки Краткий контакт слизистой оболочки с неплотным кишечным содержимым Без избытка очищенных углеводородов Нормальная кишечная флора Нормальные соли желчных кислот Мало или отсутствие канцерогенов
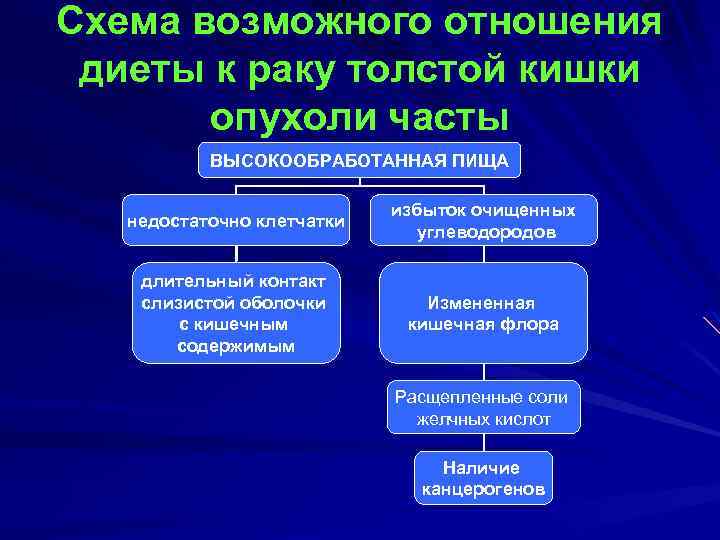
Схема возможного отношения диеты к раку толстой кишки опухоли часты ВЫСОКООБРАБОТАННАЯ ПИЩА недостаточно клетчатки избыток очищенных углеводородов длительный контакт слизистой оболочки с кишечным содержимым Измененная кишечная флора Расщепленные соли желчных кислот Наличие канцерогенов

Риск развития колоректального рака Предрасполагающие заболевания Риск (%) Язвенный колит 30 50 Болезнь Крона 20 35 Аденомы 20 Состояние после лечения рака толстой кишки, молочной железы, половых органов, 10 15 Сахарный диабет 10 15 Дивертикулез 5 10 Состояние после уретроколостомии 5 10

Генетические синдромы Наследственный неполипозный рак составляет около 10 % среди всех раков толстой кишки – диффузный семейный полипоз – синдром Гарднера–Тернера (полипоз ободочной и прямой кишки в сочетании с доброкачественными опухолями костей, мягких тканей и кожи). – синдром Пейтца–Джигерса (полипоз желудочно- кишечного тракта с пигментацией губ и щек). – болезнь Тюрка (диффузный полипоз толстой кишки с опухолями центральной нервной системы).

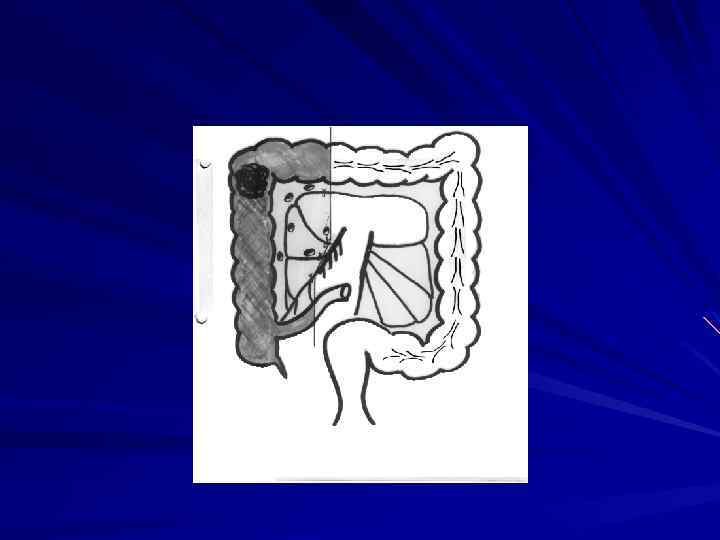
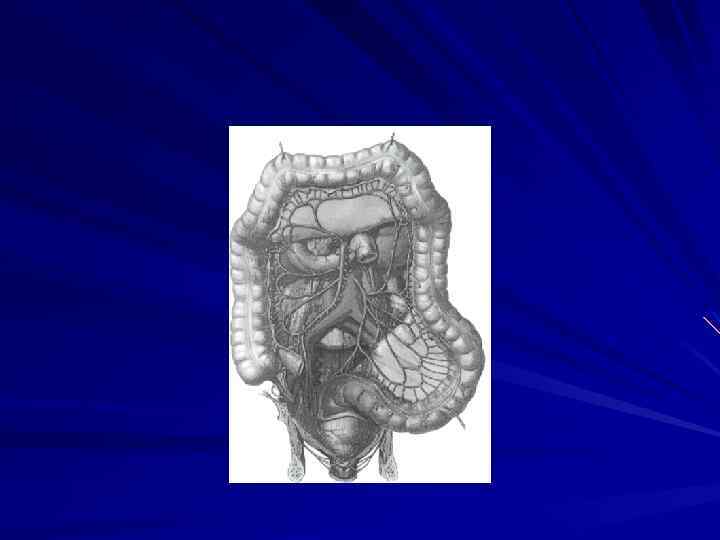
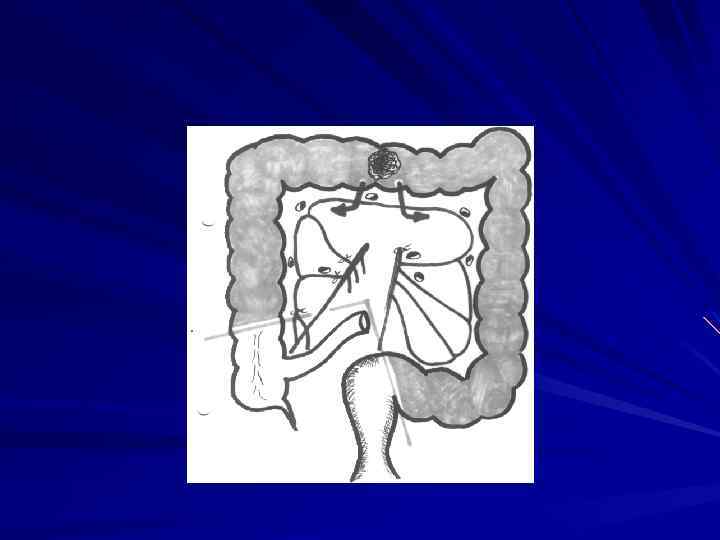
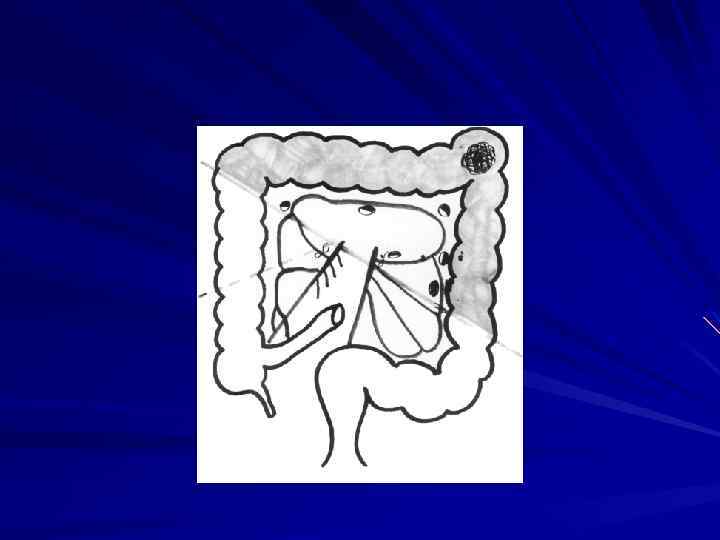
Распределение рака ободочной кишки ü Слепая кишка 25% ü Восходяший отдел ободочной кишки 9, 5% ü Поперечно ободочная кишка вместе с печеночным и селезеночным изгибами 17, 5% ü Нисходящий отдел ободочной кишки 5, 6% ü Сигмовидная кишка 42, 4%


Экзофитные формы составляют 52 63%, а эндофитные 48 37%. В правой половине ободочной кишки чаще встречаются экзофитные, а в левой – эндофитные формы.

Клинические формы рака ободочной кишки Ø Токсико анемическая Ø Обтурационная Ø Диспептическая Ø Псевдовоспалительная Ø Энтероколитическая Ø Опухолевая или атипическая

Адъювантное лечение – лекарственная терапия, направленная на уничтожение отдаленных микро метастазов с целью увеличения безрецидивной и общей выживаемости больных. Адъювантная химиотерапия должна быть начата в течение первых 5 недель после операции

В Западной Европе стандартной при адъювантном лечении больных раком ободочной кишки с регионарными метастазами считается комбинация 5 фторурацила и лейковорина. Лейковорин потенцирует способность 5 – фторурацила ингибировать активность фермента тимидилат синтетазы

Обычно проводится 6 циклов адъювантной терапии с интервалом в 4 недели. • лейковорин 20 мг/м 2 внутривенно с 1 го по 5 й день • 5 фторурацил 425 мг/м 2 внутривенно с 1 го по 5 йдень, вводится струйно сразу после лейковорина

Эффективность схемы (5 фторурацил + лейковорин) • понижается на 35% риск развития рецидива заболевания • понижается на 22% риск смерти от рака • повышается на 11% абсолютная выживаемость.
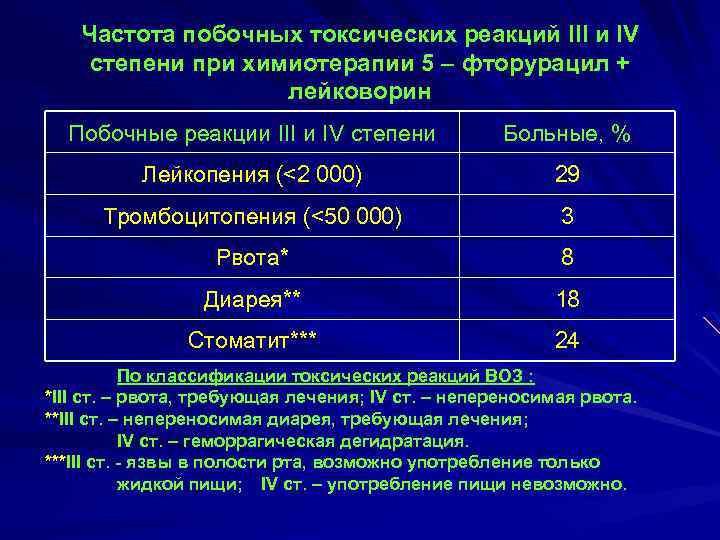
Частота побочных токсических реакций III и IV степени при химиотерапии 5 – фторурацил + лейковорин Побочные реакции III и IV степени Больные, % Лейкопения (<2 000) 29 Тромбоцитопения (<50 000) 3 Рвота* 8 Диарея** 18 Стоматит*** 24 По классификации токсических реакций ВОЗ : *III ст. – рвота, требующая лечения; IV ст. – непереносимая рвота. **III ст. – непереносимая диарея, требующая лечения; IV ст. – геморрагическая дегидратация. ***III ст. язвы в полости рта, возможно употребление только жидкой пищи; IV ст. – употребление пищи невозможно.

Схема 5 фторурацил+левамизол является стандарт ной в США для больных раком ободочной кишки с регионарными метастазами и включает: • 5 фторурацил 450 мг/(м 2 • сут) внутривенно в течение 5 дней, после 28 дневного интервала препарат вводится в дозе 450 мг/м 2 еженедельно в течение 11 мес • левамизол (декарис) принимается по 150 мг/сут в течение 3 дней каждые 2 нед в течение 12 мес. Точный механизм действия левамизола в данной схеме неизвестен, предполагается так называемое «иммуномодулирующее» действие.

Эффективность схемы (5 фторурацил + левамизол) • понижается на 40% риск развития рецидива заболевания • понижается на 33% риск смерти от рака • повышается на 12 15% абсолютная выживаемость.

Вопрос о целесообразности адъювантного лечения у больных без регионарных метастазов решается индивидуально при наличии других неблагоприятных прогностических признаков: • молодой возраст пациента • неблагоприятные гистологические признаки (прорастание стенки кишки, низкая дифференцировка) • неуверенность хирурга в радикальности вмешательства • повышение уровня раковоэмбрионального антигена выше нормы через 4 недели после операции.

В последние годы арсенал цитостатических препаратов, эффективных при раке ободочной кишки, пополнился рядом цитостатиков: томудекс, Иринотекан (кампто), оксалиплатин (элоксатин), кселода и УФТ. Эти препараты интенсивно изучаются как в монорежиме, так и в комбинации, в том числе в качестве адъювантного лечения. Предварительные результаты свидетельствуют, что, вероятно, в ближайшем будущем в стандартное адъювантное лечение больных раком ободочной кишки будут внесены коррективы.

В 2003 г. завершено международное исследование MOSAIC по использованию оксалиплатина и 5 ФУ с лейковорином, либо инфузий 5 ФУ и лейковорина. Вероятность 4 х летней безрецидивной выживаемости была выше (76% против 69%). Это различие более значимо при III стадии (70% и 61%). Основным побочным эффектом явилась периферическая нейропатия в 92% (в 12% III степени тяжести), однако спустя 18 месяцев неврологические отклонения сохранились лишь у 4%.

Использование биотерапии с адъювантной целью при раке ободочной кишки представляется очень перспективным. В настоящее время для этого применяются аутологичные вакцины и моноклональные антитела. Адъювантное применение аутологичной вакцины позволило достоверно снизить частоту рецидивов заболевания, а также число больных, умерших от данной опухоли. Причем эффективностьэтого метода оказалась сопоставимой с адъювантной химиотерапией. Основными побочными эффектами вакцинотерапии были изъязвление в месте введения (98%), лимфа денопатия (46%) и лихорадка в ближайшие 24 ч (40%).

Другим новым и также очень интересным направлением биотерапии при раке ободочной кишки является применение моноклональных антител. Эдреколомаб (панорекс) является мышиным моноклональным антителом к поверхностному антигену аденокарциномы 17 1 А Применение эдреколомаба позволило достоверно увеличить показатели общей и безрецидивной выживаемости больных. При этом препарат легко переносился, и его применение сопровождалось ограниченным числом побочных эффектов, наиболее значимыми из которых были анафилактические реакции на чужеродный белок (1, 8%). В нашей стране препарат эдреколомаб (панорекс) пока не зарегистрирован. .

Несомненным преимуществом моноклональных антител перед химиотерапией является возможность терапевтического воздействия на неделящиеся клетки в фазе G 0, которые обычно нечувствительны к цитостатикам. По этой причине чрезвычайно интересным представляется комбинация химиотерапии с моноклональными антителами. Подобное исследование проводится в в 250 онкологических центрах мира.
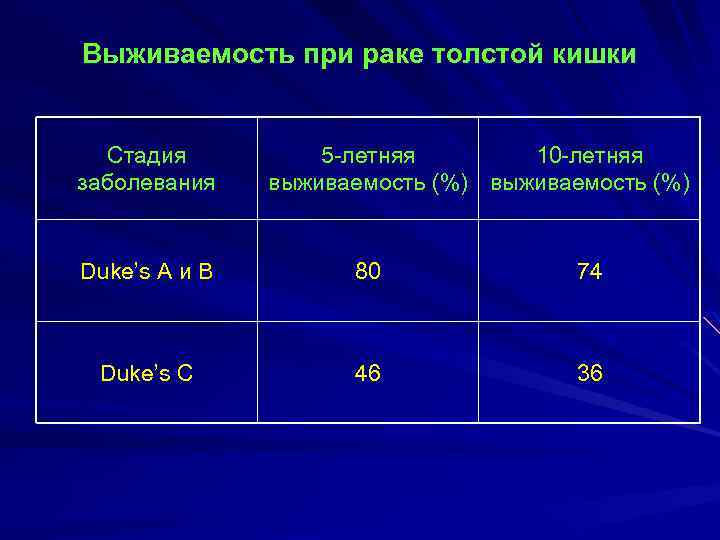
Выживаемость при раке толстой кишки Стадия заболевания 5 -летняя 10 -летняя выживаемость (%) Duke’s A и B 80 74 Duke’s C 46 36

Лечение метастатического рака ободочной кишки. Хирургическое лечение. Основной принцип – удаление всех новообразований в пределах здоровых тканей (100% циторедукция). Противопоказания к операциям по «радикальному плану» : 1) поражение печени, превышающее 50% объема 2) поражение чревного ствола и верхней брыжеечной артерии 3) тотальный карциноматоз висцеральной брюшины

Лекарственное лечение в адъювантном и неоадъювантном режимах. Наибольшего внимания заслуживают оксалиплатин и иринотекан. Эффективность режимов FOLFOX и FOLFIRI в качестве 1 и 2 линии метастатического рака сопоставимы. При режиме FOLFOX более выражена нейротоксичность, а при FOLFIRI нейтропения и алопеция.

Таргетная терапия. – воздействие на клеточные рецепторы или пути, передающие информацию в ядро клетки. Цетуксимаб (эрбитукс) – моноклональные антитела, блокирующее эпидермальный фактор роста (EGFR). Бевацизумаб (авастин) – моноклональные антитела к рецепторам сосудистого эндотелиального фактора роста (VEGF).

Применение современных режимов позволило преодолеть медиану общей выживаемости в 20 месяцев. У не леченных больных она составляла около 8 месяцев, а применении 5 ФУ/ЛВ – 11 месяцев.
КОЛОРЕКТАЛЬНЫЙ РАК.ppt