Коллоиды_дор.ppt
- Количество слайдов: 29
 Коллоидные растворы или золи
Коллоидные растворы или золи
 Коллоидные растворы или золи – это гетерогенные мелкодисперсные системы, в которых частицы дисперсной фазы не видны в микроскоп, хотя и значительно превышают размерами молекулы и ионы в истинных растворах. Золи занимают промежуточное место между истинными растворами и суспензиями (раствор глины и т. д. ), частицы которых хорошо различимы в микроскоп. Коллоидно-химические процессы играют большую роль в биологии, пищевой промышленности, производстве искусственных материалов и т. д.
Коллоидные растворы или золи – это гетерогенные мелкодисперсные системы, в которых частицы дисперсной фазы не видны в микроскоп, хотя и значительно превышают размерами молекулы и ионы в истинных растворах. Золи занимают промежуточное место между истинными растворами и суспензиями (раствор глины и т. д. ), частицы которых хорошо различимы в микроскоп. Коллоидно-химические процессы играют большую роль в биологии, пищевой промышленности, производстве искусственных материалов и т. д.
 СВОЙСТВА КОЛЛОИДНЫХ СИСТЕМ В 1861 -64 гг. английский ученый Грем, изучая диффузию различных растворов, заметил, что некоторые вещества (гидроксиды алюминия, железа, цинка, белки, танин и др. ) в растворах диффундируют очень медленно. Такие медленно диффундирующие вещества, по физическому строению напоминающие клей, Грем предложил назвать коллоидами (от греческого «колла» - клей).
СВОЙСТВА КОЛЛОИДНЫХ СИСТЕМ В 1861 -64 гг. английский ученый Грем, изучая диффузию различных растворов, заметил, что некоторые вещества (гидроксиды алюминия, железа, цинка, белки, танин и др. ) в растворах диффундируют очень медленно. Такие медленно диффундирующие вещества, по физическому строению напоминающие клей, Грем предложил назвать коллоидами (от греческого «колла» - клей).
 Установлено, что коллоиды образуют не особый класс соединений, а это особое состояние вещества. Многие вещества могут находиться как в коллоидной, так и в кристаллической формах. Известно, что если приготовить суспензию (взвесь) мела или глины в воде, то через некоторое время частицы суспензии осядут. Это явление называется седиментацией. Частицы же золя настолько малы (менее 1 мкм), что из-за хаотического теплового движения они никогда не оседают, пример – молоко. Это свойство золей называется седиментационной устойчивостью.
Установлено, что коллоиды образуют не особый класс соединений, а это особое состояние вещества. Многие вещества могут находиться как в коллоидной, так и в кристаллической формах. Известно, что если приготовить суспензию (взвесь) мела или глины в воде, то через некоторое время частицы суспензии осядут. Это явление называется седиментацией. Частицы же золя настолько малы (менее 1 мкм), что из-за хаотического теплового движения они никогда не оседают, пример – молоко. Это свойство золей называется седиментационной устойчивостью.
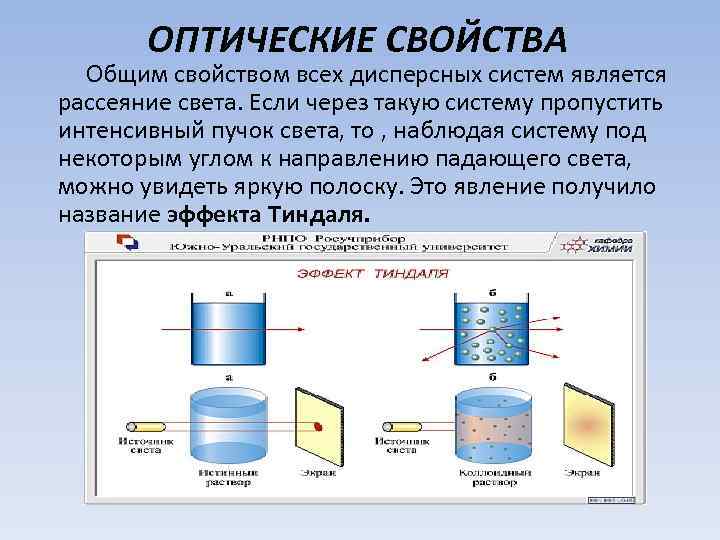 ОПТИЧЕСКИЕ СВОЙСТВА Общим свойством всех дисперсных систем является рассеяние света. Если через такую систему пропустить интенсивный пучок света, то , наблюдая систему под некоторым углом к направлению падающего света, можно увидеть яркую полоску. Это явление получило название эффекта Тиндаля.
ОПТИЧЕСКИЕ СВОЙСТВА Общим свойством всех дисперсных систем является рассеяние света. Если через такую систему пропустить интенсивный пучок света, то , наблюдая систему под некоторым углом к направлению падающего света, можно увидеть яркую полоску. Это явление получило название эффекта Тиндаля.
 В истинных растворах эффект Тиндаля не наблюдается, что позволяет отделить их от коллоидных систем. Суть эффекта Тиндаля состоит в том, что частицы дисперсной фазы рассеивают световые лучи, однако механизм этого рассеивания в суспензиях и коллоидах различен. В суспензиях свет рассеивается из-за многократных отражений и преломлений лучей на границе раздела частиц со средой. Лучи с разной длиной волны рассеиваются при этом одинаково, если падающий свет белый, то и отраженный – белый. В коллоидах размер частиц меньше длины волны света, лучи света от таких частиц не отражаются, поэтому они и не видны в микроскоп. Рассеивание света в коллоидах обусловлено дифракцией, то есть отклонением луча от прямой линии при огибании частицы.
В истинных растворах эффект Тиндаля не наблюдается, что позволяет отделить их от коллоидных систем. Суть эффекта Тиндаля состоит в том, что частицы дисперсной фазы рассеивают световые лучи, однако механизм этого рассеивания в суспензиях и коллоидах различен. В суспензиях свет рассеивается из-за многократных отражений и преломлений лучей на границе раздела частиц со средой. Лучи с разной длиной волны рассеиваются при этом одинаково, если падающий свет белый, то и отраженный – белый. В коллоидах размер частиц меньше длины волны света, лучи света от таких частиц не отражаются, поэтому они и не видны в микроскоп. Рассеивание света в коллоидах обусловлено дифракцией, то есть отклонением луча от прямой линии при огибании частицы.
 Интенсивность (яркость) света, рассеянного в результате дифракции прохождении через коллоид, описывается законом Релея: I=I 0 Kn 2/ 4 (1) где I– интенсивность рассеянного света; I 0 - интенсивность падающего света; K- константа, характерная для данного коллоида; n- концентрация частиц коллоида; - их объем; - длина волны падающего света. Из уравнения видно, что рассеивание зависит от длины волны. Сильнее всего рассеивается коротковолновый голубой свет. Красный свет рассеивается меньше всего, поэтому используется для противотуманной сигнализации. Изменение окраски коллоида, связанное со светорассеянием, называется опалесценцией.
Интенсивность (яркость) света, рассеянного в результате дифракции прохождении через коллоид, описывается законом Релея: I=I 0 Kn 2/ 4 (1) где I– интенсивность рассеянного света; I 0 - интенсивность падающего света; K- константа, характерная для данного коллоида; n- концентрация частиц коллоида; - их объем; - длина волны падающего света. Из уравнения видно, что рассеивание зависит от длины волны. Сильнее всего рассеивается коротковолновый голубой свет. Красный свет рассеивается меньше всего, поэтому используется для противотуманной сигнализации. Изменение окраски коллоида, связанное со светорассеянием, называется опалесценцией.
 Коллоидные частицы в золях часто оказываются заряженными относительно жидкости. Поэтому при пропускании электрического тока в системе происходит разделение фаз: коллоидные частицы движутся к одному электроду (электрофорез), жидкость начинает перемещаться к другому электроду (электроосмос). Эти электрокинетические явления оказываются очень сильными, что протекают даже через непроницаемые в обычных условиях перегородки. Электрофорез широко используется в промышленности – для обезвоживания нефти, в производстве изделий из латекса, в медицине.
Коллоидные частицы в золях часто оказываются заряженными относительно жидкости. Поэтому при пропускании электрического тока в системе происходит разделение фаз: коллоидные частицы движутся к одному электроду (электрофорез), жидкость начинает перемещаться к другому электроду (электроосмос). Эти электрокинетические явления оказываются очень сильными, что протекают даже через непроницаемые в обычных условиях перегородки. Электрофорез широко используется в промышленности – для обезвоживания нефти, в производстве изделий из латекса, в медицине.
 ПОЛУЧЕНИЕ КОЛЛОИДНЫХ СИСТЕМ Получают коллоиды двумя способами: - диспергационный (несамопроизвольный) дробление крупных частиц до размера 1 -0, 1 мкм в специальных коллоидных мельницах; - конденсационный (самопроизвольный) создание условий, когда атомы и молекулы истинных растворов под воздействием вандерваальсовых сил объединяются в коллоидные агрегаты.
ПОЛУЧЕНИЕ КОЛЛОИДНЫХ СИСТЕМ Получают коллоиды двумя способами: - диспергационный (несамопроизвольный) дробление крупных частиц до размера 1 -0, 1 мкм в специальных коллоидных мельницах; - конденсационный (самопроизвольный) создание условий, когда атомы и молекулы истинных растворов под воздействием вандерваальсовых сил объединяются в коллоидные агрегаты.
 Для получения устойчивых золей обычно необходим еще и третий компонент – стабилизатор, который создает защитный слой вокруг коллоидных частиц и препятствует их дальнейшему разрушению или слипанию. Стабилизаторами могут быть ионы или молекулы некоторых неорганических веществ, а также высокомолекулярные органические соединения (мыла). Стабилизирующее действие электролита можно рассмотреть на примере образования гидрозоля иодида серебра по реакции: KI + Ag. NO 3 = Ag. I + KNO Если в раствор Ag. NO 3 постепенно при интенсивном перемешивании вливать раствор KI, то осадок иодида серебра формируется в присутствии ионов на Ag+, NO 3 - и K+(ионы I- в этих условиях сразу же связываются в Ag. I и в системе отсутствуют). На поверхности кристаллов (Ag. I)k в момент их зарождения будут адсорбироваться ионы Ag+. В результате образуются ядра коллоидных частиц, несущие в среднем по m положительных электрических зарядов, поступивших с ионами Ag+ (потенциалопределяющие ионы); [(Ag. I)k m. Ag+]m+. Под действием сил электростатического взаимодействия из раствора к ядрам притягиваются в среднем по (m-x) присутствующих в системе противоионов NO 3(ионы, знак электрических заряд которых противоположен знаку зарядов ядер). В итоге образуются положительно заряженные коллоидные частицы: {[(Ag. I)k m. Ag+]m+(m-x) NO 3 - }x+
Для получения устойчивых золей обычно необходим еще и третий компонент – стабилизатор, который создает защитный слой вокруг коллоидных частиц и препятствует их дальнейшему разрушению или слипанию. Стабилизаторами могут быть ионы или молекулы некоторых неорганических веществ, а также высокомолекулярные органические соединения (мыла). Стабилизирующее действие электролита можно рассмотреть на примере образования гидрозоля иодида серебра по реакции: KI + Ag. NO 3 = Ag. I + KNO Если в раствор Ag. NO 3 постепенно при интенсивном перемешивании вливать раствор KI, то осадок иодида серебра формируется в присутствии ионов на Ag+, NO 3 - и K+(ионы I- в этих условиях сразу же связываются в Ag. I и в системе отсутствуют). На поверхности кристаллов (Ag. I)k в момент их зарождения будут адсорбироваться ионы Ag+. В результате образуются ядра коллоидных частиц, несущие в среднем по m положительных электрических зарядов, поступивших с ионами Ag+ (потенциалопределяющие ионы); [(Ag. I)k m. Ag+]m+. Под действием сил электростатического взаимодействия из раствора к ядрам притягиваются в среднем по (m-x) присутствующих в системе противоионов NO 3(ионы, знак электрических заряд которых противоположен знаку зарядов ядер). В итоге образуются положительно заряженные коллоидные частицы: {[(Ag. I)k m. Ag+]m+(m-x) NO 3 - }x+
 Средний электрический заряд x коллоидной частицы равен алгебраической сумме электрических зарядов потенциалопределяющих ионов и противоионов, входящих в состав этих частиц x = m - (m-x). Наряду с силами электростатического взаимодействия, в дисперсионной системе действуют и силы диффузии. Вследствие этого часть противоионов NO 3 - остается в растворе и обладает свободой движения. Совместно с этими свободными противоионами NO 3 - коллоидные частицы составляют так называемые мицеллы, средний состав можно описать формулой: {[(Ag. I)k m. Ag+]m+(m-x) NO 3 - }x+ х NO 3 - , в которой (Ag. I)k – зародыш, [(Ag. I)k m. Ag+]m+ -ядро, [(Ag. I)k m. Ag+]m+(m-x) NO 3 - }x+ - частица.
Средний электрический заряд x коллоидной частицы равен алгебраической сумме электрических зарядов потенциалопределяющих ионов и противоионов, входящих в состав этих частиц x = m - (m-x). Наряду с силами электростатического взаимодействия, в дисперсионной системе действуют и силы диффузии. Вследствие этого часть противоионов NO 3 - остается в растворе и обладает свободой движения. Совместно с этими свободными противоионами NO 3 - коллоидные частицы составляют так называемые мицеллы, средний состав можно описать формулой: {[(Ag. I)k m. Ag+]m+(m-x) NO 3 - }x+ х NO 3 - , в которой (Ag. I)k – зародыш, [(Ag. I)k m. Ag+]m+ -ядро, [(Ag. I)k m. Ag+]m+(m-x) NO 3 - }x+ - частица.
 При изменении условий формирования осадка (если к раствору KI добавлять Ag. NO 3) поменяется знак электрических зарядов коллоидных частиц и средний состав мицелл: {[(Ag. I)k n. I-]n-(n-y) K+ }y- y. K+. В любом случае мицеллы электронейтральны и являются структурной единицей коллоидной системы. Наличие у частиц одноименных электрических зарядов приводит к их взаимному отталкиванию. Это препятствует возможному слипанию частиц дисперсионной фазы и обеспечивает системе коллоидную устойчивость. Чем больше средний электрический заряд коллоидных частиц, тем больше силы их взаимного отталкивания.
При изменении условий формирования осадка (если к раствору KI добавлять Ag. NO 3) поменяется знак электрических зарядов коллоидных частиц и средний состав мицелл: {[(Ag. I)k n. I-]n-(n-y) K+ }y- y. K+. В любом случае мицеллы электронейтральны и являются структурной единицей коллоидной системы. Наличие у частиц одноименных электрических зарядов приводит к их взаимному отталкиванию. Это препятствует возможному слипанию частиц дисперсионной фазы и обеспечивает системе коллоидную устойчивость. Чем больше средний электрический заряд коллоидных частиц, тем больше силы их взаимного отталкивания.
 Электролит, в состав которого входят ионы, адсорбирующиеся на поверхности дисперсных частиц, называется электролитом стабилизатором. Если в дисперсионную среду вводить большое количество электролита, то произойдет увеличение количества противоионов в коллоидных частицах и уменьшится их средний электрический заряд. В итоге взаимное отталкивание частиц ослабеет и увеличится вероятность столкновений, что приведет к их слипанию (коагуляция) и может последовать оседание укрупнившихся частиц – седиментация.
Электролит, в состав которого входят ионы, адсорбирующиеся на поверхности дисперсных частиц, называется электролитом стабилизатором. Если в дисперсионную среду вводить большое количество электролита, то произойдет увеличение количества противоионов в коллоидных частицах и уменьшится их средний электрический заряд. В итоге взаимное отталкивание частиц ослабеет и увеличится вероятность столкновений, что приведет к их слипанию (коагуляция) и может последовать оседание укрупнившихся частиц – седиментация.
 Различают две стадии коагуляции – скрытую и явную. Первая стадия в коллоидных системах заканчивается, как правило, очень быстро. На этой стадии частицы укрупняются, но осадок еще не образуется, в некоторых случаях меняется окраска золя, появляется муть. Вторая стадия завершается полным разделением системы на две фазы и выпадением части или всего коллоидного вещества в виде осадка вследствие седиментации. Такой осадок называется коагель или коагулянт. Коагуляцию могут вызвать механические воздействия, изменение температуры, состава среды, свет, электрический ток, примеси электролитов. Коагулирующее действие оказывают лишь те ионы электролита, которые имеют знак электрического заряда, противоположный знаку заряда коллоидных частиц дисперсионной системы. Эти ионы называют ионамикоагуляторами, а электролит, в состав которого они входят – электролитом-коагулятором.
Различают две стадии коагуляции – скрытую и явную. Первая стадия в коллоидных системах заканчивается, как правило, очень быстро. На этой стадии частицы укрупняются, но осадок еще не образуется, в некоторых случаях меняется окраска золя, появляется муть. Вторая стадия завершается полным разделением системы на две фазы и выпадением части или всего коллоидного вещества в виде осадка вследствие седиментации. Такой осадок называется коагель или коагулянт. Коагуляцию могут вызвать механические воздействия, изменение температуры, состава среды, свет, электрический ток, примеси электролитов. Коагулирующее действие оказывают лишь те ионы электролита, которые имеют знак электрического заряда, противоположный знаку заряда коллоидных частиц дисперсионной системы. Эти ионы называют ионамикоагуляторами, а электролит, в состав которого они входят – электролитом-коагулятором.
 Минимальная концентрация электролита-коагулятора, вызывающая в системе коагуляцию, называется порогом коагуляции или критической концентрацией Скр = Vэ. C/(V+Vэ)=n/(V+Vэ) (2) где V – объем образца коллоидной системы, м 3; Vэ- объем раствора электролита-коагулятора, введение которого вызвало во взятом образце коллоидной системы быструю коагуляцию, м 3; C и n – концентрация (моль/ м 3) и количество (моль) ионов – коагуляторов.
Минимальная концентрация электролита-коагулятора, вызывающая в системе коагуляцию, называется порогом коагуляции или критической концентрацией Скр = Vэ. C/(V+Vэ)=n/(V+Vэ) (2) где V – объем образца коллоидной системы, м 3; Vэ- объем раствора электролита-коагулятора, введение которого вызвало во взятом образце коллоидной системы быструю коагуляцию, м 3; C и n – концентрация (моль/ м 3) и количество (моль) ионов – коагуляторов.
 Порог коагуляции Скр связан с валентностью z ионов-коагуляторов: Скр = k. T 5/z 6 (3) где Т – температура системы, К; k – коэффициент, зависящий от физических свойств фаз системы. Обратный процесс перевода осадка в коллоид путем добавления в систему раствора электролита называется пептизацией.
Порог коагуляции Скр связан с валентностью z ионов-коагуляторов: Скр = k. T 5/z 6 (3) где Т – температура системы, К; k – коэффициент, зависящий от физических свойств фаз системы. Обратный процесс перевода осадка в коллоид путем добавления в систему раствора электролита называется пептизацией.
 Очистка золей от присутствующих примесей растворенных веществ, главным образом электролитов, называется диализом. Он основан на разнице в скоростях диффузии истинно и коллоидно растворенных веществ через полупроницаемую мембрану. Процесс диализа часто ускоряют за счет электроосмоса.
Очистка золей от присутствующих примесей растворенных веществ, главным образом электролитов, называется диализом. Он основан на разнице в скоростях диффузии истинно и коллоидно растворенных веществ через полупроницаемую мембрану. Процесс диализа часто ускоряют за счет электроосмоса.
 При постепенном добавлении электролита в золь порог коагуляции может оказаться существенно выше, чем при одновременном добавлении всей порции электролита. Это явление получило название привыкание золей. Стабилизирующие примеси значительно повышают порог коагуляции.
При постепенном добавлении электролита в золь порог коагуляции может оказаться существенно выше, чем при одновременном добавлении всей порции электролита. Это явление получило название привыкание золей. Стабилизирующие примеси значительно повышают порог коагуляции.
 Процесс коагуляции и стабилизации коллоидов имеют большое прикладное значение. Коагуляция используется для очистки питьевой воды солями алюминия и железа, из которых в водной среде образуются хорошо оседающие коагели, захватывающие и удаляемые примеси. Получение бетона – тоже разновидность коагуляции, так же как и прокисание молока. В качестве стабилизатора иногда используют питьевую соду для нейтрализации молочной кислоты.
Процесс коагуляции и стабилизации коллоидов имеют большое прикладное значение. Коагуляция используется для очистки питьевой воды солями алюминия и железа, из которых в водной среде образуются хорошо оседающие коагели, захватывающие и удаляемые примеси. Получение бетона – тоже разновидность коагуляции, так же как и прокисание молока. В качестве стабилизатора иногда используют питьевую соду для нейтрализации молочной кислоты.
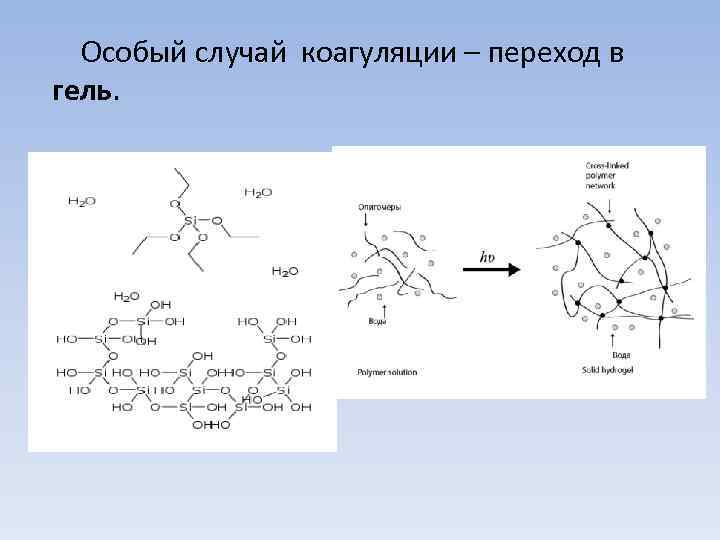 Особый случай коагуляции – переход в гель.
Особый случай коагуляции – переход в гель.
 Гель - твердая не текучая структурированная система, образовавшаяся за счет действия межмолекулярных сил между коллоидными частицами. Ячейки пространственных сеток геля обычно заполнены растворителем. Возможны жесткие гели – структурированные двухфазные системы и эластичные гели (студни) – структурированные однофазные системы. Объем жестких гелей мало зависит от количества растворителя в нем, поэтому их называют ненабухающими. К ним относятся, в частности, коагели. К эластичным гелям относятся растворы полимеров.
Гель - твердая не текучая структурированная система, образовавшаяся за счет действия межмолекулярных сил между коллоидными частицами. Ячейки пространственных сеток геля обычно заполнены растворителем. Возможны жесткие гели – структурированные двухфазные системы и эластичные гели (студни) – структурированные однофазные системы. Объем жестких гелей мало зависит от количества растворителя в нем, поэтому их называют ненабухающими. К ним относятся, в частности, коагели. К эластичным гелям относятся растворы полимеров.
 • Растворение полимеров проходит через предварительное набухание, которое заканчивается образованием жидкотекучих растворов. Если молекулы полимера имеют пространственно- развитое строение или «сшиты» между собой, то процесс растворения полимера «затормаживается» на стадии набухания – происходит ограниченное набухание.
• Растворение полимеров проходит через предварительное набухание, которое заканчивается образованием жидкотекучих растворов. Если молекулы полимера имеют пространственно- развитое строение или «сшиты» между собой, то процесс растворения полимера «затормаживается» на стадии набухания – происходит ограниченное набухание.
 Ограниченное набухание полимера характеризуется степенью набухания, определяемой как отношение приращения объема (V-V 0) или массы (m-m 0) испытываемого образца полимера к его первоначальному объему V 0 или массе m 0, соответственно: = (V-V 0)/V 0 или =(m-m 0)/ m 0, где V и m – объем и масса набухшего образца полимера.
Ограниченное набухание полимера характеризуется степенью набухания, определяемой как отношение приращения объема (V-V 0) или массы (m-m 0) испытываемого образца полимера к его первоначальному объему V 0 или массе m 0, соответственно: = (V-V 0)/V 0 или =(m-m 0)/ m 0, где V и m – объем и масса набухшего образца полимера.
 Эластичные гели, поглощая или теряя растворитель, легко и обратимо меняют свой объем. При неограниченном поглощении растворителя они переходят в золь. Пример – желатин в воде и каучук в бензине. Для эластичных гелей переход из золя в гель обычно является обратимым. Так, нагрев весьма твердого студня 10%-ного желатина переводит его в легко текучую жидкость, то есть в золь, а при охлаждении вновь образуется гель.
Эластичные гели, поглощая или теряя растворитель, легко и обратимо меняют свой объем. При неограниченном поглощении растворителя они переходят в золь. Пример – желатин в воде и каучук в бензине. Для эластичных гелей переход из золя в гель обычно является обратимым. Так, нагрев весьма твердого студня 10%-ного желатина переводит его в легко текучую жидкость, то есть в золь, а при охлаждении вновь образуется гель.
 Раствор каучука в бензине (золь) можно перевести в гель осторожным выпариванием растворителя и обратно в золь добавлением новой порции растворителя. Многие гели можно перевести в золь с помощью механического воздействия при перемешивании, а при хранении в покое они снова переходят в гель. Такой процесс называется тиксотропия и он характерен для золей гидратов окисей железа, алюминия, хрома и т. д.
Раствор каучука в бензине (золь) можно перевести в гель осторожным выпариванием растворителя и обратно в золь добавлением новой порции растворителя. Многие гели можно перевести в золь с помощью механического воздействия при перемешивании, а при хранении в покое они снова переходят в гель. Такой процесс называется тиксотропия и он характерен для золей гидратов окисей железа, алюминия, хрома и т. д.
 Переход же золя в жесткий гель обычно необратим. К обратимым коллоидам относят природные и синтетические высокомолекулярные вещества с молекулярной массой от десяти тысяч до нескольких миллионов. Молекулы этих веществ имеют размеры коллоидных частиц, поэтому такие молекулы называют макромолекулами.
Переход же золя в жесткий гель обычно необратим. К обратимым коллоидам относят природные и синтетические высокомолекулярные вещества с молекулярной массой от десяти тысяч до нескольких миллионов. Молекулы этих веществ имеют размеры коллоидных частиц, поэтому такие молекулы называют макромолекулами.
 Важнейшими свойствами полимеров, определяющими их технологические качества, являются лиофильность ( «любовь» к растворителю) и лиофобность ( «боязнь» растворителя). Полимеры не растворяются в веществах, к которым они лиофобны: гидрофобные полимеры нерастворимы в воде и других полярных растворителях, олеофобные – нерастворимы в углеводородах нефти. Растворение полимеров возможно лишь в тех растворителях, к которым они лиофильны: гидрофильные полимеры могут быть растворены в воде и других полярных растворителях, а олеофильные – растворимы в нефтепродуктах.
Важнейшими свойствами полимеров, определяющими их технологические качества, являются лиофильность ( «любовь» к растворителю) и лиофобность ( «боязнь» растворителя). Полимеры не растворяются в веществах, к которым они лиофобны: гидрофобные полимеры нерастворимы в воде и других полярных растворителях, олеофобные – нерастворимы в углеводородах нефти. Растворение полимеров возможно лишь в тех растворителях, к которым они лиофильны: гидрофильные полимеры могут быть растворены в воде и других полярных растворителях, а олеофильные – растворимы в нефтепродуктах.
 Растворы полимеров во многом подобны дисперсным системам, хотя и являются молекулярными растворами. Это сообщает им так называемую структурную вязкость, характерной особенностью которой является ее зависи-мость не только от концентрации раствора, но и от интенсивности движения жидкости. В связи с этим растворы полимеров характеризуются: - относительной вязкостью: отн = / 0 - удельной вязкостью: уд = ( - 0)/ 0 - приведенной вязкостью: пр = уд/ С
Растворы полимеров во многом подобны дисперсным системам, хотя и являются молекулярными растворами. Это сообщает им так называемую структурную вязкость, характерной особенностью которой является ее зависи-мость не только от концентрации раствора, но и от интенсивности движения жидкости. В связи с этим растворы полимеров характеризуются: - относительной вязкостью: отн = / 0 - удельной вязкостью: уд = ( - 0)/ 0 - приведенной вязкостью: пр = уд/ С
![- характеристической вязкостью: – [ ] = где и 0 - вязкости раствора полимера - характеристической вязкостью: – [ ] = где и 0 - вязкости раствора полимера](https://present5.com/presentation/49895079_62241133/image-29.jpg) - характеристической вязкостью: – [ ] = где и 0 - вязкости раствора полимера и чистого растворителя, определенные при одинаковых условиях, С- концентрация раствора, выраженная в моль/м 3, в расчете на мономерное звено ( «основной моль» ) испытываемого полимера. Характеристическая вязкость [ ] растворов полимеров не зависит от их концентрации и определяется природой полимера и растворителя. Поэтому ее используют при вискозиметрическом определении молярной массы М полимера.
- характеристической вязкостью: – [ ] = где и 0 - вязкости раствора полимера и чистого растворителя, определенные при одинаковых условиях, С- концентрация раствора, выраженная в моль/м 3, в расчете на мономерное звено ( «основной моль» ) испытываемого полимера. Характеристическая вязкость [ ] растворов полимеров не зависит от их концентрации и определяется природой полимера и растворителя. Поэтому ее используют при вискозиметрическом определении молярной массы М полимера.


