Л18 - Вмс,св-ваих,коллоидная защита.ppt
- Количество слайдов: 12
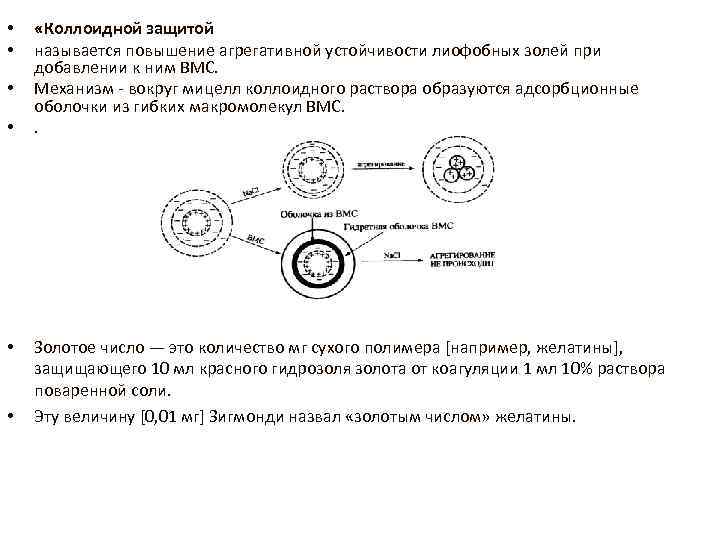 • • • «Коллоидной защитой называется повышение агрегативной устойчивости лиофобных золей при добавлении к ним ВМС. Механизм - вокруг мицелл коллоидного раствора образуются адсорбционные оболочки из гибких макромолекул ВМС. . Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10 мл красного гидрозоля золота от коагуляции 1 мл 10% раствора поваренной соли. Эту величину [0, 01 мг] Зигмонди назвал «золотым числом» желатины.
• • • «Коллоидной защитой называется повышение агрегативной устойчивости лиофобных золей при добавлении к ним ВМС. Механизм - вокруг мицелл коллоидного раствора образуются адсорбционные оболочки из гибких макромолекул ВМС. . Золотое число — это количество мг сухого полимера [например, желатины], защищающего 10 мл красного гидрозоля золота от коагуляции 1 мл 10% раствора поваренной соли. Эту величину [0, 01 мг] Зигмонди назвал «золотым числом» желатины.
 • • • Основными условиями защитного действия являются: — хорошая растворимость ВМС в дисперсионной среде коллоидного раствора; — хорошая адсорбируемость молекул ВМС на коллоидных частицах; —большая концентрация ВМС, полностью покрывающего всю поверхность мицелл. К лиофильным коллоидным растворам относятся растворы (ПАВ) и высокомолекулярных соединений (ВМС) в «хороших» растворителях. ВМС — это вещества c Мr =103 -109 По происхождению ВМС подразделяются на : природные и синтетические. Молекулы ВМС имеют: ☻ линейное строение [каучук, целлюлоза ☻ разветвлённое строение [крахмал, гликоген ☻ сетчатая, или трёхмерная структура [конденсационные смолы]. ☻ белки и нуклеиновые кислоты от всех других типов ВМС отличаются своеобразной спиральной конфигурацией макромолекул
• • • Основными условиями защитного действия являются: — хорошая растворимость ВМС в дисперсионной среде коллоидного раствора; — хорошая адсорбируемость молекул ВМС на коллоидных частицах; —большая концентрация ВМС, полностью покрывающего всю поверхность мицелл. К лиофильным коллоидным растворам относятся растворы (ПАВ) и высокомолекулярных соединений (ВМС) в «хороших» растворителях. ВМС — это вещества c Мr =103 -109 По происхождению ВМС подразделяются на : природные и синтетические. Молекулы ВМС имеют: ☻ линейное строение [каучук, целлюлоза ☻ разветвлённое строение [крахмал, гликоген ☻ сетчатая, или трёхмерная структура [конденсационные смолы]. ☻ белки и нуклеиновые кислоты от всех других типов ВМС отличаются своеобразной спиральной конфигурацией макромолекул
 ВМС свертываются в клубок: гипотеза Вант-Гоффа о свободном вращении атомов углерода вокруг связи С —С и макромолекула может принять любую форму. Переходы одной и той же макромолекулы из одной формы в другую получили название конформационных превращений Наиболее гибкие -цепи —СН 2—, наименее имеющие группы Cl–, ОН–, СООН Характеристика гибкости цепей – сегмент — часть цепи, в которой в результате суммарного вращения атомов совершается полный оборот. Сходство растворов ВМС и гидрофобных золей. – 1. ВМС медленно диффундируют. – 2. ВМС не проникают через полупроницаемые мембраны. – 3. Размер частиц ВМС соответствует коллоидным [1– 100 нм]. – Отличие растворов ВМС от гидрофобных золей: – 1. как растворы НМС, обладают термодинамической устойчивостью. – 2. обладают обратимой растворимостью. Гидрофобные золи необратимы. – 3. Растворы ВМС являются истинными растворами, не имеющими поверхности раздела; гидрофобные золи имеют поверхность раздела. – 4. ВМС самопроизвольно растворяются в определённых жидкостях, не требуя стабилизаторов и затраты внешней энергии. – Для получения растворов ВМС применяют метод растворения или самопроизвольного диспергирования.
ВМС свертываются в клубок: гипотеза Вант-Гоффа о свободном вращении атомов углерода вокруг связи С —С и макромолекула может принять любую форму. Переходы одной и той же макромолекулы из одной формы в другую получили название конформационных превращений Наиболее гибкие -цепи —СН 2—, наименее имеющие группы Cl–, ОН–, СООН Характеристика гибкости цепей – сегмент — часть цепи, в которой в результате суммарного вращения атомов совершается полный оборот. Сходство растворов ВМС и гидрофобных золей. – 1. ВМС медленно диффундируют. – 2. ВМС не проникают через полупроницаемые мембраны. – 3. Размер частиц ВМС соответствует коллоидным [1– 100 нм]. – Отличие растворов ВМС от гидрофобных золей: – 1. как растворы НМС, обладают термодинамической устойчивостью. – 2. обладают обратимой растворимостью. Гидрофобные золи необратимы. – 3. Растворы ВМС являются истинными растворами, не имеющими поверхности раздела; гидрофобные золи имеют поверхность раздела. – 4. ВМС самопроизвольно растворяются в определённых жидкостях, не требуя стабилизаторов и затраты внешней энергии. – Для получения растворов ВМС применяют метод растворения или самопроизвольного диспергирования.
 • • • 1. 2. 3. 4. Специфические свойства ВМС. 1. ВМС набухают. Набухание сопровождается увеличением массы и объёма полимера. 2. Растворы ВМС обладают большой вязкостью. 3. Растворы ВМС легко желатинируются, образуя гели. 4. ВМС лиофильны, а биополимеры гидрофильны. 5. Растворы ВМС более устойчивы, чем растворы гидрофобных коллоидов, и поэтому могут быть получены более концентрированными. 6. Растворы ВМС сами не седиментируют. 7. В растворах ВМС может иметь место коацервация. Это слияние водных оболочек частиц без объединения самих частиц. 8. ВМС [белки] могут подвергаться денатурации. 9. ВМС [белки] подвергаются высаливанию. 10. ВМС дают размытый конус Тиндаля; гидрофобные золи дают чёткий конус Тиндаля. Гидрофильность растворов биополимеров. Гидрофильность искусственных полимеров обусловлена двойными связями, аминными и спиртовыми группировками. Гидрофильность природных полимеров обусловлена главным образом пептидными, эфирными, двойными связями, карбоксильными, карбонильными, спиртовыми и аминными группами. Различают диссоциированные [ионогенные] гидрофильные группы и недиссоциированные [полярные] группы.
• • • 1. 2. 3. 4. Специфические свойства ВМС. 1. ВМС набухают. Набухание сопровождается увеличением массы и объёма полимера. 2. Растворы ВМС обладают большой вязкостью. 3. Растворы ВМС легко желатинируются, образуя гели. 4. ВМС лиофильны, а биополимеры гидрофильны. 5. Растворы ВМС более устойчивы, чем растворы гидрофобных коллоидов, и поэтому могут быть получены более концентрированными. 6. Растворы ВМС сами не седиментируют. 7. В растворах ВМС может иметь место коацервация. Это слияние водных оболочек частиц без объединения самих частиц. 8. ВМС [белки] могут подвергаться денатурации. 9. ВМС [белки] подвергаются высаливанию. 10. ВМС дают размытый конус Тиндаля; гидрофобные золи дают чёткий конус Тиндаля. Гидрофильность растворов биополимеров. Гидрофильность искусственных полимеров обусловлена двойными связями, аминными и спиртовыми группировками. Гидрофильность природных полимеров обусловлена главным образом пептидными, эфирными, двойными связями, карбоксильными, карбонильными, спиртовыми и аминными группами. Различают диссоциированные [ионогенные] гидрофильные группы и недиссоциированные [полярные] группы.
 • • • Ионогенные гидрофильные группы: R—СООН, R—СООNa, R—NН 3 ОН, R—NH 3 Cl. Недиссоциированные [полярные] гидрофильные группы: R 2 -C=0; R-COH Диссоциация ионогенных групп обеспечивает ВМС электрический заряд, а полярные группы притягивают диполи воды, образующие гидратную оболочку. Устойчивость растворов ВМС определяется двумя факторами: - наличием заряда - наличием гидратной оболочки Аномальная и структурная вязкость растворов ВМС. Вязкость — это внутреннее трение, обусловленное силами сцепления между молекулами жидкости. Для растворов ВМС - высокая вязкость; Согласно П закону Пуазейля, вязкость растворов прямо пропорциональна внешнему давлению, действующему на протекающую жидкость, но ВМС не подчиняются этому закону; в растворах ВМС обнаруживается так называемая аномальная вязкость (а. в. )
• • • Ионогенные гидрофильные группы: R—СООН, R—СООNa, R—NН 3 ОН, R—NH 3 Cl. Недиссоциированные [полярные] гидрофильные группы: R 2 -C=0; R-COH Диссоциация ионогенных групп обеспечивает ВМС электрический заряд, а полярные группы притягивают диполи воды, образующие гидратную оболочку. Устойчивость растворов ВМС определяется двумя факторами: - наличием заряда - наличием гидратной оболочки Аномальная и структурная вязкость растворов ВМС. Вязкость — это внутреннее трение, обусловленное силами сцепления между молекулами жидкости. Для растворов ВМС - высокая вязкость; Согласно П закону Пуазейля, вязкость растворов прямо пропорциональна внешнему давлению, действующему на протекающую жидкость, но ВМС не подчиняются этому закону; в растворах ВМС обнаруживается так называемая аномальная вязкость (а. в. )
 • • • Аномальной её называют потому, что: 1/ эта вязкость очень высока; 2(а. в. ) уменьшается с увеличением давления на протекающую жидкость. Причина (а. в. ) - силы сцепления гидрофильных молекул ВМС с молекулами воды очень велики. Располагаясь поперёк потока, крупные частицы ВМС оказывают сопротивление и увеличивают вязкость. При увеличении внешнего давления на жидкость эти частицы ориентируются вдоль потока и вязкость раствора уменьшается. Аномальную вязкость называют ещё и структурной вязкостью,
• • • Аномальной её называют потому, что: 1/ эта вязкость очень высока; 2(а. в. ) уменьшается с увеличением давления на протекающую жидкость. Причина (а. в. ) - силы сцепления гидрофильных молекул ВМС с молекулами воды очень велики. Располагаясь поперёк потока, крупные частицы ВМС оказывают сопротивление и увеличивают вязкость. При увеличении внешнего давления на жидкость эти частицы ориентируются вдоль потока и вязкость раствора уменьшается. Аномальную вязкость называют ещё и структурной вязкостью,
 Вязкость зависит : 1. От природы полимера [с повышением молекулярной массы вязкость растворов полимеров возрастает; у полимеров с выпрямленными цепями вязкость выше, чем у полимеров со свёрнутыми, клубкообразными молекулами]. 2. Вязкость зависит от природы растворителя, так как определяется силами сцепления между молекулами ВМС и молекулами растворителя. 3. Вязкость зависит от концентрации [с повышением концентрации вязкость сильно возрастает, так как между молекулами полимера легче образуются структурные сетки]. 4. Вязкость растворов ВМС всегда падает с ростом температуры. Это объясняется интенсивностью молекулярного движения, разрушающего структуры. : 5. На вязкость раствора ВМС влияет время приготовления раствора [при старении вязкость возрастает!]. 6. На вязкость влияет р. Н раствора. В ИЭТ растворы биополимеров имеют более компактную форму макромолекул и наименьшую вязкость. 7. На вязкость влияет добавление минеральных веществ: а/ примеси солей кальция повышают вязкость многих полимеров [например, желатина]; б/ анионы располагаются в прямой лиотропный ряд по своему действию[SO 4 2– повышает вязкость, CNS– снижает].
Вязкость зависит : 1. От природы полимера [с повышением молекулярной массы вязкость растворов полимеров возрастает; у полимеров с выпрямленными цепями вязкость выше, чем у полимеров со свёрнутыми, клубкообразными молекулами]. 2. Вязкость зависит от природы растворителя, так как определяется силами сцепления между молекулами ВМС и молекулами растворителя. 3. Вязкость зависит от концентрации [с повышением концентрации вязкость сильно возрастает, так как между молекулами полимера легче образуются структурные сетки]. 4. Вязкость растворов ВМС всегда падает с ростом температуры. Это объясняется интенсивностью молекулярного движения, разрушающего структуры. : 5. На вязкость раствора ВМС влияет время приготовления раствора [при старении вязкость возрастает!]. 6. На вязкость влияет р. Н раствора. В ИЭТ растворы биополимеров имеют более компактную форму макромолекул и наименьшую вязкость. 7. На вязкость влияет добавление минеральных веществ: а/ примеси солей кальция повышают вязкость многих полимеров [например, желатина]; б/ анионы располагаются в прямой лиотропный ряд по своему действию[SO 4 2– повышает вязкость, CNS– снижает].
 Различают относительную, удельную, приведённую и характеристическую вязкость. Относительная вязкость: Удельную вязкость : или ηуд = ηотн – 1, где η — вязкость раствора; η 0 — вязкость растворителя. Приведённая вязкость: С→ 0, можно получить величину, называемую предельной приведённой вязкостью или характеристической вязкостью: где [η] — характеристическая вязкость. Штаудингер ηуд = К • М • С, где К — константа, характерная для данного гомологического ряда полимеров, не зависящая от природы растворителя. Определяют М лишь только для коротких цепей или более жёстких.
Различают относительную, удельную, приведённую и характеристическую вязкость. Относительная вязкость: Удельную вязкость : или ηуд = ηотн – 1, где η — вязкость раствора; η 0 — вязкость растворителя. Приведённая вязкость: С→ 0, можно получить величину, называемую предельной приведённой вязкостью или характеристической вязкостью: где [η] — характеристическая вязкость. Штаудингер ηуд = К • М • С, где К — константа, характерная для данного гомологического ряда полимеров, не зависящая от природы растворителя. Определяют М лишь только для коротких цепей или более жёстких.
 • • • Строение ДНК. 1. Первичная структура ДНК представлена последовательностью мононуклеотидов, соединённых между собой сложноэфирными связями. 2. Уотсон и Крик- молекула ДНК состоит из двух правозакрученных антипараллельных полинуклеотидных спиралей, имеющих общую ось, так что образуется двойная спираль [вторичная структура ДНК]. Цепи связаны по правилу комплементарности: аденин с тимином 2 водородными связями, гуанин с цитозином — 3 водородными связями. снаружи молекулы находятся остатки фосфорной кислоты, заряженные отрицательно [Р—О–], внутри – азотистые основания. . основа принципа комплементарности--связь приводящая к образованию двойной спирали одинакового диаметра, наиболее выгодна для системы с энергетической точки зрения. 3. В хромосомах молекулы ДНК далее способны образовывать компактную структуру [третичная структура ДНК] 4. В комплексе с белками (гистонами )[четвертичная структура ДНК]. фракция Г 3 гистонов легко помещается в малом желобке двойной спирали ДНК. Г 1 гистонов тяжело совмещается с ДНК и нейтрализует фосфорные группы в отдельных точках. Роль этой фракции — образование надмолекулярной структуры: соединение ДНК-частиц. Система хромосом — это надмолекулярная система; очевидно, в хромосоме молекулы ДНК находятся в виде субъединиц.
• • • Строение ДНК. 1. Первичная структура ДНК представлена последовательностью мононуклеотидов, соединённых между собой сложноэфирными связями. 2. Уотсон и Крик- молекула ДНК состоит из двух правозакрученных антипараллельных полинуклеотидных спиралей, имеющих общую ось, так что образуется двойная спираль [вторичная структура ДНК]. Цепи связаны по правилу комплементарности: аденин с тимином 2 водородными связями, гуанин с цитозином — 3 водородными связями. снаружи молекулы находятся остатки фосфорной кислоты, заряженные отрицательно [Р—О–], внутри – азотистые основания. . основа принципа комплементарности--связь приводящая к образованию двойной спирали одинакового диаметра, наиболее выгодна для системы с энергетической точки зрения. 3. В хромосомах молекулы ДНК далее способны образовывать компактную структуру [третичная структура ДНК] 4. В комплексе с белками (гистонами )[четвертичная структура ДНК]. фракция Г 3 гистонов легко помещается в малом желобке двойной спирали ДНК. Г 1 гистонов тяжело совмещается с ДНК и нейтрализует фосфорные группы в отдельных точках. Роль этой фракции — образование надмолекулярной структуры: соединение ДНК-частиц. Система хромосом — это надмолекулярная система; очевидно, в хромосоме молекулы ДНК находятся в виде субъединиц.
 • • • • Белки. 1. Основным фактором, определяющим структуру белка, является последовательность аминокислот, - первичная структуры белка. В первичной структуре белка атомы связаны прочными ковалентными связями. 2. Под вторичной структурой белка понимают конфигурацию полипептидной цепи в пространстве- В 1951 г. Полинг и Кори ( спиральная конфигурация). Дисульфидные мостики, но основную роль играют водородные связи. белки [β-кератин волос, фиброин шёлка] образуют не α-спираль, а β‑структуру. Они имеют несколько полипептидных цепей, расположенных параллельно. 3. Трёхмерная конфигурация полипептидной спирали или β-структуры в пространстве определяет её третичную структуру : закручивается в клубок α‑спираль, и β-структура. Так образуется глобулярная структура [у глобулярных белков]. У фибриллярных [нитевидных] белков третичная структура характеризуется: а/ объединением α-спиралей в многожильный пучок —вторичную спираль; б/ объединением лент β-структур в многослойную ленту. Третичную структуру поддерживают: 1. Ионные связи. 2. Водородные связи. 3. Дисульфидные связи. 4. Ван дер Ваальсово взаимодействие. 5. Взаимодействие полярных групп с водой. 4. По Берналу четвертичная структура представляет собой комплекс субъединиц, способных к диссоциации. и поддерживается теми же связями и силами, что и третичная структура.
• • • • Белки. 1. Основным фактором, определяющим структуру белка, является последовательность аминокислот, - первичная структуры белка. В первичной структуре белка атомы связаны прочными ковалентными связями. 2. Под вторичной структурой белка понимают конфигурацию полипептидной цепи в пространстве- В 1951 г. Полинг и Кори ( спиральная конфигурация). Дисульфидные мостики, но основную роль играют водородные связи. белки [β-кератин волос, фиброин шёлка] образуют не α-спираль, а β‑структуру. Они имеют несколько полипептидных цепей, расположенных параллельно. 3. Трёхмерная конфигурация полипептидной спирали или β-структуры в пространстве определяет её третичную структуру : закручивается в клубок α‑спираль, и β-структура. Так образуется глобулярная структура [у глобулярных белков]. У фибриллярных [нитевидных] белков третичная структура характеризуется: а/ объединением α-спиралей в многожильный пучок —вторичную спираль; б/ объединением лент β-структур в многослойную ленту. Третичную структуру поддерживают: 1. Ионные связи. 2. Водородные связи. 3. Дисульфидные связи. 4. Ван дер Ваальсово взаимодействие. 5. Взаимодействие полярных групп с водой. 4. По Берналу четвертичная структура представляет собой комплекс субъединиц, способных к диссоциации. и поддерживается теми же связями и силами, что и третичная структура.
 • • • • • Молекулярная масса белков и методы её определения. Миоглобин — 16 900 Гемоглобин — 68 000 Растительный вирус — 10 600 000 Неточно М определяют: π осм. = CRT= m/M RT криоскопический метод ∆t зам. = m/M∙Kкр; (Kкр=1. 85 для Н 2 О) Наиболее точными - рентгеноструктурный анализ и метод ультрацентрифугирования. , где R — газовая постоянная; Т — абсолютная температура; S — константа, выражающая скорость седиментации; D — коэффициент диффузии; ρ — плотность среды; V — увеличение объёма при добавлении 1 г белка, или удельный объём Методы определения иэоэлектрической точки белков. Изоэлектрическая точка белков может быть определена следующими методами: 1. По величине набухания- Наименьшее набухание будет в изоэлектрической точке. 2. По скорости желатинирования. Быстрее всего желатинирование происходит в изоэлектрической точке. 3. По степени коагуляции -Наиболее выраженное помутнение раствора будет в изоэлектрической точке. 4. По электрофоретической подвижности -В растворе, где р. Н соответствует изоэлектрической точке белка, белок будет электронейтральным и перемещаться в электрическом поле не будет. 5. Потенциометрическое титрование в сочетании с определением максимальной степени коагуляции.
• • • • • Молекулярная масса белков и методы её определения. Миоглобин — 16 900 Гемоглобин — 68 000 Растительный вирус — 10 600 000 Неточно М определяют: π осм. = CRT= m/M RT криоскопический метод ∆t зам. = m/M∙Kкр; (Kкр=1. 85 для Н 2 О) Наиболее точными - рентгеноструктурный анализ и метод ультрацентрифугирования. , где R — газовая постоянная; Т — абсолютная температура; S — константа, выражающая скорость седиментации; D — коэффициент диффузии; ρ — плотность среды; V — увеличение объёма при добавлении 1 г белка, или удельный объём Методы определения иэоэлектрической точки белков. Изоэлектрическая точка белков может быть определена следующими методами: 1. По величине набухания- Наименьшее набухание будет в изоэлектрической точке. 2. По скорости желатинирования. Быстрее всего желатинирование происходит в изоэлектрической точке. 3. По степени коагуляции -Наиболее выраженное помутнение раствора будет в изоэлектрической точке. 4. По электрофоретической подвижности -В растворе, где р. Н соответствует изоэлектрической точке белка, белок будет электронейтральным и перемещаться в электрическом поле не будет. 5. Потенциометрическое титрование в сочетании с определением максимальной степени коагуляции.
 • • • Свойства белка в ИЭТ. Минимальны: 1/ вязкость; 2/ гидратация; 3/ набухание; 4/ растворимость; 5/ осмотическое давление; 6/ электропроводность; 7/ дзета-потенциал. Максимальны: 1/ степень коагуляции; 2/ желатинирование.
• • • Свойства белка в ИЭТ. Минимальны: 1/ вязкость; 2/ гидратация; 3/ набухание; 4/ растворимость; 5/ осмотическое давление; 6/ электропроводность; 7/ дзета-потенциал. Максимальны: 1/ степень коагуляции; 2/ желатинирование.


