2014.1015 кол.химия.pptx
- Количество слайдов: 31

КОЛЛОИДНАЯ ХИМИЯ

Поверхностные явления Превращения свободной энергии Гиббса представляет собой сумму превращений различных видов энергий: 1) Тепловой 2) Механической 3) Поверхностной 4) Химической 5) Электрической
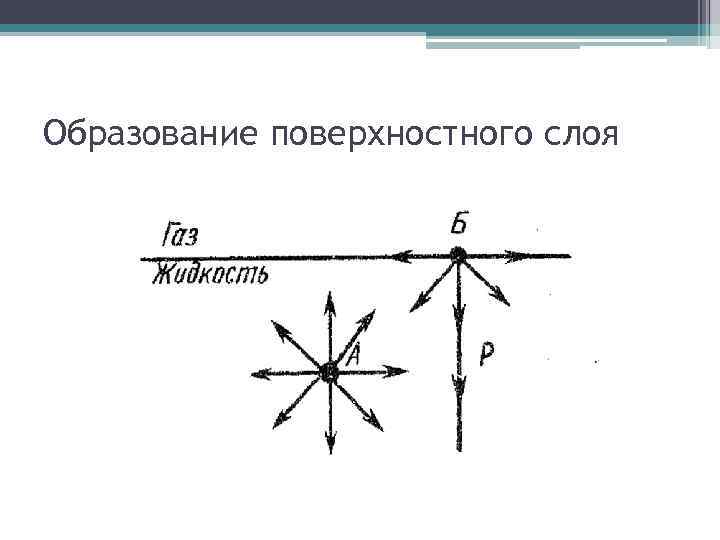
Образование поверхностного слоя

Свободная поверхностная энергия

Поверхностное натяжение • Энергетическое определение: • Силовое определение:
![Поверхностное натяжение (σ) равно работе, которую нужно совершить для создания единицы поверхности [Дж/м 2]. Поверхностное натяжение (σ) равно работе, которую нужно совершить для создания единицы поверхности [Дж/м 2].](https://present5.com/presentation/33632337_437827727/image-6.jpg)
Поверхностное натяжение (σ) равно работе, которую нужно совершить для создания единицы поверхности [Дж/м 2]. Поверхностное натяжение зависит от: ▫ природы жидкости σ(Н 2 О)=72, 8 Дж/м 2; σ(сыворотки крови)=45, 4 Дж/м 2). ▫ температуры (↑t ↓σ , при tкип σ =0). ▫ давления (↑p ↓σ ). ▫ концентрации растворенного вещества.

Виды адсорбции: • а) абсолютную адсорбцию (А) или поверхностную концентрацию, к. представляет собой количество вещества в поверхностном слое, приходящееся на единицу поверхности и массы адсорбента. А всегда положительно. • б) избыточную или гиббсовскую (Г), представляющую собой избыток вещества в поверхностном слое на единицу поверхности, по сравнению с его концентрацией в объеме фазы. Г м. б. >0 и <0.
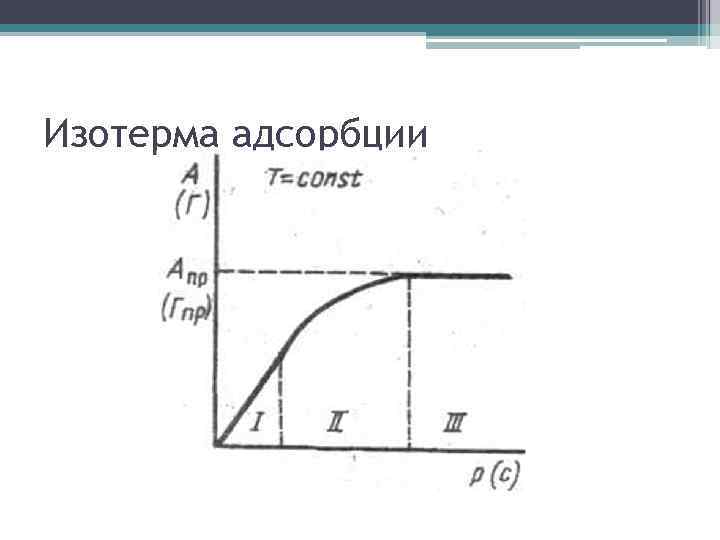
Изотерма адсорбции
![Уравнение Гиббса • Г - количество адсорбированного вещества [моль/м 2] С - молярная концентрация Уравнение Гиббса • Г - количество адсорбированного вещества [моль/м 2] С - молярная концентрация](https://present5.com/presentation/33632337_437827727/image-9.jpg)
Уравнение Гиббса • Г - количество адсорбированного вещества [моль/м 2] С - молярная концентрация раствора [моль/л] R - универсальная газовая постоянная = 8, 31 Дж/моль. град(К) - поверхностная активность растворенного вещества.

Поверхностная активность Способность растворенного вещества изменять поверхностное натяжение – поверхностная активность (g) Мера поверхностной активности:
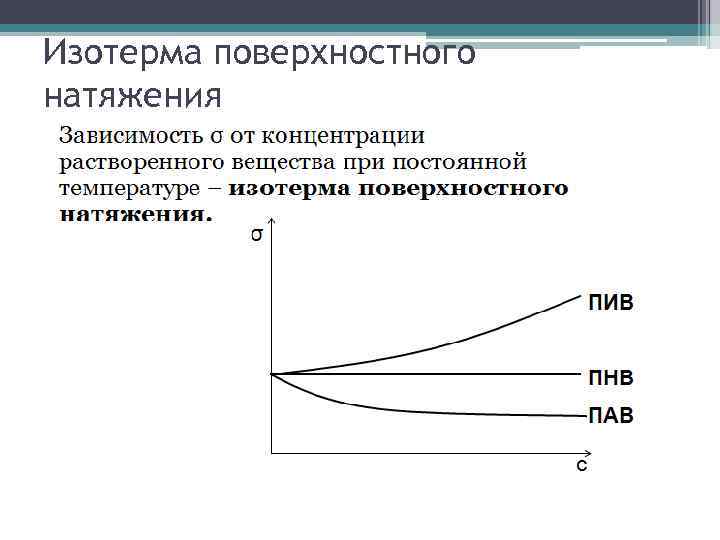
Изотерма поверхностного натяжения

ПАВ, ПИВ, ПНВ 1. Поверхностно-активные вещества (ПАВ): уменьшают σ растворителя. σ раствора < σ растворителя; g > О. ПАВ: спирты, органические кислоты, сложные эфиры, белки, холестерин, жиры, липиды, мыла. 2. Поверхностно-инактивные вещества (ПИВ): увеличивают σ растворителя. σ раствора > σ растворителя; g < О. ПИВ: неорганические кислоты, основания, соли, глицерин, α - аминокислоты. 3. Поверхностно-неактивные вещества (ПНВ): не изменяют поверхностное натяжение растворителя. σ раствора = σ растворителя; g = О. ПНВ: сахароза.

Строение молекулы ПАВ: Молекула ПАВ состоит из: § неполярной гидрофобной углеводородной группы (“хвост”) § полярной гидрофильной группы (“голова”): -ОН, -СООН, -С(О)-О, -NН 2; -SО 3 H. “хвост” “голова”

Правило Траубе-Дюкло: При удлинении цепи на группу -СН 2 - в гомологическом ряду способность к адсорбции возрастает в 3 -3, 5 раза.
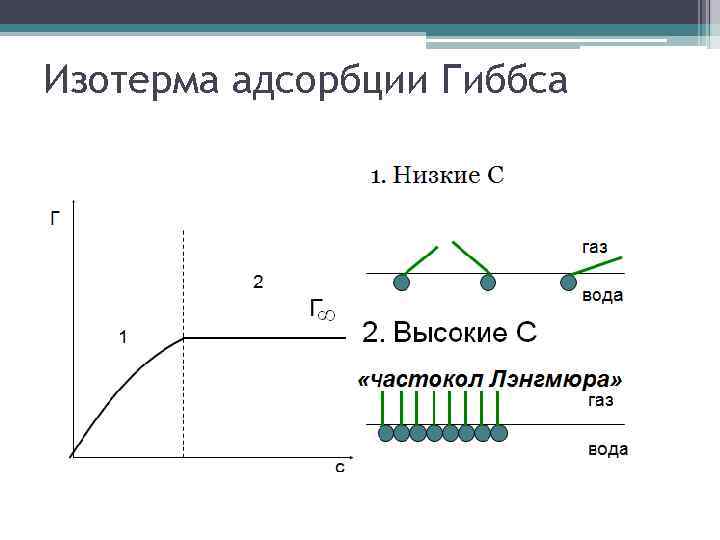
Изотерма адсорбции Гиббса
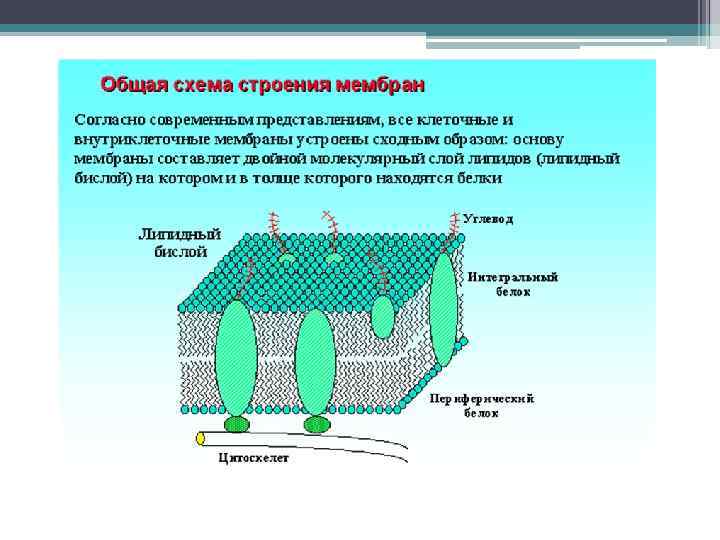

Основные понятия • Сорбент – поглотитель • Сорбтив (сорбат) – поглощаемое вещество • Сорбция – процесс поглощения одного вещества другим • Адсорбция – поглощение поверхностью сорбента • Десорбция – обратный процесс • Абсорбция – поглощение всем сорбентом

Физическая адсорбция Химическая адсорбция Ван-дер-Ваальсовые силы Химические силы Обратима Необратима Мало специфична Специфична Не локализована (адсорбируемые молекулы способны передвигаться по поверхности адсорбента) Локализована С увеличением Т адсорбция замедляется С возрастанием Т хемосорбция замедляется Энергетический барьер не велик Тепловой эффект значителен

Уравнение Ленгмюра

Уравнение Фрейндлиха

Теория БЭТ Основные положение: 1. На поверхности адсорбента имеется определенное число равноценных в энергетическом отношении активных центров. 2. Взаимодействие соседних адсорбционных молекул в первом и последнем слоях отсутствует. 3. Каждая молекула предыдущего слоя представляет собой возможный активный центр для адсорбции следующего адсорбционного слоя. 4. Предполагается, что все молекулы во втором и более далеких слоях ведут себя подобно молекулам жидкости.
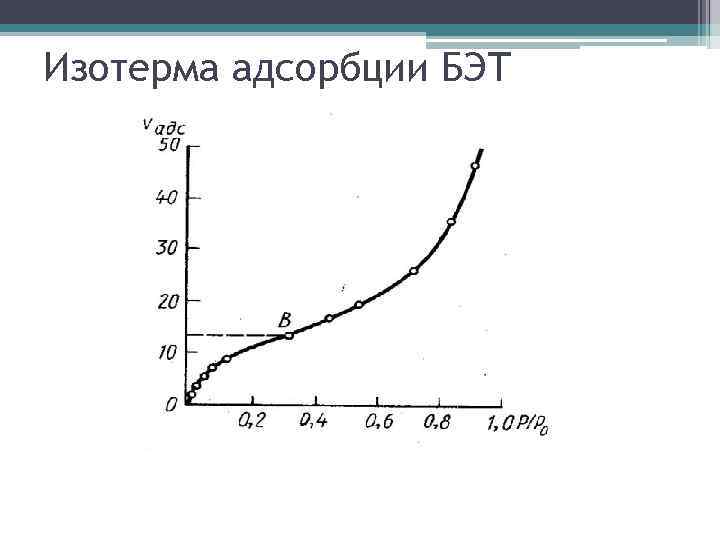
Изотерма адсорбции БЭТ

Основное уравнение БЭТ
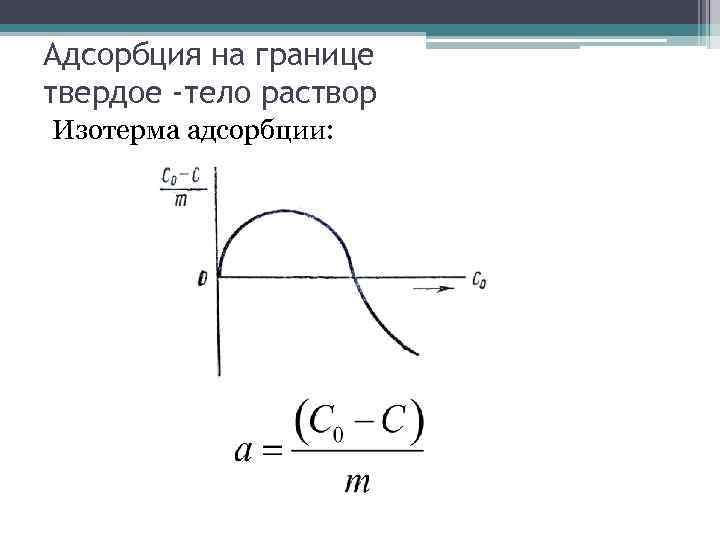
Адсорбция на границе твердое -тело раствор Изотерма адсорбции:
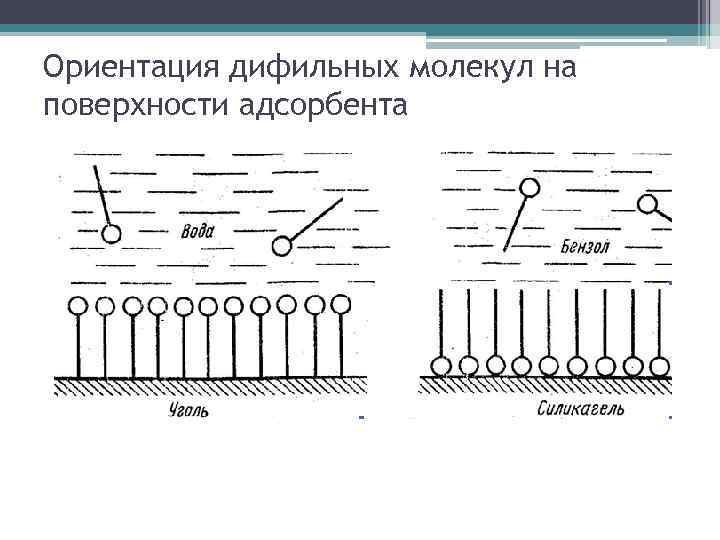
Ориентация дифильных молекул на поверхности адсорбента

Адсорбция из растворов электролитов: • Эквивалентная или ионообменная • Специфическая или избирательная

Ионообменная адсорбция – процесс, в котором адсорбент и раствор обмениваются между собой в эквивалентных количествах одноименно заряженными ионами. RM 1 + М 2+ → RM 2 + M 1+ обмен катионов катионит RА 1 + А 2 - → RА 2 + А 1 - обмен анионов анионит
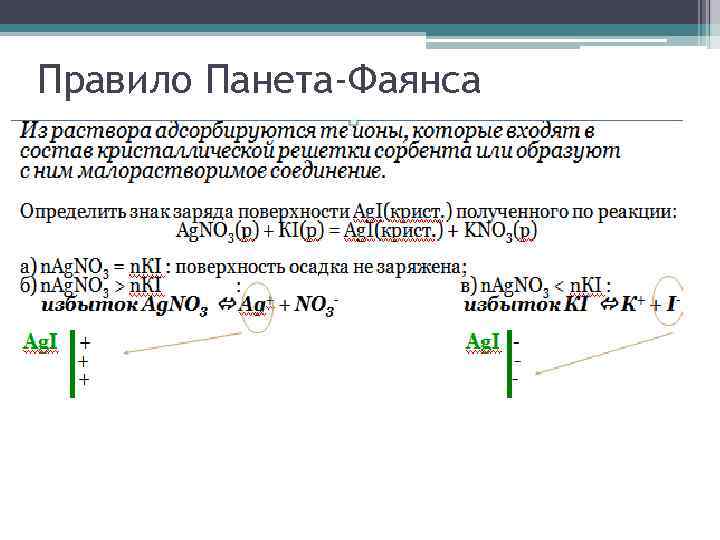
Правило Панета-Фаянса

Хроматография - динамический метод анализа, основанный на многократно повторяющихся процессах сорбции и десорбции. А+В А В

Медико-биологическое значение темы 1. Усвоение питательных и лекарственных веществ 2. Перенос О 2 и СО 2 из лёгких к тканям 3. Действие ферментов 4. Детоксикация организма: а) Гемосорбция - очистка крови б) Лимфосорбция - очистка лимфы. 5. Поглощение ядовитых веществ в желудочнокишечном тракте. 6. Хроматография: - разделение смесей аминокислот; - очистка лекарственных препаратов; - количественное определение витаминов, гормонов; - диагностика заболеваний

Спасибо за внимание
2014.1015 кол.химия.pptx