Коллоидная химия o Организмы животных и растений,















10.Коллоидная химия.ppt
- Количество слайдов: 23
 Коллоидная химия o Организмы животных и растений, гидросфера, земная кора и недра, космическое пространство – зачастую вещества в раздробленном (дисперсном) состоянии o Дисперсные системы - большинство веществ окружающего нас мира : • почвы • ткани живых организмов • пищевые продукты
Коллоидная химия o Организмы животных и растений, гидросфера, земная кора и недра, космическое пространство – зачастую вещества в раздробленном (дисперсном) состоянии o Дисперсные системы - большинство веществ окружающего нас мира : • почвы • ткани живых организмов • пищевые продукты
 Коллоидная химия o область химии, изучающая • дисперсные системы и • поверхностные явления , возникающие на границе раздела фаз
Коллоидная химия o область химии, изучающая • дисперсные системы и • поверхностные явления , возникающие на границе раздела фаз
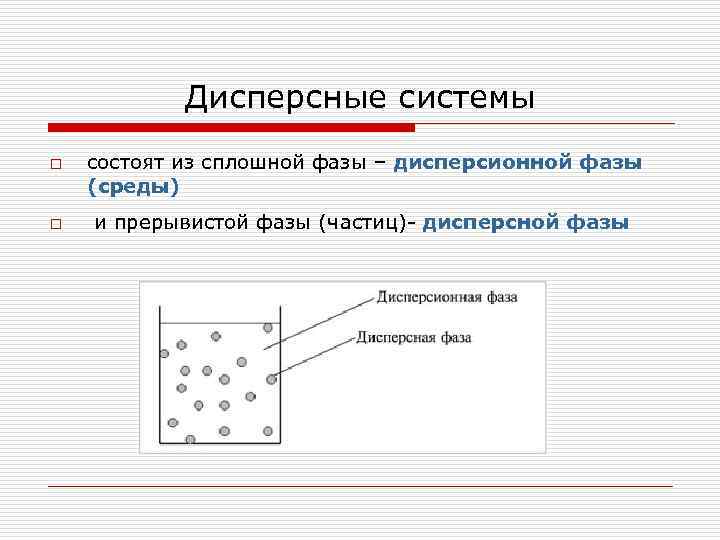
 Дисперсные системы o состоят из сплошной фазы – дисперсионной фазы (среды) o и прерывистой фазы (частиц)- дисперсной фазы
Дисперсные системы o состоят из сплошной фазы – дисперсионной фазы (среды) o и прерывистой фазы (частиц)- дисперсной фазы
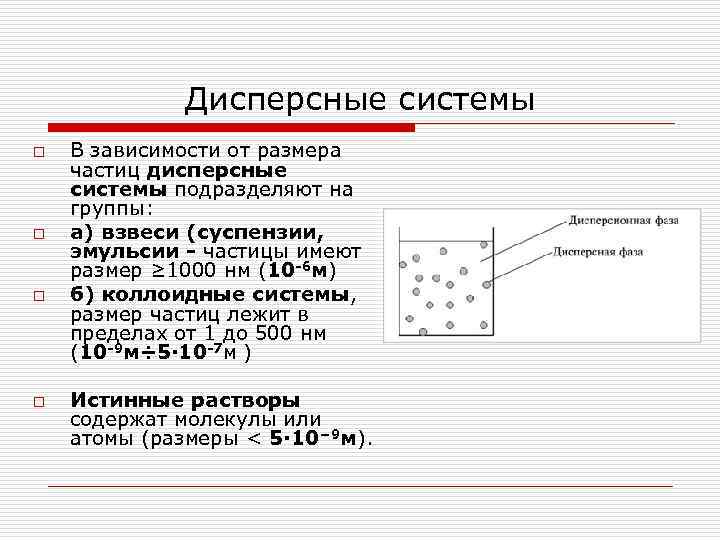
 Дисперсные системы o В зависимости от размера частиц дисперсные системы подразделяют на группы: o а) взвеси (суспензии, эмульсии - частицы имеют размер ≥ 1000 нм (10 -6 м) o б) коллоидные системы, размер частиц лежит в пределах от 1 до 500 нм (10 -9 м÷ 5· 10 -7 м ) o Истинные растворы содержат молекулы или атомы (размеры < 5· 10− 9 м).
Дисперсные системы o В зависимости от размера частиц дисперсные системы подразделяют на группы: o а) взвеси (суспензии, эмульсии - частицы имеют размер ≥ 1000 нм (10 -6 м) o б) коллоидные системы, размер частиц лежит в пределах от 1 до 500 нм (10 -9 м÷ 5· 10 -7 м ) o Истинные растворы содержат молекулы или атомы (размеры < 5· 10− 9 м).
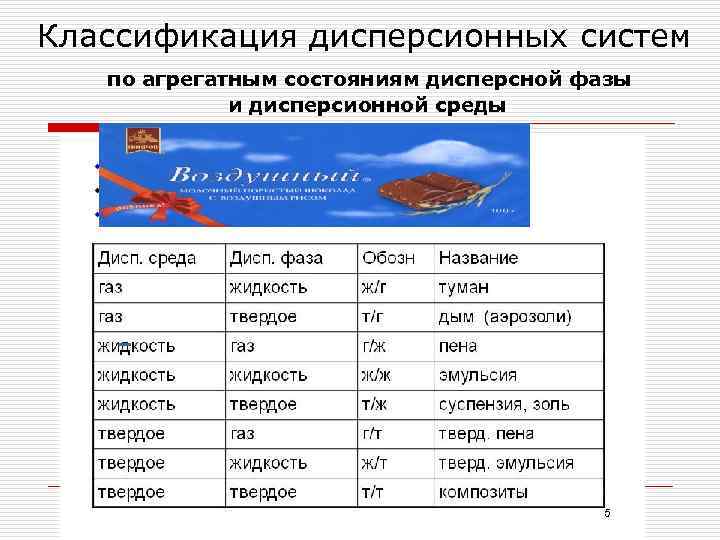
 Классификация дисперсионных систем по агрегатным состояниям дисперсной фазы и дисперсионной среды
Классификация дисперсионных систем по агрегатным состояниям дисперсной фазы и дисперсионной среды
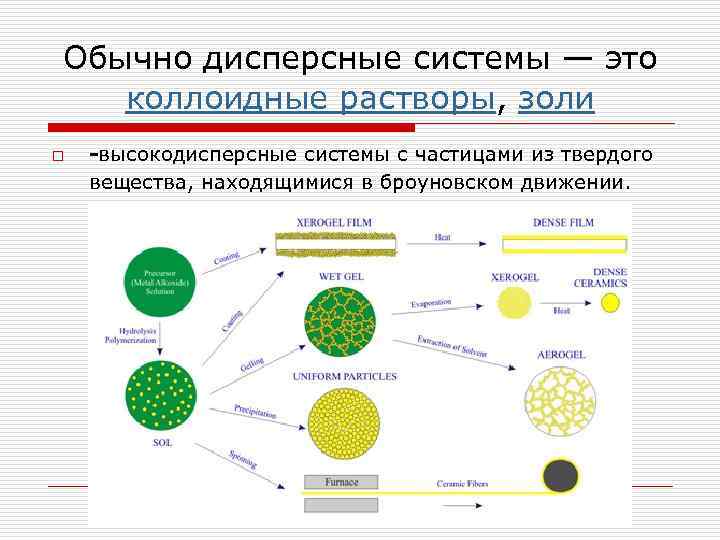
 Обычно дисперсные системы — это коллоидные растворы, золи o -высокодисперсные системы с частицами из твердого вещества, находящимися в броуновском движении.
Обычно дисперсные системы — это коллоидные растворы, золи o -высокодисперсные системы с частицами из твердого вещества, находящимися в броуновском движении.
 Строение геля и золя o Ге ли — структурированные дисперсные системы, состоящие из высокомолекулярных и низкомолекулярных веществ.
Строение геля и золя o Ге ли — структурированные дисперсные системы, состоящие из высокомолекулярных и низкомолекулярных веществ.
 Строение геля и золя o Наличие трёхмерного полимерного каркаса (сетки) сообщает гелям механические свойства твёрдых тел o Частицы дисперсной фазы гелей не могут участвовать в броуновском движении.
Строение геля и золя o Наличие трёхмерного полимерного каркаса (сетки) сообщает гелям механические свойства твёрдых тел o Частицы дисперсной фазы гелей не могут участвовать в броуновском движении.
 Строение геля и золя o Броуновское движение препятствует седиментации (оседанию) частиц под действием силы тяжести и является одной из причин устойчивости дисперсных систем.
Строение геля и золя o Броуновское движение препятствует седиментации (оседанию) частиц под действием силы тяжести и является одной из причин устойчивости дисперсных систем.
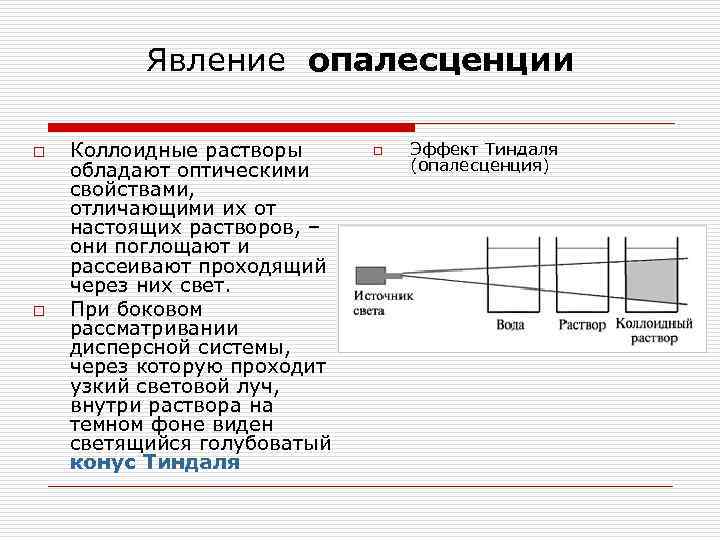
 Явление опалесценции o Коллоидные растворы o Эффект Тиндаля обладают оптическими (опалесценция) свойствами, отличающими их от настоящих растворов, – они поглощают и рассеивают проходящий через них свет. o При боковом рассматривании дисперсной системы, через которую проходит узкий световой луч, внутри раствора на темном фоне виден светящийся голубоватый конус Тиндаля
Явление опалесценции o Коллоидные растворы o Эффект Тиндаля обладают оптическими (опалесценция) свойствами, отличающими их от настоящих растворов, – они поглощают и рассеивают проходящий через них свет. o При боковом рассматривании дисперсной системы, через которую проходит узкий световой луч, внутри раствора на темном фоне виден светящийся голубоватый конус Тиндаля
 Эффект Тиндаля o Рассеяние света возможно, если размер коллоидной частицы меньше длины волны проходящего света и показатели преломления дисперсной фазы и дисперсионной среды различны
Эффект Тиндаля o Рассеяние света возможно, если размер коллоидной частицы меньше длины волны проходящего света и показатели преломления дисперсной фазы и дисперсионной среды различны
 ЛИОФИЛЬНЫЕ И ЛИОФОБНЫЕ ЗОЛИ o лиофобный - «боящийся o Лиофобные дисперсные жидкости» системы - например, дисперсии иодида o лиофильный серебра, кремнезема и «любящий жидкость» полистирольного латекса -образуются в результате o Если жидкой механической или химической обработки. дисперсионной средой является вода, o К лиофильным коллоидам относятся растворы используются термины макромолекул, например гидрофобный и желатин или крахмал в гидрофильный. воде
ЛИОФИЛЬНЫЕ И ЛИОФОБНЫЕ ЗОЛИ o лиофобный - «боящийся o Лиофобные дисперсные жидкости» системы - например, дисперсии иодида o лиофильный серебра, кремнезема и «любящий жидкость» полистирольного латекса -образуются в результате o Если жидкой механической или химической обработки. дисперсионной средой является вода, o К лиофильным коллоидам относятся растворы используются термины макромолекул, например гидрофобный и желатин или крахмал в гидрофильный. воде
 ЛИОФИЛЬНЫЕ И ЛИОФОБНЫЕ ЗОЛИ o лиофобный - «боящийся жидкости» o Лиофобные золи постепенно o лиофильный разрушаются из-за «любящий жидкость» самопроизвольного слипания твердых o Если жидкой частиц (коагуляция) дисперсионной средой или слияния жидких является вода, частиц используются термины (коалесценция) гидрофобный и гидрофильный. o Лиофильные золи образуются самопроизвольно и не разрушаются со временем
ЛИОФИЛЬНЫЕ И ЛИОФОБНЫЕ ЗОЛИ o лиофобный - «боящийся жидкости» o Лиофобные золи постепенно o лиофильный разрушаются из-за «любящий жидкость» самопроизвольного слипания твердых o Если жидкой частиц (коагуляция) дисперсионной средой или слияния жидких является вода, частиц используются термины (коалесценция) гидрофобный и гидрофильный. o Лиофильные золи образуются самопроизвольно и не разрушаются со временем
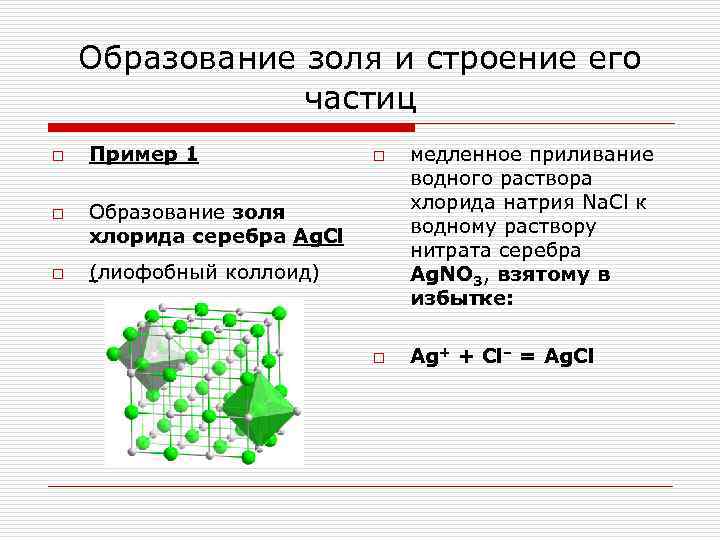
 Образование золя и строение его частиц o Пример 1 o медленное приливание водного раствора o Образование золя хлорида натрия Na. Cl к хлорида серебра Ag. Cl водному раствору нитрата серебра o (лиофобный коллоид) Ag. NO 3, взятому в избытке: o Ag+ + Cl– = Ag. Cl
Образование золя и строение его частиц o Пример 1 o медленное приливание водного раствора o Образование золя хлорида натрия Na. Cl к хлорида серебра Ag. Cl водному раствору нитрата серебра o (лиофобный коллоид) Ag. NO 3, взятому в избытке: o Ag+ + Cl– = Ag. Cl
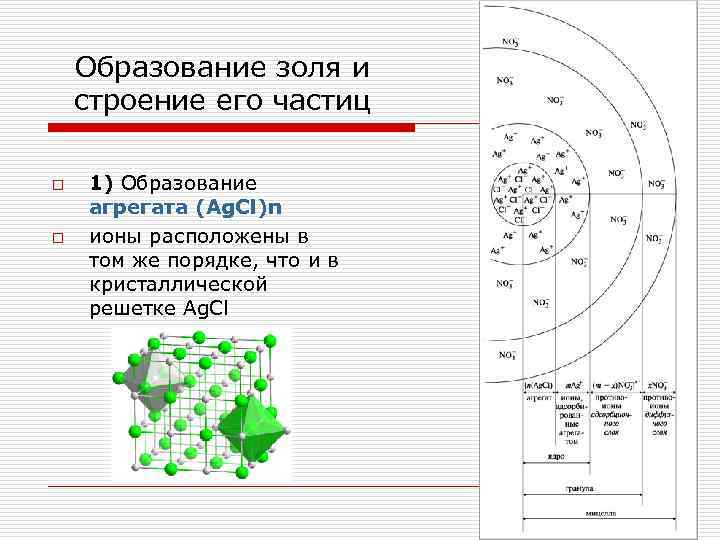
 Образование золя и строение его частиц o 1) Образование агрегата (Ag. Cl)n o ионы расположены в том же порядке, что и в кристаллической решетке Ag. Cl
Образование золя и строение его частиц o 1) Образование агрегата (Ag. Cl)n o ионы расположены в том же порядке, что и в кристаллической решетке Ag. Cl
 Образование золя и строение его частиц o 2) Агрегат (Ag. Cl)n адсорбирует на своей поверхности те ионы, которые входят в него и находятся в растворе в избытке - Ag+ o Агрегат (Ag. Cl)n со слоем ионов серебра Ag+приобретает положительный заряд. o Ионы, адсорбирующиеся на поверхности агрегата, придают частице заряд и называются потенциалопределяющими (в примере - Ag + ). {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
Образование золя и строение его частиц o 2) Агрегат (Ag. Cl)n адсорбирует на своей поверхности те ионы, которые входят в него и находятся в растворе в избытке - Ag+ o Агрегат (Ag. Cl)n со слоем ионов серебра Ag+приобретает положительный заряд. o Ионы, адсорбирующиеся на поверхности агрегата, придают частице заряд и называются потенциалопределяющими (в примере - Ag + ). {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
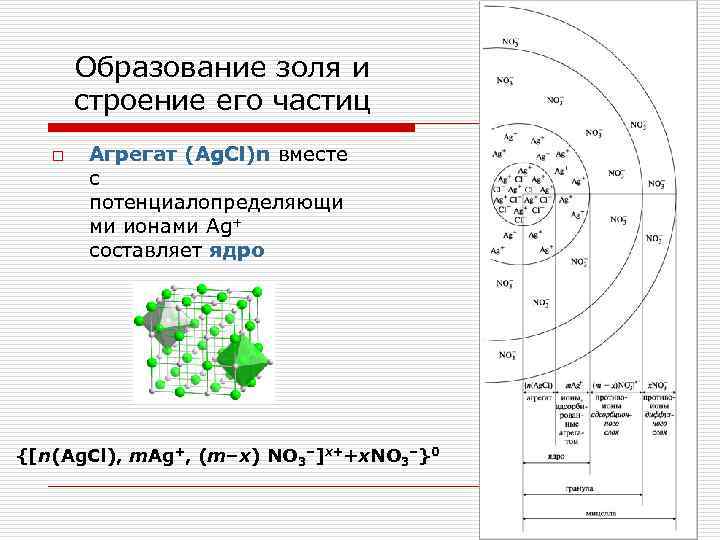
 Образование золя и строение его частиц o Агрегат (Ag. Cl)n вместе с потенциалопределяющи ми ионами Ag+ составляет ядро {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
Образование золя и строение его частиц o Агрегат (Ag. Cl)n вместе с потенциалопределяющи ми ионами Ag+ составляет ядро {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
 Образование золя и строение его частиц o 3) К заряженному ядру притягиваются ионы противоположного заряда – противоионы В примере: ионы, содержащиеся в растворе (но не входящие в состав агрегата), – нитрат- ионы NO 3– o Противоионы, непосредственно примыкающие к ядру, образуют адсорбционный слой противоионов {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
Образование золя и строение его частиц o 3) К заряженному ядру притягиваются ионы противоположного заряда – противоионы В примере: ионы, содержащиеся в растворе (но не входящие в состав агрегата), – нитрат- ионы NO 3– o Противоионы, непосредственно примыкающие к ядру, образуют адсорбционный слой противоионов {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
 Образование золя и строение его частиц o Ядро + противоионы адсорбционного слоя - коллоидная частица, или гранула {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
Образование золя и строение его частиц o Ядро + противоионы адсорбционного слоя - коллоидная частица, или гранула {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
 Образование золя и строение его частиц o 4) За адсорбционным слоем противоионов следует диффузный слой тех же противоионов. o Противоионы диффузного слоя ориентируют вокруг себя полярные молекулы растворителя, создавая дополнительную сольватную (гидратную в случае H 2 O) оболочку. o Гранула с противоионами диффузного слоя – мицелла {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
Образование золя и строение его частиц o 4) За адсорбционным слоем противоионов следует диффузный слой тех же противоионов. o Противоионы диффузного слоя ориентируют вокруг себя полярные молекулы растворителя, создавая дополнительную сольватную (гидратную в случае H 2 O) оболочку. o Гранула с противоионами диффузного слоя – мицелла {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
 Образование золя и строение его частиц o Знак заряда гранулы соответствует знаку заряда потенциалопределяющих ионов o в примере - Ag + o Суммарно заряд коллоидной частицы (гранулы) = разности зарядов адсорбированных ионов и противоионов m ─ (m – x) o Мицелла в отличие от гранулы электронейтральна {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
Образование золя и строение его частиц o Знак заряда гранулы соответствует знаку заряда потенциалопределяющих ионов o в примере - Ag + o Суммарно заряд коллоидной частицы (гранулы) = разности зарядов адсорбированных ионов и противоионов m ─ (m – x) o Мицелла в отличие от гранулы электронейтральна {[n(Ag. Cl), m. Ag+, (m–x) NO 3–]x++x. NO 3–}0
 Строение мицеллы хлорида серебра Формула мицеллы гидрозоля хлорида серебра {[n(Ag. Cl), m. Ag+, (m–x)NO 3–]x++x. NO 3–}0
Строение мицеллы хлорида серебра Формула мицеллы гидрозоля хлорида серебра {[n(Ag. Cl), m. Ag+, (m–x)NO 3–]x++x. NO 3–}0
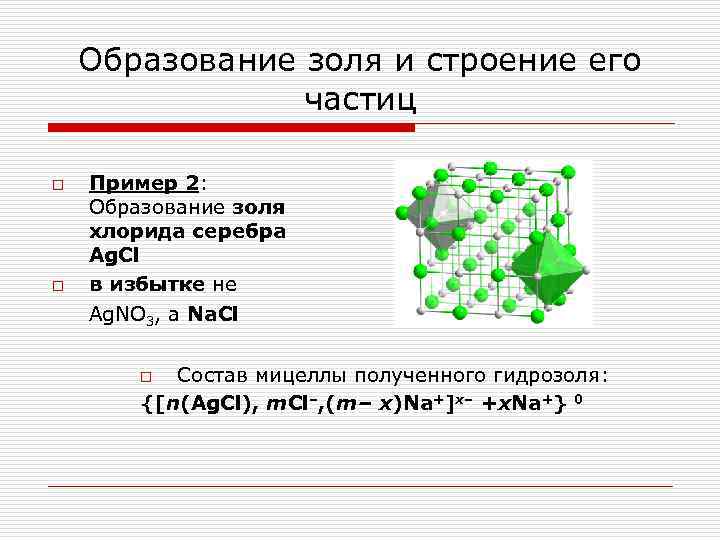
 Образование золя и строение его частиц o Пример 2: Образование золя хлорида серебра Ag. Cl o в избытке не Ag. NO 3, а Na. Cl o Состав мицеллы полученного гидрозоля: {[n(Ag. Cl), m. Cl–, (m– x)Na+]x– +x. Na+} 0
Образование золя и строение его частиц o Пример 2: Образование золя хлорида серебра Ag. Cl o в избытке не Ag. NO 3, а Na. Cl o Состав мицеллы полученного гидрозоля: {[n(Ag. Cl), m. Cl–, (m– x)Na+]x– +x. Na+} 0

