Коллоидная химия.ppt
- Количество слайдов: 123
 Коллоидная химия Лекция 2
Коллоидная химия Лекция 2
 Вопрос n Поверхностная энергия и поверхностное натяжение. Методы определения поверхностного натяжения. Зависимость поверхностного натяжения от температуры и концентрации ПАВ.
Вопрос n Поверхностная энергия и поверхностное натяжение. Методы определения поверхностного натяжения. Зависимость поверхностного натяжения от температуры и концентрации ПАВ.
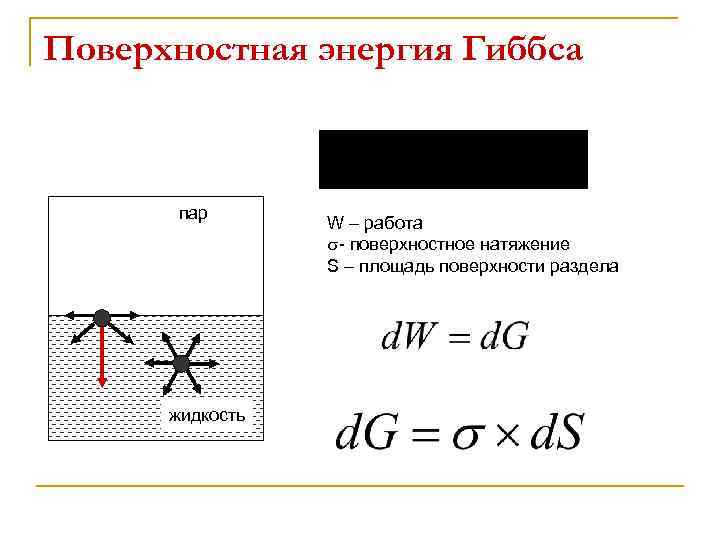 Поверхностная энергия Гиббса пар жидкость W – работа - поверхностное натяжение S – площадь поверхности раздела
Поверхностная энергия Гиббса пар жидкость W – работа - поверхностное натяжение S – площадь поверхности раздела
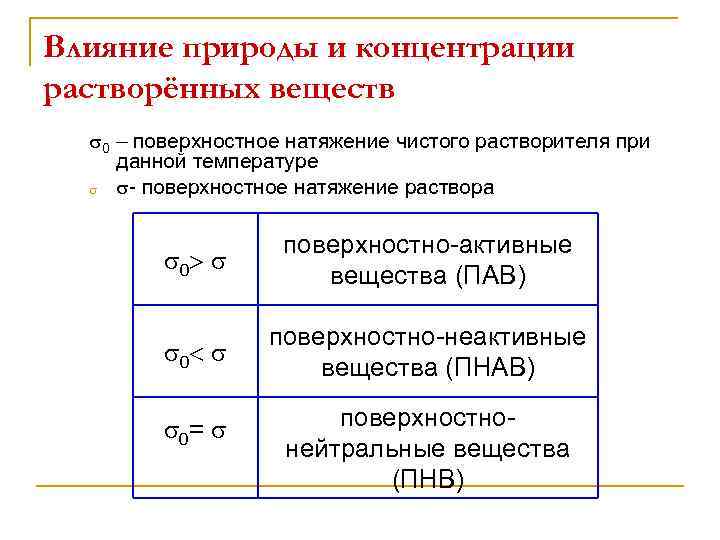 Влияние природы и концентрации растворённых веществ 0 – поверхностное натяжение чистого растворителя при данной температуре - поверхностное натяжение раствора 0 поверхностно-активные вещества (ПАВ) 0 поверхностно-неактивные вещества (ПНАВ) 0 = поверхностнонейтральные вещества (ПНВ)
Влияние природы и концентрации растворённых веществ 0 – поверхностное натяжение чистого растворителя при данной температуре - поверхностное натяжение раствора 0 поверхностно-активные вещества (ПАВ) 0 поверхностно-неактивные вещества (ПНАВ) 0 = поверхностнонейтральные вещества (ПНВ)
 Поверхностно-активные вещества (ПАВ) n n Ионогенные q Анионоактивные (соли высших карбоновых и сульфоновых кислот) q Катионоактивные (соли алкил- и ариламмониевых оснований) Неионогенные q Высшие спирты, амины и др. Схема строения ПАВ Неполярный «хвост» Полярная «голова»
Поверхностно-активные вещества (ПАВ) n n Ионогенные q Анионоактивные (соли высших карбоновых и сульфоновых кислот) q Катионоактивные (соли алкил- и ариламмониевых оснований) Неионогенные q Высшие спирты, амины и др. Схема строения ПАВ Неполярный «хвост» Полярная «голова»
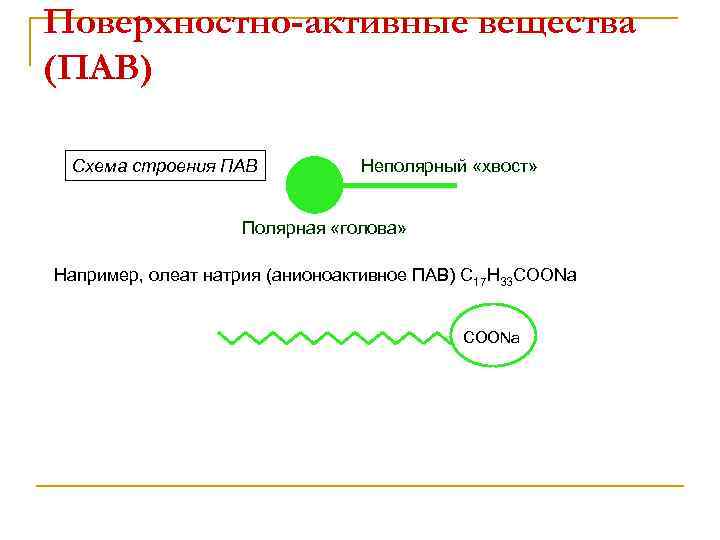 Поверхностно-активные вещества (ПАВ) Схема строения ПАВ Неполярный «хвост» Полярная «голова» Например, олеат натрия (анионоактивное ПАВ) С 17 Н 33 СООNa COONa
Поверхностно-активные вещества (ПАВ) Схема строения ПАВ Неполярный «хвост» Полярная «голова» Например, олеат натрия (анионоактивное ПАВ) С 17 Н 33 СООNa COONa
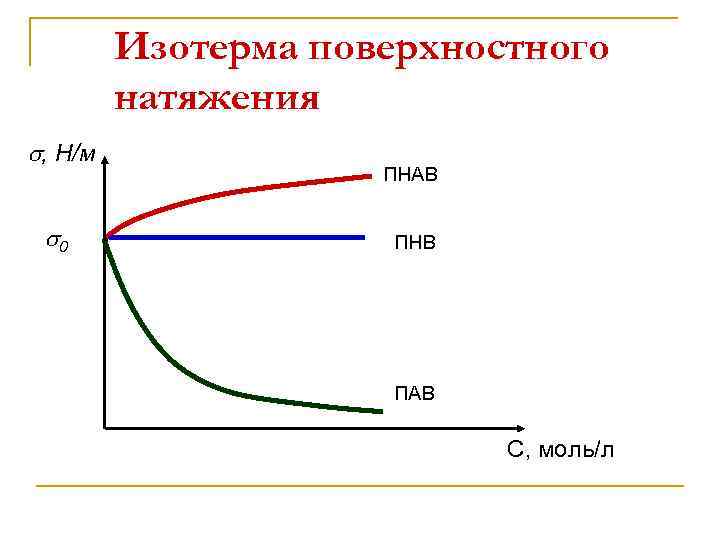 Изотерма поверхностного натяжения , Н/м 0 ПНАВ ПНВ ПАВ С, моль/л
Изотерма поверхностного натяжения , Н/м 0 ПНАВ ПНВ ПАВ С, моль/л
 Вопрос n Адсорбция на границе раздела: твердое тело – газ и твердое тело – жидкость. Факторы, влияющие на величину адсорбции газов и растворенных веществ. Уравнения изотермы адсорбции Фрейндлиха и Лэнгмюра
Вопрос n Адсорбция на границе раздела: твердое тело – газ и твердое тело – жидкость. Факторы, влияющие на величину адсорбции газов и растворенных веществ. Уравнения изотермы адсорбции Фрейндлиха и Лэнгмюра
 Адсорбция n n К. В. Шееле (18 век) – адсорбция газов Г. Е. Ловиц в 1785 год – адсорбция активированным углем из растворов n n Соссюр 1814 год – адсорбция газов Гиббс в конце 19 века – термодинамическую теорию адсорбции из растворов n Лэнгмюр, Брунауэр, Н. А. Шилов, М. М. Дубинин, А. В. Киселёв
Адсорбция n n К. В. Шееле (18 век) – адсорбция газов Г. Е. Ловиц в 1785 год – адсорбция активированным углем из растворов n n Соссюр 1814 год – адсорбция газов Гиббс в конце 19 века – термодинамическую теорию адсорбции из растворов n Лэнгмюр, Брунауэр, Н. А. Шилов, М. М. Дубинин, А. В. Киселёв
 Адсорбция на границе раздела ж/г и ж/ж. Уравнение Гиббса G – поверхностная активность
Адсорбция на границе раздела ж/г и ж/ж. Уравнение Гиббса G – поверхностная активность
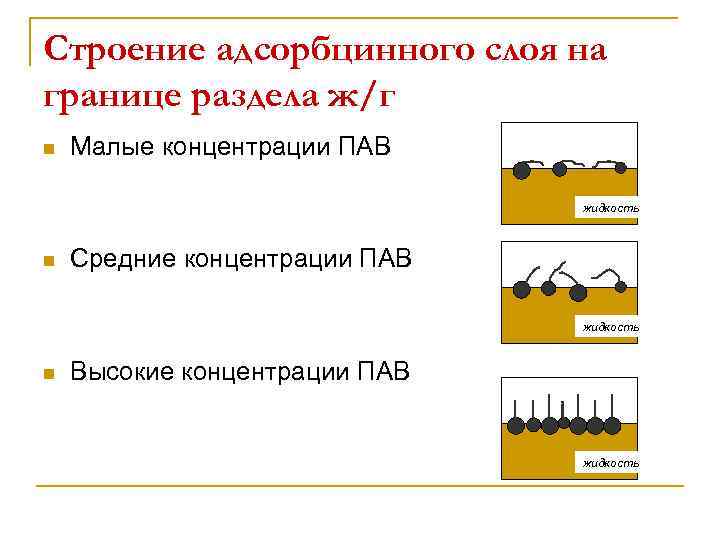 Строение адсорбцинного слоя на границе раздела ж/г n Малые концентрации ПАВ жидкость n Средние концентрации ПАВ жидкость n Высокие концентрации ПАВ жидкость
Строение адсорбцинного слоя на границе раздела ж/г n Малые концентрации ПАВ жидкость n Средние концентрации ПАВ жидкость n Высокие концентрации ПАВ жидкость
 Площадь (S 0) и длина молекулы (ℓ) ПАВ
Площадь (S 0) и длина молекулы (ℓ) ПАВ
 Теория И. Лэнгмюра n n n Гmax – максимальное значение адсорбции при условии полного заполнения всех активных центров; Р – равновесное давление газа; К – константа адсорбционного равновесия
Теория И. Лэнгмюра n n n Гmax – максимальное значение адсорбции при условии полного заполнения всех активных центров; Р – равновесное давление газа; К – константа адсорбционного равновесия
 Адсорбция т/ж Гmax – максимальное значение адсорбции при условии полного заполнения всех активных центров; С – равновесное давление газа; К – константа адсорбционного равновесия
Адсорбция т/ж Гmax – максимальное значение адсорбции при условии полного заполнения всех активных центров; С – равновесное давление газа; К – константа адсорбционного равновесия
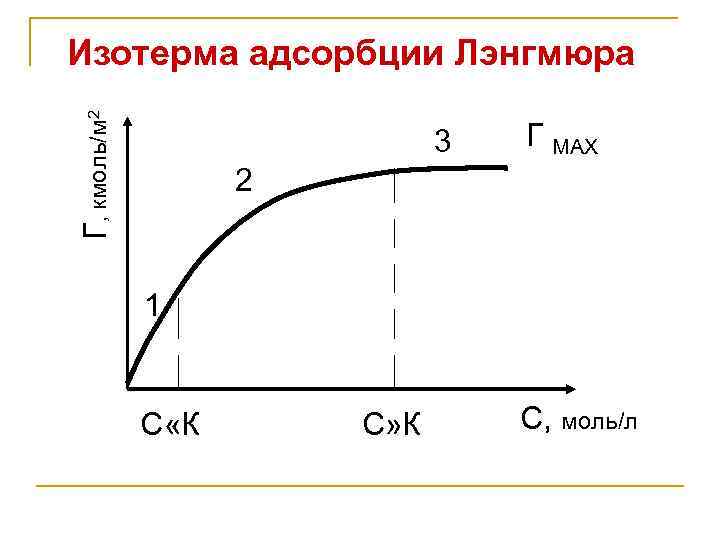 Г, кмоль/м 2 Изотерма адсорбции Лэнгмюра 3 Г МАХ 2 1 С «К С» К С, моль/л
Г, кмоль/м 2 Изотерма адсорбции Лэнгмюра 3 Г МАХ 2 1 С «К С» К С, моль/л
 Уравнение Фрейндлиха р – равновесное давление газа над поглотителем; С – равновесная концентрация адсорбтива, выраженная в моль/л. - эмпирические константы, которые легко находятся графичес
Уравнение Фрейндлиха р – равновесное давление газа над поглотителем; С – равновесная концентрация адсорбтива, выраженная в моль/л. - эмпирические константы, которые легко находятся графичес
 Вопрос n Адсорбция электролитов. Избирательная адсорбция ионов. Правило Панета. Фаянса. Ионообменная адсорбция. Иониты и их классификация. Обменная емкость. Применение ионитов в фармации.
Вопрос n Адсорбция электролитов. Избирательная адсорбция ионов. Правило Панета. Фаянса. Ионообменная адсорбция. Иониты и их классификация. Обменная емкость. Применение ионитов в фармации.
 Ионная адсорбция из растворов Виды ионной адсорбции n избирательная; n обменная
Ионная адсорбция из растворов Виды ионной адсорбции n избирательная; n обменная
 Избирательная адсорбция. Правило Панета-Фаянса На поверхности твёрдого тела адсорбируются преимущественно те ионы, которые: n достраивают кристаллическую решетку твёрдого тела и образуют с ним труднорастворимое соединение n находятся в растворе в избытке
Избирательная адсорбция. Правило Панета-Фаянса На поверхности твёрдого тела адсорбируются преимущественно те ионы, которые: n достраивают кристаллическую решетку твёрдого тела и образуют с ним труднорастворимое соединение n находятся в растворе в избытке
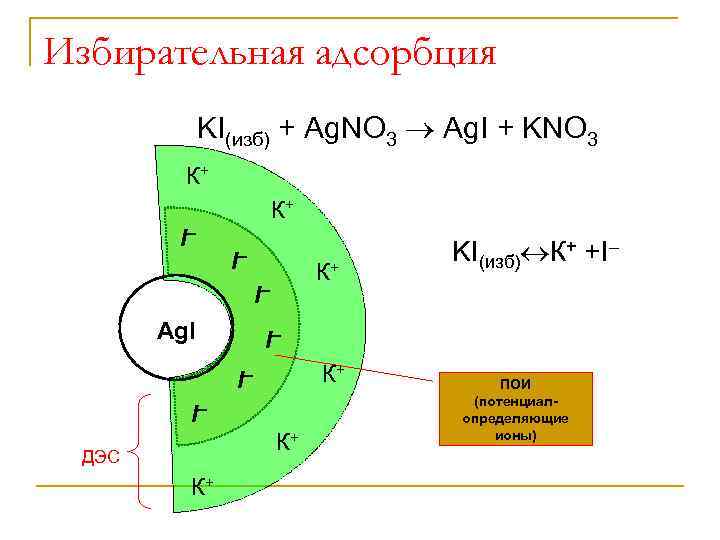 Избирательная адсорбция KI(изб) + Ag. NO 3 Ag. I + KNO 3 К+ I Ag. I I К+ ДЭС К+ KI(изб) К+ +I ПОИ (потенциалопределяющие ионы)
Избирательная адсорбция KI(изб) + Ag. NO 3 Ag. I + KNO 3 К+ I Ag. I I К+ ДЭС К+ KI(изб) К+ +I ПОИ (потенциалопределяющие ионы)
 Обменная (ионообменная) адсорбция Adˉ H+ + Na+ + Cℓˉ → Ad-Na+ + H+ + Cℓˉ Ad+OHˉ + Na+ + Cℓˉ → Ad+ Cℓˉ + Na+ + OHˉ пермутит Na 2 O. Aℓ 2 O 3. 3 Si. O 2. 2 H 2 O ПNa 2 + Ca 2+ + 2 Cℓˉ → ПСа 2+ + 2 Na+ + 2 Cℓˉ
Обменная (ионообменная) адсорбция Adˉ H+ + Na+ + Cℓˉ → Ad-Na+ + H+ + Cℓˉ Ad+OHˉ + Na+ + Cℓˉ → Ad+ Cℓˉ + Na+ + OHˉ пермутит Na 2 O. Aℓ 2 O 3. 3 Si. O 2. 2 H 2 O ПNa 2 + Ca 2+ + 2 Cℓˉ → ПСа 2+ + 2 Na+ + 2 Cℓˉ
 Обменная ёмкость ионитов (ОЕ)
Обменная ёмкость ионитов (ОЕ)
 Вопрос n Дисперсные системы. Природа коллоидного состояния вещества. Дисперсная фаза и дисперсионная среда. Степень дисперсности. Классификация дисперсных систем по степени дисперсности.
Вопрос n Дисперсные системы. Природа коллоидного состояния вещества. Дисперсная фаза и дисперсионная среда. Степень дисперсности. Классификация дисперсных систем по степени дисперсности.
 Степень дисперсности
Степень дисперсности
 Вопрос n Методы получения коллоидных растворов. Условия получения коллоидных растворов. Очистка коллоидных растворов. Диализ. Электродиализ. Ультрафильтрация
Вопрос n Методы получения коллоидных растворов. Условия получения коллоидных растворов. Очистка коллоидных растворов. Диализ. Электродиализ. Ультрафильтрация
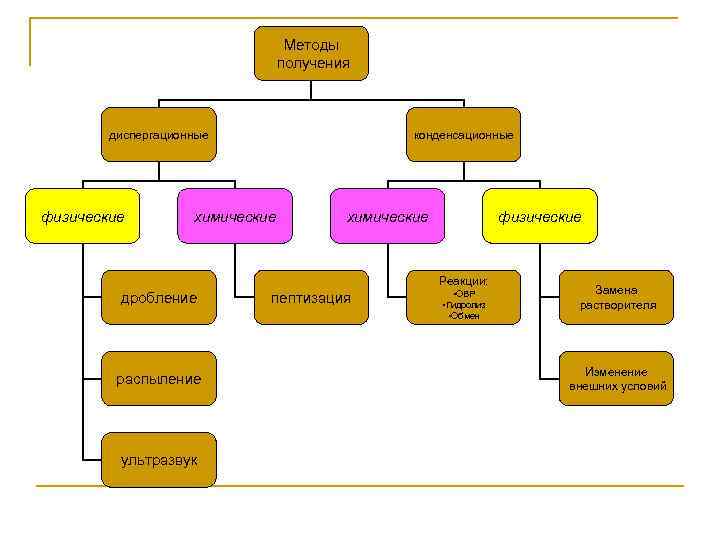 Методы получения диспергационные физические конденсационные химические физические Реакции: дробление распыление ультразвук пептизация • ОВР • Гидролиз • Обмен Замена растворителя Изменение внешних условий
Методы получения диспергационные физические конденсационные химические физические Реакции: дробление распыление ультразвук пептизация • ОВР • Гидролиз • Обмен Замена растворителя Изменение внешних условий
 Методы очистки коллоидных растворов. 1. Диализ. 2. Электродиализ. 3. Ультрафильтрация. 4. Вивидиализ. 5. Компенсационный диализ.
Методы очистки коллоидных растворов. 1. Диализ. 2. Электродиализ. 3. Ультрафильтрация. 4. Вивидиализ. 5. Компенсационный диализ.
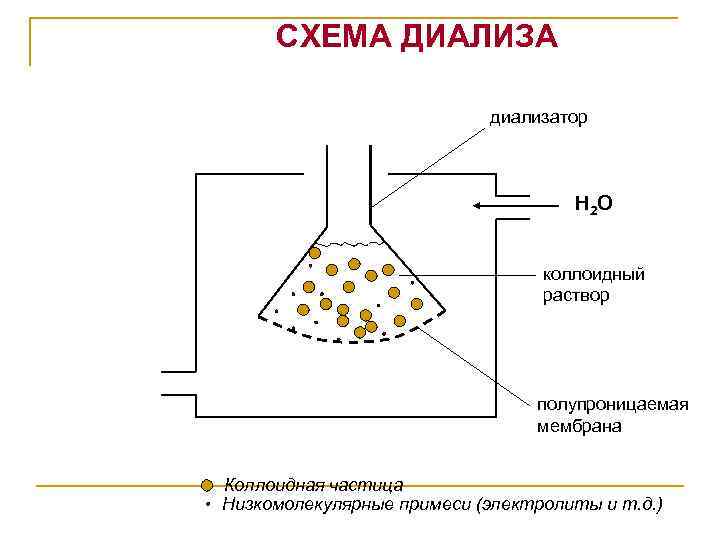 СХЕМА ДИАЛИЗА диализатор H 2 O коллоидный раствор полупроницаемая мембрана Коллоидная частица Низкомолекулярные примеси (электролиты и т. д. )
СХЕМА ДИАЛИЗА диализатор H 2 O коллоидный раствор полупроницаемая мембрана Коллоидная частица Низкомолекулярные примеси (электролиты и т. д. )
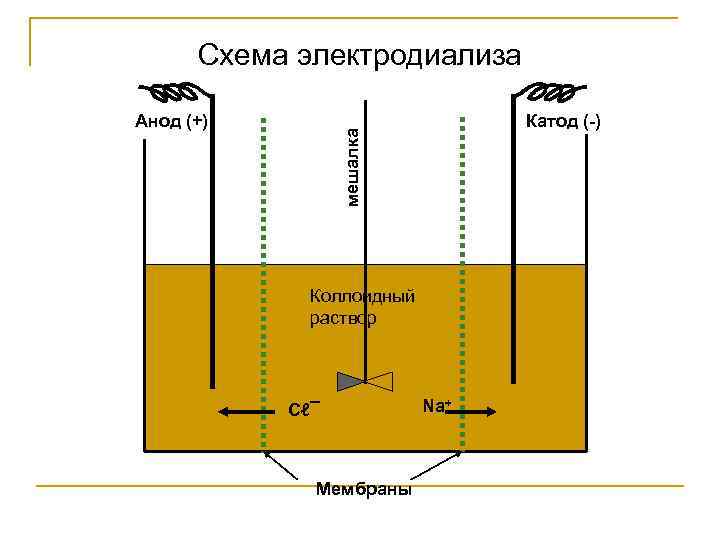 Схема электродиализа Катод (-) мешалка Анод (+) Коллоидный раствор Cℓ¯ Мембраны Na+
Схема электродиализа Катод (-) мешалка Анод (+) Коллоидный раствор Cℓ¯ Мембраны Na+
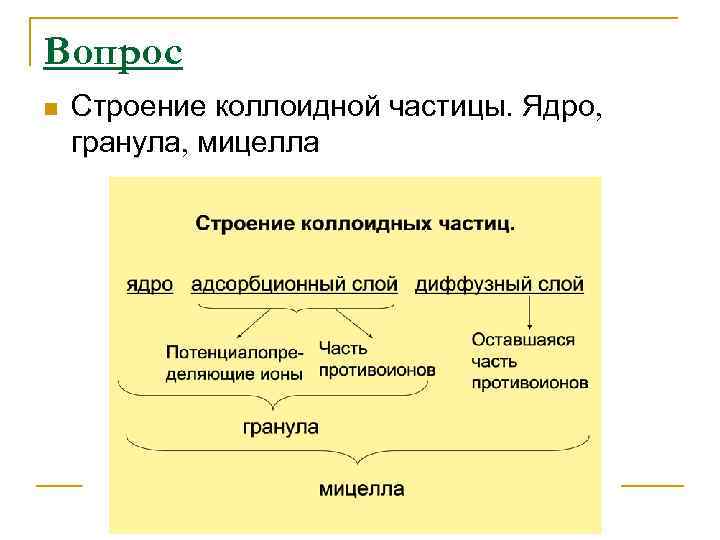 Вопрос n Строение коллоидной частицы. Ядро гранула мицелла
Вопрос n Строение коллоидной частицы. Ядро гранула мицелла
 Вопрос n Особенности молекулярно-кинетических свойств коллоидных систем. Броуновское движение (уравнение Эйнштейна), диффузия (уравнение Фика) осмотическое давление золей.
Вопрос n Особенности молекулярно-кинетических свойств коллоидных систем. Броуновское движение (уравнение Эйнштейна), диффузия (уравнение Фика) осмотическое давление золей.
 Расчёт среднего значения квадрата смещения коллоидных частиц. Уравнение Эйнштейна-Смолуховского t – время; r – радиус взвешенных частиц; η – вязкость среды; NA – число Авогадро
Расчёт среднего значения квадрата смещения коллоидных частиц. Уравнение Эйнштейна-Смолуховского t – время; r – радиус взвешенных частиц; η – вязкость среды; NA – число Авогадро
 Коэффициент диффузии. Уравнение Эйнштейна (1906)
Коэффициент диффузии. Уравнение Эйнштейна (1906)
 Осмотическое давление золей. Уравнение Вант-Гоффа. Р = с. RT (для истинных растворов) Для коллоидных растворов:
Осмотическое давление золей. Уравнение Вант-Гоффа. Р = с. RT (для истинных растворов) Для коллоидных растворов:
 Вопрос n Оптические свойства коллоидных растворов. Опалесценция и конус Тиндаля
Вопрос n Оптические свойства коллоидных растворов. Опалесценция и конус Тиндаля
 Оптические свойства коллоидных растворов 1. 2. 3. Опалесценция. Эффект Тиндаля. Окраска золей.
Оптические свойства коллоидных растворов 1. 2. 3. Опалесценция. Эффект Тиндаля. Окраска золей.
 Конус Тиндаля конус Тиндаля Истинный раствор Коллоидный раствор
Конус Тиндаля конус Тиндаля Истинный раствор Коллоидный раствор
 Вопрос n Электрокинетические явления 1 и 2 рода. Значение электрофореза и электроосмоса в изучении строения коллоидных систем.
Вопрос n Электрокинетические явления 1 и 2 рода. Значение электрофореза и электроосмоса в изучении строения коллоидных систем.
 Виды электрокинетических явлений n 1 -го рода (прямые) – электрофорез, электроосмос) n 2 -го рода (обратные) – потенциал оседания и потенциал протекания
Виды электрокинетических явлений n 1 -го рода (прямые) – электрофорез, электроосмос) n 2 -го рода (обратные) – потенциал оседания и потенциал протекания
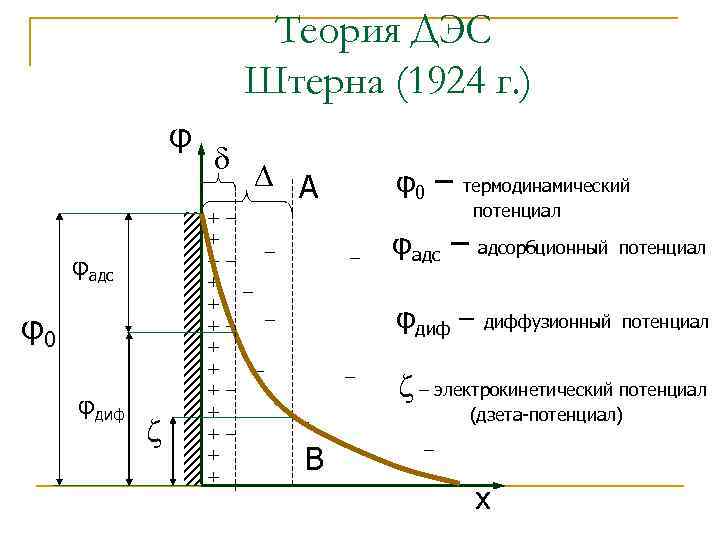 Теория ДЭС Штерна (1924 г. ) φ φадс φ0 φдиф + + + + A φ0 – – – – – φадс – адсорбционный потенциал φдиф – – – термодинамический потенциал диффузионный потенциал – электрокинетический потенциал (дзета-потенциал) – B – x
Теория ДЭС Штерна (1924 г. ) φ φадс φ0 φдиф + + + + A φ0 – – – – – φадс – адсорбционный потенциал φдиф – – – термодинамический потенциал диффузионный потенциал – электрокинетический потенциал (дзета-потенциал) – B – x
 Расчет электрокинетического потенциала n По данным электрофореза: n. По данным электроосмоса:
Расчет электрокинетического потенциала n По данным электрофореза: n. По данным электроосмоса:
 Вопрос n Коагуляция быстрая и медленная. Коагуляция золей электролитами. Правило Шульце-Гарди. Порог коагуляции
Вопрос n Коагуляция быстрая и медленная. Коагуляция золей электролитами. Правило Шульце-Гарди. Порог коагуляции
 Устойчивость дисперсных систем n n Агрегативная – способность частиц противодействовать слипанию (агрегации) Кинетическая – способность частиц противодействовать действию сил тяжести
Устойчивость дисперсных систем n n Агрегативная – способность частиц противодействовать слипанию (агрегации) Кинетическая – способность частиц противодействовать действию сил тяжести
 Коагуляция n Процесс разрушения дисперсной системы с потерей агрегативной и кинетической устойчивости
Коагуляция n Процесс разрушения дисперсной системы с потерей агрегативной и кинетической устойчивости
 Причины коагуляции n Механическое воздействие n Температура n Звук, свет, радиация и т. д. n Добавление электролитов
Причины коагуляции n Механическое воздействие n Температура n Звук, свет, радиация и т. д. n Добавление электролитов
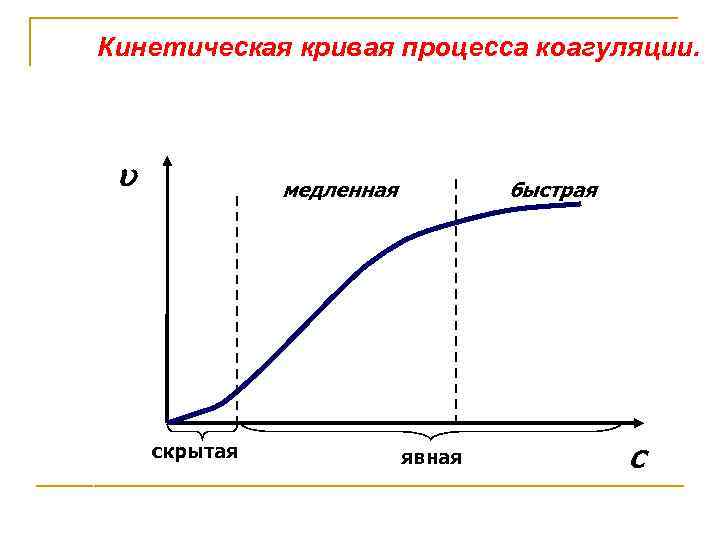 Кинетическая кривая процесса коагуляции. медленная скрытая быстрая явная С
Кинетическая кривая процесса коагуляции. медленная скрытая быстрая явная С
 Расчёт порога коагуляции - порог коагуляции; V 1 – объём электролита; V 2 – общий объём коллоидной системы (объём золя + объём электролита); С –молярная концентрация эквивалента электролита.
Расчёт порога коагуляции - порог коагуляции; V 1 – объём электролита; V 2 – общий объём коллоидной системы (объём золя + объём электролита); С –молярная концентрация эквивалента электролита.
 Правило Шульце-Гарди n Коагулирующим действием обладает ион, имеющий заряд противоположный знаку заряда коллоидной частице по
Правило Шульце-Гарди n Коагулирующим действием обладает ион, имеющий заряд противоположный знаку заряда коллоидной частице по
 Правило Шульце-Гарди n Чем больше заряд коагулирующего иона, тем больше его коагулирующая способность
Правило Шульце-Гарди n Чем больше заряд коагулирующего иона, тем больше его коагулирующая способность

 Вопрос n Коагуляция золей смесями электролитов. Антагонизм, синергизм и аддитивное действие электролитов. Чередование зон коагуляции. Привыкание золей.
Вопрос n Коагуляция золей смесями электролитов. Антагонизм, синергизм и аддитивное действие электролитов. Чередование зон коагуляции. Привыкание золей.
 Коагуляция смесями электролитов n n n аддитивность – суммирование коагулирующего действия антагонизм – ослабление одним электролитом действия другого синергизм – усиление действия одного электролита другим
Коагуляция смесями электролитов n n n аддитивность – суммирование коагулирующего действия антагонизм – ослабление одним электролитом действия другого синергизм – усиление действия одного электролита другим

 Чередование зон коагуляции n чередование электронейтральности состояний и заряженности частиц, наблюдаемое при добавлении значительных многозарядных ионов концентраций
Чередование зон коагуляции n чередование электронейтральности состояний и заряженности частиц, наблюдаемое при добавлении значительных многозарядных ионов концентраций
 Явление привыкания золей n при медленном добавлении электролита коллоидные системы теряют устойчивость при введении большего коагулятора, чем при быстром количества
Явление привыкания золей n при медленном добавлении электролита коллоидные системы теряют устойчивость при введении большего коагулятора, чем при быстром количества
 Вопрос n Коллоидная Пептизация защита. Сенсибилизация.
Вопрос n Коллоидная Пептизация защита. Сенсибилизация.
 Коллоидная защита n Стабилизация коллоидных растворов веществами, создающими структурномеханический барьер, препятствующий слипанию частиц, Такими веществами являются ПАВ и ВМВ.
Коллоидная защита n Стабилизация коллоидных растворов веществами, создающими структурномеханический барьер, препятствующий слипанию частиц, Такими веществами являются ПАВ и ВМВ.
 Сенсибилизация n снижение устойчивости коллоидов при малых добавках ВМВ
Сенсибилизация n снижение устойчивости коллоидов при малых добавках ВМВ
 Пептизация n Процесс перевода свежевыпавшего осадка в коллоидный раствор
Пептизация n Процесс перевода свежевыпавшего осадка в коллоидный раствор
 Виды пептизации n пептизация промыванием осадка; n пептизация осадка электролитом; n пептизация поверхностно-активными веществами; n химическая пептизация
Виды пептизации n пептизация промыванием осадка; n пептизация осадка электролитом; n пептизация поверхностно-активными веществами; n химическая пептизация
 Вопрос n Эмульсии: типы эмульсий, методы получения и свойства. Механизм действия эмульгаторов. Применение эмульсий в фармации. Обращение фаз эмульсий
Вопрос n Эмульсии: типы эмульсий, методы получения и свойства. Механизм действия эмульгаторов. Применение эмульсий в фармации. Обращение фаз эмульсий
 ЭМУЛЬСИИ Дисперсные системы ж/ж; Грубодисперсные (1 -50) 10 -6 м; Условие частичная образования: полная нерастворимость жидкости в другой. или одной
ЭМУЛЬСИИ Дисперсные системы ж/ж; Грубодисперсные (1 -50) 10 -6 м; Условие частичная образования: полная нерастворимость жидкости в другой. или одной
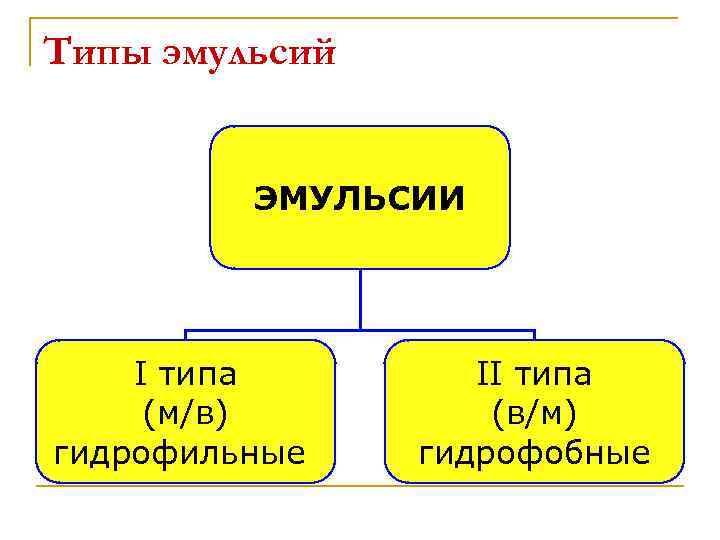 Типы эмульсий ЭМУЛЬСИИ I типа (м/в) гидрофильные II типа (в/м) гидрофобные
Типы эмульсий ЭМУЛЬСИИ I типа (м/в) гидрофильные II типа (в/м) гидрофобные
 МЕТОДЫ ПОЛУЧЕНИЯ ЭМУЛЬСИЙ n Диспергационный n Конденсационный
МЕТОДЫ ПОЛУЧЕНИЯ ЭМУЛЬСИЙ n Диспергационный n Конденсационный
 Эмульгаторы Желатин, казеин, альбумин, Смолы, ланолин, каучук и крахмал, камеди, т. д. пектиновые вещества, лецитин и т. д. Мыла щелочных металлов (Na, K), желчные кислоты Мыла многовалентных металлов (Zn, Mg, Al), холестерин ВМВ Ca. CO 3, Ca. SO 4, Fe 2 O 3, Si. O 2, Pb. O 2, тальк, сажа и т. д. глина и т. д. порошки Эмульгаторы II типа ПАВ Эмульгаторы I типа
Эмульгаторы Желатин, казеин, альбумин, Смолы, ланолин, каучук и крахмал, камеди, т. д. пектиновые вещества, лецитин и т. д. Мыла щелочных металлов (Na, K), желчные кислоты Мыла многовалентных металлов (Zn, Mg, Al), холестерин ВМВ Ca. CO 3, Ca. SO 4, Fe 2 O 3, Si. O 2, Pb. O 2, тальк, сажа и т. д. глина и т. д. порошки Эмульгаторы II типа ПАВ Эмульгаторы I типа
 Обращение фаз эмульсий n Перевод эмульсии одного типа в другой. n Может быть вызвано: Механическим воздействием Изменением типа эмульгатора n
Обращение фаз эмульсий n Перевод эмульсии одного типа в другой. n Может быть вызвано: Механическим воздействием Изменением типа эмульгатора n
 Вопрос n Получение и общие свойства суспензий. Устойчивость суспензий и ее нарушение. Флокуляция. Седиментометрический анализ суспензий. Пасты. Применение суспензий в фармации.
Вопрос n Получение и общие свойства суспензий. Устойчивость суспензий и ее нарушение. Флокуляция. Седиментометрический анализ суспензий. Пасты. Применение суспензий в фармации.
 Суспензии n микрогетерогенные (10 -7 - 10 -5 м) системы с твердой дисперсной фазой и жидкой дисперсионной средой.
Суспензии n микрогетерогенные (10 -7 - 10 -5 м) системы с твердой дисперсной фазой и жидкой дисперсионной средой.
 Получение суспензий n n n Механический - взмучивание высокодисперсных систем в дисперсионной среде; Диспергационный или дисперсионный; Конденсационный.
Получение суспензий n n n Механический - взмучивание высокодисперсных систем в дисперсионной среде; Диспергационный или дисперсионный; Конденсационный.
 Свойства суспензий Слабо проявляются n Броуновское движение n Диффузия n Осмотическое давление n Опалесценция
Свойства суспензий Слабо проявляются n Броуновское движение n Диффузия n Осмотическое давление n Опалесценция
 Устойчивость суспензий Кинетически неустойчивые дисперсные системы Устойчивость обеспечивается за счет: n Адсорбции ионов на поверхности частиц (ДЭС) n Повышения вязкости среды n Уменьшения размеров частиц n Добавления ВМВ или ПАВ
Устойчивость суспензий Кинетически неустойчивые дисперсные системы Устойчивость обеспечивается за счет: n Адсорбции ионов на поверхности частиц (ДЭС) n Повышения вязкости среды n Уменьшения размеров частиц n Добавления ВМВ или ПАВ
 Седиментометрический анализ суспензий n метод определения степени дисперсности суспензий, основанный на измерении скорости седиментации частиц Закон Стокса
Седиментометрический анализ суспензий n метод определения степени дисперсности суспензий, основанный на измерении скорости седиментации частиц Закон Стокса
 Пасты n n Концентрированные стабилизированные суспензии Содержание твердой фазы в пастах не менее 25% (до 75 -80%)
Пасты n n Концентрированные стабилизированные суспензии Содержание твердой фазы в пастах не менее 25% (до 75 -80%)
 Вопрос n Аэрозоли и их свойства. Получение, молекулярно-кинетические свойства. Электрические свойства. Агрегативная устойчивость и факторы ее определяющие. Порошки и их свойства. Применение порошков и аэрозолей в фармации
Вопрос n Аэрозоли и их свойства. Получение, молекулярно-кинетические свойства. Электрические свойства. Агрегативная устойчивость и факторы ее определяющие. Порошки и их свойства. Применение порошков и аэрозолей в фармации
 Аэрозоли n свободно-дисперсные системы с газообразной дисперсионной средой и дисперсной фазой, состоящей из твёрдых или жидких частиц
Аэрозоли n свободно-дисперсные системы с газообразной дисперсионной средой и дисперсной фазой, состоящей из твёрдых или жидких частиц
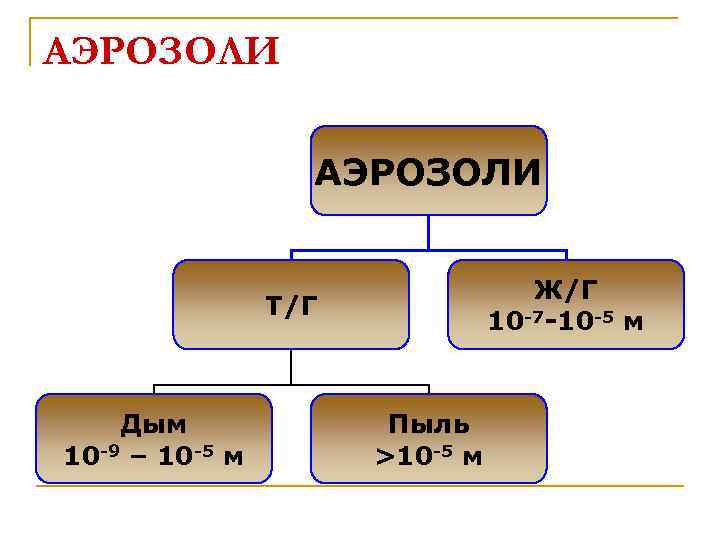 АЭРОЗОЛИ Ж/Г 10 -7 -10 -5 м Т/Г Дым 10 -9 – 10 -5 м Пыль >10 -5 м
АЭРОЗОЛИ Ж/Г 10 -7 -10 -5 м Т/Г Дым 10 -9 – 10 -5 м Пыль >10 -5 м
 МЕТОДЫ ПОЛУЧЕНИЯ АЭРОЗОЛЕЙ n Диспергационный (распыление, взрыв) n Конденсационный (химические реакции в газовой фазе, охлаждение пересыщенных паров)
МЕТОДЫ ПОЛУЧЕНИЯ АЭРОЗОЛЕЙ n Диспергационный (распыление, взрыв) n Конденсационный (химические реакции в газовой фазе, охлаждение пересыщенных паров)
 ФАКТОРЫ УСТОЙЧИВОСТИ АЭРОЗОЛЕЙ Наличие электрического заряда на частицах; Адсорбция молекул газа на частицах;
ФАКТОРЫ УСТОЙЧИВОСТИ АЭРОЗОЛЕЙ Наличие электрического заряда на частицах; Адсорбция молекул газа на частицах;
 Коагуляция аэрозолей Скорость коагуляции зависит от: Численной концентрации; Конвекционных потоков; Механического перемешивания; Ультразвуковых колебаний
Коагуляция аэрозолей Скорость коагуляции зависит от: Численной концентрации; Конвекционных потоков; Механического перемешивания; Ультразвуковых колебаний
 СВОЙСТВА АЭРОЗОЛЕЙ Интенсивное броуновское движение; Высокое светорассеивание; Выраженная агрегативная неустойчивость; СПЕЦИФИЧЕСКИЕ СВОЙСТВА Термофорез; Фотофорез; Термопреципитация.
СВОЙСТВА АЭРОЗОЛЕЙ Интенсивное броуновское движение; Высокое светорассеивание; Выраженная агрегативная неустойчивость; СПЕЦИФИЧЕСКИЕ СВОЙСТВА Термофорез; Фотофорез; Термопреципитация.
 Вопрос n Коллоидные поверхностно-активные вещества: мыла, детергенты, таниды. Мицеллообразование в растворах коллоидных ПАВ. Критическая концентрация мицеллообразования и ее определение. Солюбилизация и ее значение в фармации. Коллоидные ПАВ в фармации
Вопрос n Коллоидные поверхностно-активные вещества: мыла, детергенты, таниды. Мицеллообразование в растворах коллоидных ПАВ. Критическая концентрация мицеллообразования и ее определение. Солюбилизация и ее значение в фармации. Коллоидные ПАВ в фармации
 Коллоидные ПАВ водные растворы: n мыл n красителей n таннидов (растительных дубильных веществ) n алкалоидов Неполярная часть Полярная часть
Коллоидные ПАВ водные растворы: n мыл n красителей n таннидов (растительных дубильных веществ) n алкалоидов Неполярная часть Полярная часть
 Мицеллообразование в растворах коллоидных ПАВ n n Происходит по схеме: Ист. раствор ↔ Золь ↔ Гель Возможность перехода зависит от: q q концентрации раствора температуры р. Н среды присутствия электролита
Мицеллообразование в растворах коллоидных ПАВ n n Происходит по схеме: Ист. раствор ↔ Золь ↔ Гель Возможность перехода зависит от: q q концентрации раствора температуры р. Н среды присутствия электролита
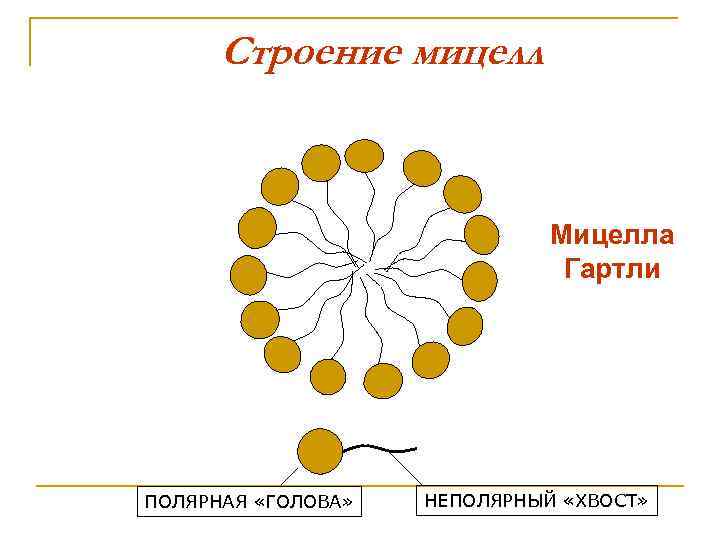 Строение мицелл Мицелла Гартли ПОЛЯРНАЯ «ГОЛОВА» НЕПОЛЯРНЫЙ «ХВОСТ»
Строение мицелл Мицелла Гартли ПОЛЯРНАЯ «ГОЛОВА» НЕПОЛЯРНЫЙ «ХВОСТ»
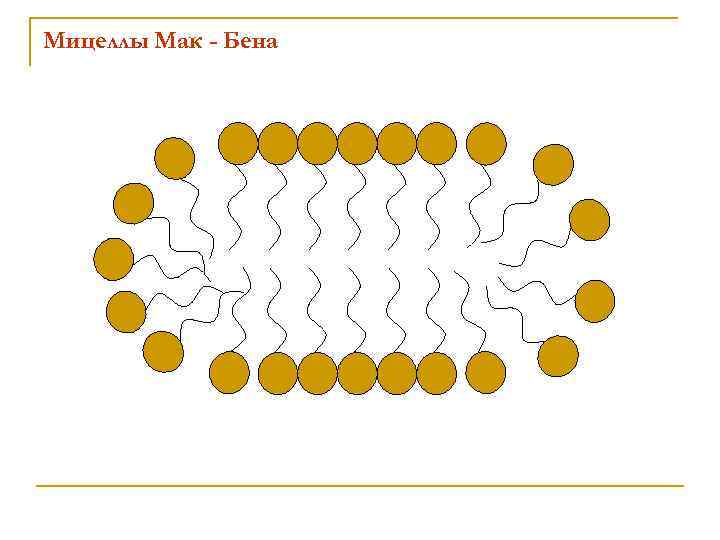 Мицеллы Мак - Бена
Мицеллы Мак - Бена
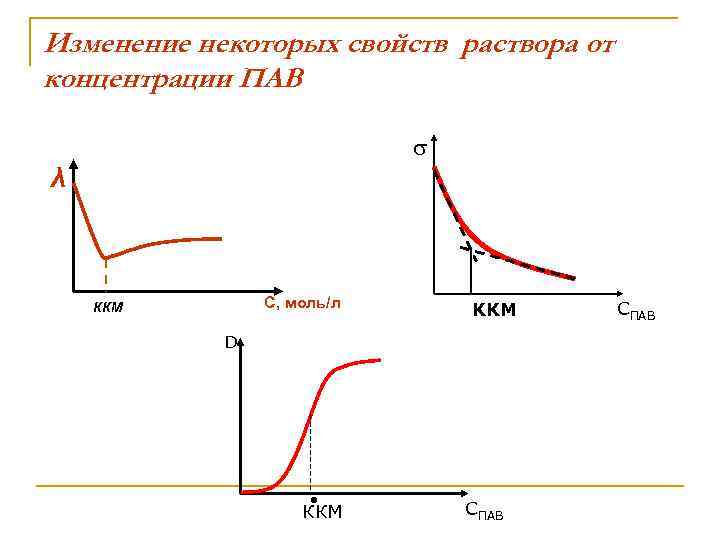 Изменение некоторых свойств раствора от концентрации ПАВ λ C, моль/л ККМ KKM D ККМ СПАВ CПАВ
Изменение некоторых свойств раствора от концентрации ПАВ λ C, моль/л ККМ KKM D ККМ СПАВ CПАВ
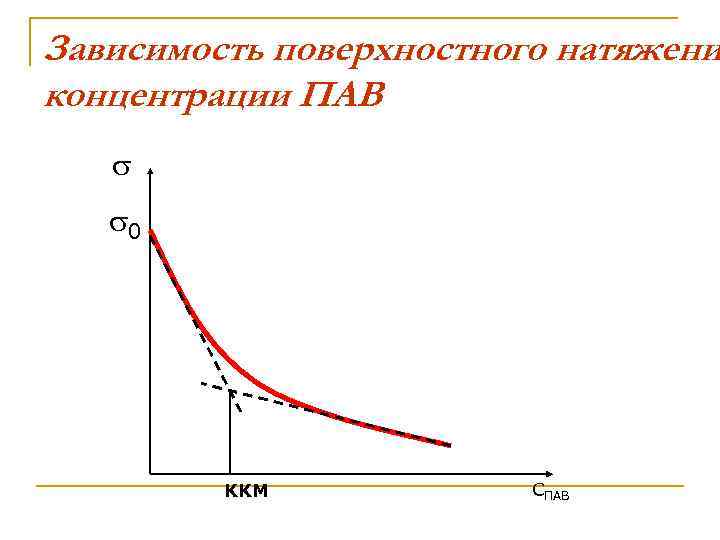 Зависимость поверхностного натяжени концентрации ПАВ 0 KKM CПАВ
Зависимость поверхностного натяжени концентрации ПАВ 0 KKM CПАВ
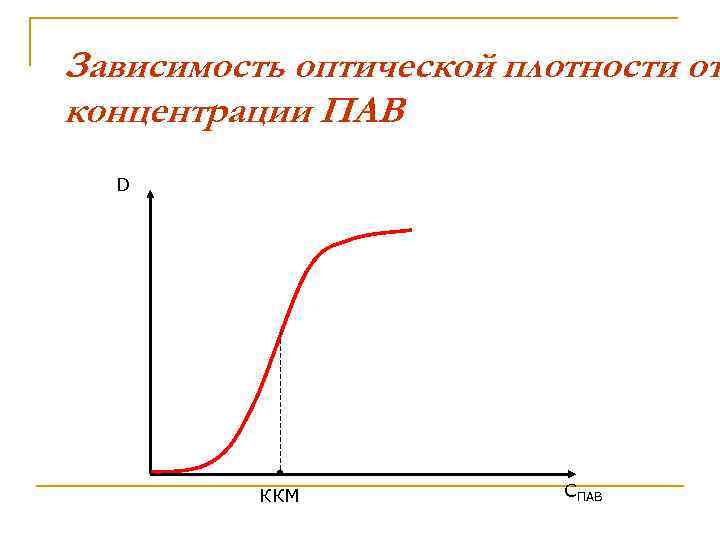 Зависимость оптической плотности от концентрации ПАВ D ККМ СПАВ
Зависимость оптической плотности от концентрации ПАВ D ККМ СПАВ
 Вопрос n Методы получения ВМВ. Классификация ВМВ. Гибкость цепи полимеров. Кристаллическое и аморфное состояние ВМВ.
Вопрос n Методы получения ВМВ. Классификация ВМВ. Гибкость цепи полимеров. Кристаллическое и аморфное состояние ВМВ.
 Классификация ВМВ (по структуре цепей) Линейные -А–А–А–Аn Разветвлённые n -А–А–А–АХ У § Пространственные (Сетчатые) -А–А–А–А-
Классификация ВМВ (по структуре цепей) Линейные -А–А–А–Аn Разветвлённые n -А–А–А–АХ У § Пространственные (Сетчатые) -А–А–А–А-
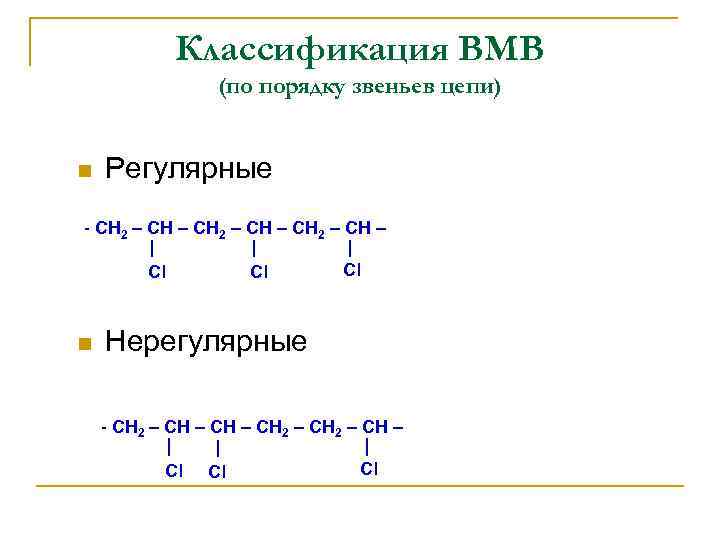 Классификация ВМВ (по порядку звеньев цепи) n Регулярные - СН 2 – СН – Сl n Сl Сl Нерегулярные - СН 2 – СН – Сl Сl Сl
Классификация ВМВ (по порядку звеньев цепи) n Регулярные - СН 2 – СН – Сl n Сl Сl Нерегулярные - СН 2 – СН – Сl Сl Сl
 Классификация ВМВ (по положению боковых радикалов) n Изотактические n Синдиотактические n Атактические
Классификация ВМВ (по положению боковых радикалов) n Изотактические n Синдиотактические n Атактические
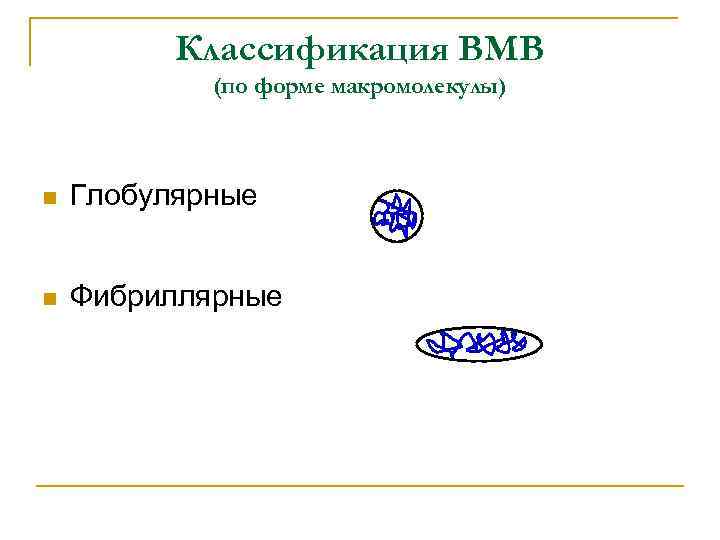 Классификация ВМВ (по форме макромолекулы) n Глобулярные n Фибриллярные
Классификация ВМВ (по форме макромолекулы) n Глобулярные n Фибриллярные
 ВМВ органические 1. Карбоцепные 2. Гетероцепные 3. Элементорганические неорганические
ВМВ органические 1. Карбоцепные 2. Гетероцепные 3. Элементорганические неорганические
 Примеры карбоцепных органических ВМВ Предельные полимеры Ненасыщенные полимеры … — СН 2 —n. . . … —СН 2 — СН = СН — СН 2 — … n полибутадиен Полимерные спирты и их … — СН 2 — … OН n производные Галогензамещенные полимеры Полимеры карбоновых кислот Полимеры с ароматическими заместителями полиэтилен поливиниловый спирт (ПВС) … — СН 2 — … поливинилхлорид спирт (ПВХ) Cl n … — СН 2 — … COOН n … — СН 2 — … С 6 Н 5 n полиакриловая кислота (ПАК) Полистирол (ПС, PS)
Примеры карбоцепных органических ВМВ Предельные полимеры Ненасыщенные полимеры … — СН 2 —n. . . … —СН 2 — СН = СН — СН 2 — … n полибутадиен Полимерные спирты и их … — СН 2 — … OН n производные Галогензамещенные полимеры Полимеры карбоновых кислот Полимеры с ароматическими заместителями полиэтилен поливиниловый спирт (ПВС) … — СН 2 — … поливинилхлорид спирт (ПВХ) Cl n … — СН 2 — … COOН n … — СН 2 — … С 6 Н 5 n полиакриловая кислота (ПАК) Полистирол (ПС, PS)
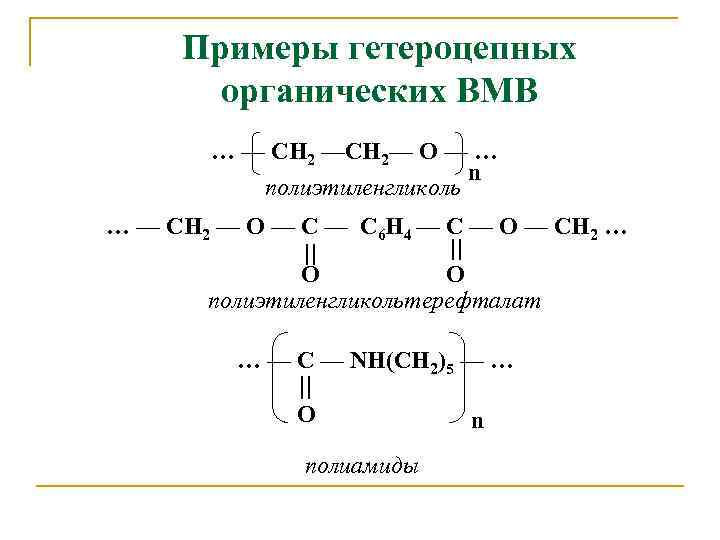 Примеры гетероцепных органических ВМВ … — СН 2 —СН 2— О — … n полиэтиленгликоль = = … — СН 2 — О — С 6 Н 4 — С — О — СН 2 … О О полиэтиленгликольтерефталат = … — С — NH(CH 2)5 — … О полиамиды n
Примеры гетероцепных органических ВМВ … — СН 2 —СН 2— О — … n полиэтиленгликоль = = … — СН 2 — О — С 6 Н 4 — С — О — СН 2 … О О полиэтиленгликольтерефталат = … — С — NH(CH 2)5 — … О полиамиды n
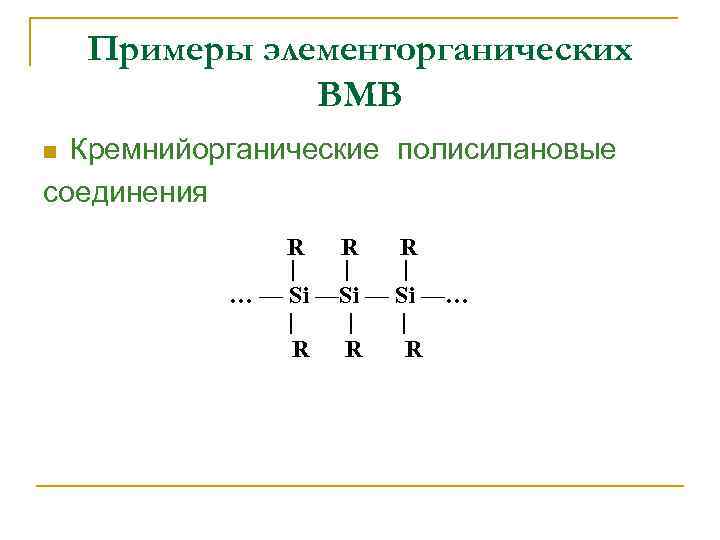 Примеры элементорганических ВМВ Кремнийорганические полисилановые соединения n R R R | | | … — Si —… | R | | R R
Примеры элементорганических ВМВ Кремнийорганические полисилановые соединения n R R R | | | … — Si —… | R | | R R
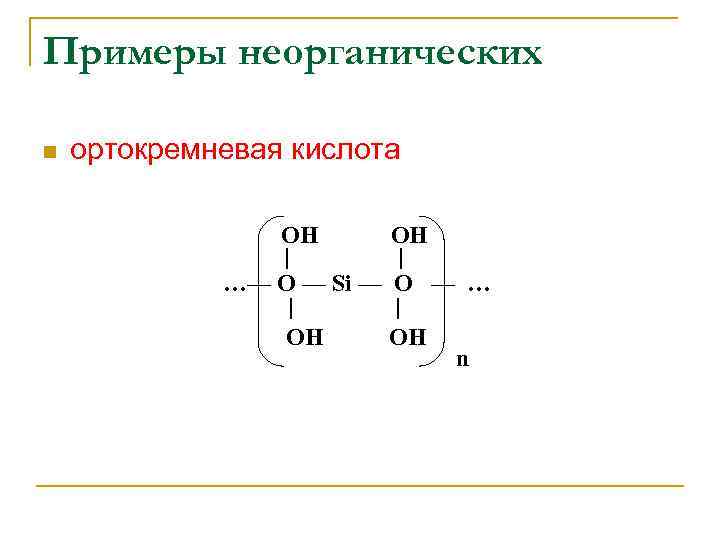 Примеры неорганических ортокремневая кислота ОН ОН | | …— О — Si — О — … | ОН | n ОН n
Примеры неорганических ортокремневая кислота ОН ОН | | …— О — Si — О — … | ОН | n ОН n
 Классификация ВМВ (по гибкости макромолекулярной цепи) n Жесткоцепные n Гибкоцепные
Классификация ВМВ (по гибкости макромолекулярной цепи) n Жесткоцепные n Гибкоцепные
 Классификация ВМВ (по значению дипольного момента) n Полярные (поливиниловый спирт, целлюлоза, крахмал, полиакрилаты); n Неполярные (полиэтилен, каучук, полистирол)
Классификация ВМВ (по значению дипольного момента) n Полярные (поливиниловый спирт, целлюлоза, крахмал, полиакрилаты); n Неполярные (полиэтилен, каучук, полистирол)
 Классификация ВМВ (по происхождению) n Природного (белки, полисахариды, нуклеиновые кислоты); n Синтетического (полиэтилен, полипропилен) n Полусинтетического (резина, метицеллюлоза)
Классификация ВМВ (по происхождению) n Природного (белки, полисахариды, нуклеиновые кислоты); n Синтетического (полиэтилен, полипропилен) n Полусинтетического (резина, метицеллюлоза)
 Классификация полимеров медицинского назначения n Полимеры для введения в организм; n Полимеры, контактирующие с тканями и органами; n Полимеры, не предназначенные для введения в организм и не контактирующие с органами и тканями.
Классификация полимеров медицинского назначения n Полимеры для введения в организм; n Полимеры, контактирующие с тканями и органами; n Полимеры, не предназначенные для введения в организм и не контактирующие с органами и тканями.
 Методы получения ВМВ: 1. Реакции полимеризации; 2. Реакции поликонденсации; 3. Полимераналогичные превращения
Методы получения ВМВ: 1. Реакции полимеризации; 2. Реакции поликонденсации; 3. Полимераналогичные превращения
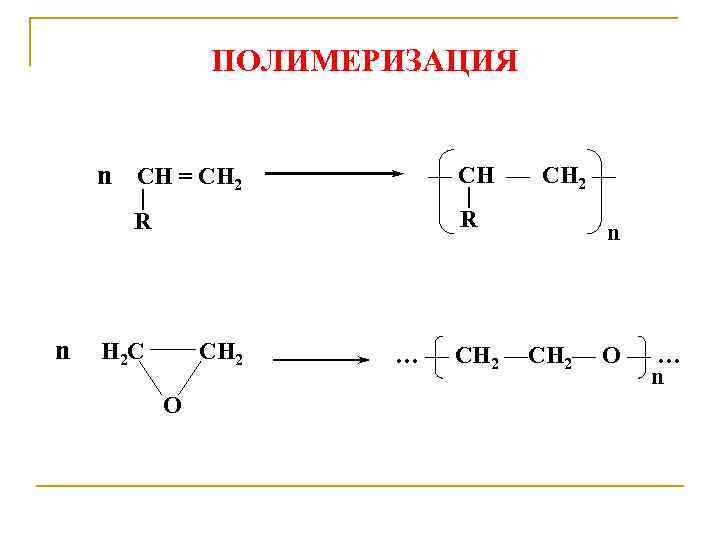 ПОЛИМЕРИЗАЦИЯ n CH = CH 2 | R n Н 2 С СН 2 O — CH 2 — | R n … — СН 2 —СН 2— О — … n
ПОЛИМЕРИЗАЦИЯ n CH = CH 2 | R n Н 2 С СН 2 O — CH 2 — | R n … — СН 2 —СН 2— О — … n
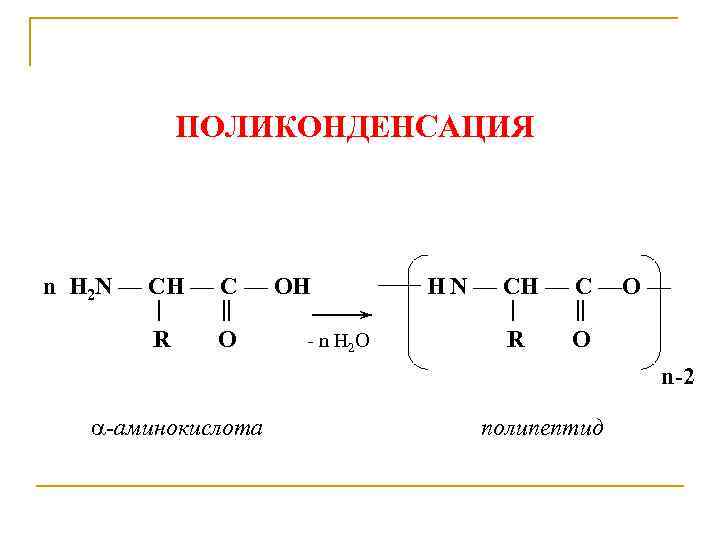 ПОЛИКОНДЕНСАЦИЯ n H 2 N — CH — C — OH | || R O - n H 2 O H N — CH — C —O — | || R O n-2 -аминокислота полипептид
ПОЛИКОНДЕНСАЦИЯ n H 2 N — CH — C — OH | || R O - n H 2 O H N — CH — C —O — | || R O n-2 -аминокислота полипептид
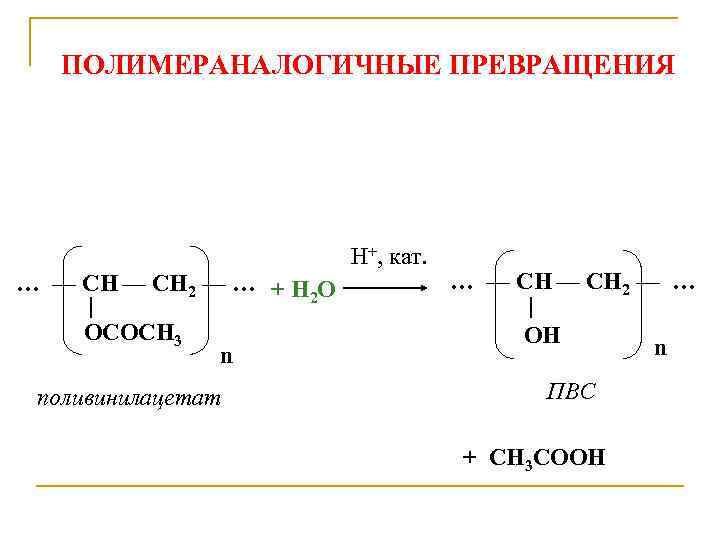 ПОЛИМЕРАНАЛОГИЧНЫЕ ПРЕВРАЩЕНИЯ Н+, кат. … — СН 2 — … + Н 2 О | OCOCH 3 n поливинилацетат … — СН 2 — … | OН n ПВС + CH 3 COOH
ПОЛИМЕРАНАЛОГИЧНЫЕ ПРЕВРАЩЕНИЯ Н+, кат. … — СН 2 — … + Н 2 О | OCOCH 3 n поливинилацетат … — СН 2 — … | OН n ПВС + CH 3 COOH
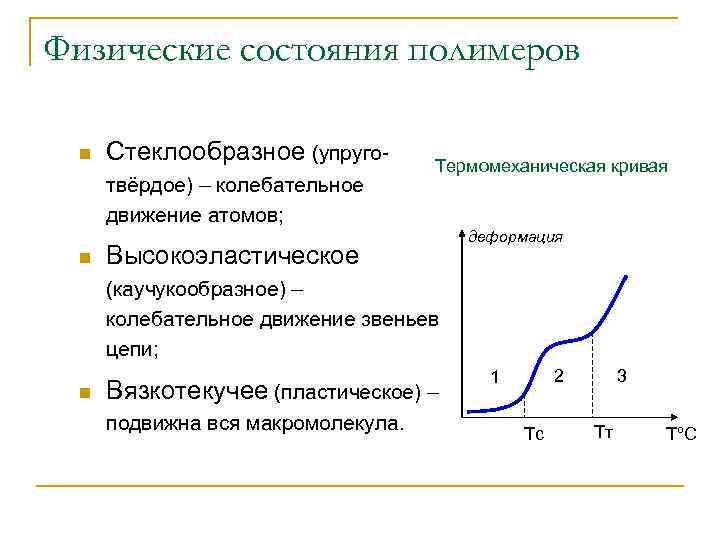 Физические состояния полимеров n Стеклообразное (упруготвёрдое) – колебательное движение атомов; n Термомеханическая кривая Высокоэластическое деформация (каучукообразное) – колебательное движение звеньев цепи; n Вязкотекучее (пластическое) – подвижна вся макромолекула. 2 1 Тс 3 Тт ТºС
Физические состояния полимеров n Стеклообразное (упруготвёрдое) – колебательное движение атомов; n Термомеханическая кривая Высокоэластическое деформация (каучукообразное) – колебательное движение звеньев цепи; n Вязкотекучее (пластическое) – подвижна вся макромолекула. 2 1 Тс 3 Тт ТºС
 Вопрос n Полимерные неэлектролиты и полиэлектролиты. Полиамфолиты. Изоионная точка полиамфолитов и методы ее определения
Вопрос n Полимерные неэлектролиты и полиэлектролиты. Полиамфолиты. Изоионная точка полиамфолитов и методы ее определения
 Полиэлектролиты ВМВ имеющие в своём составе ионогенные группы: • Кислотного типа содержат группы -СОО (крахмал), -SO 3 O (агар-агар); • Основного типа содержат –NH+3 • Полиамфолиты – белки (группы -СОО , – NH+3).
Полиэлектролиты ВМВ имеющие в своём составе ионогенные группы: • Кислотного типа содержат группы -СОО (крахмал), -SO 3 O (агар-агар); • Основного типа содержат –NH+3 • Полиамфолиты – белки (группы -СОО , – NH+3).
 Изоэлектрическая точка полиэлектролитов Значение р. Н при котором число отрицательных и положительных зарядов макромолекулы ВМВ одинаково – изоэлектрическая точка (p. I). Схема диссоциации: n + H 3 N – CH – COOH R Заряд «+» р. Н p. I H+ + H 3 N – CH – COO– R Изоэлектрическое состояние Заряд ноль р. Н=p. I OH– - Н 2 О H 2 N – CH – COO– R Заряд « » р. Н>p. I
Изоэлектрическая точка полиэлектролитов Значение р. Н при котором число отрицательных и положительных зарядов макромолекулы ВМВ одинаково – изоэлектрическая точка (p. I). Схема диссоциации: n + H 3 N – CH – COOH R Заряд «+» р. Н p. I H+ + H 3 N – CH – COO– R Изоэлектрическое состояние Заряд ноль р. Н=p. I OH– - Н 2 О H 2 N – CH – COO– R Заряд « » р. Н>p. I
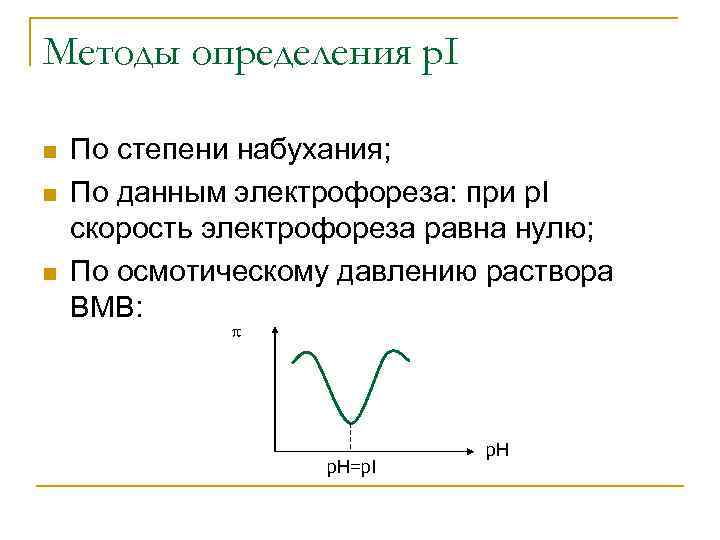 Методы определения р. I n n n По степени набухания; По данным электрофореза: при p. I скорость электрофореза равна нулю; По осмотическому давлению раствора ВМВ: р. Н=p. I р. Н
Методы определения р. I n n n По степени набухания; По данным электрофореза: при p. I скорость электрофореза равна нулю; По осмотическому давлению раствора ВМВ: р. Н=p. I р. Н
 Вопрос n Осмотические свойства ВМВ. Осмотическое давление растворов полимерных неэлектролитов. Отклонение от закона Вант-Гоффа. Уравнение Галлера
Вопрос n Осмотические свойства ВМВ. Осмотическое давление растворов полимерных неэлектролитов. Отклонение от закона Вант-Гоффа. Уравнение Галлера
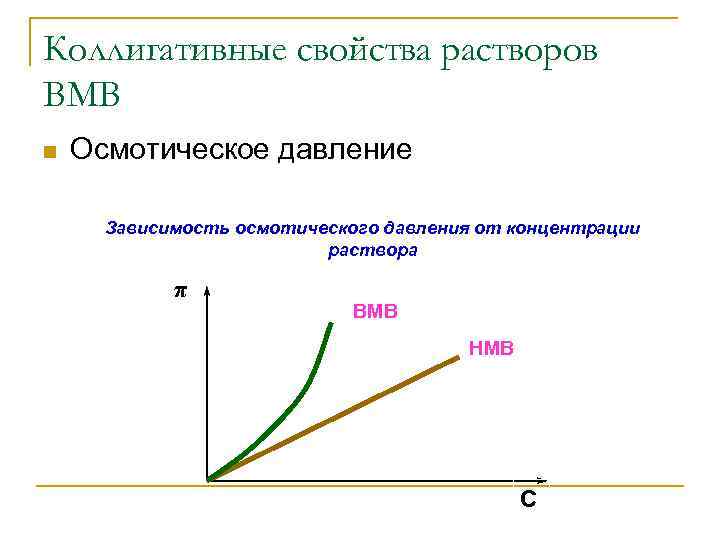 Коллигативные свойства растворов ВМВ n Осмотическое давление Зависимость осмотического давления от концентрации раствора π ВМВ НМВ C
Коллигативные свойства растворов ВМВ n Осмотическое давление Зависимость осмотического давления от концентрации раствора π ВМВ НМВ C
 Уравнение Галлера - осмотическое давление; М – молярная масса ВМВ; С – концентрация раствора, г/л; - коэффициент, учитывающий гибкость и форму макромолекулы ВМВ
Уравнение Галлера - осмотическое давление; М – молярная масса ВМВ; С – концентрация раствора, г/л; - коэффициент, учитывающий гибкость и форму макромолекулы ВМВ
 Вопрос n Методы измерения вязкости растворов ВМВ. Относительная, удельная и характеристическая вязкость. Уравнение Штаудингера и Марка-Куна-Хаувинка. Определение молекулярной массы полимера вискозиметрическим методом
Вопрос n Методы измерения вязкости растворов ВМВ. Относительная, удельная и характеристическая вязкость. Уравнение Штаудингера и Марка-Куна-Хаувинка. Определение молекулярной массы полимера вискозиметрическим методом
 Вязкость – это сила сопротивления (трения) между слоями жидкости при площади соприкасающихся слоёв равной единице и градиенте скорости течения между слоями равном единице
Вязкость – это сила сопротивления (трения) между слоями жидкости при площади соприкасающихся слоёв равной единице и градиенте скорости течения между слоями равном единице
 Уравнение Марка – Куна - Хаувинка Используется для определения молекулярной массы полимера: К и α – постоянные для данного гомологического ряда и растворителя
Уравнение Марка – Куна - Хаувинка Используется для определения молекулярной массы полимера: К и α – постоянные для данного гомологического ряда и растворителя
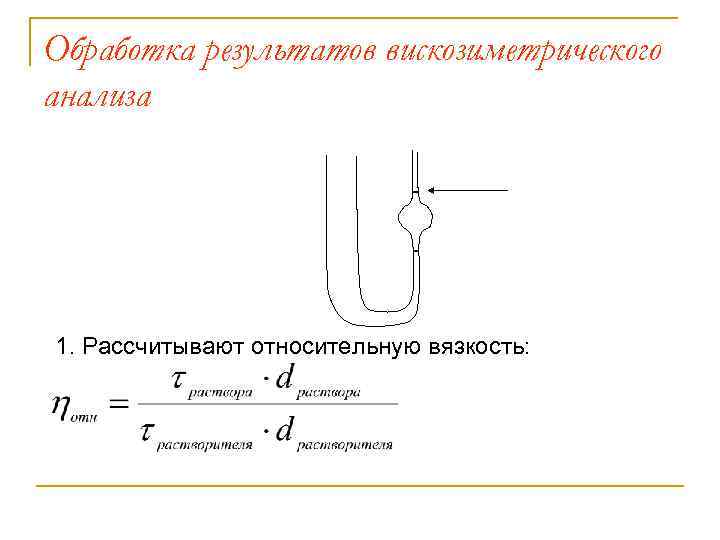 Обработка результатов вискозиметрического анализа 1. Рассчитывают относительную вязкость:
Обработка результатов вискозиметрического анализа 1. Рассчитывают относительную вязкость:
 2. Определяют удельную вязкость: 3. Находят приведённую вязкость:
2. Определяют удельную вязкость: 3. Находят приведённую вязкость:
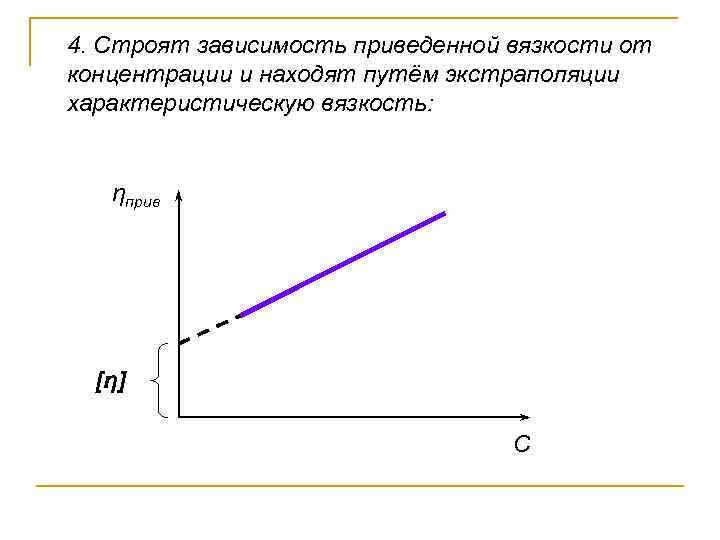 4. Строят зависимость приведенной вязкости от концентрации и находят путём экстраполяции характеристическую вязкость: ηприв [η] С
4. Строят зависимость приведенной вязкости от концентрации и находят путём экстраполяции характеристическую вязкость: ηприв [η] С
 Для расчетов молекулярной массы применяют логарифмическое уравнение: Откуда молекулярная масса полимера:
Для расчетов молекулярной массы применяют логарифмическое уравнение: Откуда молекулярная масса полимера:
 Вопрос n Факторы устойчивости растворов ВМВ. Высаливание, пороги высаливания. Лиотропные ряды ионов. Зависимость порогов высаливания полиамфолитов от р. Н среды
Вопрос n Факторы устойчивости растворов ВМВ. Высаливание, пороги высаливания. Лиотропные ряды ионов. Зависимость порогов высаливания полиамфолитов от р. Н среды
 Устойчивость растворов ВМВ и её нарушение Высаживание – добавление к к раствору ВМВ «плохого» растворителя (водный раствор белка+ацетон и т. д. ). n Высаливание – добавление электролита: катионы Li+ >Na+ > K+ > Rb+ > Cs+ > Mg+2 > Ca+2 > Sr+2 > Ba+2 анионы SO 42–> F– > CH 3 COO– > Cl– > NO 3– > Br– > I– > CNS– n Изменение р. Н. Коацервация! n Изменение температуры. n
Устойчивость растворов ВМВ и её нарушение Высаживание – добавление к к раствору ВМВ «плохого» растворителя (водный раствор белка+ацетон и т. д. ). n Высаливание – добавление электролита: катионы Li+ >Na+ > K+ > Rb+ > Cs+ > Mg+2 > Ca+2 > Sr+2 > Ba+2 анионы SO 42–> F– > CH 3 COO– > Cl– > NO 3– > Br– > I– > CNS– n Изменение р. Н. Коацервация! n Изменение температуры. n


