Коллоидная_химия_заочн_хим тех.ppt
- Количество слайдов: 19

Коллоидная химия 1) Контрольная работа 2) Лабораторные занятия 3) зачет Методические указания к контрольным работам



Дисперсные системы обладают двумя характерными признаками: 1) гетерогенность, т. е. между дисперсной средой и дисперсной фазой имеется поверхность раздела; 2) высокая раздробленность или дисперсность (D). Дисперсность − величина, обратная размерам частиц а: D=1/a. Чем меньше размеры частиц, тем больше дисперсность. Раздробленность приводит к увеличению поверхности раздела фаз, что придает дисперсным системам особые для них свойства.

По степени дисперсности они подразделяются на четыре типа: • Грубодисперсные – грубые взвеси, суспензии, эмульсии, порошки с размером частиц ≥ 10 -5 м; • Микрогетерогенные (тонкие взвеси, дымы, пористые тела) 10 -5 – 10 -7 м; • Коллоидно-дисперсные (золи) - с размером частиц 10 -7 – 10 -9 м; Молекулярные или ионные растворы с размером частиц менее 10 -9 м •

Классификация по агрегатному состоянию

Дисперсные системы по межфазному взаимодействию среды и фаз делятся на: лиофобные и лиофильные В лиофобных системах дисперсная фаза слабо взаимодействует с дисперсной средой (суспензии, эмульсии (например, растительное масло с водой); в лиофильных системах − интенсивно (растворы полимеров, поверхностно-активных веществ). Частицы дисперсной фазы, структурно связанные в дисперсной системе, образуют гели, а несвязанные − золи.



m Ag. NO 3 + (m+n) KJ → m. Ag. J∙n. J- + m. KNO 3
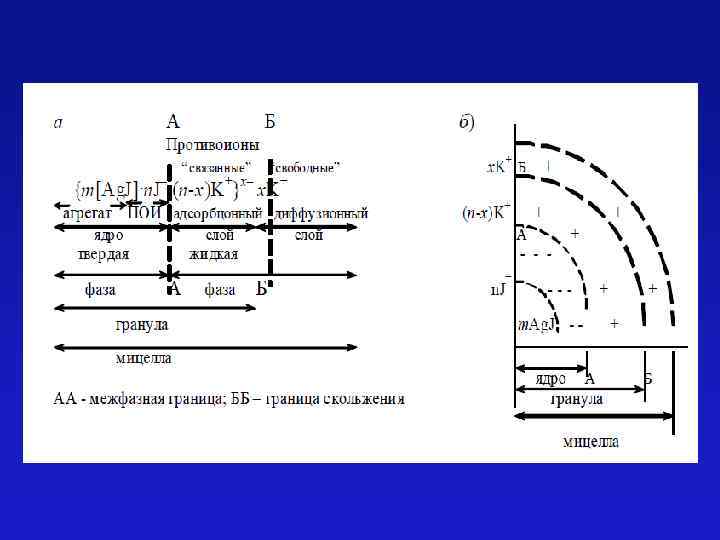

Если получают золь иодистого серебра при некотором избытке нитрата серебра (Ag. NO 3), то частицы золя йодистого серебра приобретают положительный заряд: {m[Ag. J] n. Ag+(n-x)NO 3¯}x+ Знак заряда коллоидных частиц золей определяют методами электрофореза и капилляризации.

ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ Коллоидные системы являются высокодисперсными системами и отличаются от других гетерогенных систем наличием сильно развитой поверхности раздела фаз. Основные и наиболее характерные свойства коллоидных систем определяются особым состоянием вещества в поверхностных слоях на границах раздела фаз по сравнению со всем объемом вещества.

молекулы на межфазной поверхности. Если взять молекулу, например, на поверхности жидкости, то у нее не все силы молекулярного сцепления будут скомпенсированы. Такая молекула испытывает притяжение только со стороны молекул жидкости. Это притяжение ничем не компенсируется со стороны газообразной фазы, т. е. часть силового поля этих молекул является не насыщенной.

Это обуславливает внутреннее (или молекулярное) давление в телах. Таким образом, возникает поверхностное натяжение σ, стремящееся сократить поверхность. Свободная поверхностная энергия FS выражается уравнением: FS = σ S где S – площадь поверхности; σ – свободная энергия единицы поверхности, или удельная свободная поверхностная энергия.

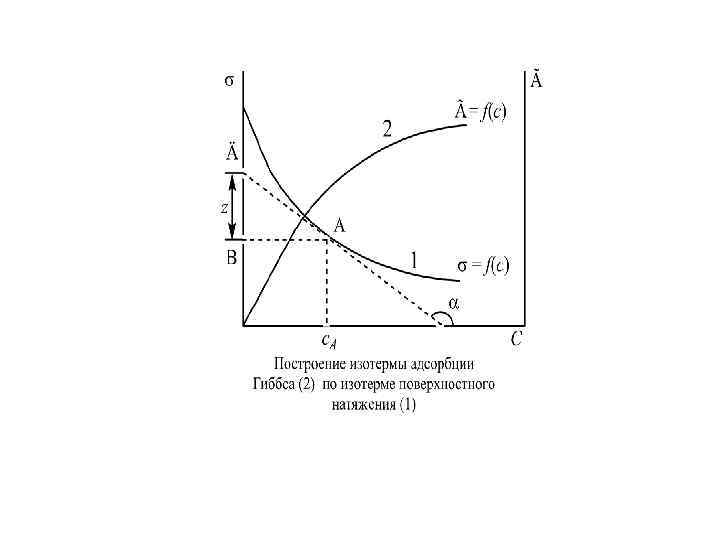
Явления, связанные с особенностями поверхности раздела, называются поверхностными. Уменьшение поверхностного натяжения часто происходит в результате самопроизвольного концентрирования в поверхностном слое веществ с меньшим поверхностным натяжением – адсорбции. Величину адсорбции обычно выражают двумя способами. Согласно одному способу ее определяют как количество вещества в поверхностном слое А, приходящееся на единицу площади или массы адсорбента (абсолютная величина адсорбции)

По другому способу величину адсорбции Г определяют как избыток компонента в поверхностном слое (на единицу площади поверхности) по сравнению с его количеством в равном объеме объемной фазы (избыточная адсорбция) Адсорбция происходит на границах раздела различных фаз и зависит от условий (температуры, давления газа, концентрации раствора, природы адсорбента и адсорбтива и др. ).
Коллоидная_химия_заочн_хим тех.ppt