лекция 5 Кол сост почв 3.ppt
- Количество слайдов: 81
 Коллоидная составляющая почв -3 На предыдущей лекции мы начали рассматривать основы коллоидной химии и примеры коллоидно-химических явлений в почвоведении. Вспомнили узнали, что причиной особых свойств, возникающих в коллоидных системах, является избыточная поверхностная энергия. Остановились на классификации коллоидных систем по агрегатному состоянию, явлениях смачивания и способах уменьшения избыточной поверхностной энергии коллоидными системами. Рассмотрели механизмы возникновения зарядов на коллоидных частицах и образование двойного электрического слоя.
Коллоидная составляющая почв -3 На предыдущей лекции мы начали рассматривать основы коллоидной химии и примеры коллоидно-химических явлений в почвоведении. Вспомнили узнали, что причиной особых свойств, возникающих в коллоидных системах, является избыточная поверхностная энергия. Остановились на классификации коллоидных систем по агрегатному состоянию, явлениях смачивания и способах уменьшения избыточной поверхностной энергии коллоидными системами. Рассмотрели механизмы возникновения зарядов на коллоидных частицах и образование двойного электрического слоя.
 Приведенные примеры показывают, что приложение законов, выведенных для идеальных систем к реальным системам, не является простой задачей. Необходимо учитывать сложность формы частиц и образующихся из них капилляров, шероховатость поверхности, ее неоднородность (мозаичность) в плане гидрофильно-гидрофобных свойств, а также изменение свойств поверхностей и контактирующих с ними жидкостей во времени при взаимодействии твердых частиц с водой. Отметим, что мы рассматривали термодинамически равновесные или близкие к равновесным процессы. В реальности на все перечисленные выше сложности накладывается кинетика – соотношение скоростей прохождения различных процессов. Это было хорошо видно из влияния вязкости почвенного раствора на усилие, необходимое при вспашке почвы.
Приведенные примеры показывают, что приложение законов, выведенных для идеальных систем к реальным системам, не является простой задачей. Необходимо учитывать сложность формы частиц и образующихся из них капилляров, шероховатость поверхности, ее неоднородность (мозаичность) в плане гидрофильно-гидрофобных свойств, а также изменение свойств поверхностей и контактирующих с ними жидкостей во времени при взаимодействии твердых частиц с водой. Отметим, что мы рассматривали термодинамически равновесные или близкие к равновесным процессы. В реальности на все перечисленные выше сложности накладывается кинетика – соотношение скоростей прохождения различных процессов. Это было хорошо видно из влияния вязкости почвенного раствора на усилие, необходимое при вспашке почвы.
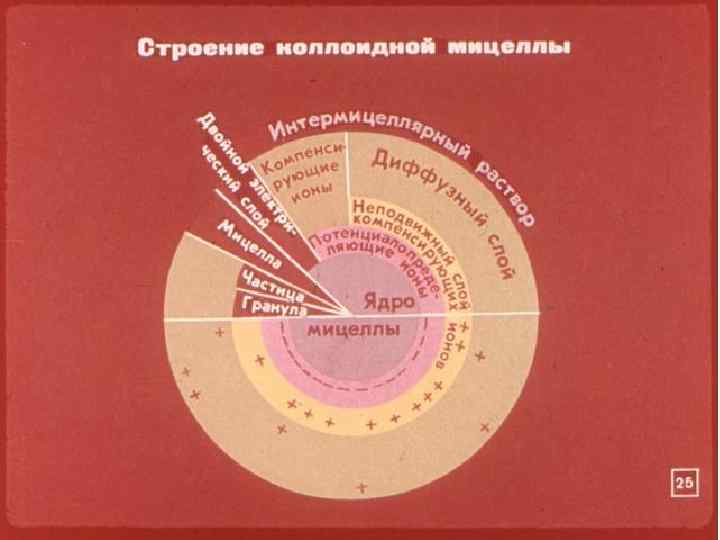
 Вспомним еще раз механизм возникновения ДЭС. Стремление к уменьшению избыточной поверхностной энергии приводит к возникновению заряда на поверхности коллоидных частиц путем диссоциации или адсорбции потенциалопределяющих ионов, прочно связанных с поверхностью коллоидных частиц. Вокруг заряженной частицы возникает слой противоионов, состоящий из двух подслоев. Подслоя противоионов адсорбированных на частице и подслоя противоионов, находящихся в растворе, примыкающем к коллоидной частице. Этот диффузный подслой размыт из-за теплового движения молекул и концентрация противоионов в нем экспоненциально падает от поверхности коллоидной частицы. При движении частиц или раствора относительно твердой поверхности плоскость скольжения располагается, как правило, в диффузном подслое.
Вспомним еще раз механизм возникновения ДЭС. Стремление к уменьшению избыточной поверхностной энергии приводит к возникновению заряда на поверхности коллоидных частиц путем диссоциации или адсорбции потенциалопределяющих ионов, прочно связанных с поверхностью коллоидных частиц. Вокруг заряженной частицы возникает слой противоионов, состоящий из двух подслоев. Подслоя противоионов адсорбированных на частице и подслоя противоионов, находящихся в растворе, примыкающем к коллоидной частице. Этот диффузный подслой размыт из-за теплового движения молекул и концентрация противоионов в нем экспоненциально падает от поверхности коллоидной частицы. При движении частиц или раствора относительно твердой поверхности плоскость скольжения располагается, как правило, в диффузном подслое.
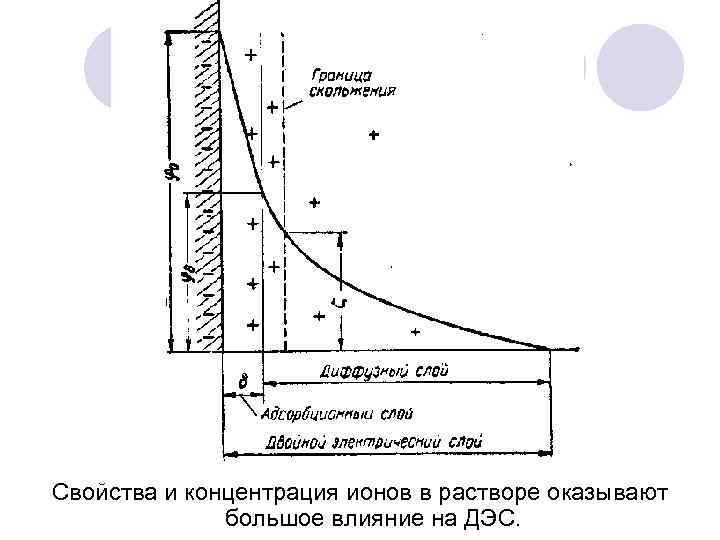 Свойства и концентрация ионов в растворе оказывают большое влияние на ДЭС.
Свойства и концентрация ионов в растворе оказывают большое влияние на ДЭС.
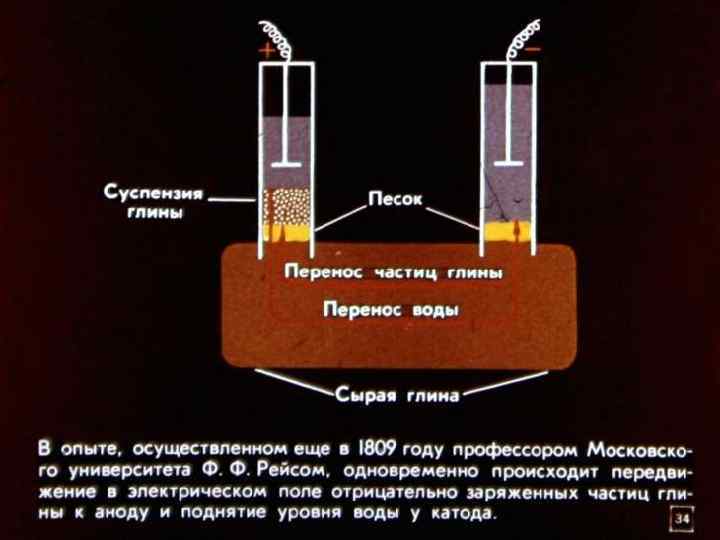
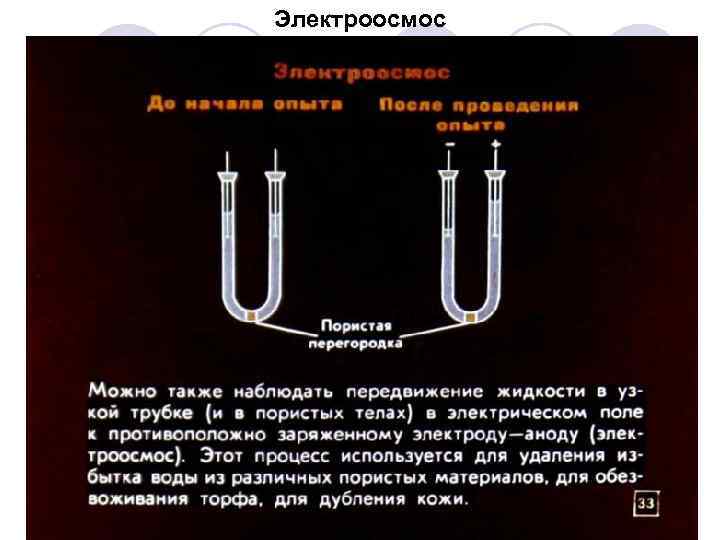
 Наличие электрического потенциала на границе скольжения между твердой поверхностью и жидкостью при их взаимном перемещении приводит к возникновению электрокинетических явлений. Электроосмос и электрофорез были открыты Ф. Ф. Рейссом в 1809, который наблюдал вызванное внешним электрическим полем перемещение жидкости в U-образной трубке, перегороженной в нижней части мембраной из кварцевого песка, и движение глинистых частиц в покоящейся жидкости при наложении электрического поля.
Наличие электрического потенциала на границе скольжения между твердой поверхностью и жидкостью при их взаимном перемещении приводит к возникновению электрокинетических явлений. Электроосмос и электрофорез были открыты Ф. Ф. Рейссом в 1809, который наблюдал вызванное внешним электрическим полем перемещение жидкости в U-образной трубке, перегороженной в нижней части мембраной из кварцевого песка, и движение глинистых частиц в покоящейся жидкости при наложении электрического поля.
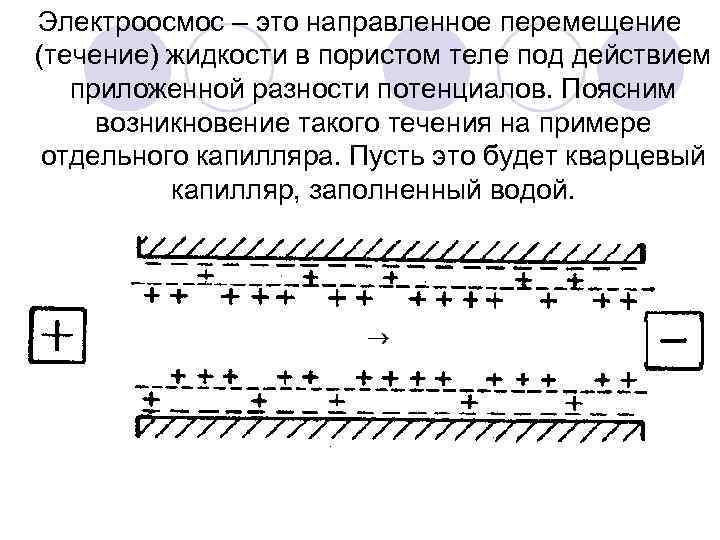 Электроосмос – это направленное перемещение (течение) жидкости в пористом теле под действием приложенной разности потенциалов. Поясним возникновение такого течения на примере отдельного капилляра. Пусть это будет кварцевый капилляр, заполненный водой.
Электроосмос – это направленное перемещение (течение) жидкости в пористом теле под действием приложенной разности потенциалов. Поясним возникновение такого течения на примере отдельного капилляра. Пусть это будет кварцевый капилляр, заполненный водой.
 Твердая фаза заряжена отрицательно, противоионы сообщают жидкости положительный заряд. Капилляр помещен во внешнее электрическое поле, силовые линии которого параллельны поверхности. Противоионы, находящиеся в периферийной части слоя Гуи и слабо связанные с поверхностью электростатическими силами, при наложении внешнего электрического поля начинают перемещаться в направлении действия поля и при этом за счет сил внутреннего трения вовлекают за собой в движение окружающую жидкость. Если диаметр капилляра не слишком велик, то приходит в движение весь цилиндрический столбик жидкости, заполняющей капилляр, за исключением тонкого пристенного слоя за границей скольжения, закрепленного на поверхности адгезионными силами.
Твердая фаза заряжена отрицательно, противоионы сообщают жидкости положительный заряд. Капилляр помещен во внешнее электрическое поле, силовые линии которого параллельны поверхности. Противоионы, находящиеся в периферийной части слоя Гуи и слабо связанные с поверхностью электростатическими силами, при наложении внешнего электрического поля начинают перемещаться в направлении действия поля и при этом за счет сил внутреннего трения вовлекают за собой в движение окружающую жидкость. Если диаметр капилляра не слишком велик, то приходит в движение весь цилиндрический столбик жидкости, заполняющей капилляр, за исключением тонкого пристенного слоя за границей скольжения, закрепленного на поверхности адгезионными силами.
 Электроосмос
Электроосмос
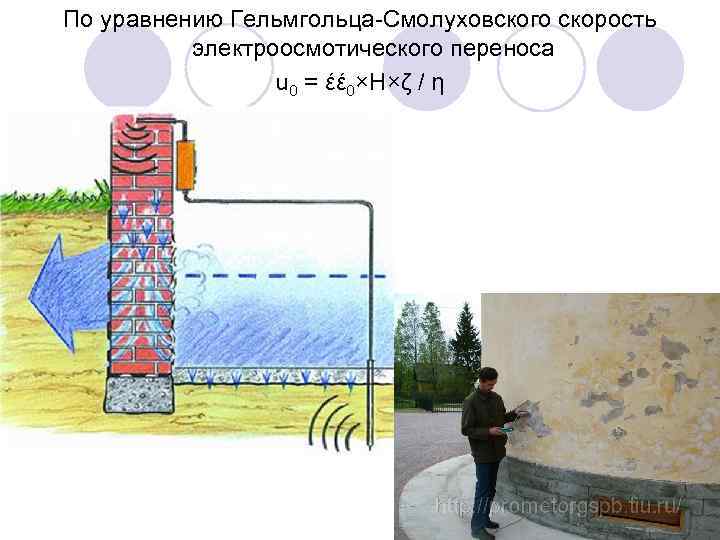 По уравнению Гельмгольца-Смолуховского скорость электроосмотического переноса u 0 = έέ 0×H×ζ / η
По уравнению Гельмгольца-Смолуховского скорость электроосмотического переноса u 0 = έέ 0×H×ζ / η
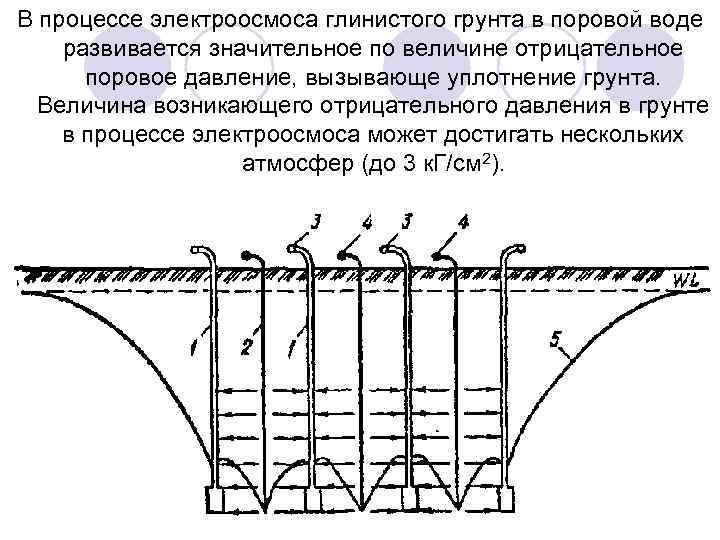 В процессе электроосмоса глинистого грунта в поровой воде развивается значительное по величине отрицательное поровое давление, вызывающе уплотнение грунта. Величина возникающего отрицательного давления в грунте в процессе электроосмоса может достигать нескольких атмосфер (до 3 к. Г/см 2).
В процессе электроосмоса глинистого грунта в поровой воде развивается значительное по величине отрицательное поровое давление, вызывающе уплотнение грунта. Величина возникающего отрицательного давления в грунте в процессе электроосмоса может достигать нескольких атмосфер (до 3 к. Г/см 2).
 Очистка засоленных почв Принцип электромелиорации состоял в ускорении перехода солей из засоленных почв и ионов натрия из солонцов в дрены. Многолетние лабораторные и полевые исследования показали высокий мелиоративный эффект постоянного электрического тока на почвы засоленного ряда – рассоление, рассолонцевание, улучшение физических свойств. Появлялась фильтрация у практически нефильтрующих солонцов. При воздействии на почвы тока намного возрастала эффективность использования химических мелиорантов.
Очистка засоленных почв Принцип электромелиорации состоял в ускорении перехода солей из засоленных почв и ионов натрия из солонцов в дрены. Многолетние лабораторные и полевые исследования показали высокий мелиоративный эффект постоянного электрического тока на почвы засоленного ряда – рассоление, рассолонцевание, улучшение физических свойств. Появлялась фильтрация у практически нефильтрующих солонцов. При воздействии на почвы тока намного возрастала эффективность использования химических мелиорантов.

 Электрофорез – это направленное перемещение частиц дисперсной фазы под действием приложенной разности потенциалов. Это явление можно наблюдать в седиментационно устойчивых дисперсных системах. При наложении на такую систему внешней разности потенциалов происходит разрыв диффузной части ДЭС по плоскости скольжения, в результате чего образуется комплекс дисперсная частица + часть противоионов внешней обкладки ДЭС (куда входят противоионы слоя Штерна и наиболее прочно связанные с поверхностью ионы диффузного слоя). Так как поверхностный заряд частицы в таком случае не полностью скомпенсирован противоионами, такой комплекс несет электрический заряд и во внешнем электрическом поле перемещается к соответствующему электроду.
Электрофорез – это направленное перемещение частиц дисперсной фазы под действием приложенной разности потенциалов. Это явление можно наблюдать в седиментационно устойчивых дисперсных системах. При наложении на такую систему внешней разности потенциалов происходит разрыв диффузной части ДЭС по плоскости скольжения, в результате чего образуется комплекс дисперсная частица + часть противоионов внешней обкладки ДЭС (куда входят противоионы слоя Штерна и наиболее прочно связанные с поверхностью ионы диффузного слоя). Так как поверхностный заряд частицы в таком случае не полностью скомпенсирован противоионами, такой комплекс несет электрический заряд и во внешнем электрическом поле перемещается к соответствующему электроду.
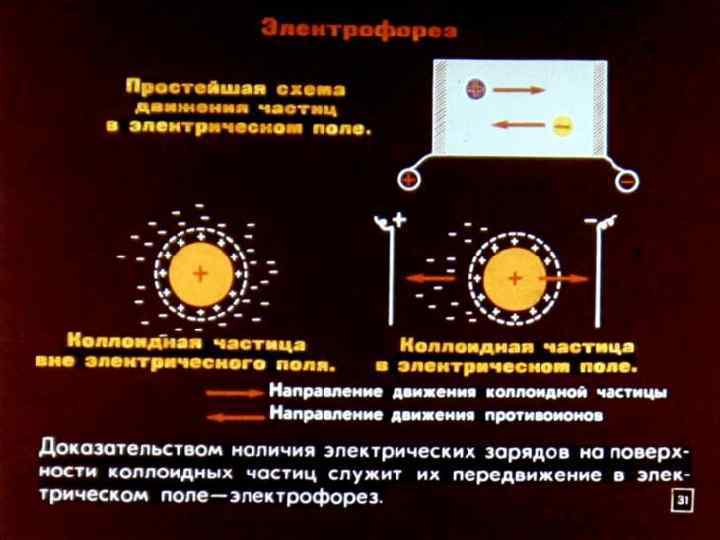
 Выражение для скорости электрофореза в зависимости от параметров системы, как и в случае электроосмоса, базируется на рассмотрении баланса движущих сил процесса – электрической силы и силы трения. Различие состоит лишь в выбранной системе координат. Если в случае электроосмоса рассматривается движение жидкости относительно твердого тела, то при электрофорезе, наоборот, частицы движутся относительно среды. Поэтому для электрофореза справедливо полученное выше уравнение Гельмгольца–Смолуховского: u 0 = έέ 0×H×ζ / η где в данном случае u 0 означает линейную скорость движения частицы относительно дисперсионной среды. Отношение скорости движения частиц к напряженности приложенного электрического поля u/H называют электрофоретической подвижностью.
Выражение для скорости электрофореза в зависимости от параметров системы, как и в случае электроосмоса, базируется на рассмотрении баланса движущих сил процесса – электрической силы и силы трения. Различие состоит лишь в выбранной системе координат. Если в случае электроосмоса рассматривается движение жидкости относительно твердого тела, то при электрофорезе, наоборот, частицы движутся относительно среды. Поэтому для электрофореза справедливо полученное выше уравнение Гельмгольца–Смолуховского: u 0 = έέ 0×H×ζ / η где в данном случае u 0 означает линейную скорость движения частицы относительно дисперсионной среды. Отношение скорости движения частиц к напряженности приложенного электрического поля u/H называют электрофоретической подвижностью.
 Микрофотографии перемещения и вращения частиц дерново -подзолистой почвы в дистиллированной воде в переменном электрическом поле частой 0, 09 Гц
Микрофотографии перемещения и вращения частиц дерново -подзолистой почвы в дистиллированной воде в переменном электрическом поле частой 0, 09 Гц
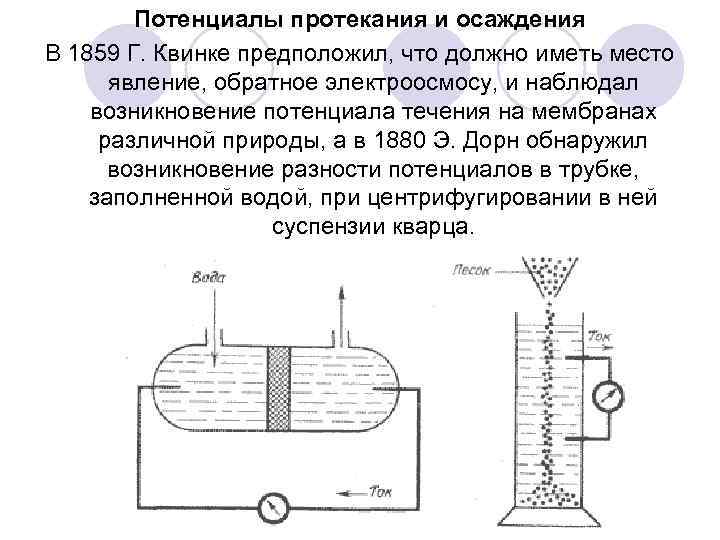 Потенциалы протекания и осаждения В 1859 Г. Квинке предположил, что должно иметь место явление, обратное электроосмосу, и наблюдал возникновение потенциала течения на мембранах различной природы, а в 1880 Э. Дорн обнаружил возникновение разности потенциалов в трубке, заполненной водой, при центрифугировании в ней суспензии кварца.
Потенциалы протекания и осаждения В 1859 Г. Квинке предположил, что должно иметь место явление, обратное электроосмосу, и наблюдал возникновение потенциала течения на мембранах различной природы, а в 1880 Э. Дорн обнаружил возникновение разности потенциалов в трубке, заполненной водой, при центрифугировании в ней суспензии кварца.
 При течении дисперсионной среды через пористую мембрану под действием перепада давления по обе стороны ее появляется разность потенциалов, называемая потенциалом течения (или потенциалом протекания). Это явление, обратное электроосмосу. Движущаяся в капилляре жидкость увлекает за собой противоионы диффузной части ДЭС и становится носителем поверхностного электрического тока (тока течения Is). На концах капилляра вследствие переноса зарядов возникает разность потенциалов, которая вызывает встречный объемный поток ионов противоположного знака по всему объему капилляра (ток утечки Iv). При установлении стационарного состояния потоки ионов становятся равными (Is = Iv), и разность потенциалов на концах капилляра принимает постоянное значение, равное потенциалу течения: Етеч = έέ 0×ΔP×ζ / ηγ
При течении дисперсионной среды через пористую мембрану под действием перепада давления по обе стороны ее появляется разность потенциалов, называемая потенциалом течения (или потенциалом протекания). Это явление, обратное электроосмосу. Движущаяся в капилляре жидкость увлекает за собой противоионы диффузной части ДЭС и становится носителем поверхностного электрического тока (тока течения Is). На концах капилляра вследствие переноса зарядов возникает разность потенциалов, которая вызывает встречный объемный поток ионов противоположного знака по всему объему капилляра (ток утечки Iv). При установлении стационарного состояния потоки ионов становятся равными (Is = Iv), и разность потенциалов на концах капилляра принимает постоянное значение, равное потенциалу течения: Етеч = έέ 0×ΔP×ζ / ηγ
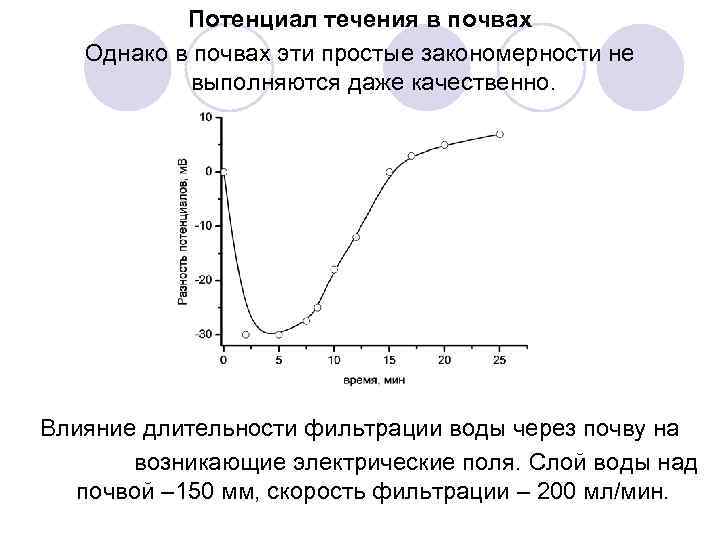 Потенциал течения в почвах Однако в почвах эти простые закономерности не выполняются даже качественно. Влияние длительности фильтрации воды через почву на возникающие электрические поля. Слой воды над почвой – 150 мм, скорость фильтрации – 200 мл/мин.
Потенциал течения в почвах Однако в почвах эти простые закономерности не выполняются даже качественно. Влияние длительности фильтрации воды через почву на возникающие электрические поля. Слой воды над почвой – 150 мм, скорость фильтрации – 200 мл/мин.
 Можно предположить, что это связано с наличием на поверхности частиц гелевого слоя. Для этого нужно рассмотреть распределение солей между гелем и раствором (описание подобной модели впервые было выполнено Доннаном). При этом выясняется, что электролит не распределяется равномерно между дисперсной системой и контактирующим с ней раствором. Если концентрация электролита в растворе намного превышает количество коллоидных частиц, то распределение происходит достаточно равномерно, в дисперсную систему переходит и вода, и электролит. Если же концентрация электролита в растворе мала, то вода из раствора переходит в дисперсную систему, а электролит в нее практически не переходит. Причем анионы входят в отрицательно заряженную коллоидную систему в большей степени по сравнению с катионами. В результате возникает разность потенциалов между гелем и раствором (потенциал Доннана), но она не соответствует тому, что наблюдается в почвах.
Можно предположить, что это связано с наличием на поверхности частиц гелевого слоя. Для этого нужно рассмотреть распределение солей между гелем и раствором (описание подобной модели впервые было выполнено Доннаном). При этом выясняется, что электролит не распределяется равномерно между дисперсной системой и контактирующим с ней раствором. Если концентрация электролита в растворе намного превышает количество коллоидных частиц, то распределение происходит достаточно равномерно, в дисперсную систему переходит и вода, и электролит. Если же концентрация электролита в растворе мала, то вода из раствора переходит в дисперсную систему, а электролит в нее практически не переходит. Причем анионы входят в отрицательно заряженную коллоидную систему в большей степени по сравнению с катионами. В результате возникает разность потенциалов между гелем и раствором (потенциал Доннана), но она не соответствует тому, что наблюдается в почвах.
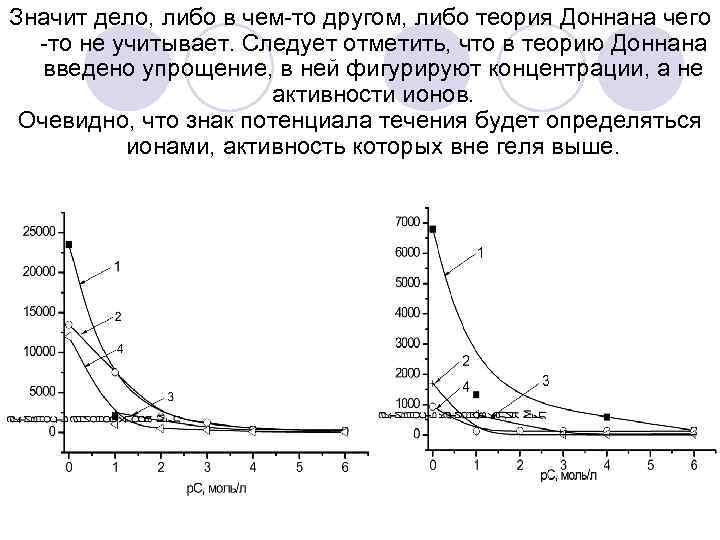 Значит дело, либо в чем-то другом, либо теория Доннана чего -то не учитывает. Следует отметить, что в теорию Доннана введено упрощение, в ней фигурируют концентрации, а не активности ионов. Очевидно, что знак потенциала течения будет определяться ионами, активность которых вне геля выше.
Значит дело, либо в чем-то другом, либо теория Доннана чего -то не учитывает. Следует отметить, что в теорию Доннана введено упрощение, в ней фигурируют концентрации, а не активности ионов. Очевидно, что знак потенциала течения будет определяться ионами, активность которых вне геля выше.
 Пристенный слой раствора, заключающий в себе диффузную часть ДЭС, всегда отличается по составу от объема благодаря наличию избытка положительных или отрицательных ионов. В результате электропроводность в двойном слое оказывается выше, чем в объеме раствора вдали от стенки. И соответственно общая (средняя) проводимость раствора в капилляре выше, чем проводимость равновесного с ним раствора вне капилляра. Общая проводимость может быть в несколько раз выше объемной. Поверхностная проводимость представляет собой приращение проводимости раствора в капилляре вследствие наличия двойного электрического слоя. Очевидно, что вклад поверхностной проводимости должен зависеть от относительной доли объема пристенного слоя раствора, обладающего повышенной проводимостью. Чем уже капилляр, тем больше доля раствора с аномальной проводимостью и выше ее вклад в общую проводимость.
Пристенный слой раствора, заключающий в себе диффузную часть ДЭС, всегда отличается по составу от объема благодаря наличию избытка положительных или отрицательных ионов. В результате электропроводность в двойном слое оказывается выше, чем в объеме раствора вдали от стенки. И соответственно общая (средняя) проводимость раствора в капилляре выше, чем проводимость равновесного с ним раствора вне капилляра. Общая проводимость может быть в несколько раз выше объемной. Поверхностная проводимость представляет собой приращение проводимости раствора в капилляре вследствие наличия двойного электрического слоя. Очевидно, что вклад поверхностной проводимости должен зависеть от относительной доли объема пристенного слоя раствора, обладающего повышенной проводимостью. Чем уже капилляр, тем больше доля раствора с аномальной проводимостью и выше ее вклад в общую проводимость.
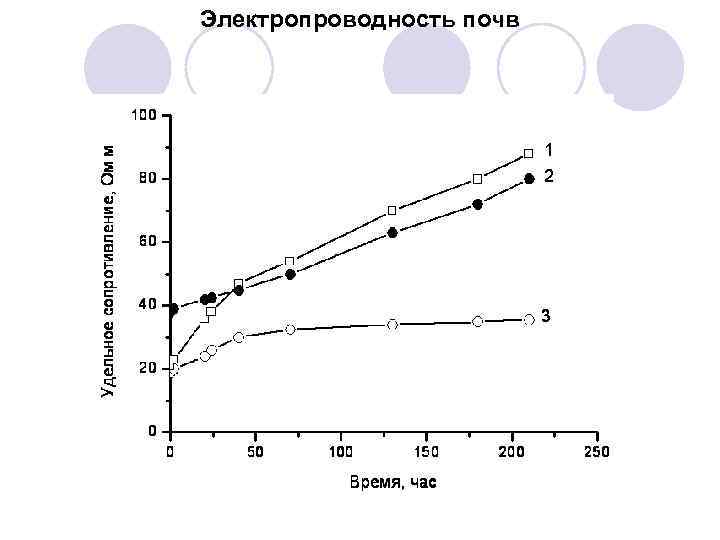 Электропроводность почв
Электропроводность почв
 Все изложенное выше, все примеры по поведению и свойствам почв свидетельствуют о нахождении на поверхности почвенных частиц гелевого слоя, обладающего определенным набором свойств. Он способен взаимодействовать с водой, включая ее в свой состав, т. е. способен набухать. Кроме того, при взаимодействии с водой его свойства изменяются. Об свидетельствуют рассмотренные нами: • наличие НО и его изменение под влиянием различных факторов; • заполнение мелких капилляров гелем; • изменение взаимодействия почв с водой от их влажности; • наличие гистерезиса в зависимости активности почвенной влаги от влажности; • сложная зависимость потенциала течения от времени фильтрации; • повышение удельного электросопротивления почв от времени после добавления воды.
Все изложенное выше, все примеры по поведению и свойствам почв свидетельствуют о нахождении на поверхности почвенных частиц гелевого слоя, обладающего определенным набором свойств. Он способен взаимодействовать с водой, включая ее в свой состав, т. е. способен набухать. Кроме того, при взаимодействии с водой его свойства изменяются. Об свидетельствуют рассмотренные нами: • наличие НО и его изменение под влиянием различных факторов; • заполнение мелких капилляров гелем; • изменение взаимодействия почв с водой от их влажности; • наличие гистерезиса в зависимости активности почвенной влаги от влажности; • сложная зависимость потенциала течения от времени фильтрации; • повышение удельного электросопротивления почв от времени после добавления воды.
 Однако на основании этих данных мы ничего не можем сказать об его строении. Почвы очень сложные системы, включающие в свой состав огромное число компонентов в различных состояниях. Среди этих компонентов присутствует и биота. Почвы живут и постоянно меняются. Пытаться выявлять закономерности на таких сложных изменяющихся системах очень трудно. Для того чтобы получить представления о строении почвенных гелей необходимо опираться на исследования и закономерности, обнаруженные на более простых системах. Поэтому в коллоидной химии нас, прежде всего, интересуют теории возникновения и существования гелей. Они могут помочь нам в решении нашей задачи. Наиболее известной теорией, описывающей агрегативную устойчивость коллоидных систем (возникновение гелей из золей), является теория Дерягина – Ландау – Фервея – Овербека (ДЛФО).
Однако на основании этих данных мы ничего не можем сказать об его строении. Почвы очень сложные системы, включающие в свой состав огромное число компонентов в различных состояниях. Среди этих компонентов присутствует и биота. Почвы живут и постоянно меняются. Пытаться выявлять закономерности на таких сложных изменяющихся системах очень трудно. Для того чтобы получить представления о строении почвенных гелей необходимо опираться на исследования и закономерности, обнаруженные на более простых системах. Поэтому в коллоидной химии нас, прежде всего, интересуют теории возникновения и существования гелей. Они могут помочь нам в решении нашей задачи. Наиболее известной теорией, описывающей агрегативную устойчивость коллоидных систем (возникновение гелей из золей), является теория Дерягина – Ландау – Фервея – Овербека (ДЛФО).
 Эта теория рассматривает устойчивость и коагуляцию лиофобных коллоидов как результат совокупного действия молекулярных (Ван-дер-ваальсовых - дисперсионных) сил притяжения и электростатических сил отталкивания между частицами, причем эти силы имеют дальнодействующий характер, их радиус действия достигает сотен и тысяч молекулярных диаметров. В зависимости от баланса этих сил в тонкой прослойке жидкости (межфазной пленке) между сближающимися телами (частицами) возникает либо положительное расклинивающее давление (отталкивание), препятствующее их соединению, либо отрицательное расклинивающее давление (притяжение), приводящее к утончению прослойки и образованию контакта между частицами. Таким образом, стабильность (устойчивость) дисперсной фазы и ее коагуляция определяются соотношением между силами притяжения и отталкивания частиц.
Эта теория рассматривает устойчивость и коагуляцию лиофобных коллоидов как результат совокупного действия молекулярных (Ван-дер-ваальсовых - дисперсионных) сил притяжения и электростатических сил отталкивания между частицами, причем эти силы имеют дальнодействующий характер, их радиус действия достигает сотен и тысяч молекулярных диаметров. В зависимости от баланса этих сил в тонкой прослойке жидкости (межфазной пленке) между сближающимися телами (частицами) возникает либо положительное расклинивающее давление (отталкивание), препятствующее их соединению, либо отрицательное расклинивающее давление (притяжение), приводящее к утончению прослойки и образованию контакта между частицами. Таким образом, стабильность (устойчивость) дисперсной фазы и ее коагуляция определяются соотношением между силами притяжения и отталкивания частиц.
 Понятие о расклинивающем давлении было введено Б. В. Дерягиным. При малых расстояниях между частицами (фаза 1) возникает тонкая прослойка дисперсионной среды (фаза 2) – межфазная пленка толщиной h. Утончение пленки, начиная с некоторой малой толщины, требует преодоления некоторого дополнительного (избыточного) давления, которое возникает при перекрывании поверхностных слоев – переходных зон вблизи границы фаз 1 и 2 (толщиной h 1 и h 2).
Понятие о расклинивающем давлении было введено Б. В. Дерягиным. При малых расстояниях между частицами (фаза 1) возникает тонкая прослойка дисперсионной среды (фаза 2) – межфазная пленка толщиной h. Утончение пленки, начиная с некоторой малой толщины, требует преодоления некоторого дополнительного (избыточного) давления, которое возникает при перекрывании поверхностных слоев – переходных зон вблизи границы фаз 1 и 2 (толщиной h 1 и h 2).
 Другими словами, речь идет о перекрытии поверхностных слоев фазы 1 со стороны фазы 2. Если расстояние между телами h > h 1 + h 2, то свободная поверхностная энергия двусторонней пленки Fпл в расчете на единицу площади равна удвоенному значению удельной межфазной энергии σ границы раздела фаз 1 и 2: Fпл = σпл = 2σ12. Если же h < h 1 + h 2, т. е. имеет место перекрытие поверхностных слоев, то дальнейшее утончение пленки требует совершения работы ΔW. В изотермическом процессе эта работа переходит в избыточную свободную энергию пленки, зависящую от толщины: ΔW = ΔFпл(h). Поэтому при h < h 1 + h 2 удельная свободная поверхностная энергия пленки будет равна: Fпл(h) = σпл = 2σ12 + ΔFпл(h) = 2σ12 + Δσпл.
Другими словами, речь идет о перекрытии поверхностных слоев фазы 1 со стороны фазы 2. Если расстояние между телами h > h 1 + h 2, то свободная поверхностная энергия двусторонней пленки Fпл в расчете на единицу площади равна удвоенному значению удельной межфазной энергии σ границы раздела фаз 1 и 2: Fпл = σпл = 2σ12. Если же h < h 1 + h 2, т. е. имеет место перекрытие поверхностных слоев, то дальнейшее утончение пленки требует совершения работы ΔW. В изотермическом процессе эта работа переходит в избыточную свободную энергию пленки, зависящую от толщины: ΔW = ΔFпл(h). Поэтому при h < h 1 + h 2 удельная свободная поверхностная энергия пленки будет равна: Fпл(h) = σпл = 2σ12 + ΔFпл(h) = 2σ12 + Δσпл.
 Изменение энергии системы при уменьшении толщины пленки h можно рассматривать как результат действия в ней некоторого избыточного давления, которое Дерягин и назвал расклинивающим давлением. Расклинивающее давление Π(h) – то избыточное давление, которое надо приложить к поверхностям, ограничивающим тонкую пленку, чтобы ее толщина оставалась постоянной, т. е. чтобы система находилась в состоянии термодинамического равновесия. Расклинивающее давление может быть обусловлено факторами различной природы и, соответственно, включает различные составляющие: 1) Молекулярная составляющая Πm(h) обусловлена межмолекулярными силами притяжения фаз; эта составляющая обычно отрицательна, т. е. способствует сближению частиц и нарушению агрегативной устойчивости дисперсных систем.
Изменение энергии системы при уменьшении толщины пленки h можно рассматривать как результат действия в ней некоторого избыточного давления, которое Дерягин и назвал расклинивающим давлением. Расклинивающее давление Π(h) – то избыточное давление, которое надо приложить к поверхностям, ограничивающим тонкую пленку, чтобы ее толщина оставалась постоянной, т. е. чтобы система находилась в состоянии термодинамического равновесия. Расклинивающее давление может быть обусловлено факторами различной природы и, соответственно, включает различные составляющие: 1) Молекулярная составляющая Πm(h) обусловлена межмолекулярными силами притяжения фаз; эта составляющая обычно отрицательна, т. е. способствует сближению частиц и нарушению агрегативной устойчивости дисперсных систем.
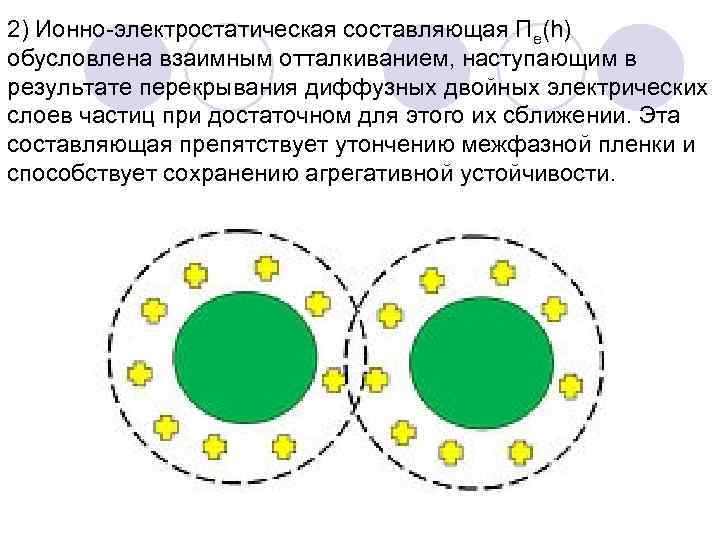 2) Ионно-электростатическая составляющая Πe(h) обусловлена взаимным отталкиванием, наступающим в результате перекрывания диффузных двойных электрических слоев частиц при достаточном для этого их сближении. Эта составляющая препятствует утончению межфазной пленки и способствует сохранению агрегативной устойчивости.
2) Ионно-электростатическая составляющая Πe(h) обусловлена взаимным отталкиванием, наступающим в результате перекрывания диффузных двойных электрических слоев частиц при достаточном для этого их сближении. Эта составляющая препятствует утончению межфазной пленки и способствует сохранению агрегативной устойчивости.
 3) На весьма малых расстояниях обнаруживается действие структурной составляющей расклинивающего давления Πs(h). Она возникает, когда толщина пленки h становится меньше суммарной толщины сольватных слоев жидкости на поверхности частиц, т. е. при перекрытии сольватных оболочек частиц. Сольватно связанная жидкость, как известно, обладает структурой и свойствами, отличными от свойств соответствующей объемной фазы. При перекрытии сольватных оболочек часть структурно измененных слоев жидкости выдавливается в объем «нормальной» жидкости. Это требует совершения работы, и ее можно рассматривать как работу по преодолению некоторого добавочного давления, которое и составляет «структурный» вклад в расклинивающее давление. Таким образом, расклинивающее давление может быть представлено как сумма трех слагаемых: Π(h) = Πe(h) + Πm(h) + Πs(h).
3) На весьма малых расстояниях обнаруживается действие структурной составляющей расклинивающего давления Πs(h). Она возникает, когда толщина пленки h становится меньше суммарной толщины сольватных слоев жидкости на поверхности частиц, т. е. при перекрытии сольватных оболочек частиц. Сольватно связанная жидкость, как известно, обладает структурой и свойствами, отличными от свойств соответствующей объемной фазы. При перекрытии сольватных оболочек часть структурно измененных слоев жидкости выдавливается в объем «нормальной» жидкости. Это требует совершения работы, и ее можно рассматривать как работу по преодолению некоторого добавочного давления, которое и составляет «структурный» вклад в расклинивающее давление. Таким образом, расклинивающее давление может быть представлено как сумма трех слагаемых: Π(h) = Πe(h) + Πm(h) + Πs(h).
 Теория ДЛФО позволяет вычислить электростатическую составляющую расклинивающего давления и соответствующее значение потенциальной энергии отталкивания частиц в зависимости от расстояния между ними. Рассмотрим взаимодействие частиц, рассматривая их как плоскопараллельные пластины (заряженные до потенциала φ0). Подобное приближение справедливо для случая не слишком малых частиц, когда их размер значительно больше толщины ДЭС. Пусть частицы заряжены до потенциала φ0 и при сближении до расстояния h = 2 x произошло перекрывание их диффузных ионных атмосфер. Тогда имеет место суперпозиция их электрических полей, и в зазоре между пластинами изменение электрического потенциала ДЭС происходит по кривой, получаемой суммированием потенциалов φ(х) каждой из двух пластин.
Теория ДЛФО позволяет вычислить электростатическую составляющую расклинивающего давления и соответствующее значение потенциальной энергии отталкивания частиц в зависимости от расстояния между ними. Рассмотрим взаимодействие частиц, рассматривая их как плоскопараллельные пластины (заряженные до потенциала φ0). Подобное приближение справедливо для случая не слишком малых частиц, когда их размер значительно больше толщины ДЭС. Пусть частицы заряжены до потенциала φ0 и при сближении до расстояния h = 2 x произошло перекрывание их диффузных ионных атмосфер. Тогда имеет место суперпозиция их электрических полей, и в зазоре между пластинами изменение электрического потенциала ДЭС происходит по кривой, получаемой суммированием потенциалов φ(х) каждой из двух пластин.
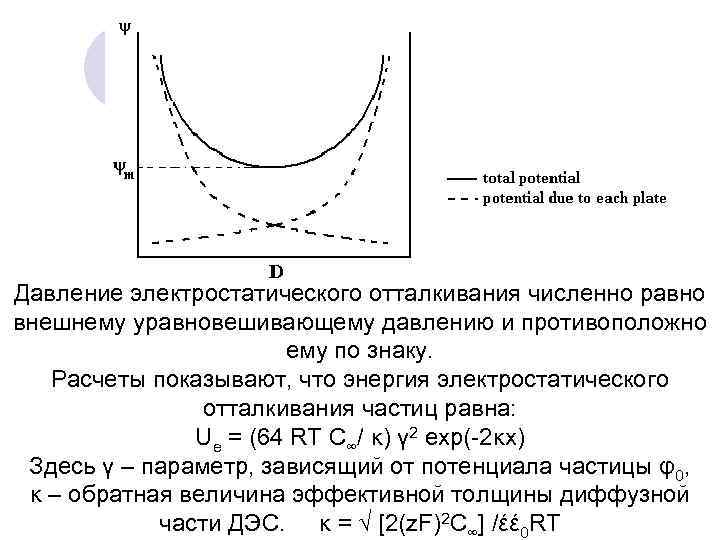 Давление электростатического отталкивания численно равно внешнему уравновешивающему давлению и противоположно ему по знаку. Расчеты показывают, что энергия электростатического отталкивания частиц равна: Ue = (64 RT С∞/ κ) γ 2 exp(-2κх) Здесь γ – параметр, зависящий от потенциала частицы φ0, κ – обратная величина эффективной толщины диффузной части ДЭС. κ = √ [2(z. F)2 С∞] /έέ 0 RT
Давление электростатического отталкивания численно равно внешнему уравновешивающему давлению и противоположно ему по знаку. Расчеты показывают, что энергия электростатического отталкивания частиц равна: Ue = (64 RT С∞/ κ) γ 2 exp(-2κх) Здесь γ – параметр, зависящий от потенциала частицы φ0, κ – обратная величина эффективной толщины диффузной части ДЭС. κ = √ [2(z. F)2 С∞] /έέ 0 RT
 Таким образом, энергия электростатического отталкивания падает по экспоненциальном закону с увеличением расстояния между частицами. Расчеты Ue показывают снижение энергии отталкивания с увеличением концентрации С∞, что согласуется с результатами, полученными на основании прямых измерений электростатического расклинивающего давления. Согласно теории ДЛФО силы притяжения между частицами, вызывающие их слипание (коагуляцию), имеют ту же природу, что и силы взаимного притяжения молекул в газах и конденсированных телах, т. е. это силы дисперсионного межмолекулярного взаимодействия Ван-дер-Ваальса. Выражение для расчета энергии молекулярного притяжения между частицами имеет вид: Um = 48 А/х2 Здесь А – константа Гамакера, характеризующая энергию Ван -дер-ваальсова взаимодействия двух частиц и зависящая от природы частиц.
Таким образом, энергия электростатического отталкивания падает по экспоненциальном закону с увеличением расстояния между частицами. Расчеты Ue показывают снижение энергии отталкивания с увеличением концентрации С∞, что согласуется с результатами, полученными на основании прямых измерений электростатического расклинивающего давления. Согласно теории ДЛФО силы притяжения между частицами, вызывающие их слипание (коагуляцию), имеют ту же природу, что и силы взаимного притяжения молекул в газах и конденсированных телах, т. е. это силы дисперсионного межмолекулярного взаимодействия Ван-дер-Ваальса. Выражение для расчета энергии молекулярного притяжения между частицами имеет вид: Um = 48 А/х2 Здесь А – константа Гамакера, характеризующая энергию Ван -дер-ваальсова взаимодействия двух частиц и зависящая от природы частиц.
 Электростатические силы отталкивания убывают от расстояния между частицами, как мы уже говорили, по экспоненциальному закону, а силы притяжения по степенному закону. На малых расстояниях между частицами преобладает притяжение. На больших расстояниях также преобладает притяжение, поскольку степенная функция убывает значительно медленнее, чем экспонента. На средних расстояниях может преобладать отталкивание. В результате в общем случае энергетическая функция взаимодействия частиц имеет два потенциальных минимума и разделяющий их энергетический барьер.
Электростатические силы отталкивания убывают от расстояния между частицами, как мы уже говорили, по экспоненциальному закону, а силы притяжения по степенному закону. На малых расстояниях между частицами преобладает притяжение. На больших расстояниях также преобладает притяжение, поскольку степенная функция убывает значительно медленнее, чем экспонента. На средних расстояниях может преобладать отталкивание. В результате в общем случае энергетическая функция взаимодействия частиц имеет два потенциальных минимума и разделяющий их энергетический барьер.
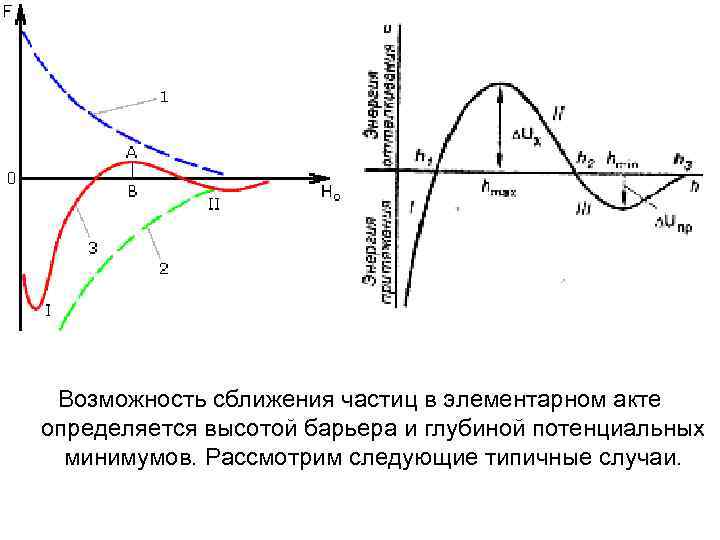 Возможность сближения частиц в элементарном акте определяется высотой барьера и глубиной потенциальных минимумов. Рассмотрим следующие типичные случаи.
Возможность сближения частиц в элементарном акте определяется высотой барьера и глубиной потенциальных минимумов. Рассмотрим следующие типичные случаи.
 l Если высота барьера, а также глубина второго (дальнего) минимума невелики ( к. Т) частицы сближаются в броуновском движении до наименьшего, возможного расстояния (порядка долей нм) с уменьшением энергии системы на величину, равную глубине первого минимума. Элементарный акт коагуляции происходит, таким образом, в результате ближнего взаимодействия частиц, при достаточной глубине первого минимума. Такие системы неустойчивы и коагуляция идет в большинстве случаев необратимо, поскольку глубина первого минимума обычно к. Т. Снижение высоты барьера, может быть вызвано либо увеличением ионной силы раствора, либо уменьшением потенциала на границе адсорбционного и диффузного слоев в результате специфической адсорбции. Поэтому можно говорить о двух видах коагуляции – концентрационной и адсорбционной.
l Если высота барьера, а также глубина второго (дальнего) минимума невелики ( к. Т) частицы сближаются в броуновском движении до наименьшего, возможного расстояния (порядка долей нм) с уменьшением энергии системы на величину, равную глубине первого минимума. Элементарный акт коагуляции происходит, таким образом, в результате ближнего взаимодействия частиц, при достаточной глубине первого минимума. Такие системы неустойчивы и коагуляция идет в большинстве случаев необратимо, поскольку глубина первого минимума обычно к. Т. Снижение высоты барьера, может быть вызвано либо увеличением ионной силы раствора, либо уменьшением потенциала на границе адсорбционного и диффузного слоев в результате специфической адсорбции. Поэтому можно говорить о двух видах коагуляции – концентрационной и адсорбционной.
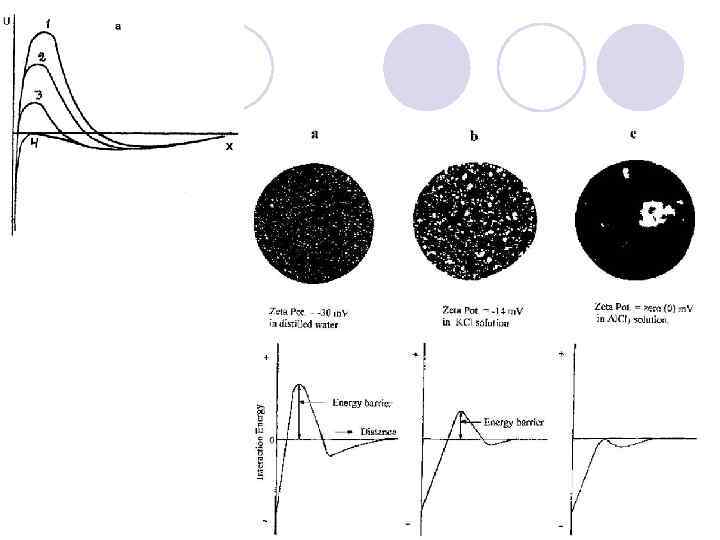
 l Если высота барьера велика ( к. Т), а глубина второго минимума мала ( к. Т), частицы не могут преодолеть барьера и расходятся без взаимодействия. Это – случай агрегативно устойчивой системы. Если частиц много, то они стараются разойтись как можно дальше друг от друга, образуя псевдокристаллические решетки, в узлах которых расположены коллоидные частицы. Такие системы получили название периодических коллоидных структур (ПКС) ограниченного объема.
l Если высота барьера велика ( к. Т), а глубина второго минимума мала ( к. Т), частицы не могут преодолеть барьера и расходятся без взаимодействия. Это – случай агрегативно устойчивой системы. Если частиц много, то они стараются разойтись как можно дальше друг от друга, образуя псевдокристаллические решетки, в узлах которых расположены коллоидные частицы. Такие системы получили название периодических коллоидных структур (ПКС) ограниченного объема.
 Если глубина второго минимума достаточно велика ( к. Т), то, независимо от высоты барьера, происходит, так называемое дальнее взаимодействие коллоидных частиц, и они фиксируются на расстоянии соответствующем второму минимуму. При этом устанавливается гибкая связь, частицы не могут ни разойтись, ни приблизиться друг к другу. Частицы, связанные на столь больших расстояниях (иногда на порядок превышающих размеры частиц), приобретают фазэвую устойчивость, а система в целом сохраняет свою дисперсность и удельную поверхность. Как показывают расчеты, глубина второго минимума возрастает с увеличением числа частиц (уменьшением среднего расстояния между ними), что способствует протеканию коллективных взаимодействий. При достаточной концентрации дисперсной фазы это приводит к превращению золя в сильно структурированную жидкость с аномалией вязкого течения или даже в полностью структурированную систему (гель).
Если глубина второго минимума достаточно велика ( к. Т), то, независимо от высоты барьера, происходит, так называемое дальнее взаимодействие коллоидных частиц, и они фиксируются на расстоянии соответствующем второму минимуму. При этом устанавливается гибкая связь, частицы не могут ни разойтись, ни приблизиться друг к другу. Частицы, связанные на столь больших расстояниях (иногда на порядок превышающих размеры частиц), приобретают фазэвую устойчивость, а система в целом сохраняет свою дисперсность и удельную поверхность. Как показывают расчеты, глубина второго минимума возрастает с увеличением числа частиц (уменьшением среднего расстояния между ними), что способствует протеканию коллективных взаимодействий. При достаточной концентрации дисперсной фазы это приводит к превращению золя в сильно структурированную жидкость с аномалией вязкого течения или даже в полностью структурированную систему (гель).

 Подобные системы получили название локальных ПКС, а процесс их образования – дальней агрегации. Следует отметить, что подобные структуры весьма распространены. Среди факторов, обусловливающих агрегацию и коагуляцию дисперсных частиц, особенно большое внимание было уделено влиянию размера и формы частиц. Было рассмотрено взаимодействие двух пластин и двух одинаковых шаров, двух частиц разных форм и размеров, трех пластин различной толщины. Ряд специальных исследований был посвящен рассмотрению взаимодействия двух частиц с одинаковыми низкими и высокими потенциалами, а также частиц, имеющих произвольные значения потенциала. Рассмотрено влияние концентрации порового раствора на развитие процессов агрегации и коагуляции.
Подобные системы получили название локальных ПКС, а процесс их образования – дальней агрегации. Следует отметить, что подобные структуры весьма распространены. Среди факторов, обусловливающих агрегацию и коагуляцию дисперсных частиц, особенно большое внимание было уделено влиянию размера и формы частиц. Было рассмотрено взаимодействие двух пластин и двух одинаковых шаров, двух частиц разных форм и размеров, трех пластин различной толщины. Ряд специальных исследований был посвящен рассмотрению взаимодействия двух частиц с одинаковыми низкими и высокими потенциалами, а также частиц, имеющих произвольные значения потенциала. Рассмотрено влияние концентрации порового раствора на развитие процессов агрегации и коагуляции.
 В результате этих работ были установлены общие закономерности взаимодействия дисперсных частиц, которые находятся в согласии с опытными данными. l При взаимодействии пластин в условиях их малой объемной концентрации и отсутствия электролитов в растворе энергетический барьер у тонких пластин выше, чем у толстых. Иными словами, тонкие пластины более устойчивы против коагуляции, чем толстые. Однако с увеличением содержания твердой фазы расстояние между поверхностями и соответственно устойчивость более резко уменьшаются для тонких пластин, что обусловливает наступление у них стесненной коагуляции, в то время как более толстые пластины остаются еще стабилизированными. Следовательно, в концентрированных системах тонкие пластины оказываются менее устойчивыми к коагуляции по сравнению с толстыми пластинами.
В результате этих работ были установлены общие закономерности взаимодействия дисперсных частиц, которые находятся в согласии с опытными данными. l При взаимодействии пластин в условиях их малой объемной концентрации и отсутствия электролитов в растворе энергетический барьер у тонких пластин выше, чем у толстых. Иными словами, тонкие пластины более устойчивы против коагуляции, чем толстые. Однако с увеличением содержания твердой фазы расстояние между поверхностями и соответственно устойчивость более резко уменьшаются для тонких пластин, что обусловливает наступление у них стесненной коагуляции, в то время как более толстые пластины остаются еще стабилизированными. Следовательно, в концентрированных системах тонкие пластины оказываются менее устойчивыми к коагуляции по сравнению с толстыми пластинами.
 l В отличие от пластин мелкие сферические частицы менее устойчивы по сравнению с крупными, независимо от их концентрации в системе. Это объясняется тем, что энергия молекулярного притяжения и ионно-электростатического отталкивания двух сферических частиц пропорциональны их радиусу r. Следовательно, высота потенциального барьера, равная алгебраической сумме величин этих энергий, также пропорциональна r. l В целом при взаимодействии мелких частиц чаще всего наблюдается их коагуляция, в то время как для больших сферических частиц, толстых пластин и крупных микрообъектов другой формы характерно наличие глубокого вторичного минимума. Поэтому в грубодисперсных системах идет развитие процесса агрегации.
l В отличие от пластин мелкие сферические частицы менее устойчивы по сравнению с крупными, независимо от их концентрации в системе. Это объясняется тем, что энергия молекулярного притяжения и ионно-электростатического отталкивания двух сферических частиц пропорциональны их радиусу r. Следовательно, высота потенциального барьера, равная алгебраической сумме величин этих энергий, также пропорциональна r. l В целом при взаимодействии мелких частиц чаще всего наблюдается их коагуляция, в то время как для больших сферических частиц, толстых пластин и крупных микрообъектов другой формы характерно наличие глубокого вторичного минимума. Поэтому в грубодисперсных системах идет развитие процесса агрегации.
 l При процессах гетерокоагуляции, то есть присутствии в системе частиц разной формы и размеров, столкновение крупных частиц с крупными и крупных с мелкими приводит к их взаимной фиксации на далеких расстояниях, в то время как столкновение мелких частиц между собой менее эффективно из-за малой величины второго энергетического минимума. В результате блокирования мелкими частицами поверхности крупных частиц образующиеся агрегаты оказываются устойчивыми к слипанию и прекращают свой дальнейший рост. l Величина силового барьера между двумя частицами любой формы, имеющими различный потенциал, зависит только от потенциала частицы, заряженной слабее. Отсюда фиксация на неоднородной поверхности всегда развивается быстрее, чем их взаимная коагуляция. В то же время глубина второго потенциального минимума слабо зависит от потенциала поверхностей частиц.
l При процессах гетерокоагуляции, то есть присутствии в системе частиц разной формы и размеров, столкновение крупных частиц с крупными и крупных с мелкими приводит к их взаимной фиксации на далеких расстояниях, в то время как столкновение мелких частиц между собой менее эффективно из-за малой величины второго энергетического минимума. В результате блокирования мелкими частицами поверхности крупных частиц образующиеся агрегаты оказываются устойчивыми к слипанию и прекращают свой дальнейший рост. l Величина силового барьера между двумя частицами любой формы, имеющими различный потенциал, зависит только от потенциала частицы, заряженной слабее. Отсюда фиксация на неоднородной поверхности всегда развивается быстрее, чем их взаимная коагуляция. В то же время глубина второго потенциального минимума слабо зависит от потенциала поверхностей частиц.
 l При увеличении концентрации электролитов в растворе идет сжатие диффузного слоя ионов, уменьшение барьера отталкивания и увеличение глубины второго потенциального минимума. Поэтому небольшое увеличение содержания электролитов в системе способствует фиксации частиц во втором минимуме. Однако последующее увеличение концентрации электролита приводит к исчезновению барьера отталкивания и непосредственному слипанию частиц, то есть их коагуляции. Изложенные закономерности получены для широкого круга лиофобных коллоидов, но подобный подход по отношению к почвам является сильно упрощенным, так касается только однородно поляризованных частиц, имеющих шарообразную или пластинчатую форму, и он позволяет понять далеко не все изменения, происходящие с почвенными коллоидами.
l При увеличении концентрации электролитов в растворе идет сжатие диффузного слоя ионов, уменьшение барьера отталкивания и увеличение глубины второго потенциального минимума. Поэтому небольшое увеличение содержания электролитов в системе способствует фиксации частиц во втором минимуме. Однако последующее увеличение концентрации электролита приводит к исчезновению барьера отталкивания и непосредственному слипанию частиц, то есть их коагуляции. Изложенные закономерности получены для широкого круга лиофобных коллоидов, но подобный подход по отношению к почвам является сильно упрощенным, так касается только однородно поляризованных частиц, имеющих шарообразную или пластинчатую форму, и он позволяет понять далеко не все изменения, происходящие с почвенными коллоидами.
 Так при рассмотрении процессов коагуляции и агрегации глинистых систем необходимо учитывать высокую гидрофильность частиц и наличие у них толстых сольватных оболочек. В глинистых минералах стабилизация частиц граничными гидратными пленками может быть неодинаковой по поверхности частиц. Согласно исследованиям Дерягина и Ландау, она наибольшая на плоских поверхностях и наименьшая на участках повышенной кривизны, то есть на боковых сколах и ребрах частиц. Поэтому при расположении частиц по типу базис-скол глубина дальнего потенциального минимума будет больше, чем при расположении их по типу базис.
Так при рассмотрении процессов коагуляции и агрегации глинистых систем необходимо учитывать высокую гидрофильность частиц и наличие у них толстых сольватных оболочек. В глинистых минералах стабилизация частиц граничными гидратными пленками может быть неодинаковой по поверхности частиц. Согласно исследованиям Дерягина и Ландау, она наибольшая на плоских поверхностях и наименьшая на участках повышенной кривизны, то есть на боковых сколах и ребрах частиц. Поэтому при расположении частиц по типу базис-скол глубина дальнего потенциального минимума будет больше, чем при расположении их по типу базис.
 В связи с недостаточность равновесного подхода в более поздних работах концепция поверхностных сил была распространена на такие системы, для которых благодаря протеканию необратимых процессов нарушается термодинамическое равновесие. Деформация ДЭС, наступающая под влиянием внешнего поля или конвективного движения жидкости, а также других факторов, продуцирует электрическое поле, радиус действия которого часто на несколько порядков выше радиуса действия недеформированного слоя в тех же условиях. Поляризация ионных слоев, наступающая вследствие деформации ДЭС, обусловливает появление дальнодействующих сил притяжения между индуцированными диполями. Следует отметить, что ряд авторов считает, что коллоидные частицы существуют, в основном, в виде диполей, образующихся за счет униполярной ориентации молекул растворителя или молекул адсорбируемых из растворов веществ или вследствие ориентации полярных групп самого вещества частиц.
В связи с недостаточность равновесного подхода в более поздних работах концепция поверхностных сил была распространена на такие системы, для которых благодаря протеканию необратимых процессов нарушается термодинамическое равновесие. Деформация ДЭС, наступающая под влиянием внешнего поля или конвективного движения жидкости, а также других факторов, продуцирует электрическое поле, радиус действия которого часто на несколько порядков выше радиуса действия недеформированного слоя в тех же условиях. Поляризация ионных слоев, наступающая вследствие деформации ДЭС, обусловливает появление дальнодействующих сил притяжения между индуцированными диполями. Следует отметить, что ряд авторов считает, что коллоидные частицы существуют, в основном, в виде диполей, образующихся за счет униполярной ориентации молекул растворителя или молекул адсорбируемых из растворов веществ или вследствие ориентации полярных групп самого вещества частиц.
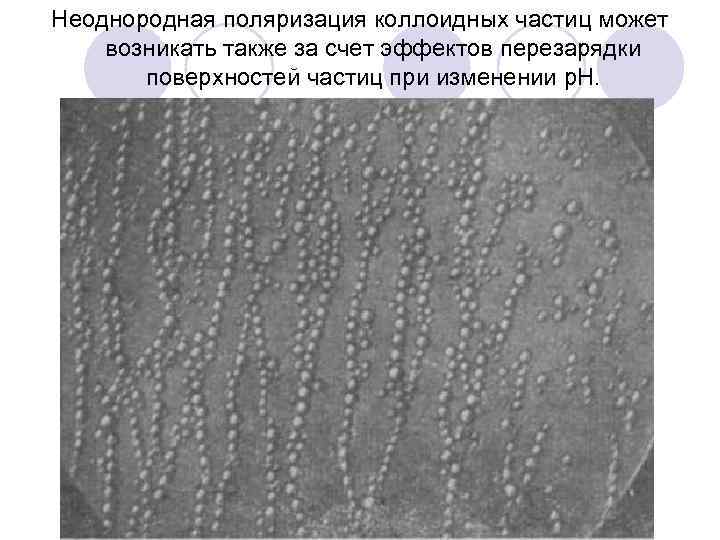 Неоднородная поляризация коллоидных частиц может возникать также за счет эффектов перезарядки поверхностей частиц при изменении р. Н.
Неоднородная поляризация коллоидных частиц может возникать также за счет эффектов перезарядки поверхностей частиц при изменении р. Н.
 Все это позволяет выдвинуть предположение об образовании почвенных коллоидных структур из поляризованных коллоидных частиц. При неоднородной поляризации возможно возникновение значительно большего числа структур. В этом случае силы отталкивания между частицами зависят от их взаиморасположения. Существуют и другие теории агрегации коллоидных частиц. В частности, ставится под сомнение возможность осуществления притяжения за счет Ван-дер-ваальсовых сил. В этих теориях предполагают, что и силы притяжения, и силы отталкивания имеют электростатическую природу. Отталкивание возникает за счет броуновского движения игнорируемого теорией ДЛФО. Появляется исключенный объем. Притяжение объясняют с позиций «коллоидного орбитального подхода» . Оно обеспечивается за счет перераспределения плотности противоионов между коллоидными частицами, аналогично электронам, формирующим молекулярные орбитали.
Все это позволяет выдвинуть предположение об образовании почвенных коллоидных структур из поляризованных коллоидных частиц. При неоднородной поляризации возможно возникновение значительно большего числа структур. В этом случае силы отталкивания между частицами зависят от их взаиморасположения. Существуют и другие теории агрегации коллоидных частиц. В частности, ставится под сомнение возможность осуществления притяжения за счет Ван-дер-ваальсовых сил. В этих теориях предполагают, что и силы притяжения, и силы отталкивания имеют электростатическую природу. Отталкивание возникает за счет броуновского движения игнорируемого теорией ДЛФО. Появляется исключенный объем. Притяжение объясняют с позиций «коллоидного орбитального подхода» . Оно обеспечивается за счет перераспределения плотности противоионов между коллоидными частицами, аналогично электронам, формирующим молекулярные орбитали.
 Приведенные теории взаимодействия между коллоидными частицами не могут объяснить всех эффектов, наблюдаемых в реальных системах, и пока не всегда позволяют не только рассчитать, но даже на качественном уровне предсказать их поведение. Однако из этих теорий, основанных на большом числе экспериментальных данных, следует, что коллоидные частицы могут взаимодействовать друг с другом и на дальних расстояниях, образуя системы с определенной структурной организацией. Причем подобное поведение не представляет собой некое исключение из правил, а является обычным для концентрированных коллоидных систем, и его необходимо принимать во внимание, анализируя поведение коллоидной составляющей почв.
Приведенные теории взаимодействия между коллоидными частицами не могут объяснить всех эффектов, наблюдаемых в реальных системах, и пока не всегда позволяют не только рассчитать, но даже на качественном уровне предсказать их поведение. Однако из этих теорий, основанных на большом числе экспериментальных данных, следует, что коллоидные частицы могут взаимодействовать друг с другом и на дальних расстояниях, образуя системы с определенной структурной организацией. Причем подобное поведение не представляет собой некое исключение из правил, а является обычным для концентрированных коллоидных систем, и его необходимо принимать во внимание, анализируя поведение коллоидной составляющей почв.
 При этом трудно ожидать, что почвенные коллоиды покажут идеальное поведение, демонстрируемое той или иной моделью, частично потому что они – полидисперсны и имеют различную форму, а также, потому что они имеют отличающиеся заряды различных граней минеральных частиц. Дополнительный вклад в их неидеальное поведение вносят смешанный состав электролитов в растворе, а также сложный состав молекул и ионов, адсорбируемых на поверхности частиц, что изменяет их заряд и распределение ионов в двойном электрическом слое. Однако происхождение фундаментальных сил притяжения и отталкивания в этих коллоидных системах, должно быть тем же самым, что и в модельных коллоидах, и, следовательно, в них неизбежно должна возникать определенная структурная организация, предопределяющая как их свойства, так и свойства почв.
При этом трудно ожидать, что почвенные коллоиды покажут идеальное поведение, демонстрируемое той или иной моделью, частично потому что они – полидисперсны и имеют различную форму, а также, потому что они имеют отличающиеся заряды различных граней минеральных частиц. Дополнительный вклад в их неидеальное поведение вносят смешанный состав электролитов в растворе, а также сложный состав молекул и ионов, адсорбируемых на поверхности частиц, что изменяет их заряд и распределение ионов в двойном электрическом слое. Однако происхождение фундаментальных сил притяжения и отталкивания в этих коллоидных системах, должно быть тем же самым, что и в модельных коллоидах, и, следовательно, в них неизбежно должна возникать определенная структурная организация, предопределяющая как их свойства, так и свойства почв.
 При разработке концепции структурной организации почвенных гелей исходили из следующего: l Коллоидные частицы в почвах должны взаимодействовать между собой, образуя гелевые системы. l Восприятие гелей почв только как плотноупакованных систем, образующихся за счет непосредственного контакта между коллоидными частицами может не соответствовать действительности. l В случае образования в почвах из коллоидных частиц пространственных структур получение информации о составе коллоидной составляющей почв является явно недостаточным и не позволяет однозначно охарактеризовать почвы.
При разработке концепции структурной организации почвенных гелей исходили из следующего: l Коллоидные частицы в почвах должны взаимодействовать между собой, образуя гелевые системы. l Восприятие гелей почв только как плотноупакованных систем, образующихся за счет непосредственного контакта между коллоидными частицами может не соответствовать действительности. l В случае образования в почвах из коллоидных частиц пространственных структур получение информации о составе коллоидной составляющей почв является явно недостаточным и не позволяет однозначно охарактеризовать почвы.
 l Лабильность гелевых структур значительно усложняет процесс исследования, так как практически любые воздействия на почвы (нагревание, высушивание, обработка теми или иными растворами) изменяют изучаемые системы, и перенесение выводов, полученных на «измененных» системах, на реальные почвы может приводить к значительным ошибкам. l Рассмотрение почвенного раствора во всех случаях как свободной неструктурированной жидкости вызывает с точки зрения возможности существования в почвах гелевых структур, включающих в свой состав большие количества воды, большие сомнения. l Роль органического вещества в образовании почвенных гелей неизвестна. l Необходимо учесть, что в теориях агрегативной устойчивости коллоидных систем рассматривают образование гелевых структур. В почвах гелевые структуры существуют длительное время и должны изменяться – уплотняться.
l Лабильность гелевых структур значительно усложняет процесс исследования, так как практически любые воздействия на почвы (нагревание, высушивание, обработка теми или иными растворами) изменяют изучаемые системы, и перенесение выводов, полученных на «измененных» системах, на реальные почвы может приводить к значительным ошибкам. l Рассмотрение почвенного раствора во всех случаях как свободной неструктурированной жидкости вызывает с точки зрения возможности существования в почвах гелевых структур, включающих в свой состав большие количества воды, большие сомнения. l Роль органического вещества в образовании почвенных гелей неизвестна. l Необходимо учесть, что в теориях агрегативной устойчивости коллоидных систем рассматривают образование гелевых структур. В почвах гелевые структуры существуют длительное время и должны изменяться – уплотняться.
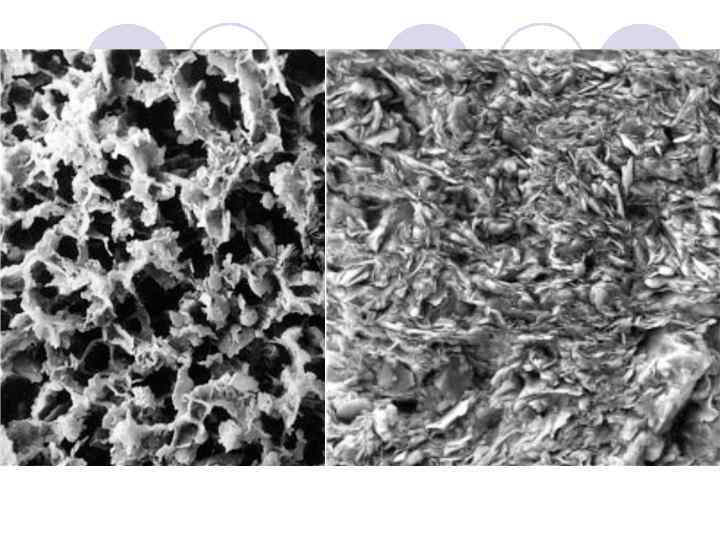
 На основании всего изложенного выше можно предположить существование несколько типов гелевых структур: • Плотные пленки-гели, в которых коллоидные частицы контактируют между собой, плотно заполняя пространство; • Ажурные гелевые структуры, возникающие при непосредственном контакте коллоидных частиц и включающие в свой состав почвенную влагу; • Периодические коллоидные структуры, возникающие за счет дальней агрегации и тоже включающие в свой состав большие количества почвенного раствора.
На основании всего изложенного выше можно предположить существование несколько типов гелевых структур: • Плотные пленки-гели, в которых коллоидные частицы контактируют между собой, плотно заполняя пространство; • Ажурные гелевые структуры, возникающие при непосредственном контакте коллоидных частиц и включающие в свой состав почвенную влагу; • Периодические коллоидные структуры, возникающие за счет дальней агрегации и тоже включающие в свой состав большие количества почвенного раствора.
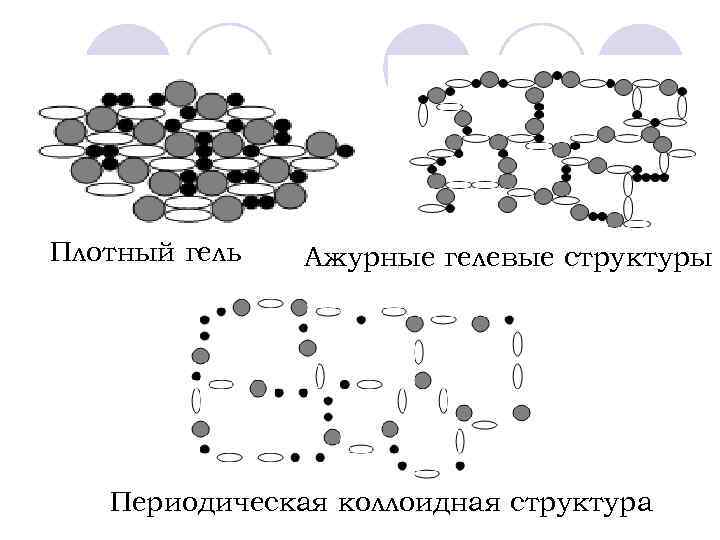 Плотный гель Ажурные гелевые структуры Периодическая коллоидная структура
Плотный гель Ажурные гелевые структуры Периодическая коллоидная структура
 Экспериментальные результаты по изучению процессов, проходящих в почвах, позволяют предполагать, что гели не являются плотными пленками, а включают в свой состав жидкость и способны изменять свои свойства во времени при контакте с водой. Однако было необходимо экспериментально получить ответ на этот вопрос. При планировании экспериментов исходили из того, что при выпрессовывании из почв в выделяющийся раствор попадают «обломки» гелей. Следовательно, их можно выделить и изучить их строение на электронном микроскопе. В зависимости от того, в каком виде находятся коллоидные частицы в почвенном растворе, можно ожидать три варианта их расположения на подложке.
Экспериментальные результаты по изучению процессов, проходящих в почвах, позволяют предполагать, что гели не являются плотными пленками, а включают в свой состав жидкость и способны изменять свои свойства во времени при контакте с водой. Однако было необходимо экспериментально получить ответ на этот вопрос. При планировании экспериментов исходили из того, что при выпрессовывании из почв в выделяющийся раствор попадают «обломки» гелей. Следовательно, их можно выделить и изучить их строение на электронном микроскопе. В зависимости от того, в каком виде находятся коллоидные частицы в почвенном растворе, можно ожидать три варианта их расположения на подложке.
 l Если бы коллоидные частицы присутствовали в почвенном растворе в виде золя они должны были бы относительно равномерно размещаться на поверхности подложки. l При выделении с почвенным раствором плотных гелей на подложке должны были бы наблюдаться сгустки непосредственно контактирующих друг с другом коллоидных частиц. l При наличии гелевых структур на подложке должны были бы наблюдаться разветвленные структуры из непосредственно контактирующих друг с другом коллоидных частиц. l При наличии же в почвенном растворе обломков периодических коллоидных структур они должны были бы осаждаться на подложку, так что коллоидные частицы, весьма вероятно, закрепились бы на подложке, сохраняя между собой расстояния, характерные для коллоидной структуры.
l Если бы коллоидные частицы присутствовали в почвенном растворе в виде золя они должны были бы относительно равномерно размещаться на поверхности подложки. l При выделении с почвенным раствором плотных гелей на подложке должны были бы наблюдаться сгустки непосредственно контактирующих друг с другом коллоидных частиц. l При наличии гелевых структур на подложке должны были бы наблюдаться разветвленные структуры из непосредственно контактирующих друг с другом коллоидных частиц. l При наличии же в почвенном растворе обломков периодических коллоидных структур они должны были бы осаждаться на подложку, так что коллоидные частицы, весьма вероятно, закрепились бы на подложке, сохраняя между собой расстояния, характерные для коллоидной структуры.
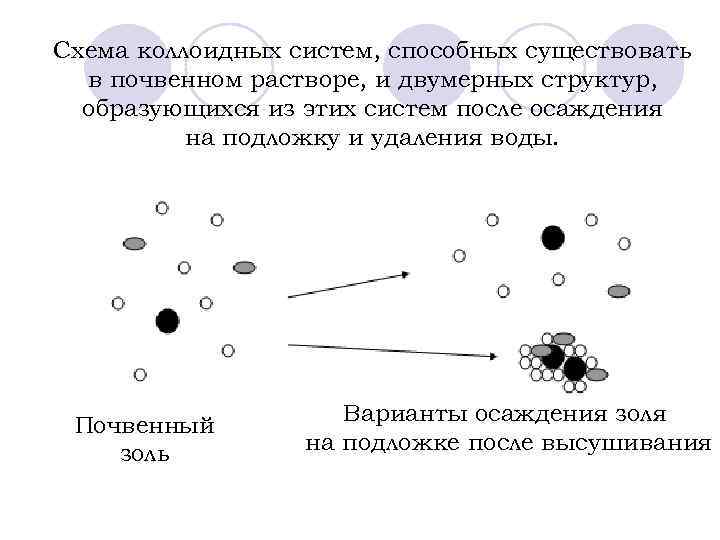 Схема коллоидных систем, способных существовать в почвенном растворе, и двумерных структур, образующихся из этих систем после осаждения на подложку и удаления воды. Почвенный золь Варианты осаждения золя на подложке после высушивания
Схема коллоидных систем, способных существовать в почвенном растворе, и двумерных структур, образующихся из этих систем после осаждения на подложку и удаления воды. Почвенный золь Варианты осаждения золя на подложке после высушивания
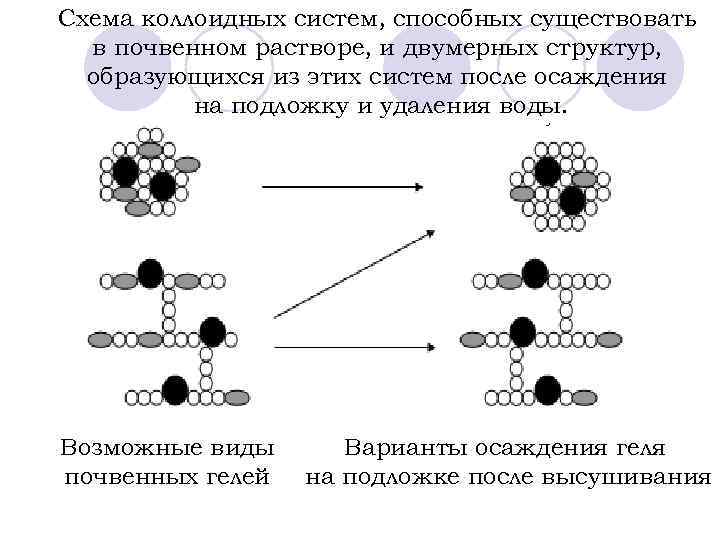 Схема коллоидных систем, способных существовать в почвенном растворе, и двумерных структур, образующихся из этих систем после осаждения на подложку и удаления воды. Возможные виды почвенных гелей Варианты осаждения геля на подложке после высушивания
Схема коллоидных систем, способных существовать в почвенном растворе, и двумерных структур, образующихся из этих систем после осаждения на подложку и удаления воды. Возможные виды почвенных гелей Варианты осаждения геля на подложке после высушивания
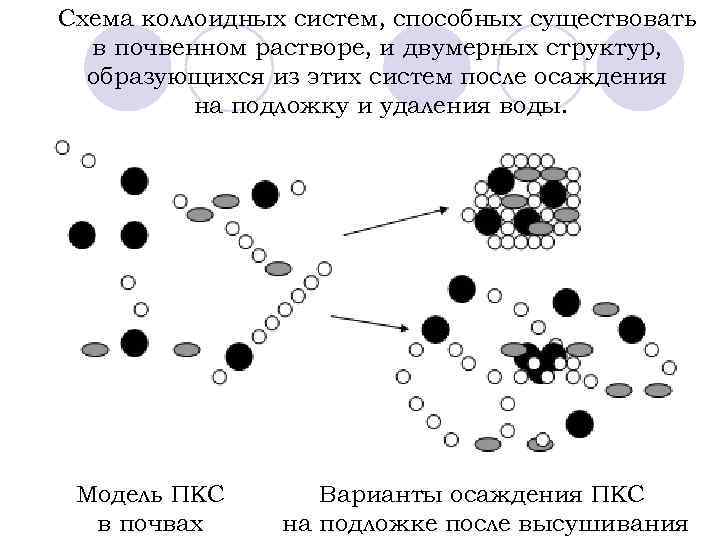 Схема коллоидных систем, способных существовать в почвенном растворе, и двумерных структур, образующихся из этих систем после осаждения на подложку и удаления воды. Модель ПКС в почвах Варианты осаждения ПКС на подложке после высушивания
Схема коллоидных систем, способных существовать в почвенном растворе, и двумерных структур, образующихся из этих систем после осаждения на подложку и удаления воды. Модель ПКС в почвах Варианты осаждения ПКС на подложке после высушивания
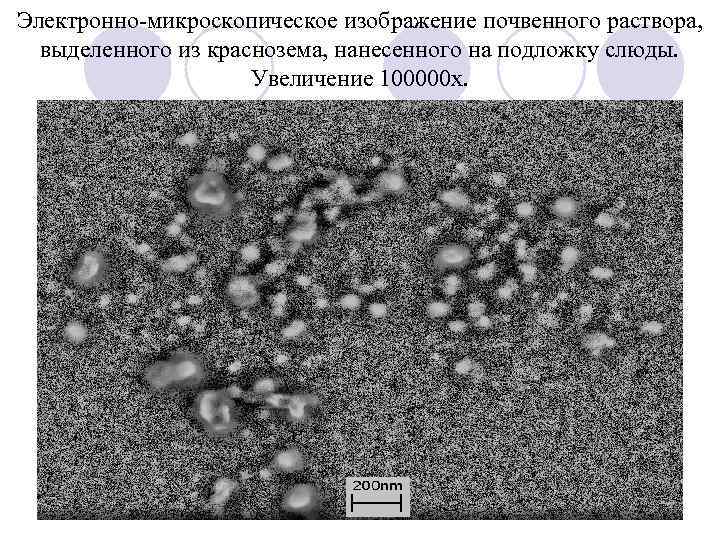 Электронно-микроскопическое изображение почвенного раствора, выделенного из краснозема, нанесенного на подложку слюды. Увеличение 100000 х.
Электронно-микроскопическое изображение почвенного раствора, выделенного из краснозема, нанесенного на подложку слюды. Увеличение 100000 х.
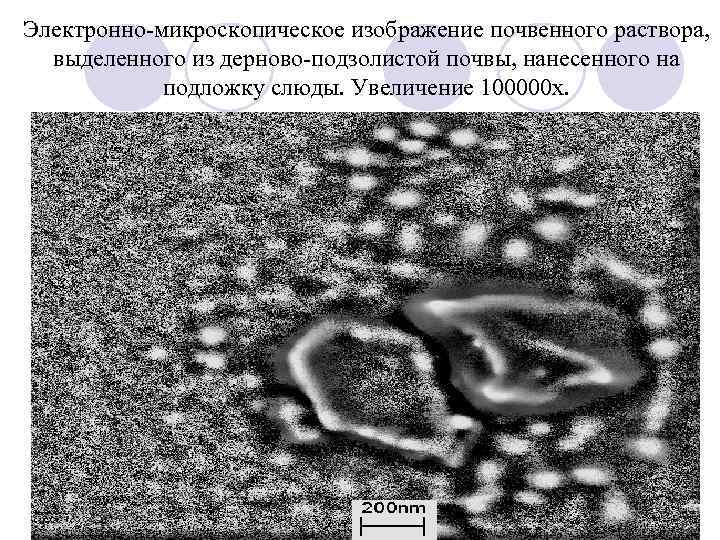 Электронно-микроскопическое изображение почвенного раствора, выделенного из дерново-подзолистой почвы, нанесенного на подложку слюды. Увеличение 100000 х.
Электронно-микроскопическое изображение почвенного раствора, выделенного из дерново-подзолистой почвы, нанесенного на подложку слюды. Увеличение 100000 х.
 Электронно-микроскопическое изображение почвенного раствора, выделенного из чернозема, нанесенного на подложку слюды. Увеличение 100000 х.
Электронно-микроскопическое изображение почвенного раствора, выделенного из чернозема, нанесенного на подложку слюды. Увеличение 100000 х.
 Электронно-микроскопическое изображение почвенного раствора, выделенного из тепличного субстрата, нанесенного на подложку слюды. Увеличение 200000 х.
Электронно-микроскопическое изображение почвенного раствора, выделенного из тепличного субстрата, нанесенного на подложку слюды. Увеличение 200000 х.
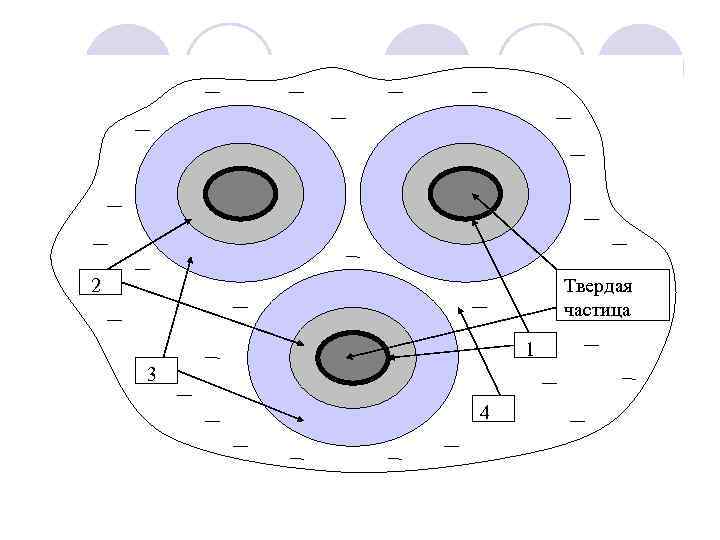 2 Твердая частица 1 3 4
2 Твердая частица 1 3 4
 Однако ряд экспериментальных данных трудно объяснить с позиций существования гелей в почвах в виде ПКС. Например, обнаруженное в середине ХХ века явление роста набухания почв при частичном окислении органического вещества перекисью водорода. На некоторых почвах набухание возрастает больше чем в 1, 5 раза. Корректного объяснения этому явлению до сих пор не существовало. Маттсоном была обнаружена зависимость давления набухания от влажности почвы: W ³√ P = const При этом науке о полимерах известна формула Позняка, связывающая давление набухания полимеров с их концентрацией в студне: Р = А×СК, где А – константа, зависящая от вида полимера, С – массовая концентрация полимера в студне, К – константа, близкая для большинства полимеров к 3.
Однако ряд экспериментальных данных трудно объяснить с позиций существования гелей в почвах в виде ПКС. Например, обнаруженное в середине ХХ века явление роста набухания почв при частичном окислении органического вещества перекисью водорода. На некоторых почвах набухание возрастает больше чем в 1, 5 раза. Корректного объяснения этому явлению до сих пор не существовало. Маттсоном была обнаружена зависимость давления набухания от влажности почвы: W ³√ P = const При этом науке о полимерах известна формула Позняка, связывающая давление набухания полимеров с их концентрацией в студне: Р = А×СК, где А – константа, зависящая от вида полимера, С – массовая концентрация полимера в студне, К – константа, близкая для большинства полимеров к 3.
 Отметим, что « С » представляет собой отношение массы полимера в студне к массе воды и полимера в студне. Предположим, что почвенный гель представляет собой студень гумуса. Применяя данное выражение к гумусовому студню почв, можно принять, что масса воды, при которой начинается набухание, заметно больше массы образующего студень полимера. В этом случае « С » определяется как отношение массы полимера в студне к массе воды в студне. В одной и той же почве количество образующего гумусовый студень полимера не зависит от влажности почвы. Следовательно: С = В × Мпочвы / Мводы, где В – константа, Мпочвы – масса абсолютно сухой почвы, Мводы – вес воды в почве.
Отметим, что « С » представляет собой отношение массы полимера в студне к массе воды и полимера в студне. Предположим, что почвенный гель представляет собой студень гумуса. Применяя данное выражение к гумусовому студню почв, можно принять, что масса воды, при которой начинается набухание, заметно больше массы образующего студень полимера. В этом случае « С » определяется как отношение массы полимера в студне к массе воды в студне. В одной и той же почве количество образующего гумусовый студень полимера не зависит от влажности почвы. Следовательно: С = В × Мпочвы / Мводы, где В – константа, Мпочвы – масса абсолютно сухой почвы, Мводы – вес воды в почве.
 Отношение массы воды в почве к массе абсолютно сухой почвы в почвоведении принято считать влажностью почвы. Подставляя полученное выражение для концентрации полимера: С=В/W в формулу Позняка и принимая К = 3 получаем: W 3× Р = А×В 3 , где А×В 3 – константа. Извлекая кубический корень получаем выражение идентичное формуле Маттсона (W ³√ P = const). Все это заставляет взглянуть на почвенные гели и с других позиций – как на системы на основе гумусового студня.
Отношение массы воды в почве к массе абсолютно сухой почвы в почвоведении принято считать влажностью почвы. Подставляя полученное выражение для концентрации полимера: С=В/W в формулу Позняка и принимая К = 3 получаем: W 3× Р = А×В 3 , где А×В 3 – константа. Извлекая кубический корень получаем выражение идентичное формуле Маттсона (W ³√ P = const). Все это заставляет взглянуть на почвенные гели и с других позиций – как на системы на основе гумусового студня.
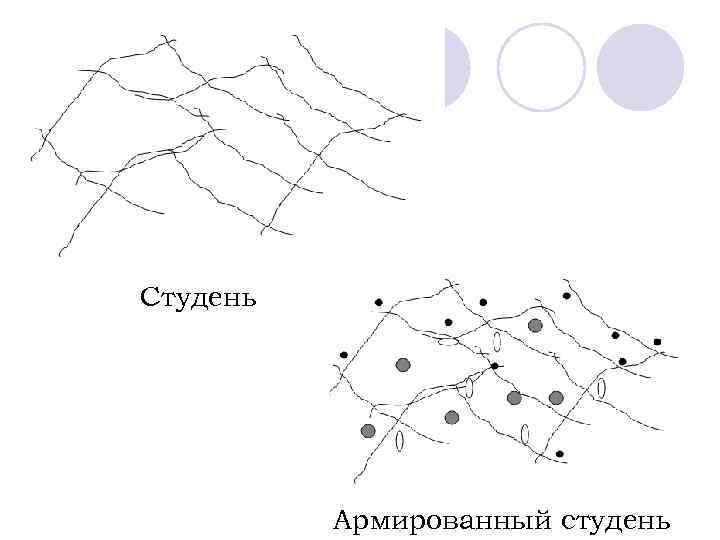 Студень Армированный студень
Студень Армированный студень
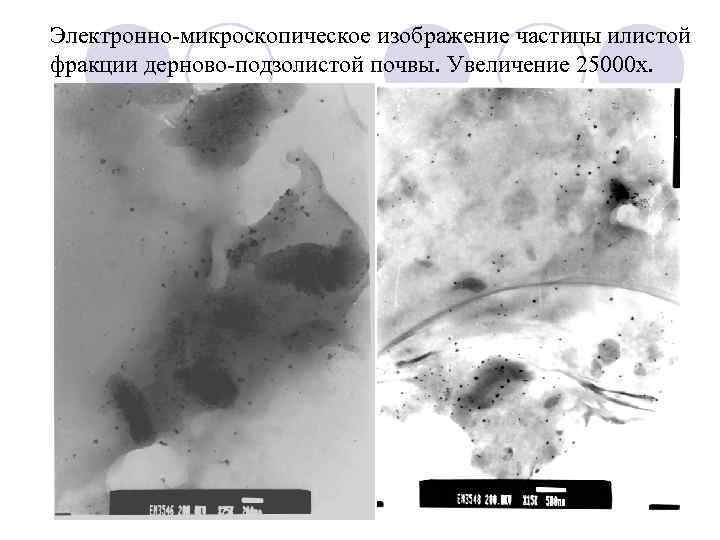 Электронно-микроскопическое изображение частицы илистой фракции дерново-подзолистой почвы. Увеличение 25000 х.
Электронно-микроскопическое изображение частицы илистой фракции дерново-подзолистой почвы. Увеличение 25000 х.
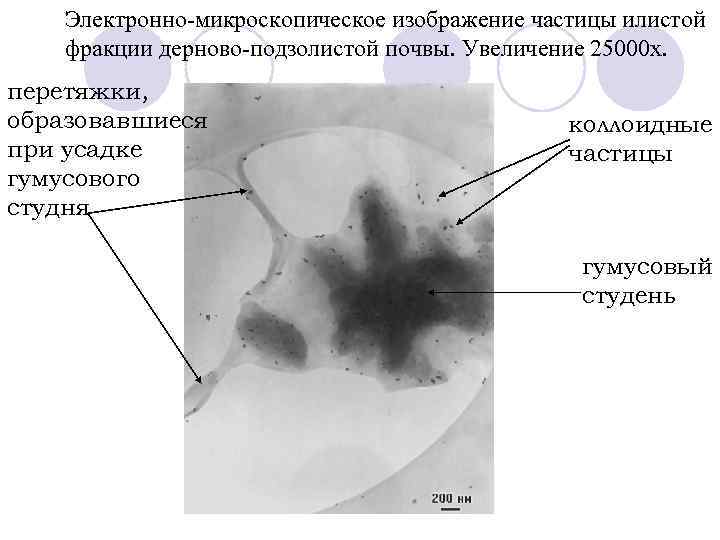 Электронно-микроскопическое изображение частицы илистой фракции дерново-подзолистой почвы. Увеличение 25000 х. перетяжки, образовавшиеся при усадке гумусового студня коллоидные частицы гумусовый студень
Электронно-микроскопическое изображение частицы илистой фракции дерново-подзолистой почвы. Увеличение 25000 х. перетяжки, образовавшиеся при усадке гумусового студня коллоидные частицы гумусовый студень
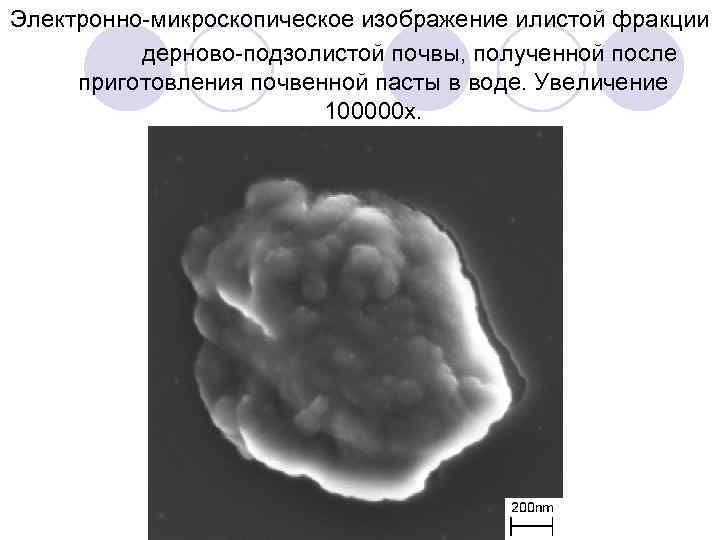 Электронно-микроскопическое изображение илистой фракции дерново-подзолистой почвы, полученной после приготовления почвенной пасты в воде. Увеличение 100000 х.
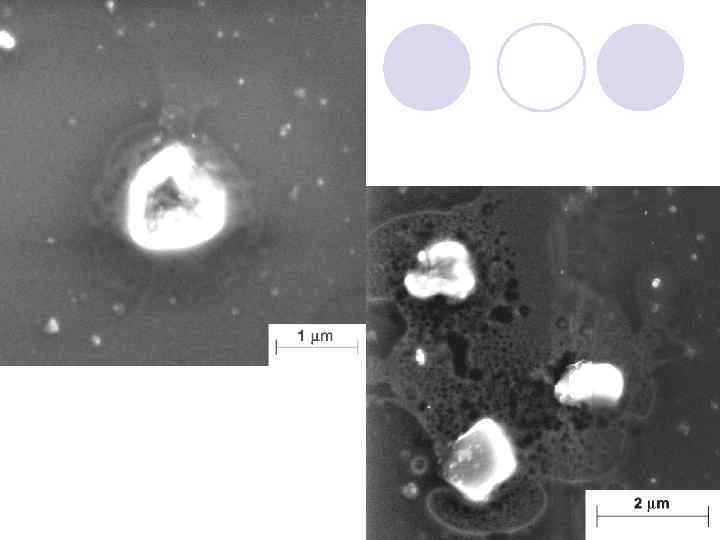
Электронно-микроскопическое изображение илистой фракции дерново-подзолистой почвы, полученной после приготовления почвенной пасты в воде. Увеличение 100000 х.
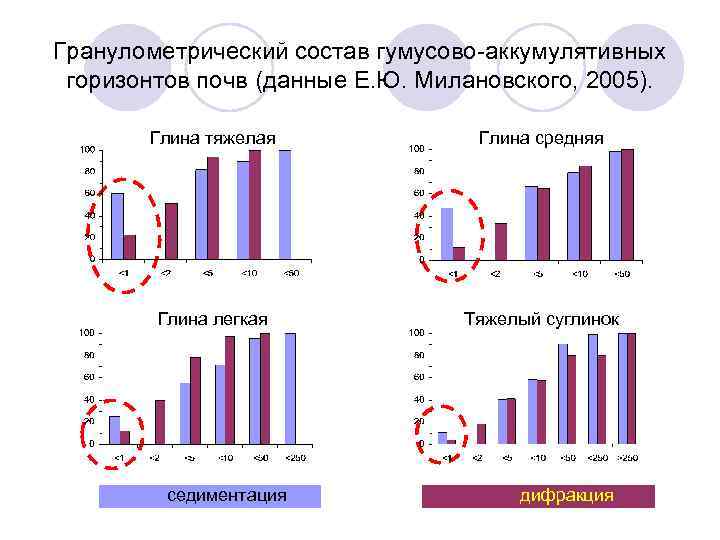 Гранулометрический состав гумусово-аккумулятивных горизонтов почв (данные Е. Ю. Милановского, 2005). Глина тяжелая Глина средняя Глина легкая Тяжелый суглинок седиментация дифракция
Гранулометрический состав гумусово-аккумулятивных горизонтов почв (данные Е. Ю. Милановского, 2005). Глина тяжелая Глина средняя Глина легкая Тяжелый суглинок седиментация дифракция
 Совершенно другую трактовку получают данные по определению гранулометрического состава почв седиментометрическим методом, которые активно используются при характеристике почв и в мелиоративных расчетах. Ранее в соответствии с законом Стокса предполагалось, что наименьшей скоростью оседания обладают частицы минимальных размеров. Наличие гелевых оболочек меняет эти представления. С наименьшей скоростью оседают частицы, у которых максимальна толщина гелевой оболочки. Так как плотность последней близка к плотности воды, то при осаждении гелевая оболочка срабатывает как парашют, искажая размеры частиц, определяемые седиментометрическим методом.
Совершенно другую трактовку получают данные по определению гранулометрического состава почв седиментометрическим методом, которые активно используются при характеристике почв и в мелиоративных расчетах. Ранее в соответствии с законом Стокса предполагалось, что наименьшей скоростью оседания обладают частицы минимальных размеров. Наличие гелевых оболочек меняет эти представления. С наименьшей скоростью оседают частицы, у которых максимальна толщина гелевой оболочки. Так как плотность последней близка к плотности воды, то при осаждении гелевая оболочка срабатывает как парашют, искажая размеры частиц, определяемые седиментометрическим методом.
 Становятся понятными экспериментальные данные по удельной поверхности почв. Известно, что удельная поверхность почв, определенная по методу адсорбции воды, на два порядка превосходит удельную поверхность, определенную методом тепловой десорбции инертных газов. С точки зрения предлагаемой модели результат абсолютно естественный. Определяемая по адсорбции почвой паров воды удельная поверхность складывается из поглощения влаги поверхностью твердых частиц и поглощения воды полимерной матрицей – растворения воды в полимерной матрице. Инертные газы не абсорбируются полимерами, а адсорбируются только твердой поверхностью. Этим объясняется расхождение результатов, но появляется вопрос о правомерности определения удельной поверхности почв с использованием веществ способных растворяться в полимерной матрице гумуса.
Становятся понятными экспериментальные данные по удельной поверхности почв. Известно, что удельная поверхность почв, определенная по методу адсорбции воды, на два порядка превосходит удельную поверхность, определенную методом тепловой десорбции инертных газов. С точки зрения предлагаемой модели результат абсолютно естественный. Определяемая по адсорбции почвой паров воды удельная поверхность складывается из поглощения влаги поверхностью твердых частиц и поглощения воды полимерной матрицей – растворения воды в полимерной матрице. Инертные газы не абсорбируются полимерами, а адсорбируются только твердой поверхностью. Этим объясняется расхождение результатов, но появляется вопрос о правомерности определения удельной поверхности почв с использованием веществ способных растворяться в полимерной матрице гумуса.



