Общая химия. Коллигативные свойства растворов.ppt
- Количество слайдов: 26
 Коллигативные свойства растворов Раствор это гомогенная система, состав которой можно непрерывно изменять в определенных пределах, и в которой имеется взаимодействие между частицами веществ. При теоретическом рассмотрении растворов вводится понятие идеальных растворов – это такие растворы, в которых энергии взаимодействия между всеми видами частиц одинаковы: Е(А–А) = Е(В–В) = Е(А–В).
Коллигативные свойства растворов Раствор это гомогенная система, состав которой можно непрерывно изменять в определенных пределах, и в которой имеется взаимодействие между частицами веществ. При теоретическом рассмотрении растворов вводится понятие идеальных растворов – это такие растворы, в которых энергии взаимодействия между всеми видами частиц одинаковы: Е(А–А) = Е(В–В) = Е(А–В).
 Термодинамика растворения G= H-T· S • Hдестр >0 Нсольв<0 Hдестр >0 Нсольв<0 • ∆Sв-ва ≥ 0 ∆Sводы <0 ∆Sв-ва ≥ 0 ∆Sводы <0
Термодинамика растворения G= H-T· S • Hдестр >0 Нсольв<0 Hдестр >0 Нсольв<0 • ∆Sв-ва ≥ 0 ∆Sводы <0 ∆Sв-ва ≥ 0 ∆Sводы <0
 • Коллигативными называются такие свойства растворов, которые зависят только от концентрации растворенных частиц и не зависят от их природы. К коллигативным (общим) свойствам растворов относятся: • понижение давления насыщенного пара над раствором по сравнению с чистым растворителем; • понижение температуры замерзания раствора; • повышение температуры кипения раствора; • осмотическое давление.
• Коллигативными называются такие свойства растворов, которые зависят только от концентрации растворенных частиц и не зависят от их природы. К коллигативным (общим) свойствам растворов относятся: • понижение давления насыщенного пара над раствором по сравнению с чистым растворителем; • понижение температуры замерзания раствора; • повышение температуры кипения раствора; • осмотическое давление.
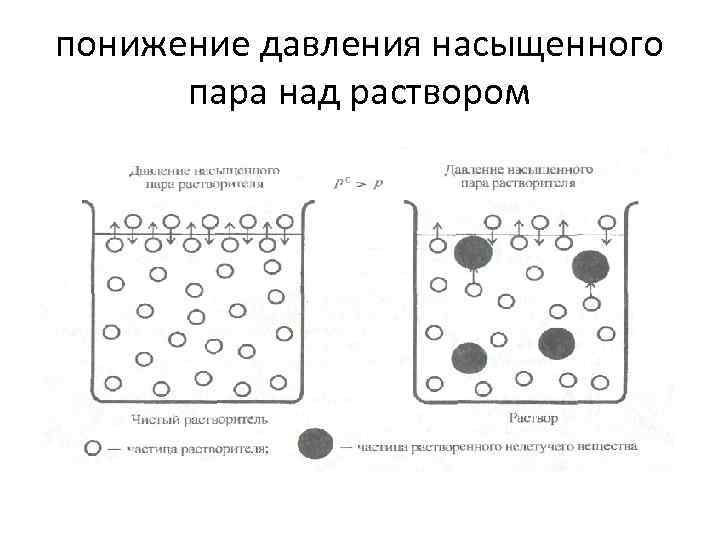 понижение давления насыщенного пара над раствором
понижение давления насыщенного пара над раствором
 закон Рауля • давление пара растворителя над раствором, содержащим нелетучее растворенное вещество, прямо пропорционально молярной доле растворителя. p = Kp x (А), • где p - давление пара над раствором, Па; Kp - константа Рауля, Па; x(А) - молярная доля растворителя А.
закон Рауля • давление пара растворителя над раствором, содержащим нелетучее растворенное вещество, прямо пропорционально молярной доле растворителя. p = Kp x (А), • где p - давление пара над раствором, Па; Kp - константа Рауля, Па; x(А) - молярная доля растворителя А.
 закон Рауля • относительное понижение давления насыщенного пара растворителя над раствором нелетучего неэлектролита равно молярной доле растворенного вещества. • • где p˚ - давление пара над чистым растворителем, p - давление пара растворителя над раствором нелетучего вещества, Па; p˚- p - абсолютное понижение давления пара над раствором, Па; (p˚- p)/p˚ - относительное понижение давления пара над раствором; x(X) - молярная доля растворенного вещества X.
закон Рауля • относительное понижение давления насыщенного пара растворителя над раствором нелетучего неэлектролита равно молярной доле растворенного вещества. • • где p˚ - давление пара над чистым растворителем, p - давление пара растворителя над раствором нелетучего вещества, Па; p˚- p - абсолютное понижение давления пара над раствором, Па; (p˚- p)/p˚ - относительное понижение давления пара над раствором; x(X) - молярная доля растворенного вещества X.
 Понижение температуры замерзания и повышение температуры кипения растворов • ΔТкип = Ткип (раствора) – Ткип (растворителя) • ΔТзам = Тзам (растворителя) - Тзам (раствора) ΔТз = K· b; ΔТк = E· b;
Понижение температуры замерзания и повышение температуры кипения растворов • ΔТкип = Ткип (раствора) – Ткип (растворителя) • ΔТзам = Тзам (растворителя) - Тзам (раствора) ΔТз = K· b; ΔТк = E· b;
 Осмос • Осмосом называется явление самопроизвольного переноса растворителя через полупроницаемую мембрану из чистого растворителя в раствор, или из раствора с меньшей концентрацией растворенного вещества в раствор с большей концентраций.
Осмос • Осмосом называется явление самопроизвольного переноса растворителя через полупроницаемую мембрану из чистого растворителя в раствор, или из раствора с меньшей концентрацией растворенного вещества в раствор с большей концентраций.
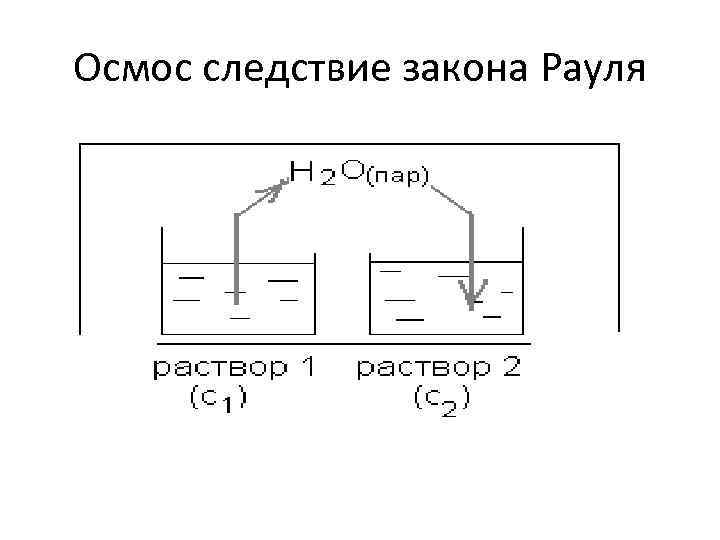 Осмос следствие закона Рауля
Осмос следствие закона Рауля
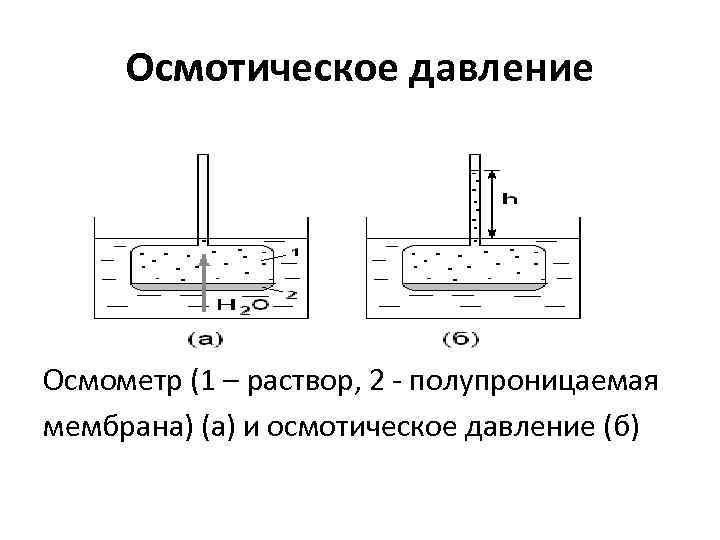 Осмотическое давление Осмометр (1 – раствор, 2 - полупроницаемая мембрана) (а) и осмотическое давление (б)
Осмотическое давление Осмометр (1 – раствор, 2 - полупроницаемая мембрана) (а) и осмотическое давление (б)
 Осмотическое давление • величина гидростатического давления столба раствора h называется осмотическое давление (обозначается π – «пи» ). • для разбавленных растворов неэлектролитов осмотическое давление рассчитывается по уравнению Вант-Гоффа π = с. RT
Осмотическое давление • величина гидростатического давления столба раствора h называется осмотическое давление (обозначается π – «пи» ). • для разбавленных растворов неэлектролитов осмотическое давление рассчитывается по уравнению Вант-Гоффа π = с. RT
 отклонения от закона Рауля и следствий для реальных растворов изотоническим коэффициентом (i) называется отношение реально наблюдаемой величины коллигативного свойства к рассчитаной: Для электролитов i > 1, что является прямым доказательством электролитической диссоциации; для неэлектролитов i = 1; для веществ, склонных к ассоциации (например, для раствора фтороводорода) i < 1.
отклонения от закона Рауля и следствий для реальных растворов изотоническим коэффициентом (i) называется отношение реально наблюдаемой величины коллигативного свойства к рассчитаной: Для электролитов i > 1, что является прямым доказательством электролитической диссоциации; для неэлектролитов i = 1; для веществ, склонных к ассоциации (например, для раствора фтороводорода) i < 1.
 отклонения от закона Рауля и следствий для реальных растворов ΔТз = i. K· b; ΔТк = i. E· b; π = iс. RT
отклонения от закона Рауля и следствий для реальных растворов ΔТз = i. K· b; ΔТк = i. E· b; π = iс. RT
 Биожидкости организма осмолярность (Сосм) Сосм (x)= ic(x) осмоляльность (Сm, осм) C m, осм (x) = i. Cm (x) Практическое определение ΔТз /K = ic(x) = Сосм (x) Осмотическому давлению крови (740 -780 к. Па) соответствует осмолярность 0, 29 - 0, 30 осмоль/л.
Биожидкости организма осмолярность (Сосм) Сосм (x)= ic(x) осмоляльность (Сm, осм) C m, осм (x) = i. Cm (x) Практическое определение ΔТз /K = ic(x) = Сосм (x) Осмотическому давлению крови (740 -780 к. Па) соответствует осмолярность 0, 29 - 0, 30 осмоль/л.
 Биожидкости организма
Биожидкости организма
 Свойства растворов электролитов • Образование ионов в растворах электролитов является результатом ионизации. Ионизация – это процесс образования свободных ионов. Разновидностями ионизации являются • – перенос протонов от молекул кислот к молекулам воды: • CH 3 COOH + H 2 O CH 3 COO– + H 3 O+ • – перенос протонов от молекул воды к молекулам оснований: • NH 3 + H 2 O NH 4+ + OH– • – растворение веществ с ионными кристаллическими структурами: • Na. Cl(кр) Na+(aq) + Cl–(aq) • – диссоциация молекул на ионы: • [Pt(NH 3)2(NO 2)Cl] + H 2 O [Pt(NH 3)2(NO 2)H 2 O] + Cl–
Свойства растворов электролитов • Образование ионов в растворах электролитов является результатом ионизации. Ионизация – это процесс образования свободных ионов. Разновидностями ионизации являются • – перенос протонов от молекул кислот к молекулам воды: • CH 3 COOH + H 2 O CH 3 COO– + H 3 O+ • – перенос протонов от молекул воды к молекулам оснований: • NH 3 + H 2 O NH 4+ + OH– • – растворение веществ с ионными кристаллическими структурами: • Na. Cl(кр) Na+(aq) + Cl–(aq) • – диссоциация молекул на ионы: • [Pt(NH 3)2(NO 2)Cl] + H 2 O [Pt(NH 3)2(NO 2)H 2 O] + Cl–
 Свойства растворов электролитов • Электролитическая диссоциация – обратимый процесс, характеризующийся константой равновесия, называемой константой ионизации.
Свойства растворов электролитов • Электролитическая диссоциация – обратимый процесс, характеризующийся константой равновесия, называемой константой ионизации.
 Свойства растворов электролитов Ионизация слабых электролитов KA K+ + A– моль/л c–αc αc αc
Свойства растворов электролитов Ионизация слабых электролитов KA K+ + A– моль/л c–αc αc αc
 Свойства растворов электролитов Ионизация слабых электролитов
Свойства растворов электролитов Ионизация слабых электролитов
 Растворы сильных электролитов Зависимость эквивалентной электропроводности от концентрации для двух электролитов разного типа c, моль/л Λ, Ом– 1·см 2·моль– 1 KCl сильный электролит 1 108, 9 CH 3 COOH слабый электролит 1, 65 0, 1 126, 0 5, 2 0, 01 138, 7 16, 2 0, 001 144, 1 49, 0 0, 0001 146, 1 134, 3 0, 00001 146, 4 277, 2 … 146, 8 390, 5
Растворы сильных электролитов Зависимость эквивалентной электропроводности от концентрации для двух электролитов разного типа c, моль/л Λ, Ом– 1·см 2·моль– 1 KCl сильный электролит 1 108, 9 CH 3 COOH слабый электролит 1, 65 0, 1 126, 0 5, 2 0, 01 138, 7 16, 2 0, 001 144, 1 49, 0 0, 0001 146, 1 134, 3 0, 00001 146, 4 277, 2 … 146, 8 390, 5
 Растворы сильных электролитов (кажущаяся степень ионизации) 0. 9% раствор Na. Cl ΔТз теор = 1. 86· 9/58. 5· 0. 991 = 0. 2888 ΔТз прак = 0. 564 I = 1. 953 α = 0. 953
Растворы сильных электролитов (кажущаяся степень ионизации) 0. 9% раствор Na. Cl ΔТз теор = 1. 86· 9/58. 5· 0. 991 = 0. 2888 ΔТз прак = 0. 564 I = 1. 953 α = 0. 953
 Активность • В растворах сильных электролитов межионное взаимодействие является главной причиной кажущегося уменьшения концентрации ионов в физико-химических свойствах раствора проявляется кажущаяся или эффективная концентрация, называемая • активностью a. • Математически она выражается следующим образом: a= f·c • где f – коэффициент активности, c – аналитическая концентрация. По мере разбавления раствора значение f приближается к единице, а активность a – к концентрации c.
Активность • В растворах сильных электролитов межионное взаимодействие является главной причиной кажущегося уменьшения концентрации ионов в физико-химических свойствах раствора проявляется кажущаяся или эффективная концентрация, называемая • активностью a. • Математически она выражается следующим образом: a= f·c • где f – коэффициент активности, c – аналитическая концентрация. По мере разбавления раствора значение f приближается к единице, а активность a – к концентрации c.
 ионная сила По теории Дебая-Хюккеля для очень разбавленных водных растворов коэффициент активности иона вычисляется по формуле где z – заряд иона, I – ионная сила раствора, определяемая как половина суммы произведений концентраций ионов на квадраты их зарядов:
ионная сила По теории Дебая-Хюккеля для очень разбавленных водных растворов коэффициент активности иона вычисляется по формуле где z – заряд иона, I – ионная сила раствора, определяемая как половина суммы произведений концентраций ионов на квадраты их зарядов:
 • Пример. Рассчитайте ионную силу растворов Ca. Cl 2 (c = 0, 0033 моль/л) и Na. Cl (c = 0, 1 моль/л). • I(Ca. Cl 2) = 0, 5(0, 0033· 22 + 0, 0066· 12) = 0, 01 • I(Na. Cl) = 0, 5(0, 1· 12 + 0, 1· 12) = 0, 1
• Пример. Рассчитайте ионную силу растворов Ca. Cl 2 (c = 0, 0033 моль/л) и Na. Cl (c = 0, 1 моль/л). • I(Ca. Cl 2) = 0, 5(0, 0033· 22 + 0, 0066· 12) = 0, 01 • I(Na. Cl) = 0, 5(0, 1· 12 + 0, 1· 12) = 0, 1
 • Пример. Вычислите активности ионов в растворе Ca. Cl 2 (c = 0, 0033 моль/л) • Ионная сила раствора вычислена выше. Коэффициенты активности находим в таблице и вычисляем активности: • a(Ca 2+) = 0, 68· 0, 0033 = 0, 00226 моль/л • a(Cl–) = 0, 90· 0, 0066 = 0, 006 моль/л
• Пример. Вычислите активности ионов в растворе Ca. Cl 2 (c = 0, 0033 моль/л) • Ионная сила раствора вычислена выше. Коэффициенты активности находим в таблице и вычисляем активности: • a(Ca 2+) = 0, 68· 0, 0033 = 0, 00226 моль/л • a(Cl–) = 0, 90· 0, 0066 = 0, 006 моль/л
 • Пример. Вычислите изотонический коэффициент хлорида кальция при концентрации раствора 0, 0033 моль/л. • Решение. В разобранном выше примере были определены активности ионов: • a(Ca 2+) = 0, 00226 моль/л; a(Cl–) = 0, 006 моль/л • Суммарная активность ионов составляет: • a(сумма) = 0, 00226 + 0, 006 = 0, 00826 моль/л • Делим активность ионов на концентрацию соли, что и дает изотонический коэффициент:
• Пример. Вычислите изотонический коэффициент хлорида кальция при концентрации раствора 0, 0033 моль/л. • Решение. В разобранном выше примере были определены активности ионов: • a(Ca 2+) = 0, 00226 моль/л; a(Cl–) = 0, 006 моль/л • Суммарная активность ионов составляет: • a(сумма) = 0, 00226 + 0, 006 = 0, 00826 моль/л • Делим активность ионов на концентрацию соли, что и дает изотонический коэффициент:


