Коллигативные свойства 2.ppt
- Количество слайдов: 27
 Коллигативные свойства растворов.
Коллигативные свойства растворов.
 Коллигативные свойства растворовэто свойства растворов, не зависящие от природы частиц растворенного вещества, а зависящие только от их концентрации. К ним относятся: 1) Понижение давления насыщенного пара(ДНП) растворителя над раствором. 2) Понижение температуры замерзания (Тз) и повышение температуры кипения (Тк) раствора. - 3) Осмотическое давление (π).
Коллигативные свойства растворовэто свойства растворов, не зависящие от природы частиц растворенного вещества, а зависящие только от их концентрации. К ним относятся: 1) Понижение давления насыщенного пара(ДНП) растворителя над раствором. 2) Понижение температуры замерзания (Тз) и повышение температуры кипения (Тк) раствора. - 3) Осмотическое давление (π).
 1 закон Рауля (1886 г) для очень разбавленных (идеальных) растворов. В изолированной (закрытой) системе, содержащей растворитель (H 2 O) устанавливается равновесие между H 2 O(ж) испарение H 2 O(пар) конденсация Когда v исп = v конд, то, пар, находящийся в равновесии с жидкостью, называют насыщенным, а его давление P°называют ДНП чистого растворителя Т P°. Для H 2 O: О°С- P° =4, 6 мм. рт. ст. 20°С – 17, 4 мм. рт. ст. 100°С- 760 мм. рт. ст. Чистая H 2 O закипает, когда P°=Рвнеш
1 закон Рауля (1886 г) для очень разбавленных (идеальных) растворов. В изолированной (закрытой) системе, содержащей растворитель (H 2 O) устанавливается равновесие между H 2 O(ж) испарение H 2 O(пар) конденсация Когда v исп = v конд, то, пар, находящийся в равновесии с жидкостью, называют насыщенным, а его давление P°называют ДНП чистого растворителя Т P°. Для H 2 O: О°С- P° =4, 6 мм. рт. ст. 20°С – 17, 4 мм. рт. ст. 100°С- 760 мм. рт. ст. Чистая H 2 O закипает, когда P°=Рвнеш
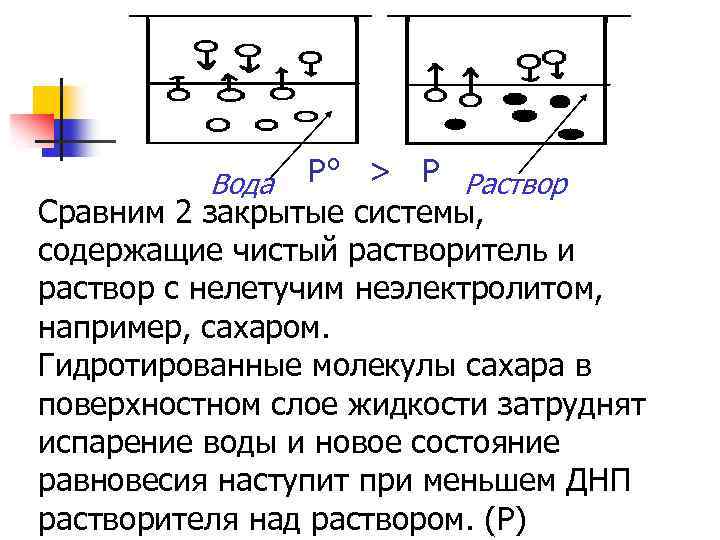 P° > Р Раствор Сравним 2 закрытые системы, содержащие чистый растворитель и раствор с нелетучим неэлектролитом, например, сахаром. Гидротированные молекулы сахара в поверхностном слое жидкости затруднят испарение воды и новое состояние равновесия наступит при меньшем ДНП растворителя над раствором. (Р) Вода
P° > Р Раствор Сравним 2 закрытые системы, содержащие чистый растворитель и раствор с нелетучим неэлектролитом, например, сахаром. Гидротированные молекулы сахара в поверхностном слое жидкости затруднят испарение воды и новое состояние равновесия наступит при меньшем ДНП растворителя над раствором. (Р) Вода
 По закону Рауля: «При постоянной температуре относительное понижение ДНП растворителя над раствором нелетучего неэлектролита равно молярной доле растворенного вещества» (N(X 2)) P° - Р n(X 2) m(x)г = N(X 2); N(X 2)= ; n(x)= , моль P° n(X 2) +n(X 1) M(x) г/моль Чем > концентрация растворенного вещества (Х 2), тем ниже Р.
По закону Рауля: «При постоянной температуре относительное понижение ДНП растворителя над раствором нелетучего неэлектролита равно молярной доле растворенного вещества» (N(X 2)) P° - Р n(X 2) m(x)г = N(X 2); N(X 2)= ; n(x)= , моль P° n(X 2) +n(X 1) M(x) г/моль Чем > концентрация растворенного вещества (Х 2), тем ниже Р.
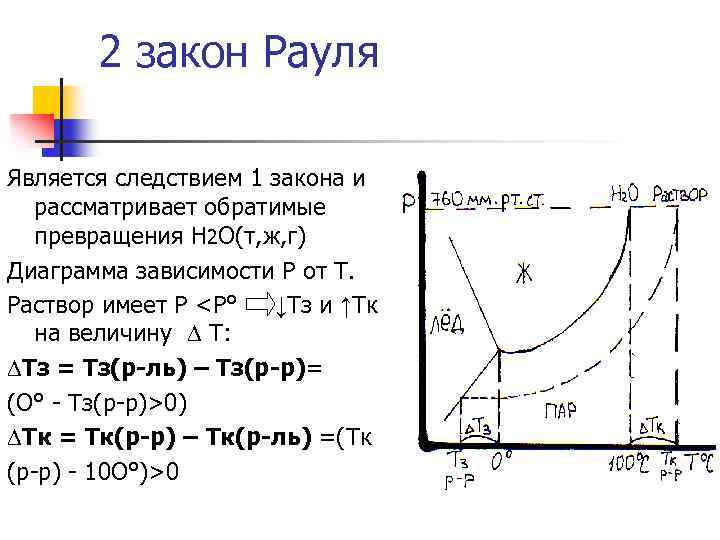 2 закон Рауля Является следствием 1 закона и рассматривает обратимые превращения H 2 O(т, ж, г) Диаграмма зависимости Р от Т. Раствор имеет Р
2 закон Рауля Является следствием 1 закона и рассматривает обратимые превращения H 2 O(т, ж, г) Диаграмма зависимости Р от Т. Раствор имеет Р
 По 2 закону Рауля: ↓∆Тз и ↑∆Тк растворов нелетучих веществ прямо пропорциональны моляльной концентрации раствора Сm. ↓∆ Тз=Кз. Сm ↑∆ Тк=Кэ. Сm , где m(x) Сm = M(x)*m(р-ль) Моляльная концентрация (Сm) равна количеству моль вещества в 1 кг растворителя;
По 2 закону Рауля: ↓∆Тз и ↑∆Тк растворов нелетучих веществ прямо пропорциональны моляльной концентрации раствора Сm. ↓∆ Тз=Кз. Сm ↑∆ Тк=Кэ. Сm , где m(x) Сm = M(x)*m(р-ль) Моляльная концентрация (Сm) равна количеству моль вещества в 1 кг растворителя;
 Кз – криоскопическая Кэ – эбулиоскопическая константы. Они зависят от природы растворителя и численно равны: Кз = ∆Тз, Кэ = ∆Тк при Сm = 1 моль/кг (физический смысл данных констант). Для H 2 O: Кз=1, 86 град. кг/моль; Кэ=0, 52 град. кг/моль
Кз – криоскопическая Кэ – эбулиоскопическая константы. Они зависят от природы растворителя и численно равны: Кз = ∆Тз, Кэ = ∆Тк при Сm = 1 моль/кг (физический смысл данных констант). Для H 2 O: Кз=1, 86 град. кг/моль; Кэ=0, 52 град. кг/моль
 Применение 2 закона Рауля Криометрия и эбулиометрия – определение молекулярной массы растворимых веществ по ↓∆Тз и ↑∆Тк Кз*m(x) г Кэ* m(x) М(х)= ∆ Тз*m(р-ль), кг ∆Тк*m(р-ль), кг -При гололеде для понижения травматизма дороги посыпают солью. Тз понижается и лед тает. - Овощи и фрукты не замерзают при температуре -1°С: при гидролизе полисахаридов число частиц (глюкозы) повышается и Тз клеточного сока понижается. -
Применение 2 закона Рауля Криометрия и эбулиометрия – определение молекулярной массы растворимых веществ по ↓∆Тз и ↑∆Тк Кз*m(x) г Кэ* m(x) М(х)= ∆ Тз*m(р-ль), кг ∆Тк*m(р-ль), кг -При гололеде для понижения травматизма дороги посыпают солью. Тз понижается и лед тает. - Овощи и фрукты не замерзают при температуре -1°С: при гидролизе полисахаридов число частиц (глюкозы) повышается и Тз клеточного сока понижается. -
 Осмос. Осмотическое и онкотическое давление. Осмос наблюдается в живой клетке, окруженной полупроницаемой мембраной, которая служит для её защиты и регуляции внутриклеточной среды. п/п мембраны м. б животными (стенки кишечника или мочевого пузыря) растительными (оболочка клетки) или искусственными (пленки целлофана, глиняные с Cu 2[Fe(CN 6)] в порах). Они пропускают молекулы воды и наглядно объясняют явление осмоса.
Осмос. Осмотическое и онкотическое давление. Осмос наблюдается в живой клетке, окруженной полупроницаемой мембраной, которая служит для её защиты и регуляции внутриклеточной среды. п/п мембраны м. б животными (стенки кишечника или мочевого пузыря) растительными (оболочка клетки) или искусственными (пленки целлофана, глиняные с Cu 2[Fe(CN 6)] в порах). Они пропускают молекулы воды и наглядно объясняют явление осмоса.
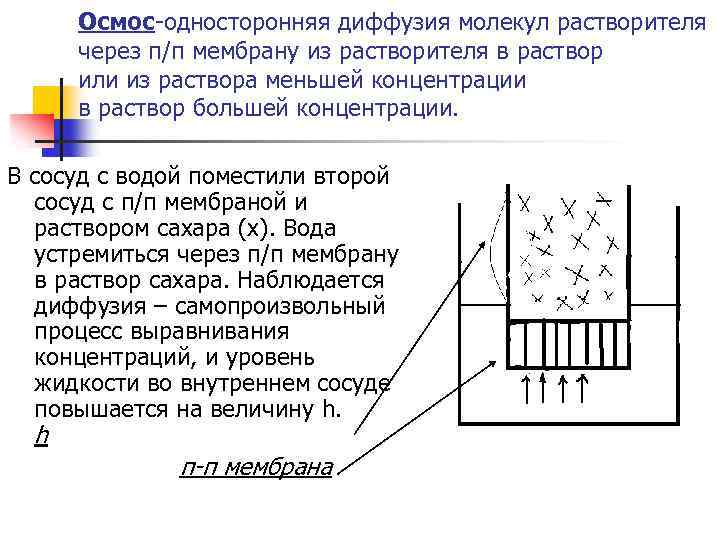 Осмос-односторонняя диффузия молекул растворителя через п/п мембрану из растворителя в раствор или из раствора меньшей концентрации в раствор большей концентрации. В сосуд с водой поместили второй сосуд с п/п мембраной и раствором сахара (х). Вода устремиться через п/п мембрану в раствор сахара. Наблюдается диффузия – самопроизвольный процесс выравнивания концентраций, и уровень жидкости во внутреннем сосуде повышается на величину h. h п-п мембрана
Осмос-односторонняя диффузия молекул растворителя через п/п мембрану из растворителя в раствор или из раствора меньшей концентрации в раствор большей концентрации. В сосуд с водой поместили второй сосуд с п/п мембраной и раствором сахара (х). Вода устремиться через п/п мембрану в раствор сахара. Наблюдается диффузия – самопроизвольный процесс выравнивания концентраций, и уровень жидкости во внутреннем сосуде повышается на величину h. h п-п мембрана
 При этом действует две силы: - - молекулы воды, проходя через п/п мембрану создают силу Р, равную π и тем >, чем > С (сахара) в растворе; столб жидкости высотой h создает гидростатическое давление (Р), действующие в противоположном направлении и тем >, чем > высота h. Осмос прекратится, когда π =Р (гидростатич. ) Вывод: π– сила, вызывающая осмос или гидростатическое давление столба жидкости высотой h, от которого прекращается осмос
При этом действует две силы: - - молекулы воды, проходя через п/п мембрану создают силу Р, равную π и тем >, чем > С (сахара) в растворе; столб жидкости высотой h создает гидростатическое давление (Р), действующие в противоположном направлении и тем >, чем > высота h. Осмос прекратится, когда π =Р (гидростатич. ) Вывод: π– сила, вызывающая осмос или гидростатическое давление столба жидкости высотой h, от которого прекращается осмос
 Закон Вант – Гоффа (1887 г) для очень разбавленных растворов. π = С(х)RТ, π не зависит от природы растворенного вещества и растворителя, а зависит от молярной концентрации растворенного вещества и Т(К). (R= 0, 083 атм. л/к. моль) - На практике π определяют по понижению Тз, т. к. в очень разбавленных растворах С(х)~Сm и ∆ Тз π = RT* Кз
Закон Вант – Гоффа (1887 г) для очень разбавленных растворов. π = С(х)RТ, π не зависит от природы растворенного вещества и растворителя, а зависит от молярной концентрации растворенного вещества и Т(К). (R= 0, 083 атм. л/к. моль) - На практике π определяют по понижению Тз, т. к. в очень разбавленных растворах С(х)~Сm и ∆ Тз π = RT* Кз
 Значение осмоса - - - Упругость, тургор клеток; Эластичность тканей, форма органов; Распределение воды между кровью, тканями, клетками; Постоянный объем крови (~5 л), у беременных женщин (~6 л), Специфические свойства биомембран клеток. Они задерживают ВМС (белки) и пропускают НМС тремя путями.
Значение осмоса - - - Упругость, тургор клеток; Эластичность тканей, форма органов; Распределение воды между кровью, тканями, клетками; Постоянный объем крови (~5 л), у беременных женщин (~6 л), Специфические свойства биомембран клеток. Они задерживают ВМС (белки) и пропускают НМС тремя путями.
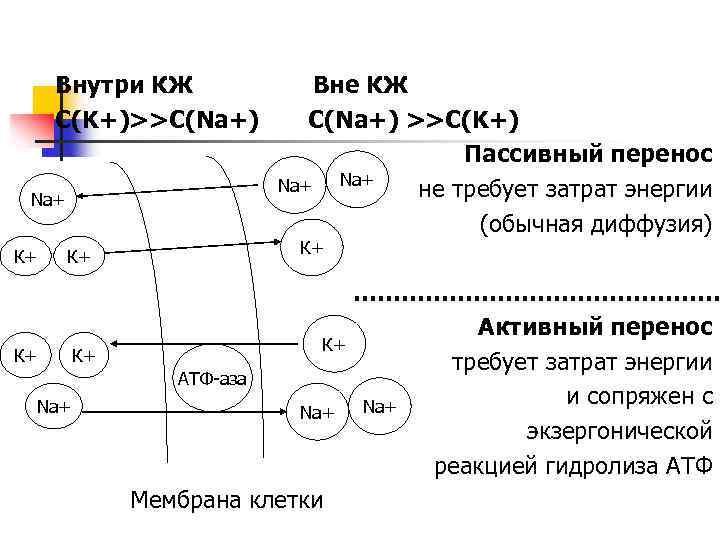 Внутри КЖ С(K+)>>С(Na+) Na+ К+ К+ К+ Na+ К+ Вне КЖ С(Na+) >>С(K+) Пассивный перенос Na+ не требует затрат энергии (обычная диффузия) К+ ……………………. Активный перенос К+ требует затрат энергии АТФ-аза и сопряжен с Na+ экзергонической реакцией гидролиза АТФ Мембрана клетки
Внутри КЖ С(K+)>>С(Na+) Na+ К+ К+ К+ Na+ К+ Вне КЖ С(Na+) >>С(K+) Пассивный перенос Na+ не требует затрат энергии (обычная диффузия) К+ ……………………. Активный перенос К+ требует затрат энергии АТФ-аза и сопряжен с Na+ экзергонической реакцией гидролиза АТФ Мембрана клетки
 Облегченный перенос в виде комплексов с белками ~5 л, состоящей из эмульсии форменных тел, невлияющих на π крови.
Облегченный перенос в виде комплексов с белками ~5 л, состоящей из эмульсии форменных тел, невлияющих на π крови.
 Осмотическое давление крови (5 л), Состоящей из истинного раствора – плазмы (3, 5 л) и эмульсии форменных тел, не влияющих на π крови. Состав плазмы: 90% H 2 O, 6 -8% белков, 0, 9 % электролитов (>Na. Cl); ~2%: липиды (0, 8%), глюкоза (0, 1%), аминокислоты и другие органические кислоты. πпл = π нмс + π вмс = (7, 7 -8, 1)атм при Т=37°С эл-ты, неэл-ты белки Uз Тз(крови)=0, 56 π пл = 0, 56/1, 86*0, 83*(273+37)=7, 65 атм
Осмотическое давление крови (5 л), Состоящей из истинного раствора – плазмы (3, 5 л) и эмульсии форменных тел, не влияющих на π крови. Состав плазмы: 90% H 2 O, 6 -8% белков, 0, 9 % электролитов (>Na. Cl); ~2%: липиды (0, 8%), глюкоза (0, 1%), аминокислоты и другие органические кислоты. πпл = π нмс + π вмс = (7, 7 -8, 1)атм при Т=37°С эл-ты, неэл-ты белки Uз Тз(крови)=0, 56 π пл = 0, 56/1, 86*0, 83*(273+37)=7, 65 атм
 π создаваемое белками плазмы, называется онкотическим давлением. π онк = 0, 03 -0, 04 атм невелико, но его роль в распределении воды между кровью и тканями значительна. При голодании, беременности, нарушении пищеварения, болезни почек концентрация плазменных белков понижается, вызывая понижение π онк. Вода поступает в ткани, и возникают онкотические отеки ( «голодные» , «почечные» ).
π создаваемое белками плазмы, называется онкотическим давлением. π онк = 0, 03 -0, 04 атм невелико, но его роль в распределении воды между кровью и тканями значительна. При голодании, беременности, нарушении пищеварения, болезни почек концентрация плазменных белков понижается, вызывая понижение π онк. Вода поступает в ткани, и возникают онкотические отеки ( «голодные» , «почечные» ).
 По отношению к π плазмы другие биожидкости можно разделить на 3 группы: 1. изотонические, π = π пл=7, 7 атм; спинно-мозговая жидкость, материнское молоко 2. гипотонические, π < π пл; слюна, моча разбавленная(после обильного питья) 3. гипертонические, π > π пл; в очаге воспаления повышается до 25 атм; моча концентрированная (утренняя) π повышается до 17 атм. π
По отношению к π плазмы другие биожидкости можно разделить на 3 группы: 1. изотонические, π = π пл=7, 7 атм; спинно-мозговая жидкость, материнское молоко 2. гипотонические, π < π пл; слюна, моча разбавленная(после обильного питья) 3. гипертонические, π > π пл; в очаге воспаления повышается до 25 атм; моча концентрированная (утренняя) π повышается до 17 атм. π
 Применение в медицине изотонических и гипертонических растворов. Изотонические растворы: 0, 9% Na. Cl (физ. раствор), раствор Рингера и другие заменители крови – при обезвоживании, кровопотерях, 5% раствор глюкозы вводят в/в в больших количествах. Гипертонические растворы: - 10% Na. Cl наружно ввиде марлевых повязок для оттока гноя из раны; - 10%Ca. Cl 2 при аллергических отеках, кровотечениях; - 20%, 40% глюкоза при глаукоме, отеке мозга. Чтобы избежать «осмотического конфликта» такие растворы вводят в/в очень медленно и в небольших количествах.
Применение в медицине изотонических и гипертонических растворов. Изотонические растворы: 0, 9% Na. Cl (физ. раствор), раствор Рингера и другие заменители крови – при обезвоживании, кровопотерях, 5% раствор глюкозы вводят в/в в больших количествах. Гипертонические растворы: - 10% Na. Cl наружно ввиде марлевых повязок для оттока гноя из раны; - 10%Ca. Cl 2 при аллергических отеках, кровотечениях; - 20%, 40% глюкоза при глаукоме, отеке мозга. Чтобы избежать «осмотического конфликта» такие растворы вводят в/в очень медленно и в небольших количествах.
 ● Na 2 SO 4*10 H 2 O(глауберова соль), Mg. SO 4*4 H 2 O(горькая соль) обладает слабительным действием, из-за их плохой всасываемости кишечный сок становится гипертоничным (π ), вода поступает в кишечник, оказывая слабительное действие. ● В быту при заготовке овощей и фруктов используют рассол (Na. Cl) и сахарный сироп. Они обладают стойким плазмолизом, и микроорганизмы погибают.
● Na 2 SO 4*10 H 2 O(глауберова соль), Mg. SO 4*4 H 2 O(горькая соль) обладает слабительным действием, из-за их плохой всасываемости кишечный сок становится гипертоничным (π ), вода поступает в кишечник, оказывая слабительное действие. ● В быту при заготовке овощей и фруктов используют рассол (Na. Cl) и сахарный сироп. Они обладают стойким плазмолизом, и микроорганизмы погибают.
 Гемолиз и плазмолиз эритроцитов в растворах Na. Cl разной концентрации. c 1=c 2 (наруж. ) c 1>c 2 c 1
Гемолиз и плазмолиз эритроцитов в растворах Na. Cl разной концентрации. c 1=c 2 (наруж. ) c 1>c 2 c 1
 n n В гипотоническом растворе осмос воды в клетку, где c и π >. Происходит «осмотический шок» гемолиз эритроцитов: клетка набухает, π увеличивается, оболочка разрывается и гемоглобин выливается в плазму. Образуется прозрачная «лаковая» кровь. Полный гемолиз при π =2, 5 -3 атм. В гипертоническом растворе осмос воды из клетки в раствор, где c и π >. Наблюдается плазмолиз – дегидратация, сжатие, высушивание клетки.
n n В гипотоническом растворе осмос воды в клетку, где c и π >. Происходит «осмотический шок» гемолиз эритроцитов: клетка набухает, π увеличивается, оболочка разрывается и гемоглобин выливается в плазму. Образуется прозрачная «лаковая» кровь. Полный гемолиз при π =2, 5 -3 атм. В гипертоническом растворе осмос воды из клетки в раствор, где c и π >. Наблюдается плазмолиз – дегидратация, сжатие, высушивание клетки.
 Коллигативные свойства растворов электролитов, диссоциирующих на ионы, и число частиц в растворе увеличивается. Вант-Гофф ввел поправочный изотонический коэффициент (i): Σ всех частиц в р-ре(ионы, молекулы) i= первоначальное число молекул У электролитов i >1; у неэлектролитов i=1.
Коллигативные свойства растворов электролитов, диссоциирующих на ионы, и число частиц в растворе увеличивается. Вант-Гофф ввел поправочный изотонический коэффициент (i): Σ всех частиц в р-ре(ионы, молекулы) i= первоначальное число молекул У электролитов i >1; у неэлектролитов i=1.
 С учетом степени диссоциации (α) и n-числа ионов из 1 молекулы электролита: i=1+α (n-1) Для бинарных электролитов(n=2 иона): Na. Cl, Na. HCO 3, Mg. SO 4 i= 1+ α Для тринарных электролитов(n=3 иона): Na 2 SO 4, Ca. Cl 2, Na 2 HPO 4 i=1+2 α При сильном разбавлении сильных электролитов α → 1, отсюда i (Na. Cl)=2; i (Ca. Cl 2) =3
С учетом степени диссоциации (α) и n-числа ионов из 1 молекулы электролита: i=1+α (n-1) Для бинарных электролитов(n=2 иона): Na. Cl, Na. HCO 3, Mg. SO 4 i= 1+ α Для тринарных электролитов(n=3 иона): Na 2 SO 4, Ca. Cl 2, Na 2 HPO 4 i=1+2 α При сильном разбавлении сильных электролитов α → 1, отсюда i (Na. Cl)=2; i (Ca. Cl 2) =3
 На практике i определяют по ↓Тз, ↑Тк, изменению ∆ Тз(прак) i= = π: π(прак) ∆ Тк(прак) = ∆ Тз(теор) ∆Тк(теор) π(теор) В числителе экспериментальные данные для электролитов, а в знаменателе – неэлектролитов той же концентрации. Законы Рауля и Вант-Гоффа для электролитов: P°-Р =i. N(X 2); P° ∆Тз=i. Кз. Сm; ∆Тк=i. Кэ. Сm; π =ic(X)RТ
На практике i определяют по ↓Тз, ↑Тк, изменению ∆ Тз(прак) i= = π: π(прак) ∆ Тк(прак) = ∆ Тз(теор) ∆Тк(теор) π(теор) В числителе экспериментальные данные для электролитов, а в знаменателе – неэлектролитов той же концентрации. Законы Рауля и Вант-Гоффа для электролитов: P°-Р =i. N(X 2); P° ∆Тз=i. Кз. Сm; ∆Тк=i. Кэ. Сm; π =ic(X)RТ
 Например, рассчитайте π(0, 9%Na. Cl) при 37°С. Решение: 1)По формуле ω%(X)*10ρ 0, 9*10*1 С(Х)= = =0, 15 моль/л M(X) 58, 5 π =ic(x)RT=2*0, 15*0, 83*310=7, 65 атм Вывод: π(0, 9% Na. Cl)= π пл=7, 65 атм при 37°С, 2) т. е. изотоничен плазме.
Например, рассчитайте π(0, 9%Na. Cl) при 37°С. Решение: 1)По формуле ω%(X)*10ρ 0, 9*10*1 С(Х)= = =0, 15 моль/л M(X) 58, 5 π =ic(x)RT=2*0, 15*0, 83*310=7, 65 атм Вывод: π(0, 9% Na. Cl)= π пл=7, 65 атм при 37°С, 2) т. е. изотоничен плазме.


