Коллекция учебных динамических слайдов по химии


Коллекция учебных динамических слайдов по химии 8 класс.

1/22/201 8 Содержание: 1. Химический элемент. 2. Тренировочный материал для изучения знаков химических элементов. 3. Чтение химических формул. 4. Валентность. 5. Орбитально – планетарное модель строение атома. 6. Строение электронной оболочки. (Часть 1) 7. Строение электронной оболочки. (Часть 2) 8. Ионы и ионная химическая связь. Далее 9. Ковалентная неполярная связь. Содержание Назад 10. Ковалентная полярная связь. 2

1/22/201 8 Содержание: 11. Молярный объем газов. 12. Степень окисления. 13. Классификация неорганических веществ. 14. Кристаллические решетки. 15. Чистые вещества и смеси. 16. Уравнения химических реакций. 17. Составление уравнений химических реакций. 18. Скорость химической реакции. 19. Прибор для определения электролитов. 20. Реакции ионного обмена. Далее Содержание 21. Условия протекания реакций ионного обмена. Назад 3

1/22/201 8 Содержание: Примечание. Далее Содержание Назад 4
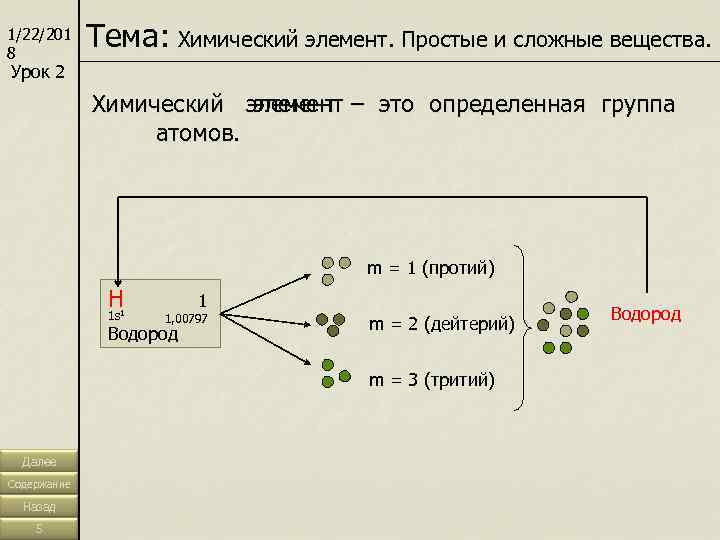
1/22/201 8 Тема: Химический элемент. Простые и сложные вещества. Урок 2 Химический элемент – это определенная группа Химический элемент атомов. m = 1 (протий) Н 1 s 1 1, 00797 Водород m = 2 (дейтерий) Водород m = 3 (тритий) Далее Содержание Назад 5

Тема: Mn Mg Ca Cu Br Al Se 1/22/201 Строение периодической системы. Знаки Ag Hg IFb B Na Au F K O P Ha 8 Cl Zn C N Si Урок 5 -6 химических элементов. Тренировочный материал к Сейчас на экране будут изучению знаков знаки появляться химических элементов. химических элементов. Четко и правильно проговаривай название и произношение химического элемента. Желаю тебе удачи! Далее Содержание Назад 6

1/22/201 8 Тема: Химические формулы. Урок 7 Чтение химических формул. Примеры: 1. NH 3 – молекула эн аш три состоит из одного атома азота и трех атомов водорода. 2. Al(OH) 3 – молекула алюминий о аш трижды состоит из одного атома алюминия , трех атомов кислорода и трех атомов водорода. 3. K 3 BO 3 – молекула калий три бор о три состоит из трех атомов калия, одного атома бора и трех атомов кислорода. Далее Содержание C 8 HO)3 PO 4 Al. Cl. SO 442 (NH 183 3 Na 4 Ba. CO Fe 2 5 P 2 O 3 Zn. Mn. O CH 23 COOH Pb. Si. O KHCO Ag. NO Ca(OH) Назад 7

1/22/201 8 Тема: Валентность. Урок 11 Составление химических формул по валентности. Правило нахождения валентности: - У металла валентность ставится по номеру группы. - У неметалла, стоящего на первом месте в формуле, ставится высшая валентность. - У неметалла, стоящего на втором месте в формуле, ставится низшая валентность. Пример: Порядок действий: 10 2 6 1. Находим валентность химических элементов. 2. Находим наименьшее общее V I VI II кратное. P Na O S O 3. Находим индексы. : ==21 2 Далее Содержание : =15 3 Назад 8
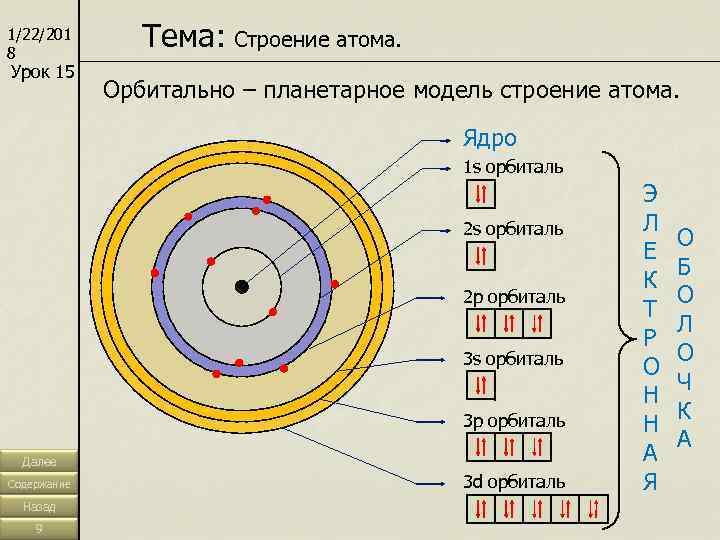
1/22/201 8 Тема: Строение атома. Урок 15 Орбитально – планетарное модель строение атома. Ядро 1 s орбиталь Э 2 s орбиталь Л О Е Б К 2 p орбиталь О Т Л Р 3 s орбиталь О Ч Н К 3 p орбиталь Н А Далее А Содержание 3 d орбиталь Я Назад 9

1/22/201 8 Тема: Строение электронных оболочек атомов. Урок 17 Электронная оболочка – это совокупность электронов, двигающихся вокруг ядра атома. Электроны в электронной оболочке Номер периода совпадает с числом Номер группы совпадает с числом электронов на Число электронов (N) на уровне рассчитывается n – главное квантовое число – определяет число располагаются на энергетических уровнях. энергетических уровней элемента. последнем энергетическом уровне. по формуле. энергетических уровней. N = 2 n 2 Период Группа n = 1, N = 2. 12 = 2 V 5 n = 2, N = 2. 22 = 8 8 3 Р 15 30, 9748 Общее число электронов е = Фосфор Проверка Далее 15 Содержание Назад 10

1/22/201 8 Тема: Строение электронных оболочек атомов. Урок 18 - Энергетический уровень состоит из орбиталей. - Орбиталь состоит из квантовых ячеек. - На одной квантовой ячейке могут находиться два электрона с разными спинами. Первый уровень 3 d 0 Р 31 0 s – орбиталь 3 p 3 +15 Второй уровень 3 s 2 2 8 5 s – орбиталь 2 p 6 p – орбиталь 2 s 2 - квантовая ячейка Третий уровень 1 s 2 s – орбиталь - Краткая электронная запись. p – орбиталь Далее d – орбиталь Содержание Назад 11

1/22/201 8 Тема: Ионы и ионная химическая связь. Урок 20 Химическая связь, образующуюся между ионами, называется ионной. Ион – это частица образующаяся в результате отдачи или принятия электрона. Пример: Ионная связь как правило возникает между металлом и неметаллом. Na. Cl – хлорид натрия (поваренная, пищевая соль) 23 Na 0 ++17 Cl Механизм: 35 0 23 +1 Na 35 Cl -1 +11 Na. Cl 2 8 1 2 8 7 +11 2 8 -1 +17 2 8 8 ион натрия ион хлора Na 1 e + Cl Na Cl Далее 0 +1 -1 Содержание Назад Na + Cl Na Cl 12
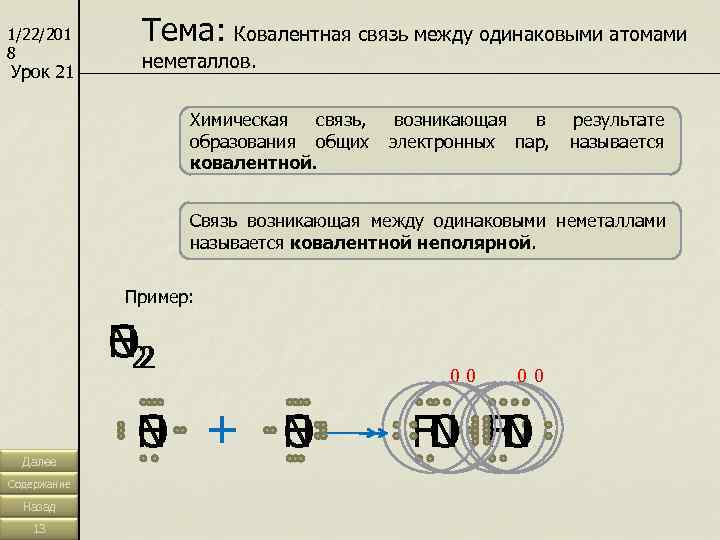
1/22/201 Тема: Ковалентная связь между одинаковыми атомами 8 неметаллов. Урок 21 Химическая связь, возникающая в результате образования общих электронных пар, называется ковалентной. Связь возникающая между одинаковыми неметаллами называется ковалентной неполярной. Пример: N O F 2 Н 2 00 00 Далее Н + Н N O FO FO Н Н N N Содержание Назад 13

1/22/201 8 Тема: Ковалентная полярная химическая связь. Урок 22 Химическая связь, возникающая в результате образования общих электронных пар, называется ковалентной. Ряд неметаллов. Связь возникающая между разными неметаллами F, O, N, Cl, Br, S, C, P, Si, H. называется ковалентной полярной. Электроотрицательность (ЭО) – это способность ЭО уменьшается NН О NН 3 Пример: атомов химического элемента притягивать к себе Н 2 электроны. НCl с большей ЭО, при образовании ковалентной Элемент +δ + δ - δ - δ + δ полярной связи, приобретает частично отрицательный + δ + заряд (- δ). + Н О Н - δ Н Nковалентной + связи, приобретает частично положительный Н Cl + δ Элемент с меньшей ЭО, при образовании Н полярной + δ Н Далее заряд (+ δ). Содержание Назад 14

1/22/201 8 Тема: Молярный объем газов. Урок 31 Молярный объем (Vm) (л/моль). V N m M = Mr Vm – буквенное обозначение молярного объема II. Задача. – единицы измерения NA л/моль Vm n n M n Определите массу 89, 6 л аммиака (NH 3) Молярный объем – это объем занимаемый 1 молем любого газа при нормальных условиях (22, 4 л/моль). Дано: Решение: V(NH– объем (л) 1. n(NH ) - ? V ) = 89, 6 л 3 n = 3 n – количество вещества (моль) Vm 89, 6 л Нормальные условия (н. у. ) – Т = 0 о. С ; = 4 моль m(NH 3) = ? n(NH 3) = 22, 4 л/моль Р = 760 мм рт. ст. (101, 3 к. Па) 2. M(NH 3) - ? M = Mr V Mr(NH 3) = Ar(N) + 3. Ar(H) = 14 + 3. 1 = 17 = = x M(NH 3) = 17 г/моль Далее 3. m(NH 3) = ? m = M. n m(NH 3) = 17 г/моль . 4 моль = 61 г Содержание Vm n Назад Ответ: m(NH 3) = 61 г 15

1/22/201 8 Тема: Степень окисления. Урок 34 Степень окисления – это заряд приобретаемый элементом в соединении, в результате полной отдачи или принятия электрона. Правила: 1. Степень окисления элемента в простом веществе равна 0. H 20 ; O 20 ; F 20 ; Cl 20 ; Ca 0. 2. Степень окисления некоторых элементов в соединении: H+1; О-2; Na+1 ; K+1 ; Ca+2 ; Mg+2 ; Ba+2 ; Al+3. - H+1 - О-2 Пример: 2. (+1) + Х + 3. (-2) = 0 - степень окисления металла совпадает с его валентностью: H 2 СO 3 Na+1 ; K+1 ; Ca+2 ; Mg+2 ; Ba+2 Х - 6 = 0 2 + ; Al . Х = +4+4 +3 3. Сумма степеней окисления элементов в соединении, с учетом коэффициентов, равна 0. 3. Составляем и решаем уравнение. Правило пока ее не 2. Расставляем степени окисления элементов, 1. Степень окисления элемента, у которого 3. которые Далее можем определить , обозначим за X можем определить по правилу 2. Х H ; О Содержание +1 -2 Назад 16
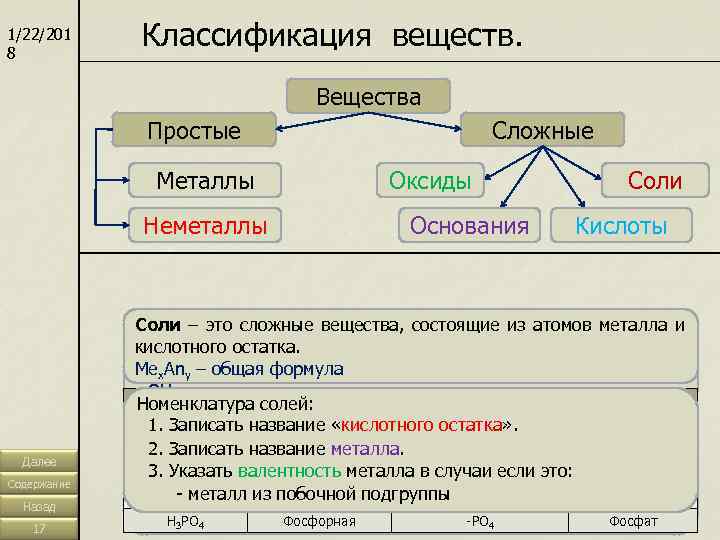
1/22/201 8 Классификация веществ. Вещества Простые Сложные Металлы Оксиды Соли Неметаллы Основания Кислоты Соли – это сложные вещества, состоящие из атомов металла и Кислоты – – это сложные вещества, состоящие из атомов Основания это сложные вещества, состоящие из Оксиды – это сложные вещества, состоящие из двух элементов, кислотного остатка. водорода и кислотного остатка. металла и гидроксогрупп. один из которых кислород. Эх. Оу – общая формула. Mex. Any – общая формула Hx. An – общая формула Me(ОH)x – общая формула - OH - гидроксогруппа Номенклатура оксидов: Номенклатура солей: Формула Название Кислотный остаток Название 1. Записать название «кислотного остатка» . Номенклатура оснований: 1. Записать слово «оксид» . HCl Соляная -Cl Хлорид 1. Записать слово «гидроксид» . 2. Записать название металла. 2. Записать название элемента. -NO 3 HNO 3 Азотная Нитрат Далее 2. Записать название металла. 3. Указать валентность элемента в случаи если это: 3. Указать валентность металла в случаи если это: Сульфат H 2 SO 4 Серная -SO 4 Содержание 3. Указать валентность металла в случаи если это: Карбонат H- металл из побочной подгруппы -CO 3 2 CO 3 - неметалл. Угольная Назад H 3 PO 4 - металл из побочной подгруппы 4 - металл из побочной подгруппы-PO Фосфорная Фосфат 17
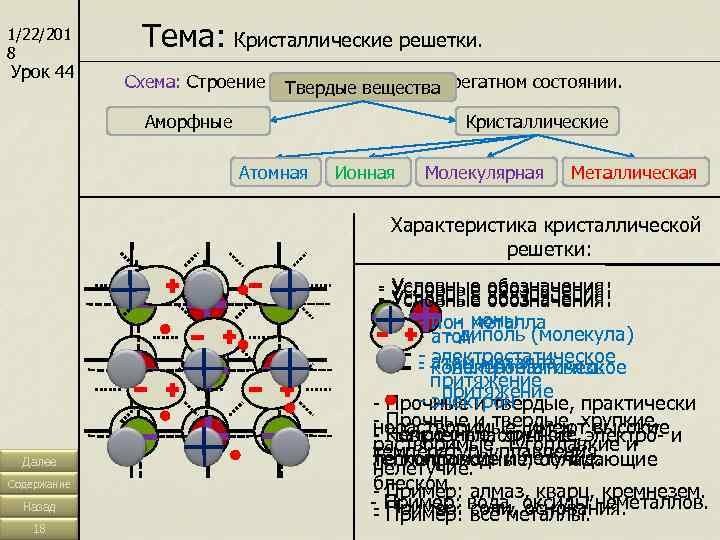
1/22/201 8 Тема: Кристаллические решетки. Урок 44 Схема: Строение веществ в твердом агрегатном состоянии. Твердые вещества Аморфные Кристаллические Атомная Ионная Молекулярная Металлическая Характеристика кристаллической решетки: - Условные обозначения: - ионы - ион металла - диполь (молекула) - атом - электростатическое - атом металла - электростатическое - ковалентная связь притяжение - электрон - Прочные и твердые, практически - Прочные и твердые, хрупкие, нерастворимые, имеют высокие - Непрочные, хрупкие, - Ковкие, пластичные, электро- и растворимые, тугоплавкие и температуры плавления. Далее легкоплавкие и летучие. теплопроводные, обладающие нелетучие. Содержание блеском. - Пример: алмаз, кварц, кремнезем. Назад - Пример: вода, оксиды неметаллов. - Пример: соли, основания. - Пример: все металлы. 18
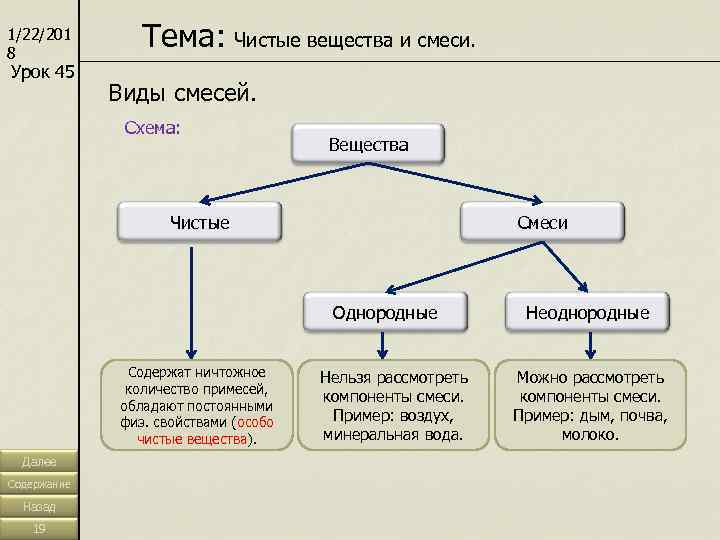
1/22/201 8 Тема: Чистые вещества и смеси. Урок 45 Виды смесей. Схема: Вещества Чистые Смеси Однородные Неоднородные Содержат ничтожное Нельзя рассмотреть Можно рассмотреть количество примесей, компоненты смеси. обладают постоянными физ. свойствами (особо Пример: воздух, Пример: дым, почва, чистые вещества). минеральная вода. молоко. Далее Содержание Назад 19

1/22/201 8 Тема: Уравнения химических реакций. Урок 58 Уравнение химической реакции – это условная запись химического процесса, посредством химических знаков и символов. Пример: N 2 ; + H 2 t 0 C кат. NH 3 - реагирующие вещества - продукты реакции - взаимодействие - условие протекания реакции Далее Содержание Назад 20

1/22/201 СОСТАВЛЕНИЕ УРАВНЕНИЙ ХИМИЧЕСКИХ РЕАКЦИЙ 8 Пример: Составить уравнение реакции взаимодействия фосфора и кислорода. 9. Определи: есть ли еще не уравненные (не соединенные) 1. В левой части уравнения запиши формулы веществ, 3. Определи: атомов, какого элемента в левой части атомы: которые вступают чисел атомов в левой и правой частях 7. В правой части в реакцию. (Формулы простых 5. Раздели Н. О. К. на число атомов каждого соединенного 4. Соедини фигурной стрелкой атомы этого элемента в левой 2. Определи Н. О. К. уравнения запиши формулы веществ 8. Запиши полученный коэффициент перед формулой. 6. Запиши Н. О. К. в квадратике под стрелкой. уравнения больше. (Вначале уравнивают число атомов, газообразных веществ состоят из двух атомов: Н 2 , О 2 , N 2 , Cl 2 а) Если есть, то вернись к пункту 3. элемента. уравнения. и правой частях. образующихся в результате реакции. которых в левой части уравнения больше. ) и. т. д. ) б) Если нет, то ВСЁ. 4 : 1= 4 4 : 4= 1 4 P + 5 O 2 = 2 P 2 O 5 Материал взят из презентации Лебедева Сергея Николаевича ГОУ школа-интернат V-VI вида. Костромской области. Далее Содержание 10 : 2 = 5 10 : 5 = 2 Назад 21
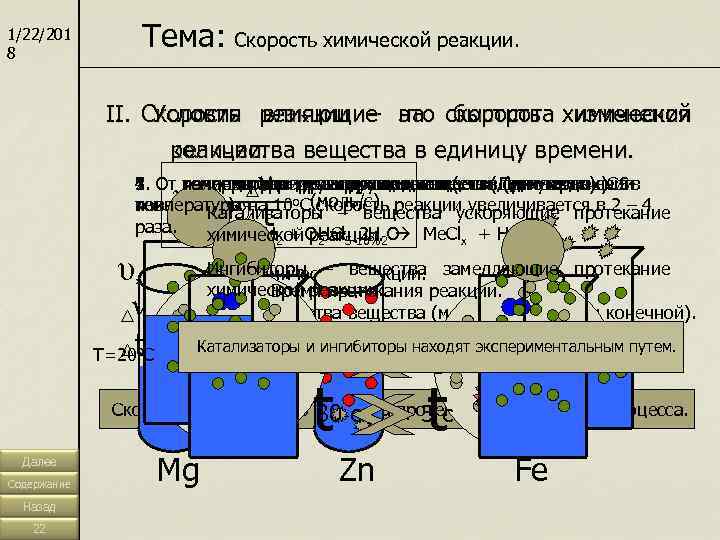
1/22/201 8 Тема: Скорость химической реакции. II. Условия влияющие это быстрота изменения I. Скорость реакции – на скорость химической реакции. количества вещества в единицу времени. ν 5. От наличия определенных веществ. 4. От температуры реагирующих веществ. При увеличении 3. От поверхности реагирующих веществ (для твердых). S- 2. От концентрации реагирующих веществ (для газов). С- 1. От природы реагирующих веществ (если одно из веществ υ х. р. = (моль/с) температуры на 10 о. С скорость реакции увеличивается в 2 – 4 поверхность. концентрация неизвестно). раза. t Катализаторы – вещества ускоряющие протекание химической реакции. О 2 H + О 2 H Ме. Cl + H Ме + HCl 2 2 5 -10% 2 x 2 υ х. р. - Скорость химической реакции. замедляющие протекание Ингибиторы – вещества химической реакции. Время протекания реакции. ν - Разность количества вещества (между начальной и конечной). Т=20 о t t. С - Разность времени (между конечным и начальным). Т=50 С Время протекания Катализаторы и ингибиторы находят экспериментальным путем. 30 сек реакции. 10 сек о 30 с t 5 с t Скорость реакции – это быстрота протекания химического процесса. Далее Содержание Mg Zn Fe Назад 22
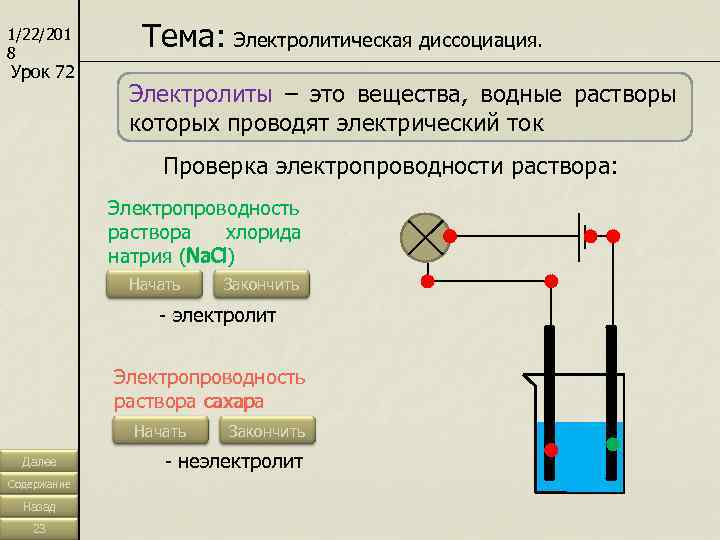
1/22/201 8 Тема: Электролитическая диссоциация. Урок 72 Электролиты – это вещества, водные растворы которых проводят электрический ток Проверка электропроводности раствора: Электропроводность раствора хлорида Na. Cl натрия (Na. Cl) Начать Закончить - электролит Электропроводность раствора сахара сахар Начать Закончить Далее - неэлектролит Содержание Назад 23

1/22/201 8 Тема: Реакции ионного обмена. РИО ( реакции ионного обмена ) – это реакции протекающие между электролитами. Пример: Взаимодействие хлорида бария с сульфатом натрия. Порядок действий: 2. Расставить коэффициенты. 1. Записать уравнение реакции в молекулярном виде. 6. Составить сокращенное ионное уравнение. 5. Сократить одинаковые ионы в левой и правой части полного 4. Составить полное ионное уравнение (растворимые вещества 3. По таблице растворимости, определить нерастворимые вещества ионного уравнения. расписать на ионы. Обозначить их стрелкой вниз. Ba. Cl 2 + Na+SO 42 - Ba 2+ - 2 Cl 2 Na 2 Ba. SO 4 + Na. Cl Ba. SO 2 Na+ 2 2 Cl- Ba 2+ + + SO 42 - Ba. SO 4 + Далее Содержание Назад 24

1/22/201 8 Тема: Условия протекания реакций ионного обмена. II. Если образуется газ. I. Если образуется осадок. H 2 O 2 Na 2 CO 3 -2 - 2 H+SO 42 -2 - 2 Na+SO 42 - 2 2 CO 3 Na +2 Cl 3 + H 2 +SO Na 2 Ba. Cl 2 + Na 2 4 Ba. SO 4 + H 2 Cl- Ba 2+ 2 Na Ba. SO + Na. Cl CO 2 2 Na+ Ba 2+ + CO 3 + 2 H + SO 42 - Ba. SO 4 + + H 2+ + CO 2 O 2 - + + + + III. Если образуется вода. Mg(NO 3)2 H+SO Na + Mg. CO 3 + Na. NO 3 Mg 2 NO - 2 + Na+CO 3 Mg. CO O 2 2 NO 3 - 2 Na 2 OH 2+ 2 Na. OH + H + - 2 Na 2 2 Na SO + 2 H 2 Na+ 2 - 3 2 - 2 H 2 4 2 Mg 2++ + CO 32 - Mg. CO 3 + 2 H O+ + 2 OH + 2 H + - + + 2 ++ H + Далее OH- H 2 O Содержание Назад 25 +

1/22/201 8 Тема: Кислоты, их классификация и свойства. II. Свойства кислот. I. Кислоты. 1. Физические свойства. Кислоты – это сложные вещества, состоящие из атомов водорода и кислотного остатка. - г – HCl; H 2 S. - Взаимодействие с металлами - Взаимодействие с оксидами металлов Hx. An – общая формула . - ж – H 2 SO 4; HNO 3 I II II 2 2 Кислоты Са + HCl Nа SO 4 + H 2 O Nа 2 O + H; H 3 BO Са. Cl + H 2 - тв – H 3 PO 4 SO 3. 2 4 2 2. Химические свойства. II II Бескислородные Кислородсодержащие Сu + HCl Сu SO 4 + H 2 O - Диссоциация Сu. O + H 2 SO 4 H+ HCl- Cl + П Р Порядок действий: Одноосновные HCl; HBr III HNO 3; HNO 2 П И Al 2 OSO 42 -3 2 SO 4 2 H 2 + H H + 4 3 + Al SO + H O ( ) 3 Р И М 1. В дописанных реакциях над металлом и CO 2 SO 2 4 3 4. Определить положение металла в ряду кислотным 2. Если металл стоит до водорода, то дописать реакцию. В Двухосновные H 2 активности Е Механизм: H 2 S 5. Если валентности разные, поставить индексы. 3; H 2 6. Расставить коэффициенты. 3. Если металл стоит после водорода, то реакция не идет. 4 М остатком поставьте валентности. результате реакции образуется соль и водород. металлов. Е Р Ы 1 ст. H 2 SO 4 H+ HSO Порядок действий: 4 - + Р Ы Далее Ряд активности металлов Трехосновные H 3 PO 4; H 3 BO 3 Содержание 2 ст. HSO 4 HSO + - 2 - + Li, K, Ba, Ca, Na, Mg, Al, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H 2 , Cu, Hg, Ag, Pt, 4. Расставить коэффициенты. 3. Если валентности разные, расставить коэффициенты. 2. Определить валентности металла и кислотного остатка. 1. Дописать реакции. В результате образуется соль и вода. Назад Au 26
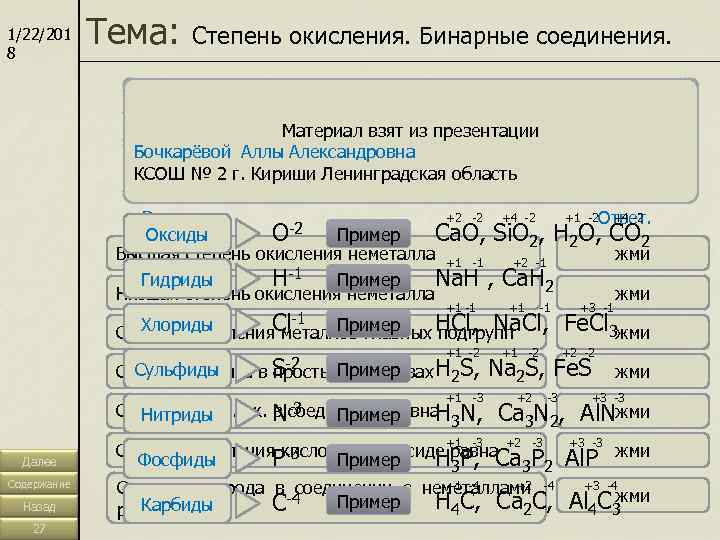
1/22/201 8 Тема: Степень окисления. Бинарные соединения. Степень окисления – условный заряд атома химического Бинары – это сложные вещества, состоящие из двух элементов. элемента, который образуется за счет полного присоединения Материал взят из презентации или отдачи электронов. Бочкарёвой –– классов бинаров. вещества, состоящие из двух Хлориды Аллы Александровна(Нажми состоящие Карбиды Фосфиды Нитриды Сульфиды Гидриды это сложные вещества, состоящие из Оксиды – это сложные вещества, состоящие из двух элементов, Определение – это сложные вещества, на класс, определение это сложные КСОШ № 2 г. Кириши Ленинградская область элементов, один из которых углерод. элементов, один из которых фосфор. элементов, один из которых азот. элементов, один из которых сера. элементов, один из которых хлор. элементов, один из которых водород. один из которых кислород. появится. Нажми еще раз, оно закроется. ) Основные понятия. Вопрос. Ответ. +2 -2 +4 -2 +1 -2 +4 -2 Оксиды О -2 Пример Ca. O, Si. O 2, H 2 O, CO 2 Высшая степень окисления неметалла +1 -1 +2 -1 = № группы жми Гидриды Н-1 Пример Na. H , Ca. H 2 Низшая степень окисления неметалла = 8 - № группы жми +1 -1 +1 -1 +3 -1 Хлориды Cl-1 Пример HCl, Na. Cl, Fe. Cl 3 жми Степень окисления металлов главных подгрупп = № группы +1 -2 +1 -2 +2 -2 Ст. ок. элемента в простых веществах H 2 S, Na 2 S, Fe. S Сульфиды S-2 Пример = 0 жми +1 -3 +2 -3 +3 -3 Нитриды N-3 Пример H Сумма всех ст. ок. в соединении равна 3 N, Ca 3 N 2, Al. N = 0 жми +1 -3 +2 -3 +3 -3 Степень окисления кислорода в оксиде равна Далее Фосфиды P-3 Пример H 3 P, Ca 3 P 2 Al. P жми -2 Содержание Ст. ок. водорода в соединении с неметаллами +1 -4 +2 -4 +3 -4 Назад Карбиды равна C-4 Пример H 4 C, Ca 2 C, Al 4 C 3 жми +1 27

1/22/201 Коллекция учебных динамических слайдов по 8 химии 8 класс. Если, разработанные мною слайды, пригодятся Вам в работе, я буду очень рад. По ходу просмотра могли возникнуть вопросы или замечания, которые стоит исправить, не поленитесь дайте знать. Возможно у вас есть собственные, подобные разработки. Я могу их обработать и разместить рядом с указанием вашего авторства. Может быть в будущем получится отличная разработка, которая поможет многим при подготовки к урокам. Надеюсь, что заинтересовал Вас, пишите aleksei. bazhenov@mail. ru С Уважением Баженов А. А. Верьте в себя и у Вас все получится Далее Содержание Назад 28
Коллекция слайдов.ppt
- Количество слайдов: 28

