04.ppt
- Количество слайдов: 21
 Клінічна токсикологія Лекція № 4 Тема: Хроматографічні методи аналізу в токсикологічній хімії. Аналіз спиртів методом газо-рідинної хроматографії Лектор – Чорнокнижний С. І.
Клінічна токсикологія Лекція № 4 Тема: Хроматографічні методи аналізу в токсикологічній хімії. Аналіз спиртів методом газо-рідинної хроматографії Лектор – Чорнокнижний С. І.
 2 Хроматографія - фізико-хімічний метод розділення і аналізу сумішей, заснований на розподілі їх компонентів між двома фазами - нерухомою і рухомою (елюент), що протікає через нерухому. Хроматографічний аналіз є критерієм однорідності речовини: якщо яким-небудь хроматографічним способом аналізована речовина не розділилася, то її вважають однорідною (без домішок). Принциповою відмінністю хроматографічних методів від інших фізико-хімічних методів аналізу є можливість поділу близьких за властивостями речовин. Після поділу компоненти аналізованої суміші можна ідентифікувати (встановити природу) і кількісно визначати (масу, концентрацію) будь-якими хімічними, фізичними і фізико-
2 Хроматографія - фізико-хімічний метод розділення і аналізу сумішей, заснований на розподілі їх компонентів між двома фазами - нерухомою і рухомою (елюент), що протікає через нерухому. Хроматографічний аналіз є критерієм однорідності речовини: якщо яким-небудь хроматографічним способом аналізована речовина не розділилася, то її вважають однорідною (без домішок). Принциповою відмінністю хроматографічних методів від інших фізико-хімічних методів аналізу є можливість поділу близьких за властивостями речовин. Після поділу компоненти аналізованої суміші можна ідентифікувати (встановити природу) і кількісно визначати (масу, концентрацію) будь-якими хімічними, фізичними і фізико-
 9 Історія хроматографії Метод хроматографії був вперше застосований російським ученим-ботаніком Михайлом Семеновичем Цвєтом в 1900 році. Він використовував колонку, заповнену карбонатом кальцію, для поділу пігментів рослинного походження. У 1910 -1930 роки метод був незаслужено забутий і практично не розвивався. У 1931 році Р. Кун, А. Винтерштейн і Е. Ледерер за допомогою хроматографії виділили з сирого каротину α і β фракції в кристалічному вигляді, чим продемонстрували препаративну цінність
9 Історія хроматографії Метод хроматографії був вперше застосований російським ученим-ботаніком Михайлом Семеновичем Цвєтом в 1900 році. Він використовував колонку, заповнену карбонатом кальцію, для поділу пігментів рослинного походження. У 1910 -1930 роки метод був незаслужено забутий і практично не розвивався. У 1931 році Р. Кун, А. Винтерштейн і Е. Ледерер за допомогою хроматографії виділили з сирого каротину α і β фракції в кристалічному вигляді, чим продемонстрували препаративну цінність
 10 Історія хроматографії У 1941 році А. Дж. П. Мартін і Р. Л. М. Сінг розробили новий різновид хроматографії, в основу якої лягла відмінність в коефіцієнтах розподілу розділяємих речовин між двома несмешивающимися рідинами. Метод отримав назву «розподільна хроматографія» . У 1947 році Т. Б. Гапон, Е. Н. Гапон і Ф. М. Шемякін розробили метод «іонообмінної хроматографії» . У 1952 році Дж. Мартіну і Р. Сінгу була присуджена Нобелівська премія в галузі хімії за створення методу розподільної хроматографії. З середини XX століття і до наших днів хроматографія інтенсивно розвивалася і стала одним з найбільш широко застосовуваних аналітичних методів.
10 Історія хроматографії У 1941 році А. Дж. П. Мартін і Р. Л. М. Сінг розробили новий різновид хроматографії, в основу якої лягла відмінність в коефіцієнтах розподілу розділяємих речовин між двома несмешивающимися рідинами. Метод отримав назву «розподільна хроматографія» . У 1947 році Т. Б. Гапон, Е. Н. Гапон і Ф. М. Шемякін розробили метод «іонообмінної хроматографії» . У 1952 році Дж. Мартіну і Р. Сінгу була присуджена Нобелівська премія в галузі хімії за створення методу розподільної хроматографії. З середини XX століття і до наших днів хроматографія інтенсивно розвивалася і стала одним з найбільш широко застосовуваних аналітичних методів.
 11 Термінологія Колонка - містить хроматографічний сорбент, виконує функцію розділення суміші на індивідуальні компоненти. Елюент - рухома фаза: газ, рідина або (рідше) надкритичний флюїд. Нерухома фаза - тверда фаза або рідина, пов'язана на інертному носії, в адсорбційної хроматографії - сорбент. Хроматограма - результат реєстрування залежності концентрації компонентів на виході з колонки від часу. Детектор - пристрій для реєстрації концентрації компонентів суміші на виході з колонки. Хроматограф - прилад для проведення хроматографії.
11 Термінологія Колонка - містить хроматографічний сорбент, виконує функцію розділення суміші на індивідуальні компоненти. Елюент - рухома фаза: газ, рідина або (рідше) надкритичний флюїд. Нерухома фаза - тверда фаза або рідина, пов'язана на інертному носії, в адсорбційної хроматографії - сорбент. Хроматограма - результат реєстрування залежності концентрації компонентів на виході з колонки від часу. Детектор - пристрій для реєстрації концентрації компонентів суміші на виході з колонки. Хроматограф - прилад для проведення хроматографії.
 Основні переваги хроматографічного аналізу • • Експресність; Висока ефективність; Можливість автоматизації і отримання об'єктивної інформації; Поєднання з іншими фізико-хімічними методами; Широкий інтервал концентрацій сполук; Можливість вивчення фізико-хімічних властивостей сполук; Можливість проведення якісного та кількісного аналізу; Застосування для контролю та автоматичного регулювання технологічних процесів. 12
Основні переваги хроматографічного аналізу • • Експресність; Висока ефективність; Можливість автоматизації і отримання об'єктивної інформації; Поєднання з іншими фізико-хімічними методами; Широкий інтервал концентрацій сполук; Можливість вивчення фізико-хімічних властивостей сполук; Можливість проведення якісного та кількісного аналізу; Застосування для контролю та автоматичного регулювання технологічних процесів. 12
 Класифікація хроматографічних методів За природою взаємодії між рухомою і нерухомою фазою: • • • Адсорбційна хроматографія заснована на різниці сорбції речовин, що розділяються, адсорбентом (тверде тіло з розвиненою поверхнею); Розподільна хроматографія - на різній розчинності компонентів суміші в нерухомій фазі (висококипляча рідина, нанесена на твердий макропористий носій) і елюенті; Іонообмінна хроматографія - на різниці констант іонообмінної рівноваги між нерухомою фазою (іонітом) і компонентами суміші, що розділяється; Ексклюзіонна (молекулярно-ситова) хроматографія - на різній проникності молекул компонентів в нерухому фазу (високопористий неіоногенний гель). Осадова хроматографія заснована на різній здатності компонентів, що розділяються випадати в осад на твердій нерухомій фазі. 13
Класифікація хроматографічних методів За природою взаємодії між рухомою і нерухомою фазою: • • • Адсорбційна хроматографія заснована на різниці сорбції речовин, що розділяються, адсорбентом (тверде тіло з розвиненою поверхнею); Розподільна хроматографія - на різній розчинності компонентів суміші в нерухомій фазі (висококипляча рідина, нанесена на твердий макропористий носій) і елюенті; Іонообмінна хроматографія - на різниці констант іонообмінної рівноваги між нерухомою фазою (іонітом) і компонентами суміші, що розділяється; Ексклюзіонна (молекулярно-ситова) хроматографія - на різній проникності молекул компонентів в нерухому фазу (високопористий неіоногенний гель). Осадова хроматографія заснована на різній здатності компонентів, що розділяються випадати в осад на твердій нерухомій фазі. 13
 Класифікація хроматографічних методів 14 За агрегатним станом елюента: • Газова хроматографія (ГХ) застосовується для розділення, визначення домішок шкідливих речовин в повітрі, воді, грунті, промислових продуктах; визначення складу продуктів основного органічного та нафтохімічного синтезу, вихлопних газів, лікарських препаратів, а також в криміналістиці і т. д. • Рідинна хроматографія (ВЕРХ) використовується для аналізу, розділення і очищення синтетичних полімерів, лікарських препаратів, детергентів, білків, гормонів та інших біологічно важливих сполук. Використання високочутливих детекторів дозволяє працювати з дуже малими кількостями речовин (10 -11 - 10 -9 г), що виключно важливо в біологічних дослідженнях.
Класифікація хроматографічних методів 14 За агрегатним станом елюента: • Газова хроматографія (ГХ) застосовується для розділення, визначення домішок шкідливих речовин в повітрі, воді, грунті, промислових продуктах; визначення складу продуктів основного органічного та нафтохімічного синтезу, вихлопних газів, лікарських препаратів, а також в криміналістиці і т. д. • Рідинна хроматографія (ВЕРХ) використовується для аналізу, розділення і очищення синтетичних полімерів, лікарських препаратів, детергентів, білків, гормонів та інших біологічно важливих сполук. Використання високочутливих детекторів дозволяє працювати з дуже малими кількостями речовин (10 -11 - 10 -9 г), що виключно важливо в біологічних дослідженнях.
 Класифікація хроматографічних методів В залежності від агрегатного стану нерухомої фази газова хроматографія буває газо-адсорбційна (нерухома фаза - твердий адсорбент) і газорідинна (нерухома фаза - рідина), а рідинна хроматографія - рідинно-адсорбційна (або твердо-рідинна) і рідинно-рідинної. Також розрізняють колонкову і площинну хроматографію. У колонковій сорбентом заповнюють спеціальні трубки - колонки, а рухома фаза рухається усередині колонки завдяки перепаду тиску. Площинна хроматографія підрозділяється на тонкошарову і паперову. У тонкошарової хроматографії тонкий шар гранульованого сорбенту або пориста плівка наноситься на скляну або металеву пластинки; У разі паперової хроматографії використовують спеціальний хроматографічний папір. Тонкошарова (ТШХ) і паперова хроматографія використовуються для аналізу жирів, вуглеводів, білків і ін природних речовин і неорганічних сполук. 15
Класифікація хроматографічних методів В залежності від агрегатного стану нерухомої фази газова хроматографія буває газо-адсорбційна (нерухома фаза - твердий адсорбент) і газорідинна (нерухома фаза - рідина), а рідинна хроматографія - рідинно-адсорбційна (або твердо-рідинна) і рідинно-рідинної. Також розрізняють колонкову і площинну хроматографію. У колонковій сорбентом заповнюють спеціальні трубки - колонки, а рухома фаза рухається усередині колонки завдяки перепаду тиску. Площинна хроматографія підрозділяється на тонкошарову і паперову. У тонкошарової хроматографії тонкий шар гранульованого сорбенту або пориста плівка наноситься на скляну або металеву пластинки; У разі паперової хроматографії використовують спеціальний хроматографічний папір. Тонкошарова (ТШХ) і паперова хроматографія використовуються для аналізу жирів, вуглеводів, білків і ін природних речовин і неорганічних сполук. 15
 16 Хроматограф Ряд видів хроматографії здійснюється за допомогою приладів, які називаються хроматографами. Хроматографи використовують для аналізу і для препаративного (в т. ч. промислового) розділення сумішей речовин. При аналізі розділені в хроматографічній колонці речовини разом з елюентом потрапляють у встановлений на виході з колонки спеціальний пристрій - детектор, реєструючий їх концентрації в часі.
16 Хроматограф Ряд видів хроматографії здійснюється за допомогою приладів, які називаються хроматографами. Хроматографи використовують для аналізу і для препаративного (в т. ч. промислового) розділення сумішей речовин. При аналізі розділені в хроматографічній колонці речовини разом з елюентом потрапляють у встановлений на виході з колонки спеціальний пристрій - детектор, реєструючий їх концентрації в часі.
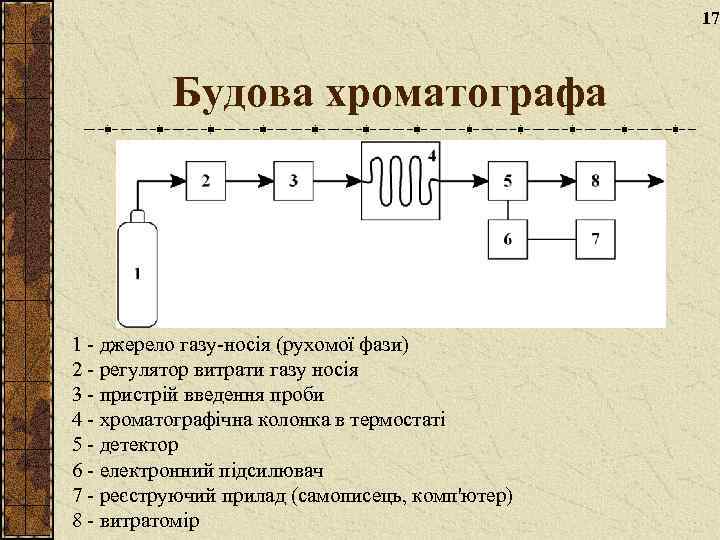 17 Будова хроматографа 1 - джерело газу-носія (рухомої фази) 2 - регулятор витрати газу носія 3 - пристрій введення проби 4 - хроматографічна колонка в термостаті 5 - детектор 6 - електронний підсилювач 7 - реєструючий прилад (самописець, комп'ютер) 8 - витратомір
17 Будова хроматографа 1 - джерело газу-носія (рухомої фази) 2 - регулятор витрати газу носія 3 - пристрій введення проби 4 - хроматографічна колонка в термостаті 5 - детектор 6 - електронний підсилювач 7 - реєструючий прилад (самописець, комп'ютер) 8 - витратомір
 18 Принцип дії хроматографа Після введення аналізованої суміші з потоком рухомої фази в колонку зони всіх речовин розташовані на початку хроматографічної колонки. Під дією потоку рухомої фази компоненти суміші починають переміщатися уздовж колонки з різними швидкостями, величини яких обернено пропорційні коефіцієнтам розподілу (К) хроматографуємих компонентів. Речовини, що добре сорбуються, пересуваються вздовж шару сорбенту по колонці повільніше, ніж ті, що погано сорбуються. Наприклад, якщо КА<КБ<КВ, то швидше за всіх з колонки виходить компонент А, потім компонент Б і останнім покидає колонку компонент В.
18 Принцип дії хроматографа Після введення аналізованої суміші з потоком рухомої фази в колонку зони всіх речовин розташовані на початку хроматографічної колонки. Під дією потоку рухомої фази компоненти суміші починають переміщатися уздовж колонки з різними швидкостями, величини яких обернено пропорційні коефіцієнтам розподілу (К) хроматографуємих компонентів. Речовини, що добре сорбуються, пересуваються вздовж шару сорбенту по колонці повільніше, ніж ті, що погано сорбуються. Наприклад, якщо КА<КБ<КВ, то швидше за всіх з колонки виходить компонент А, потім компонент Б і останнім покидає колонку компонент В.
 19 Принцип дії хроматографа Сигнал детектора, величина якого пропорційна концентрації визначаємої речовини в потоці елюента, автоматично безперервно записується і реєструється (на діаграмній стрічці або в комп’ютері). Отримана хроматограма відображає розташування хроматографічних зон на шарі сорбенту або в потоці рухомої фази в часі.
19 Принцип дії хроматографа Сигнал детектора, величина якого пропорційна концентрації визначаємої речовини в потоці елюента, автоматично безперервно записується і реєструється (на діаграмній стрічці або в комп’ютері). Отримана хроматограма відображає розташування хроматографічних зон на шарі сорбенту або в потоці рухомої фази в часі.
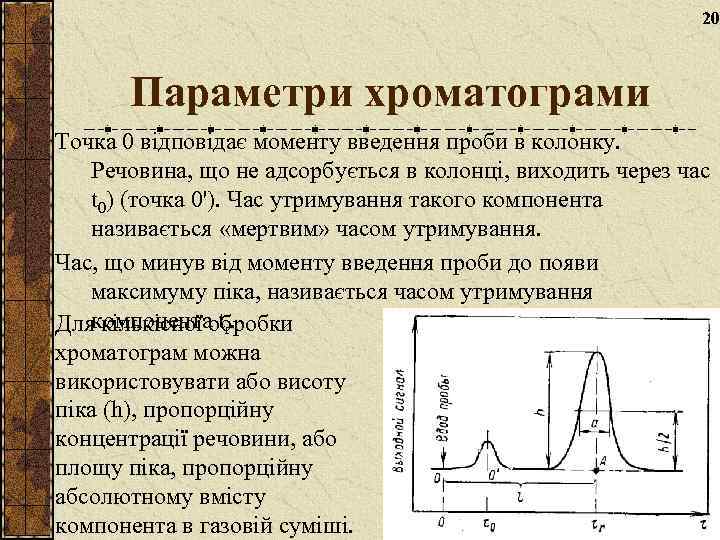 20 Параметри хроматограми Точка 0 відповідає моменту введення проби в колонку. Речовина, що не адсорбується в колонці, виходить через час t 0) (точка 0'). Час утримування такого компонента називається «мертвим» часом утримування. Час, що минув від моменту введення проби до появи максимуму піка, називається часом утримування компонента tr. Для кількісної обробки хроматограм можна використовувати або висоту піка (h), пропорційну концентрації речовини, або площу піка, пропорційну абсолютному вмісту компонента в газовій суміші.
20 Параметри хроматограми Точка 0 відповідає моменту введення проби в колонку. Речовина, що не адсорбується в колонці, виходить через час t 0) (точка 0'). Час утримування такого компонента називається «мертвим» часом утримування. Час, що минув від моменту введення проби до появи максимуму піка, називається часом утримування компонента tr. Для кількісної обробки хроматограм можна використовувати або висоту піка (h), пропорційну концентрації речовини, або площу піка, пропорційну абсолютному вмісту компонента в газовій суміші.
 21 Тонкошарова хроматографія (ТШХ) є планарним різновидом рідинної хроматографії, в якій рухома фаза (Елюент) рухається в пористому середовищі шару адсорбенту. На шар сорбенту наносять краплі (обсягом 1 -5 мкл) аналізованого розчину і занурюють край пластинки в елюент, який знаходиться на дні герметично закритої скляної камери. Елюент просувається по шару сорбенту під дією капілярних і гравітаційних сил; аналізована суміш переміщається в тому ж напрямку. У результаті багаторазового повторення актів сорбції та десорбції відповідно до коефіцієнту розподілу в обраній системі компоненти розділяються і розташовуються на пластинці окремими зонами.
21 Тонкошарова хроматографія (ТШХ) є планарним різновидом рідинної хроматографії, в якій рухома фаза (Елюент) рухається в пористому середовищі шару адсорбенту. На шар сорбенту наносять краплі (обсягом 1 -5 мкл) аналізованого розчину і занурюють край пластинки в елюент, який знаходиться на дні герметично закритої скляної камери. Елюент просувається по шару сорбенту під дією капілярних і гравітаційних сил; аналізована суміш переміщається в тому ж напрямку. У результаті багаторазового повторення актів сорбції та десорбції відповідно до коефіцієнту розподілу в обраній системі компоненти розділяються і розташовуються на пластинці окремими зонами.
 22 Тонкошарова хроматографія Після завершення процесу пластинку виймають з камери, висушують і виявляють розділені зони по власному забарвленню або після обприскування їх розчинами реагентів, що утворюють забарвлені або флуоресціюючі плями з компонентами суміші, що розділяється. Положення хроматографічних зон на хроматограмі характеризує величина Rf відношення шляху li, пройденого центром зони i-го компонента від лінії старту, до шляху l, пройденому елюентом: Rf = li / l; Величина Rf залежить від коеф. розподілу (адсорбції) і від співвідношення обсягів рухомої і нерухомої фаз.
22 Тонкошарова хроматографія Після завершення процесу пластинку виймають з камери, висушують і виявляють розділені зони по власному забарвленню або після обприскування їх розчинами реагентів, що утворюють забарвлені або флуоресціюючі плями з компонентами суміші, що розділяється. Положення хроматографічних зон на хроматограмі характеризує величина Rf відношення шляху li, пройденого центром зони i-го компонента від лінії старту, до шляху l, пройденому елюентом: Rf = li / l; Величина Rf залежить від коеф. розподілу (адсорбції) і від співвідношення обсягів рухомої і нерухомої фаз.
 Визначення етилового спирту методом ГЖХ Побудова калібрувального графіка. Спочатку готують серію стандартних розчинів, що містять 2, 3, 4 і 5% етилового спирту, та розчин внутрішнього стандарту, що містить 4% пропилового спирту. У кілька флаконів з під пеніциліну вносять по 2 мл розчину, що містить по 4% пропилового спирту. У кожний флакон додають по 2 мл розчину етилового спирту різної концентрації (2, 3, 4 і 5%). Вміст флаконів добре перемішують, а потім беруть по 1 мл суміші спиртів з кожного флакона і переносять в інші флакони з під пеніциліну. У кожний флакон додають по 0, 5 мл 50%-го розчину трихлороцтової кислоти. Флакони закривають гумовими пробками, які закріплюють фіксаторами. Потім за допомогою шприца через гумову пробку у флакони вносять по 0, 25 мл 30%-го розчину нітриту натрію. Вміст флаконів збовтують протягом однієї хвилини. Після цього за допомогою іншого сухого шприца з флаконів відбирають по 3 мл газоподібної фази, яку вводять в дозатор хроматографа, і 23
Визначення етилового спирту методом ГЖХ Побудова калібрувального графіка. Спочатку готують серію стандартних розчинів, що містять 2, 3, 4 і 5% етилового спирту, та розчин внутрішнього стандарту, що містить 4% пропилового спирту. У кілька флаконів з під пеніциліну вносять по 2 мл розчину, що містить по 4% пропилового спирту. У кожний флакон додають по 2 мл розчину етилового спирту різної концентрації (2, 3, 4 і 5%). Вміст флаконів добре перемішують, а потім беруть по 1 мл суміші спиртів з кожного флакона і переносять в інші флакони з під пеніциліну. У кожний флакон додають по 0, 5 мл 50%-го розчину трихлороцтової кислоти. Флакони закривають гумовими пробками, які закріплюють фіксаторами. Потім за допомогою шприца через гумову пробку у флакони вносять по 0, 25 мл 30%-го розчину нітриту натрію. Вміст флаконів збовтують протягом однієї хвилини. Після цього за допомогою іншого сухого шприца з флаконів відбирають по 3 мл газоподібної фази, яку вводять в дозатор хроматографа, і 23
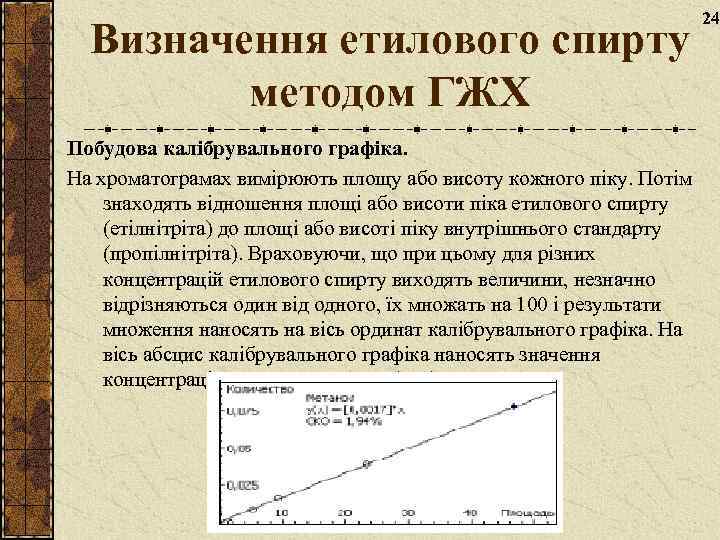 Визначення етилового спирту методом ГЖХ Побудова калібрувального графіка. На хроматограмах вимірюють площу або висоту кожного піку. Потім знаходять відношення площі або висоти піка етилового спирту (етілнітріта) до площі або висоті піку внутрішнього стандарту (пропілнітріта). Враховуючи, що при цьому для різних концентрацій етилового спирту виходять величини, незначно відрізняються один від одного, їх множать на 100 і результати множення наносять на вісь ординат калібрувального графіка. На вісь абсцис калібрувального графіка наносять значення концентрацій етилового спирту (в %). 24
Визначення етилового спирту методом ГЖХ Побудова калібрувального графіка. На хроматограмах вимірюють площу або висоту кожного піку. Потім знаходять відношення площі або висоти піка етилового спирту (етілнітріта) до площі або висоті піку внутрішнього стандарту (пропілнітріта). Враховуючи, що при цьому для різних концентрацій етилового спирту виходять величини, незначно відрізняються один від одного, їх множать на 100 і результати множення наносять на вісь ординат калібрувального графіка. На вісь абсцис калібрувального графіка наносять значення концентрацій етилового спирту (в %). 24
 Визначення етилового спирту методом ГЖХ Визначення етилового спирту в крові та сечі. У флакон з під пеніциліну вносять 2 мл розчину внутрішнього стандарту (пропилового спирту, концентрація якого становить 4%), додають 2 мл крові або сечі, що підлягає дослідженню на наявність етилового спирту. Вміст флакона добре збовтують, а потім 1 мл рідини (суміші крові або сечі з внутрішнім стандартом) переносять в інший флакон з під пеніциліну і додають 0, 5 мл 50% -го розчину трихлороцтової кислоти. Флакон закривають гумовою пробкою, яку закріплюють фіксатором. За допомогою шприца через пробку у флакон вносять 0, 25 мл 30%-го розчину нітриту натрію. Вміст флакона збовтують протягом однієї хвилини. Потім за допомогою іншого сухого шприца відбирають з флакона 3 мл газоподібної фази, яку переносять у дозатор хроматографа, і проводять хроматографування. 25
Визначення етилового спирту методом ГЖХ Визначення етилового спирту в крові та сечі. У флакон з під пеніциліну вносять 2 мл розчину внутрішнього стандарту (пропилового спирту, концентрація якого становить 4%), додають 2 мл крові або сечі, що підлягає дослідженню на наявність етилового спирту. Вміст флакона добре збовтують, а потім 1 мл рідини (суміші крові або сечі з внутрішнім стандартом) переносять в інший флакон з під пеніциліну і додають 0, 5 мл 50% -го розчину трихлороцтової кислоти. Флакон закривають гумовою пробкою, яку закріплюють фіксатором. За допомогою шприца через пробку у флакон вносять 0, 25 мл 30%-го розчину нітриту натрію. Вміст флакона збовтують протягом однієї хвилини. Потім за допомогою іншого сухого шприца відбирають з флакона 3 мл газоподібної фази, яку переносять у дозатор хроматографа, і проводять хроматографування. 25
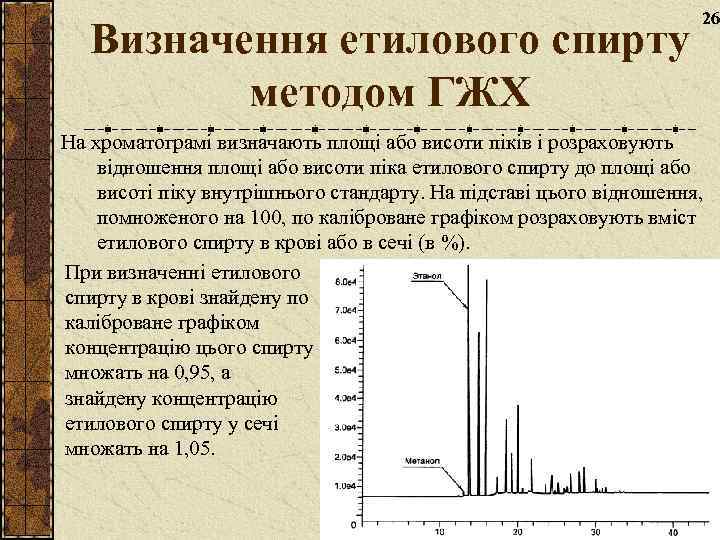 Визначення етилового спирту методом ГЖХ 26 На хроматограмі визначають площі або висоти піків і розраховують відношення площі або висоти піка етилового спирту до площі або висоті піку внутрішнього стандарту. На підставі цього відношення, помноженого на 100, по каліброване графіком розраховують вміст етилового спирту в крові або в сечі (в %). При визначенні етилового спирту в крові знайдену по каліброване графіком концентрацію цього спирту множать на 0, 95, а знайдену концентрацію етилового спирту у сечі множать на 1, 05.
Визначення етилового спирту методом ГЖХ 26 На хроматограмі визначають площі або висоти піків і розраховують відношення площі або висоти піка етилового спирту до площі або висоті піку внутрішнього стандарту. На підставі цього відношення, помноженого на 100, по каліброване графіком розраховують вміст етилового спирту в крові або в сечі (в %). При визначенні етилового спирту в крові знайдену по каліброване графіком концентрацію цього спирту множать на 0, 95, а знайдену концентрацію етилового спирту у сечі множать на 1, 05.
 Дякую за увагу
Дякую за увагу


